סוכרת וויטמין Diabetes and vitamin D - D
| סוכרת וויטמין D | ||
|---|---|---|
| Diabetes and vitamin D | ||
| שמות נוספים | ויטמין D וסוכרת – פאטה מורגנה קלינית? | |
| יוצר הערך | פרופ' יאיר ליאל 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – טיפול בסוכרת, ויטמין D
המעבר בין שנות השישים לשנות השבעים של המאה ה-20 סימן את תחילת תקופת התחייה של המחקר בוויטמין D, שהתפתח לאטו במהלך המאה ה-19 ובתחילת המאה ה-20, וכלל תצפיות שתרמו להבנת הקשר שבין קרינת השמש למשק הסידן ולמטבוליזם השלד. ב-1936 הסתיים אפיונו של המבנה הכימי של ויטמין D, והמחקר בוויטמין D קפא, במידה רבה, עד תחילת שנות השבעים, עם גילוי D2(OH)1,25 על ידי קבוצתו של DeLuca, ופענוח מסלול הייצור והשפעול של ויטמין D - ייצורו בעור כפרו-הורמון (Prohormone) בהשפעת קרינת אור UVB (Ultraviolet B), השפעול הראשוני בכבד, יצירת D(OH)25, והשפעול הסופי באמצעות alpha-hydroxylase-1 D3 Hydroxyvitamin-25 להפקת החליף (Metabolite) הפעיל, D2(OH)1,25, בכליה.
גילויים אלו הגדירו מערכת הורמונלית משולבת - הורמון בלוטת יותרת התריס (PTH, Parathyroid Hormone) וויטמין D - ששולטת על ריכוז הסידן החוץ תאי. קולטנים תוך-תאיים לוויטמין D זוהו לראשונה ב-1979 ואותרו לאחר מכן כמעט בכל תאי הגוף - נתון שרמז להשפעה פיזיולוגית של ויטמין D במערכות גוף נוספות, מלבד אלו הקשורות במשק המינרלים והעצם.
מחקרים מעבדתיים מצביעים על מנגנונים אפשריים יעילים שבאמצעותם אפשר לווסת רבים מהמנגונים הלקויים בסוכרת מסוג 1 ומסוג 2. מחקרים אפידמיולוגיים רבים תומכים בקשר בין חסר בוויטמין D לבין תחלואה בסוכרת, אולם תוצאות המחקרים ההתערבותיים-המבוקרים המעטים שפורסמו הן הססניות ומדגישות את הפער שבין הסביבה המעבדתית, המעוקרת (Sterile) והמבוקרת לבין המציאות הקלינית המורכבת. למרות ניסיונות לתקנון, חלק מהמחקרים התצפיתיים מעוותים בגלל היעדר תקנון לערפלנים ידועים (לא כל שכן לאפשרות של קיומם של ערפלנים סמויים). עובדה זו אינה שוללת לחלוטין קיומה של השפעה מטיבה של ויטמין D על מהלך מחלת הסוכרת, אך מעמידה אותה בפרופורציה לעומת גורמי סיכון אחרים. יש לקוות שמחקרים התערבותיים מבוקרים, דוגמת מחקר VITAL - המנוהל בחסות מכוני הבריאות של ארצות הברית, החל ב-2012 וצפוי להסתיים ב-2017, ובוחן השפעת ויטמין D ו/או אומגה-3 על הארעות סרטן ומחלות של הלב וכלי הדם - יוכלו לספק הבנה ברורה יותר לגבי יכולות קידום הבריאות של ויטמין D מחוץ למערכת השלד בכלל ובסוכרת בפרט.
מחקרים היסטוריים על הקשר בין ויטמין D לסוכרת
אף שיש הרואים רמז ראשון לזיקה שבין ויטמין D לסוכרת במחקר של Campbell ואחרים[1] - שתיארו שינויים עונתיים בסבילות לסוכר במתנדבים צעירים ובריאים במחנה מחקר באנטארקטיקה - ספק אם אפשר לייחס את הממצאים לשינויים ברמת ויטמין D, שכן ויטמין D לא נמדד ולא נמסרו פרטים על שימוש בתוספי ויטמין D. אפשר להניח שגם בקיץ חשיפת העור לשמש הייתה ככל הנראה מזערית, שכן הטמפרטורה בקיץ לא עלתה על C0°; ואפילו נחשף העור לשמש - הזווית החדה של השמש באנטארקטיקה מונעת במידה רבה חדירה של קרינת UVB לצורך יצירה ממקור פנימי (Endogenous synthesis) של ויטמין D. מכל מקום, האפשרות שההבדלים שנצפו קשורים בוויטמין D לא הוזכרה על ידי המחברים, אשר העלו אפשרויות אחרות.
ההתייחסות המפורשת הראשונה להשפעה הדדית בין סוכרת וויטמין D הופיעה ב-1976, במחקר שבדק ספיגת סידן בהשפעת ויטמין D במעי של חולדות סוכרתיות, וזאת לנוכח דיווחים קודמים על הפרעה בספיגת סידן בחולדות סוכרתיות[2], ובעקבות זאת, שורה של מחקרים נוספים שבדקו את השפעת ויטמין D על משק הסידן והעצם בחולדות ובבני אדם[3] ומטרתם הייתה לספק הסבר לשכיחות גבוהה של חוסר מינרלים בעצם - אוסטאופניה (Osteopenia), במובנה באותם ימים - בחולי סוכרת.
בתחילת שנות השמונים של המאה ה-20 הופיעו הדיווחים הראשונים על ריכוזים נמוכים יחסית של D(OH)25 בחולי סוכרת[4],[5]. התגברות העניין בהשפעות החוץ שלדיות של ויטמין D, עם תצפיות שרמזו להשפעות של ויטמין D ברקמות מרכזיות בפתוגנזה של סוכרת, עוררו את המחשבה ואת המחקר לגבי הקשר שבין ויטמין D לסוכרת.
מנגנון הפעולה של ויטמין D
D2(OH)1,25 - החליף הפעיל של ויטמין D - פועל בתיווך קולטנים תוך-תאיים לוויטמין D (VDR, Vitamin D Receptor) הפועלים כגורמי שיעתוק בגרעיני התאים, ומשפיעים על ייצור חלבונים ועל פעילויות תאיות ופיזיולוגיות מגוונות. קיימות עדויות המצביעות על אפשרות ש-D2(OH)1,25 עשוי להשפיע גם באמצעות קולטנים ממברנליים מהירי תגובה.
קולטנים לוויטמין D זוהו לראשונה ב-1979 ואותרו לאחר מכן כמעט בכל תאי הגוף, לרבות באיי הלבלב ובתאי שומן. יש לציין שלא נצפה ביטוי של קולטנים לוויטמין D בתאי רקמת התָּוֶךְ (Parenchyma) של הכבד ושקיים כיום ספק לגבי נוכחות קולטנים לוויטמין D בתאי שריר[6].
סמוך ל-1980 - לאחר שתועד התפקיד הפתוגנטי (Pathogenetic) של D2(OH)1,25 בסרקואידוזיס (Sarcoidosis) ובמחלות גרנולומטוטיות (Granulomatous) אחרות - התברר שבניגוד למה שרווח עד אז (ששפעול ויטמין D מתקיים בכליות בלבד), המערכת האנזימטית לשפעול ויטמין D פעילה גם מחוץ לכליות, וזאת תחת בקרה שונה מזו הקשורה לבקרת משק הסידן. האנזים המשפעל, alpha-hydroxylase-1 D3 Hydroxyvitamin-25, זוהה במספר רב של סוגי תאים ורקמות, כולל תאי ביתא (β) בלבלב[7]. הימצאות קולטנים לוויטמין D בתאי הלבלב רומזת על השפעה אפשרית של המערכת האנדוקרינית (Endocrine) של ויטמין D על פעילות תאים אלו - באופן אנדוקריני-מערכתי (Systemic), או באופן אוטוקריני (Autocrine) או פאראקריני (Paracrine).
הימצאות קולטנים ומערכת שפעול לוויטמין D בתאי שומן[8],[9] ועדות להשפעה מעכבת של D2(OH)1,25 על התבטאות PPAR-γ (Peroxisome Proliferator-Activated Receptor) והתמיינות תאי שומן[10],[11], רומזות להשפעה של ויטמין D בחולי סוכרת, הן ברמת הלבלב והן ברמת הפריפריה (רקמת השומן).
סוכרת מסוג 2
סוכרת מסוג 2 היא תסמונת מטבולית מורכבת ורבת פנים המאופיינת בהפרעה בתהליך הפרשת אינסולין מהלבלב ובתנגודת להשפעת אינסולין (Insulin resistence) בכבד וברקמות השומן והשריר. בצורתה הטיפוסית המחלה קשורה בעודף משקל, רמה גבוהה של שומנים בדם (Hyperlipidemia) ויתר לחץ דם, שמובילים לשיעור גבוה של סיבוכים טרשתיים המושפעים, בין השאר, מקיומם של תהליכים דלקתיים. ההשפעה של ויטמין D על סוכרת מסוג 2 נבדקה ברמה התאית, בבעלי חיים ובבני אדם.
תצפיות בבעלי חיים ובתרביות רקמה
לאחר שהתגלו קולטנים לוויטמין D בלבלב, נבדקה השפעת ויטמין D על פעילות איי הלבלב, ונמצא שהפרשת אינסולין מרקמת לבלב מחולדה עם חסר בוויטמין D הייתה נמוכה, וכי הוספת ויטמין D לחולדות הביאה לשיפור בהפרשת אינסולין מהלבלב, אך לא השפיעה על הפרשת גלוקגון[12]. תגובה לקויה להעמסת גלוקוז נצפתה בחולדות בריאות בעלות חסר בוויטמין D. התגובה תוקנה במידה רבה לאחר תיקון מאגרי ויטמין D, אם כי התיקון לא היה מלא[13]. במודל של חולדות עם סוכרת מסוג 2 [חולדות Goto-Kakizaki (GK)] נמצא ריכוז נמוך של D2(OH)1,25 בנסיוב ועדות לפעילות מוגברת של האנזים Hydroxyvitamin d-1-Alpha Hydroxylase-25, שמטה את המסלול המטבולי של ויטמין D בכיוון ייצור D2(OH)[14],[15] (חליף לא פעיל של ויטמין D).
מצב זה עלול להגביר את קצב הפירוק של D(OH)25 במסלול לא יעיל[16]. השפעה מתקנת על ריכוז גלוקוז בדם עם טיפול ב-D2(OH)1,25 נצפתה בחולדות שמנות מסוג ob/ob (Obese) בעלות סוכרת מסוג 2[17], אך טיפול בוויטמין D במודל חולדות עם יתר לחץ דם בעלות סוכרת מסוג 2, לאחר הזנה עתירת קלוריות/עתירת שומנים, הביא לתיקון חלקי בלבד בריכוז גלוקוז בדם[18].
מחקרים אפידמיולוגיים ומחקרי התערבות
כבר ב-1982 מצאו Stepan ואחרים עדות לרמות נמוכות של D(OH)25 בחולי סוכרת שטופלו בSulfonylurea[4]. במחקרים תצפיתיים רבים לאחר מכן נמצא קשר הפוך בין רמת ויטמין D להארעות סוכרת מסוג 2, ולמרות תצפיות לא מעטות שלא תמכו במגמה, מסקנת ניתוח העל (Meta analysis) הייתה שהקשר אמנם קיים. כמה מאותם מחקרים בחנו מדדים של תנגודת לאינסולין וכמה מהם הצביעו גם על קשר בין ויטמין D למדדים של תנגודת לאינסולין. סקירה נרחבת של המחקרים ושל ניתוח העל פורסמה על ידי Pittas ואחרים[19].
התוצאות של מחקרים התערבותיים במתן ויטמין D ובנגזרותיו הפעילות לחולי סוכרת מסוג 2, היו פושרות. מבין 7 מחקרים שבדקו השפעה של ויטמין D על מדדים קליניים של סוכרת, רק מחקר אחד הראה בו זמנית הורדה של ריכוז הסוכר בצום ועלייה ברגישות לאינסולין. בשני מחקרים אחרים נצפה שיפור ברגישות לאינסולין, אך לא נמצאה השפעה על ריכוז סוכר בצום - מדד שהיווה מטרה ראשית של המחקרים. ב-4 המחקרים האחרים לא גרם טיפול בוויטמין D או בנגזרת פעילה שלו לשיפור במדדי הסוכרת[19].
כמה מחקרים הצביעו על מתאם אפשרי בין נאותות מאגרי ויטמין D, כפי שמשתקפים מריכוז D(OH)25 בנסיוב, לבין איזון סוכרת, ריכוז המוגלובין מסוכרר (Hemoglobin A1C) בנשים הרות והתפתחות סוכרת במהלך ההיריון[20],[21].
מנגנוני פעולה אפשריים של ויטמין D במניעת סוכרת מסוג 2
סוכרת מסוג 2 היא תוצא של פגמים מטבוליים רבים בלבלב, בכבד וברקמות היקפיות (שריר ורקמת שומן). קיימים רמזים לקשר בין רב-צורתיות (Polymorphism) של קולטן ויטמין D, לנטייה לסוכרת מסוג 2[22]. מגוון הפגמים המטבוליים שבבסיס הפתוגנזה של סוכרת מסוג 2 בא לידי ביטוי במנגנוני הפעולה האפשריים (Potential) של ויטמין D בהקשר של סוכרת מסוג 2[23]:
- חסר בוויטמין D נקשר בירידה בהפרשת אינסולין. נמצא שטיפול בוויטמין D או בחליף הפעיל שלו, D2(OH)1,25, משפר את הפרשת האינסולין מאיי הלבלב. הפעילות עשויה להיות ישירה - באמצעות הקולטנים לוויטמין D, שהם בעלי אתרי קישור באזורים המהווים אתרי בקרה של הגן לאינסולין[24], ו/או בעקיפין - באמצעות הגברת ייצור של אוסטיאוקלצין (Osteocalcin) שמקורו בתאים בוני עצם (Osteoblasts) בשלד[25], וכן באמצעות שמירה על מצב האיזון (Homeostasis) של סידן שנחוץ לצורך הפרשה תקינה של אינסולין
- D2(OH)1,25 עשוי להקטין את התנגודת ההיקפית לאינסולין באמצעות שפעול PPAR-γ (מנגנון מקביל לזה של תרופות מסדרת ה-Thiazolidinediones)[14] ובאמצעות העלאת הביטוי של קולטני אינסולין ושיפור מעבר גלוקוז לתאים ברקמות שונות[15],[26] [במחקרים אחרים נמצא ש-D2(OH)1,25 דווקא מעכב ביטוי של PPAR-γ ובאופן זה מעכב יצירת תאי שומן (Adipogenesis)][10]
- השפעה ממתנת על תהליכים דלקתיים התורמים להתפתחותם של סיבוכים במערכת הלב וכלי הדם (Cardiovascular) ולעיכוב התמרתם של מקרופאגים (Macrophages) לתאי קצף בדופנות כלי דם[27] , [28]
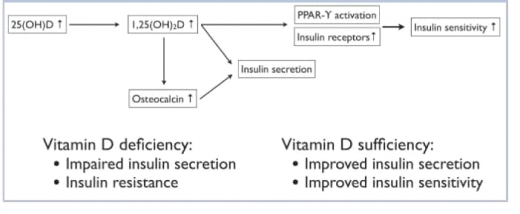
ויטמין D, באמצעות החליף הפעיל, D2(OH)1,25, מגביר יצירה של אינסולין באמצעות פעולה ישירה על תאי ביתא בלבלב ו/או בעקיפין באמצעות הגברת ייצור אוסטיאוקלצין בלבלב. במקביל קיימת הגברה של הרגישות לאינסולין באמצעות הגברת הביטוי של קולטני אינסולין בתאי שומן ושפעול מערכת PPAR
סוכרת בהיריון
כמה מחקרים חשפו ריכוז נמוך של D(OH)25 בנשים עם סוכרת היריונית[29],[30] ומתאם הפוך בין ריכוזים נמוכים של D(OH)25 למידת האיזון בנשים עם סוכרת היריונית. עם זאת, במחקר אחר שפורסם אחריהם, לא נמצא מתאם בין ריכוז D(OH)25 בדם בשליש הראשון להיריון לבין התפתחות סוכרת היריונית[21]. אין בנמצא מחקרים התערבותיים לגבי השפעת טיפול בוויטמין D או בנגזרותיו על מהלך סוכרת היריונית, למעט מחקר אחד שמצא שיפור מה ברגישות לאינסולין בעקבות טיפול תוך-ורידי באנלוג (Analog) של D2(OH)1,25 - 1 אלפא-ויטמין D (בארץ - אלפא D3) לפני העמסת סוכר, אך לא לאחר טיפול פומי בתכשיר למשך שבועיים[31].
סוכרת מסוג 1
סוכרת מסוג 1 מאופיינת בחסר מוחלט של אינסולין. סוכרת מסוג 1 היא במרבית המקרים תוצאה של תהליך חיסון עצמי (Autoimmune), שבמהלכו מתרחש תהליך דלקתי ההורס את תאי בטא (Beta cells) בלבלב וגורם לחסר באינסולין. קיימים רמזים לאפשרות של מעורבות מחוללי מחלה נגיפיים (Viral pathogens) בהתהוות המחלה. השפעה של ויטמין D ושל נגזרותיו הפעילות על הפתוגנזה (Pathogenesis) של המחלה נצפתה במחקרים בבעלי חיים ובמחקרים אפידמיולוגיים.
תצפיות בבעלי חיים
בעקבות תצפיות שהצביעו על הפרעה בספיגת סידן במעי בחולדות סוכרתיות, נמצא שרמת החליף הפעיל, D2(OH)1,25, בבעלי חיים אלו נמוכה (למרות רמות תקינות של D(OH)25), וכן שקיימת פעילות ירודה של האנזים alpha-hydroxylase-1 D3 Hydroxyvitamin-25 האחראי לייצורו. נמצא גם כי טיפול באינסולין נמצא יעיל לתיקון רמת החליף הפעיל[32].
רמזים למעורבות אפשרית של ויטמין D בסוכרת מסוג 1 התקבלו מתצפיות על השפעה מונעת של D2(OH)1,25 על התפתחות סוכרת בעכברים מסוג NOD (Non-Obese Diabetic) - מודל של סוכרת מסוג 1[33], והשפעה מגנה של D2(OH)1,25 על איי הלבלב בזמן טיפול ב-Streptozocin במינון נמוך וחוזר (אך לא כאשר ניתן במינון חד-פעמי גבוה).
ממצא בולט היה היעדר הסננת תאי דלקת באיי הלבלב (Insulitis) של החולדות שטופלו במקביל ב-D2(OH)1,25. ממצא זה פורש כהשפעה ממתנת של ויטמין D על מערכת החיסון (Immunomodulator) בלבלב[34]. לעומת זאת, חסר בוויטמין D הגביר התפתחות סוכרת בעכברי NOD בעלי נטייה עצמונית (Spontaneous) לסוכרת מסוג 1[27]. ביסוס לאפשרות זו נמצא בתצפיות שהראו השפעה ממתנת של D2(OH)1,25 על ביטוי ציטוקינים (Cytokines) ועל הסננה דלקתית באיי לבלב בעכברי NOD שהם מודל לסוכרת מסוג חיסון עצמי[35].
מחקרים אפידמיולוגיים ומחקרי התערבות
מחקרי אוכלוסיות הצביעו על שכיחות גבוהה יותר של סוכרת מסוג 1 באזורים מרוחקים מקו המשווה[36]. מחקרים אחרים הראו הופעה שכיחה יותר של סוכרת מסוג 1 בעונת החורף[37]. אחד ההסברים האפשריים לתופעה עשוי להיות קשור ברמות הנמוכות יחסית של ויטמין D בעונה זו של השנה. כמה מחקרים הצביעו על קשר הפוך בין שימוש בתוספי ויטמין D בתינוקות (עם התייחסות למינון ויטמין D ותזמון מתן התוסף - יתרון למתן בחצי השנה השנייה, לעומת ששת החודשים הראשונים לאחר הלידה) לסיכון לפיתוח סוכרת מסוג 1[38]. חיסרון בולט של המחקרים האפידמיולוגיים הללו נעוץ בעובדה שבמרביתם, לרבות אלו שבהם נבדקה השפעת תוסף, לא נבדקה רמת ויטמין D, והמסקנות לגבי רמתו נגזרו מהערכה שהסתמכה על שאלונים או על ראיונות.
זאת ועוד, נמצא קשר הפוך בין מצב מאגרי ויטמין D של האם בעת ההיריון, להארעות סוכרת מסוג 1 בצאצאים[39], אם כי הקשר בין צריכת ויטמין D לסוכרת מסוג 1 בצאצאים לא היה עקיב[40],[41].
אין מחקרים מבוקרים על השפעת ויטמין D או נגזרותיו על הארעותה של סוכרת מסוג 1 או על המהלך הקליני שלה, למעט מחקר אחד שבדק השפעת טיפול ב-D2(OH)1,25 לעומת Nicotinamide (שנרמז לגביו כבעל השפעה מגנה על תאי ביתא) בחולים בשלב מוקדם של סוכרת מסוג 1, ולא נמצאו הבדלים משמעותיים בין שתי הקבוצות[42].
הנה כי כן, מחקרים בבעלי חיים מרמזים על השפעה משמעותית של ויטמין D או של נגזרותיו הפעילות על ההתפתחות ועל המהלך של סוכרת מסוג 1. מחקרים אפידמיולוגיים תומכים במידה רבה באפשרות זו, אולם אין בנמצא מחקרים מבוקרים תומכים, והנתונים הקיימים מצביעים על השפעה קלושה, אם בכלל, של השפעת טיפול בוויטמין D על מניעה או על בלימה של סוכרת מסוג 1.
מנגנוני פעולה אפשריים של ויטמין D במניעת סוכרת מסוג 1
בהיות סוכרת מסוג 1 מחלת חיסון עצמי, ולנוכח השפעתו הממתנת של ויטמין D ושל נגזרותיו הפעילות על תאי המערכת החיסונית ועל תהליכים חיסוניים[43], המנגנון המשוער העיקרי להשפעה המונעת של ויטמין D על ההתפתחות ועל המהלך של סוכרת מסוג 1 קשור קודם כל להשפעתו על המערכת החיסונית. אפשרות זו נתמכת בתצפיות על השפעת ויטמין D ונגזרותיו במודלים של סוכרת מסוג 1 בבעלי חיים. אולם, לנוכח השערות הקושרות סוכרת מסוג 1 בזיהומים נגיפיים שונים[44], לא מן הנמנע שבתנאים מסוימים ויטמין D עשוי למנוע סוכרת מסוג 1 באמצעות השפעתו נוגדת האורגניזמים (Antimicrobial) ונוגדת הנגיפים (Antiviral)[43].
נוסף להשפעה באמצעות עצם נוכחותו ברקמות, הקשר בין ויטמין D לסוכרת מסוג 1 עשוי להיות מושפע גם מתגובתיות לקויה של תאי המטרה לוויטמין D, כתוצאה מקיומה של רב-צורתיות סגולית של הקולטן לוויטמין D בכלל, והשפעתה על המערכת החיסונית בפרט[45]. ממצא זה אינו עקיב ומשמעותו, אם בכלל, שנויה במחלוקת.
כמו בסוכרת מסוג 2, גם בסוכרת מסוג 1 היכולת של ויטמין D להשפיע על הפתוגנזה מקבלת משנה תוקף מהעובדה שאיי הלבלב מכילים את המערכת האנזימטית המאפשרת את שפעולו של ויטמין D לנגזרתו הפעילה (D2(OH)1,25), עובדה המעוררת השערות לגבי קיומו של מנגנון פעולה אוטוקריני או פאראקריני, כלומר, ויסות מקומי של ריכוז D2(OH)1,25 בתגובה למתקפה חיסונית או אורגניזמית בעלת אפשרות (Potential) הרסנית על תאי ביתא.
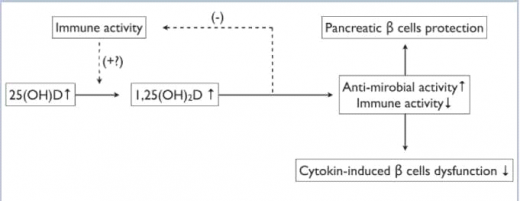
ויטמין D - באמצעות החליף הפעיל [D2(OH)1,25] - ממתן את התגובה החיסונית ומגביר פעילות נוגדת אורגניזמים, שנתפסת כאחראית להרס תאי ביתא בלבלב. לא מן הנמנע שהפעילות החיסונית בלבלב מגבירה את הייצור המקומי של [D2(OH)1,25], במעגל של היזון חוזר שאמור למתן את התגובה החיסונית המקומית. ציטוקינים מעכבים הפרשת אינסולין מתאי ביתא, והפחתת ייצורם בהשפעת [D2(OH)1,25] עשויה לשפר פעילות שיורית של תאי ביתא
הקושי בפענוח השפעתו של חסר בוויטמין D בוויסות התחלואה בסוכרת
הצְרִימָה (Dissonance) שבין ממצאים הקושרים סוכרת לוויטמין D במחקרים אפידמיולוגיים ובמחקרים בסיסיים, לבין הממצאים הדלים במחקרים התערבותיים בבני אדם, קשורה בקשיים מובנים שקיימים כיום בפענוח משמעות הקשר שבין רמת ויטמין D, וגרוע מכך - בתלות בסמנים עקיפים של רמת ויטמין D בדם (תת-חשיפה לשמש או מגורים בקו רוחב מרוחק מקו המשווה), לתחלואה חוץ-שלדית בכלל וסוכרת בפרט.
כמה נתונים מבטאים את הקושי:
- הפיזור הרחב של הנקודות המייצגות את ריכוזי הורמון בלוטת יותרת התריס סביב עקום התסוגה (Regression) - בעיקר בריכוזים נמוכים של D(OH)25 - יוצר קושי מהותי באחת מהנחות היסוד בהגדרות השונות של הרמה המיטבית (Optimal) של ויטמין D, המתבססת על קיומו של מתאם הפוך בין ריכוז D(OH)25 לבין ריכוז הורמון בלוטת יותרת התריס בדם[46]
- מחד גיסא, החליף D(OH)25, שרמתו בדם מקובלת כמייצגת את מאגרי ויטמין D, איננו החליף הפעיל ביולוגית. מאידך גיסא, ריכוזו בדם של החליף הפעיל, D2(OH)1,25, נשמר בריכוז תקין גם לאחר ירידה משמעותית במאגרי ויטמין D, כפי שמשתקפים מרמת D(OH)25. השפעול של ויטמין D ל- D2(OH)1,25 מתרחש בכליות וברקמות אחרות. בכל רקמה התהליך מבוקר באופן שונה. משתנים כגון גיל, תפקוד כלייתי, ריכוז החלבון הנושא של ויטמין D בדם[47], גנוטיפים (Genotypes) של הקולטן לוויטמין D ומוצא אתני, הם חלק מהגורמים הידועים שיכולים להשפיע על הפעילות הביולוגית של ויטמין D ברקמות
- ערפלנים (Confounders) רבים עלולים לשבש את הבנת הקשר שבין ויטמין D לתחלואות שונות, בעיקר לסוכרת
- במחקרים תצפיתיים עלו הממצאים הבאים:
- קיום מתאם הפוך בין מסת הגוף לרמת ויטמין D (שכיחות גבוהה של חסר בוויטמין D בשמנים) מצויה במקביל למתאם ישיר בין מסת הגוף למגוון רחב של תחלואות מטבוליות ושקשורות למערכת הלב וכלי הדם
- קיום מתאם ישיר בין פעילות גופנית לרמת ויטמין D, כך שלפעילות גופנית קשר בו-זמני לרמות גבוהות יותר של ויטמין D ולהשפעה בריאותית מטיבה
- חלק מהמחקרים התצפיתיים מניחים שקיים מתאם הפוך בין מרחק מקו המשווה לרמת ויטמין D - הנחה שאינה בהכרח נכונה. לפחות בחלק מהמחקרים שנעשו בארצות הברית ובאירופה נמצא היעדר השפעה של המרחק מקו המשווה, ואפילו מתאם ישיר בין מרחק מקו המשווה לרמת ויטמין D (רמת ויטמין D הייתה גבוהה יותר בארצות צפוניות)[48],[49]
- זיהום אוויר עירוני משפיע על רמת ויטמין D: זמן זהה של חשיפה לשמש מייצר כמות מופחתת של ויטמין D בתושבי עיר מאשר בתושבי אזורים כפריים[50]. בה בעת גם אורח החיים הכפרי עשוי להשפיע על הפחתת גורמי סיכון לסוכרת
- חלבון בשתן (Proteinuria) בחולים בעלי נפרופתיה סוכרתית (Diabetic nephropathy) גורם איבוד בשתן של ויטמין D הקשור לחלבון הנושא שלו, שעלול להשפיע על מאגרי ויטמין D ועל ריכוזו בדם[51]
- מצב חברתי-כלכלי (Socioeconomic status) עשוי להשפיע בו זמנית ובאופן שלילי הן על רמת ויטמין D והן על מצב הבריאות[52],[49]. האוכלוסייה הענייה מתאפיינת בתזונה לקויה ובנטייה לעודף משקל[52]. התזונה הלקויה ועודף המשקל הם גורמי סיכון משמעותיים לחסר בוויטמין D כמו גם לסוכרת מסוג 2
דגלים אדומים
ביבליוגרפיה
- ↑ Campbell IT, Jarrett RJ, Keen H. Diurnal and Seasonal Variation in Oral Glucose Tolerance: Studies in The Antarctic. Diabetologia. 1975;11:139-145.
- ↑ Schneider LE, Omdahl J, Schedl HP. Effects of Vitamin D and Its Metabolites on Calcium Transport in The Diabetic rat. Endocrinology. 1976; 99: 793-799.
- ↑ Heath Hr, Lambert PW, Service FJ, Arnaud SB. Calcium Homeostasis in Diabetes Mellitus. J Clin Endocrinol Metab. 1979; 49: 462-466.
- ↑ 4.0 4.1 Stepan J, Wilczek H, Justova V et al. Plasma 25-Hydroxycholecalciferol in Oral Sulfonylurea Treated Diabetes Mellitus. Horm Metab Res. 1982; 14:98-100.
- ↑ Christiansen C, Christensen MS, McNair P, Nielsen B, Madsbad S. Vitamin D Metabolites in Diabetic Patients: Decreased Serum Concentration of 24,25-Dihydroxyvitamin D. Scand J Clin Lab Invest. 1982; 42: 487-491.
- ↑ Wang Y, DeLuca HF. Is The Vitamin D Receptor Found in Muscle? Endocrinology. 2011;152:354-363.
- ↑ Zehnder D, Bland R, Williams MC et al. Extrarenal Expression of 25-Hydroxyvitamin d(3)-1 Alpha-Hydroxylase. J Clin Endocrinol Metab. 2001; 86: 888-894.
- ↑ Li J, Byrne ME, Chang E, et al. 1 Alpha, 25-Dihydroxyvitamin D Hydroxylase in Adipocytes. J Steroid Biochem Mol Biol. 2008; 112: 122-126.
- ↑ Sato M, Hiragun A. Demonstration of 1 Alpha, 25-Dihydroxyvitamin D3 Receptor-Like Molecule in ST 13 and 3T3 L1 Preadipocytes and Its Inhibitory Effects on Preadipocyte Differentiation. J Cell Physiol. 1988; 135: 545-550.
- ↑ 10.0 10.1 Hida Y, Kawada T, Kayahashi S, Ishihara T, Fushiki T. Counteraction of Retinoic Acid and 1,25-Dihydroxyvitamin D3 on Up-Regulation of Adipocyte Differentiation With PPARgamma Ligand, an Antidiabetic Thiazolidinedione, in 3T3-L1 Cells. Life Sci. 1998; 62: PL205-11.
- ↑ Kelly KA, Gimble JM. 1,25-Dihydroxy Vitamin D3 Inhibits Adipocyte Differentiation and Gene Expression in Murine Bone Marrow Stromal Cell Clones and Primary Cultures. Endocrinology. 1998; 139: 2622-2628.
- ↑ Norman AW, Frankel JB, Heldt AM, Grodsky GM. Vitamin D Deficiency Inhibits Pancreatic Secretion of Insulin. Science. 1980; 209: 823-825.
- ↑ Cade C, Norman AW. Vitamin D3 Improves Impaired Glucose Tolerance and Insulin Secretion in The Vitamin D-Deficient Rat in Vivo. Endocrinology. 1986; 119: 84-90.
- ↑ 14.0 14.1 Dunlop TW, Vaisanen S, Frank C, Molnar F, Sinkkonen L, Carlberg C. The Human Peroxisome Proliferator-Activated Receptor Delta Gene is a Primary Target of 1Alpha, 25-Dihydroxyvitamin D3 and Its Nuclear Receptor. J Mol Biol. 2005; 349: 248-260.
- ↑ 15.0 15.1 Maestro B, Campion J, Davila N, Calle C. Stimulation by 1,25-Dihydroxyvitamin D3 of Insulin Receptor Expression and Insulin Responsiveness for Glucose Transport in U-937 Human Promonocytic Cells. Endocr J. 2000; 47: 383-391.
- ↑ Ishimura E, Nishizawa Y, Koyama H, Shoji S, Inaba M, Morii H. Impaired Vitamin D Metabolism and Response in Spontaneously Diabetic GK Rats. Miner Electrolyte Metab. 1995; 21: 205-210.
- ↑ Kawashima H, Castro A. Effect of 1 Alpha-Hydroxyvitamin D3 on The Glucose and Calcium Metabolism in Genetic Obese Mice. Res Commun Chem Pathol Pharmacol. 1981; 33: 155-161.
- ↑ de Souza Santos R, Vianna LM. Effect of Cholecalciferol Supplementation on Blood Glucose in an Experimental Model of Type 2 Diabetes Mellitus in Spontaneously Hypertensive Rats and Wistar rats. Clin Chim Acta. 2005; 358: 146-150.
- ↑ 19.0 19.1 Pittas AG, Harris SS, Stark PC, Dawson-Hughes B. The Effects of Calcium and Vitamin D Supplementation on Blood Glucose and Markers of Inflammation in Nondiabetic Adults. Diabetes Care. 2007; 30: 980-986.
- ↑ Lau SL, Gunton JE, Athayde NP, Byth K, Cheung NW. Serum 25-Hydroxyvitamin D and Glycated Haemoglobin Levels in Women With Gestational Diabetes Mellitus. Med J Aust. 2011; 194: 334-337.
- ↑ 21.0 21.1 Makgoba M, Nelson SM, Savvidou M, Messow CM, Nicolaides K, Sattar N. First-Trimester Circulating 25-Hydroxyvitamin D Levels and Development of Gestational Diabetes Mellitus. Diabetes Care. 2011; 34: 1091-1093.
- ↑ Reis AF, Hauache OM, Velho G. Vitamin D Endocrine System and The Genetic Susceptibility to Diabetes, Obesity and Vascular Disease. A Review of Evidence. Diabetes Metab. 2005; 31: 318-325.
- ↑ Pittas AG, Lau J, Hu FB, Dawson-Hughes B. The Role of Vitamin D and Calcium in Type 2 Diabetes. A systematic Review and Meta-Analysis. J Clin Endocrinol Metab. 2007; 92: 2017-2029.
- ↑ Maestro B, Davila N, Carranza MC, Calle C. Identification of a Vitamin D Response Element in The Human Insulin Receptor Gene Promoter. J Steroid Biochem Mol Biol. 2003; 84: 223-230.
- ↑ Lee NK, Sowa H, Hinoi E et al. Endocrine Regulation of Energy Metabolism by The Skeleton. Cell. 2007; 130: 456-469.
- ↑ Calle C, Maestro B, Garcia-Arencibia M. Genomic Actions of 1,25-Dihydroxyvitamin D3 on Insulin Receptor Gene Expression, Insulin Receptor Number and Insulin Activity in The Kidney, Liver and Adipose Tissue of Streptozotocin-Induced Diabetic Rats. BMC Mol Biol. 2008; 9: 65.
- ↑ 27.0 27.1 Giulietti A, Gysemans C, Stoffels K et al. Vitamin D Deficiency in Early Life Accelerates Type 1 Diabetes in Non-Obese Diabetic Mice. Diabetologia. 2004; 47: 451-462.
- ↑ Riek AE, Oh J, Bernal-Mizrachi C. Vitamin D Regulates Macrophage Cholesterol Metabolism in Diabetes. J Steroid Biochem Mol Biol. 2010; 121: 430-433.
- ↑ Soheilykhah S, Mojibian M, Rashidi M, Rahimi-Saghand S, Jafari F. Maternal Vitamin D Status in Gestational Diabetes Mellitus. Nutr Clin Pract. 2010; 25: 524-527.
- ↑ Kuoppala T. Alterations in Vitamin D Metabolites and Minerals in Diabetic Pregnancy. Gynecol Obstet Invest. 1988; 25: 99-105.
- ↑ Rudnicki PM, Molsted-Pedersen L. Effect of 1,25-Dihydroxycholecalciferol on Glucose Metabolism in Gestational Diabetes Mellitus. Diabetologia. 1997; 40: 40-44.
- ↑ Spencer EM, Khalil M, Tobiassen O. Experimental Diabetes in The Rat Causes an Insulin-Reversible Decrease in Renal 25-Hydroxyvitamin D3-1 Alpha-Hydroxylase Activity. Endocrinology. 1980; 107: 300-305.
- ↑ Mathieu C, Laureys J, Sobis H, Vandeputte M, Waer M, Bouillon R. 1,25-Dihydroxyvitamin D3 Prevents Insulitis in NOD Mice. Diabetes. 1992; 41: 1491-1495.
- ↑ Inaba M, Nishizawa Y, Song K et al. Partial Protection of 1 Alpha-Hydroxyvitamin D3 Against The Development of Diabetes Induced by Multiple Low-Dose Streptozotocin Injection in CD-1 Mice. Metabolism. 1992; 41: 631-635.
- ↑ Gysemans CA, Cardozo AK, Callewaert H et al. 1,25-Dihydroxyvitamin D3 Modulates Expression of Chemokines and Cytokines in Pancreatic Islets: Implications for Prevention of Diabetes in Nonobese Diabetic Mice. Endocrinology. 2005; 146: 1956-1964.
- ↑ Mohr SB, Garland CF, Gorham ED, Garland FC. The Association Between Ultraviolet B Irradiance, Vitamin D Status and Incidence Rates of Type 1 Diabetes in 51 Regions Worldwide. Diabetologia. 2008; 51: 1391-1398.
- ↑ Fishbein HA, LaPorte RE, Orchard TJ, Drash AL, Kuller LH, Wagener DK. The Pittsburgh Insulin-Dependent Diabetes Mellitus Registry: Seasonal Incidence. Diabetologia. 1982; 23: 83-85.
- ↑ Zipitis CS, Akobeng AK. Vitamin D Supplementation in Early Childhood and Risk of Type 1 Diabetes: A Systematic Review and Meta-Analysis. Arch Dis Child. 2008; 93: 512-517.
- ↑ Sorensen IM, Joner G, Jenum PA, Eskild A, Torjesen PA, Stene LC. Maternal Serum Levels of 25-Hydroxy-Vitamin D During Pregnancy and Risk of Type 1 Diabetes in The Offspring. Diabetes. 2012; 61: 175-178.
- ↑ Marjamaki L, Niinisto S, Kenward MG et al. Maternal Intake of Vitamin D During Pregnancy and Risk of Advanced Beta Cell Autoimmunity and Type 1 Diabetes in Offspring. Diabetologia. 2010; 53: 1599-1607.
- ↑ Brekke HK, Ludvigsson J. Vitamin D Supplementation and Diabetes-Related Autoimmunity in The ABIS Study. Pediatr Diabetes. 2007; 8: 11-14.
- ↑ Pitocco D, Crino A, Di Stasio E et al. The Effects of Calcitriol and Nicotinamide on Residual Pancreatic Beta-Cell Function in Patients With Recent-Onset Type 1 Diabetes (IMDIAB XI). Diabet Med. 2006; 23: 920-923.
- ↑ 43.0 43.1 White JH. Vitamin D Signaling, Infectious Diseases, and Regulation of Innate Immunity. Infect Immun. 2008; 76: 3837-3843.
- ↑ Richer MJ, Horwitz MS. Preventing Viral-Induced Type 1 Diabetes. Ann N Y Acad Sci. 2009; 1173: 487-492.
- ↑ Pani MA, Knapp M, Donner H et al. Vitamin D Receptor Allele Combinations Influence Genetic Susceptibility to type 1 Diabetes in Germans. Diabetes. 2000; 49: 504-507.
- ↑ Vieth R, Ladak Y, Walfish PG. Age-related Changes in The 25-Hydroxyvitamin D Versus Parathyroid Hormone Relationship Suggest a Different Reason Why Older Adults Require More Vitamin D. J Clin Endocrinol Metab. 2003; 88: 185-191.
- ↑ Powe CE, Ricciardi C, Berg AH et al. Vitamin D-Binding Protein Modifies The Vitamin D-Bone Mineral Density Relationship. J Bone Miner Res. 2011; 26: 1609-1616.
- ↑ Holick MF, Siris ES, Binkley N et al. Prevalence of Vitamin D Inadequacy Among Postmenopausal North American Women Receiving Osteoporosis Therapy. J Clin Endocrinol Metab. 2005; 90: 3215-3224.
- ↑ 49.0 49.1 Kuchuk NO, van Schoor NM, Pluijm SM, Chines A, Lips P. Vitamin D Status, Parathyroid Function, Bone Turnover, and BMD in Postmenopausal Women With Osteoporosis: Global Perspective. J Bone Miner Res. 2009; 24: 693-701.
- ↑ Manicourt DH, Devogelaer JP. Urban Tropospheric Ozone Increases The Prevalence of Vitamin D Deficiency Among Belgian Postmenopausal Women With Outdoor Activities During Summer. J Clin Endocrinol Metab. 2008; 93: 3893-3899.
- ↑ Thrailkill KM, Jo CH, Cockrell GE, Moreau CS, Fowlkes JL. Enhanced Excretion of Vitamin D Binding Protein in Type 1 Diabetes: A Role in Vitamin D Deficiency? J Clin Endocrinol Metab. 2011; 96: 142-149.
- ↑ 52.0 52.1 Ludwig J, Sanbonmatsu L, Gennetian L et al. Neighborhoods, Obesity, and Aiabetes-a Randomized Social Experiment. N Engl J Med. 2011; 365: 1509-1519.
קישורים חיצוניים
- ויטמין D וסוכרת – פאטה מורגנה קלינית?, מדיקל מדיה
המידע שבדף זה נכתב על ידי פרופ' יאיר ליאל, מנהל היחידה לאנדוקרינולוגיה, המרכז הרפואי האוניברסיטאי סורוקה, באר שבע


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק