אימונותרפיה למחלת הודג'קין
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| אימונותרפיה למחלת הודג'קין | ||
|---|---|---|
| יוצר הערך | פרופ' עירית אביבי | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לימפומה
לימפומת הודג'קין, הקרויה על שמו של ד"ר תומס הודג'קין, מאופיינת על ידי תאים לימפוציטים דמוי משקפיים (תאי ריד-שטרנברג) ושכיחה בעיקר בצעירים. מרבית החולים במחלה זו נרפאים לאחר שטופלו בקו טיפול יחיד. מאידך, אלה החווים הישנות מחלתם נזקקים לטיפולים כימותרפיים נוספים כולל השתלת מח עצם עצמית.
אפשרויות הטיפול בחולים צעירים אלה אשר מחלתם נשנתה על אף הטיפולים שנמנו, בפרט לאחר השתלה עצמית, הן מוגבלות ותוחלת חייהם היא על פי רוב קצרה. מתן ברנטוקסימאב ודוטין - BV (Brentuximab vedotin) - נוגדן מכוון כנגד CD30 על פני תאי ההודגקין, מצומד ל-MMAE, מביא לתגובה ב-75 אחוזים מהמטופלים ולהשגת הפוגה מלאה בכשליש מהם, אך משך התגובה על פי רוב קצר (כ-6-5 חודשים עבור כלל המגיבים, ו-20.5 חודשים במטופלים אשר השיגו הפוגה מלאה). חלק מהחולים מועמדים בשלב זה להשתלה מתורם, אך חלק גדול אינם משיגים תגובה מספקת על-אף טיפול ב-BV או שמצבם הכללי אינו מאפשר טיפול באמצעות השתלת מח עצם מתורם. השתלה מתורם מביאה להפגה ממושכת בכשליש מהחולים בלבד.
אחד הטיפולים החדשים והיעילים שהתווספו כטיפול במחלת הודג'קין ואשר אושרו לשימוש על ידי ה-FDA (Food and Drug Administration) הוא טיפול אימונותרפי המפעיל את תאי מערכת החיסון של המטופל כנגד תאי הודג'קין הממאירים.
בלימפומת הודג'קין, אחוז נמוך בלבד מהתאים בבלוטת הלימפה המוגדלת הם תאים ממאירים, והם מוקפים בתאי דלקת ותאי מערכת חיסון מרובים. מסתבר עם זאת שתאי חיסון אלה אינם מצליחים לפעול כנגד תאי ההודג'קין ולהשמידם. אחד השינויים הגנטיים שתאי ההודג'קין עוברים במהלך הפיכתם מתאים לימפתיים בריאים לתאים חולים, מערב אמפליפיקציה של מקטע בכרומוזום 9, האחראי על ביטוי יתר של חלבון "משתק" חיסונית" Program Death Ligand 1 (PDL1) על פני תאי ההודג'קין. חלבון זה נקשר לרצפטור ייחודי (PD1) על פני התאי ה-T התוקפים של המטופל וגורם לתאי ה-T לאבד זמנית את יכולתם לתקוף את תאי ההודג'קין (תרשים מספר 1).
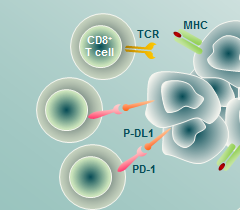
שימוש בנוגדן הנקשר לחלבון ה-PD1 מונע מהחלבון ה"משתק" (PDL1) על פני תאי ההודג'קין מלהיקשר ל-PD1 על פני תאי ה-T ומביא להתעוררות תגובה חיסונית כנגד תאי המחלה (תרשים מספר 2).
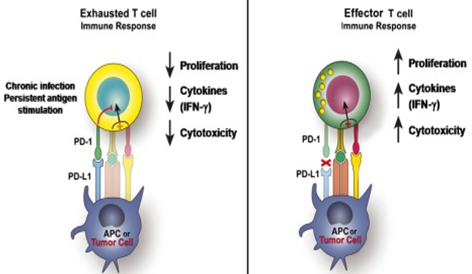
מימין, שימוש בנוגדן כנגד PD1 מביא לשחזור יכולתם של תאי ה-T לתקוף את תאי הגידול
מחקרים שפורסמו והוצגו אשר בדקו יעילות נוגדן כנגד PD1 בחולי הודג'קין אשר מחלתם נשנתה או לא הגיבה לטיפולים קודמים, כולל השתלה עצמית וטיפול בברנטוקסימאב ודוטין, הצביעו על יעילות גבוהה ביותר של טיפול זה.
מחקר (KYNOTE-087 ASCO 2016), אשר בדק יעילות נוגדן כנגד PD1 הקרוי Pembrolizumab ב-120 חולי הודג'קין נשנית/ עמידה לטיפול (60 חולים אשר מחלתם נשנתה על אף השתלה עצמית ו-BV, 60 נוספים אשר מחלתם נשנתה לאחר השתלה עצמית וטרם קיבלו BV, ו-60 חולים שאינם מועמדים להשתלה, אשר מחלתם לא הגיבה לקווי טיפול בהישנות, כולל BV) הצביע על שיעורי תגובה גבוהים ביותר: ORR (Objective Response Rate)=83 אחוזים עם CR (Complete Response)=30.
שיעור התגובה בחולים אשר מחלתם התקדמה לאחר השתלה עצמית (עם או ללא טיפול קודם ב-BV) היה כ-73 אחוזים ובאלה שלא טופלו בהשתלה מהיותם לא מתאימים לטיפול כימותרפי גבוה, שיעור התגובה היה גבוה אף יותר (83 אחוזים). כ-30 אחוזים מהחולים ב-3 הקבוצות השיגו הפוגה מלאה של מחלתם, וב-10 אחוזים בלבד מכלל המטופלים, חלה התקדמות מחלתם על אף הטיפול.
תופעות הלוואי של טיפול זה הן על פי רוב קלות ומקורן בתגובה אוטואימונית.
תופעות הלוואי המשמעותיות ביותר הן: פריחה עורית, על כל דרגותיה המתוארת ב-4 אחוזים. פנאומוניטיס דרגה 2, המתוארת ב-2 אחוזים וקוליטיס דרגה 3 ב-1 אחוזים מהמטופלים.
מחקר דומה שפורסם ב-NEJM (New England Journal of Medicine) אשר בדק תכשיר נוסף (Nivolumab) כנגד PD1 בקרב 23 חולי הודג'קין, 78 אחוזים לאחר שטופלו ב-BV ו-78 אחוזים לאחר השתלה עצמית, תיאר שיעורי תגובה גבוהים ביותר: 87 אחוזים תגובה, כולל הפוגות מלאות.
חלק מהחולים אשר משיגים הפוגה חלקית בלבד שומרים על תגובה לאורך זמן. 83 אחוזים מהמטופלים נותרו בחיים לאחר מעקב של שנה וחצי, ממצא מעודד ביותר בהתחשב בכך שמדובר במטופלים אשר מחלתם נשנתה לאחר מספר קווי טיפול רב, כולל טיפולים ביולוגיים והשתלת מח עצם עצמית, ואשר הישרדותם הצפויה נאמדה כקצרה יותר.
לסיכום, לטיפול זה יש יעילות ניכרת בחולים במחלת הודג'קין, בפרט מתקדמת. טיפול זה הודגם כמביא לתגובה משמעותית במרבית המטופלים עם לימפומת הודג'קין שנשנתה על אף קווי טיפול רבים, ומלווה בתופעות לוואי מעטות יחסית.
טיפול זה הודגם כיעיל גם ב-40 אחוזים מהחולים עם לימפומה מדיאסטיינלית ראשונית נשנית/עמידה לקווי טיפול (ASCO 2016 - American Society of Clinical Oncology) ואף בחלק מהמטופלים הסובלים מלימפומה אגרסיבית של תאי B ולימפומה אינדולנטית.
בחולי הודג'קין לימפומה הסובלים ממחלה מתקדמת, מקובל לתת את הטיפול עד התקדמות מחלתם, אך אין היום מידע ברור האם גם בחולים שהשיגו תגובה משמעותית, בפרט מלאה, יש צורך בהמשך טיפול לפרק זמן בלתי מוגבל.
ביבליוגרפיה
קישורים חיצוניים
המידע שבדף זה נכתב על ידי פרופ' עירית אביבי, מנהלת המערך ההמטולוגי, המרכז הרפואי תל אביב ע"ש סוראסקי


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק