גליצנטין - Glicentin
| מדריך בדיקות מעבדה | |
| גליצנטין | |
|---|---|
| Glicentin | |
| מעבדה | כימיה בדם |
| תחום | תפקיד גליצנטין במצבי רעב ושובע. |
| טווח ערכים תקין | 18.6±2.4 פיקומול/ליטר בדם בצום. |
| יוצר הערך | פרופ' בן-עמי סלע |
הורמונים גסטרו-אינטסטינליים הם משפחה גדולה של פפטידים שונים המופרשים במערכת העיכול, כולל בקיבה, במעי הדק, ובמעי הגס, כמו גם מהפנקריאס (Murphey ו-Brown ב-Nature משנת 2006, Holst ב-Curr Opin Pharmacol משנת 2013, Sala וחב' ב-Diabetol Metab Syndr משנת 2014, ו-Baggio ו-Drucker משנת 2007). הורמונים אלה משחקים תפקיד מרכזי במבחר גדול של תהליכים פיזיולוגיים, הכוללים פיקוח על תיאבון, ויסות של המטבוליזם של גלוקוז ושל ליפידים ותנועות המעיים. חלק מהורמונים אלה הם תולדה של קודמנים פרו-הורמונליים, החסרים פעילות הורמונלית ומייצגים בדרך כלל צורה לא-פעילה של ההורמונים, ומשופעלים במהלך שינויים בתר-תרגומיים. פרוגלוקגון הוא ארכי-טיפוס של פרו-הורמון. בשעה שהתפקידים של חלק מחברי משפחת הפרוגלוקגון, כגון GLP-1 ו-GLP-2 ו-oxyntomodulin מתועדים היטב, glicentin נחקר באופן מועט.
הביוגנזה של glicentin
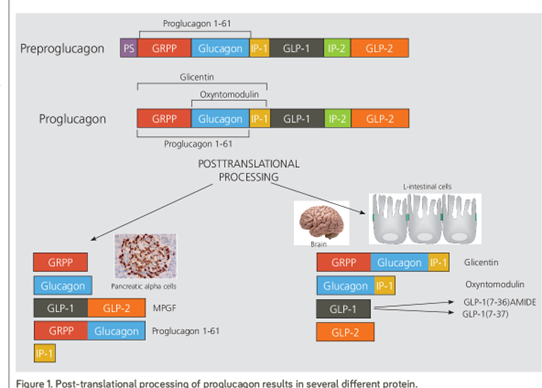
Glicentin שייך לפפטידים שמקורם ב-proglucagon, שהגן שלו מבוטא בעיקר בתאי αב של הלבלב האנדוקריני, כמו גם בתאי L במעיים (Holst ב-Ann Rev Physiol משנת 1997). הגן המקודד ל-proglucagon ממוקם על כרומוזום 2 והוא מורכב מ-6 אקסונים ומ-5 אינטרונים. שעתוק הגן מוביל ל-mRNA המתורגם ל-proglucagon שהוא חלבון קודמן בעל 178 חומצות אמינו. בה בשעה שהמבנה של proglucagon זהה בלבלב ובמעיים, העיבוד הבתר-תרגומי שלו שונה בשתי רקמות אלו, מה שמוביל לפפטידים שונים, עם תפקודים ביולוגיים שונים.
באופן סכמטי, הבשלות של הלבלב קשורה לאנזים proconvertase 2 בתהליך בו נוצרים 4 תוצרים עיקריים: glicentin related pancreatic polypeptide (להלן GRPP), גלוקגון, intervening peptide-1 (להלן IP-1) ו-major proglucagon fragment (להלן MPF) (Bataille ב-J Mol Med משנת 2007, ו-Whiting וחב' ב-Physiol Rep משנת 2015). בתאי L האנתרו-אנדוקריניים, העיבוד הבתר-תרגומי של proglucagon המתבצע על ידי proconvertases 1 ו-proconvertases 3 מביא לשחרור glicentin בנוסף ל-oxyntomodulin ,IP-2 ,GLP-1 ו-GLP-2. הצורה הבשלה של glicentin כוללת 69 חומצות אמינו ומכילה את הרצפים המלאים של glucagon ושל oxyntomodulin (Timm ו-Moody ב-Regul Pept משנת 1981). כיוון שתאי L האנתרו-אנדוקריניים נמצאים בין התריסריון עד לחלחולת, glicentin יכול להיות מסונתז לאורך כל צינור העיכול. אף-על-פי-כן, תאי L נדירים לפני ה-ileum הטרמינלי, ומחקרים במודלים של חיות גילו שהריכוזים הרקמתיים של oxyntomodulin ושל glicentin גבוהים יותר באילאום הדיסטלי, ב-caecum ובמעי הגס הפרוקסימלי בהשוואה לתריסריון ול-jejunum הפרוקסימלי (Gunawardena וחב' ב-Int J Exp Pathol משנת 2011, ו-Albrechtsen וחב' ב-BMC Res Notes משנת 2016). תוצאות אלה מעידות על כך שהמעי הדק הדיסטלי והמעי הגס הפרוקסימלי הם האתרים העיקריים לסינתזה של glicentin. הגן של proglucagon מבוטא גם על ידי נוירונים ספציפיים ב-CNS.
Glicentin והפיזיולוגיה של המעי
מחקרים במספר מודלים של חיות כגון חזירונים, כלבים וחולדות גילו את תפקידו של glicentin בפיזיולוגיה של המעי. ראשית, הפרשת glicentin מגורה על ידי צריכת מזון, כפי שנמצא על ידי רמות glicentin מוגברות בפלזמה לאחר החדרת גלוקוז, ליפידים, וחומצות אמינו לתוך התריסריון (Ohneda וחב' ב-Diabetes Res Clin Pract משנת 2016, ו-Ohneda באותו כתב עת משנת 1987). מספר מחקרים במודל של חולדה הבהירו את התפקיד של glicentin בתאי רירית המעי. אכן, מספר פרמטרים של שגשוג הרירית, כולל משקלה, כמות ה-DNA והחלבון בתוכה, alkaline phosphatase ופעילות ornithine decarboxylase נמצאו ב-jejunum לאחר הזרקה תת-עורית של glicetin (Myojo וחב' ב-J Gastroenterol משנת 1997).
מחקרים in vitro אישרו את התפקיד הפרוליפרטיבי של glicentin בשורת תאים אפיתליאליים מסוג IEC-6. מחקר אחר הראה את השפעתו של glicentin במעי הדק, עם השפעה יותר בולטת ב-ileum (Sasaki וחב' ב-Aliment Pharmacol Ther משנת 2001). תוצאות הטרוגניות אלו, יכולות להיות מוסברות על ידי הבדלים בשיטות המחקר, כולל האכלת החולדות, ריכוז ה-glicentin והחדרתו. נמצאה ירידה ב-crypt fission ב-ileum לאחר החדרת glicentin. ההרחבה של מוטציות סומטיות באפיתל של המעי הגס באדם מתבצעת דרך crypt fission. תהליך בו ה-crypt הפרנטלי מתחלק ויוצר שתי קריפטות בנות. חלוקת הקריפטות היא בשיעור נמוך במעי הגס של אנשים בריאים, ושכיחה יותר במצבי מחלה שונים. התצפית לפיה glicentin כרוך במנגנונים המפקחים על התפתחות הרירית וחידושה, הביא חוקרים אחדים לבחון את השפעת glicentin על התגובה האדפטיבית לכריתת המעי (Hirotani וחב' ב-Ann N Y Acad Sci משנת 1998). עלייה משמעותית במשקל של מה שנותר מהתריסריון, משקל הרירית, רמת החלבון ופעילות האנזים diamine oxidase, נמצאו בחולדות שעברו כריתה של 70% של המעי הדיסטלי, ואשר קיבלו glicentin בהשוואה לחולדות ביקורת. תוצאות אלה מדגישות את ההשפעה התזונתית של glicentin במעי לאחר ניתוח.
מחקרים אחדים מצביעים על ההשפעה של glicentin בהיכנסו למנגנונים הפיזיולוגיים. מספר חוקרים ניסו לברר האם ההשפעה התזונתית של glicentin תווכה על ידי מסלולים הכרוכים בגורמים של נהור המעי או כאלה שאינם כרוכים בו (Hashimoto וחב' ב-J Pediatr Surg משנת 2003). על מנת להשיג מטרה זו, הם עשו שימוש במודל של חולדה עם בְּנִיָּה של לולאות ב-jejunum ופיסטולות ב-ileum שמקורן בנהור המעי. הם מצאו גידול ברירית של הפיסטולות של ה-ileum כמו גם ב-jejunum, מה שמצביע על האפשרות שהשפעת glicentin על רירית המעי הפרוקסימלי נגרמת על ידי שילוב של גורמים נהוריים ולא-נהוריים. לעומת זאת, glicentin עודד את השגשוג של רירית ה-ileum, אך היה ללא השפעה על פיסטולות של ה-ileum, שמשמעותם שהשפעת glicentin על רירית ה-ileum יכולה להיות מושפעת על ידי תכולת הנהור ועל ידי הפרשות אנדוגניות. תוצאות אלו מצביעות על כך שקיים הבדל בין ההשפעה התזונתית של glicentin על הרירית של ה-jejunum הפרוקסימלי ועל זו של ה-ileuim הדיסטלי. בנוסף, ההשפעה של glicentin רקומביננטי על חדירת חיידקים כגון סלמונלה אנטריטידיס, E. coli ואנטרוקוקוס פקאליס על ידי שורת התאים האנטרוציטים NT407 נמדדה (Chiba וחב' ב-Pediatr Surg Int משנת 2007). מחקר זה הראה חדירת חיידקים נמוכה יותר על ידי אנטרוציטים מטופלים עם glicentin בהשוואה לתאים אלה ללא טיפול עם glicentin, מה שמצביע על השפעה מעכבת של glicentin על פלישת חיידקים.
מחקרים in vivo במודלים של חיות הציעו על השפעה של glicentin על התנועתיות של המעיים, כפי שהודגם על ידי ירידה של משך הפעילות המיו-חשמלית בשלב שלאחר ארוחה בתריסריון וב-jejunum של חולדות שעברו עירוי על ידי glicentin (Pellissier וחב' ב-Neurogastroenterol Motil משנת 2004). מחקרים ex vivo תוך שימוש ברצועות של שריר נורמלי של ה-jejunum, הצביעו אף הם על ההשפעה המעכבת של glicentin על תגובת הכיווץ לאחר חסימה של העצב האדרנגי והכולינרגי (Tomita וחב' ב-Hepatogastroenterology משנת 2005). מנגד, מחקרים על תאי שריר חלק שבודדו מה-antrum של קיבת ארנבות גילה את ההשפעה המעודדת של glicentin על התכווצות שריר (Rodier וחב' ב-Endocrinology משנת 1999). באופן דומה למה שנמצא תוך שימוש בתאי שריר חלק מהאנטרום של ארנבת, על כיווץ של השריר החלק שבודדו מהמעי הגס באדם, שהשפעה זו עוכבה לאחר הדגרה עם exendin (Ayachi וחב' ב-Neurogastro enterol Motil משנת 2005). תוצאות אלו מצביעות על תפקיד מעודד של glicentin בכווץ תאי שריר חלק בצינור העיכול, השפעה שעשויה לכרוך את הקולטן של GLP-1. לבסוף, מחקר בחולדות גילה את ההשפעה המעכבת של glicentin על הפרשת חומצת קיבה. בהתבסס על השפעתו בקיבה, מספר חוקרים ניסו לבחון את התפקיד של glicentin ב-metaplasia (התמרה של סוג תאים והפיכתו לסוג תאים אחר) והשפעתו על ההדבקה של Helicobacter pylori (Ishihara וחב' ב-Scand J משנת 1997). שימוש בביופסיות של הקיבה גילה שביטוי של mRNA של glicentin היה כרוך במטפלזיה של תאי המעי כמו גם כרוך בהדבקות עם החיידק הליקובקטר.
Glicentin והמטבוליזם של גלוקוז
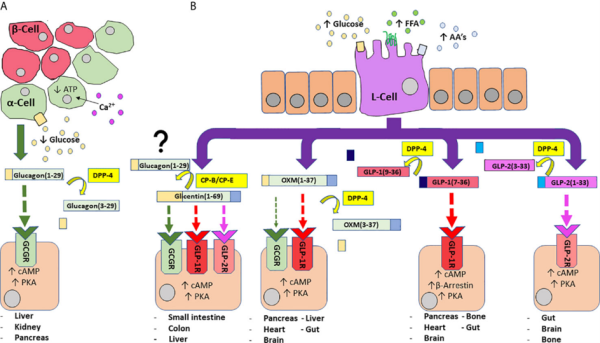
גלוקגון ידוע בשל פעולתו ההיפר-גליקמית. לעומת זאת, הורמונים הנובעים מגלוקגון הנוצרים במעי מאזנים ישירות את פעולת גלוקגון על ידי פעולתם ההיפו-גליקמית. GLP-1 מעודד הפרשת אינסולין, משפר את הרגישות לאינסולין ומדכא את הפרשת גלוקגון. Oxyntomodulin גם כן משפיע חיובית על הפרשת אינסולין. התפקיד של GRPP במטבוליזם של גלוקוז נחקר פחות והוא שנוי יותר במחלוקת. לפני מספר עשרות שנים, Ohneida וחב' הבחינו בעלייה ברמת אינסולין בפלזמה ביחד עם ירידה ברמת גלוקגון לאחר החדרת GRPP לתוך העורק הפנקריאטי-תריסריוני בכלבים, מה שמצביע על השפעה דמוית incretin (Ohneida ו-Ohneida ב-Tohoku J Exp Med משנת 1988). היה דווח על כך ש-GRPP עיכב את הפרשת אינסולין בעידוד גלוקוז מהלבלב של חולדות מבוגרות. אי הסכמה בין שני הדיווחים מצביעה על הצורך לחקור היטב את התפקיד הספציפי של כל חבר במשפחת ה-proglucagon. בהקשר זה נחקרה גם השפעת glicentin. מחקר ראשון מצא ש-glicentin מעודד את הפרשת גלוקוז מהפטוציטים של חולדות, השפעה הדומה למה נמצא לאחר הדגרה עם גלוקגון (Thieden וחב' ב-Biochim Biophys Acta משנת 1981). חוקרים אלה מצאו שבמהלך הדגרה עם הפטוציטים, glicentin התפרק למקטעים בעלי משקל מולקולרי נמוך, שחלקם היו מאוד דומים לגלוקגון, מה שהעלה את השאלה האם glicentin יכול להשפיע בדומה לגלוקגון. למעשה, מספר מחקרים עדכניים יותר in vivo, הראו שהחדרת glicentin הביאה לעלייה ברמת אינסולין בפלזמה, ולהפחתת רמת גלוקגון. לפיכך, בדומה ל-GLP-1 ול-oxyntomodulin ל-glicentin יש השפעה אינסולינו-טרופית ודמוית incretin.
Glicentin בצירקולציה של האדם
בגלל מבנהו, קביעת הריכוזים של glicentin בצירקולציה מאתגרת בקביעת מדידה ספציפית, בגלל הדמיון שלו לפפטידים אחרים של פרוגלוקגון. אכן, הפפטיד glicentin מכיל את הרצף המלא של גלוקגון, של GRPP ושל oxyntomodulin. היעדר ערכות מסחריות למדידת glicentin מסביר את הספרות הדלה על glicentin בצירקולציה. הדיווחים הראשונים שחקרו ריכוז glicentin בצירקולציה, עשו שימוש ב-radioimmunoassay לא-מסחרי, הכרוך בכרומטוגרפיה (Orskiov וחב' ב-J Clin Invest משנת 1991, או בשיטת ELISA לא-מסחרית (Tadokoro וחב' ב-Acta Pediatr משנת 2003, ו-Shimizu וחב' ב-J Pediatr Child Health משנת 2006). במדידה העדכנית ביותר נעשה שימוש בשני נוגדנים כנגד הרצפים של GRPP ושל גלוקגון שנתנו תוצאה יותר ספציפית לקביעת רמת glicentin. בהתבסס על ממצאים אלה פותחה two-site enzyme ELISA על ידי חברת Mercodia באופסלה, שנעשה בה שימוש במספר מחקרים (Manell וחב' ב-J Clin Endocrinol Metab משנת 2016, ו-Raffort וחב' ב-Ann Clin Biochem משנת 2017). לבסוף, פותחה ערכת ELISA מסחרית נוספת על ידי חברת Merck-Millipore ושמשה במחקר אחד (Pendharkar וחב' ב-Clin Transl Gastroenterol משנת 2017). שיטות ELISA אלה הן בעלות סף רגישות לגילוי glicentin בריכוז של 3 פיקוגרם/ליטר. על פי היצרנים, אנזימים דוגמת פרוטאז ואסטראז לא השפיעו על דיוק מדידה, בנוכחות מעכב דוגמת DPP-4.
המחקרים שפורסמו אישרו את ההשפעה של גלוקוז על הפרשת glicentin. בדומה למה שהושג במחקרים בחיות, אכילת מזון מעודדת הפרשת glicentin כמון שנמצא גם בילדים. מספר חוקרים בחנו ילדים מלידתם ועד גיל 15 שנה, וגילו הבדלים ניכרים בהפרש glicentin בהתאם לגיל. נתון אחר הוא שלא נמצא כל קשר בין רמות glicentin ורמת ה-BMI. נראה שהשפעת ההומאוסטאזיס על הפרשת glicentin נובעת ממכניזמים מורכבים שאינם ברורים עדיין. גם אם צריכת גלוקוז מעודדת הפרשת glicentin, לא נמצאה קורלציה ליניארית בין רמת glicentin בצום, לבין רמת גלוקוז בפלזמה. פרט לכך, בבני נוער עם obesity וסוכרת type 2 היחס בין glicentin לגלוקגון, וכן היחס בין GLP-1 לגלוקגון בצום ולאחר OGTT (שהוא oral glucose tolerance test שקובע כיצד הגוף מעבד גלוקוז), היו נמוכים יותר בהשוואה לבני נוער obese עם צינור נזו-גסטרי. מטופלים obese היו בעלי רמות נמוכות יותר של glicentin בהשוואה לאלה הרזים כביקורת. יתרה מכך עלייה משמעותית ברמת glicentin נמצאה במטפלים obese שעברו ניתוח בריאטרי 6 ו-12 חודשים לאחר הניתוח. מטופלים העוברים מעקף קיבה מסוג Roux-en-Y (להלן RYGB) בו מקטינים את גודל הקיבה לכיס קטן הושוו למטופלים שעברו בלפרסקופיה sleeve gastrectomy (להלן SLG) על ידי כריתה מאורכת של הקיבה. LSG היא פרוצדורה מוגבלת בעוד ש-RYGB כרוכה בהשפעות מוארכות ומגבילות ספיגה. ההגדלה של glicentin לאחר הניתוח, בולטת יותר לאחר RYGB בהשוואה ל-LSG. לפיכך, ניתוח בריאטרי נראה של מה שמשחזר לפחות חלקית את הפרשת glicentin. תוצאות אלו מאששות את הממצאים במודלים של חיות, לפיהם המעי הדק עשוי להיות המקור העיקרי ליצירת glicentin. לבסוף, ניתוח בריאטרי הוכיח את יעילותו בשיפור מפגעים מטבוליים שמקורם ב-obesity (Sjöström וחב' ב-New England Journal of Medicine משנת 2004).
במאמר שהתפרסם ב-J Clin Endocrinol Metab בשנת 2024, Nielsen וחב' בחנו את התגובה לאחר ארוחה של חמישה הורמונים גסטרואינטסטינליים חשובים (GLP-1 ,ghrelin ,PYY,oxyntomodulin ו-glicentin, ביחס לאיבוד משקל, קליטת אנרגיה, והעדפת סוג מזון לאחר Roux-en-Y bypass או sleeve gastrectomy במטופלים עם obesity. החוקרים הדגימו ש־glicentin ו-oxyntomodulin הם המנבאים הטובים ביותר של איבוד משקל לאחר 6 חודשים מביצוע הפרוצדורה הכירורגית, ואיבוד של 22% מהמשקל לאחר 18 חודשים מאז פרוצדורות אלו. לסיכום, כל הראיות שלמעלה, מציעות ש-glicentin ו-oxyntomodulin יכולים להיות סמנים מועילים של תפקוד תאי-L ושל בריאות מטבולית (Kokkinos וחב' ב-Metabolism משנת 2019).
הוראות לביצוע הבדיקה
את דגימת הדם יש לסרכז ריכוזי בצנטריפוגה מקוררת, תוך 30 דקות לאחר הוצאת הדם, ואת הנוזל העליון יש להקפיא בטמפרטורה של מינוס 80 מעלות צלזיוס. רמת glicentin בנסיוב נקבעת תוך שימוש בשיטה המבוססת על ELISA בערכה תוצרת Mercodia France, FR-75001 Paris. שיטה זו היא למעשה solid phase two-site enzyme immunoassay. בשלב ההדגרה, ה-glicentin שבדגימה מגיב עם נוגדן כנגד glicentin אנושי המכיר את הרצף הפוליפפטידי של glicentin (שבט C7H9G) הקשור לבארות של פלטת midrotitre. לאחר שטיפת הבארות, מוסיפים לבארות נוגדן כנגד רצף של גלוקגון (שבט RG-OC5), המזהה את ה-glicentin הקשור לפאזה הסולידית. לאחר הריאקציה, קריאה מתבצעת באופן ספקטרו-פוטומטרי באורך גל של 450 ננומטר (Tecan Group Ltd, 8708 Männedorf, Switzerland). כל הדגימות עוברים אנליזה בדופליקטים, וכל התוצאות אמורות להתקבל בתוך הטווח האנליטי של עקומת הקליברציה (0–304 פיקומול/לליטר) ומעל סף הגילוי של 3 פיקומול/לליטר.
קטגוריה:סטטוס תזונתי


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק