מונומר מסיס של פיברין - Soluble fibrin monomer
| מדריך בדיקות מעבדה | |
| מונומר מסיס של פיברין | |
|---|---|
| Soluble fibrin monomer | |
| שמות אחרים | SFM |
| מעבדה | כימיה בדם |
| תחום | קרישת דם. |
| טווח ערכים תקין | פחות מ-8 מיקרוגרם/מ"ל. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
עזר באבחון של מצבים קדם-תרומבוטיים בעורקים או בוורידים בתרחישים פתולוגיים וקליניים שונים הכוללים disseminated intravascular coagulation או intravascular coagulation ופיברינוליזה, וניטור בתר-ניתוחי עם סיכון גדול של פקקות.
מידע קליני
מונומרים של פיברין הם תוצרי ביניים הנוצרים במהלך פרוטאוליזה של פיברינוגן על ידי תרומבין (Blombäck ב-Thromb Res משנת 1996). במהלך קואגולציה תוך-וסקולרית, רמות נמוכות של תרומבין זמינות בדם, אך כמות המונומרים של פיברין הנוצרות אינן מספיקות לעבור אגירה ליצירת פקקת, ובמקום זאת הם עוברים אסוסיאציה עם פיברינוגן או עם תוצרי פירוק של פיברינוגן ליצור קומפלקסים מסיסים (דהיינו קומפלקס של מונומר מסיס של פיברין). Disseminated intravascular coagulation (DIC)/intravascular coagulation ופיברינוליזה (ICF), המכונים ביחד כ-DIC/ICF הוא אבחון קליני. אין בדיקה בודדת שהיא רגישה לחלוטין או ספציפית ל-DIC/ICF. קומפלקס נורמלי של soluble fibrin monomer אינו שולל את הנוכחות של פקקת או של early disseminated intravascular coagulation (DIC)/intravascular coagulation ופיברינוליזה. קומפלקס של soluble fibrin monomer יכול להימצא במטופלים עם תסחיף פקקתי ורידי או עורקי. הוא יכול גם להיות מוגבר בצורה מתונה בדגימות פקקתיות. הרמות של מונומרים של פיברין יכולות להימדד ולשמש כסמן של in vivo fibrinogenesis ושפעול של קואגולציה (Rafaai וחב' ב-Thromb Haemos משנת 2018, Douxfils וחב' ב-Semin Thromb Hemost משנת 2020 ו-Farris וחב' ב-Expert Rev Clin Pharmacol משנת 2017). הם יכולים לסייע בהערכה של hypercoagulability. רמות של מונומרים של פיברין יכולות לגדול בהיריון, או במהלך צריכה של גלולות למניעת הריון המכילות אסטרוגן (Grossman וחב' ב-Am J Obstet Gynecol משנת 2016). רמות מוגברות של SFM בדם ביחד עם D-dimers בנסיוב נמצאו כמצביעים של תרומבו-אמבוליזם ורידי. זיהוי של VTE, עשוי לסייע בטיפול ב-VTE במהלך היריון ולאחר ניתוח של hepatobiliary-pancreaty (Hayashi וחב' ב-Ann Gastroenterol Surg משנת 2022).
מונומר של פיברין בפקקת ובהמוסטאזיס
מונומר של פיברין (FM) הוא תוצר ביניים בר-חלוף בקואגולציה של הדם הפועל הן כווסת פעיל של המוסטאזיס וכסמן רגיש של מצבים פרו-תרומבוטיים (Blombäck ב-Thromb Res משנת 1996). קלינית, מונומר של פיברין נמדד באופן לא ישיר כנגזרת שלו, soluble fibrin monomer. מונומר של פיברין מאפנן את יצירת תרומבין ואת הפיברינוליזה, על ידי תגובתו עם קולטנים על פני טסיות כולל integrin αIIbβ3 ו-GPVI. מונומר של פיברין נוצר בעת ביקוע של פיברינוגן על ידי תרומבין. במצב נורמלי, FM עובר אסוסיאציה עצמית ליצירת פרוטו-פיברילות ובסוף התהליך ליצירת רשת פיברין המייצב פקקות (Ząbczyk וחב' ב-Cardiovasc Res משנת 2023). עם זאת, FM שיכול להימלט מפולימריזציה מיידית, יכול להיקשר תוצרי פירוק של פיברינוגן או של פיברין, וליצור קומפלקסים של SFM (Litvinov ו-Weisel ב-Semin Thromb Hemost משנת 2016). כתוצר בקסקדה של הקואגולציה, FM מופיע בשלבים המוקדמים של יצירת פיברין על ידי תרומבין. כתוצאה מכך, FM עולה מוקדם במצבים קדם-תרומבוטיים, לרוב לפני גילוי עליות ברמת D-dimer ותוצרי פירוק אחרים של פיברין (Vogel וחב' ב-Thromb Res משנת 1996). קלינית, מצב זה מאפשר את השימוש ב-SFM כסמן קדם-תרומבוטי או כאינדיקטור מוקדם של סיכון ליצירת פקקות. מתרבות הראיות ש-FM יכול לשמש במגוון של מצבים קליניים, כולל disseminated intravascular coagulation ,VTE, שבץ ופקקת במהלך ניתוח (Dempfle ב-Thromb Haemost משנת 1999, Wada ו-Sakuragawa משנת Semin Thromb Hemost משנת 2008), ו-Refaai וחב' ב-Thromb. Haemost משנת 2018). לאחר ביקוע של פיברינוגן על ידי תרומבין, FM מייצג תוצר ביניים קריטי השומר על על מספר תכונות דמויות פיברינוגן (Risman וחב' ב-J Thromb Haemost משנת 2025). ההימצאות ברת החלוף של FM באתרים של יצירה פעילה של תרומבין, מצביעה על תפקידים רגולטוריים בשלבים המוקדמים של יצירת הפקקת. פיברין מאפנן תהליכים תרומבוטיים על ידי אינטראקציה עם טסיות ועם גורמי קואגולציה (Swieringa וחב' ב-Res Pract Thromb Haemost משנת 2018), והוא משפיע על מסלולי פרו-קואגולציה ואנטי-קואגולציה (Hulshof וחב' ב-Int J Mol Sci משנת 2021), והוא מעורב גם בתהליכי דלקת ותיקן רקמתי (Kearney וחב' ב-Thromb Hemost משנת 2022). הזהות הכפולה של FM, כמשתתף בוויסות ההמוסתטי וכאינדיקטור דיאגנוסטי רגיש של מצבים פרו-תרומבוטיים, שימשה חוקרים רבים מתחום ההמוסטאזיס.
התפקידים המרובים של פיברינוגן ושל פיברין
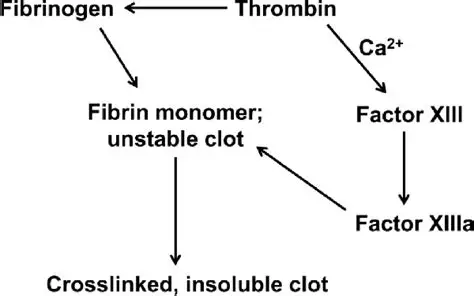
פיברין הוא המרכיב החיוני ביותר של יצירת פקקת. פיברין נוצר מפיברינוגן השכיח ביותר בדם האדם, על ידי האנזים תרומבין (Wolberg ב-J Thromb Haemost משנת 2023). היצירה של תרומבין מווסתת על ידי אינטראקציות ביוכימיות ותאיות (Versteeg וחב' ב-Physiol Rev משנת 2013). כאשר הסטימולציה מספקת, מתרחשת יצירת תרומבין, המובילה להיפוך מהיר של פיברינוגן למונומר של פיברין ולפולימריזציה. בעקבות זאת (Al Dieri וחב' ב-Blood Rev משנת 2012). תרומבין מבקע פיברינוגן תוך שהוא משחרר את הפיברינו-פפטידים A ו-B (Blombäck וחב' ב-Nature משנת 1978).
אינטראקציה בין מונומרים
אינדיבידואליים של פיברין, מביאים ליצירת אוליגומרים של פיברין ושל פרוטו-פיברילים. השחרור של פיברינו-פפטיד B משנה את הקונפורמציה של אזורי αC בפיברין, ומאפשר אגירה לטרלית של פרוטו-פיברילות ליצירת סיבים עבים יותר. תהליך הפולימריזציה מביא ליצירת רשת פיברין מסועפת (Weisel ו-Litvinov ב-Blood משנת 2013). בנוסף להמרת פיברינוגן לפיברין, תרומבין גם מווסת את יציבות הפקקת על ידי שפעול של פקטור XIIIa, (Muszbek וחב' ב-Physiol Rev משנת 2011). בצורתו המשופעלת, פקטור XIIIa קושר קו-ולנטית את שרשרות α ו-γ של פיברין ומגבירים בכך את יציבות הפקקת (Wolberg ו-Sang ב-Arteriosclr משנת 2022). פיברין כשלעצמו בעל השפעה מעכבת של יצירת תרומבין, תוך גרימת משוב רגולטורי שלילי (Mosesson ב-Thromb Haemost משנת 2003).
פיברינוגן ופיברין נוטלים חלק בתהליכים של שפעול הטסיות, איגור וספיחה על ידי תגובה עם קולטנים שונים על פני הטסיות ועם פקטור von Willebrand (van der Meijden ו-Hemskerk ב-Nat Rev Cardiol משנת 2019). נמצא שתהליך זה תלוי במידה רבה בהתקשרות התלויה בפקטור XIII, המווסת את האֲצִירָה של כדוריות דם אדומות בתוך הפקקת (Byrnes וחב' ב-Blood משנת 2015). לבסוף, רשת הפיברין היא מצע לליזיס של הפקקת הנוצרת על ידי פלזמין. המערכת הפיברינוליטית המיועדת לפתיחה של נהור (lumen) כלי הדם ולאפשר צירקולציה תקינה, מווסתת על ידי מגוון של פקטורים פלזמטיים ותאיים (Whyte וחב' ב-Semin Thromb Hemost משנת 2017, ו-Urano וחב' ב- J Thromb Haemost משנת 2018). המבנה של רשת הפיברין קובע את התכונות הפיזיקליות של הפקקת, יציבותה, האלסטיות שלה והעמידות שלה לפיברינוליזה (Feller וחב' ב-J Thromb Haemost משנת 2022).
קרישת הדם
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק