אבחון וטיפול של מיוקרדיטיס חדה - נייר עמדה - Diagnosis and treatment of acute myocarditis
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
|
| |
|---|---|
| אבחון וטיפול של מיוקרדיטיס חדה - נייר עמדה של האיגוד הקרדיולוגי הישראלי | |
| תחום | קרדיולוגיה |

| |
| האיגוד המפרסם | האיגוד הקרדיולוגי הישראלי |
| תאריך פרסום | 2023 |
| יוצר הערך | פרופ' אנדרי קרן, פרופ' רביע עאסלה, פרופ' עידו י . בירתי, דר' טוביה בן גל, פרופ' מיכאל ארד |
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – דלקת
מטרות
מיוקרדיטיס מהווה אתגר אבחוני וטיפולי עקב השונות באתיולוגיות וההסתמנות שלה. אין אחידות בניירות העמדה וההנחיות של האיגודים הקרדיולוגיים השונים לגבי הגדרת המחלה, אופן האבחון (כולל מתי לבצע ביופסיה אנדומיוקרדיאלית), והמלצות לטיפול, בפרט טיפולים מדכאי חיסון[1][2][3]. כמו כן, קיימת שונות בין המרכזים הרפואיים בישראל בגישות האבחוניות והטיפוליות לדלקת חריפה של שריר הלב. מטרת מסמך זה היא לנסח קריטריונים אבחוניים וגישות טיפוליות למיוקרדיטיס חדה, המתאימים למציאות של מערכת הבריאות הישראלית.
הגדרה
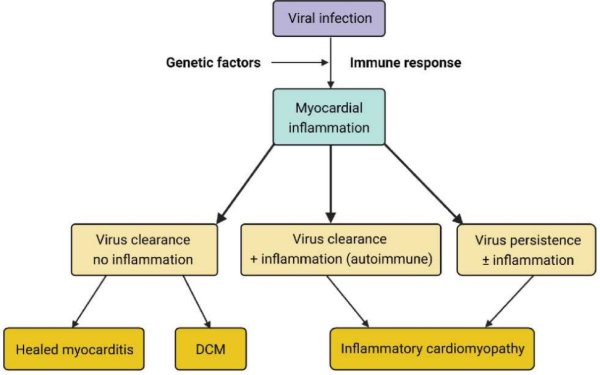
מיוקרדיטיס היא דלקת של שריר הלב הנובעת מזיהום, מחשיפה לחומרים רעילים או מתגובה אימונית ראשונית או פוסט זיהומית. האטיולוגיה השכיחה ביותר הינה נגיפית. ההתייצגות הקלינית יכולה להיות חריפה, תת-חריפה, או כרונית. התקופה החריפה של המחלה הוגדרה בעבר כעד שלושה חודשים[1][2] אך צומצמה לחודש אחד בלבד מתחילת התלונות[3]. מיוקרדיטיס תת-חריפה מתייחסת לתהליך דלקתי לבבי הנמשך בין 1-3 חדשים לאחר ההתייצגות הקלינית[3]. קרדיומיופתיה דלקתית כרונית (לשעבר "מיוקרדיטיס כרונית") מוגדרת כהמשך התהליך הדלקתי מעבר לתקופה החריפה (תרשים 1). לפיכך, תהליך דלקתי בלב הנמשך מעבר ל- 3 חודשים, ומלווה בירידה בהתכווצות שריר הלב עם או ללא הרחבת חדרי הלב יקרא קרדיומיופתיה דלקתית[4].
במיוקרדיטיס, הגורם האטיולוגי יכול לגרום לדרגות שונות של נזק ישיר לשריר הלב. במקרים אחרים, מיוקרדיטיס היא תוצאה של תגובה אימונולוגית הפוגעת בשריר הלב, אם במבודד או כחלק ממחלה דלקתית רב מערכתית, דהיינו מחלה אוטואימונית[3][4] (תרשים 1).
קריטריונים לאבחון קליני ומעבדתי
אבחנה של מיוקרדיטיס חדה יכולה להיות מורכבת. אבחנה ודאית מסתמכת על ביופסיה אנדומיוקרדיאלית. אולם, עקב הסיכון הכרוך בביופסיה, המיומנות הנדרשת לביצועה ולפיענוח הממצאים, היא אינה מבוצעת במרבית החולים עם חשד קליני למיוקרדיטיס. על כן, חשד הקליני למיוקרדיטיס (clinically suspected myocarditis) מתבסס על שילוב של ממצאים קליניים ובדיקות עזר בהעדר הסבר אלטרנטיבי לממצאים, כגון תסמונת כלילית חדה. על פי נייר העמדה של האגוד הקרדיולוגי האירופי מ-2013, חשד קליני למיוקרדיטיס חדה מתבסס על שילוב של הסתמנות קלינית (כאבים בחזה, קוצר נשימה, דפיקות לב, התעלפות, הלם לבבי או מוות פתאומי) ועדות לתהליך דלקתי או/ו נזק מיוקרדיאלי על פי אק"ג, בדיקות מעבדה (בפרט טרופונין), ובדיקות הדמיה (טבלה 1). דרוש ממצא קליני 1 או יותר וממצא 1 או יותר בבדיקות עזר לבסס חשד למיוקרדיטיס. במטופל אי תסמיני נדרשים >2 ממצאים חיוביים בבדיקות העזר. פרודרומה המתאימה לזיהום ויראלי מחזקת את החשד[1].
מאז פרסום נייר עמדה זה ב-2013 חלה התקדמות בשימוש השגרתי בבדיקת טרופונין בעלת רגישות גבוהה וב- MRI לב עם שפור האמינות של האבחון הקליני של מיוקרדיטיס חדה. בעקבות זאת נוספה אבחנה של מיוקרדיטיס מוכחת קלינית (clinically confirmed myocarditis) המתבססת על שילוב של סימנים קליניים , עליה בטרופונין, ומילוי קריטריונים מקובלים למיוקרדיטיס חדה ב-MRI[5] (תרשים 2). האבחנה של מיוקרדיטיס וודאית (proven myocarditis) מבוססת על תוצאות ביופסיה אנדומיוקרדיאלית. לפי כך, לצורך בהירות, אנו ממליצים להשתמש בטרמינולוגיה של חשד קליני למיוקרדיטיס, מיוקרדיטיס מוכחת קלינית, ומיוקרדיטיס וודאית המוכחת בפתולוגיה (בביופסיה אנדומיוקרדיאלית, רקמת לב שהוצאה בעת השתלת לב/LVAD או בנתיחה לאחר המוות) (תרשים 2). הומלץ לנקוט בגישה דומה באבחון מיוקרדיטיס לאחר חיסון למניעת 19 COVID[6] ולאבחון מיוקרדיטיס בילדים[5].
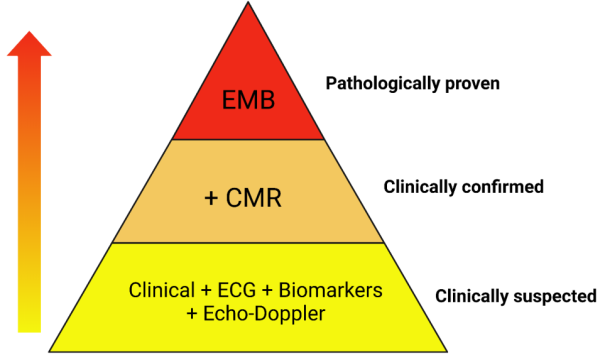
מקרא: cardiac magnetic resonance = CMR
endomyocardial biopsy = EMB
התייצגות קלינית
|
בדיקות עזר
|
מרבית החולים המאובחנים עם מיוקרדיטיס חריפה סובלים מכאבים בחזה (עד 95% מהמקרים) ומחציתם מתייצגים עם קוצר נשימה ו/או עייפות[1][2][3]. תסמינים אחרים כוללים דפיקות לב, התעלפות ואף מוות פתאומי. התלונות יכולות להימשך שעות עד מספר שבועות לפני פניה לקבלת סיוע רפואי.
התייצגות קלינית
חום הוא הפרודרום הנפוץ ביותר, המופיע בכ-65% מהחולים, לצד תסמינים דמויי שפעת, תסמינים גסטרואינטסטינלים, כאבי גרון וכדומה. תסמינים אלה מחזקים את החשד לזיהום נגיפי אך עקב הסגוליות הנמוכה שלהם, הם אינם נכללים בקריטריונים לאבחון מיוקרדיטיס חדה[1].
בדיקות עזר
בדיקות מעבדה: יש לבצע בדיקות דם לכל חולה החשוד כסובל ממיוקרדיטיס כולל ספירת דם עם מבדלת, טרופונין בעל רגישות גבוהה, NTproBNP, CK, שקיעת דם ו- CRP. בנוסף יש לשקול בהתאם לנסיבות הקליניות ביצוע משטח גרון לווירוסים, PCR1 לווירוסים בדם (כגון, שפעת, COVID-19 ,CMV ו- Parvo B19), ובדיקות למחלות קולגן (בפרט ANA ופאנל מורחב בהתאם לחשד קליני ספציפי הכולל אנטי C3-4 ,DNA , אנטי RNP, אנטי RO אנטי P-ANCA ,C- ANCA , LA וראומטואיד פקטור). היעדר אאוזינופיליה אינה שוללת מיוקרדיטיס אאוזינופילית,והערכה היא שבעד 25% מהמקרים עם אבחנה של מיוקרדיטיס אאוזינופילית בביופסיה אנדומיוקרדיאלית, לא הייתה אאוזינופיליה בספירת דם בזמן קבלה לבית החולים[7]. בדיקות סרולוגיה לווירוסים הינן בעלות רגישות נמוכה. תשובה שלילית אינה שוללת שהסיבה למיוקרדיטיס הינה מחלה וירלית, ולא נמצאה התאמה בין הממצאים בסרולוגיה לזיהוי נגיפים בביופסיה אנדומיוקרדיאלית[1] . מאידך, בדיקות סרולוגיות להפטיטיס C Q fever , Borellia burgdorferi ,HIV , ו- Trypanosoma cruzi עשויים לתרום במקרים ספציפיים לביסוס האבחנה[8].
אק"ג: הממצאים במיוקרדיטיס יכולים לכלול עליות קעורות ומפושטות במקטע ST-T, ככלל ללא שינויים הופכיים (רציפרוקלים), ומעבר לאזור המסופק על ידי עורק כלילי ספציפי. גלי Q יכולים להופיע גם במיוקרדיטיס ולכן נוכחותם אינה שוללת אבחנה זו. הפרעות הולכה עלייתיות-חדריות והפרעות קצב חדריות מורכבות עלולות להופיע בשכיחות גבוהה יותר במיוקרדיטיס משני ל- Giant cell, מיוקרדיטיס אאוזינופילית, סרקואידוזיס, מחלת Lyme ומיוקרדיטיס בעקבות טיפול בתכשירי ICI (Immune checkpoint inhibitors).
אקוקרדיוגרם: כל החולים עם חשד למיוקרדיטיס צריכים לעבור בדיקה אקוקרדיוגרפית בקבלתם. יש לחזור על הבדיקה במהלך האשפוז בהתאם למצב הקליני, במיוחד בחולים עם תפקוד לבבי ירוד בקבלה או עם החמרה קלינית באשפוז. מיוקרדיטיס יכולה להתייצג גם כעיבוי שריר לב, תפקוד סיסטולי תקין של חדר שמאל, ירידה גלובלית בתפקוד החדר או הפרעה אזורית בהתכווצות. ממצאי האקוקרדיוגרם עלולים לדמות לקרדיומיופתיה רסטריקטיבית, היפרטרופית, מורחבת או ARVC.
שלילת איסכמיה כגורם לתסמינים - בחולים עם מיוקרדיטיס, מומלץ לשלול מחלה כלילית חריפה בסמוך לקבלה , על ידי צנתור עורקים כליליים או טומוגרפיה ממוחשבת של העורקים הכליליים, אלא אם כן הסבירות לכך נמוכה ביותר (תרשים 3).
תהודה מגנטית של הלב (Cardiac MRI) - תהודה מגנטית של הלב מאפשרת זיהוי דלקת, פרפוזיה ובצקת בעזרת מיפוי T2 1T, הערכת נפח חוץ תאי, עם מידע על מיקום וחומרת השינויים וכן למדוד את מקטע הפליטה של חדר שמאל וחדר ימין. בנוסף, תהודה מגנטית מאפשרת בעזרת LGE להעריך קיום נזק לרקמת שריר הלב והצטלקויות (פיברוזיס). נקבעו קריטריונים לאבחון מיוקרדיטיס חריפה בתהודה מגנטית (Updated Lake Louise Criteria) בעלי רגישות של 87.5% וסגוליות של 96%[9]. חשוב לציין שהדיוק האבחנתי של MRI משתנה בהתאם לרקע הקליני. הרגישות הגבוהה ביותר מתקבלת בבדיקה הנעשית בתוך 2-3 שבועות מההתייצגות הקלינית[8]. המספרים המוזכרים למעלה טיפוסיים למיוקרדיטיס השכיחה שמתבטאת ככאב בחזה. הדיוק האבחנתי נמוך יותר במיוקרדיטיס המתבטאת כהפרעת קצב או כאי ספיקת לב[10].
לבדיקת ה MRI גם ערך באבחנה מבדלת[11] ומשמעות פרוגנוסטית[12]. סריקת MRI שלילית בחולה עם חשד קליני לדלקת שריר הלב קשורה לפרוגנוזה טובה. לעומת זאת, ממצא של- LGE בשכבה האמצעית של המחיצה הבין-חדרית ומקטע פליטה ירוד של חדר שמאל באשפוז זוהו כמנבאים החזקים ביותר לסיבוכים קרדיווסקולאריים, במיוחד כאשר הממצאים מתמידים בבדיקה חוזרת[12].
מומלץ לבצע MRI בכל החולים עם חשד קליני למיוקרדיטיס[3][13], במקרים קלים יש לבצע את הבדיקה תוך 2-3 שבועות מהתחלת התסמינים, במקרים קשים ובחולים מורכבים - במהלך האשפוז כשמצבם הקליני מתייצב[3][8]. אין לבצע בדיקת MRI בחולים לא יציבים המודינמית.
פירוט טכניקת ההדמיה הוא נושא בפני עצמו והקורא המעוניין מופנה להנחיות העדכניות בפרט רצפי המיפוי ושיטות הסריקה. חשוב שהבדיקה תתבצע תוך שימוש בטכנולוגיות מתקדמות, המספקות מידע אבחוני ופרוגנוסטי על פי אמות המידה המומלצות בהנחיות העדכניות[9][11].
הדמיה גרעינית: השימוש בהדמיה גרעינית (כגון PET-CT) אינו מומלץ באופן כשגרה. הבדיקה יכולה לסייע במקרים בהם קיימת התוויית נגד לביצוע תהודה מגנטית ובמקרים החשודים לסרקואידוזיס. יש לבצע את בדיקת PET-CT תוך שימוש בפרוטוקול "לבבי", הכולל תזונה מיוחדת ולאחריה צום ממושך במטרה לדכא קליטה פיזיולוגית של גלוקוז על ידי תאים תקינים של שריר הלב.
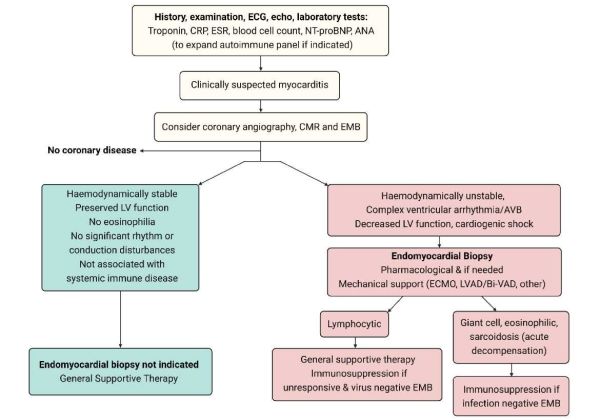
ביופסיה אנדומיוקרדיאלית
ביופסיה אנדומיוקרדיאלית נחשבת לשיטת האבחון הדפיניטיבית של מיוקרדיטיס ויכולה לזהות את האתיולוגיה הבסיסית ואת סוג הדלקת ובכך לכוון לטיפולים אפשריים (תרשים 3). הביופסיה כרוכה בסיכונים 2%-1% במרכזים רפואיים מנוסים ועד 9% במרכזים בעלי נפח נמוך[3] ולכן מומלץ להגביל את השימוש בה למקרים בהם הטיפול תלוי באבחנה ההיסטולוגית ו/או הווירולוגית[15][16]. עם התקדמות שיטות הדמיה, במיוחד MRI לב, ביופסיית לב אינה נחוצה במקרים של מיוקרדיטיס "לא מסובכת", דהיינו במצב המודינמי יציב, ללא ירידה בתפקוד הלב (50%>LVEF) וללא הפרעות קצב/הולכה מסכנות חיים.
במטופלים בהם קיימת התוויה לביצוע ביופסיית לב, ההמלצה היא להעבירם למרכזים רפואיים בעלי יחידות לאי-ספיקת לב מתקדמת עם ניסיון בביצוע ביופסיות לב כדי למזער את שיעורי הסיבוכים הכרוכים בפעולה.
התוויות לביצוע ביופסיה אנדומיוקרדיאלית[1][2][3], [12][13][15][16][17], (תרשים 3):
- מיוקרדיטיס חדה המתייצגת כאי ספיקת לב קשה או הלם קרדיוגני (מיוקרדיטיס פולמיננטית)
- מיוקרדיטיס חדה המתייצגת כאי ספיקת לב בנוכחות ירידה משמעותית בתפקוד הלב הסיסטולי (LVEF תחת ל-40%) שאינה משתפרת תחת טיפול
- הפרעות קצב חדריות מורכבות (אריתמיה חדרית SUSTAINED או אירועים חוזרים של NSVT), או חסם הולכה עלייתי-חדרי בדרגה גבוהה , ללא קשר לדרגת הירידה בתפקוד הלב
- מיוקרדיטיס חדה הקשורה לטיפול ב- (Immune checkpoint inhibitors (ICI כאשר האבחנה אינה ודאית. במקרים אלה, לאבחנה השלכה על המשך הטיפול בסרטן
- קרדיומיופתיה מורחבת עם אי ספיקת לב שאובחנה לאחרונה, עם או ללא סיפור של מיוקרדיטיס , בנוכחות ירידה בינונית או קשה בתפקוד הלב שאינה מגיבה לטיפולים המקובלים למשך 3-6 חודשים. ביופסיה במקרים אלה עשויה לאבחן קרדיומיופתיה דלקתית כרונית שיכולה להגיב לטיפול אימונוסופרסיבי [18]{{הערה|שם=הערה18|Chimenti C, Russo MA, Frustachi A. Immunosuppressive therapy in virus-negative inflammatory cardiomyopathy: 20-year follow-up of the TIMIC trial. Eur Heart J 2022;43:3463-3473})
- חשד לקרדיומיופתיה דלקתית עם נזק מתמשך לשריר הלב שביטוייה הפרשה מתמשכת של טרופונין בדם, במיוחד בקרב חולים עם אי ספיקת לב או בנוכחות של הפרעת הולכה עלייתית חדרית מתקדמת או הפרעות קצב חדריות. כמו כן, יש לשקול ביצוע ביופסיה בחשד למחלה אוטואימונית או אאוזינופיליה בלתי מוסברת
- יש לשקול ביופסיה במיוקרדיטיס חדה חוזרת[16]
שיטה ודגימות: ביופסיה מהלב מתבצעת בדרך כלל מחדר ימין אך ניתן לבצעה מחדר שמאל במקרים מסוימים וזאת בהתאם למידע הקליני וממצאי ההדמיה )כמו MRI או/ו PET-CT(, וכן מיפוי אלקטרו-אנאטומי, אשר יכולים לכוון להיקף ומיקום המחלה בלב. מומלץ לבצע ביופסיית לב בשלב מוקדם של המחלה ולקחת מספר דגימות )רצוי 5-7 דגימות( על מנת להקטין את שגיאות הדגימה. יש לשמור את הדגימות לפתולוגיה בפורמלין 10% בטמפרטורת החדר או במקרר )4 Co( ואת הדגימות לוירולוגיה יש להקפיא בחנקן נוזלי או לשמור במדיום של דגימות וירולוגיות מייד לאחר הלקיחה. במקרים מסוימים ניתן להקפיא דגימות טריות בטמפ' של 70- מעלות צלזיוס ובגלוטראלדהיד לצורך שימוש במיקרוסקופ אלקטרוני. במסגרת העיבוד הפאתולוגי נהוג לבצע תחילה צביעה של הרקמה על ידי המטוקסילין-אאוזין. להגברת רגישות הבדיקה יש להוסיף צביעות אימונוהיסטוכימיות על ידי נוגדנים ספציפיים נגד סמנים ייחודיים של תאי דלקת המסנינים את רקמת הלב ובפרט תאי CD3( T( ומקרופגים )CD68(. סמנים אפשריים נוספים הם HLA DR, תתי הסוגים של תאי CD4 ( T ו- CD8(, ותאי CD20( B(. לאחר בדיקה ראשונית יש לשקול גם ביצוע צביעות נוספות כגון MASSON's TRICHROME לפיברוזיס ו- CONGO RED לעמילואיד. בדיקת PCR לווירוסים מהרקמה הינה כלי חשוב כדי לסייע בזיהוי האטיולוגיה במקרים של מיוקרדיטיס ויראלית, והרגישות של בדיקה זו גבוהה בהרבה מבדיקות PCR מהדם וממשטח גרון, בפרט כשמדובר בזיהום ויראלי המוגבל ללב )cardiotropic(. מומלץ לבדוק 11 הנגיפים הבאים: )HHV6 ,Parvovirus B19 (PVB19), Enteroviruses )Coxsackie, Echo, ולשקול במקרים ספציפיים גם CMV, HIV ,Influenza ,HCV ,EBV, ו- PVB19 . Coronaviruses הינו הנגיף השכיח ביותר כיום בביופסיות לבביות, אך הוא שכיח גם באוכלוסייה בריאה וכך גם HHV6. לכן, למספר ההעתקים של PVB19 ו- HHV6 בביופסיה יש משמעות קלינית: מקובל שמעל 500 עותקים למק"ג חומצות גרעין של וירוסים אלה שהופקו מדגימת ביופסיה, מבטאים תהליך הדלקתי פעיל בשריר הלב )8,19,20(. הגדרת דרגות חומרה של מיוקרדיטיס
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 Caforio AL, Pankuweit S, Arbustini E, Basso C, Gimeno-Blanes J, Felix SB, Fu M, Helio T, Heymans S, Jahns R, Klingel K, Linhart A, Maisch B, McKenna W, Mogensen J, Pinto YM, Ristic A, Schultheiss HP, Seggewiss H, Tavazzi L, Thiene G, Yilmaz A, Charron P, Elliott PM; European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2013 Sep;34(33):2636-48, 2648a-2648d.
- ↑ 2.0 2.1 2.2 2.3 Bozkurt B, Colvin M, Cook J, Cooper LT, Deswal A, Fonarow GC, Francis GS, Lenihan D, Lewis EF, McNamara DM, et al; American Heart Association Committee on Heart Failure and Transplantation of the Council on Clinical Cardiology; Council on Cardiovascular Disease in the Young; Council on Cardiovascular and Stroke Nursing; Council on Epidemiology and Prevention; and Council on Quality of Care and Outcomes Research. Current diagnostic and treatment strategies for specific dilated cardiomyopathies: a scientific statement from the American Heart Association. Circulation. 2016;134:e579-e646. doi: 10.1161/CIR.0000000000000455.
- ↑ 3.0 3.1 3.2 3.3 3.4 3.5 3.6 3.7 3.8 Ammirati E, Frigerio M, Adler ED, Basso C, Birnie DH, Brambatti M, Friedrich MG, Klingel K, Lehtonen J, Moslehi JJ, Pedrotti P, Rimoldi OE, Schultheiss H-P, Tschope C, Cooper LT, Camici PG. Management of Acute Myocarditis and Chronic Inflammatory Cardiomyopathy: An Expert Consensus Document. Circ Heart Fail. 2020;13:e007405.
- ↑ 4.0 4.1 . Tschope C, Cooper LT, Torre-Amione G, Van Linthout S. Management of Myocarditis-Related Cardiomyopathy in Adults. Circulation Research 2019;124:1568-1583.
- ↑ 5.0 5.1 5.2 Law YM, Lal AK, Chen S, Cihakova D, Cooper LT Jr, Deshpande S, Godown J, Grosse-Wortmann L, Robinson JD, Towbin JA; Diagnosis and Management of Myocarditis in Children: A Scientific Statement From the American Heart Association. American Heart Association Pediatric Heart Failure and Transplantation Committee of the Council on Lifelong Congenital Heart Disease and Heart Health in the Young and Stroke Council. Circulation. 2021 Aug 10;144(6):e123-e135. doi: 10.1161/CIR.0000000000001001.
- ↑ Truong DT, Dionne A, Muniz JC, McHugh KE, Portman MA, Lambert LM, Thacker D, Elias MD, Li JS, Toro-Salazar OH, Anderson BR, Atz AM, Bohun CM, Campbell MJ, Chrisant M, D'Addese L, Dummer KB, Forsha D, Frank LH, Frosch OH, Gelehrter SK, Giglia TM, Hebson C, Jain SS, Johnston P, Krishnan A, Lombardi KC, McCrindle BW, Mitchell EC, Miyata K, Mizzi T, Parker RM, Patel JK, Ronai C, Sabati AA, Schauer J, Sexson Tejtel SK, Shea JR, Shekerdemian LS, Srivastava S, Votava-Smith JK, White S, Newburger JW. Clinically Suspected Myocarditis Temporally Related to COVID-19 Vaccination in Adolescents and Young Adults: Suspected Myocarditis After COVID-19 Vaccination. Circulation. 2022;145(5):345-356.
- ↑ Brambatti M, Matassini MV, Adler ED, Klingel K, Camici PG, Ammirati E. Eosinophilic Myocarditis: Characteristics, Treatment, and Outcomes. J Am Coll Cardiol. 2017;70:2363-2375. doi: 10.1016/j.jacc.2017.09.023.
- ↑ 8.0 8.1 8.2 Basso C. Myocarditis. N Engl J Med. 2022 Oct 20;387(16):1488-1500. doi: 10.1056/NEJMra2114478
- ↑ 9.0 9.1 Ferreira VM, Schulz-Menger J, Holmvang G, Kramer CM, Carbone I, Sechtem U, Kindermann I, Gutberlet M, Cooper LT, Liu P, Friedrich MG. Cardiovascular magnetic resonance in nonischemic myocardial inflammation: expert recommendaions. J Am Coll Cardiol 2018;72(24):3158-3176.
- ↑ Francone M, Chimenti C, Galea N, Scopelliti F, Verardo R, Galea R, Carbone I, Catalano C, Fedele F, Frustaci A. CMR sensitivity varies with clinical presentation and extent of cell necrosis in biopsy-proven acute myocarditis. JACC Cardiovasc Imaging. 2014 Mar;7(3):254-63. doi: 10.1016/j.jcmg.2013.10.011
- ↑ 11.0 11.1 Lintingre PF, Nivet H, Clement-Guinaudeau S, Camaioni C, Sridi S, Corneloup O, Gerbaud E, Coste P, Dournes G, Latrabe V, Laurent F, Montaudon M, Cochet H. High-Resolution Late Gadolinium Enhancement Magnetic Resonance for the Diagnosis of Myocardial Infarction With Nonobstructed Coronary Arteries. JACC Cardiovasc Imaging. 2020;13(5):1135-1148.
- ↑ 12.0 12.1 12.2 Aquaro GD, Ghebru Habtemicael Y, Camastra G, et al. Prognostic value of repeating cardiac magnetic resonance in patients with acute myocarditis. J Am Coll Cardiol 2019; 74: 2439-48.
- ↑ 13.0 13.1 McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Bohm M, Burri H, Butler J, Celutkiene J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, Kathrine Skibelund A; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail. 2022 Jan;24(1):4-131. doi: 10.1002/ejhf.2333. PMID: 35083827.
- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה21- ↑ 15.0 15.1 Cooper LT, Baughman KL, Feldman AM, Frustaci A, Jessup M, Kuhl U, Levine GN, Narula J, Starling RC, Towbin J, Virmani R, American Heart Association, American College of Cardiology, European Society of Cardiology. The role of endomyocardial biopsy in the management of cardiovascular disease: a scientific statement from the American Heart Association, the American College of Cardiology, and the European Society of Cardiology. Circulation. 2007;116:2216-33.
- ↑ 16.0 16.1 16.2 Seferovic PM, Tsutsui H, McNamara DM, Ristic AD, Basso C, Bozkurt B, Cooper LT, Filippatos G, Ide T, Inomata T, Klingel K, Linhart A, Lyon AR, Mehra MR, Polovina M, Milinkovic I, Nakamura K, Anker SD, Veljic I, Ohtani T, Okumura T, Thum T, Tschope C, Rosano G, Coats AJS, Starling RC. Heart Failure Association of the ESC, Heart Failure Society of America and Japanese Heart Failure Society Position statement on endomyocardial biopsy. Eur J Heart Fail. 2021;23:854-871.
- ↑ Kociol RD, Cooper LT, Fang JC, Moslehi JJ, Pang PS, Sabe MA, Shah RV, Sims DB, Thiene G, Vardeny O; American Heart Association Heart Failure and transplantation Committee of the Council on Clinical Cardiology. Recognition and initial management of fulminant myocarditis: a scientific statement From the American Heart Association. Circulation. 2020;141:e69-e92.
- ↑ Frustaci A, Russo MA, Chimenti C. Randomized study on the efficacy of immunosuppressive therapy in patients with virus-negative inflammatory cardiomyopathy: the TIMIC study. Eur Heart J. 2009;30:1995-2002.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק