אונקוגנטיקה - הרחבת הבדיקות לחולים - נייר עמדה - Oncogenetics tests for cancer patients
הופניתם מהדף אונקוגנטיקה - הרחבת הבדיקות לחולים - נייר עמדה לדף הנוכחי.
|
| |
|---|---|
| אונקוגנטיקה - הרחבת הבדיקות לחולים | |
| תחום | אונקולוגיה, גנטיקה |
| 250px | |
צביעה אימונו היסטוכימית לאונקוגן ErbB2 בריקמה של סרטן השד
| |
| האיגוד המפרסם | איגוד הגנטיקאים הרפואיים בישראל |
| קישור | נייר העמדה |
| תאריך פרסום | ינואר 2017 |
| יוצר הערך | ד"ר יעל גולדברג ד"ר רינת ברנשטין מולכו ענבל קדר, חברת ועדת היגוי |
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
הקדמה
האונקוגנטיקה (Oncogenetics) עוסקת באיתור גורמי סיכון גנטים-תורשתיים לתחלואה בסרטן. אנו עדים להתקדמות ושינוי מגמות בתחום. מהבולטים שבהם:
- המודעות לנושא וכמות הבדיקות גדלה באופן משמעותי, בעיקר הודות לטכנולוגיות הריצוף, להרחבת אפשרויות הגילוי המוקדם ולאירועים תקשורתיים, דוגמת "אפקט אנג׳לינה"
- הממשק בין האונקולוגיה (Oncology) והאונקוגנטיקה מתרחב ומעמיק; הידע לגבי הגנטיקה הופך משמעותי גם עבור בחירת הטיפול האונקולוגי. במקרים רבים, הטיפול האונקולוגי אינו 'תלוי גידול', אלא 'תלוי גנטיקה של גידול'. דוגמאות: נשאים של BRCA (BReast CAncer) יהיו מועמדים לטיפול במעכבי PARP, ונשאים של תסמונת לינץ' (Lynch syndrome) (HNPCC, Hereditary Non-Polyposis Colorectal Cancer) לאימונותרפיה (Immunotherapy). בדיקות מולקולריות של רקמת הגידול, הופכות חלק משגרת הטיפול במקרים רבים. איפיון היסטופתולוגי (Histopathology) ותוצאות הבדיקות הסומטיות (Somatic), מגדירים גם את הסיכון לנשאות גרמינלית (Germinal) ומזמינות ברור נוסף, לדוגמה: חותמת של MSI (Microsatellite Instability) בגידול, מעלה חשד לנשאות לתסמונת לינץ'; גידולי שד שהם Triple negative מחשידים לנשאות של BRCA
- מספר הגנים הידועים, הנקשרים לסיכון מוגבר לסרטן, הולך וגדל. יותר ויותר מסתבר, שהחפיפה בין הגידולים השונים והייחוס הגנטי שלהם, והחפיפה בין תסמונות הסרטן- גבוהה
נהוג למיין את הגנים המעלים סיכון לסרטן בשני אופנים:
- על בסיס חדירותם- HPG; MPG; LPG) High/ Moderate/ Low Penetrant Genes)
- על בסיס השלכותיהם על ההמלצות הקליניות (Clinical), לפעולות מנע/ מעקב/ טיפול- Actionable/ Non actionable genes (טבלה 1)
נראה שהידע לגבי חלק גדול מהגנים, בייחוד 'החדשים', עדיין חלקי ונדרשת חלוקה מדויקת עוד יותר, המתייחסת גם לחדירות וביטוי המוטציות (Mutations) השונות.
המצב בישראל - מציאות ובעיות
עליית המודעות והביקוש יצרו מצב, בו הביקוש רב מההיצע וברוב חלקי ישראל התורים לייעוץ אונקוגנטי ארוכים. רוב הפונים לייעוץ גנטי אינם נמצאים בסיכון גבוה לנשאות, ואילו חלק משמעותי מהחולים, הזקוקים לייעוץ, לא מקבלים מענה בזמן; המכונים השונים מנסים לפתור בעיה זו באופן פרטני. יש צורך בקביעת דרכים, לתעדוף בעלי הסיכון הגבוה על האחרים ומתן מענה דיפרנציאלי (Differential) לחולים, לבעלי סיכון גבוה ולבעלי סיכון נמוך לנשאות.
לגבי הבדיקות עצמן, הקופות מסתמכות על חוזרי מנהל הרפואה משנת 2004 ו-2012. חוזר 2004 מתייחס למוטציות נפוצות בלבד, ואילו חוזר 2012 מרחיב לבדיקות ריצוף של גנים בודדים. אין התייחסות בשלב זה לפאנל רב-גני ממוקד.
שני החוזרים מתייחסים רק לתסמונת לינץ' ו-BRCA, ואינם מתייחסים לגנים מנחי פעולה אחרים. ההמלצות לגבי BRCA מוגבלות רק לחולי סרטן שד ושחלה, ולא לחולים עם גידולים אחרים המיוחסים לגנים אלו. כמו כן, קיימים פערים בין ההמלצות בארץ להמלצות הנהוגות בעולם.
האיגוד הגנטי המליץ ב-2014 להמשיך לבדוק מוטציות נפוצות ב-BRCA לפי מוצא, ולהשלים מידע אודות המוטציות (981delT, R2336P) ואודות שכיחות מוטציות מייסד נוספות. בפועל, רב המעבדות בודקות את כל המוטציות ה'ידועות' ליוצאי כל העדות.
למרות החפיפה הקיימת בין התסמונות השונות (לדוגמה: סרטן הלבלב או השחלה, יכולים להתפתח על רקע נשאות ל-BRCA או לתסמונת לינץ'), עדיין מסלולי הבדיקות לתסמונות השונות מופרדים: מוטציות נפוצות ב-BRCA נבדקות בפאנל נפרד, מוטציות לתסמונת לינץ' בפאנל נפרד, מוטציות ל-MYH (MUTYH, mutY DNA glycosylase) בפאנל נפרד וכולי. הפרדה זו גורמת להליך מסורבל ויקר, בו המטופלים נאלצים לבצע בדיקות שונות למוטציות הגורמות למצבים הנפוצים ולהגיע לייעוצים חוזרים, בזמן שבמקרים רבים נכון יותר לבדוק, כבר בשלב הראשון, את מכלול המוטציות הנפוצות בגנים גורמי סרטן.
בנוסף, חוזרי מנהל כללי והמלצות הגנטיקאים מתייחסים רק לאוכלוסיית החולים או לבני משפחה של נשאים, אך לא מתייחסים לבריאים עם סיפור משפחתי או השייכים לקבוצת סיכון מתוקף מוצאם (אשכנזים).
נייר עמדה זה, דן בהרחבת הבדיקות למטופלים שחלו בסרטן ובמקרים ייחודיים לבני משפחה בריאים. מטרתו לאפשר את הבירור המתאים לאוכלוסייה המקומית באופן יעיל, שיפחית במידת האפשר התמודדות עם תוצאות שמשמעותן לא ברורה.
ההמלצות לבירור גנטי
- מומלץ להציע בדיקות גנטיות למטופלים, שלהם סיכון גבוה מ-10 אחוזים לנשאות של מוטציות, בגנים המוגדרים כבעלי חדירות בינונית/גבוהה
- מומלץ על הבדיקה רק אם הידע אודות מצב הנשאות ישפיע על המעקב המומלץ, על הנחיות טיפוליות או על אבחון טרום לידתי
הערכת הסיכון לנשאות תסתמך על תוכנות ניבוי מקובלות, שקיימים בספרות הרפואית נתונים לגבי אמינותן, על סמך ספרות רפואית מבוססת ועדכנית או על סמך קווים מנחים המקובלים בעולם, כדוגמת ה-NCCN guidelines, Revised Bethesda guidelines, Updated 2009 Chompret Criteria
אלגוריתם הבירור הגנטי
- בתחילה, תיבדקנה מוטציות נפוצות- בשל החפיפה הרבה בין תסמונות הסרטן השונות, מומלץ לבדוק בשלב ראשון, בבדיקה אחת, את מכלול המוטציות הפתוגניות השכיחות באוכלוסייה בגנים כגון: BRCA1&2, MMR (MisMatch Repair) genes, MUTYH, CHEK2 (Checkpoint kinase 2).
- ניתן להסתפק בבדיקת מוטציות בגן אחד, אם החשד ממוקד לגן זה
- אם לא אותרו מוטציות נפוצות, או אם הבדיקה לא רלוונטית (בשל מוצא או בשל העדר מוטציות נפוצות בגנים החשודים), והסיכון השארי לנשאות נאמד בלמעלה מ-10 אחוזים, מומלץ לעבור לריצוף ובדיקת חסרים בגנים החשודים. אם החשד ממוקד לגן מסוים ניתן לבדוק רק אותו; ניתן, לחלופין, לבצע ריצוף עמוק של פאנל גנטי, הכולל את הגנים שהוגדרו כמנחי פעולה (Actionable genes)
- מומלץ להתמקד, ככל האפשר, רק בגנים מנחי הפעולה, שגוררים המלצות רפואיות עבור נשאים
- אנו מציעים לעבור לשיטה זו באופן מסודר ומאורגן וליצור מאגר מידע משותף, שיאגד ויגדיר את המידע שיתקבל מבדיקות אלו. כצפוי, יתקבלו ממצאים לא ברורים שידרשו גיבוש מדיניות מוסכמת, אולם איתור ממצאים ברורים יאפשר הפחתה משמעותית בתחלואה. השימוש בטכנולוגיה ועיבוד משותף, יאפשרו הסקת מסקנות וגיבוש המלצות ייחודיות לאוכלוסייה המקומית
נתונים אודות שכיחות הנשאות והצידוק לבדיקה זו יאספו בעוד כשנתיים, וההמלצות תישקלנה שוב.
קריטריונים לבירור מוטציה ידועה או מוטציות שכיחות בחולים מקבוצות אתניות מתאימות
בדיקת מוטציה משפחתית, אם ידועה נשאות אצל קרובי משפחה מדרגה 1/2/3 (סיכוי לנשאות >10 אחוזים)
- BRCA1/2
- אדם ממוצא אשכנזי שחלה בסרטן שד או לבלב, בכל גיל
- כל אישה שחלתה בסרטן שחלות
- אישה שחלתה בסרטן שד, כשמתקיים אחד מהמצבים הבאים:
- גיל אבחנה קטן מ-50
- גידול Triple negative בגיל קטן מ-60
- מחלה דו צדדית או פעמיים סרטן שד (לא הישנות המחלה)
- חישוב סיכוי לנשאות גדול מ-10 אחוזים, לפי מודלים מקובלים
- גבר עם סרטן שד
- חולה בסרטן פרוסטטה (Prostate, ניקוד גליסון גדול מ-7), בתנאי שאחד או יותר קרובי משפחה, מדרגה 1 או 2, חלו בסרטן שחלות או בסרטן לבלב או בסרטן שד לפני גיל 50
- חולה בסרטן לבלב, בתנאי שאחד או יותר קרובי משפחה מדרגה 1 או 2 חלו בסרטן שחלות או בסרטן לבלב, או בסרטן שד לפני גיל 50
- אדם בריא עם סיפור משפחתי של סרטן המקנה לו סיכון של למעלה מ-10 אחוזים לנשאות, לפי מודלים מוקבלים
קריטריונים לבירור מוטציות שכיחות בגנים של תסמונת לינץ'
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – תסמונת לינץ'
- חולה בסרטן המעי הגס/רחם ומתאים לקווים המנחים של בתסדה
- סרטן הרחם לפני גיל 50
- H-MSI (High Microsatellite Instability) או IHC (Immunohistochemistry) פתוגני ל-MMR genes באוכלוסייה, שידועות בה מוטציות מייסד
קריטריונים לבירור מוטציות שכיחות ב- MUTYH
- מעל 15 אדנומות (Adenomas) או מעל 10 אדנומות וסרטן מעי, בחולים ממוצא צפון אפריקאי.
קריטריונים לבירור מוטציות בגנים גורמי סרטן אחרים
- ברור גרמינלי של מוטציה שאותרה ברקמת גידול, יישקל רק בנוכחות כל התנאים הבאים:
- בוצע ייעוץ גנטי מקדים על ידי רופא/יועץ גנטי, המתייחס באופן ברור לסוגיה התורשתית
- קיים מידע מהימן ומספיק אודות השינוי הסומטי, המאפשר אומדן סיכון להיותו גרמינלי
- המוטציה המדווחת הוגדרה כפתוגנית באחד מה- Actionable genes
- המוטציה מוגדרת כמוטציה הגורמת לתסמונת תורשתית
- חולה העונה על קריטריונים אבחנתיים של תסמונת סרטן נדירה [[[Li Fraumeni]], PTEN (Phosphatase and TENsin homolog) etc], וידועה מוטציה נפוצה בקבוצה האתנית לה שייך או ידועות מוטציות נפוצות (Hot spots) הגורמות לתסמונת זו
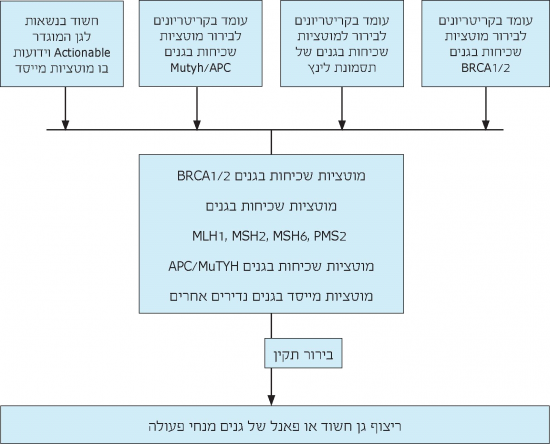
תרשים זרימה לפאנל מוטציות שכיחות
אגוד הגנטיקאים ממליץ להציע בדיקה אחת, הכוללת את כל המוטציות השכיחות בתסמונות הסרטן השונות. עד שבדיקה כזו תהיה אפשרית, ניתן לבצע בדיקות סצפיציות לחוד.
קריטריונים לבירור רחב (ריצוף וחסרים) של גנים גורמי סרטן
המכון/ המעבדה הגנטית יכולים לבצע בדיקת פאנל רחב, לחולים העומדים בקריטריונים לבירור, או להעדיף בדיקת גן בודד, אם החשד ממוקד לגן זה.
תסמונת לינץ׳
חולה בסרטן לאחר שלילת מוטציות נפוצות, העומד באחד הקריטריונים הבאים:
- חולה בסרטן המעי הגס/רחם ועומד בקריטריונים של בתסדה (גם המעודכנים), סרטן הרחם לפני גיל 50
- H-MSI ו/או העדר ביטוי של אחד הגנים בבדיקת IHC
פוליפוזיס (Polyposis) על רקע APC (Adenomatous Polyposis Coli)/MUTYH
מטופל לאחר שלילת מוטציות נפוצות, העומד באחד הקריטריונים הבאים:
- מעל 20 אדנומות במעי הגס
- מעל 10 אדנומות וסרטן מעי
- גידול דסמואיד (Desmoid)
- הפטובלסטומה (Hepatoblastoma)
- מעל 15 אדנומות אצל המטופל וסרטן מעי אצל קרוב משפחה מדרגה 1
- מעל 15 אדנומות אצל המטופל והורים/ קרובי משפחה
ריצוף BRCA1/2
חולה בסרטן, לאחר שלילת מוטציות נפוצות, העומד באחד הקריטריונים הבאים:
- כל אישה שחלתה בסרטן שחלות
- כל אשה שחלתה בסרטן השד Triple negativ לפני גיל 60
- אישה שחלתה פעמיים בסרטן שד
- אישה שחלתה בסרטן שד וחישוב הסיכון לנשאות אצלה נאמד במעל ל-10 אחוזים, על פי אחת מתוכנות הניבוי המקובלות או על פי מאמרים קובעי מדיניות
- גבר עם סרטן שד
- חולה בסרטן פרוסטטה (ניקוד גליסון גדול מ-7), בתנאי שאחד או יותר קרובי משפחה, מדרגה 1 או 2, חלו בסרטן שחלות או בסרטן לבלב או בסרטן שד לפני גיל 50
- חולה בסרטן לבלב, בתנאי שאחד או יותר קרובי משפחה, מדרגה 1 או 2, חלו בסרטן שחלות או בסרטן לבלב או בסרטן שד לפני גיל 50
ריצוף TP53 (Tumor Protein p53)
חולה סרטן העונה על הקריטריונים הקלאסים ל-LFS (Li-Fraumeni syndrome) או עונה על ה-Chompret Criter.
קריטריונים לריצוף גנים גורמי סרטן אחרים
חולה העונה על קריטריונים אבחנתיים של תסמונת סרטן נדירה [HDGC (Hereditary Diffuse Gastric Cancer), PTEN, JPS (Juvenile Polyposis Syndrome), PJS (Peutz–Jeghers syndrome), MEN (Multiple Endocrine Neoplasia), MEN2].


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק