אי ספיקת לב - השתלת דפיברילטור וקוצב לב דו-חדרי - Congestive heart failure - implementation of intracardiac defibrillator and cardiac-resynchronization therapy
הופניתם מהדף אי ספיקת לב - השתלת דפיברילטור וקוצב לב דו-חדרי לדף הנוכחי.
| אי ספיקת לב - השתלת דפיברילטור וקוצב לב דו-חדרי | ||
|---|---|---|
| Congestive heart failure - implementation of intracardiac defibrillator and cardiac-resynchronization therapy | ||
| 250px | ||
| יוצר הערך | ד"ר מחמוד סולימן
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – אי ספיקת לב, קוצב לב
מספר החולים הסובלים מאי ספיקת לב הולך וגדל עם הזמן. חולים אלה מתים משתי סיבות עיקריות:
- אי ספיקה מכנית של הלב
- הפרעת קצב חדרית מסוכנת - פרפור חדרים (VF - Ventricular fibrillation) או מאוץ חדרים (VT - Ventricular tachycardia).
הוכח במספר רב של עבודות שדפיברילטור מושתל (ICD - Implantable cardioverter defibrillator) מביא לירידה משמעותית בתמותה מהפרעות קצב חדריות בקרב הלוקים בירידה קשה בתפקוד חדר שמאל, עם סימני אי ספיקת לב או ללא סימנים אלה.
ברבע עד שליש מחולי אי ספיקת לב יש הפרעת הולכה חדרית, כמו חסם צרור הולכה שמאלי (LBBB - Left bundle branch block), כעדות לחוסר תיאום (סינכרון) בכיווץ חדר שמאל. בעזרת קיצוב דו-חדרי מסונכרן ניתן לשפר את התפקוד של חדר שמאל (תהליך שנקרא Reverse remodeling), להביא לשיפור משמעותי בדרגה התפקודית שלהם, ואף להורדה בשיעור התמותה.
אפידמיולוגיה
אי ספיקת לב היא סיבה מובילה לתחלואה לתמותה. מספר האנשים שחיים עם אי ספיקת לב הולך וגדל עם הזמן - זאת בשל הירידה בתמותה מאוטם לבבי בזכות טיפולים חדשניים.
מטרות הטיפול באי ספיקת לב
מוות לבבי פתאומי (Sudden cardiac death) הוא סיבה שכיחה למוות בחולים עם אי ספיקת לב בדרגה תפקודית II או III בדירוג התפקודי של אי ספיקת לב על פי האגודה הלבבית של ניו-יורק, ה-NYHA (The New York Heart Association (NYHA) functional classification). ברוב המכריע של המקרים הסיבה היא הפרעת קצב חדרית - פרפור חדרים או מאוץ חדרים. החולים לרוב מתים אם אינם מקבלים טיפול על ידי הלם חשמלי תוך דקות.
סיבה נוספת למוות בחולים אלה היא התקדמות המחלה עצמה וכשל מכני.
מטרות הטיפול בחולי אי ספיקת הלב היא הארכת תוחלת החיים עם שיפור איכות החיים. שתי מטרות אלה ניתנות להשגה בעזרת טיפולים שמונעים ו/או מטפלים בהפרעות קצב חדריות מסוכנות וכן ומשפרים את התפקוד והמבנה של שריר הלב(1).
גורמי סיכון להתפתחות הפרעות קצב חדריות ומוות פתאומי
גורמי הסיכון העיקריים להתפתחות הפרעות קצב חדריות ולמוות פתאומי כוללים:
- מקטע פליטה של חדר שמאל (LVEF - Left ventricular ejection fraction) הנמוך מ-35% (LVEF<35%), עם או בלי סימני אי ספיקת לב
- חולים שחוו בעבר הפרעת קצב חדרית
- מחלות גנטיות עם נטייה למוות פתאומי - תסמונת ברוגדה (Brugada syndrome), תסמונת מקטע QT מוארך (Long QT syndrome), ועוד.
קיימים גורמי סיכון אחרים, שעודם שנויים במחלוקת.
דפיברילטור מושתל (ICD - Implantable cardioverter defibrillator)
דפיברילטור מושתל הוא מכשיר שמשמש לטיפול בהפרעות קצב חדריות ולמניעת מוות פתאומי. המכשיר מושתל מתחת לעור, ומחובר באמצעות אלקטרודות לפנים הלב. הוא מנטר את הפעילות החשמלית של הלב, ומטפל באופן אוטומטי בהפרעות קצב הלב מסכנות החיים על ידי קיצוב מהיר ובמידת הצורך במתן מכת חשמל. יעילות המכשיר הוכחה במספר רב של מחקרים חשובים שבדקו את יעילותו הן במניעה ראשונית (חולים הנמצאים בסיכון להפרעות קצב חדריות/ מוות פתאומי אך מעולם לא חוו אירוע כזה) והן במניעה שניונית (חולים לאחר אירוע של הפרעת קצב חדרית/ מוות לבבי פתאומי)(2).
בחירת מטופלים המתאימים להשתלת דפיברילטור
בחירת חולים המתאימים להשתלת דפיברילטור היא עדיין בעיה קשה, ויש צורך בחקירת גורמי סיכון המעלים את הסיכון להתפתחות הפרעות קצב חדריות.
ההתוויות להשתלת דפיברילטור מבוססות על מספר רב של עבודות קליניות חשובות שהוכיחו את יעילות הדפיברילטור המושתל במניעת מוות פתאומי. התוויות אלה פורסמו מטעם האיגודים הקרדיולוגיים האמריקאיים והאירופאיים(3), ולהלן עיקרי קווים מנחים אלה. קווים מנחים אלה אומצו על ידי האיגוד הקרדיולוגי הישראלי וכן על ידי משרד הבריאות.
מניעה שניונית של מוות פתאומי
- חולים בהם היה אירוע של הפרעת קצב חדרית משמעותית - פרפור חדרים או מאוץ חדרים ממושך (Sustained ventricular tachycardia): השתלת דפיברילטור מפחיתה את שיעור התמותה הכוללת בכ-30%. התועלת רבה יותר ככל שהחולה נמצא בדרגת סיכון גדולה יותר, כגון חולים עם ליקוי משמעותי בתפקוד חדר שמאל.
- מניעה שניונית של מוות פתאומי בחולים עם אירוע של עילפון ללא תיעוד של הפרעת קצב חדרית: יש להדגיש כי לפני שמחליטים על השתלת דפיברילטור, חשוב לשלול באופן אקטיבי גורמים לעילפון שאינם קשורים בהפרעות קצב, ולבחון את מכלול הנתונים הקליניים וגורמי הסיכון בחולה. יש לקחת בחשבון את התמונה הקלינית של אירוע העילפון, גיל החולה, סיפור משפחתי של מוות פתאומי, נוכחות מחלה של העורקים הכליליים, התפקוד הסיסטולי של חדר שמאל, נוכחות קרדיומיופתיה היפרטרופית (Hypertrophic cardiomyopathy) או מורחבת (Dilated cardiomyopathy) ועוד. בחלק מהמקרים ניתן לאבחן את האטיולוגיה של עילפון על ידי ביצוע בדיקה אלקטרופיזיולוגית (Electrophysiology study).
מניעה ראשונית של מוות פתאומי
מניעה ראשונית של מוות פתאומי מתייחסת להשתלת דפיברילטור בחולים שנמצאים בסיכון גבוה למוות פתאומי, אך טרם חוו אירוע כזה או פיתחו הפרעות קצב חדריות מסוכנות. יעילות השימוש בדפיברילטור למטרה זו הוכחה במספר רב של עבודות. המדד החשוב ביותר לניבוי התועלת שבהשתלת דפיברילטור הוא התפקוד הסיסטולי של חדר שמאל כפי שהוא מתבטא על ידי מקטע הפליטה של חדר שמאל. השתלת דפיברילטור מומלצת במקרים הבאים:
- 40 יום ומעלה לאחר אוטם שריר הלב, עם מקטע הפליטה של חדר שמאל הקטן מ-30-35%
- קרדיומיופתיה לא איסכמית בנוכחות מקטע פליטה הקטן מ-35% ודרגה תפקודית II-III בדירוג NYHA
- חולים עם קרדיומיפתיה היפרטרופית ונוכחות גורמי סיכון למוות פתאומי
קיצוב דו-חדרי (CRT - Cardiac resynchronization therapy)
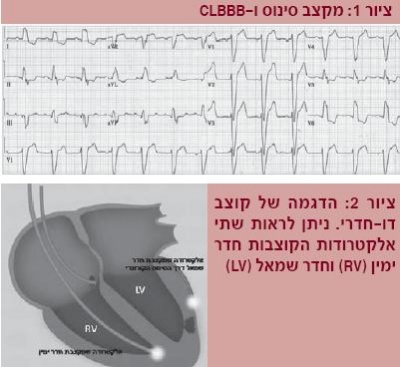
בחלק מהחולים הסובלים מאי ספיקת לב קיים חוסר תיאום בהתכווצות חלקים שונים של הלב. כך למשל, המחיצה הבין חדרית מתכווצת לפני החלק הצידי (לטרלי) של חדר שמאל, מצב שגורם לפגיעה קשה בכושר ההתכווצות של הלב וירידה משמעותית בתפוקת הלב. חולים הלוקים בחוסר תיאום לבבי מאופיינים בנוכחות מקטע QRS רחב בתרשים האלקטרוקרדיוגרם (ECG - Electrocardiogram), לרוב בצורת חסם צרור הולכה שמאלי (ציור 1).
במצבים כאלה קיימת אפשרות לתאם מחדש את כיווץ חלקי הלב השונים, טיפול שנקרא קיצוב דו חדרי (CRT - Cardiac resynchronization therapy). בטיפול זה מושתלות בגופו של החולה שלוש אלקטרודות - בעלייה ימנית, בחדר ימני ובחדר השמאלי - דרך הסינוס הכלילי (Coronary sinus) (ציור 2)(4). הסבר מפורט על האופן שבו עובד הרעיון של קיצוב דו-חדרי הוא מעבר להיקף הסקירה הנוכחית.
כיוון שחולים אלה סובלים מליקוי קשה בתפקוד חדר שמאל, ונמצאים בסיכון מוגבר למוות לבבי פתאומי, לרוב משולב הקוצב הדו-חדרי עם דפיברילטור, ואז המכשיר נקרא CRTD (Cardiac resynchronization therapy defibrillator).
בחולים המתאימים מביא קוצב דו-חדרי לשיפור ניכר בתסמינים, שיפור ביכולת לבצע מאמץ, ירידה בשיעור האשפוזים בגלל אי ספיקת הלב, שיפור בתפקוד חדר שמאל, הקטנת הממדים של חללי הלב והפחתה במידת הדליפה של המסתם המיטרלי.
עבודות שפורסמו לאחרונה הראו שקיצוב דו-חדרי מביא לירידה משמעותית בתמותה הכוללת, ללא תלות בסוג המכשיר: מכשיר משולב בדפיברילטור או שאיננו משולב בדפיברילטור(6 ,5). היום הנטייה היא להמליץ על השתלת קוצב דו-חדרי בשלבים מוקדמים של הקרדיומיופתיה, עוד לפני שהתפתחו סימני אי ספיקת לב, כדי למנוע את תהליך העיצוב מחדש (Remodeling) שמאפיין חולים לאחר אוטם בשריר הלב.
בחירת מטופלים להשתלת קוצב דו חדרי
התוויה קלאסית להשתלת קוצב דו חדרי - בהינתן התנאים הבאים:
- אי ספיקת לב בדרגה תפקודית III או IV לפי ה-NYHA
- ליקוי קשה בתפקוד חדר שמאל - מקטע פליטה של חדר שמאל קטן מ-35%
- נוכחות מקצב סינוס והפרעת הולכה חדרית עם רוחב QRS≥120 מילישניות
- כל זאת בתנאי שהחולה מקבל טיפול תרופתי מיטבי
קוצב דו-חדרי עם דפיברילטור (CRTD - Cardiac resynchronization therapy defibrillator)
מומלץ לשלב את הקוצב הדו-חדרי בדפיברילטור לפי ההנחיות המקובלות להשתלת דפיברילטור.
לאחרונה התקבל מידע חדש וחשוב ממספר עבודות על התועלת שבהשתלת קוצב דו-חדרי באוכלוסיות חולים אחרות, למשל: חולים ללא תסמינים עם ירידה קשה בתפקוד חדר שמאל ועדות לחוסר תיאום בכיווץ חדר שמאל. מידע חדש זה היה כה חשוב, שהוא הביא את האיגוד האירופאי לקרדיולוגיה(7) ואת מנהל המזון והתרופות האמריקאי (FDA - United States Food and Drug Administration) לפרסם עדכונים חדשים לגבי התוויות נוספות להשתלת קוצב דו-חדרי. עיקרי עדכונים אלה מפורטים להלן:
- קוצב דו-חדרי עם דפיברילטור בחולים עם אי ספיקת לב קלה או ללא תסמיני אי ספיקת לב: קיצוב דו-חדרי עם דפיברילטור (CRTD - Cardiac resynchronization therapy defibrillator) בחולים עם אי ספיקת לב קלה (NYHA I-II) או ללא תסמיני אי ספיקת לב נבדקה בארבע עבודות עיקריות שבהן בוצעה השוואה בין קיצוב דו-חדרי עם דפיברילטור לדפיברילטור מושתל לבדו(9 ,8 ,6). בעבודת אלה הוכח שהוספת קיצוב דו-חדרי לדפיברילטור גורמת לשיפור בתפקוד חדר שמאל (עלייה במקטע הפליטה של חדר שמאל והקטנת ממדי החדר השמאלי במנגנון של Reverse remodeling), להקטנת חומרת אי הספיקה של המסתם המיטרלי ולהורדת שיעור האשפוזים בגלל אי ספיקת לב. עבודה שפורסמה לא מכבר - מחקר RAFT (Resynchronization–defibrillation for ambulatory heart failure trial) - הראתה אף ירידה בשיעור התמותה הכוללת בחולים בהם הושתל קוצב דו-חדרי עם דפיברילטור לעומת חולים בהם הושתל דפיברילטור בלבד.
יצוין כאן שעיקר התועלת מקיצוב דו-חדרי בחולים עם אי ספיקת לב קלה או ללא תסמיני אי ספיקת לב היה מוגבל לחולים שבהם רוחב מקטע ה-QRS היה גבוה מ-150 מילישניות או גבוה מ-130 מילישניות בנוכחות חסם צרור הולכה שמאלי מלא (CLBBB - Complete left bundle branch block) לעומת צורה אחרת של הפרעת הולכה חדרית, כמו חסם צרור הולכה ימני (RBBB - Right bundle branch block) או עיכוב הולכה תוך חדרי (IVCD - Intraventricular conduction delay) לא ספציפי(10). כמו כן, לראשונה בהיסטוריה של הטיפולים הלבביים, נשים הפיקו תועלת רבה יותר מהוספת קיצוב דו-חדרי לעומת גברים(11).
- קוצב דו-חדרי עם דפיברילטור בחולים עם אי ספיקת לב ופרפור פרוזדורים קבוע: במחקרים המבוקרים של קיצוב דו-חדרי נכללו בעיקר חולים בקצב סינוס או בעלי פרפור התקפי. דבר זה עומד בסתירה לשימוש הקליני הנרחב בקוצב דו-חדרי בחולים עם פרפור פרוזדורים, כפי שזה בא לידי ביטוי בסקר האחרון של האיגוד הקרדיולוגי האירופאי(12). חמישית ממושתלי הקוצב הדו-חדרי באירופה לוקים בפרפור פרוזדורים קבוע. שכיחות פרפור פרוזדורים בקרב חולי אי ספיקת לב תלויה בחומרת המחלה: 5% ב-NYHA דרגה I לעומת 24-50% ב-NYHA דרגה III/IV. חשוב להדגיש שחולים עם אי ספיקת לב, פרפור פרוזדורים ומקטע פליטה הנמוך מ-35% עונים על הקריטריונים להשתלת דפיברילטור. בנוכחות QRS מורחב (ארוך מ-130 מילישניות) יש העדפה להשתיל קוצב דו-חדרי עם דפיברילטור בחולים אלה.
אין תמיכה לשימוש בקיצוב דו-חדרי בדרגה תפקודית I–II אם הקצב הוא פרפור פרוזדורים קבוע.
- קוצב דו-חדרי בחולים עם אי ספיקת לב והתווייה מקובלת להשתלת קוצב: ידוע שקיצוב חדר ימין לזמן ממושך עלול לגרום פגיעה בתפקוד חדר שמאל, או להחמיר פגיעה כזו.
קיימים מספר פרסומים רטרוספקטיביים ומחקרים פרוספקטיביים קטנים שהראו תועלת קלינית כאשר משתמשים מראש בקיצוב דו-חדרי או לאחר שדרוג בקיצוב דו-חדרי, במקרים שבהם נדרש קיצוב חדר ימין בנוכחות פגיעה קשה בתפקוד חדר שמאל, NYHA דרגה III, ללא קשר לרוחב ה-QRS הבסיסי ללא קיצוב.
שימוש בקוצב דו-חדרי מאפשר לנו להתחיל טיפול בחסמי ביטא (Beta blockers), ואף להעלות מינון של טיפול זה כדי להגיע למינונים המרביים שהוכחו כיעילים בחולי אי ספיקת לב, וזאת מבלי לחשוש מעלייה בשיעור הקיצוב בחדר ימין.
סיפור מקרה
אישה בת 68 שנים עם סיפור של אוטם לפני 5 שנים הגיעה בתלונה על קוצר נשימה במאמץ גופני קל. הטיפול התרופתי כולל:
- Acetylsalicylic Acid
- Furosemide
- Atorvastatin במינון 40 מ"ג
- Bisoprolol במינון 10 מ"ג
- Ramipril במינון 10 מ"ג
בבדיקה גופנית: דופק 76 לדקה וסדיר, לחץ דם של 120/74 ממ"כ. יש עלייה בלחץ ורידי הצוואר, חוד הלב מוסט שמאלה ונשמע קול שלישי. בדיקת הריאות תקינה. בדיקת אקוקרדיוגרפיה (Echocardiogram) הדגימה הרחבה של חדר שמאל וירידה גלובלית בתפקוד חדר שמאל, מקטע פליטה של 33%.
החולה נמצאת בדרגה תפקודית III עם ירידה קשה בתפקוד חדר שמאל ובנוכחות חסם צרור הולכה שמאלי ומקטע QRS ארוך מ-130 מילישניות. החולה מקבלת טיפול תרופתי אופטימלי, לכן יש התוויה להשתלת קוצב דו-חדרי. מכיוון שהחולה היא בסיכון מוגבר להפרעות קצב חדריות, קיימת התוויה להשתלת דפיברילטור למניעה ראשונית, ולכן צריך להשתיל מכשיר משולב: קוצב דו-חדרי עם דפיברילטור.
ביבליוגרפיה
- McMurray JJ. Clinical practice. Systolic heart failure. NEJM 362(3):228-238
- Myerburg RJ. Implantable cardioverter-defibrillators after myocardial infarction. NEJM 2008;359(21):2245-2253
- Epstein AE, et al. ACC/AHA/HRS 2008 Guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the ACC/AHA/NASPE 2002 Guideline Update for Implantation of Cardiac Pacemakers and Antiarrhythmia Devices) developed in collaboration with the American Association for Thoracic Surgery and Society of Thoracic Surgeons. J Am Coll Cardiol 2008;51(21):1-62
- Jarcho JA. Biventricularpacing. NEJM 2006;355(3):288-294
- Cleland JG, et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure. NEJM 2005;352(15):1539-1549
- Tang AS, et al. Cardiac-resynchronization therapy for mild-to-moderate heart failure. NEJM 363(25):2385-2395
- Dickstein K, et al. Focused Update of ESC Guidelines on device therapy in heart failure: an update of the 2008 ESC Guidelines for the diagnosis and treatment of acute andchronic heart failure and the 2007 ESC guidelines for cardiac and resynchronization therapy. Developed with the special contribution of the Heart Failure Association and the European Heart Rhythm Association. Eur Heart J 2010;31(21):2677-2687
- Daubert C, et al. Prevention of disease progression by cardiac resynchronization therapy in patients with asymptomatic or mildly symptomatic left ventricular dysfunction: insights from the European cohort of the REVERSE (Resynchronization Reverses Remodeling inSystolic Left Ventricular Dysfunction) trial. J Am Coll Cardiol 2009;54(20):1837-1846
- Jessup M. MADIT-CRT--breathtaking or time to catch our breath? NEJM 2009;361(14):1394-1396
- Zareba W, et al. Effectiveness of Cardiac Resynchronization Therapy by QRS Morphology in the Multicenter Automatic Defibrillator Implantation Trial-Cardiac Resynchronization Therapy (MADIT-CRT). Circulation
- Arshad A, et al. Cardiac Resynchronization Therapy Is More Effective in Women Than in MenThe MADIT-CRT (Multicenter Automatic Defibrillator Implantation Trial With Cardiac Resynchronization Therapy) Trial. J Am Coll Cardiol 57(7):813-820
- Dickstein K, et al. The European cardiac resynchronization therapy survey. Eur Heart J 2009;(20)30:2450-2460
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר מחמוד סולימן, היחידה לאלקטרופיזיולוגיה, המחלקה הקרדיולוגית, רמב"ם - הקריה הרפואית לבריאות האדם, חיפה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק