אלפא-2 אנטי-פלזמין - Alfa-2 anti plasmin
| מדריך בדיקות מעבדה | |
| אלפא-2 אנטי פלזמין | |
|---|---|
| Alfa-2 anti plasmin | |
| שמות אחרים | plasmin inhibitor, A2AP, AAP, API, alfa2AP, alfa-2-PI, SERPINF2 |
| מעבדה | המטולוגיה בדם |
| תחום | קרישת דם |
| טווח ערכים תקין | במבוגרים -80-140%. ביילודים (full term) או בפגים יכולים להיות 50% מערכי מבוגרים במהלך 90 יום מתאריך הלידה. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
אבחון של חסר ב- plasmin inhibitor-2 מולד. או הערכה מושלמת של DIC (disseminated intravascular coagulation) ופיברינוליזה או של היפר-פיברינוליזה, כאשר אלה נמדדים בהקשר של רמת פיברינוגן, של fibrin D-dimer, של fibrin degradation products, של soluble fibrin monomer complex, או של פלסמינוגן. הבדיקה עשויה לסייע בהערכת מחלת כבד. כמו כן הבדיקה מסייעת בהערכה של השפעות התרפיה הפיברינוליטית או האנטי-פיברינוליטית.
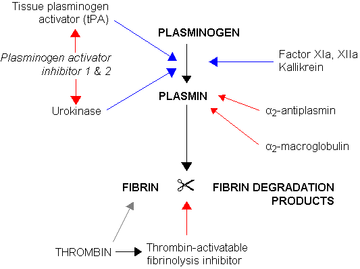
אלפא-2 אנטי-פלזמין (להלן A2AP) או plasmin inhibitor, הוא מעכב של serine protease (serpin) האחראי לאינאקטיבציה של פלזמין (Wu וחב' ב-Biochem Soc Transact משנת 2019). פלזמיו הוא אנזים חשוב המשתתף בפיברינוליזה ובביקוע של חלבונים אחדים. החלבון מקודד על ידי הגן serpinF2, הממוקם בעמדה chr 17:1.74-1.76. A2AP מסונתז בכבד עם תקופת מחצית חיים ביולוגית של בערך 3 ימים. הוא גורם לאינאקטיבציה של פלזמין, שהוא האנזים הפיברינוליטי הראשוני האחראי ליצירת פקקת פיברין, וקושר פיברין ביחד עם פקטור VIII, באופן הגורם לפקקת להיות קשה יותר להמסה. חסר של מעכב של A2AP מביא לשבירת הפיברין באופן שאינו מבוקר על ידי פלזמין, וגורם לדימום.
תפקיד A2AP בתחלואה
תוארו מעט מאוד מקרים של חסר ב-A2AP (פחות מ-20). כיוון שפלזמין מפרק קרישי דם, עיכוב פגום של פלזמין גורם נטייה לדימום, שהיה חמור במקרים שתוארו (Shieh ו-Travis ב-J Biol Chem. משנת 1987, Brower ו-Harpel באותו כתב עת משנת 1982, ו-Wiman ו-Collen באותו כתב עת משנת 1979). בשחמת כבד, יש יצירה מופחתת של A2AP מה שמוביל לאינאקטיבציה מוחלשת של פלזמין ולהגברת פיברינוליזה. זה מוביל לסיכון מוגבר של דימום במחלת כבד (Sattar ב-Pathoma LLC משנת 2011).
הביטוי של A2AP
A2AP מסונתז בעיקר בהפטוציטים בכבד ומשתחרר לדם. לאחר הסינתזה, A2AP עובר מודיפיקציה אנזימטית בצירקולציה בקצוות ה-N וה-C טרמינליים, מה שמשפיע על ההצמדות לפיברין ועל הקישור לפלסמינוגן, בהתאמה. רמות נמוכות יותר של A2AP מופיעות בכליות האדם, בטסיות הדם, במערכת העיכול, בשרירים, בריאות, בשלייה, ובמוח (בקליפת המוח, בהיפוקמפוס ובמוחון). A2AP נמצא במגוון מינים החל מיונקים וכלה בדגים ובעופות, ויש הומולוגיה משמעותית ברצף במגוון מינים כגון אדם, עכברים בקר וכד'. ל-A2AP של אדם ועכבר יש קבועי קינטיקה דומים לעיכוב פלזמין אוטולוגי והטרולוגי in vitro. החדרת ריכוזים פיזיולוגיים של A2AP מאדם לעכברים עם חסר בחלבון זה (−/−α2AP), משחזרת את יכולת העיכוב הפיברינוליטי והתרומבוזה לרמותיו הנורמליות. כיוון ש-A2AP מאדם ומעכבר הם בעלי תכונות דומות, עכברים −/−α2AP, מספקים מודל תרגומי מצוין לבחינה של α2AP.
A2AP קשור קו-ולנטית לפיברין בפקקת על ידי פקטור VIII משופעל, שהוא טרנסגלוטמינזה (Kluft וחב' ב-Thromb Res משנת 1984) המהווה מקור לעמידות in vitro של קרישים בפלזמה לפיברינוליזה המתוכת על ידי פלזמין (Rijken וחב' ב-Biomed Res Int משנת 2017, Fraser וחב' ב-Blood משנת 2011). הפעילות של פלזמין מוגנת בחלקה מעיכוב על ידי A2AP כאשר אתרי הקישור של ליזין, מנוטרלים על ידי קישור לפיברין בפקקת (Wiman וחב' ב-Biochim Biophys Acta משנת 1979, ו-Lee וחב' ב-Thromb Hemost משנת 2001), או על פני תאי אנדותל (Hall וחב' ב-J Biol Chem משנת 1991). רוב המחקרים מציעים שהקישור בין פיברין לבין A2AP הוא הגורם המרכזי של העמידות הפיברינוליטית של הפקקת (Reed ו-Houng ב-Circulation משנת 1999, ו-Rijken וחב' ב-J Thromb Hemost משנת 2016). בתנאי in vivo, פקטור VIII משופעל יכול לתרום לדינמיקה של תרומבוזה, על ידי תגובות שניוניות כגון קישור של מעכבים פיברינוליטיים כגון plasminogen activator inhibitor-1 (להלן PAI-1) או thrombin-activatable fibrinolysis inhibitor (להלן TAFI). במבחנים in vitro (Byrnes וחב' ב-Blood משנת 2015) הראו התמוססות של פקקות פולמונריות ex vivo, בהשוואה לעכברים החסרים PAI-1, מה שמרמז לכך ש-A2AP היא תורמת דומיננטית ביצירת עמידות לפיברינוליזה של הפקקת (Dewerchin וחב' ב-Thromb Hemost משנת 2001).
התפקיד של A2AP בפקקת ורידית עמוקה
מאז שהתגלה ההשפעות של A2AP נחשבו ככאלה המוגבלות לעיכוב ההמסה של פקקות שכבר נוצרו, ולא נחשב כבעל תפקיד בוויסות יצירת פקקת (Mukhopadhyay וחב' ב-Front Immunol משנת 2019). עם זאת, ראיות חדשות מראות ש-A2AP מווסת את אתחול הפקקת ואת התפתחותה, והוא נדרש ליצירת פקקת ורידית עמוקה בעכברים, בהם רמות נורמליות של A2AP ליצירת פלזמין מושרה על ידי תרומבוזה, אלא שהאחרונה מתקדמת כיוון שהפלזמין שנוצר אינו מספיק להתגבר על ההשפעות האנטי-פיברינוליטיות של A2AP. למעשה, בחסר של A2AP, הפיברינוליזה המושרית על ידי פלזמין, מונעת את האתחול והמיצוב של תהליך הפקקת. אכן, בפקקת ורידית המושרית על ידי סטאזיס (אי שפיעת דם) או על ידי סטנוזיס (שפיעת דם מוגבלת), עכברים מסוג −/−α2AP אינם מפתחים פקקת אפילו לאחר שעות אחדות עד שבועות. הדרישה מצד A2AP לאפשר את ההתפתחות של פקקת נראית מתווכת דרך העיכוב על ידי A2AP של פלזמין, כיוון שמעכב פלזמין אחר, ε-aminocaproic acid, משחזר את יצירת הפקקת בהיעדר A2AP. במודל בעכברים של פקקת ווריד הצוואר (jugular vein) הנגרמת כתוצאה מפגיעה אנדותליאלית, חסר של A2AP גרם להשהיה בחסימה ולזילוח מוקדם (reperfusion) בהשוואה לעכברי ביקורת (Matsuno ב-Thromb Hemost משנת 2002).
A2AP בתסחיף ריאתי
תסחיף ריאתי נגרם כאשר פקקת הנוצרת בוורידים העמוקים ברגליים, נתלשת מהדופן הווסקולרי ונודדת לריאות, שם היא גורמת לסיבוכים מסכני-חיים (Huisman וחב' ב-Nat Rev Dis Primers משנת 2018). מחקרים in vivo בעכברים ובחיות אחרות הראו שהמסת הפקקת יכולה להיות מושגת על ידי מעכב של A2AP ביעילות מוגברת ללא דימום מוגבר. במודל של תסחיף ריאתי בחֲמוס הבית (ferret).
עיכוב של A2AP על ידי נוגדן חד-שבטי, הגביר את המסת הפקקת הניסויית, על ידי tPA ללא הגברה בפירוק של פיברינוגן. בדומה, עכברי -/-A2AP הראו המסה מוגברת של תסחיפים ריאתיים הנוצרים בפלזמה של עכברי +/+A2AP-Blood (Lijnen וחב' ב-Blood משנת 1999), אם כי בשני מבדקים של דימום עכברי -/-A2AP לא הראו דימום מוגבר בהשוואה לעכברי +/+A2AP. פרמטרים המוסטאטיים אחרים, כולל פלסמינוגן, רמות PAI-1, המטוקריט ורמות פיברינוגן היו ברי השוואה בעכברים -/-A2AP ובעכברים +/+A2AP. התפקיד של A2AP נלמד גם במודל של פקקת פולמונרית המושרית על ידי קרינה פוטוכימית, בווריד הצוואר בעכברי -/-A2AP (Matsuno וחב' ב-Thromb Hemoist משנת 2003). במודל זה, חסר של A2AP היה כרוך עם שקיעה מופחתת של פיברין אנדוגני בכלי הדם הפולמונריים והישרדות מוגברת בהשוואה לביקורת של עכברי +/+A2AP. עיכוב של הקישור של A2AP לפיברין על ידי פקטור VIII משופעל, הגביר פיברינוליזה באופן בולט בתרומבו-תסחיפי פולמונרי ניסויי. לבסוף, ההשפעות ההשוואתיות של מעכבי A2AP, נלמדו במודל אנושי של תסחיף ריאתי בעכברים.
השפעות לא-פיברינוליטיות של A2AP
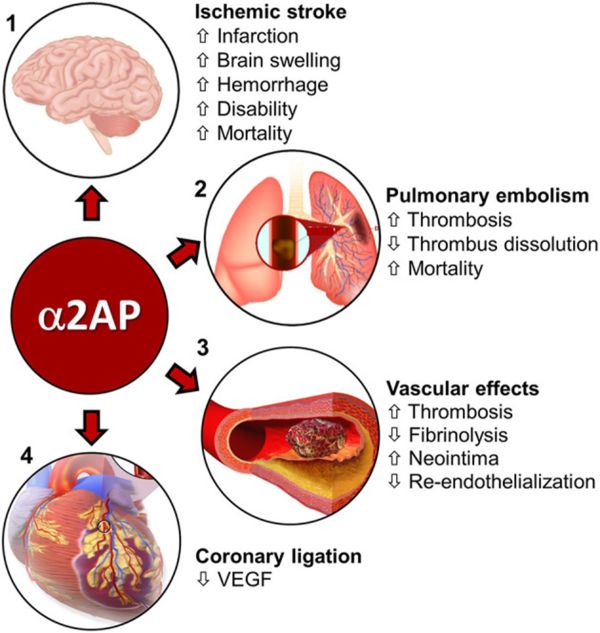
ל-A2AP יכולות להיות השפעות לא-פיברינוליטיות במצבים פתו-פיזיולוגיים שונים. חסר של A2AP בעכברים, מפחית את הפיברוזיס במודלים שונים של מחלות פיברוטיות (Kanno וחב' ב-Arthritis Rheum משנת 2013). סרטן הוא אחד מגורמי הסיכון של DVT, ו-A2AP מאפשר הופעת DVT. עם זאת, A2AP מפחית הופעת גרורות במודל סרטן בעכברים (Paquet-Fifield וחב ' ב-Growth Factors משנת 2013). במוח, A2AP מופיע בעיקר בנוירונים בהיפוקמפוס והוא חיוני לצמיחה של דנדריטים דרך מסלולי פרוטאין קינאז הכרוכים ב-p38 microtubule בעכברים (Kawashita וחב' ב-J Neurochem משנת 2014, ו-Kanno וחב' ב-PLoS One משנת 2014). חסר ב-A2AP נכרך בפגיעה בתפקוד מוטורי, בתפקוד קוגניטיבי, בדאגנות, ובהתנהגות דיכאונית בעכברים. במודל בעכברים של מחלת אלצהיימר, הפחתה כרונית של רמת A2AP בדם על ידי טיפול עם antisense oligonucleotide, הגבירה את השפעול של מקרופאגים ותאי glia והגדילה את יצירת הטרשת הפיברילרית, אף על פי שהיא לא שינתה את סך שקיעת הטרשת (Baker וחב' ב-Proc Natl Acad Sci USA משנת 2018). חסר ב-A2AP מחיש ריפוי פצעים, כנראה דרך הגדלת ההפרשה של VEGF (ללKanno חב' ב-J Thromb Hemost משנת 2006). מעכבים של A2AP בעכבר מגבירים את התיקון של נזק פציעתי בכבד בהשוואה לביקורת (Okada וחב' ב-J Hepatol משנת 2004). חסר של A2AP מפחית הארתריו-סקלרוזיס לאחר פגיעה בכלי-דם (Matsuno וחב' ב-Blood משנת 2003).
חסר של A2AP באדם: מולד ונרכש
חסר מולד של A2AP (מחלת Miyasato) נדיר ביותר, נכרך עם פנוטיפ של טראומה מעוכבת או של דימום ספונטני בצורת המטומה או על ידי hemarthosis (דימום אל תוך מפרק, בדרך-כלל עקב פציעה, או קשור למחלת דם, כגון המופיליה). דימום בחסר A2AP בדרך כלל מבוקר על ידי tranexamic acid או על ידי Ɛ-aminocaproic acid, החוסמים פיברינוליזה מתווכת על ידי פלזמין (Favier וחב' ב-Br J Hematol משנת 2001). חסר גנטי הומוזיגוטי תואר במטופל בן 62 שנה (Vigano וחב' ב-Thromb Res משנת 2018), מה שמצביע על כך שחסר של A2AP למשך כל החיים, יכול להיות נסבל. מטופלים עם חסר הטרוזיגוטי של A2AP אינם מראים באופן נורמלי דימומים פנוטיפיים, אלא אם כן היה מדובר בטראומה או בניתוח, ויש דיווחים ספורדיים של חסר הטרוזיגוטי של A2AP במטופלים בני 83 שנה (Ikematsu וחב' ב-Thromb Res משנת 1996).
חסר מולד יכול להיות כמותי עם רמות מופחתות של A2AP, או איכותי עם תפקוד חלבון מופחת, אך את שניהם קשה לגלות בבדיקות קואגולציה שגרתיות, כאשר פרמטרים המוסטטיים אחרים נורמליים במטופלים. חסר כמותי של A2AP עם רמות חלבון נמוכות יכול להיגרם על ידי מוטציה נקודתית כגון מוטציית A2AP-Paris-Trousseay בה רמת A2AP היא 15% מהנורמה, או מוטציית Val384-Met בה רמת A2AP שווה בערך ל-50% מהנורמה, או מוטציית שמט (deletion) הידועה כ-A2AP-Okinawa, בה רמת החלבון נמוכה מ-1% מהנורמה, או מוטציית frameshift הידועה כ-A2AP-Nara הנמוכה מ-1% של הנורמה. חסר כמותי או פונקציונלי של A2AP אנושי (Enschede), נגרם על ידי על ידי מוטציית תוסף (insertional) בלולאת הפעילות המרכזית של החלבון כאשר יש אלנין המתווסף, הגורמת לו להתנהג כמו מצע של פלזמין, במקום שיתנהג כמעכב שלו (Holmes וחב' ב-Science משנת 1987, ו-Rijken וחב' ב-Biochem J משנת 1988).
חסר נרכש של A2AP יכול להיגרם על ידי גורמים תרומבוליטיים כגון משפעלים של פלסמינוגן, פלסמין או מיקרו-פלסמין, או על ידי מצבי מחלה כגון מחלת כבד חמורה, או לויקמיה חריפה (Reed וחב' ב-Semin Thromb Hemost משנת 2017). רמות מוגברות של A2AP כרוכות פרוספקטיבית עם סיכון מוגבר של אוטם שריר לב (Meltzer וחב' ב-Blood משנת 2010), או של שבץ מוחי איסכמי (Suri וחב' ב-Cerebrovasc Dis משנת 2010). בחולי אלצהיימר, הביטוי של A2AP גדל ברקמת המוח וכרוך עם הרבדים של amyloid-β (Barker וחב' ב-J Cell Mol Med משנת 2012). במהלך מחקרים מוקדמים של משפעלי פלסמינוגן. נמצא שרמות A2AP היו נמוכות לפני או ביחד עם רמות פיברינוגן, שהיו מבשרים של סיבוכי דימומים קליניים (Collen ו-Verstraete ב-Thromb Res משנת 1979,ו-Leebeek וחב' ב-J Am Coll Cardiol משנת 1990). אכן, הוספה של A2AP נחשבה עזר לתרפיה עם tPA למניעת סיבוכי דימומים (Weitz וחב' ב-J Clin Invst משנת 1993). עם זאת, מחקרים עדכניים יותר מראים ש-A2AP הוא המעכב של פיברינוליזה פיזיולוגית ושרמות מוגברות של A2AP עלולות להזיק במחללות קרדיו-וסקולריות וצרברו-וסקולריות (Lijnen ו-Collen ב-Blood Coagul Fibrinolysis משנת 1989, ו-Coughlin ב-FEBS J משנת 2005).
נוגדנים חד-שבטיים המעכבים פעילות של A2AP
השימוש בנוגדנים חד-שבטיים לעיכוב פעילות A2AP על מנת להגביר את המסת הקריש (Reed וחב' ב-Proc Natl Acad sci USA משנת 1990, ו-Sakata וחב' ב-Blood משנת 1989). נוגדנים חד-שבטיים מעכבר גרמו להמסה ספונטנית של קריש באדם. למרות הגברת הפיברינוליזה, שילוב של A2AP עם ריכוז נמוך ביותר של משפעלי פלסמינוגן, גרם לשבירה פחותה של פיברינוגן בהשוואה למשפעלי פלסמינוגן לבד. כפי שהוזכר למעלה, A2AP מגביר פיברינוליזה במספר מודלים שונים של פקקת ורידית בחיות, של תסחיפים ריאתיים, ושל שבץ איסכמי (Su ו-Lawrence ב-Artherioscer Thromb Vasc Biol משנת 2014, Butte וחב' ב-Circulation משנת 1997, ו-Singh וחב' ב-Blood משנת 2019). במודל אנושי של תסחיפי ריאות בעכברים, נוגדן חד שבטי הידוע כ-TS23 המעכב את A2AP האנושי, הגביר את המסת התסחיפים הריאתיים במינון של 3 מיליגרם/ק"ג, אף על פי שנוגדן זה לא הגביר את הדימום העורקי או הוורידי (Singh וחב' ב-Circulation משנת 2017). עירוי של פלזמין, גורם לחסר ב-α2AP, ועובדה זו שימשה כטיפול ניסיוני בפגיעה תרומבוטית בעכברים, Marler עשה שימוש באסטרטגיה דומה עם היפותזה שונה, דהיינו שהצנתר המחדיר פלזמין באופן מקומי, יגביר את פירוק הקריש ולאחר מכן אספקת הפלזמין המופרש תנוטרל על ידי A2AP בצירקולציה באופן שפלזמין לא יכיל השפעות צדדיות (J Thromb Haemosts משנת 2010 ו-Novokhatny וחב' ב־J Pharmacol Sci משנת 2004). תרומבוציטים מומסים בפלזמין בריכוז של 4 מיליגרם/ק"ג הומסו באבי העורקים האבדומינלי ולא הגבירו את הדימום (Marler וחב' ב-Thromb Hemost משנת 2001). פלזמין במינון של עד 8 מיליגרם/ק"ג, נטרל לחלוטין 60% מפעילות A2AP, אך גם גרם לחסר בפיברינוגן כמו גם בפקטור VIII, והגביר את הדימום (Stewart וחב' ב-Blood משנת 2003).
הוראות לביצוע הבדיקה
איסוף הדגימה: את הדם יש ליטול במבחנת סודיום-ציטראט (3.2% sodium citrate, פקק בצבע תכלת) ולאחר הסרכוז של להעביר את הדם למבחנת פלסטיק ולסרכז את הפלזמה פעם נוספת. יש להעביר את הפלזמה לאחר הסרכוז השני למבחנת פלסטיק ולהקפיא את הדגימה מייד (לא יאוחר מ-4 שעות לאחר נטילת הדם) בטמפרטורה של מינוס 20 מעלות צלזיוס, או אף עדיף בטמפרטורה של מינוס 40. הסרכוז הכפול קריטי להרחקת טסיות מהדגימה. יש לפסול דגימות מאוד המוליטיות מאוד ליפמיות ומאוד איקטריות. כאשר הדגימה מועברת למבחנת סודיום-ציטראט ומוקפאת היא יציבה למשך 14 יום. הבדיקה נעשית בשיטה כרומוגנית.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק