בלוטת התריס - מבנה, תפקוד ובדיקות - The thyroid gland - anatomy, physiology and testing
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הבלוטות האנדוקריניות | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – בלוטת התריס
אמבריולוגיה
הבלוטה מופיעה בגיל שלושה שבועות כפרוליפרציה של תאי אפיתל ברצפת הפרינקס, במקום בו נמצא foramen cecums בלשון. התירואיד יורד ורוכש תאים מזודרמלים, כמו התאים הפראפוליקולרים מסוג C המפרישים קלציטונין. בסוף החודש השלישי נוצרים הפוליקולי, המכילים קולואיד וייתכן שכבר אז הבלוטה מפרישה הורמון. בירידתה, בלוטת התריס קשורה ל- thyroglossal duct הנסגר במרבית התינוקות. המיקום הסופי של הבלוטה בעובר הוא קדמית ל-hyoid והסחוס של הלרינקס.
נדידה של רקמת הבלוטה למיצר הקדמי שכיחה, לכן בחלק מהחולים הזפק הוא סובסטרנלי. נדיר למצוא רקמת תירואיד במדיאסטינום האחורי, ובדרך כלל לא קיים קשר אנטומי בינו לבין הבלוטה הצווארית. לעתים ניתן למצוא בלוטת תריס תחת הלשון. כריתת הבלוטה הזו יכולה לגרום להיפותירואידיזם, עקב היותה רקמת התירואיד היחידה.
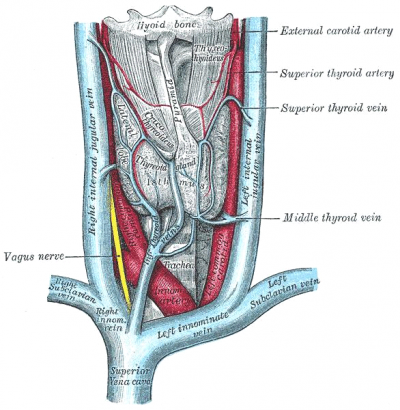
אנטומיה
בלוטת התריס שוקלת כ-20 גר' וממוקמת בחלק התחתון של הצוואר, קדמית לקנה הנשימה. היא מורכבת ברוב המקרים משתי אונות המחוברות אחת לשנייה ומבנה בעל צורת פרפר. איזור החיבור נקרא המיצר (isthmus), כאשר חלקו העליון נמצא למטה מסחוס הקריקואיד. ב-30% מהאנשים קיימת אונה נוספת מרכזית באזור החיבור בין שתי האונות הצדדיות - האונה הפירמידלית, על שום צורתה הדומה לפירמידה (איור 1.14-2.14).הבלוטה מוקפת בקפסולה פיברוטית דקה החודרת לבלוטה ויוצרת אוניות מדומות (פסוידו-לוביולים).
מבנה הרקמה של בלוטות התריס הוא של ACINI המוקפים שכבת תאי אפיתל. במרכז החלל יש נוזל המכיל חלבונים בעיקר תיירוגלובולין - thyroglobulin. בנוסף, קיימים ברקמת בלוטת התריס תאי C שמקורם ברקמה מיוחדת של "הרכס הנוירולי" (Neural crest). תאים אלו מייצרים את הקלציטונין.
גנטיקה של התפתחות בלוטת התריס: ההתפתחות הגדולה שחלה בהבנת הגנום האנושי הביאה גם לזיהוים של גנים האחראיים בצורה ישירה על התפתחות בלוטת התריס. הגנים השולטים על התפתחות הבלוטה הם ( Thyroid Transcription Factor) TTF2, TTF1 וה- PAX8. למרות זאת, רוב הבעיות המולדות הגורמות לחוסר בבלוטת התריס או להפרעה בתפקודה אינן נובעות ממוטציות בגנים אלו.
אספקת הדם
אספקת הדם מקורה בעיקר מ-inferior thyroid artery שהוא ענף של ה- sub-clavian artery ומה-superior thyroid artery, היוצא מה- .external carotid artery ה- thyroidea ima artery יכול להיות בקוטר שונה ומוצאו מה-innominate artery או מקשת אבי העורקים. הוא עולה לאורך הטרכאה וחודר לחלק התחתון של בלוטת התריס (איור 1.14). אספקת הדם לבלוטה מצוינת, ומיוחסת לתפקוד האנדוקריני שלה. בכל דקה עוברים בבלוטה כ-6-4 מ"ל של דם לכל גרם רקמת בלוטה. כמות זו גבוהה פי 50 מזו העוברת לכל גרם רקמה בגוף.
היסטולוגיה
בהיסטולוגיה ניתן לראות מבנים פוליקולריים המלאים בקולואיד חלבוני. קיר האציני בנוי מתאים קובואידלים, בשכבה בודדת, היושבים על ממברנה בסיסית עשירה בקפילרות. 40-20 אציני יוצרים lobule, המקבל אספקת דם עשירה מענף עורקי נפרד. גובה תאי האפיתל נגזר מתפקודו ומפעילותו של התא והוא בממוצע 15 מיקרון. קוטר כל פוליקל הוא כ- 200 מיקרון.
פיזיולוגיה
התפקיד הראשוני של בלוטת התריס הוא לייצר כמות מספקת של תירוקסין לתצרוכת הגוף. תפקודה של בלוטת התריס קשור בצורה הדוקה ליוד. בלוטת התריס היא בעלת יכולת מדהימה לריכוז יוד והיא למעשה מאגר היוד הגדול ביותר בגוף. בתאי הבלוטה קיימת משאבה מולקולרית רבת עוצמה המחליפה יוני נתרן (הנפלטים החוצה) ביוני יוד (המוכנסים לתאי בלוטה). משאבה זו מסוגלת להביא לריכוז של יוני יוד בתאי בלוטת התריס ביחס של 50-100:1 לריכוז בדם. תצרוכת היוד היומית המומלצת עבור מבוגר העומדת על כ-150 -200 מייקרוגרם (בילדים הדרישה היא בין 120-70 מייקרוגרם ליום, ובתינוקות 30 מייקרוגרם לקילו ליום), נובעת רק מהאיבוד המינורי של יוד המתרחש בכליה. שאר היוד הקיים בגוף עובר מחזור יומי בזכות יכולתה של בלוטת התריס ללכוד אותו מהדם. תפקידו העיקרי של היוד הוא ביצור הורמוני בלוטת התריס. בתזונה הממוצעת למבוגר כיום יש די והותר יוד למניעה. יש לציין שחוסר ביוד שכיח מאוד באזורים הרריים רבים (מי השלגים עניים ביוד) ובמרכז אפריקה. עקב מצבי רעב נוצר חוסר תזונתי ביוד, המהווה את הסיבה השכיחה ביותר לפיגור שכלי הניתן למניעה (קראטיניזם). תוספות של כמויות יוד קטנות למלח וללחם הפחיתו בצורה משמעותית את מספר הילדים שנפגע באזורים עניי יוד ברחבי העולם. לעמת זאת, עודף ביוד אף הוא אינו מומלץ ולא בריא ועלול להביא למחלות אוטואימוניות של בלוטת התריס.
הבסיס הביוכימי של הורמונים אלו הינה החומצה האמינית טירוזין. כדי שהיוד יוכל לחבור לחומצה זו עליו לעבור תהליך אורגניפיקציה, כלומר חמצון המבוצע בעזרת האנזים הפראוקידאז של בלוטת התריס .(TPO -Thyroidal Peroxidase)
בזמן דרישה להורמוני תריס מועבר חלבון זה אל גוף התאים. מהחלבון שעבר יודינזיה נקטעים שיירי הטירוזין (שתי מולקולות טירזין ועליהן ארבעה יוני יוד) המהווים את הורמוני התריס המופרשים לדם. מבלוטת התריס מופרשים שני סוגי הורמונים התירוקסין. האחד, ה-4T מכיל שני שיירי טירוזין וארבע מולקולות יוד. ההורמון השני, הטרי-יודותירוקסין ה-3T מכיל שני שיירי טירוזין אך רק שלוש מולקולות יוד. רוב ההורמונים המופרשים מבלוטת התריס הם מסוג T4 ורק מיעוט הוא מסוג T3 (היחס הוא 20:1). אולם, הורמוני ה-T3 הם בעלי פעילות ביולוגית משמעותית הרבה יותר מהורמוני ה-4T מחקרים מראים שפעילותו הביולוגית של T3 גדולה פי 3 עד 4 מזו של T4.
לאחר הפרשת ההורמונים מהבלוטה הם נשאים בדם על ידי חלבונים קושרי הורמוני בלוטת התריס (TBG-Thyroxine Binding Globulin) ועל ידי האלבומין. למעשה רק חלק קטן נמצא במצב חופשי ופעיל (כ-0.03 אחוז מכלל ה- T4 בדם ו-0.3 אחוז מה-3T) ושאר ההורמונים הקשורים לחלבונים השונים אינם פעילים כלל מבחינה ביולוגית. על הורמון ה-T4 פועל אנזים המכונה דה-יודינאז המוריד מולקולת יוד בודדת מהורמון ה-T4 ובכך הופך אותו ל-3T .
קיימים שני סוגי דה-יודינאז. פעילות הדה-יודינז מסוג 1 מתבצעת בעיקר בכבד ובכליות ובמספר רקמות נוספות. במוח ובבלוטת התריס קיים אנזים שונה מזה שבשאר רקמות הגוף המבצע את פעולת הדה- יודינציה המכונה דה-יודינאז מסוג 2. אנזים זה מגביר את פעילותו בזמן חוסר בהורמוני בלוטת התריס, ובכך הוא מעלה את רמת ההורמונים הפעילים ברקמות אלו.
קיימת מולקולת דה-יודנאז נוספת המכונה מספר 3 ותפקידה הוא דווקא הפוך - היא גורמת להפסקת פעילותם של הורמוני בלוטת התריס. האנזים דה-יודינאז זקוק למולקולת סלניום לצורך פעילותו. רוב פעילותם של הורמוני התריס מבוצעת למעשה על-ידי ה-T3 ולא ה-4T למרות שריכוזו בדם נמוך בהרבה מזה של ה-T4 ביחס של 1:50.
בקרה על פעילות בלוטת התריס
הבקרה על תפקוד הבלוטה מחולקת למספר רמות, כשבין הרמות השונות קיימות מערכות איזון ובקרה המתאמות את השליטה בהפרשת הורמוני התריס מהבלוטה בכל רגע נתון. ההורמון שנמצא בראש הפירמידה הוא TSH- Releasing Hormone) TRH). הורמון זה מופרש על-ידי ההיפותלמוס בגרעינים הקדמיים, ומשפיע על בלוטת יותרת המוח (היפופיזה) להפריש את ה-TSH (Thyroids Stimulating Hormone ) המיוצר ומופרש בחלק הקדמי של בלטות יותרת המוח. הוא מורכב משתי שרשראות חלבוניות. האחת מכונה שרשרת אלפא, המשותפת למספר הורמונים המופרשים מבלוטת יותרת המוח. השרשרת השניה והייחודית להורמון זה מכונה שרשרת בטא. ההפרשה הנורמלית של TSH היא כ-125מיקרוגרם ליום.
כאשר יש גירוי של TRH, מופרש TSH בכמות גדולה יותר גורם לתאי בלוטת התריס לייצור והפריש הורמוני בלוטת התריס וכן גורם להגדלת נפח הבלוטה. הורמוני בלוטת התריס עצמם הם בעלי השפעה מעכבת על הפרשת TRH- TSH ובכך נוצרת לולאת משוב שלילית (negative feedback), המאפשר עיכוב ייצור של הורמונים כשרמתם גבוהה, מחד גיסא, וייצור כמויות רצויות של הורמונים כשרמתן בדם יורדת, מאידך גיסא.
ה-TSH פועל על התאים השונים של בלוטת התריס דרך קולטן. כאשר נקשרת מולקולת TSH אל הקולטן שלה נוצרת יחידת חלבון פעילה המסוגלת לגרום לתא לפעילויות ספציפיות שלא ניתן היה לבצע טרם לכן.
קיימות מולקולות נוספות המשפיעות על פעילות בלוטת התריס, למשל יוד עצמו. חוסר ביוד, עקב צריכת כמויות קטנות מהנדרש, מעכבת את פעילות הבלוטה וגורמת לחוסר בהורמוני התריס, הגורם לעליה ברמות ה- TSH והיווצרות זפק (goiter). לעומת זאת, מתן כמות גדולה וחדה של יוד הוא בעל השפעה מעכבת מידית על פעילות הבלוטה, הנגרמת עקב הקפאת תהליך האורגניפיקציה של היוד - אפקט וולף-צייקוב (Wolf-Chaikoff Eeffect). העיכוב הזה הינו זמני בלבד, אולם ניתן להשתמש באפקט זה, למשל, כאשר יש חשד לחשיפה לזיהום רדיואקטיבי המכיל יוד רדיואקטיבי. מתן תמיסת יוד (המכונה תמיסת לוגול) מונע את חדירת היוד הרדיואקטיבי לבלוטה ומונע התמרה עתידית סרטנית עקב חשיפה לרדיואקטיביות. באנשים שלהם הפרעה אוטואימונית של בלוטת התריס לאפקט וולף-צייקוב יש השפעה מתמשכת יותר.
מגוון גדול יחסית של מולקולות ביולוגיות נוספות נמצאו כבעלי השפעה על תפקוד הבלוטה, כגון: IGF-1, TGF-Bn ואחרים.
קישור ההורמון לקולטן, הוא זה שמתחיל את מפל האירועים בתא. הקולטן של הורמוני התריס נמצא דווקא בגרעין ויש לו שתי גרסאות המכונות אלפא ובטא. כאשר הורמוני התריס חודרים לתא, הם נקשרים לקולטנים הללו והקומפלקס שנוצר מסוגל להתקשר ל-DNA שבגרעין התא ולגרום להפעלתם של גנים שלא היו פעילים לפני כן, או לחילופין למנוע את פעילותם של גנים אחרים. כאשר הקולטנים אינם קשורים להורמוני תריס, הם נקשרים לחלבונים שונים ופעילות זו מקנה להם פעילות מעכבת על גנים שונים ב- DNA. פעילות מעכבת זו מסבירה מדוע חוסר של הורמוני תריס (בתת פעילות של הבלוטה) כרוכה בהשפעות שליליות כל כך על הפיזיולוגיה התקינה בגוף (מעבר לנזק הנגרם עקב חוסר בהורמוני התריס). הורמון ה-T3 נקשר ביעילות הרבה יותר גדולה לקולטנים. עובדה זו תורמת לפעילותו החזקה יותר ביחס לזו של T4.
מבחנים לתפקודי בלוטת התריס
- TSH - רמת ^TSH בדם ניתנת למדידה. הרמות הנורמליות הן בטווח שבין 0.4 ל-4 מיקרו יח'/מ"ל. רמה נמוכה מזו מצביעה על דיכוי הפרשת ^TSH על-ידי תירוקסין ממקור חיצוני או אנדוגני. רמות גבוהות של TSH מצביעות על ירידה ברמת התירוקסין או הפרשה אנדוגנית שלא ממקור היפופיזרי.
- נוגדנים לבלוטת התריס הם:
- (antithyroglobulin (TGHA.
- (thyroid anti-microsomal (MCHA הניתנים למדידה בנסיוב.
רמה גבוהה של האנטיבודיס הללו ניתן למצוא בחולים הלוקים במחלת Graves או בדלקת של בלוטת התריס.
- רמות T3 ו-T4 נבדקות ב- radioimmunoassay. הערך הנורמלי של T4 הוא 11.5-4.6 מיקרו"ג% ושל T3 220-80 מיקרו"ג%. כיום ניתן למדוד את הרמה של ההורמון הבלתי קשור: הערך הנורמלי של FT4 הוא 2.5-0.4 מיקרו"ג%.
- 131-thyroid uptake of Iodine - במבחן זה נותנים יוד מסומן במינון 15-2 מיקרו׳׳ג דרך הפה, וקוראים את הקליטה הרדיואקטיבית מעל הבלוטה, כעבור 24 שעות. שיעורי הקליטה התקניים נעים בין 15% ל-45% לאחר 24 שעות.
- T3 רזין - במבחן זה מוסיפים לנסיוב החולה T3 מסומן ורזין. אם ה-TBG קשור ל-T3 מקורי הרי ברזין תימצא ספיחה גבוהה של T3 מסומן ולהיפך. בפעילות יתר של בלוטת התריס הספיחה גבוהה, ובתת-פעילות הספיחה נמוכה.
- TRF stimulation test - מתן TRF גורם להפרשת יתר של TSH, הניתן למדידה. מבחן זה חשוב באבחון hypothyroidism (טבלה 1.14).
- thyroid supression test - מבחן הבודק את הציר הפיטואיטרי-תירואיד ומבוסס על ההנחה שמתן T3 לא מדכא את תפקוד בלוטת התריס במצב של שיווי משקל נורמלי. נותנים לנבדק T3 לשבוע במינון של 100 מיקרו"ג ליום ובודקים את קליטת היוד המסומן בבלוטה. אם שיעור הקליטה נמוך מ-20% הרי קיים דיכוי, אם שיעור הקליטה גבוה מ-20% זו הוכחה לפעילות יתר של הבלוטה או לשאת. אין לבצע את המבחן באנשים עם BMR גבוה מאוד או בחולים הלוקים במחלות קרדיאליות ווסקולריות קשות.
- מבחן הגירוי על-ידי התירוטרופין (thyrotropin stimulation test) - מבחן זה בודק את השפעת ה-TSH על הבלוטה. נותנים לחולה 10-5 יחידות TSH. עלייה של 10% בקליטת היוד המסומןבבלוטה, או עלייה של 2 מיקרו"ג ברמת התירוקסין בנסיוב מוכיחה שהבלוטה מגיבה ל-TSH.
- כולסטרול בנסיוב - מוגבר בהיפותירואידיזם.
תירואיד היפופיזה היפותלמוס
נמוך נמוך נמוך בנסיוב TSH
יותר גבוה אין תגובה מוגבר TSF אחר גירוי
אין תגובה מוגבר מוגבר חיצוני TSH
טבלה 1.14: היפותירואידיזם בהתאם למקום הפגיעה
בדיקות לקיום שינויים אנטומיים בבלוטת התריס:
- אולטרה-סאונד של הבלוטה - האולטרה-סאונד הינה הבדיקה המקובלת כיום לאבחון שינויים אנטומיים בבלוטת התריס. בעזרת האולטרה-סאונד ניתן לבצע מדידות של גודל הבלוטה ולראות נגעים סולידיים או כיסתיים בתוכה.
- טומוגרפיה ממוחשבת - בטומוגרפיה ממוחשבת ניתן לראות את גודל הבלוטה, אם קיימים בה נגעים ובמיוחד האם הבלוטה גולשת לתוך המיצר (מדיאסטינום גויטר רטרוסטרנלי) (תצלום 1.14 -2).
תצלום 1.14: CT צוואר - חזה עליון המראה זפק צווארי הדוחק את הוושט והקנה (החצים מראים את גודל הזפק)
תצלום 2.14: CT צוואר המראה גויטר גדול מלווה בלחץ על הקנה (החצים מצביעים על גבול הגויטר באזור הקנה)
- מיפוי הבלוטה על-ידי חומר מסומן כמו פרטכנטט מראה את מבנה הבלוטה ופגמים שבה (תצלום 3.14).
תצלום 3.14: מיפוי בלוטת התריס - קשר קר-לא קולט חומר (חץ)
- מיפוי עם יוד מסומן - מלמד על התפקוד של הבלוטה והאם הנגע שבה קולט יוד או לא. קשר קר משמעותו קשר שלא קולט יוד ולכן מחייב בירור לשלילת שאת; קשר חם - קולט יוד ובדרך כלל מלמד על קשר המתפקד עצמאית. קליטה ירודה בכל הבלוטה מלמדת על ירידה בתפקוד עקב תירואידיס או היפותירואידיזם וכו'.
- דיקור מחטי של נגעים בבלוטת התריס מלמד על אופי הנגע.
דיקור שאיבה במחלות בלוטת התריס
אחת הבעיות במחלות בלוטת התריס היא, כיצד להבדיל בין קשרית שפירה, ששכיחותה גבוהה, לבין קשרית ממארת, שהיא נדירה, יחסית. קיימות טכניקות קדם-ניתוחיות להשלמת ההערכה הקלינית של קשרית בבלוטת התריס. החשובה שבהן היא סריקה בעזרת חומר רדיואקטיבי, המסווגת את הקשריות ל"חמות" - שהן בעלות פעילות הורמונלית ושיעור ממאירות קטן מאוד, ול"קרות" - שאינן פעילות; מקובלת הדעה, שרוב השאתות הממאירות הן קרות. עם זאת, רוב הקשריות הקרות - שפירות.
דיקור בשיטת השאיבה הוכנס לשימוש ב-1952 והיה מקובל במרכז אירופה ובסקנדינביה. דיקור השאיבה במחט עדינה היא בדיקה פשוטה, בטוחה וניתנת לביצוע אמבולטורי. אין צורך באלחוש מקומי ואי-הנעימות לחולה - היא מזערית. הדיקור מבוצע באמצעות מחט בקוטר 25-23 G, כאשר המזרק מוצמד למתקן תת-לחץ מיוחד. מהחומר המתקבל מתקינים משטח העובר קיבוע וצביעה. הסיבוכים האפשריים בעקבות הבדיקה, כגון התהוות דימומים, זיהום מקומי או דיקור קנה, נדירים ביותר.
אבחנה ציטולוגית של ממאירות מתאפשרת כאשר קיים שגשוג ניכר של תאים המראים אטיפיה או פליאומורפיסם של גרעינים. מבנים פאפילריים או "גופיפי פסמומה" אופייניים לשאת ממארת פאפילרית. צביעת קונגו-אדום חיובית לעמילואיד ו/או מדידה של רמות גבוהות של היסטאמינאזה בספירט מאפשרות אבחנה של שאת ממארת לימפטית. קיים קושי באבחנה בין שאת זקיקית (פוליקולרית) לשאת שפירה (אדינומה) ולשאת ממארת (well differentiated follicular carcinoma), כיוון שההבדל ביניהן הוא בחדירות הקפסולרית והווסקולרית. משום כך הבדיקה הציטולוגית אינה מספקת במקרים אלה.
הצלחת הבדיקה בחיזוי מחלה קשריתית שפירה או ממארת הגיעה לשיעורים של 94%-75%. שיעור תוצאות כוזבות חיוביות (false positive) נע בין 0% ל-15%. שיעור תוצאות כוזבות שליליות (false negative) נע בין 1.2% ל-6%. ההתאמה הדיאגנוסטית בלטה בשאתות פאפילריות מוצקות ובשאתות ממאירות גרורתיות; במקרים של גושים ניווניים ופורמציות כיסייתיות (ציסטיות) עם נוזל דמי, הבדיקה פחות אמינה.
גילוי מקרים של ממאירות סמויה בניתוח תוארה בסדרות אחדות. שאתות מיקרוסקופיות אלו אינן נדירות בבלוטות תקינות מבחינה קלינית ואי-גילוין על-ידי דיקור שאיבה אינו צריך להחשב ככישלון השיטה.
לדיקור שאיבה נודע גם ערך טיפולי. היעלמות כיסית (ציסטה) לאחר ריקון תוכנה, ללא אגירה מחודשת של נוזל היא תופעה מדווחת.
הכנסת בדיקת האולטרה-סאונד באה לסייע בבחירת חולים לדיקור שאיבה. בדיקה זו מאפשרת להבדיל בין קשרית מוצקה, כיסייתית או מעורבת. האבחנות הציטולוגיות מדויקות יותר בקשריות מוצקות, ופחות אמינות בגושים ניווניים גדולים, שבהם קיימת גם נטייה לצבירה מהירה של נוזל לאחר ריקון. לכן, הרקת נוזל דמי מגושים ניווניים אלה אינה מוצדקת, ויש בה צורך רק כאשר המטרה היא להקל על לחץ מקומי. דיקור בזמן שיקוף אולטרה-סאונד נעשה מקובל ביותר וזאת במטרה להימנע מדיקור אזורים ניווניים.
הדעות חלוקות לגבי הצלחת דיקור השאיבה והאבחנה הציטולוגית בדלקות של בלוטת התריס. בסדרה של Galvan אובחנו נכונה 7 מקרים של דלקת חדשה בבלוטת התריס. לעומת זאת, מתוך 24 מקרי האשימוטו, אובחנו 11 כשינוי שפיר לא-דלקתי, ורק 13 הנותרים אובחנו נכונה. Wang וחבריו לא הצליחו להבדיל בין מחלת האשימוטו לבין לימפומה ממארת; לכן, לדעתם, במקרה של תירואידיטיס לימפוציטית יש לסמוך על שאר הנתונים הקליניים יותר מאשר על תוצאת דיקור השאיבה. לעומתם, טוענים Kalendorf וחבריו שדיקור השאיבה מוצדק כאשר יש חשד לתירואידיטיס ומצביעים על יתרון הבדיקה לעומת בדיקת נוגדנים אנטי-תירואידיים, שאינה ספציפית.
ניתן לסכם, שדיקור שאיבה במחט עדינה היא שיטה המספקת מידע בלתי-אמצעי על סוג הפתולוגיה. גם מבקרי השיטה מסכימים, שזו בדיקה משלימה חיונית לבחירת חולים לניתוח. משטח ציטולוגי, המעיד על ממאירות יצדיק התערבות כירורגית; תוצאה ציטולוגית שלילית לממאירות - לא תשנה את החלטת הניתוח, אם קיים חשד קליני לממאירות.
ראו גם
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: בקעים
- לפרק הבא: המערכת הוורידית
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק