גן תיבה מזווג 8 - Paired box gene 8
| מדריך בדיקות מעבדה | |
| גן תיבה מזווג 8 | |
|---|---|
| Paired box gene 8 | |
| שמות אחרים | PAX8, ISPAX8IHCTO |
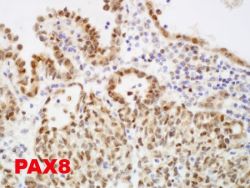
צביעה אימונו-היסטוכימית של PAX8 בתאים של סרטן השחלה.
| |
| מעבדה | פתולוגיה |
| תחום | סמן של תאים סרטניים, בעיקר של התירואיד והשחלות |
| יוצר הערך | פרופ' בן-עמי סלע |
תפקוד PAX8
PAX8 הוא חלבון באדם המקודד על ידי הגן PAX8 הממוקם בכרומוזום 2 בעמדה q14.1.2. הגן הוא חבר במשפחת גורמי השעתוק הידועה כ-paired box family. חברים במשפחת גנים זו מקודדים באופן אופייני לחלבונים המכילים מקטע paired box, המכיל octapeptide וכן homeodomain מצומד. למשפחת הגנים PAX תפקיד חשוב ביצירה של רקמות ואיברים בשלב ההתפתחות העוברית, ושמירה על התפקוד הנורמלי של תאים אחדים לאחר הלידה. הגנים ממשפחת PAX נותנים הוראות ליצירת חלבונים הנקשרים לאזורים מסומים של DNA. אחד מחלבונים גרעיניים אלה כרוך בהתפתחות התאים הפוליקולריים בתירואיד, כמו גם בביטוי של גנים ספציפיים של התירואיד. PAX8 מפריש את ההורמונים החשובים לוויסות הגדילה, התפתחות המוח, וחילוף החומרים. PAX8 מתפקד גם בשלבים מאוד מוקדמים, של האורגנו-גנזה של הכליה, של המערכת המולריאנית (müllerian system) ושל הטימוס (Laury וחב' ב- Am J Surg Pathol משנת 2011). בנוסף, PAX8 מבוטא במערכת ההפרשה הכלייתית, בתאי האפיתל של ה-endocervix, ב-endometrium, בשחלות, בחצוצרות (Fallopian tubes), בשלפוחית הזרע, באפידידימיס, בתאי האיים בלבלב ובתאים לימפואידיים (Fernández וחב' ב- Nature Rev Endocrinol משנת 2015). PAX8 וגורמי שעתוק אחרים משחקים תפקיד בקישור ל- DNA ובוויסות הגנים האחראיים לסינתזה של הורמוני התירואיד כגון Tg, TPO, Slc5a5 ו-Tshr. PAX8 ו-PAX2 הם רגולטורים חשובים של המורפוגנזה של המערכת האורו-גניטלית, ומשחקים גם תפקיד בספציפיקציה של תאי הכליה הראשונים בעובר, ונותרים גורמים חיוניים בהמשך מהלך ההתפתחות הכלייתית (Sharma וחב' ב- Semin Cell Develop Biol משנת 2015).
הגן PAX8 כרוך גם בתרחיש של היפו-תירואידיזם מולד כתוצאה מדיסגנזה של התירואיד. מוטציה בגן PAX8 עלולה למנוע או לפגוע התפתחות נורמלית של איברים מסוימים. מוטציות אלו עלולות להשפיע על פונקציות שונות של חלבונים כולל הקישור ל-DNA, יציבות חלבונים, ופעילות משותפת עם המשפעל p300.
מוטציות בגן PAX8
בהכילו מקטע מאוד משומר המכיל 128 חומצות אמינו מצומדות, PAX8 מזהה אלמנטים ספציפיים של תגובת DNA, ומשמש מווסת של הביטוי של thyroglobulin, של thyroperoxidase (להלן TPO) ושל sodium ,iodide symporte על ידי קישור לאזורי ה-promoter שלהם. יתרה מכך, PAX8 ו-thyroid transcription factor 1 (להלן TTF1) משפעלים באדם באופן סינרגיסטי את ה-promoter של .thyroglobulin בעוד שעכברים החסרים PAX8 הם בעלי בלוטות תירואיד היפופלסטיות עם חסר של תאים פוליקולריים, עכברים הטרוזיגוטיים לפגיעה בגן PAX8 אינם סובלים מפנוטיפ ברור של התירואיד. הגן PAX8 באדם, מכיל 12 אקסונים, המקודדים לחלבון שהוא בעל 450 חומצות אמינו. באדם, הטרוזיגוטיות של מוטציות loss-of-function בגן של PAX8, יכולה להיות כרוכה עם היפופלזיה אורתוטופית של התירואיד, או למצב בו אין אנומליה מבנית גלויה של בלוטת התירואיד. הסטאטוס התפקודי של אלה עם ההטרוזיגוטיות האמורה יכול להיות וריאבילי מאוד אפילו בתוך אותה משפחה עצמה, שיכול לנוע בין היפו-תירואידיזם חמור לבין תפקוד נורמלי של הבלוטה. וריאביליות בולטת זו תומכת בהשערה שגורמים רמים קשורים למודולציה של הביטוי הפנוטיפי של המוטציות בגן PAX8.
נמצאו 19 מוטציות שונות ברצף המקודד של הגן PAX8. רוב המוטציות הללו ממוקמות במקטע המצומד (paired domain) וזהו הפירוט שלהן:, ,R108X ,L62R ,C57Y ,H55Q ,S54R ,S54G ,R52P ,S48F D46SfsX24 ,G41V ,Q40P ,R31H ,R31C ,P25R ,F20S ,L16P ו-R133Q עם היוצא מהכלל של S48F, שיש לו זיקה נורמלית של קישור ל-DNA, אך עם יכולת מוגבלת לגייס את הקו-משפעל p300. כל שאר המוטנטים הם בעלי הפחתה חמורה ביכולת של PAX8 להיקשר ל-DNA. דיווח מקורי הצביע על מטופל בו נתגלתה מוטציה ב-PAX8 עם מיקום אקטופי של התירואיד שלא התבסס על scinitigraphy (בדיקה שמציגה את הפיזור של נותב רדיואקטיבי בחלק של הגוף. התרשים המתקבל נקרא סינטיגרם, והוא נוצר על-ידי רישום ניצוצות אור שנפלטים על-ידי סינטילטור כאשר הם נתקלים בקרינה בעוצמות שונות). מטופל זה לקה בהיפופלזיה אורתוטופית, כפי שנמצא מאז במטופלים רבים עם מוטציות ב-PAX8. במטופלים אחדים בקבוצה זו נפח התירואיד היה נורמלי, ובחלק מהם התירואיד הכיל ציסטות שהתגלו באולטרה-סאונד.
כאמור, הגן PAX8 מבוטא גם בכליה. תוארה גם משפחה עם מוטציה בגן PAX8 האחראית בדרך כלל לצורה חמורה של היפו-תירואידיזם מולד, כאשר מוטציה זו הייתה כרוכה במשפחה זו באי-סדירויות של המערכת האורו-גניטלית (כגון כליית פרסה, אשכים טמירים, hydrocele ו-uterocele. עם זאת, אי-סדירות כלייתית אינה שכיחה באלה עם מוטציות בגן PAX8 ודווחה בשלושה מקרים בלבד.
מנגנון הפעולה של PAX8
הגן ל-PAX מקודד ל-9 גורמי שעתוק paired-box (PAX1-9), שחשיבותם באמבריוגנזה ובתחלואה (Muratovska וחב' ב- Oncogene משנת 2003). חלבוני PAX נכרכים כרגולטורים של בניית איברים וכגורמי מפתח בשמירה על הפוטנציאל הכוללני של אוכלוסיות תאי-גזע במהלך ההתפתחות. בין הגנים הללו, יש השערה ש-PAX8 קריטי בקביעה של "גורל" התא במהלך התפתחות התירואיד, כליות, מוח, עיניים, והמערכת המולריאנית, וכן הוא מווסת את הביטוי של הגן WT1 המדכא את הגידול ע"ש Wilms (Siehl וחב' ב- Br J Haematol משנת 2003, Nonaka וחב' ב- Am J Surg Pathol משנת 2008, Poleev וחב' ב-Eur J Biochem משנת 1995, Mittag וחב' ב-Endocrinology משנת 2007, Macchia וחב' ב-Nat Genet משנת 1998, ו-Dehbi ו- Pelletier ב-EMBO J משנת 1996).
PAX8 נחשב כ "גורם שעתוק מווסת שַׁלִּיט", ובתור שכזה ייתכן שהוא מווסת את הביטוי של גנים שאינם ספציפיים לתירואיד. מספר גנים מדכאי סרטן ידועים כגון p53 ו-WT1 זוהו כיעדים שעתוקיים בתאי אסטרוציטומה באדם. מעל 90% של גידולי תירואיד נובעים מתאים פוליקולריים בבלוטה זו. חלבוני איחוי PAX8-PPAR-γ מיוחסים לקרצינומה פוליקולרית של התירואיד, וגם לקרצינומה פפילרית של התירואיד (Raman ו-Koenig ב-Nature Rev Endocrinol משנת 2014). המנגנון של טרנספורמציה זו אינו ברור לחלוטין אך קיימות מספר אפשרויות שהועלו:
- עיכוב של התפקוד הנורמלי של PPAR-γ על ידי החלבון הכימרי PAX8-PPAR-γu על ידי אפקט שלילי דומיננטי
- שפעול של יעדים נורמליים של כתוצאה מביטוי-יתר של החלבון הכימרי המכיל את כל המקטעים התפקודיים של ה-wild type PPAR-γ
- דה-רגולציה של PAX8
- שפעול של סדרת גנים שאינם קשורים לצורות ה-wildytype של מסלולי PAX8 ו-PPAR-γ (Rusch וחב' ב-Proc Natl Acad Sci USA משנת 1998, Nikiforova וחב' ב-J Clin Endocrinol Metab משנת 2003, ו-Abel וחב' ב-J Clin Invest משנת 1999).
מספר מחקרים הציעו שהגנים PAX בכליה מאפשרים לתאים סרטניים להיות עמידים לאפופטוזיס. אכן, הפחתה של ביטוי גני של PAX מעכבת את שגשוג התאים הסרטניים על ידי השרייה של אפופטוזיס. מחקרים אחדים של ריצוף הגנום השלם, הראו ש-PAX8 קשור למסלולי BRCA1 ו-MAPK (הקשור לסרטן התירואיד), כמו גם ל-Ccnb1 ול-Ccnb2 המעורבים בתהליכים של מחזור חיי התא. PAX2 מעורב אם כן בשגשוג ובהתמיינות של תאים סרטניים, בהעברת איתותים, באפופטוזיס, בקיטוב התאים וטרנספורט, ביכולת הנדידה של תאים וביכולת הספיחה שלהם.
הביטוי של PAX8 בסוגי סרטן שונים
הביטוי של PAX8 מוגבר ברקמות סרטניות של הכליה, ב-Wilms tumor, בסרטני השחלות, ובקרצינומות מולריאניות. השפעול של ביטוי PAX8 בא לביטוי בגידולי Wilms בילדים, כמעט בכל הסוגים של קרצינומת תאי הכליה, באדנומות נפרוגניות, בתאי סרטן השחלות, ובקרצינומות של שלפוחית השתן, הערמונית, האנדומטריום, ובסרטן צוואר הרחם. גידולים המבטאים PAX8/PPARγ בדרך כלל מופיעים בגיל צעיר, הם קטנים בגודלם, ולעיתים קרובות וכרוכים בחדירה לכלי הדם.
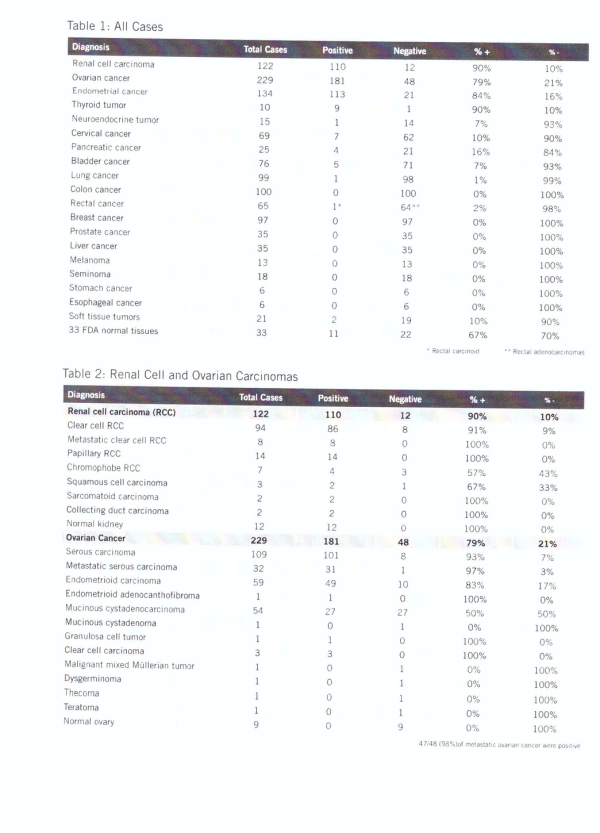
מספר מחקרים זיהו ש-PAX8 מבוטא ברמות גבוהות במיוחד בסוגי סרטן מסוימים, כולל קרצינומה של התירואיד ושל הכליה, וגידול נוירו-אנדוקריני של הלבלב (Haynes וחב' ב-Cancer Cytopathol משנת 2011, Knoepp וחב' ב-Diagn Cytopathol משנת 2012, Marques וחב' ב-J Clin Endocrinol Metab משנת 2002, ו-Nikifotov ב-Arch Pathol Lab Med משנת 2011). בנוסף, PAX8 התגלה ברמות גבוהות בקרצינומה של השחלות ובתפליטים סרוזיים (Tong וחב' ב-Diagn Cytopathol משנת 2011), מה שיכול להצביע על כך שגילוי PAX8 עשוי להיות מועיל קלינית. להלן תוצאות ביטוי אימונו-היסטוכימי של PAX8 במספר סוגי קרצינומה:
בקרצינומה של התירואיד PAX8 מופיע ב-79–90% מהמקרים (Nikiforova וחב' ב-J Clin Endocrinol Metab משנת 2003, ו-Nonaka ב-Mod Pathol משנת 2008). בנוסף, קרצינומה של התאים הפוליקולריים של הלבלב מהווה 10–20% מכלל סרטני התירואיד ועד 40% ממקרי התמותה מסרטן זה. יצוין שחלבון האיחוי -PAX8/perixosome proliferator-activated receptor (PPAR)-γ,, התגלה ב-50% ממקרי קרצינומה פוליקולרית של התירואיד (Kroll וחב' ב-Science משנת 2000, ו-Nikiforova וחב' ב-Am J Surg Pathol משנת 2002). טרנסלוקציות כרומוזומליות בהן כרוכים הגנים של PAX5 ו-PAX8 בסרטן התירואיד, מצביעות על כך שהגנים של PAX הם בעלי יכולת אונקוגנית כאשר הם מבוטאים קונסטיטוטיבית, אם כחלק מגן מאוחה או כגן שלם (Cazzaniga וחב' ב-Cancer Res משנת 2001).
יתרה מכך, PAX8 הוכר כסמן אימונו-היסטוכימי פוטנציאלי של גידולים נוירואנדוקרניים של הלבלב. דווח שבין גידולים נוירו-אנדוקריניים בדרגת התמיינות גבוהה, רק הגידולים בלבלב נמצאו חיוביים לסמן זה (ב-56% מהמקרים), בעוד שלא נמצא אף לא מקרה אחד בו גידול נוירו-אנדוקריני בדרגת התמיינות גבוהה של האילאום, התריסריון, פי הטבעת או השחלות, נמצא חיובי ל-PAX8 . הממצא שגידולים נוירו-אנדוקריניים בדרגת התמיינות גבוהה מבטאים לרוב PAX8 ,יכול לשמש אמצעי להבדלה בין גידולים ראשוניים של הלבלב, לבין גידולים באתרים אנטומיים אחרים. בין הגרורות לכבד, רק אלו ממקור של גידול נוירו-אנדוקריני פנקראטי היו חיוביים ל-PAX8 ב-65% מהמקרים.
סרטן השחלות הוא אחד מסוגי הסרטן הקטלניים ביותר בנשים, והוא חסר סמן ספציפי של ממש (Jemal וחב' ב-Cancer Epidemiol Biomarkers Prev משנת 2010). הסמן השגרתי CA-125 חסר את הרגישות והספציפיות כדי לשמש בבדיקות סקר, עם רמות בנסיוב המתקבלות בתחום הנורמלי במחצית הנשים בשלב I של המחלה (Nagele וחב' ב-Obstet Gynecol משנת 1995, ו-Eltabbakh וחב' ב-Gynecol Oncol משנת 1999). אנליזה של הגן PAX8 על ידי DNA microarray חשפה ביטוי גבוה שלו בסרטן השחלות, בהשוואה לסרטן השד (Schaner וחב' ב- Mol Biol Cell משנת 2003). גם Bowen וחב' אישר באנליזת microarray ש-PAX8 מבוטא במידה רבה בתאי אפיתל בקרצינומה של השחלות, ונעדר מתאי האפיתל של שחלות בנשים בריאות. מחקרים אלה הראו מציאות של PAX8 בשלושה תת-סוגים של סרטן שחלות אפיתליאלי (סרוזי, אנדומטריודי ותאי Clear). צביעה חיובית של PAX8 התגלתה ב-99% של קרצינומות שחלה סרוזיות בשלב מתקדם של המחלה, וב-100% של קרצינומות שחלה (low grade) ובגידולם סרוזיים גבוליים. Tacha וחב' זיהו ש-79% מכלל סוגי סרטן השחלות ביטאו את PAX8.
אבחון מבדיל של סרטני השחלות והשד
קרצינומה גרורתית של השד דומה מורפולוגית לקרצינומה ראשונית של השחלות, מה שגורם קושי בהבדלה בין שני סוגי סרטן אלה. נמצא בעבר ש-WTI הוא סמן מתאים לאבחון מבדיל בין 2 סוגי סרטן אלה, אך מאוחר יותר נמצא WTI בסרטן שד מקומי, מה שגרם לתוצאות חיוביות כזובות. לעומת זאת, PAX8 לא נמצא באף לא אחד מסרטני השד, מה שהופך אותו לסמן עדיף באבחון דיפרנציאלי זה.
גילוי של קרצינומת שחלות ממאירה
סרטני השחלות כרוכים לעיתים קרובות בגרורות, שניתן למצוא בנוזל הפריטונאלי (Edge וחב' ב- AJCC Cancer Staging Handbook משנת 2010). אך תאים מזותליאליים פעילים דומים מורפולוגית לתאי קרצינומה סרוזיים של השחלה, מה שמקשה על האבחון (Shivakumarswamy וחב' ב-J Cytol משנת 2012). בעבר זוהה calretinin כסמן אימונו-היסטוכימי אמין לתאים מזותליאליים, והייתה השערה ש-WTI יהיה תועלתי באבחון של קרצינומה סרוזית של השחלה, אך תאים מזותליאליים נמצאו גם כמפגינים אימונו-ריאקטיביות כנגד WTI (Bárcena ו-Oliva ב-Adv Anat Pathol משנת 2011). PAX8 מבוטא במידה רבה בתאי אנדותל של קרצינומת השחלות, ולעומת זאת PAX8 אינו מבוטא כלל בתאי מזותליאליים (Li וחב' ב-Mod Pathol משנת 2011). לפיכך, צביעה חיובית ל-PAX8 ושלילית ל-calretinin, היא מאוד ספציפית ורגישה לזיהוי של קרצינומה גרורתית סרוזית של השחלות בפרפרטים ציטולוגיים, וטובה להבדיל בין התאים הללו לבין תאים מזותליאליים בציטולוגיה נוזלית.
הביטוי של PAX8 בגידולים אפיתליאליים של הטימוס: אנליזה אימונו-היסטוכימית
השימוש האבחוני של ביטוי PAX8 בגידולים אפיתליאליים של בלוטת הטימוס לא נלמד באופן יסודי, ולפיכך בחנו Weissferdt וחב' (Am J Surg Pathol משנת 2011), את הביטוי של PAX8 בשיטה אימונו-היסטוכימית בסדרה של גידולים אפיתליאליים של הטימוס שכללה 31 דגימות מקרצינומה של בלוטה זו: 30 דגימות של thymoma type A, ו-30 דגימות של thymoma type B . צביעה אימונית חיובית של PAX8 נמצאה ב-77% מדגימות הקרצינומה, ב-100% מדגימות thymoma type A וב-93% מדגימות thymoma type B . צביעה עקבית אם כי חלשה יותר של PAX8 זוהתה גם כן בתאי אפיתל שְׁאֵרִיתיים (remnant) הממוקמים בשולי הגידול. ממצאים אלה מרחיבים את הספקטרום של גידולים המבטאים PAX8 בהכילם גם את הגידולים האפיתליאליים של הטימוס. הביטוי העקבי של PAX8 בגידולים אלה, הוא כלי אבחוני בעל ערך שעשוי לשמש באבחון המבדיל של גידולים מדיאסטינליים קדמיים.
החיוניות של PAX8 בזיהוי סרטן השחלות בצורך לקבוע האם להתחיל בטיפול נאו-אדג'ובנטי לפני ביצוע ניתוח
החיוניות של בחינת דגימות החשודות כמתאימות לסרטן השחלות לצורך החלטה על טיפול נאו-אדג'בנטי גדולה ביותר (Schwartz ו-Zheng ב-Gynecol Oncol משנת 2003, Vergote וחב' ב-N Eng J Med משנת 2010, McCluggage ו-Young ב-Semin Diagn Pathol משנת 2005, Laury וחב' ב-Am J Surg Pathol משנת 2011, ו-Sneige ו-Fanning ב-Acta Cytol משנת 1986). Wang וחב' דווחו בשנת 2013 ב-J Haematol Oncol על מחקרם לזיהוי סרטן השחלות בעיקר בגלל הקושי בהבדלה בין סרטן ממקור גינקולוגי או לא-גינקולוגי, בגלל חסר של סמנים ספציפיים לסרטנים גינקולוגיים. במחקר נבחן PAX8 כסמן פוטנציאלי למטרה זו. נבחנו 202 דגימות ציטולוגיות שכללו 120 דגימות של סרטן השחלות לפני-טיפול, 60 דגימות ביקורת שפירות, ו-22 דגימות סרטניות לא גינקולוגיות, התוצאות של ניסוי זה היו כדלקמן: בין 96 דגימות מיימת של מטופלות לפני כימותרפיה נאו-אדג'ובנטית, 76 דגימות המהוות 79% מהדגימות שהראו מאפיינים מורפולוגיים התואמים סרטן ראשוני של השחלות נמצאו -PAX8/+Calretinin. שאר 20 הדגימות המהוות 21% מכלל הדגימות היו חיוביות ל-adenocarcinoma. בין 50 דגימות הביקורת השפירות של שטיפות המיימת, נמצאו 5 מקרים של -Calretinin+/PAX8 מתוכם 4 מקרים של endosalpingiosis ומקרה אחד של אנדומטריוזיס. 25 מקרים של -Calretinin+/PAX8 אובחנו כתאים מזותליאלים, ושאר 20 הדגימות עם צביעה -Calretinin+/PAX8 ייצגו תאי דלקת או תאי-דם לא אפיתליאליים. מסקנת המחקר הייתה ש-PAX8 מזהה את כל תאי האפיתל הממאירים או השפירים ממקור מולריאני. בשילוב של צביעת calretinin נמצא ש-PAX8 הוא סמן רגיש לאבחון קרצינומות ממוצא שחלתי (Mhawech-Fauceglia וחב' ב-Gynecol Oncol משנת 2012).
הוראות לביצוע הבדיקה
הבדיקה מתבצעת על ידי צביעה אימונו-היסטוכימית של רקמה בעובי 3 מ"מ שעברה קיבוע על ידי תמיסת 2% paraformaldehyde למשך 18 שעות בטמפרטורת החדר. לאחר שטיפת הרקמה במים למשך 5 דקות, ודהידרציה בפרקי זמן של 5 דקות באלכוהול בריכוזים של 70%, 80% ו-95%, המלוות ב-3 השריות באלכוהול 96% למשך 5 דקות כל אחת, השרייה כפולה ב-xylene למשך 5 דקות, טבילה משולשת כל פעם למשך 5 דקות בפרפין, כאשר את הבלוק שעבר embedding בפרפין ניתן לשמור בטמפרטורת החדר לחודשים אחדים, אם כי ההמלצה היא לבצע את חיתוך הבלוק עד 6 שבועות מהטיפול בפרפין. החיתוך מתבצע במיקרוטום לפרוסות של 2–5 מיקרון ולאחריו שטיפה נוספת במים מזוקקים בטמפרטורה של 40 מעלות. העברה של החתכים לזכוכית נושא טעונה חיובית, ומתן שהות של 18 שעות לחתכים להתייבש בטמפרטורת החדר. חסימה של פעילות אנדוגנית של peroxidase מתבצעת על ידי הדגרת החתכים בתמיסת 3% H2O2 במתנול בטמפרטורת החדר למשך 10 דקות, ולאחריה שטיפה כפולה ב-PBS למשך 5 דקות כל אחת. ניתן לבצע IHC בערכת Envision ,Plus/Horseradish Peroxidase system (Dako, Calif) שהוא נוגדן רב-שבטי כנגד PAX8 (במיהול של 1:300). אִחְזוּר (retrieval) של האנטיגן PAX8 מתבצע לאחר טיפול מוקדם בסיר לחץ, בבופר ציטראט (pH-6.0) שלאחריו מודגרים חתכי הרקמה עם הנוגדן הראשוני, למשך 40 דקות בטמפרטורת החדר. לאחר שטיפות ב-tris-buffered saline, החתכים מודגרים למשך 30 דקות עם הנוגדן השני שעבר biotinylation בערכת Envision Plus, ולאחר מכן מוסף המצע diaminobenzidine בריכוז 0.05% ב-PBS המכיל 0.015% H2O2 למשך 5 דקות עד להופעת צבע בעוצמה הנדרשת לבדיקה המיקרוסקופית.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק