דימום מדליות הוושט - היבטים כירורגיים - Esophageal variceal bleeding - surgical aspects
הופניתם מהדף דימום מדליות הוושט לדף הנוכחי.
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הכבד | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – דליות
דימום מדליות הוושט נחשב לאחד ממצבי החירום הקשים ביותר ברפואה. דימום מדליות הוושט מלווה בשיעורי תחלואה ותמותה ניכרים, ורוב החולים הנותרים בחיים מדממים שוב בתוך פחות משנה. כשליש מחולי צמקת הכבד ידממו מדליות במהלך מחלתם וכ- 40% ימותו במהלך הדימום הראשון. דימום מדליות הוושט הוא הגורם העיקרי לתחלואה ולתמותה בחולים הלוקים בצמקת הכבד ובעיקר בחולי צמקת בדרגה היותר קשה Child C, המבטאת אי-ספיקת כבד סופנית ומתאפיינת בעיקר על-ידי מיימת, היפואלבומינמיה ואנצפלופתיה. לכן, מניעת דימום מדליות נחשבת לאתגר חשוב, משום שאם לא תבוצע יוחמר מהלך המחלה בחולים הלוקים בצמקת הכבד.
דליות יכולות להופיע לכל אורך מערכת העיכול, אך כמעט תמיד הדימום נובע מהדליות בוושט התחתון. הסיבה לכך היא, שרק באזור זה הדליות שוכנות מתחת לרירית, מופרדות מחלל צינור העיכול על-ידי דופן הווריד ושכבה דקה של רירית בלבד. ביתר חלקי מערכת העיכול נמצאות הדליות בעומק, מוגנות על-ידי שכבה עבה של תת-רירית ושל שריר דופן צינור העיכול. דימום מדליות הוושט מופיע רק כאשר הלחץ בוורידים הפורטלים עולה במידה ניכרת, אם כי אין התאמה מלאה בין לחץ הדם הפורטלי לגודלן של הדליות ולשכיחות הדימום מהן. מאחר שהנזק הכבדי, שהוא הגורם הישיר ליתר-לחץ-דם פורטלי, הוא בלתי הפיך, רק טיפול ישיר במערכת הפורטלית יביא להפחתת הלחץ בדליות הוושט. 10% מהחולים הלוקים בשחמת הכבד יפתחו דליות בוושט. מאלה המדממים כמעט כולם ימותו תוך שנתיים לאחר האבחנה. חולים בעלי דליות משניות לחסימה פורטלית ידממו פחות לעומת חולים בעלי דליות עקב שחמת. 70% מהמדממים ימותו תוך שנה, 60% מהמדממים פעם אחת ידממו שוב.
קיימות שתי גישות למניעת דימום חוזר מדליות. האחת - להפחית את הלחץ בוורידים הפורטלים, והשנייה - לחסל את הדליות בוושט התחתון או לפחות לגרום להתעבות הרירית סביב הדליות. לצורך כך קיימות כיום 3 שיטות טיפול:
- ניתוחית:
- התקנת דלף
- חיתוך ושט (Transection)
- אנדוסקופית - טיפול מטרש (Sclerosing) או קשירה בגומיות לחיסול הדליות, או לעיבוי דופנן
- תרופתית - הפחתת הלחץ בוורידים הפורטלים
ניתוחי דלף הם, ללא ספק, השיטה היעילה ביותר להפחתת לחץ-הדם הפורטלי. יחד עם זאת ניתוחים אלה, שהיו מקובלים מאוד בעבר, זוכים לחוסר אהדה בשנים האחרונות בגלל שיעור גבוה של אנצפלופתיה ותמותה ניתוחית ניכרת, בעיקר בניתוחים דחופים בחולי צמקת הנתונים במצב קשה. הסיבה לכך קשורה בהטיית מחזור הדם הפורטלי והחומרים ההפאטוטרופיים שבתוכו לכלי הדם המערכתיים. בחולים רבים חוזר הדימום לאחר הניתוח עקב סתימת הדלף ודרוש ניתוח חוזר. ניתוחי הדלף המקובלים לא שיפרו את תוחלת החיים, וגם דלף ברירני (Distal spleno-renal shunt), או חיתוך הוושט (Transection) לא הוכיחו את עצמם מבחינה זו. בחולים שטרם דיממו ואשר מצבם הקליני טוב, נוסו בעבר ניתוחי דלף מונעים, אך נזנחו. ניתוחים אלה הקטינו אמנם את שיעור הדימומים, אך הגבירו את התחלואה והפחיתו את תוחלת החיים של החולים.
חלק ניכר מהחולים המגיעים לבית חולים עקב דימומים מדליות הוושט נפטרים עוד באותו אשפוז. שיעור התמותה המיידית עקב דימום ראשון מגיע עד 40%, ולכן הטיפול בחולים בעלי דימומים מהדליות הוא דחוף ביותר. לא ברור מה גורם לדימומים מדליות הוושט. בעבר חשבו שחולים אלה מפתחים אזופגיטיס הגורמת לכיבים, החודרים לכלי הדם ולכן החולים מדממים. כיום ברור שהסבר זה אינו נכון, והסיבה היא מכנית. הלחץ הגבוה בווריד לעומת הלחץ הנמוך בוושט גורם להיבקעות הדופן הדקה של הווריד ולדימומים.
אבחנה דחופה
את מקור הדימום וסיבתו יש לברר מהר. על מנת לתת לחולה את הטיפול הדרוש יש לענות על מספר שאלות:
- האם לחולה יש שחמת?
- האם לחולה יש יתר-לחץ-דם פורטלי?
- מה מקור הדימום?
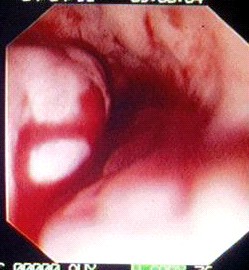
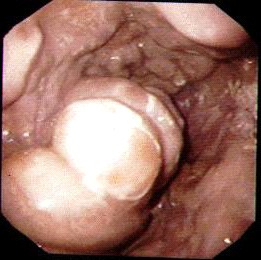
אנמנזה טובה ובדיקה פיזיקלית יכולות לספק אינפורמציה רבה על שאלות אלה. פירוט של האנמנזה והממצאים בבדיקה הפיזיקלית כפי שצוינו בתחילת פרק זה הם המרכיבים העיקריים באבחנה. לכל חולה כזה יש לבצע בדיקות דם מקיפות, כולל תפקודי כבד, תפקודי קרישה ותפקודי כליות. לאחר הערכה ראשונית וטיפול במצב החד, יש לבצע אנדוסקופיה על מנת לברר מה מקור הדימום ולראות האם לחולה יש דליות מדממות (תמונה 2.10). אם לחולה יש דליות מדממות אפשר להזריק לתוכן חומר מטרש ועל-ידי כך לעצור את הדימום. אפשר גם לבצע בליעת בריום על מנת להדגים דליות, כיבים פפטים, בקעים בסרעפת וכו'. ל- 52% מהחולים בעלי דליות יש גם כיבים פפטים. רק ב- 50% מהחולים בעלי דליות הוושט ניתן לראות דליות בבליעת בריום ולכן העדיפות המוחלטת של האזופגוסקופיה לבירור דליות.
|
|
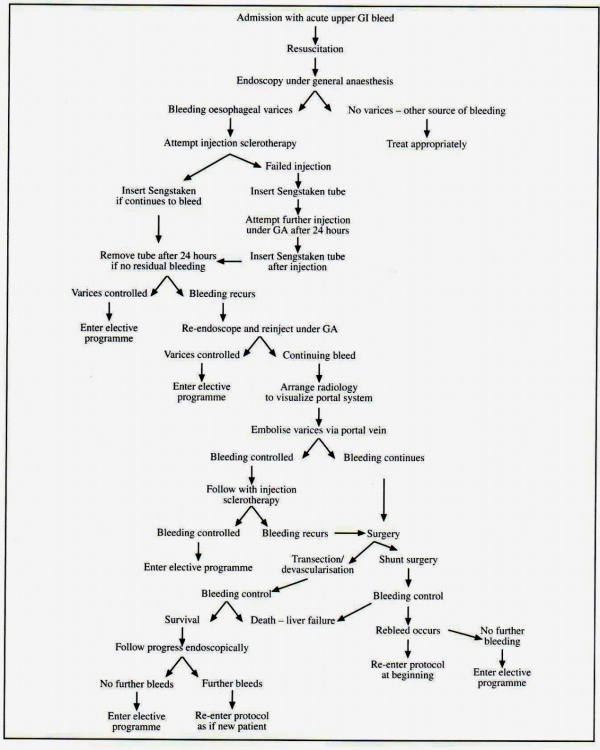
הגישה המקובלת לבירור ולטיפול דחוף בדימומים מדליות הוושט מוצגת בתרשים 1.10.
לאחר קביעת האבחנה של שחמת הכבד צריך לענות על השאלה האם לחולה יתר-לחץ-דם פורטלי ומה סיבתו? כדי לענות על שאלה זו יש לבצע צנתור של וריד השער, וזאת במטרה למדוד לחצים בוורידי הכבד ולצלם אותם על מנת להדגים את כיוון זרימת הדם. בעזרת צעדים ראשונים אלה ניתן לקבל אינפורמציה מדויקת ב- 95% מהחולים, כך שניתן להביאם לניתוח, במידת הצורך, תוך 6 שעות.
בדיקות נוספות שניתן לבצע, אולם בשלב מאוחר יותר, הן:
- ספלנוגרפיה ומנומטריה שיכולות להוסיף אינפורמציה על אופי החסימה ועל הלחצים במערכת הפורטלית.
- ארטריוגרפיה של עורק הצליאק והעורק המזנטרי העליון, הנותנת אינפורמציה המודינמית טובה. בבדיקה זו ניתן להדגים את המערכת הפורטלית בשלב הוורידי המאוחר של האנגיו. הזרקת החומר דרך עורק הקיבה השמאלי נותנת הדגמה מצוינת של המערכת הפורטלית. בדיקה זו איבדה מערכה מכיוון שבעזרת ה CT-הספירלי ניתן לבצע שחזורים של כלי הדם ולקבל תמונה הזהה לאנגיוגרפיה.
- מדידת זרימת הדם בעזרת חומרים רדיואקטיביים. שיטה זו עדיין אינה אמינה.
טיפול דחוף
מטרת הטיפול היא להפסיק את הדימום החריף ולמנוע דימומים נוספים. בחולים מדממים, המוות נובע מדקומפנסציה של הכבד, אי-ספיקת כליות וזיהומים, ולאו דווקא מאיבוד דם מסיבי. חולים אלה הם בדרך כלל במצב קשה המחייב שימוש בשיטות ניטור מתוחכמות הכוללות: Swan-Ganz catheter, CVP, Arterial line, וטכניקות למדידת נפח הדם, תפוקת הלב ועוד.
הטיפול הראשוני מבוסס על החזרת נפח הדם. יש לתת לחולה דם טרי, תרומבוציטים ופלסמה טרייה קפואה. לחולה יש ירידה ב- 2,3DPG ולכן מתן של דם ישן החסר מרכיב זה משבש עוד יותר את תהליך החמצון ברקמות ומחמיר את מצב ההלם.
יש למנוע שקיעה של החולה בתרדמת הפטית, עקב ספיגת חלבונים ואמוניה מהמעי. חיידקי המעי יוצרים אמוניה מחלבוני הדם המגיעים למעי בזמן דימום, האמוניה נספגת במחזור הדם ויכולה לגרום לתרדמת הפטית. מסיבה זו יש לטפל בחולים אלה על-ידי:
- משלשלים, כמו מגנזיום סולפט - 60 מ"ל - על מנת לסלק את הדם מהמעי.
- 1 גרם Neomycin דרך הפה כל 6 שעות על מנת להפחית את אוכלוסיית החיידקים במעי.
- חוקנים עם Neomycin, 4 גרם בכל ליטר מים.
- צריך להכניס לחולה זונדה על מנת לשטוף את הקיבה מהדם שבה.
- יש לתת לחולים אלה נוזלים עשירים בסוכרים (10% גלוקוז), המכילים גם ויטמין K, B ו- C. יש להימנע מלתת לחולים תמיסות המכילות נתרן, מכיוון שלמרות ההיפונתרמיה הם בעלי עודף נתרן בגוף.
- חולים אלה מפתחים בקלות היפוקלמיה ובססת מטבולית; שינויים אלה גורמים להפרעות בשחלוף החמצן, להפרעות בקצב הלב, ובמיוחד בולט הדבר בחולים המקבלים Digitalis, המגדיל את מעבר האמוניה למוח, ויוצר טטניות עקב ירידה בסידן היוני. מסיבה זו רצוי לתת לחולים אלה כמויות גדולות של אשלגן.
טיפול לא-ניתוחי
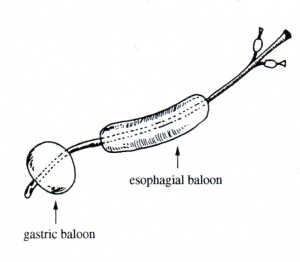
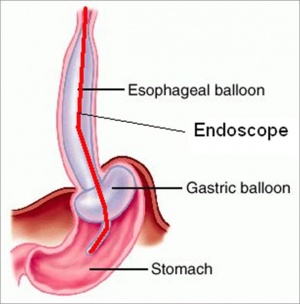
- טמפונדה על-ידי החדרת בלון לוושט. טכניקה זו נכנסה לשימוש עם פיתוח הזונדה על-שם Blackmore-Sengstaken, שבה בלון אחד מצוי בקיבה ומנופח ב- 250-300 סמ"ק אוויר. בלון זה מונע מעבר של תוכן מהקיבה אל הוושט ומקבע את הזונדה במקומה. הבלון השני מנופח בתוך הוושט בלחץ של 40 מ"מ כספית והוא יוצר לחץ על הדליות המדממות ולכן מפסיק את הדימום (איור 4.10).
|
|
יש להקפיד שהלחץ בבלון יישאר קבוע על מנת שהמערכת תתפקד. אין להשאיר את הבלון מנופח יותר מ- 24 שעות, מכיוון שהוא יגרום לנמק של הרירית והדופן. השימוש ב- Blackmore כרוך בסיבוכים רציניים:
- חנק, עקב עליית הבלון שבוושט אל האורופרינקס.
- אספירציות מלוות בדלקות ריאה.
- חלק מהחולים מדממים שוב לאחר הורדת הלחץ בבלון שבוושט.
עבודות הראו ששיטה זו אינה מקטינה את התמותה של חולים בעלי דימומים של דליות. שיטה זו טובה להפסקת דימומים קצרה כהכנה לטיפול.
- מתן וזופרסין סיסטמי - חומר זה גורם להקטנת זרימת הדם במערכת הפורטלית על-ידי התכווצות הארטריולות של המערכת הספלנכנית. השימוש בשיטה זו הביא להפסקת הדימומים במרבית החולים, אולם רובם חזרו לדמם כעבור 8 שעות. הנטייה כיום היא לתת את הוזופרסין באופן ממושך ולא בבולוסים. בשיטת הבולוסים נותנים 20 יחידות של וזופרסין בתוך 200 סמ"ק נוזל למשך 20 דקות. התוצאות בשיטה זו דומות לאלה של הטמפונדה בעזרת בלון. זו שיטה פשוטה יותר ליישום ופחות מסוכנת. בהזלפה ממושכת נותנים 0.2-0.4 יחידות/דקה במשך 8 שעות. במספר מרכזים משתמשים במינונים גבוהים ביותר המגיעים ל- 1.4 יחידות/דקה, תוך מתן תרופות המרחיבות את העורקים הכליליים (Glyceryl trinitrate, Isosorbide Dinitrate).
- הזרקת וזופרסין סלקטיבית - הזרקת וזופרסין דרך העורק המזנטרי היא בעלת השפעה מקומית חזקה יותר, הגורמת להפחתת הלחץ במערכת הפורטלית ועקב כך להפסקת הדימומים. לשיטה זו תופעות לוואי רבות הכוללות: ירידה בלחץ החמצן בדם, עלייה בלחץ הדם וירידה בלחץ החמצן במערכת הפורטלית. התוצאות הראשוניות דומות להזלפה סיסטמית ולכן העדיפות היא לשיטה פחות פולשנית. שתי שיטות אלה לא הקטינו את התמותה עקב דימומים מדליות בחולים אלה.
- הקפאה גסטרואזופגיאלית לטמפרטורה של 10-14 מעלות צלזיוס. שיטה זו לא הוכיחה את עצמה.
- טיפול אנדוסקופי מטרש של דליות מקובל כיום כאחד מטיפולי הבחירה בדימום מדליות הוושט. כטיפול הבחירה הראשוני. טיפול זה זכה להכרה בשנים האחרונות בעיקר בעקבות האכזבה מניתוחי הדלף למיניהם. הטיפול המטרש הוכיח את יעילותו, הן בעצירת דמם חד והן במניעת הישנותו על-ידי חיסול הדליות. ב- 90% מהחולים ניתן לעצור דימום חריף. קיימות שתי גישות עיקריות להזרקה של החומר המטרש: הזרקה לתוך הדליות או לתת-הריריות שמסביב לדליות. לשתי הגישות שיעורים דומים של הצלחה וסיבוכים. במטרה להביא לחיסול הדליות יש צורך לחזור על ההזרקות בהפרשים של שבוע עד 3 שבועות עד להיעלמות הדליות. פעולה זו מלווה בשיעור נמוך של סיבוכים ותמותה. מקצת הסיבוכים, כגון התנקבות הדליות או התנקבות הוושט, יכולים להיות קטלניים. בין יתר הסיבוכים מציינים בעיקר מדיאסטיניטיס, תפליט פלאורלי, התכייבות הוושט, והיצרות הוושט. סיבוכים אלה חולפים בדרך כלל בטיפול שמרני בלבד. בעבודות מבוקרות צוין, שטיפול זה משפר במעט את תוחלת החיים של החולים שטופלו בעקבות דימום. לעומתן, בעבודות אחרות לא נמצא שינוי בתוחלת החיים. בשנים האחרונות גברה ההתעניינות בטיפול אנדוסקופי מטרש מונע, בחולים בעלי דליות וושט שטרם דיממו. להבדיל מהגישה לטיפול מטרש בדליות שכבר דיממו, נטוש ויכוח לגבי ערכו של טיפול מטרש מונע בדליות. בסדרות גדולות באירופה, נמצא שטיפול מטרש מונע השיג תוצאות טובות במניעת דימומים. הטיפול בוצע רק בחולים בעלי דליות גדולות מאוד עם כיבים ברירית שעל פניהן או בחולים בעלי דליות בגודל בינוני בנוכחות הפרעה בתפקודי הקרישה. בניגוד לניסיון הזה, בסדרה רב-מרכזית גדולה בארה"ב לא נמצא יתרון להזרקות מונעות, ומחברי הסדרה בדעה, שכל עוד לא הוכחה יעילותן ונוכח האפשרות לסיבוכים בחולים, שאולי גם ממילא לא ידממו, יש להימנע מהזרקות מנע. עצירת הדימום מוצלחת פחות אצל חולים הלוקים בצמקת מדרגה Child C, שלרובם היו גם דליות גדולות בקיבה באזור הקרדיה. בחולים אלה תוחלת החיים היתה קצרה יותר לאחר הופעת דימום מדליות הוושט. הטיפול המטרש היה מוצלח במיוחד בדימום מדליות הוושט של חולים בעלי חסימה של וריד השער (ללא צמקת כבד), וזאת גם במקרים עם דימום ראשון חמור, שחייב מתן עשרות מנות דם. סיבוכים הקשורים בשיטה זו הם: כיבים ברירית ודימומים חוזרים. יש דיווחים בספרות שבחולים שבהם בוצעו הזרקות רבות התפתחו דליות בקרדיה, ואלה שדיממו וקשה מאוד היה לעצור את הדימומים הללו. בשיטה זו ניתן להפסיק את הדימום הראשוני בכ- 80% מהחולים. אפשר גם למנוע חזרת הדימום על-ידי סקלרותרפיה מניעתית בדליות המתבצעת בתקופות שהחולה לא מדמם. הרושם היום הוא, שהתוצאות של שיטה זו הן לא פחות טובות מאשר התוצאות הניתוחיות.
- קשירה אנדוסקופית על-ידי גומיות היא שיטה חלופית להזרקה אנדוסקופית של חומר מטרש לטיפול בדימום מדליות הוושט. ההוריות לביצועה זהות לאלה של הטרשה. מבחינה טכנית הקשירה היא פעולה פשוטה למדי לביצוע, נלמדת בנקל על-ידי רופא המיומן בביצוע אנדוסקופיות, ועלותה נמוכה בכ- 60% מזו של הזרקת חומר מטרש. יתרון חשוב הוא, שבקשירה זו הדיוק במקום הקשירה אינו נקודתי. לעומת זאת, הזרקה תוך-דלייתית או סביב-דלייתית של חומר מטרש, מחייבת דיוק במקום ההזרקה, כדי לגרום לפקקת של דליה מסוימת ולמנוע גרימת נזק כימי לרירית ושט תקינה. ליתרון זה משמעות מיוחדת בחולה המדמם באופן פעיל מדליות, מאחר שבחלל הוושט מצויים דם והפרשות בכמות רבה, המקשים במידה ניכרת על מיקום האמצעי הטיפולי הנבחר. בין החסרונות הטכניים של הקשירה יש למנות את שדה הראייה המוגבל על-ידי הגליל המותקן בקצה האנדוסקופ, והקושי היחסי בהכנסת צינור-העל, המחייב לעתים מתיחת-יתר של הצוואר. בהשוואת השפעות הלוואי והסיבוכים יש לציין, כי לקשירה מספר יתרונות על הטרשה אנדוסקופית. בעוד ששיעור הדימום החוזר לאחר טיפול ראשון בקשירה הוא 47%, בדומה לזה שבטיפול המטרש, הרי שעם גמר סדרת הטיפולים והיעלמות הדליות, פוחת שיעור הדימום החוזר במידה ניכרת. שתי צורות הטיפול האנדוסקופיות גורמות לכיבים, אולם בעוד שלאחר הזרקת חומר מטרש הכיבים הנוצרים הם גדולים ועמוקים, הרי שלאחר קשירה ונשירת הדליה הקשורה, נותרת במקום הקשירה התכייבות קטנה יחסית ושטחית המערבת את הרירית והתת-רירית ונרפאת במהירות בתהליך של רה-אפיתליאליזציה. הבדל זה בגודל הכיבים ובעומקם, מסביר גם את השכיחות הנמוכה יותר של היצרויות הוושט לאחר הטיפול. היצרויות לאחר קשירה שכיחות ב- 2% מהמטופלים והן קצרות וקלות לטיפול. התנקבות הוושט לאחר טיפול מטרש דווחה ב- 6.5% מהחולים. סיבוך כזה לא תואר עד כה בקשירה. כיוון שמנגנון פעולתו של החומר המטרש גורם להתהוות דלקת כימית במקום ההזרקה, הרי שיש לצפות לתגובה דלקתית שכזאת ולסיבוכיה גם בהזרקה לא-מכוונת לרירית תקינה של הוושט. מאידך גיסא, בקשירת רירית תקינה של הוושט על-ידי גומיה, לא דווח על סיבוכים כלשהם. שאיפת דם והפרשות היא סיכון המאיים על כל חולה המדמם מדליות ועובר בדיקה אנדוסקופית. השימוש בצינור-על בקשירה מקטין את הסיכון לדלקת ריאות עקב שאיפה. חיסרון הקשירה הוא אי-התאמתה לשימוש בחולים, שבהם רירית הוושט היא קשיחה כמו לאחר הטרשה חוזרת. למרות שהתוצאות לטווח ארוך של הטיפול בקשירה עדיין אינן ברורות, כנראה יש מקום להשתמש בו כיום, בין כשיטה יחידה ובין כשילוב עם הטרשה אנדוסקופית לטיפול בדימום מדליות.
- שיטה חדשה אחרת, לא כירורגית, היא ה- Transhepatic catheterization של וריד השער ודרכו מגיעים לוורידי הוושט המדממים, מזריקים דרך הצנתר חומר מטרש החוסם את הוורידים המדממים. שיטה זו היא חדשנית ומבטיחה, אולם דורשת מיומנות רבה.
- (Transjugular intrahepatic portosystemic shunt (TIPS - בפעולה זו חודרים דרך הווריד הגיגולרי לוריד הכבד וממנו לתוך הכבד. הכנסת תותב המתנפח מעצמו גורמת ישירות לעלייה בזרימת הדם מוריד השער לוורידי הכבד. בשיטה זו ניתן להוריד את הלחץ הפורטלי ב- 10 מ"מ כספית. שיטה זו מומלצת לחולים המועמדים לשתילת כבד.
טיפול כירורגי דחוף
כשליש עד מחצית מהחולים נפטרים לאחר אירוע ראשון של דימום, ורק 10-20% מהחולים יגיעו לניתוח אלקטיבי. מסיבה זו יש מנתחים הממליצים על ניתוחים דחופים לחולים אלה. לטענתם - על-ידי ניתוח ניתן להעלות משמעותית את שיעור המחלימים לאחר דימום ראשון.
קיימות 2 קבוצות של ניתוחים, שאותם מקובל לבצע:
- Non-shunt Procedure
- קשירה טרנסאזופגיאלית של הדליות - ניתוח על-שם בוארמה (Boerema-Crile). בניתוח זה ניגשים דרך בית החזה במיטת הצלע ה- 8 משמאל. חושפים את הוושט, מבצעים Longitudinal esophagotomy ותופרים תפר ממושך לאורך הדליות. ניתוח זה, שנראה לכאורה פשוט, הוא ניתוח גדול הכרוך בשיעור תמותה גבוה (15-50%). תוצאות ניתוחים אלה מראות שיעור היוותרות בחיים של 54% לשנה, לעומת 15% בטיפול התרופתי. שיעור ההיוותרות בחיים של 5 שנים הוא 21% לעומת 3% בהתאמה. יש מנתחים הסבורים שלאחר מכן חולים אלה צריכים לעבור ניתוחי דלף אלקטיביים, מכיוון ששכיחות הדימומים החוזרים בהם גבוהה.
- Oesophagial transection - בניתוח זה מבצעים חיתוך הוושט ותפירתו מחדש. על-ידי טכניקה זו מנתקים את הקשר שבין כלי הדם של הקיבה והוושט, משאירים לוושט את הניקוז הסיסטמי בלבד ולכן הלחץ בוורידי הוושט יורד והחולים מפסיקים לדמם. הגישה יכולה להיות דרך בית החזה (Milnes Walker operation), או דרך הבטן. ניתוח זה הוא ניתוח גדול לחולה הלוקה בשחמת הכבד, ולכן נעזב. בשנים האחרונות, השימוש במכשיר E.E.A הפך ניתוח זה לפרוצדורה פשוטה יחסית ולכן נכנס לשימוש במספר מרכזים. התוצאות המדווחות בשיטה זו הן טובות. יש המוסיפים לניתוח זה גם את כריתת הטחול. הוצאת הטחול מקטינה את כמות הדם הזורמת במערכת הפורטלית. שיעור התמותה המדווח לאחר ניתוחים אלה בחולים המנותחים בזמן הדימום החד הוא 30%. 80% ידממו פעם נוספת.
- Tunner הציע לבצע חיתוך הקיבה בגובה הקרדיה ותפירה מחדש של הקיבה מתחת לקרדיה, במטרה לנתק את הקשרים התוך-דופניים בין ורידי הוושט והקיבה. אחרים מוסיפים לשיטה זו גם דהסקלטיזציה של הקיבה הכוללת: קשירת העורק והווריד הקיבתי השמאלי, כריתת הטחול וקשירת הוורידים הקורונרים. שיעור התמותה המדווח בניתוח זה הוא כ- 20%, 40% מהחולים מדממים שוב, מהם נפטרים כמחצית במהלך הדימום השני.
- Yamamoto תיאר 3 מערכות של ורידים בוושט: האחת ברירית (Mucosa), השנייה בשריר הוושט והשלישית מחוץ לוושט. כל אחת מהמערכות האלה יכולה להיות מעורבת ביצירת הדליות, ולכן הוא מציע לבצע ניתוח נרחב הכולל: כריתת החלק הרחיקני של הוושט והחלק הקריבני של הקיבה (Proximal gastrectomy, distal esophagectomy) והשקה מחדש בין הקיבה לוושט. בניתוח זה מושג ניתוק מוחלט של המערכת הוורידית הקשורה למערכת הפורטלית בוושט ולכן הלחץ בוורידי הוושט יורד. ניתוח זה נקרא על-שם מתארו. יתרון הניתוח הזה הוא שהוא מנתק את כל הקבוצות המקשרות את המערכת הפורטלית בוושט למערכת הסיסטמית, ולכן מבטיח תוצאות טובות יותר בטיפול בדליות הוושט. אולם חסרונו הוא בכך שמדובר בניתוח נרחב עם תמותה ניתוחית גבוהה.
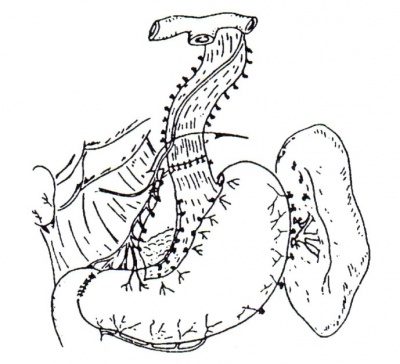
- Sugiura מציע לבצע ניתוח (הנקרא על שמו) בשני שלבים: שלב ראשון - גישה דרך בית החזה, ביצוע דהסקלטיזציה של כל הוושט התחתון וחיתוך של הוושט בגובה הסרעפת, ותפירתו מחדש. בשלב שני, כעבור 60 יום, הוא מציע לגשת דרך הבטן, לבצע דהסקלטיזציה של 2/3 הקיבה, כריתת הטחול, ואגוטומיה ופילורופלסטיקה (הואגוטומיה מתבצעת בזמן קשירת כלי הדם ולכן יש לבצע פילורופלסטיקה בנוסף) (איור 5.10). שיעור התמותה הניתוחית המדווח הוא 7%, שיעור הדימומים החוזרים הוא 2-4%, ושיעור היוותרות בחיים ל- 5 שנים הוא 80%. התוצאות האלה מיוחסות בחלקן לבחירה של חולים המתאימים לניתוח.
- Shunt Procedure
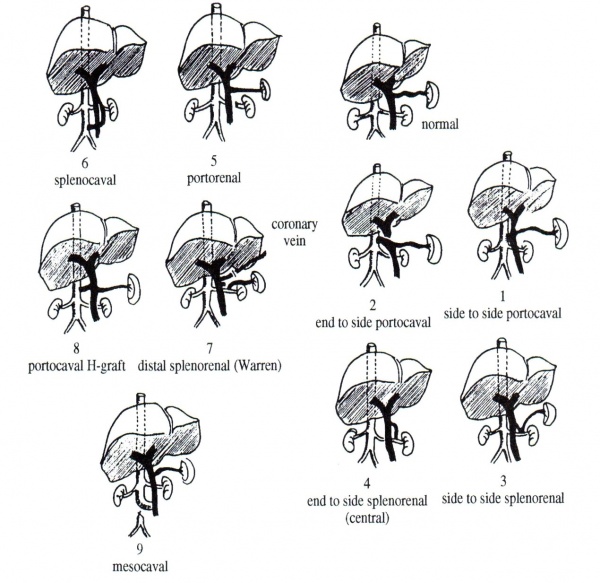
- Portocaval Shunt - בניתוח זה מבצעים השקה בין וריד השער לווריד החלול התחתון (איור 6.10), ועל-ידי כך מורידים את הלחץ בוורידי הוושט. הדם מוריד השער נכנס ישירות לווריד החלול ואינו עובר דרך הכבד. שיעור התמותה בחולים אלה הוא 25-50%. בחולים שאינם מנותחים שיעור התמותה הוא 65-75%. טיפול זה הוא דפיניטיבי. רוב החולים לאחר דלף זה לא ידממו יותר. התוצאות הניתוחיות לטווח הקצר בקבוצת החולים, שבוצע בהם דלף בין וריד השער לבין הווריד החלול (Portocaval shunt), דומות לאלה שבוצעה בהם קשירת דליות. אולם שיעור היוותרות בחיים של 30% ל- 10 שנים נרשם בקבוצה שבה בוצע Portocaval shunt לעומת שיעור של 11% בקבוצות החולים שבהן בוצעה קשירת דליות, ולעומת 0% הצלחה בקבוצת החולים שקיבלו טיפול תרופתי. הסיבוך של אנצפלופתיה לאחר ניתוח מופיע ב- 26% מהחולים ודורש טיפול מתאים. האנצפלופתיה נובעת מחדירת חומרים מהמערכת הפורטלית למערכת הסיסטמית ולמוח, ההופכים לטרנסמיטורים מדומים כתוצאה מאי סילוקם על-ידי הכבד עקב המעקף. בוצעו ניסיונות טיפול על-ידי קשירה של העורק הגסטרי השמאלי, קשירה של העורק ההפטי, העורק הספלני ודלף תת-עורי בין הווריד האומבליקלי לבין הספנה. כל השיטות האלה לא הוכחו כמוצלחות ולא נמצאות כיום בשימוש.
טיפול ניתוחי ברירני (Elective)
לאחר דימום ראשון, עקב יתר לחץ דם פורטלי, 93% מהחולים מדממים שוב, 74% מהם נפטרים וההיוותרות בחיים לטווח של 5 שנים, לאחר דימום שני, היא אפסית. ביצוע של Portocaval shunt ימנע דימומים חוזרים ב- 90% מהחולים. רק 10-20% מהחולים המדממים פעם אחת ונותרים בחיים ללא טיפול ניתוחי דחוף יכולים לעמוד בניתוח אלקטיבי. הקריטריונים לקביעת החולים המועמדים לניתוח אלקטיבי אינם חדים. חולים הלוקים במיימת, בצהבת קבועה, באנצפלופתיה ובדלדול שרירים הם מועמדים גרועים לניתוח. שיעור התמותה הניתוחית קטן לכ- 10%, כאשר מוציאים חולים אלה מנתוני העיבוד הסטטיסטי.
שאלה חשובה אחרת היא, האם יש מקום לביצוע של דלף מניעתי (פרופילקטי) בחולים בעלי יתר-לחץ-דם פורטלי שלא דיממו. מכיוון שרק 1/3 מהחולים בעלי הדליות מדממים יוצא שכ- 60% מהחולים יעברו ניתוח שאינם זקוקים לו ושאינו חסר סיבוכים, ולכן כיום נראה שאין מקום לניתוח מניעתי.
בחירת דלף שערי-מערכתי (Porto Systemic Shunt)
המערכת הפורטלית היא ללא מסתמים, כך שהשקה בכל מקום במערכת הפורטלית - בעלת הלחץ הגבוה - תביא לירידת הלחץ במערכת זו.
- השיטה שהיתה מקובלת ביותר היא Portocaval shunts עם השקת קצה לצד (איור 6.10(2)). שיטה זו גורמת לניתוק של זרימת הדם בוריד השער והטיית הזרימה לכיוון הווריד החלול. תהליך זה גורם לירידת הלחץ במערכת הספלנכנית ולכן לירידת הלחץ בדליות. הכבד בחולים אלה ניזון רק מעורק בכבד.
- שיטה אחרת לבצע Portocaval shunt היא פיום צד לצד (איור 6.10 (1)). בשיטה זו נגרמת דקומפרסיה של המערכת הספלנכנית, וכן דקומפרסיה של המערכת הפורטו-הפטית, על-ידי זרימה הפוכה של הדם מהכבד אל הדלף. מצב זה היה עלול לגרום לכך שדם רב יותר יזרום בדלף העורקי-ורידי שבתוך הכבד, דבר שיגרום לליקוי באספקת הדם ונזק לכבד. תהליך זה אינו קורה מכיוון שיש תהליך התאמה עקב זרימת דם מוגברת דרך עורק הכבד ולכן אספקת הדם לכבד לא נפגעת. אין הבדל בין שתי השיטות האלה מבחינת יעילות פעולתן. אולם, בחולים עם השקה של קצה לצד ניתן לראות יותר חולים המפתחים מיימת, ההולכת וגוברת, וגם עליית הלחץ בסינוסואידים עקב ניתוק הזרימה החוזרת של הדם מהכבד לוריד השער. לכן רבים מעדיפים את ההשקה צד לצד.
- סוג אחר של השקה היא ההשקה בין הווריד הכלייתי לווריד הטחולי, הנקראת Spleno-renal shunt. קיימות מספר שיטות לביצוע דלף זה:
- יש מנתחים המבצעים כריתת הטחול והשקה של קצה וריד הטחול לצד של וריד הכליה (איור 6.10 (4)).
- יש מנתחים המשאירים את הטחול ויוצרים השקה צד לצד בין שני הוורידים האלה. דלף זה נקרא Central reno-splenic shunt ובו אין צורך לבצע כריתת הטחול (איור 6.10 (3)).
- הגישה האומרת שככל שהזרימה דרך הדלף תקטן ויותר דם יגיע לכבד, כך יקטן הנזק לתאי הכבד, הביאה את Warren וחבריו לפתח את Distal splenorenal shunts, אשר אמור להקל על הלחץ רק בדליות הוושט, מבלי לפגוע בצורה בולטת בזרם הדם הפורטלי (איור 6.10 (7)). בניתוח מנתקים את וריד הטחול בסמוך לווריד הפורטלי, ומבצעים השקה בין וריד הטחול לבין וריד הכליה השמאלי. בנוסף מבצעים ניתוק של הוורידים הקורונרים, וריד הקיבה הימני והווריד הגסטרואפיפלואי הימני, וכן ניתוק של הליגמנטים: Hepatogastric ligaments ,Gastrocolic ligaments וה- Splenocolic ligament. בדרך זו מבצעים ניתוק של מערכת הוורידים היוצאת מהוושט למערכת הפורטלית. ניתוח זה הוצע לחולים בדרגות קלות של אי-ספיקת כבד, כאשר נוכחות מיימת מהווה הוראת נגד לניתוח. שיעור התמותה הניתוחית הוא 17%, שכיחות הדימומים החוזרים או שכיחות האנצפלופתיות נמוכה מאוד. היתרונות התיאורטיים של שיטה זו בולטים, ולכן הופכים ניתוח זה לאטרקטיבי, אולם הקשיים הטכניים בביצועו, חוסר הידע על תוצאות לטווח ארוך וכן שכיחות הסתימות של ההשקה מהווים בעיה שיש לתת עליה את הדעת. דלפים אלה הם בעלי קוטר קטן יותר ולכן הטיית הזרימה קטנה יותר. עקב כך פחות חלבונים עוברים למערכת הסיסטמית ולכן פחות מנותחים מפתחים אנצפלופתיות. המחיר לכך הוא שכיחות גבוהה יותר של דימומים חוזרים. עקב הקוטר הקטן של הדלפים חלק מהם נסתמים.
- Mesocaval shunt הינו דלף בין הווריד המזנטרי העליון לבין החלק העליון של הווריד החלול המנותק בגובה ההשקה. ניתוח זה נותן דקומפרסיה טובה אולם כרוך בבצקות בגפיים התחתונות עם נטייה לצבירת נוזלים ואלקטרוליטים (איור 6.10 (9)).
- סוג אחר של דלף הוא ה-H-graft בין הווריד הפורטלי או הווריד המזנטרי העליון לבין הווריד החלול, בעזרת גרפט של דקרון, טפלון או הווריד הגיוגולרי. שיטה זו נראתה מבטיחה משום שנתנה תוצאות טובות מבחינת הדקומפרסיה ושכיחות נמוכה יחסית של אנצפלופתיות, כמו בהשקה צד לצד של הווריד הפורטלי והווריד החלול. אולם הזרימה האיטית בגרפט גורמת להיווצרות של תרומבים אשר סותמים את הגרפט ב- 5-25% מהמקרים, זמן קצר לאחר הניתוח, ובמשך הזמן אחוז החסימות גדל והולך (איור 6.10 (8)).
- נעשו ניסיונות לשפר את זרימת הדם לכבד לאחר ניתוחי הטיה של המערכת הפורטלית, על-ידי חיבור של עורק הטחול לחלק הקרוב לכבד של וריד השער הסגור, לאחר ביצוע של השקה קצה לצד של וריד השער לווריד החלול. ניתוחים אלה לא נתנו את התוצאות המצופות ולכן נזנחו.
- כל ה- Nonshunt procedures שתוארו מקובלים גם כטיפול בחולים אלקטיביים. אחד הסיבוכים לאחר ניתוחי דלף הוא: אנצפלופתיה, שסיבתה אינה ברורה, וקשורה בכניסת אמוניה מהמערכת הפורטלית למערכת הסיסטמית. תופעה זו שכיחה בכ- 30% מהמנותחים. הטיפול בחולים אלה כולל הגבלת החלבונים בדיאטה וכן מתן אנטיביוטיקה שאינה נספגת, על מנת להקטין את אוכלוסיית החיידקים במעי. יש מנתחים הממליצים לנתק את הכרכשת מהמעי הדק, ולבצע אילאוסטומיה או אילאוסיגמואידוסטומיה. חלק מהחולים מפתחים כיב פפטי, הנובע מחוסר פירוק של הורמונים, המגרים להפרשת חומצה, כתוצאה מעקיפת הכבד. יש לציין שניתוחים אלה אינם משפרים את תפקודי הכבד של החולים. דימומים בסמוך לניתוח קשורים בדרך כלל בסתימה של הדלף. התפתחות מהירה של מיימת מופיעה לאחר ביצוע דלף ומטופלת על-ידי הגבלת נתרן בדיאטה ומתן משתנים. במקרים חמורים קיימת הוראה ל-Peritoneal venous shunt. אי-ספיקה כלייתית היא בלתי צפויה.
תוצאות
כ- 90% מה- Portosystemic shunts יישארו פתוחים. 5% ידממו שוב במשך שנתיים לאחר הניתוח, לעומת 40% בקבוצת הסקלרותרפיה. שיעור ההיוותרות בחיים 5 שנים הוא 45%. 30% יפתחו אנצפלופתיה לאחר ניתוחים אלה, ללא קשר לחומרת האנצפלופתיה לפני הניתוח. 5-20% מהחולים העוברים Splenorenal shunt יפתחו אנצפלופתיה.
- מי ייהנה מניתוחי הדלף?
רק חלק מהחולים מפתחים אנצפלופתיה בעקבות הטיה שלמה של הדם מהמערכת הפורטלית למערכת הסיסטמית. לא ניתן לחזות אלו חולים אכן יפתחו אנצפלופתיה, ואלו חולים לא יפתחו אנצפלופתיה. ידוע שחולים שמחלתם חמורה יותר יפתחו פחות אי-ספיקת כבד ואנצפלופתיה, עקב תהליכי פיצוי שהם עוברים בעקבות חומרת מחלתם. נוצר מצב פרדוקסלי, שככל שהחולה מתאים יותר לניתוח, מבחינת תפקודי הכבד שלו, כך הוא ייהנה פחות מהניתוח. נמצא שאין התאמה בין הלחצים בוורידים לתוצאות הניתוח, אולם ישנה התאמה טובה בין הלחץ בעורק ההפטי לבין תוצאות הניתוחים, או ליתר דיוק בין הגברת הזרימה בעורק ההפטי לבין הצלחת הניתוחים. את הזרימה בעורק ההפטי ניתן למדוד רק בזמן הניתוח וגם זה לא תמיד במדויק, כך שאין כיום מכשיר שיסייע לצפות מי הם המועמדים המתאימים לניתוח.
אחד הדברים החשובים בהצלחת ניתוחים אלה הוא בחירת קבוצת החולים המתאימה לניתוח ובכך להוריד את שיעור התמותה הניתוחית. בחולים שלהם ערכי SGOT יותר מ- 100 יחידות, מיימת ודלדול שרירים, ניתן למצוא שיעור תמותה ניתוחית גבוה מאוד. בשאר הפרמטרים לא נמצאה התאמה דומה. לצהבת הגבוהה מ- 3 מ"ג% יש גם משמעות פרוגנוסטית גרועה. חולים הלוקים באנצפלופתיה הם מועמדים גרועים ביותר לניתוח.
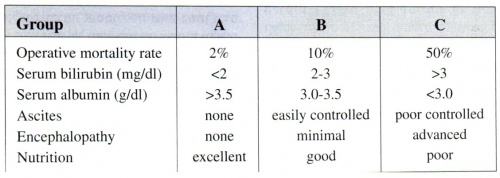
Child קבע מספר קריטריונים לחיזוי הצלחת הניתוח מבחינת ההיוותרות בחיים של החולים לאחר הניתוח. הוא חילק את החולים ל- 3 קבוצות (טבלה 3.10):
- קבוצה A: אין צהבת, אין אנצפלופתיה, חולים במצב תזונתי טוב, אין מיימת ורמת האלבומין בנסיוב גבוהה מ- 3.5.
- קבוצה B: הבילירובין בנסיוב נמוך מ-3, אין אנצפלופתיה, חולים במצב תזונתי בינוני, אין מיימת או קיימת מיימת קלה, ורמת האלבומין בנסיוב גבוהה מ- 3.
- קבוצה C: הבילירובין גבוה מ-3, קיימת אנצפלופתיה, מצב תזונתי ירוד, קיימת מיימת בולטת, ורמת האלבומין בנסיוב נמוכה מ- 3.
קיימת התאמה טובה בין התמותה הניתוחית לבין הקבוצות על-פי Child כאשר שיעור ההיוותרות בחיים הוא גבוה בקבוצה A ונמוך בקבוצה C. כיום מקובל שחולים בקבוצה C אינם מועמדים לניתוח, אלא רק לטיפולים כמו סקלרותרפיה, קשירת דליות בעזרת גומיות או אמבוליזציה של הוורידים, ו- TIPS באם הם מדממים.
טיפול בתר-ניתוחי
הטיפול לאחר הניתוח חייב להיות קפדני וביחידה לטיפול נמרץ. יש לארגן מערכת ניטור קפדנית ומעקב קבוע אחר תפקודי הכבד, הנשימה, הכליות וקרישת הדם. מתן נוזלים הוא מסובך, מכיוון שחולים אלה גדושים בנוזלים ונוטים לצבור נוזלים ונתרן. יש לשמור את החולים יבשים יחסית. עיקר הנוזלים צריכים להיות תמיסות המכילות 10% גלוקוז עם ויטמינים, כאשר הכמות המתוכננת צריכה להביא בחשבון איבוד נוזלים דרך מערכת השתן, איבוד נוזלים בלתי נראה והפרשות דרך הזונדה. כמו-כן יש להפחית 250-500 סמ"ק של מים אנדוגנים הנוצרים בתהליך הקטבולי. יש לתת נתרן רק לפי האיבוד בזונדה, ולרוב לא יותר מ- 50 מיליאקויוולנט. חולים אלה זקוקים לכמויות גדולות של אשלגן 150-200 מיליאקויוולנט ליום, ולתיקון הבססת המטבולית. חלק מהחולים זקוקים לדם טרי ולפלסמה קפואה טרייה, לאלבומין ולתרומבוציטים. יש לתת לחולים אלה הזנת-על תוך-ורידית המכילה 3000-4000 קלוריות, בעיקר ממקור סוכרים, אולם ניתן לתת להם גם שומנים. חלבונים צריך לתת בזהירות, ובעיקר תמיסות בעלות שרשראות לא ארומטיות (BCAA).
החולים נוטים להסתבך בתסמונת המצוקה הנשימתית של המבוגר ובזיהומים ריאתיים ולכן צריך להנשים אותם במשך 48-72 שעות לאחר הניתוח, ולבצע שאיבה קפדנית של דרכי הנשימה. חולים שאינם מונשמים זקוקים למסכת חמצן למשך 5-7 ימים, מכיוון שקיימים דלפים עורקיים-ורידיים ריאתיים בחולים אלה.
משתנים (Diuretics) הם בעלי ערך טיפולי בחולים המפתחים אי-ספיקת לב. לכל החולים בשחמת יש כישלון לב יחסי היפרדינמי, עקב הדלף העורקי-ורידי, המתפתח בכבד. מסיבה זו התנגודת ההיקפית שלהם ירודה ותפוקת הלב גדולה. חולים אלה זקוקים לעתים גם לDigitalis.
חולים אלכוהוליסטים נוטים לפתח Delirium tremens, לאחר דימום או לאחר דלף ניתוחי. שיעור התמותה ממחלה זו הוא 50-60%. הטיפול הוא על-ידי מתן של מגנזיום סולפט 5 גרם כל שעתיים, או Chlordiazepoxide 25-50 מ"ג לשריר, מתן גלוקוז, ויטמינים וחומרים להורדת חום. חולים אלה הם היפר-אקטיביים ויש להבדיל בינם לבין חולים הלוקים באנצפלופתיה, אשר להם אסור לתת חומרים שמדכאים את מערכת העצבים.
אי-ספיקת כבד מתפתחת בחלק מהחולים החל ביום השלישי לאחר הניתוח, אולם המצב מתייצב ומשתפר לאחר מכן ברוב החולים. בחלק קטן מהחולים ההדרדרות נמשכת עד לתרדמת הפטית. במקרים אלה התרדמת נובעת מפגיעה בתאים ולא מעודף של אמוניה. הטיפול בחולים אלה הוא תומך בלבד, כמו בחולים מדממים.
לאחר ניתוח דלף נוטים החולים לפתח הפרשת יתר של חומצה בקיבה וכיבים. לכן צריך לטפל בהם על-ידי טיפול מונע בסותרי חומצה. חולים אלה נוטים לפתח גם אי-ספיקה כלייתית על רקע של היפוולמיה מלווה באוליגוריה ובטובולר נקרוזיס, המתבטאת באזוטמיה, היפרקלמיה, וברמת אוסמולליות שווה בשתן ובדם. בשתן ניתן למצוא ריכוז גבוה של נתרן, כדוריות אדומות וגלילים. אי-ספיקה כלייתית מסוג אחר, שיכולה להתפתח, היא תסמונת הפטורנלית (Hepatorenal syndrome), המתבטאת באי-ספיקה כלייתית מתקדמת, עם אזוטמיה, ללא אוליגאוריה וללא נוכחות נתרן בשתן, עם אוסמולליות גבוהה בשתן.
הטיפול בחולים אלה הוא טיפול תומך והתמותה גבוהה מאוד. זיהומים שכיחים בחולי שחמת הכבד, בפצעי הניתוח או בחלל הצפקי. זיהומים בריאות וזיהומים בדרכי השתן שכיחים. חולים אלה זקוקים לטיפול אנטיביוטי מונע. התזונה חייבת לכלול כ- 4000 קלוריות, מעט נתרן - 200 מ"ג ו- 20 גרם חלבון. אם מינון זה של חלבון לא גורם בעיות, אפשר להגדילו עד 80 גרם. לאחר מכן יש לתת דיאטה קבועה של 50-60 גרם חלבון. יש להגביל את הנתרן ל- 2.5 גרם ליום. חולים אלה חייבים להפסיק לשתות אלכוהול. שיעור ההיוותרות בחיים של חולים שהפסיקו לשתות אלכוהול עולה מ- 52% ל- 80%. חולים אלה יישארו במעקב כל ימי חייהם.
טיפול תרופתי מונע
מאחר ששתי השיטות, הניתוחית והאנדוסקופית, אינן משפיעות על התקדמות מחלת הכבד, ובשתיהן קיימת הישנות הדימום מדליות, נמשך החיפוש אחר טיפול תרופתי שיביא להורדה קבועה בלחץ הווריד הפורטלי. מאז תחילת שנות השמונים רבו הדיווחים על יעילותו של Propranolol, חוסם קולטנים ביתא אדרנרגיים, בהורדת הלחץ בוריד השער. המינון המומלץ של התרופה הוא המינון שגורם להאטת קצב הלב ב- 25%. הוריית נגד למתן הטיפול היא חולים הלוקים באי-ספיקת לב ובאי-ספיקה נשימתית. בחלק מהעבודות המבוקרות עבודות מבוקרות דווח על הפחתה בשיעור של דמם חוזר מדרכי העיכול בחולים שטופלו בPropranolol, ועל שיפור בתוחלת החיים של חולים אלה. במחקרים מבוקרים אחרים לא נמצא שיפור בטיפול בPropranolol. נמצא שהתרופה יעילה גם כאשר המינון נמוך ולא הביא להאטה בקצב הלב. מסיבה זו הועלתה ההשערה, שייתכן שPropranolol משפיע גם דרך גורמים אחרים ולא רק על-ידי השפעה ישירה על הלחץ הפורטלי. תרופה זו עלולה לגרום לסיבוכים, לעלייה בשיעור האנצפלופתיה ולאי-ספיקת לב, אך אלו נדירים מאוד.
מיימת
התפתחות המיימת בחולי שחמת מעניינת. מתברר שעליית הלחץ במערכת הפורטלית אינה מספיקה על מנת לגרום למיימת, יש צורך בגורם נוסף; סתימה של וריד השער או של הסינוסואידים. סתימה של וריד הכבד תגרום להופעת מיימת קשה.
מתברר שלכבד מערכת לימפטית ענפה, אשר בדרך כלל מנקזת את הנוזל הפלסמתי שלא נכנס לתאים. בחולי שחמת הכבד ניתן לראות עלייה בזרימה הלימפטית מהכבד ל- Thoracic duct. הופעת המיימת מלמדת על אי-ספיקה של המערכת הלימפתית. בחולים הלוקים בשחמת הכבד ומיימת יש איבוד של נוזלים ואלקטרוליטים אל הצפק. היפוולמיה זו גורמת להפרשת יתר של אלדוסטרון, הגורמת לאגירת מים ולהיפונתרמיה מיהולית. מנגנון זה משפעל את עצמו וגורם למיימת קבועה.
טיפול
הטיפול כולל:
- דיאטה דלת מלח.
- תזונה טובה.
- משתנים משמרי אשלגן.
- תרופות אנטיאלדוסטרוניות.
טיפולים ניתוחיים
ניתוחים להקלת המיימת תוארו בספרות, אולם רק ההשקה צד לצד של הווריד הפורטלי לווריד החלול נמצאה יעילה. כיום, ניתן לבצע הכנסה של דלף מלאכותי הנקרא Leveen shunt או Denver shunt, אשר מחבר בין הצפק לבין הווריד החלול העליון. בזמן נשימה יש שאיבה של הנוזלים מהצפק אל הווריד, ובדרך זו ניתן להקל על המיימת. התוצאות המדווחות בספרות מבחינת ההקלה במיימת הן טובות. הסיבוכים המדווחים הם רבים. הסיבוכים של דלף זה הם:
- ירידה בהמטוקריט.
- DIC - 1/3 מהם קליני. DIC סובקלינית ניתן למצוא כמעט בכל המנותחים.
- דימומים ממערכת העיכול, בעיקר ב- 3 השבועות הראשונים.
- אלח-דם.
- זיהומים בפצע.
- דליפה של נוזל מהפצע.
- סתימת המסתם — 1/3 מהמסתמים נסתמים בשבוע הראשון. רק 40% מהמסתמים נשארים פתוחים לאחר כחודש וחצי.
- אמבוליות אוויר בזמן הכנסת הדלף.
- תפליט פלאורלי.
- אמבוליות של כולסטרול.
אנצפלופתיה הפטית
אטיולוגיה
אנצפלופתיה הפטית מופיעה ב- 15-30% מהחולים שלקו בדלפים, או בחולים הלוקים באי-ספיקת כבד קשה. סיבות רבות ניתנו לתופעה זו. אחת התיאוריות טוענת שסיבת האנצפלופתיה נעוצה בחדירה של חלבונים מסוימים למערכת הדם הסיסטמית, בלא שעברו טיפול בכבד. חלבונים אלה חודרים למערכת העצבים המרכזית, ושם עוברים מטבוליזם תוך יצירת טרנסמיטורים מדומים הגורמים לשפעול מערכת העצבים בתחילה, ולאחר מכן לדיכויה. רמת האמוניה בנסיוב מעידה על מידת הדלף, אבל לרוב אין מתאם בין הרמה של האמוניה בנסיוב לחומרה או להתפתחות האנצפלופתיה. נמצא שלרמת הגלוטמין בנוזל הצרברו-ספינלי מתאם טוב עם ההתפתחות של האנצפלופתיה. דימומים, הפרעות במאזן הנוזלים והאלקטרוליטים, תרופות משתנות מסוג Chlorothiazide, תרופות סדטיביות ואנלגטיות ושתיית אלכוהול, מסייעים להתפתחות האנצפלופתיה (טבלה 4.10).
תסמינים קליניים
התמונה הקלינית כוללת: שינויים בהכרה; בתחילה אופוריה, בלבול, שינויים באישיות ולאחר מכן דיכאון, ערפול הכרה ותרדמת. באנצפלוגרפיה ניתן לראות שינויים בגלי ה- EEG ההופכים לסינכרונים, בעלי אמפליטודה גבוהה ואיטיים.
טיפול
הטיפול הינו תומך בלבד וכולל משלשלים ואנטיביוטיקה. ניסיונות עם חומרים משחלפי אמוניה, לא עלו יפה. הLactulose הניתן דרך הפה, משנה את ה-PH של מערכת העיכול, ומונע ספיגה יעילה של האמוניה, אולם גורם לשלשולים. נמצא שמתן גלוקוז עם ויטמינים לחולים אלה מקל על מצבם. ניסיונות לרפא את החולים במצב חריף של אנצפלופתיה על-ידי המודיאליזה, או על-ידי חיבור מחזור הדם של החולה לכבד חיצוני של בעל חיים או תורם לא הביאו לתוצאות טובות קבועות. עדיין יש מקום לנסות גם החלפת דם לחולה בנוסף לטיפול התומך.
בשנים האחרונות הוכחה היעילות של הזנת-על המבוססת על חומצות אמיניות, שאינן ארומטיות (BCAA), בטיפול בחולים אלה. בחולים הלוקים באי-ספיקת כבד סופנית יש לבצע השתלת כבד. הקטנה בכמות החלבון לפחות מ- 50 גרם, מתן סוכרים ואשלגן ומניעת דימום או הצטברות דם במערכת העיכול הם העקרונות החשובים בטיפול השמרני בחולים אלה.
הפרשת חומצת קיבה ביתר וכיבים פפטים בחולי שחמת
השכיחות המדווחת של כיבים פפטים בחולים צירוטים היא 2.6%-25%. שכיחות זו דומה למדווח באוכלוסייה הכללית. הפרשת החומצה בחולים אלה נמצאה ירודה או נורמלית. בחולים שעברו Portocaval shunt הפרשת החומצה עולה בצורה ניכרת וזאת בשל הפרשת פפטיד על-ידי המעי הדק, אשר מגרה את הקיבה להפרשת חומצה. פפטיד זה עובר פירוק מושלם על-ידי הכבד, ולכן כמעט ואינו משפיע בדרך-כלל. בחולים שקיים בהם מעקף של המערכת הפורטלית ניתן לראות עלייה בריכוז ההורמון בנסיוב ולכן הפרשת יתר של חומצה. השכיחות של הופעת כיבים פפטים בחולים בעלי דלף גבוהה יותר מאשר בחולים צירוטים, אולם בהשוואה לאוכלוסייה הכללית ההבדל אינו בולט.
אי-ספיקה כלייתית
10-15% מהחולים הלוקים באי-ספיקת כבד מפתחים אי-ספיקה כלייתית. הרקע יכול להיות של טובולר נקרוזיס על רקע של היפוולמיה, המתפתחת עם המיימת, ומלווה באוליגוריה, באוסמולליות שווה בשתן ובנסיוב, בדם ובמשקעים בשתן. סוג שני של אי-ספיקה כלייתית, שהוא גם החמור והמסוכן יותר, הינו אי-ספיקה הנגרמת על-ידי התסמונת ההפטורנלית שביסודה גם היא נגרמת כנראה מהטיית זרימת הדם מהכליה. כליות כאלה המושתלות בחולים ללא בעיות של ספיקה כבדית מתפקדות בצורה תקינה. כלומר מדובר במצב שבו יש הטיה של זרם הדם מהכליה, התכווצות של עורקי הכליה והתפלגות פתולוגית של הדם בין המדולה לבין קורטקס הכליה - כל אלה גורמים לכך שלמרות שיש הפרשת שתן בהתחלה אין כלל נתרן בשתן. השתן מרוכז יותר מהפלסמה ורק בשלבים סופיים יש מיעוט שתן ועלייה באשלגן בדם. שיעור התמותה הוא 70% עד 100% ואין טיפול ספציפי לחולים אלה.
ראו גם
- לנושא הקודם: יתר-לחץ-דם פורטלי - היבטים כירורגיים - Portal hypertension - surgical aspects
- לנושא הבא: יתר-לחץ-דם פורטלי עקב חסימות של וריד השער מחוץ לכבד - Portal hypertension due to extra-hepatic portal vein obstruction
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הלבלב
- לפרק הבא: כירורגיה של הטחול
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק