דלקת מפרקים שגרונתית - טיפול באבטספט - Abatacept in the treatment of rheumatoid arthritis
| דלקת מפרקים שגרונתית - טיפול באבטספט | ||
|---|---|---|
| Abatacept in the treatment of rheumatoid arthritis | ||
| שמות נוספים | שחקן חדש־ישן במגרש השיגרוני, ORENCIA) Abatacept): עידכונים וחידושים | |
| יוצר הערך | פרופ' הווארד עמיטל |
|
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – דלקת מפרקים , Abatacept
דלקת מפרקים שגרונתית (Rheumatoid arthritis) היא מחלה המערבת מפרקים רבים ומסבה להם נזק מבני ותפקודי. מחלה זו פוגעת ב-0.5-1% מכלל האוכלוסייה הבוגרת, ומעבר לפגיעה המפרקית הקשה, היא מובילה להאצת התהליך של טרשת עורקים (Atherosclerosis), לפגיעה ריאתית ועינית ולקיצור תוחלת החיים[1],[2].
הדגש בטיפול המודרני בדלקת מפרקים שגרונתית עיקרו בבלימת הנזק המפרקי ודיכוי הדלקת. עם השגת מטרות אלו מובטחים הפגת הכאבים שיפור איכות החיים, ושיפור התפקוד של החולים. מטרות אלו מושגות בראש ובראשונה באמצעות שימוש ב-DMARDs (Disease Modifying Antirheumatic Drugs), בין אם במתן בודד ובין אם בשילוב של מספר תכשירים גם יחד. תכשירים אלה מביאים להטבה משמעותית במחצית מהחולים לפחות, בכך שהם מאטים את קצב ההרס שפוקד את המפרקים. לרוב נדרשים מספר שבועות עד שמורגשת הטבה קלינית משמעותית.
בשנים האחרונות, עומדות לרשות המטפלים והמטופלים חלופות טיפוליות, אלו הם התכשירים הביולוגיים, והם בעלי יכולות שהתרופות ההיסטוריות רחוקות מלתת. עם זאת, העלות הגבוהה של התכשירים הללו מציבה מחסום שעדיין מעכב חולים מלקבל תכשירים אלה בשלב מוקדם של מחלתם.
בישראל, על פי הגדרות סל הבריאות, מוגדרת חובה לנסות לפחות שלושה תכשירים מקבוצת ה-DMARDs (כשאחד מהם הוא Methotrexate) בטרם מתקדמים לטיפול בתכשירים ביולוגיים. על פי הקווים המנחים של האיגודים האירופאי והאמריקאי לראומטולוגיה, עיקרון זה אינו נדרש, אם כי רבים בכל זאת גורסים כי יש ערך ממשי בשילוב של תכשירים פומיים בטרם פונים לטיפול ביולוגי[3],[4]. מחקר שנערך ב-2013 אף הצביע על השפעה יעילה וזהה בשילוב של תכשירים פומיים בהשוואה לשימוש בתכשיר ביולוגי מקבוצת נוגדי ה-TNF-α (Tumor Necrosis Factor alpha)[5].
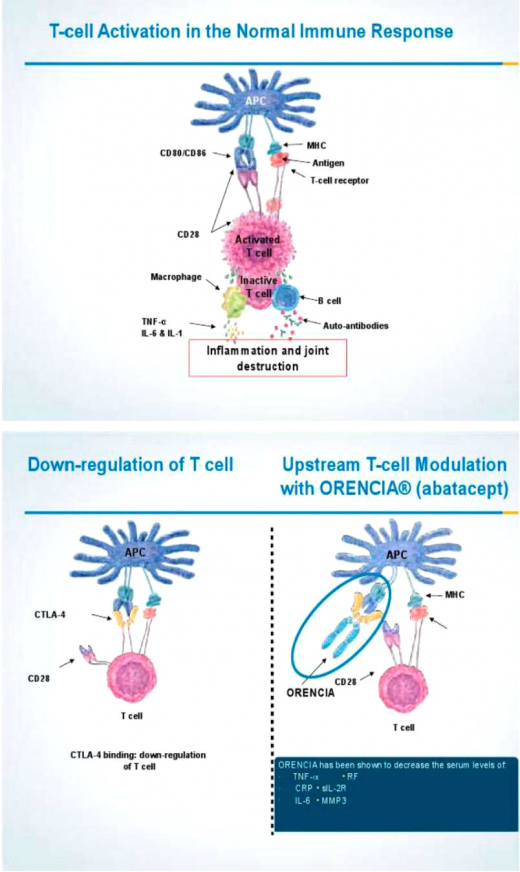
אל קבוצת התכשירים הביולוגים הצטרף בישראל חלבון אנושי המורכב ממקטע החלק הקבוע (Fc) של הנוגדן IgG1 ומהחלבון האנושי Human Cytotoxic Lymphocyte Antigen 4 (CTLA4). חלבון מלאכותי זה זכה לשם Orencia (Abatacept), והוא אינו נופל מהתכשירים הביולוגיים האחרים הקיימים בשוק התרופות הישראלי. ה-Orencia מעכב את ההתקשרות שבין CD28 הנישא על גבי תאי ה-T לבין CD80/86 המצויים על קרומי התאים מציגי האנטיגן (Antigen Presenting Cells, APCs) (תרשים 1).
תפקידם של תאי ה־T בהתפתחות דלקת מפרקים שגרונתית
הפתוגנזה של דלקת מפרקים שגרונתית מורכבת מהשפעות שונות של זרועות מערכת החיסון (Immune system), הן המולדת והן הנרכשת. כל תאי מערכת החיסון משתתפים בתגובה הדלקתית המערבת את המפרקים. מעורבותם של תאי ה-T מתבצעת באמצעות הקולטן הסגולי המאפיין את תאי ה-T יחד עם האנטיגן הנישא על פני קרומי התאים מציגי האנטיגן. במקביל להתקשרות זאת מתקיימת תגובה נוספת באמצעות המשיכה שבין הקולטנים CD80/86 לבין CD28 המצוי על תאי ה-T. תגובה בו זמנית של שתי מערכות אלו מביאה את תאי ה־T להשלים את תהליך שפעולם ולשגשג, לייצר ולהפריש ציטוקינים מעוררי דלקת (Proinflammatory cytokines). מולקולת ה-Orencia מעכבת זרוע חשובה בתהליך זה (ראו תרשים 1).
עקרונות הטיפול ב-Orencia
שימוש תוך ורידי של Orencia אושר על ידי ארגון המזון והתרופות האמריקני (FDA) בארצות הברית ב-2005, ובאירופה על ידי ה-European Medicines Agency (EMA) ב-2007. מאוחר יותר אישרו שתי רשויות אלה גם מתן תת עורי של התכשיר. כיום ה-Orencia מאושרת לשימוש במבוגרים הלוקים בדלקת מפרקים שגרונתית בינונית וקשה אשר לא הגיבה די לטיפול בתכשירים מקבוצת ה-DMARDs, הכוללת בין השאר Methotrexate, או לטיפול בתכשירים נוגדי TNF-α. באירופה יש לשלב את הטיפול ב-Orencia יחד עם Methotrexate ואילו בארצות הברית הותר שימוש ב-Orencia גם כמונותרפיה. ה-Orencia ניתנת בדרך כלל בעירוי אל תוך הווריד במשך כ-30 דקות בשבועות 0,2,4 ומדי ארבעה שבועות במינון של כ-10 מיליגרם (מ"ג) לקילוגרם (ק"ג) עד למינון מירבי של 1 גרם (טבלה מספר 1). התרופה מצליחה להוריד את ריכוזם של ציטוקינים רבים בנסיוב, כגון אינטרלויקין 2 (IL-2), אינטרלויקין 6 (IL-6) ו-TNF-α. כמו כן היא מורידה את ריכוזם של אנזימים קטליטיים כגון מטלופרוטאינזות (Metalloproteinases) וגורם שגרוני (Rheumatoid Factor, RF) וגם של חלבון מגיב עם סי (C-Reactive Protein, CRP)[6].
| משקל גוף בק"ג | מינון ה-Orencia במ״ג |
|---|---|
| <60 | 500 |
| 100-60 | 750 |
| >100 | 1,000 |
טיפול ב-Orencia תוך ורידית
מספר מחקרים אקראיים כפולי סמיות הדגימו את השפעתה הברוכה של ה-Orencia על התסמינים, על התפקוד הגופני ועל איכות החיים של החולים בדלקת מפרקים שגרונתית. כמו כן, הודגמה באופן ברור יעילותה של Orencia בעיכוב הנזק המפרקי, כפי שמשתקף בצילומי רנטגן (X-RAY) עוקבים.
השפעה קלינית בחולים אשר לא הגיבו ל-Methotrexate באופן מספק
מחקרי AIM ו-ATTEST הדגימו את ההשפעה המיטיבה של Orencia בחולים בדלקת מפרקים שגרונתית שלא השתפרו באופן מספק באמצעות טיפול ב-Methotrexate[7],[8]. מחקרי שלב IIB הדגימו יתרון של טיפול משולב ב-Orencia עם Methotrexate על פני Methotrexate בלבד. במחקרים אלה הובהר כי המינון המקובל כיום (10 מ"ג לק"ג) היה האופטימלי גם לאחר טיפול בן שישה חודשים[9]. השפעה קלינית מיטיבה יחד עם מניעת נזק מפרקי ומניעת נכות הודגמו גם בטיפול ארוך טווח של 5 ו-7 שנים[10],[11].
מחקר ה-AIM הדגים את היתרון הקליני בשילוב Methotrexate עם Orencia בהשוואה לטיפול ב-Methotrexate בלבד החל מהחודש הראשון לטיפול. יתר על כן, המשתנים של כאב והערכה עצמית של חומרת המחלה הוטבו כבר לאחר שבועיים מתחילה הטיפול[7].
מחקר המשך פתוח שארך 5 שנים אישר שקיימות השפעות קליניות ורדיוגרפיות ארוכות טווח המתבטאות גם במדדי איכות חיים ותפקוד.
מחקר ה-ATTEST היה מורכב יותר וכפול סמיות, והוא כלל קבוצה שטופלה בפלצבו בלבד, קבוצה של מטופלי Orencia וקבוצה נוספת של חולים שטופלה בתרופה הביולוגית מקבוצת נוגדי ה-TNF-α, הניתנת אף היא אל תוך הווריד - Remicade (Infliximab). מחקר זה הוכיח יעילות משמעותית אך שווה בחולים שטופלו בכל אחד מהתכשירים הביולוגיים בהשוואה למטופלי הפלצבו, אולם פרופיל הבטיחות של ה-Orencia היה טוב יותר בהשוואה לזה של Remicade. מחקר המשך שארך שנה נוספת הדגים שההשפעה המיטיבה של שתי התרופות הביולוגיות ממשיכה להתקיים ואף להתעצם[12].
השפעה קלינית בחולים אשר לא הגיבו לנוגד TNF-α באופן מספק
במחקר ATTAINS הוערכו לראשונה חולי דלקת מפרקים שגרונתית אשר לא הגיבו באופן משביע רצון לטיפול ביולוגי קודם בנוגדי TNF-α. מטבע הדברים, מדובר באוכלוסיית חולים הלוקים במחלה אגרסיבית ושוחקת יותר מאשר זו שנכללה במחקרים הקודמים[13]. גם פה הודגם שהחל מהשבוע השני לטיפול היה הבדל בין החולים שטופלו ב-Methotrexate בלבד לבין אלה שטופלו בשילוב של Methotrexate ו-Orencia. ניתן היה גם לראות ששיעור התגובה ל-Orencia לא היה תלוי במשך הטיפול הקודם בנוגדי TNF-α ובנסיבות הפסקתו, כלומר בין אם מדובר בהפסקת נוגדי ה-TNF-α בגין נסיגה בתגובה הקלינית ובין אם בגין התפתחותן של תופעות לוואי. דהיינו, כישלון של טיפול בתכשיר ביולוגי מסוג אחד לא העיב על התגובה הצפויה בטיפול ביולוגי מקבוצה אחרת, אשר פועלת במנגנון אחר, דוגמת ה-Orencia. במחקר ההמשך למחקר זה ניתן היה להיווכח שחולים רבים נהנו מהשפעת ה-Orencia גם 5 שנים מתום מחקר ATTAINS הראשוני[14].
מספר מחקרים, דוגמת מחקרי ה-ARRIVED וה-ATTEST, הוכיחו שאין כל צורך בתקופת ביניים של התנקות (Washout) מנוגדי TNF-α בטרם מוחל טיפול ב-Orencia, אלא ניתן בהחלט, עם הפסקת השימוש בתכשיר הראשון, לעבור ל-Orencia מיידית ובכך להימנע מסכנת ההתלקחות של דלקת המפרקים[8],[15].
התגובה הקלינית בחולים נאיביים לטיפול ב-DMARDs
שני מחקרים עסקו בקבוצה זו של חולים, ובהם נבחנה תגובה קלינית עוד בשלב מוקדם של התפתחות מחלתם: מחקר AGREE ומחקר ADJUST. בשניהם נמצאה יעילות קלינית במקביל לשיפור במניעת נזקים רדיוגרפיים[16],[17].
במחקר AGREE נכללו חולים במחלה מוקדמת מאוד שמשכה הממוצע עמד על 6.5 חודשים בלבד. כמו כן נכללו חולים בעלי מנבאים שהעידו על קיומה של מחלה אגרסיבית, כגון נוכחות גורם שגרוני, נוגדנים ל-CCP או עדות רנטגנית לארוזיות. שיעור החולים אשר הצליחו להשיג הפוגה קלינית באמצעות טיפול ב-Orencia בשילוב עם Methotrexate עמד על 41.4% בהשוואה ל-23.3% בחולים אשר טופלו ב-Methotrexate ופלצבו. במחקר ההמשך בחולי ה-AGREE שארך שנתיים הוכח שיעילות התכשיר נשמרת ואף משתבחת עם הזמן: 80% מהחולים שהשיגו הפוגה קלינית הצליחו לשמרה לאורך שנתיים של טיפול רציף ב-Orencia.
במחקר ADJUSTS נבחנה השפעת התכשיר בחולים הלוקים בדלקת מפרקים עוד בטרם ענו לקריטריונים הרשמיים של דלקת מפרקים שגרונתית. חולים אלה לקו, מטבע הדברים, בתסמינים תוך זמן קצר והוגדרו כלוקים במחלה מאוד מוקדמת (Very early disease). לאחר שנה מתחילת טיפול ניתן היה לראות כי רק 46% ממטופלי ה-Orencia ענו להגדרת האבחון של דלקת מפרקים שגרונתית, בעוד ש-67% מכלל מטופלי הפלצבו ענו על קריטריונים אלה. תוצאות אלו רומזות כי מתן מוקדם של Orencia במחלה עשוי לשנות את מהלכה הטבעי ואולי אף לקטוע את הרצף שמוביל להתפתחותה של דלקת מפרקים שגרונתית. יש, כמובן, צורך לסייג שזו תצפית ראשונית ושיש צורך בקבוצה גדולה של חולים ובזמן מעקב ארוך יותר בכדי לבסס טענה זו[16].
למרות האופטימיות המתקבלת מנתונים אלו, טרם אושר על ידי גורמי הרישוי בעולם השימוש ב-Orencia או בתרופות ביולוגיות אחרות בחולים שלא קיבלו טיפול קודם ב-DMARDs.
השפעה על התקדמות רדיוגרפית
מחקר ה-AIM הוא הראשון אשר הדגים כי טיפול משולב ב-Orencia וב-Methotrexate מוביל להאטה משמעותית בהתקדמות השחיקה במפרקים כפי שנמדד בצילומי רנטגן עוקבים. במחקר זה, הודגמה הפחתה של 50% בקצב השחיקה של המפרקים על פי צילומי רנטגן עוקבים בטיפול המשולב בהשוואה לטיפול ב-Methotrexate בלבד. יתר על כן, במחקר המשך פתוח וארוך טווח, ניתן היה להיווכח כי בשנה השנייה למחקר קצב ההתקדמות נסוג אף יותר, ואותו הדין באשר לשנה השלישית למחקר הפתוח. כלומר, ככל שנקף הזמן, פחת קצב ההתקדמות של הנזק הרדיוגרפי[10],[18],[19].
מחקר ה-ASSET הדגים באמצעות שימוש בטכניקת דימות תהודה מגנטית (Magnetic resonance imaging, MRI) השפעה משמעותית של Orencia על דלקת בממברנה הסינוביאלית (Synovitis) של שורשי כפות הידיים, על דלקת בעצם (Osteitis) ועל היווצרות ארוזיות. אוכלוסייה זו הייתה בעלת מדדים מנבאים פחות טובים (לאור קיומם של נוגדנים כנגד CCP, גורם שגרוני, נוכחות ארוזיות והיסטוריה של היעדר השפעה מספקת של טיפול ב-Methotrexate) ונצפתה בהם השפעה חיובית לטיפול ב-Orencia כבר לאחר 4 חודשים, וביתר שאת לאחר שנה של טיפול. השפעה ברורה הייתה ל-Orencia על המטבוליזם של העצם ועל דיכוי דלקת העצם. השפעה זו ניתן לייחס לאפקט הממתן של ה-Orencia על התמיינותם של אוסטאטקלסטים (Osteoclasts) ועל ספיגת העצם[20].
מחקר AGREE, אשר נערך בחולים הלוקים באבחנה של דלקת מפרקים מוקדמת, הדגים השפעה חיובית של Orencia על שחיקת העצם בהשוואה למטופלי Methotrexate בלבד, שינוי אשר לא הגיע להבדל מובהק סטטיסטית וזאת כנראה בשל השלב המקדמי בו נמצאו החולים. יחד עם זאת, אותם החולים שלכאורה לא ניכרה בהם עדיין השפעה מיטיבה של Orencia על ההתקדמות הרדיוגרפית, נהנו מהשפעה קלינית מיטיבה של התכשיר והציגו מדדים נמוכים של פעילות המחלה[17].
טיפול ב-Orencia בזריקות תת עוריות
המנה המקובלת לטיפול כיום עומדת על 125 מ"ג בזריקה תת עורית מדי שבוע.
הטיפול ב-Orencia במתן תת עורי נבחן במחקר ה-ACCOMPANY, בו נערכה השוואה בין הטיפול ב-Orencia עם או ללא תוספת של Methotrexate. נמצא שתוך 15 ימים מתחילת הטיפול התפתחה תגובה קלינית, ובפרק זמן של 18 חודשים כ-80% ממשתתפי המחקר השיגו תגובה קלינית יפה או מתונה על פי כללי EULAR (European League Against Rheumatism). רק כרבע מהחולים שהוגרלו לקבוצת המונותרפיה נזקקו בהמשך לתוספת Methotrexate[21].
מחקר ה-ACQUIRE, הדגים את היעדר הנחיתות (Noninferiority) של Orencia במתן תת עורי (עם מנת העמסה ראשונית אל תוך הווריד) אל מול טיפול תוך ורידי חודשי סטנדרטי. הן התוצאות הקליניות המשקפות פעילות של מחלה שגרונתית והן התוצאות המלמדות על תפקוד היו זהות בשתי זרועות הטיפול[22]. מחקר ה-ATTUNE, הדגים כי ניתן לעבור מטיפול ארוך טווח שניתן בעירוי לווריד אל טיפול תת עורי ללא קושי. חולים שטופלו ב-Orencia באמצעות עירוי לווריד לפרקי זמן של מספר שנים ועברו לטיפול תת עורי לא איבדו מיעילותו של התכשיר וכן לא נחשפו לסיכונים או לתופעות לוואי יוצאות דופן. מחקר זה הורכב מחולים שהשתתפו במחקרי המשך למחקרי AIM ו-ATTAIN שהורכבו מחולים שלא הגיבו די לטיפול ראשוני ב-Methotrexate או בנוגדי TNF-α, בהתאמה. בתום תקופה בת 12 חודשים שבמהלכה טופלו החולים בתכשיר תת עורי, מעל ל-51% השיגו דרגת פעילות נמוכה של המחלה (Low disease activity) ומעל ל-40% השיגו הפוגה קלינית מלאה על פי סקלת DAS28-CRP[23].
מחקר שזכה להרבה תשומת לב הינו מחקר ה-AMPLE, שעסק בחולים שלא הגיבו לטיפול Methotrexate באופן מספק וטרם נחשפו לטיפולים ביולוגיים מסוג נוגד TNF-α. במחקר השתתפו חולים רבים עם מחלה מוקדמת (משך הזמן הממוצע של המחלה עמד על 1.7 שנים). ייחודיות המחקר נבעה מכך שהוא נערך כמחקר ראש בראש בין שתי תרופות ביולוגיות שניתנו באופן תת עורי ומיטבי, כאשר ברקע החולים טופלו במינון קבוע של Methotrexate: הראשונה היא Orencia והשנייה היא Humira (Adalimumab), תרופה קלאסית ממשפחת נוגדי TNF-α. המחקר תוכנן לשם בחינת היעדר נחיתות בין שני התכשירים בהיבטים של יעילות ובטיחות. ואמנם, כעבור שנה, 63.4% מקבוצת מטופלי ה-Humira הגיעו לשיפור של כ-20% (American College of Rheumatology score 20) ומטופלי ה-Orencia השיגו יעד דומה של 64.8%. בתום מעקב של שנתיים, התוצאות היו 60.1% ו-59.7% בהתאמה. כלומר, מעבר לכך שהיעדים הקליניים שהוצבו במחקר היו זהים לחלוטין, כך גם הייתה הדינמיקה של קצב השפעת התכשירים[24],[25].
יעילות הטיפול ב-Orencia
מסקרנים במיוחד הם הנתונים הקשורים בפרמטר "הישרדות הטיפול", כלומר מה משך הזמן בו נותרים החולים המטופלים בתכשיר ללא שינוי בשל אובדן/היעדר יעילות או בשל תופעות לוואי. נתון זה מלמד רבות אודות היעילות האמיתית של הטיפול, שלא באמצעות מחקרים קליניים, ואודות מידת ההפרעה להמשך טיפול בשל תופעות לוואי.
במסד הנתונים מדנמרק, הידוע באיכות נתוניו, נמצא שבקרב חולים אשר טופלו בנוגדי TNF-α ללא הטבה והועברו לטיפול ב-Orencia, 19% ו-26% השיגו הפוגה קלינית שנמדדה על פי DAS28-CRP כעבור 24 ו-48 שבועות, בהתאמה[26]. תוצאות אלו לא נופלות מההישגים של המרת טיפול לנוגד TNF-α אחר או מעבר לטיפול ביולוגי המכוון כנגד 6-IL - Actemra (Tocaiizumab). מסד הנתונים של חולים שטופלו ב-Orencia (ORA), הדגים שלחולים בעלי כייל גבוה של נוגדנים כנגד CCP יש את הסיכוי הגבוה ביותר ליהנות משיפור קליני ומהיוותרות עם התרופה לאורך זמן[27]. מנתוני DANBIO, נמצא ששיעורי ההיוותרות בשימוש ב-Orencia עומדים על 54% מקץ 48 שבועות לטיפול, ואילו מנתוני ORA עולה כי שיעור ההיוותרות עומד על 73% לאחר 28 שבועות מתחילת הטיפול[26],[27].
פרופיל הבטיחות של Orencia
ככלל, נתוני הבטיחות של Orencia הם טובים מאוד, ושיעורם של אירועים מסכני חיים הוא נמוך, על פי מחקרים אקראיים וכפולי סמיות, מטא-אנליזות ומסד נתוני חולים ממדינות שונות.
במחקר ASSURE, שכלל חולים עם תחלואות צולבות כגון אי ספיקת לב (Congestive Heart Failure), מחלת ריאות חסימתית כרונית (Chronic Obstructive Pulmonary Disease, COPD) וסוכרת, לא נצפתה נסיגה במצבם הרפואי של המשתתפים להם תחלואה נוספת. סך כל תופעות הלוואי המדווחות ובפרט התופעות הרציניות לא היה שונה בהשוואה למטופלי הפלצבו[28].
מחקר כפול סמיות שבחן שילוב של נוגד ה-TNF-α Enbrel (Etanercept) עם Orencia אל מול פלצבו עם Orencia, הראה ששילובם של התכשירים הביולוגיים הביא לעלייה בשיעור הזיהומים מבלי שנתקבל ערך מוסף בשיפור הקליני[29].
המידע שהצטבר ממחקרים ארוכי טווח מצביע על היעדר סכנה בטווח הארוך במטופלי ה-Orencia. מטא-אנליזה שפורסמה ב-2010 ב-Cochrane חיזקה את הממצא ששיעור תופעות הלוואי החמורות והזיהומים החמורים היה נמוך ב-Orencia בהשוואה לתכשירים ביולוגיים אחרים ועמד על 0.65 ו-0.57, בהתאמה מול 1.11 ו-1.19 בתכשירים הביולוגיים האחרים, בהתאמה[30].
במחקר ה־ATTEST, נמצא ששיעור הפסקות הטיפול בגין תופעות לוואי היה נמוך יותר בקרב מטופלי ה-Orencia בהשוואה למטופלי Remicade. תוצאות דומות נצפו במחקר AMPLE, שהשווה בין Orencia ל-Humira, ומצא שבעוד ששיעור הזיהומים היה זהה בשני הטיפולים, פחות מטופלים הפסיקו את הטיפול בזריקות תת עוריות בקרב מטופלי ה-Orencia לאור מספר נמוך יותר של תופעות לוואי מקומיות באתר ההזרקה[8],[24].
שיעור התגובות לעירוי התוך ורידי הוא נמוך יותר בהשוואה לתכשירים ביולוגיים אחרים ועומד על 5-10%, כאשר על פי רוב, הפסקה זמנית והאטה בקצב העירוי פותרת את הבעיה. רק 0.6% מהמטופלים מפתחים בתגובה לעירוי תופעות לוואי חמורות המחייבות הפסקת טיפול[28],[30]. שיעור התגובות באתר ההזרקה של Orencia נמוך בהשוואה לתכשירים ביולוגיים אחרים ונע בין 1.2-8.2%. במחקר AMPLE הוא עמד על 4.1% בהשוואה ל־10.4% בקרב מוזרקי Humira[24].
שיעורם של זיהומים הוא נמוך ואינו עולה בטיפול ממושך. הזיהומים החמורים שהובילו לאשפוז הם, על פי שיעור הדיווח, דלקת ריאות, דלקת דרכי האוויר העליונות (Upper respiratory tract infections) וצלוליטיס. שיעור הזיהומים המזדמנים הוא נמוך ביותר ועומד על 0.35 ל-100 שנות חולה, כאשר הנפוץ מביניהם הוא הקנדידיאזיס (Candidiasis). שחפת ריאתית נמצאת בשיעור נמוך במיוחד העומד על 0.01-0.05 ל-100 שנות חולה, אולם יש להקפיד על כללי הסיקור לשחפת פעילה וסמויה בדומה למקובל בכל יתר התכשירים הביולוגיים. יש לציין כי אין כל הבדל בשיעור הזיהומים בין שיטות הטיפול ב-Orencia, בין אם בעירוי דרך הווריד ובין אם בזריקה תת עורית[9],[10],[11],[23],[24],[25],[28],[30].
מניתוח מלוא הנתונים של המחקרים הקליניים, ניתן ללמוד שלא חלה עלייה בשיעור הממאירויות בקרב מטופלי ה-Orencia בהשוואה לחולי דלקת מפרקים שגרונתית אשר טופלו ב-DMARDs או בפלצבו. העלייה היחידה שנצפתה, בדומה לשימוש בתכשירים ביולוגיים אחרים, היא עליה בממאירויות העור שאינן מלנומה. שיעור הממאירויות נע בין 0.8-1.2 ל-100 שנות חולה, נתונים המתאימים לאוכלוסיית חולי המפרקים שלא מטופלים בתכשירים ביולוגיים[9],[10],[11],[23],[24],[25],[27],[28],[30],[31].
- מחלות אוטואימוניות (Autoimmune diseases)
הופעתן של מחלות אוטואימוניות תוארה בקרב מטופלי ה-Orencia. פסוריאזיס (Psoriasis), דלקת בכלי הדם (Vasculitis), תסמונת שיוגרן (Sjogren’s syndrome) ואריתמה נודוזום (Erythema nodosum) דווחו בשכיחות נמוכה. לא חלה עלייה בהיארעות מחלות בקרב חולים אשר טופלו ב-Orencia באופן ממושך[28].
- טיפול בהיריון
באשר לחשיפה בעת היריון, המידע עדיין מצומצם, וההמלצה הקיימת כיום היא להפסיק היריון אם האישה נחשפה ל-Orencia. אמנם יש מספר מועט של אירועים של הרות בעת טיפול, ואף מתואר היריון שהסתיים בהצלחה וללא כל בעיה לאחר חשיפה במהלך השליש הראשון של ההיריון, אך ההמלצה היא שלא להרות במהלך הטיפול ב-Orencia[32].
- מתן חיסון
בדומה לטיפולים ביולוגיים אחרים, קיימת הוריית נגד מוחלטת לחיסון מטופלים ב-Orencia בחיסונים חיים. כמו כן, מומלץ שלא לחסן שבועיים טרם התחלת טיפול ועד שלושה חודשים מתום הטיפול. באשר לחיסון שאינו חי, הרי שנמצא שיש ירידה ביעילותו, ככל הנראה לאור הפגיעה במערכת החיסון התאית. תצפיות אלו דווחו במחוסנים כנגד שפעת, פנאומווקס (Pneumovax) וחיסוני טוקסואיד של טטנוס[30],[33],[34],[35].
דגלים אדומים
ביבליוגרפיה
- ↑ BieberV, Cohen AD, Freud T, Agmon-Levin N, Gertel S, Amital H. Autoimmune smoke and fire-coexisting rheumatoid arthritis and chronic obstructive pulmonary disease: a cross-sectional analysis. Immunol Res 2013;56:261-266.
- ↑ Mclnnes IB, Schett G.The pathogenesis of rheumatoid arthritis. N Engl J Med 2011;365:2205-2219.
- ↑ Colebatch AN, Edwards CJ, Ostergaard M, van der Heijde D, Balint PV, D'Agostino MA, Forslind K, Grassi W, Haavardsholm EA, Haugeberg GJurik AG, LandeweRB, Naredo E, O'Connor PJ, Ostendorf B, Potocki K, Schmidt WA, Smolen JS, Sokolovic S, Watt I, Conaghan PG. EULAR recommendations for the use of imaging of the joints in the clinical management of rheumatoid arthritis. Ann Rheum Dis 2013;72:804-814,
- ↑ Harrold LR, Harrington JT, Curtis JR, Furst DE, Bentley MJ, Shan Y, Reed G, Kremer J, Greenberg JD. Prescribing practices in a US cohort of rheumatoid arthritis patients before and after publication of the American College of Rheumatology treatment recommendations. Arthritis Rheum 2012;64:630-638.
- ↑ O'Dell JR, Mikuls TR, Taylor TH, Ahluwalia V, BrophyM, Warren SR, Lew RA, Can-nella AC, Kunkel G,PhibbsCS, Anis AH, Leatherman S, Keystone E. Therapies for ac¬tive rheumatoid arthritis after methotrexate failure. N Engl J Med 2013;369:307-318.
- ↑ Maneiro RJ, Salgado E, Carmona L, Gomez-ReinoJJ. Rheumatoid factor as predic¬tor of response to abatacept, rituximab and tocilizumabin rheumatoid arthritis: Systematic review and meta-analysis. Semin Arthritis Rheum 2013;43:9-17.
- ↑ 7.0 7.1 Kremer JM, Genant HK, Moreland LW, Russell AS, Emery P, Abud-Mendoza C, Szechinski J, Li T, Ge Z, Becker JC, Westhovens R. Effects of Abatacept in patients with methotrexate-resistant active rheumatoid arthritis: a randomized trial. Ann Intern Med 2006;144:865-876.
- ↑ 8.0 8.1 8.2 Schiff M, Keiserman M, Codding C, SongcharoenS, Berman A, Nayiager S, Saldate C, Li T, Aranda R, Becker JC, Lin C, Cornet PL, Dougados M. Efficacy and safety of Abatacept or infliximab vs placebo in ATTEST: a phase III, multi-centre, randomised, double-blind, placebo-controlled study in patients with rheumatoid arthritis and an inadequate response to methotrexate. Ann Rheum Dis 2008:67:1096-1103.
- ↑ 9.0 9.1 9.2 Kremer JM, Westhovens R, Leon M, Di GE, Alten R, Steinfeld S, Russell A, Dougados M, Emery P, Nuamah IF, Williams GR, Becker JC, Hagerty DT, Moreland LW. Treatment of rheumatoid arthritis by selective inhibition of T־cell activation with fusion protein CTLA4lg. N Engl J Med 2003;349:1907-1915.
- ↑ 10.0 10.1 10.2 10.3 Schiff M. Abatacept treatment for rheumatoid arthritis. Rheumatology (Oxford) 2011;50:437-449.
- ↑ 11.0 11.1 11.2 Westhovens R, Kremer JM, Moreland LW, Emery P, Russell AS, Li T, Aranda R, Becker JC, Qi K, Dougados M. Safety and efficacy of the selective costimulation modulator Abatacept in patients with rheumatoid arthritis receiving background methotrexates 5-year extended phase IIB study. J Rheumatol 2009;36:736-742.
- ↑ Kremer JM, Russell AS, Emery P, Abud-Mendoza C, Szechinski J, Westhovens R, Li T, Zhou X, Becker JC, Aranda R, Peterfy C, Genant HK. Long-term safety, efficacy and inhibition of radiographic progression with Abatacept treatment in patients with rheumatoid arthritis and an inadequate response to methotrexate: 3-year results from the AIM trial. Ann Rheum Dis 2011;70:1826-1830.
- ↑ Genovese MC, Schiff M, Luggen M, Le BM, Aranda R, Elegbe A, Dougados M. Longterm safety and efficacy of Abatacept through 5 years of treatment in patients with rheumatoid arthritis and an inadequate response to tumor necrosis factor inhibitortherapy.J Rheumatol 2012;39:1546-1554.
- ↑ Genovese MC, Schiff M, Luggen M, LeBM, Aranda R, Elegbe A, Dougados M. Longterm safety and efficacy of Abatacept through 5 years of treatment in patients with rheumatoid arthritis and an inadequate response to tumor necrosis factor inhibitor therapy.J Rheumatol 2012;39:1546-1554.
- ↑ Schiff M, Pritchard C, Huffstutter JE, Rodriguez-Valverde V, Durez P, Zhou X, Li T, Bahrt K, Kelly Sr Le BM, Genovese MC. The 6-month safety and efficacy of Abatacept in patients with rheumatoid arthritis who underwent a washout after anti-tumour necrosis factor therapy or were directly switched to abatacept: the ARRIVE trial. Ann Rheum Dis 2009;68:1708-1714.
- ↑ 16.0 16.1 Emery P, Durez P, Dougados M, Legerton CW, Becker JC, VratsanosG, Genant HK, Peterfy C,Mitra P, Overfield S, Qi K, Westhovens R. Impact of T-cell costimulation modulation in patients with undifferentiated inflammatory arthritis or very early rheumatoid arthritis: a clinical and imaging study of Abatacept (the ADJUST trial). Ann Rheum Dis 2010;69:510-516.
- ↑ 17.0 17.1 Westhovens R, RoblesM, Ximenes AC, NayiagerS, Wollenhaupt J, Durez P, Gomez-Reino J, Grassi W, Haraoui B, Shergy W, Park SH, Genant H, Peterfy C, Becker JC, Covucci A, Helfrick R, Bathon J. Clinical efficacy and safety of Abatacept in metho-trexate-naive patients with early rheumatoid arthritis and poor prognostic factors. Ann Rheum Dis 2009;68:1870-1877.
- ↑ Genant HK, Peterfy CG, Westhovens R, Becker JC, Aranda R, Vratsanos G, Teng J, Kremer JM. Abatacept inhibits progression of structural damage in rheumatoid arthritis: results from the long-term extension of the AIM trial. Ann Rheum Dis 2008;67:1084-1089.
- ↑ Kremer JM, Russell AS, Emery P, Abud-Mendoza C, Szechinski J, Westhovens R, Li T, Zhou X, Becker JC, Aranda R, PeterfyC, Genant HK. Long-term safety, efficacy and inhibition of radiographic progression with Abatacept treatment in patients with rheumatoid arthritis and an inadequate response to methotrexate: 3-year results from the AIM trial. Ann Rheum Dis 2011;70:1826-1830.
- ↑ Buch MH, Boyle DL, Rosengren S, Saleem B, Reece RJ, Rhodes LA, Radjenovic A, English A, Tang H, VratsanosG, O'Connor P, Firestein GS, Emery P. Mode of action of Abatacept in rheumatoid arthritis patients having failed tumour necrosis factor blockade: a histological, gene expression and dynamic magnetic resonance imaging pilot study. Ann Rheum Dis 2009;68:1220-1227.
- ↑ Nash P, Nayiager S, Genovese MC, Kivitz AJ.OelkeK, Ludivico C, Palmer W, Rodri-guezC, Delaet I, Elegbe A, CorboM. Immunogenicity, safety, and efficacy of abata-cept administered subcutaneously with or without background methotrexate in patients with rheumatoid arthritis: results from a phase III, international, multicenter, parallel-arm, open-label study. Arthritis Care Res (Hoboken ] 2013;65:718-728.
- ↑ Genovese MC, Covarrubias A, Leon G, Mysler E, Keiserman M, Valente R, Nash P, Simon-Campos JA, Porawska W, Box J, Legerton C, III, Nasonov E, Durez P, Aranda R, Pappu R, Delaet I, Teng J, Alten R. Subcutaneous Abatacept versus intravenous abatacept: a phase Nib noninferiority study in patients with an inadequate response to methotrexate. Arthritis Rheum 2011;63:2854-2864.
- ↑ 23.0 23.1 23.2 Keystone EC, Kremer JM, Russell A, Box J, Abud-Mendoza C, ElizondoMG, Luo A, Aranda R, Delaet I, Swanink R, Gujrathi S, Luggen M. Abatacept in subjects who switch from intravenous to subcutaneous therapy: results from the phase lllb AT¬TUNE study. Ann Rheum Dis 2012;71:857-861.
- ↑ 24.0 24.1 24.2 24.3 24.4 Schiff M, Weinblatt ME, Valente R, van der Heijde D, Citera G, Elegbe A, Mai-donado M, Fleischmann R. Head-to-head comparison of subcutaneous Abatacept versus Adalimumab for rheumatoid arthritis: two-year efficacy and safety findings from AMPLE trial. Ann Rheum Dis 2013
- ↑ 25.0 25.1 25.2 Weinblatt ME, Schiff M, Valente R, van der Heijde D, Citera G, Zhao C, Maldonado M, Fleischmann R. Head-to-head comparison of subcutaneous Abatacept versus Adalimumab for rheumatoid arthritis: findings of a phase lllb, multinational, pro¬spective, randomized study. Arthritis Rheum 2013;65:28-38,
- ↑ 26.0 26.1 Letters HC, Ostergaard M, Glintborg B, Krogh NS, Foged H, Tarp U, Lorenzen T, Hansen A, Hansen MS, Jacobsen MS, Dreyer L, Hetland ML. Efficacy of Abatacept and tocilizumabin patients with rheumatoid arthritis treated in clinical practice: results from the nationwide Danish DANBIO registry. Ann Rheum Dis 2011;70:1216-1222.
- ↑ 27.0 27.1 27.2 G0ttenberg JE, Ravaud P, Cantagrel A, Combe B, FlipoRM, SchaeverbekeT, Houvenagel E, Gaudin P, Loeuille D, Rist S, Dougados M, Sibilia J, Le L, X, Marcelli C, Bardin T, Pane I, Baron G, MarietteX. Positivity for anti-cyclic citrullinated peptide is associated with a better response to abatacept: data from the'Orencia and Rheuma¬toid Arthritis1 registry. Ann Rheum Dis 2012;71:1815-1819.
- ↑ 28.0 28.1 28.2 28.3 28.4 Weinblatt M, Combe B, Covucci A, Aranda R, Becker JC, Keystone E. Safety of the selective costimulation modulator Abatacept in rheumatoid arthritis patients receiv¬ing background biologic and nonbiologic disease-modifying antirheumatic drugs: A one-year randomized, placebo-controlled study. Arthritis Rheum 2006;54:2807-2816.
- ↑ Weinblatt M, Schiff M, Goldman A, Kremer J, Luggen M, Li T, Chen D, Becker JC. Selective costimulation modulation using Abatacept in patients with active rheuma¬toid arthritis while receiving etanercept: a randomised clinical trial. Ann Rheum Dis 2007;66:228-234.
- ↑ 30.0 30.1 30.2 30.3 30.4 Maxwell LJ, Singh JA. Abatacept for rheumatoid arthritis: a Cochrane systematic review. Rheumatol 2010;37:234-245.
- ↑ Simon TA, Smitten AL, Franklin J, Askling J, LacailleD, Wolfe F, Hochberg MC, Qi K, Suissa S. Malignancies in the rheumatoid arthritis Abatacept clinical development programme: an epidemiological assessment. Ann Rheum Dis 2009;68:1819-1826.
- ↑ Ruperto N, Lovell DJ, Quartier P, Paz E, Rubio-Perez N, Silva CA, Abud-Mendoza C, Burgos-Vargas R, Gerloni V, Melo-Gomes JA, Saad-Magalhaes C, Chavez-Corrales J, Huemer C, Kivitz A, Blanco FJ, Foeldvari I, Hofer M, Horneff G, Huppertz HI, Job-Deslandre C, Loy A, Minden K, PunaroM, Nunez AF, Sigal LH, Block AJ, Nys M, Martini A, Giannini EH. Long-term safety and efficacy of Abatacept in children with juvenile idiopathic arthritis. Arthritis Rheum 2010;62:1792-1802.
- ↑ Borba EF, Saad CG, Pasoto SG, Calich AL, Aikawa NE, Ribeiro AC, Moraes JC, Leon EP, Costa LP, Guedes LK, Silva CA, Goncalves CR, Fuller R, Oliveira SA, Ishida MA, Precioso AR, Bonfa E. Influenza A/H1N1 vaccination of patients with SLE:can antimalarial drugs restore diminished response under immunosuppressive therapy? Rheumatology (Oxford) 2012;51:1061-1069.
- ↑ Ribeiro AC, Laurindo IM, Guedes LK, Saad CG, Moraes JC, Silva CA, Bonfa E. Abatacept and reduced immune response to pandemic 2009 influenza A/H1N1 vaccination in patients with rheumatoid arthritis. Arthritis Care Res (Hoboken) 2013;65:476-480.
- ↑ Tay L, Leon F, VratsanosG, Raymond R, Corbo M. Vaccination response to tetanus toxoid and 23-valent pneumococcal vaccines following administration of a single dose of abatacept: a randomized, open-label, parallel group study in healthy subjects. Arthritis ResTher 2007;9:R38.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי פרופ' הווארד עמיטל, מומחה לרפואה פנימית וריאומטולוניה, מנהל מחלקה פנימית ב', המרכז הרפואי ע"ש שיבא, תל-השומר.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק