דנ"א חופשי במחזור הדם - Circulating free DNA
| מדריך בדיקות מעבדה | |
| דנ"א חופשי במחזור הדם | |
|---|---|
| Circulating free DNA | |
| שמות אחרים | cfDNA, cell-free DNA |
| מעבדה | כימיה בדם |
| תחום | זיהוי של סרטן ומפגעים אחרים |
| טווח ערכים תקין | 1.0-1.8 ננוגרם/מיקרוליטר. |
| יוצר הערך | פרופ' בן-עמי סלע |
ראו גם – בדיקת דם ל-Circulating tumor DNA
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – איתור ומניעת מחלות ממאירות
מטרת הבדיקה
חלופה לביופסיות חודרניות של רקמה לקביעת סטטוס המוטציה של KRAS 12, 13, 61,146 (G12A, G12C, G12D, G12R, G12S, G12V, Q61K, Q61L, Q61R, Q61H, A146T ו־V13D.
כללי
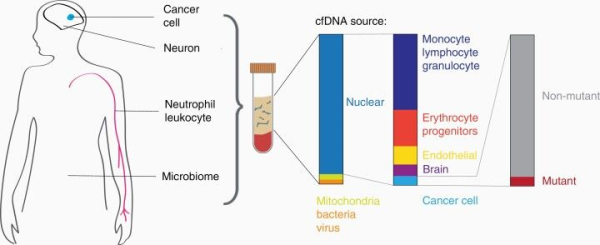
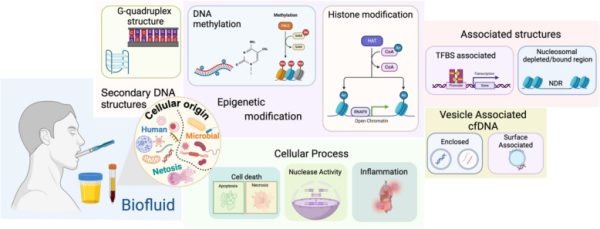
פרגמנטים מבוקעים של DNA (הידועים גם כ-cell-free DNA) משתחררים לנוזלי הגוף כגון פלזמת הדם, שתן, נוזל צרברוספינלי. גדלים אופייניים של cfDNA משקפים חלקיקים כרומטוזומיים (בגודל של בערך 165bp), כמו גם נוקלאוזומים המגינים על DNA מעיכול על ידי נוקלאזות אפופטוזיות (Shtumpf וחב' ב-Chromosoma משנת 2022). המושג cfDNA יכול לשמש לתיאור צורות שונות של DNA המסתובבות בנוזלי הגוף, כולל circulating tumor DNA (להלן ctDNA), כמו גם cell-free mitochondrial DNA (להלן ccf mtDNA), כמו גם cell-free fetal DNA (להלן cffDNA) ו-donor-derived cell-free DNA (להלן dd-cfDNA (Dholakia וחב' ב-Transplantation משנת 2020). רמות מוגברות של cfDNA נראות בסרטן, בעיקר במחלה מתקדמת (Shaw ו-Stebbing ב־Ann Translational Med משנת 2014). יש ראיות לכך ש-cfDNA נעשה שכיח באופן הולך וגדל בצירקולציה בהַתְחָלָת הגיל (Gravina וחב' ב-Aging Cell משנת 2016). נמצא ש-cfDNA הוא סמן שימושי במגוון של תחלואות מלבד סרטן ורפואת העובר. סמן זה כולל אם כי לא מוגבל לטראומה, ספסיס, דלקת אספטית, אוטם שריר הלב, שבץ, שתילת איברים, סוכרת ומחלת sickle cell (Butt ו-Swaminathan ב-Ann NY Acad Sci משנת 2008). ה-cfDNA הוא בעיקר מולקולה חוץ-תאית של DNA בעלת גדיל כפול, המורכבת מפרגמנטים קטנים בגודל של 50-200bp, וכן היא מכילה פרגמנטים גדולים (21kb), ונמצאה סמן מדויק של סרטני הערמונית והשד (Gall וחב' ב-Am J Pathol משנת 2019, ו-Casadio וחב' ב-Biomed Res Int משנת 2013). מחקרים עדכניים הניחו את היסודות להפרעה לביטוי גני על ידי cfDNA (Esfahani וחב' ב-Nature Biotechnol משנת 2022). מחקרים אחרים אישרו את המקור של cfDNA בקרצינומות בשלב מתקדם של המחלה. CfDNA מצוי בפלזמה ובנוזלי גוף אחרים (Teo וחב' ב-Aging Cell משנת 2019). השחרור של cfDNA לזרם הדם מתקיים מסיבות שונות, כולל אפופטוזיס, נמק ו-NETosis (שמשמעותו neutrophil extracellular traps המוגדרת כתהליך בו נויטרופילים פעילים משחררים את תכולת הכרומטין שלהם ליצירה של מלכודות חוץ-תאיות, המסייעות להשמדה של אורגניזמים פתוגניים. מנגנון זה קריטי להילחם בזיהומים אך הוא קשור גם למפגעים שונים כגון אסתמה, טרשת עורקים וגרורות סרטניות. ההצטברות המהירה של cfDNA בדם במהלך התפתחות הנגע הסרטני, נגרמת על ידי עודף DNA המשתחרר על ידי תאים אפופטוטיים ותאי נמק. CfDNA נע בצירקולציה בצורת נוקלאוזומים, שהם קומפלקסים של DNA והיסטונים (Roth וחב' ב-BMC Cancer משנת 2011). מולקולות cfDNA מוגברות לעיתים קרובות באופן לא-ספציפי בסרטן, אך יכולים להיות יותר ספציפיים בניטור של תרפיה ציטוטוקסית של סרטן, בעיקר להערכת היעילות של התרפיה (Stoetzer וחב' ב-Cancer Lett משנת 2013).
היסטוריה
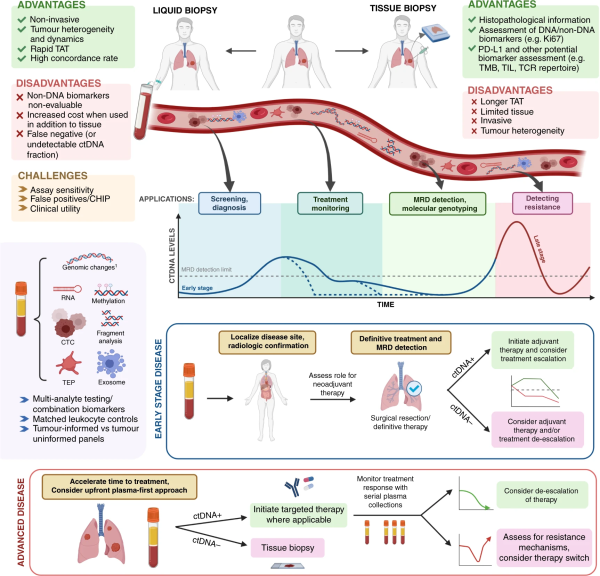
חומצות גרעין בצירקולציה התגלו לראשונה על ידי Mandel ו-Metais בשנת 1948 במאמר שהתפרסם ב-Comptes Rendus des Séances de la Société de Biologie et de ses Filiales[1]. לאחר מכן התגלה שרמת cfDNA עלתה משמעותית בפלזמה של אנשים חולים. תגלית זו נעשתה לראשונה בחולי זאבת (Tan וחב' ב-J Clin Invest משנת 1966) ומאוחר יותר נמצא שרמות cfDNA מוגברות בלמעלה מ-50% מחולי סרטן (Leon וחב' ב-Cancer Res משנת 1977). ניתוח מולקולרי של cfDNA הסתיים בתגלית החשובה ש-DNA בפלזמה של חולי סרטן הכיל מוטציות הקשורות לגידול וניתן להשתמש בו לאבחון ומעקב אחר סרטן (Vasioukhin וחב' ב־Br J Haematol משנת 1994). היכולת למצות circulating tumor DNA (ctDNA) מפלזמה אנושית הביאה להתקדמות עצומה בגילוי של סרטן לא-גרורתי (Sorenson חב' ב-Cancer Epidemiol Biomarkers Preven משנת 1994). ממצא זה הוביל למה שידוע היום כביופסיה נוזלית. בקצרה, ביופסיה נוזלית עושה שימוש בסמנים ובתאי סרטן בדם כאמצעי לאבחן את סוג הסרטן ואת שלב המחלה (Arneth ב-BMC Cancer משנת 2018). סוג ביופסיה זו אינו פולשני, ומאפשר אבחון שגרתי שמגלה חזרת המחלה לאחר טיפול (Babayan ו-Pantel ב-Genome Med משנת 2018).
מקורות שונים של cfDNA
המקור התוך-תאי של cfDNA (או מגרעין תא או מהמיטוכונדריה) יכול להשפיע על הפוטנציאל הדלקתי של cfDNA. ה-mtDNA הוא גריין של דלקת (Lood וחב' ב-Nature Med משנת 2016), ובגלל מוצא הפרוקריוטי שלו, הוא בעל תכונות דומות לאלה של DNA בקטריאלי, כולל הנוכחות הגבוהה יחסית של מוטיפים מסוג CpG שלא עברו מתילציה, שמוצאים רק באופן נדיר ב-DNA גרעיני (Yang וחב' ב-Proc Natl Acad Sci U S A משנת 1985). המוטיפים האחרונים הם בעלי חשיבות כיוון ש-TLR9 הוא הקולטן-חיישן של DNA היחיד האנדו-ליזוזומלי, הוא בעל ספציפיות ייחודית ל-CpG DNA שלא עבר מתילציה. mtDNA נמצא משפעל נויטרופילים דרך המעורבות של TLR9 (לDuvvuri ו-Lood ב-Frontiers Immunol משנת 2019). אלא אם כן mtDNA קשור לחלבונים נשאים, mtDNA אך לא DNA גרעיני יכול להזדהות עם מתווה מולקולרי כרוך בסכנה המשרה דלקת דרך TLR9 (Collins וחב' ב-J Leukocyte Biol משנת 2004). Collins קובע שהזרקה תוך-ארטיקולרית של mtDNA, משרה ארטריטיס in vivo, מה שמרמז לתפקיד של סילוק mtDNA בפתוגניות של מחלה דוגמת rheumatoid arthritis ומחלות ראומטיות אחרות. MtDNA, בניגוד ל-DNA גרעיני, מאופיין על ידי רמות בסיסיות מוגברות של 8OHdG, סמן של נזק חמצוני. התכולה הגבוהה של נזק חמצוני ב-mtDNA, מיוחסת לקרבה הגדולה של mtDNA ל-reactive oxygen species (ROS), וחוסר יעילות יחסי של מנגנוני תיקון של DNA, שעלולים לגרום להצטברות של נגעי DNA (Clatyton וחב' ב-Basic Life Sciences משנת 1975).
אנליזה של cfDNA
באופן כללי, הזיהוי של רצפים ספציפיים של DNA ב-cfDNA, יכול להתבצע בשתי דרכים: זיהוי דרך ריצוף ספציפי על ידי PCR, ועל ידי אנליזה גנומית כללית של כל ה-cfDNA הנמצא בדם. הנוכחות של cfDNA המכיל DNA של תאי סרטן, אופיינה לראשונה תוך שימוש באמפליפיקציה של PCR של גנים עם מוטציות מה-cfDNA הממוצה. האנליזה של cfDNA המבוססת על PCR מסתמכת על הטבע האנליטי של qPCR ושל PCR דיגיטלי. שתי טכניקות אלו יכולות להיות רגישות ובעלות עלות-יעילות טובה לצורך זיהוי של מספר מוגבל של מוטציות. ריצוף עמוק של cfDNA נדרש כדי לגלות מוטנט של circulating tumor DNA (ctDNA) שנמצא בכמויות קטנות בפלזמה. שתי טכניקות עיקריות של ריצוף, נמצאות בשימוש לצורך אנליזה של cfDNA מוטנטי: ריצוף PCR amplicon (Forshew וחב' ב-Sci Translational Med משנת 2012), וריצוף hybrid capture (Newman וחב' ב-Nature Med משנת 2014).
cfDNA ותחלואה
סרטן: רוב המחקר על cfDNA מתמקד ב-DNA שמקורו בסרטן (ctDNA). בקצרה, ה-DNA מתאי סרטן משתחרר במות תאים סרטניים (van der Pol ו-Mouliere ב-Cancer Cell משנת 2019). פרקציית cfDNA המשתחררת על ידי תאים סרטניים, מושפעת מממדיו של הגידול כמו גם מסוג הגידול ומשלבי המחלה (Mouliere. וחב' ב-EMBO Mol Med משנת 2021, ו-Eibl ו-Schneemann ב-Extracell Vesicles Circ Nucleic Acid משנת 2022).
טראומה: רמות מוגברות של cfDNA התגלו בטראומה כתוצאה מחבטה קשה או במקרים של כוויות קשות (Chiu וחב' ב-Clin Chem Lab Med משנת 2006). בשתי הטראומות הללו ריכוז cfDNA בפלזמה היו כרוכות בחומרת הפגיעה ובתוצאותיהן.
ספסיס: נמצא שהגברת cfDNA בפלזמה של מאושפזים ביחידת טיפול נמרץ מסיבה של ספסיס (Rhodes וחב' ב-Crit Care משנת 2006,ו-Martins וחב' ב-Ann NY Acad Sci משנת 2000).
אוטם שריר לב: מטופלים עם סמנים של אוטם שריר לב נמצאו בעלי רמה מוגברת של cfDNA (ללChang וחב' ב-Clin Chim Acta משנת 2003). רמה מוגברת זו נמצאת במתאם טוב עם אירועי לב נוספים ואפילו עם תמותה במהלך השנתיים הקרובות.
דחיית שתל: רמה מוגברת של cfDNA נמצאה בפלזמה של מטופלים מושתלים. CfDNA זה מקורו באיבר המושתל והוא מוגדר כ-donor-derived cell-free DNA (להלן dd-cfDNA). ערכי dd-cfDNA מגיעים לשיאם לאחר פרוצדורת ההשתלה, עם ערכים התלויים בעוצמה באיבר המושתל, ויורדים אופיינית כשבוע לאחר ההשתלה (Beck וחב' ב־Transplant Proc משנת 2015, Grskovic ב-J Mol Diagnost משנת 2016 ו-Kueng וחב' ב-Front Genet משנת 2023). אם המושתל דוחה את השתל ריכוז ה-dd-cfDNA בפלזמת הדם יעלה לרמה הגבוהה פי-5 מזו במקרי השתלה מוצלחים. עלייה זו בריכוז dd-cfDNA יכולה להתגלות לפני סימנים קליניים וביוכימיים אחרים של דחיית השתל. פרט ל-dd-cfDNA בפלזמה, מחקרים אחדים התמקדו בהפרשת dd-cfDNA בשתן. זהו בעל עניין מיוחד בשתל של כליות. כאשר נמדדת רמת dd-cfDNA בשיטה של next-generation sequencing הכימות של dd-cfDNA נעשה אפשרי ללא צורך ב-genotyping קודם של תורם הכליה. יתרון זה נמצא מספק יתרונות קליניים, אם המספר האבסולוטי של עותקי cfDNA המשולב עם הפרקציה של dd-cfDNA מעל cfDNA של המושתל יסייע בקביעה האם השתל האלוגרפטי יידחה או לא.
שיטת הבדיקה
איסוף וניקוי: הניקוי של cfDNA נוטה להזדהם דרך DNA גנומי כיוון שתאי דם פגועים עלולים להשפיע במהלך האיסוף (Lui וחב' ב-Clin Chem משנת 2002). מסיבה זו, שיטות ניקוי שונות יכולות להוביל לכמויות שונות של cfDNA ממוצה (Page וחב' ב-PLoS One משנת 2013, ו-Bartak וחב' ב-Pathol Oncol Res משנת 2018). שיטות ניקוי אופייניות, כורכות איסוף תאים בלקיחת דם ורידי, סרכוז להשקעת התאים ומיצוי cfDNA מהפלזמה (Pérez-Barrios וחב' ב-Translational Lung Cancer Res משנת 2016). CfDNA עובר כימות על ידי שיטות פלואורסצנטיות, כגון צביעת PicoGreen וספקטרומטריה אולטרה-ויולט, אם כי השיטה הרגישה ביותר היא PCR כמותית (SYBR Green or TaqMan) של אלמנטים חוזרים של גנים, או שיטות של ריצוף עמוק. נוקלאוזומים בצירקולציה, שהם היחידה הראשונית החוזרת על עצמה בארגון ה-DNA בכרומטין, עוברים כימות בשיטת ELISA. הדגימות אמורות להישלח למעבדה בטמפרטורת החדר (מועדף) או בקירור. בשתי דרכי ההעברה יציבות הדגימה היא 7 ימים. סרכוז כפול של המבחנה נועד להיפטר מטסיות בפלזמה.
ביבליוגרפיה
- ↑ Mandel P, Metais P (February 1948). "Les Acides Nucléiques Du Plasma Sanguin Chez l'Homme". Comptes Rendus des Séances de la Société de Biologie et de ses Filiales. 142 (3–4): 241–3. PMID 18875018
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק