המדריך לטיפול בסוכרת - היפוגליקמיה בסוכרת - Hypoglycemia in diabetic patients
הופניתם מהדף המדריך לטיפול בסוכרת - היפוגליקמיה בסוכרת לדף הנוכחי.
המדריך לטיפול בסוכרת
מאת המועצה הלאומית לסוכרת, משרד הבריאות. עורכים מדעיים: ד"ר עופרי מוסנזון, פרופ׳ איתמר רז
| המדריך לטיפול בסוכרת | ||
|---|---|---|

| ||
| שם המחבר | ד"ר עפיף נח'לה, פרופסור נעים שחאדה, פרופסור מיכה רפופורט | |
| שם הפרק | היפוגליקמיה בסוכרת | |
| עורך מדעי | פרופסור איתמר רז | |
| מאת | המועצה הלאומית לסוכרת, משרד הבריאות |
|
| מועד הוצאה | 2022 | |
| מספר עמודים | 614 | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – היפוגליקמיה, טיפול בסוכרת
היפוגליקמיה מוגדרת כמצב שבו רמת הסוכר נמוכה בפלזמה ועלולה לחשוף את המטופל לנזק אפשרי. מצב זה נפוץ בקרב מטופלים עם סוכרת מסוג 1, וכ-30 אחוזים ממטופלים אלה חווים בממוצע 1 עד 3 אירועים של היפוגליקמיה קשה בשנה. שכיחות ההיפוגליקמיה הקשה בקרב מטופלים עם סוכרת מסוג 2 נמוכה פי שלושה בהשוואה לסוכרת מסוג 1[1][2].
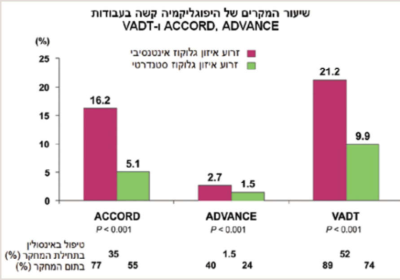
השאיפה ליעדי איזון נמוכים יותר בסוכרת במטרה למנוע התפתחות סיבוכים מיקרו ומאקרווסקולריים הובילה לעלייה בסיכון להיפוגליקמיה. במחקר ה-UKPDS (UK Prospective Diabetes Study) שבו יעד ה-HbA1c היה 7 אחוזים בזרוע הטיפול האינטנסיבי, שיעור ההיארעות השנתי של היפוגליקמיה קשה נע בין 0.7 אחוזים בחולים שקיבלו טיפול פומי עד ל-1.8 אחוזים בחולים שטופלו באינסולין[3]. במחקר ה-DCCT (Diabetes Control and Complications Trial), עד 65 אחוזים מהמטופלים בזרוע הטיפול האינטנסיבי חוו לפחות אירוע אחד של היפוגליקמיה קשה במהלך תקופת המעקב[4]. כמו כן, בקבוצות הטיפול האינטנסיבי במחקרי ADVANCE (Action in Diabetes and Vascular Disease: Preterax and Diamicron Modified Release Controlled Evaluation), ACCORD (Action to Control Cardiovascular Risk in Diabetes) ו-VADT (Veterans Affairs Diabetes Trial) נצפתה עלייה מובהקת באירועי ההיפוגליקמיה בהשוואה לקבוצות הטיפול הסטנדרטי[5][6][7].
יתרה מזאת, עבודות תצפיתיות חושפות שיעור גבוה יותר של אירועי היפוגליקמיה, לרבות היפוגליקמיה קשה. נתון נוסף, העולה מעבודות תצפיתיות, מצביע על היעדר ירידה משמעותית בשיעור ההיפוגליקמיה הקשה, למרות השימוש באנלוגים חדשים של אינסולין ובמשאבות אינסולין (טבלה 1)[8][9][10][11][12][13].
| עבודת המחקר | מספר החולים | גיל (שנים) חציון (טווח) או ממוצע ± סטיית תקין | מעקב (חודשים) | תדירות ההיפוגליקמיה (מקרים/מטופל/שנה) | שיעור המטופלים עם היפוגליקמיה קשה (%) |
| 1993 ,MacLeod (סקוטלנד)[9] | 600 | 41 (79-14) | 12 | 1.6 | 29 |
| 2000 Ter Braak (דנמרק)[10] | 195 | 14 ± 41 | 12 | 1.5 | 41 |
| 2004 Pedersen-Bjergaard
(דנמרק)[11] |
1,076 | 40 (81-18) | 12 | 1.3 | 37 |
| UK Hypoglycaemia Study
2007 Group (בריטניה)[12] |
100 מתוכם 46 עם משך סוכרת של פחות מ-5 שנים (5y>)
54 עם משך סוכרת של יותר מ-15 שנים (15y<) |
5y: 41 ± 13>
15y: 53 ± 10< |
12-9 | 1.1
3.2 |
22
46 |
| Kristensen 2012 (דנמרק)[13] | 3,861 | 15 ± 48 | 12 | 1.2 | 31 |
במטופלים עם סוכרת קשה להגדיר ערך אחיד של גלוקוז בפלזמה לצורך אבחון היפוגליקמיה, היות שהסף להופעת תסמיני היפוגליקמיה משתנה בין מטופלים שונים. סף זה יורד בעקבות מקרי היפוגליקמיה חוזרים ועולים באנשים עם סוכרת לא מאוזנת.
הקלסיפיקציה העדכנית לאירועי היפוגליקמיה בסוכרת כוללת שלוש דרגות בהתאם לחומרת ההיפוגקלימיה[14]:
היפוגליקמיה דרגה 1: מוגדרת כרמת סוכר בפלזמה הנמוכה מ-70 מיליגרם לדציליטר אך מעל או שווה ל-54 מיליגרם לדציליטר. סוכר 70 מיליגרם לדציליטר בפלזמה מהווה את ערך הסף שמתחתיו מופיעה בדרך כלל תגובה נוירואנדוקרינית להיפוגליקמיה באנשים ללא סוכרת. חולי סוכרת רבים סובלים מפגיעה במנגנוני ההגנה מפני היפוגליקמיה ו/או חוסר מודעות להיפוגליקימיה לכן רמת סוכר בפלזמה הנמוכה מ-70 מיליגרם לדציליטר מוגדרת כבעלת משמעות קלינית בסוכרת ודורשת התערבות ללא קשר לחומרת הסימפטומים.
היפוגליקמיה דרגה 2: מוגדרת כרמת סוכר בפלזמה הנמוכה מ-54 מיליגרם לדציליטר הדורשת התערבות מיידית לתיקון ההיפגליקמיה. בהיפוגליקמיה דרגה 2 המטופלים יכולים להתייצג עם תסמינים נוירוגליקופניים.
היפוגליקמיה דרגה 3: מוגדרת כאירוע קשה המאופיין בשינוי במצב ההכרה או פגיעה ביכולת התפקוד הפיזי של המטופל ודורש התערבות של בן אדם אחר לצורך תיקון רמות הסוכר.
תסמינים של היפוגליקמיה
ניתן לחלק את התסמינים של היפוגליקמיה לשתי קטגוריות: תסמינים אוטונומיים ותסמינים נוירוגליקופניים. התסמינים משתנים בין המטופלים בהתאם לגיל ולסוג הסוכרת. לדוגמה, ילדים מבטאים שינויים רגשיים והתנהגותיים משנית להיפוגליקמיה בנוסף לתסמינים האוטונומיים והנוירוגליקופניים הקלאסיים.
התסמינים האוטונומיים כוללים: רעד, חרדה, פלפיטציות, הזעות, תחושת רעב ונימול.
התסמינים הנוירוגליקופניים כוללים: כאבי ראש, טשטוש ראיה, חוסר ריכוז, הפרעה בדיבור, סחרחורת, אי שקט, בלבול, פרכוסים ואיבוד הכרה.
גורמי הסיכון להיפוגליקמיה
ניתן לחלק את גורמי הסיכון להיפוגליקמיה בסוכרת לשתי קטגוריות: גורמי סיכון הקשורים להיפראינסולינמיה תרפויטית וגורמים הקשורים לכשל ב"מנגנוני ההגנה" מפני ירידה בערכי הסוכר בפלזמה.
להלן דוגמאות של מצבים הגורמים להיפראינסולינמיה תרפויטית[15]:
- טיפול באינסולין, Sulfonylurea או Glinide, אם הטיפול ניתן במינון גבוה, או בתזמון לא נכון ביחס לארוחה
- מחסור בגלוקוז אקסוגני כגון אכילת מנה דלה מאוד בפחמימות, או צום ממושך
- מחסור בייצור גלוקוז אנדוגני לאחר שתיית אלכוהול
- עלייה בצריכת הגלוקוז במהלך או אחרי פעילות גופנית
- עלייה ברגישות לאינסולין בעקבות ירידה במשקל או מאמץ גופני
- ירידה בפינוי האינסולין במצבים כמו אי ספיקת כליות, אי ספיקה כבדית, תת-פעילות של בלוטת התריס
פגיעה במנגנוני ההגנה מפני היפוגליקמיה
במצב תקין, הירידה ברמות הסוכר בפלזמה עשויה להוביל לשתי תגובות עיקריות בגוף: עלייה ביצור הסוכר האנדוגני על ידי גליקוגנוליזה וגלוקונאוגנזה, ושינוי התנהגותי המביא לתחושת הרעב והגישה לאוכל[8].
במטופלים לא סוכרתיים, התגובה הראשונית לירידה בערכי הסוכר הי ירידה בהפרשת האינסולין. תגובה זו מתרחשת בעוד ערכי הסוכר הם בתחום הפיזיולוגי הנמוך. ירידה נוספת בסוכר תגרום להפרשה מוגברת של גלוקגון ואפינפרין (כמו גם קורטיזול והורמון גדילה, שתפקידם פחות משמעותי), כך שערכי סוכר נמוכים יותר משפעלים תגובה סימפתואדרנלית אינטנסיבית המובילה להופעת תסמינים רלוונטיים. ירידה נוספת ברמות הסוכר עלולה לגרום להידרדרות קוגניטיבית ותופעות נוירולוגיות קשות כגון פרכוסים או איבוד הכרה[16].
במספר רב של מטופלים עם סוכרת, מנגנוני ההגנה הנזכרים למעלה לקויים. התגובה הראשונה של ירידה בהפרשת האינסולין נעלמת בחולים עם כשל משמעותי של תאי בטא, דבר המוביל לעיכוב בהפרשת הגלוקוז מהכבד בעת היפוגליקמיה. שיעור אירועי ההיפוגליקמיה עולה עם משך הסוכרת, כנראה משנית למחסור הדרגתי באינסולין אנדוגני אשר מתקדם בצורה דוהרת במטופלים עם סוכרת מסוג 1 ובצורה איטית יותר בסוכרת מסוג 2[8].
בנוסף, על אף היותה תקינה בשלבים הראשונים של מחלת הסוכרת, תגובת הגלוקגון להיפוגליקמיה הולכת ודועכת עם הזמן בסוכרת מסוג 1 ובצורה איטית יותר בסוכרת מסוג 2. בשלבים מתקדמים ניכרת גם הפרעה בתגובות הסימפתואדרנליות להיפוגליקמיה. הירידה בתגובת האדרנלים הינה, ככל הנראה, משנית לירידה בסף הסוכר בדם הדרוש לשפעול מנגנון זה. הירידה המשולבת בתגובות הגלוקגון והאפינפרין להיפוגליקמיה מובילה לעלייה בסיכון להיפוגליקמיה בחולים עם סוכרת מסוג 1. מנגנונים אלה שמורים בשלבים הראשונים של סוכרת מסוג 2, אך עם התקדמות הסוכרת והירידה בהפרשת האינסולין האנדוגני, תתפתח הפרעה גם בהם[8].
חוסר מודעות להיפוגליקמיה
הפגיעה בתגובה הסימפתואדרנלית נובעת מאפיזודות חוזרות של היפוגליקמיה אשר מפחיתות את התגובה האוטונומית לאירועי היפוגליקמיה נוספים, דבר החושף את המטופל למעגל קסמים שלילי של אירועי היפוגליקמיה תכופים ומכוון את סף הופעת הסימפטומים לערכי סוכר נמוכים יותר בדם. שכיחות תופעה זו בחולים עם סוכרת מסוג 1 מגיעה ל-25 אחוזים ועולה עד ל-50 אחוזים כעבור 25 שנים של טיפול. בסוכרת מסוג 2 שכיחותה מוערכת סביב 10 אחוזים ולא ברור אם תופעה זו מתפתחת בסוכרתיים הנוטלים טיפול פומי בלבד[8].
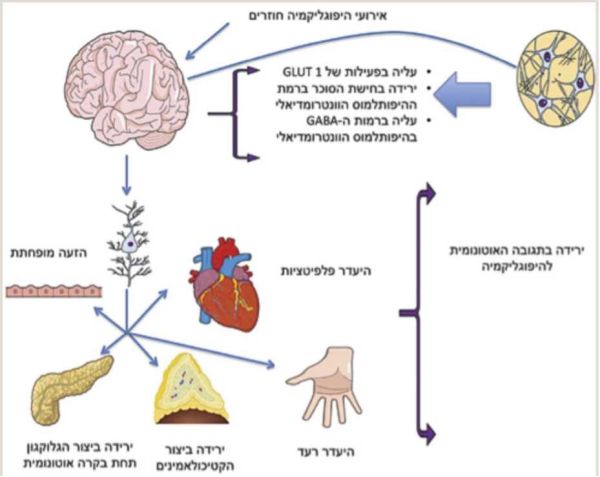
Cryer הגדיר מצב זה ככשל אוטונומי הקשור להיפוגליקמיה HAAF (Hypoglycemia-Associated Autonomic Failure)[17]. אירועי היפוגליקמיה חוזרים, פעילות גופנית רצנטית ושינה עלולים לפגוע במנגנוני ההגנה ולתרום להתפתחות חוסר מודעות להיפוגליקמיה.
תמונה מספר 2 מסכמת את המנגנונים המשוערים בחוסר מודעות להיפוגליקמיה[8].
ההשלכות של היפוגליקמיה בסוכרת
היפוגליקמיה גורמת לתחלואה גופנית ופסיכולוגית במטופלים סוכרתיים. היפוגליקמיה תסמינית מהווה מטרד ומסיחה את הדעת. היא יכולה לפגוע ביכולת השיפוט, בהתנהגות ובביצוע פעולות יומיומיות פשוטות כגון נהיגה. במקרים קשים, היפוגליקמיה עלולה לגרום לפרכוסים ואיבוד הכרה. לעיתים מופיע חסר נוירולוגי חולף ובמקרים נדירים נזק נוירולוגי שארי. במעקב סיסטמטי שנערך במשך 18 שנים אחרי מטופלים מה-DCCT/EDIC לא הודגמה ירידה משמעותית בתפקוד הקוגניטיבי לטווח הארוך במבוגרים עם סוכרת מסוג 1[18]. מידע זה לא כולל ילדים או זקנים עם סוכרת. בספרות קיימות מספר עדויות לקשר בין היפוגליקמיה לירידה קוגניטיבית בשתי הקבוצות הנזכרות למעלה. בעבודה אחת נצפה קשר בין היפוגליקמיה לירידה בתפקוד הקוגניטיבי בילדים לרבות יכולות שפתיות, זיכרון עבודה ומהירות עיבוד לא שפתית[19]. בעבודה נוספת, נראה כי היפוגליקמיה מכפילה את הסיכון להתפתחות דמנציה בקרב חולי סוכרת זקנים[20].
אין ספק כי החשש מהיפוגליקמיה מהווה גם הוא מחסום לטיפול ואיזון הסוכרת. יתרה מכך, אנשים שחווים אירועי היפוגליקמיה חוזרים נמצאים בסיכון לדיכאון והפרעות חרדה.
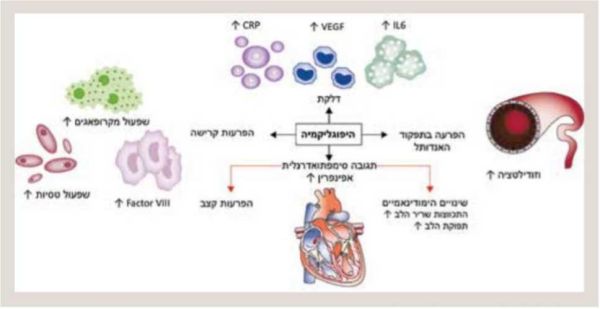
במטא-אנליזה שכללה יותר מ-900,000 מטופלים עם סוכרת מסוג 2, נצפתה עלייה פי 2 בסיכון לתחלואה קרדיווסקולרית בקרב מטופלים עם היפוגליקמיה קשה. ניתן להסביר תופעה זו על ידי התגובה הסימפתואדרנלית והעלייה הניכרת ברמת הקטכולאמינים בדם הכרוכה בהשפעה ישירה על המיוקרד והמערכת הווסקולרית, אקטיבציה ואגריגציה של טסיות[21]. במקרים קשים יותר היפוגליקמיה עלולה לגרום לתמותה. שיעור התמותה מהיפוגליקמיה מהווה כ-4–10 אחוזים ממקרי התמותה במטופלים עם סוכרת מסוג 1[22][23]. בחולים עם סוכרת מסוג 2 שיעור התמותה מהיפוגליקמיה אינו ידוע.
אף על פי שהיפוגליקמיה קשה מתמשכת עלולה לגרום למוות מוחי, רוב המקרים של תמותה היפוגליקמית פתאומית קשורים להפרעות קצב לבביות הנובעות מתגובה סימפתואדרנלית מוגברת, אשר עלולה לגרום להארכת מקטע QT[24]. עבודות קליניות ואפידמיולוגיות שכללו עשרות אלפי מטופלים עם סוכרת מסוג 1 וסוכרת מסוג 2 ממגוון שירותי בריאות באזורים שונים בעולם הראו עלייה של פי 1.5 עד פי 6 בסיכון למאורעות קרדיווסקולריים ולתמותה בקרב מטופלים אשר חוו היפוגליקמיה קשה[25].
היפוגליקמיה בהיריון
לאיזון הסוכרת בנשים הרות חשיבות רבה למניעה סיבוכים אצל האם והעובר. ההגדרה והאבחון של היפוגליקמיה בהיריון מאתגרים, וזאת לאור העובדה שיעדי הסוכר בהיריון נמוכים ב-20 אחוזים מהיעדים לפני ההיריון[27]. עדויות מהספרות מצביעות על עלייה ניכרת של עד פי חמישה בשיעור ההיפוגליקמיה הקשה בטרימסטר הראשון אצל נשים עם סוכרת מסוג 1[28]. לרוב, היפוגליקמיה אצל האם לא מסכנת את העובר כל עוד האם נמנעת מחבלה במהלך האירוע. הנקה גם מעלה את הסיכון להיפוגליקמיה בנשים סוכרתיות המטופלות באינסולין[29].
היפוגליקמיה באשפוז
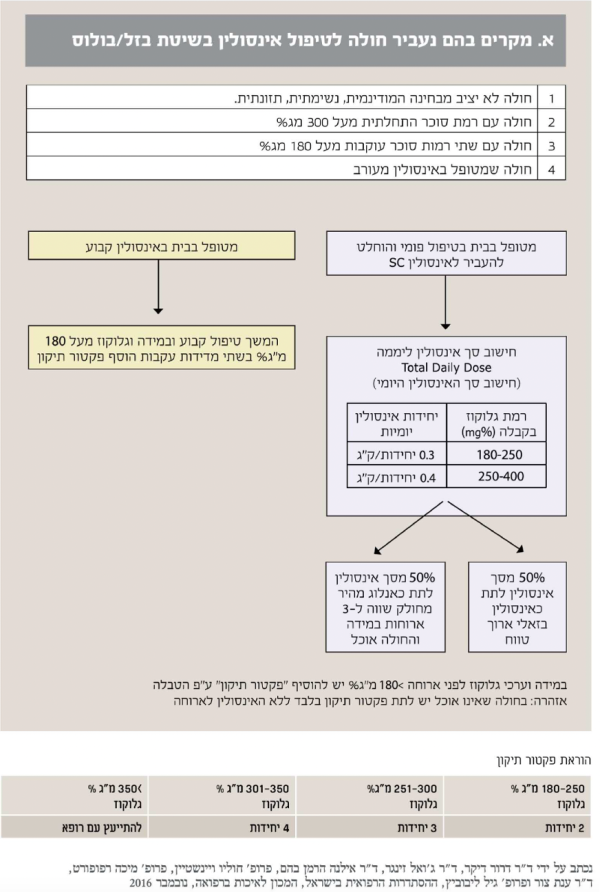
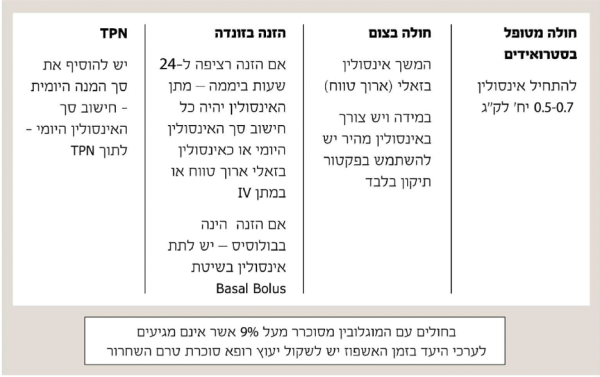
בכל רגע נתון מהווים חולי הסוכרת כ-30–40 אחוזים מחולי הסוכרת המאושפזים במחלקה הפנימית. שיעור זה אף גבוה יותר ביחידות לטיפול נמרץ ו/או דיאליזה ומגיע עד כדי 70 אחוזים ויותר. מידת האיזון של רמות הסוכר בזמן האשפוז עברה טלטלות בעשורים האחרונים ושונתה מגישה מחמירה של איזון הדוק לגישה מקלה יותר של איזון פחות הדוק, כאשר הטווח הרצוי הוא בין 140 ל-180 מיליגרם לדציליטר. שינוי זה בגישה נבע בעיקר מהתצפית שאיזון כרוך יותר בהופעת היפוגליקמיה קשה ואף מסכנת חיים, שאינה תורמת לשיפור בתחלואה או במדדי האשפוז של החולה הסוכרתי. שני ניירות עמדה בנושא שנכתבו על ידי קלינאים מובילים בסוכרת העובדים בבתי חולים, מסכמים את הגישה לאיזון רמות הסוכר אצל החולה המאושפז במחלקה הפנימית ואת דפוס ההתמודדות עם מניעת היפוגליקמיה באשפוז והטיפול בה (נספח 1, נספח 2).
טיפול בהיפוגליקמיה
רוב המקרים של היפוגליקמיה תסמינית או היפוגליקמיה לא תסמינית המאובחנים בניטור עצמי ניתנים לטיפול בצורה יעילה על ידי נטילת פחמימה פשוטה, המקבילה לכ-20 גרם גלוקוז ומהווה מינון סביר במרבית המקרים הנזכרים למעלה עם צפי לשיפור קליני תוך 20 דקות.
יש להדגיש את חשיבות המתן של פחמימה מורכבת לאחר תיקון רמת הסוכר, כי בהיפראינסולינמיה מתמשכת האפקט של הגלוקוז הפומי זמני ונמשך פחות משעתיים.
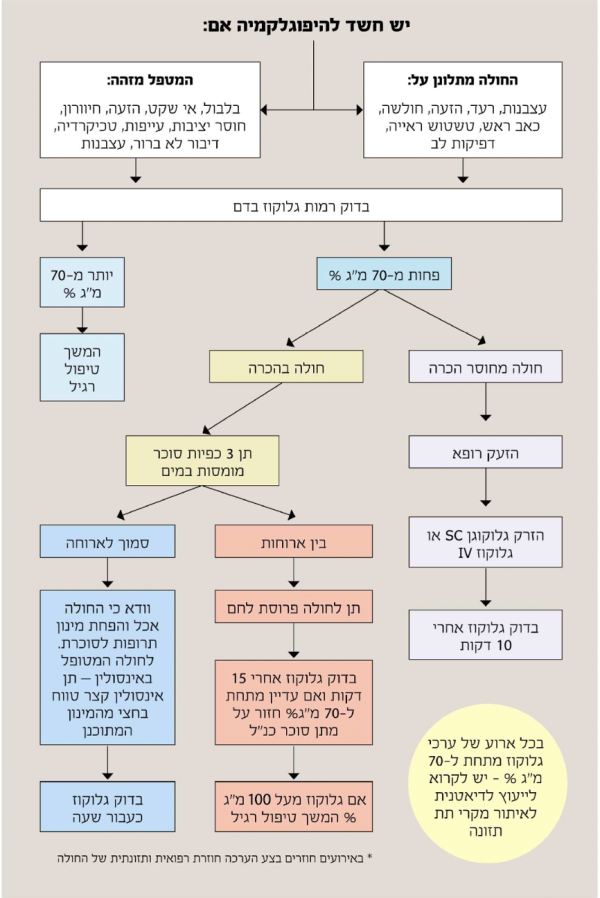
להלן הפרוטוקול לטיפול בהיפוגליקמיה, שנערך ברובו בהתאם להנחיות ה-Joint British Diabetes Societies[30].
מטופל ערני, בהכרה מלאה:
- אם המטופל מקבל אינסולין (משאבה, עירוי) יש להפסיקו מיידית
- יש לתת 20-15 גרם של גלוקוז או פחמימה פשוטה אחרת. דוגמאות: 20-15 גרם של טבליות גלוקוז ללעיסה, מיץ תפוזים 150–200 מיליליטר, 4 כפיות סוכר מומסות במים
- יש לחזור על בדיקת סוכר בדם קפילרי כעבור 10 דקות. אם הוא עדיין נמוך מ-70 מיליגרם לדציליטר יש לחזור על הצעד הקודם עד 3 פעמים
- אם הסוכר בדם קפילרי עדיין נמוך מ-70 מיליגרם לדציליטר כעבור 30–45 דקות או 3 מחזורים של טיפול, יש לשקול:
- מתן תוך ורידי IV של 200 מיליליטר של גלוקוז 10 אחוזים (או 100 מיליליטר של גלוקוז 20 אחוזים) תוך 15 דקות או:
- מתן תוך שרירי IM של גלוקגון 1 מיליגרם
- לאחר עלית הסוכר בדם מעל 70 מיליגרם לדציליטר, מומלץ לתת פחמימה מורכבת (לפחות 20 גרם), כגון פרוסות לחם, כוס חלב 200–300 מיליליטר או ארוחה אחרת שמכילה פחמימה מורכבת
הערות:
הגלוקגון עלול להיות פחות יעיל במטופלים שטופלו בסולפונילאוריאה או תחת השפעה של אלכוהול. לאנשים שקיבלו גלוקוגון דרושה מנה גדולה יותר של פחמימה מורכבת (40 גרם) על מנת לחדש את מאגרי הגליקוגן. יש לקחת בחשבון כי לפעמים מופיעות בחילות אחרי מתן גלוקגון. אם ההיפוגליקמיה משנית לסולפונילאוריאה או אינסולין ארוך טווח, הסיכון להיפוגליקמיה עלול להימשך 24–36 שעות אחרי נטילת המנה האחרונה, במיוחד באנשים עם אי ספיקה כלייתית.
אם המטופל בהכרה, מבולבל ולא משתף פעולה, אך מסוגל לבלוע:
- אם המטופל מקבל אינסולין (משאבה, עירוי) יש להפסיקו מיידית
- אם המטופל לא משתף פעולה אך מסוגל לבלוע, מומלץ לתת שפופרת של גלוקוז 15 גרם (לדוגמה: גלוקו-ג׳ל), או זריקה תוך שרירית IM של גלוקגון 1 מיליגרם
- יש לחזור על בדיקת סוכר בדם קפילרי כעבור 10 דקות. אם הוא עדיין נמוך מ-70 מיליגרם לדציליטר יש לחזור על הצעד הקודם עד 3 פעמים (זריקת הגלוקגון תינתן פעם אחת בלבד)
- אם הסוכר בדם קפילרי עדיין נמוך מ-70 מיליגרם לדציליטר כעבור 30–45 דקות או 3 מחזורים של טיפול, יש לתת 200 מיליליטר של גלוקוז 10 אחוזים (או 100 מיליליטר של גלוקוז 20 אחוזים) דרך הווריד IV במשך 15 דקות
לאחר עלית הסוכר בדם מעל 70 מיליגרם לדציליטר, מומלץ לתת פחמימה מורכבת (כמפורט מקודם).
מטופל עם פרכוס, או מחוסר הכרה:
- דרושה הערכה רפואית דחופה. יש לבדוק את הדברים הבאים ולתת מענה וטיפול בהתאם, לרבות נתיב אויר (מתן חמצן בהתאם), נשימות, סירקולציה (דופק), מצב הכרה, רמת סוכר בדם וטמפרטורת הגוף. אם המטופל מקבל אינסולין (משאבה, עירוי) יש להפסיקו מיידית
- אם אין גישה מיידית לווריד אזי מומלץ לתת גלוקגון 1 מיליגרם דרך השריר IM
- אם קיימת גישה מיידית לווריד (המטופל עם "וריד פתוח") אזי מומלץ לתת 100 מיליליטר של גלוקוז 20 אחוזים דרך הווריד IV או 200 מיליליטר של גלוקוז 10 אחוזים במשך 15 דקות. ניתן גם לתת 25-10 גרם של גלוקוז (50-20 מיליליטר של גלוקוז 50 אחוזים) דרך הווריד IV במשך 1–3 דקות בהתאם להנחיות Diabetes Canada[31]. חשוב לבצע מעקב על העירוי ויש להדגיש את הסיכון הכרוך בדליפת עירוי פריפרי (אקסטרווזציה) בעת מתן תמיסת גלוקוז היפרטונית, דבר אשר עלול לגרום לנזק מקומי לווריד ולרקמות הרכות. יש לחזור על בדיקת סוכר בדם קפילרי כעבור 10 דקות. אם הוא עדיין נמוך מ-70, יש לחזור על טיפול זה. גלוקגון פחות יעיל במקרים של שימוש בסולפונלאוריאה, שתית אלכוהול ובחולים עם מחלת כבד כרונית. אם קיים צורך בטיפול ממושך, מתן גלוקוז תוך ורידי IV הוא טיפול הבחירה
- לאחר עלית הסוכר בדם מעל 70 מיליגרם לדציליטר, מומלץ לתת פחמימה מורכבת (כמפורט מקודם)
מניעת היפוגליקמיה
חשוב לקבוע את יעדי האיזון של המטופל הסוכרתי בצורה מותאמת אישית לפי גיל, תוחלת חיים, מחלות רקע וסיכון להיפוגליקמיה[31]. למשל, בילדים צעירים מאוד חשוב להימנע בכל מחיר מהיפוגליקמיה קשה, לאור השפעתה השלילית על התפתחות המוח. במבוגרים "בריאים" עם סוכרת, יעד האיזון שלנו יהיה הגעה ל-HbA1c הנמוך ביותר שלא במחיר של היפוגליקמיה קשה. יעדי האיזון יהיו גמישים יותר במטופלים עם סוכרת ארוכת שנים המלווה בסיבוכים מתקדמים או תוחלת חיים קצרה, ומטופלים מבוגרים עם סיכון גבוה לנפילות.
בנוסף, כאשר יש עדות לחוסר מודעות להיפוגליקמיה, מומלץ להעלות את יעדי האיזון לערכים גבוהים יותר. הוכח, כי הימנעות מוחלטת מהיפוגליקמיה במשך שבועות ספורים משפרת את התגובה ההורמונלית (הפרשת האדרנלין) ואת המודעות להיפוגליקמיה[17].
כלים למניעת היפוגליקמיה
הגישה למניעת היפוגליקמיה כוללת הדרכת המטופל, התאמת משטר הדיאטה והפעילות הגופנית, ניטור עקומת הסוכר על ידי המטופל ומעקב קליני צמוד4,. נכתב והופץ בקרב מרפאות הסוכרת בקהילה שאלון שמטרתו לזהות את חולה הסוכרת הנמצא בסיכון גבוה להיפוגליקמיה תסמינית וחמורה ולנקוט בפעולה המתאימה כדי למנוע אותה (נספח מס׳ 3).
הדרכת המטופל
יש להדריך את המטופל והסובבים אותו לזהות תסמינים של היפוגליקמיה ולתת טיפול הולם בהקדם האפשרי. חשוב לדון באופן רוטיני בסיכונים להתפתחות היפוגליקמיה ואופן הטיפול בה, בחולים המטופלים באינסולין, סולפונילאוריאה, או גליניד. בכל תיעוד של היפוגליקמיה יש לחקור יחד עם המטופל את נסיבות האירוע ולנסות להבחין בסיבה, כגון: דילוג על ארוחה׳צום ממושך, פעילות גופנית מאומצת, שתית אלכוהול והזרקת מינון גבוה של אינסולין.
חולי סוכרת הנמצאים בסיכון מוגבר להיפוגליקמיה מתבקשים לשאת איתם תמיד גלוקגון. בני משפחה ואנשים הנמצאים בסביבת חולי הסוכרת אמורים לעבור הדרכה על אופן מתן הגלוקגון לחולה, הם גם אמורים להכיר את מיקום אחסון הגלוקגון. תכשירי גלוקגון כוללים תמיסה להזרקה תת-עורית או תוך שרירית, וכן תכשיר גלוקגון לשימוש דרך האף (שאושר על ידי ה-FDA, Food and Drug Administration, בשנת 2019).
התערבות דיאטטית
התערבות דיאטטית תכלול הדרכה לגבי כמות הפחמימות בארוחה והשפעתן על רמות הסוכר בדם ובניית תוכנית לארוחות סדירות בצורה מותאמת אישית. בחולים המטופלים על ידי אינסולין יש להדגיש את חשיבות מתן האינסולין במינון ובתזמון המתאים לארוחה. יש להנחות מטופלים בסיכון להיפוגליקמיה להצטייד בגלוקוז או במאכלים המכילים פחמימות ולשאת עימם בכל עת. בחלק מהמטופלים, במיוחד אלה עם סוכרת מסוג 1 וסיכון גבוה להיפוגליקמיה לילית, ניתן להתאים ארוחת לילה במטרה למנוע היפוגליקמיה.
ייעוץ פעילות גופנית
פעילות גופנית מעלה את צריכת הסוכר ואת הסיכון להיפוגליקמיה. גורמי הסיכון כוללים: פעילות גופנית מאומצת לזמן ממושך והיעדר מקור אנרגיה ביחס לאינסולין בגוף. בעזרת מעקב רמות הסוכר בדם לפני ואחרי הפעילות הגופנית, ניתן לנקוט בצעדים מקדימים למניעת היפוגליקמיה. מומלץ לאכול ארוחות קטנות טרם הפעילות הגופנית אם קיימת ירידה בערכי הסוכר. מומלץ להצטייד בפחמימות פשוטות בעת הפעילות הגופנית. חשוב להתאים את מינון האינסולין בימים שבהם מתוכננת פעילות גופנית.
ניטור סוכר
ניטור עצמי של רמות הסוכר בדם ומד סוכר רציף מהווים כלים חיוניים לאבחון היפוגליקמיה בשלבים מוקדמים. ניטור עצמי של רמות הסוכר בדם (SMBG, Self-Monitoring of Blood Glucose) מהווה חלק אינטגרלי מהמאמצים למניעת היפוגליקמיה. ה-ADA (American Diabetes Association) ממליץ כי רוב המטופלים במשטרי אינסולין אינטנסיביים (MDI או משאבה) יבדקו סוכר לפני ארוחות ומדי פעם אחריהן, לפני שינה, לפני פעילות גופנית, בעת קיום חשד לסוכר נמוך בדם, לאחר טיפול בהיפוגליקמיה ולפני פעולות מסוימות הדורשות ריכוז גבוה כמו נהיגה[32].
אין מספיק מידע בספרות לגבי תדירות ניטור הסוכר העצמי הדרושה בחולים עם סוכרת מסוג 2 המטופלים באינסולין בזאלי ו/או בטיפול פומי. על פי רוב, המעקב יהיה פחות תכוף עם מדידות בצום בבוקר ולעיתים לפני ארוחת ערב. מד הסוכר הרציף (CGM, Continuous Glucose Monitoring) אשר מודד את הסוכר האנטרסטיציאלי בזמן אמת, מהווה כלי פוטנציאלי לשיפור איזון הסוכרת והפחתת אירועי ההיפוגליקמיה.
ניטור סוכר רציף נבחן במספר רב של עבודות, חלקן בדקו יעילות CGM באיזון הסוכרת וחלקן בחנו שילוב של CGM במטרה להפחית אירועי היפוגליקמיה. בחולים עם סוכרת (מסוג 1 ומסוג 2) לא מאוזנת, שימוש ב-CGM תרם לשיפור באיזון וירידה של 0.3 אחוזים עד 0.6 אחוזים ב-HbA1c[33]. רוב העבודות שבחנו שימוש ב-CGM למניעת היפוגליקמיה בסוכרת מסוג 1 הראו ירידה משמעותית בזמן השהייה בהיפוגליקמיה בטווח שבין 54 עד 70 מיליגרם לדציליטר. עם זאת, עד היום אף עבודה לא הראתה ירידה משמעותית באירועי היפוגליקמיה מדרגה 3[33].
בעבודה שכללה 120 מטופלים, ילדים ומבוגרים, עם סוכרת מסוג 1 ועם HbA1c הנמוך מ-7.5 אחוזים אשר חולקו לקבוצת מעקב על ידי CGM וקבוצת ביקורת למשך 26 שבועות - זמן השהייה בהיפוגליקמיה ליממה היה קצר בצורה משמעותית ולווה באיזון טוב יותר בקבוצה שהשתמשה ב-CGM לעומת קבוצת הביקורת[34].
עבודה אחרת שכללה 322 מטופלים עם סוכרת מסוג 1 שטופלו במשטר אינסולין אינטנסיבי הראתה ירידה של 0.5 אחוזים ב-HbA1c במבוגרים בני 25 שנים ומעלה, שהשתמשו ב-CGM לעומת אלה שביצעו ניטור עצמי של ערכי הסוכר (SMBG), ללא הבדל משמעותי בשיעור ההיפוגליקמיה. לא נצפה הבדל משמעותי ב-HbA1c או באירועי ההיפוגליקמיה בצעירים מתחת לגיל 25[35].
עבודה נוספת במטופלים עם סוכרת מסוג 1 ו-HbA1c התחלתי של פחות מ-7 אחוזים הדגימה יתרונות לשימוש ב-CGM הן מבחינת איזון הסוכרת והן מבחינת הפחתת היפוגליקמיה[36].
מחקר HypoDE הראה כי שימוש ב-CGM הוריד בצורה משמעותית את שיעור ההיפוגליקמיה במטופלים מבוגרים עם סוכרת מסוג 1 ורקע של היפוגליקמיה קשה או חוסר מודעות להיפוגליקמיה, אשר טופלו באינסולין במשטר MDI[37]. עם זאת, לא נראתה הפחתה משמעותית באירועי ההיפוגליקמיה הקשה שדורשת התערבות רפואית (למתן גלוקוז או גלוקגון) בהשוואה לקבוצת הביקורת[37].
במחקר DIAMOND שנערך בקרב מטופלים עם סוכרת מסוג 1, שימוש ב-CGM לתקופה של 24 שבועות הביא לשיפור באיזון הסוכרת (ירידה של 0.6 אחוזים ב-HbA1c) עם ירידה משמעותית בווריאביליות הגליקמית ובזמן השהייה בהיפוגליקמיה, אך ללא שינוי באירועי היפוגליקמיה קשה[38].
טכנולוגית CGM עשויה להיות שימושית במטופלים עם סוכרת מסוג 1 ואפיזודות חוזרות של היפוגליקמיה ו/או חוסר מודעות להיפוגליקמיה. אולם, יעילות ה-CGM לטווח ארוך טרם נקבעה.
אין מספיק מידע בספרות בנוגע ליעילות CGM במניעת היפוגליקמיה בסוכרת מסוג 2. במטא-אנליזה ריצנטית לא נצפה יתרון משמעותי ל-CGM על פני SMBG במניעת היפוגליקמיה בחולי סוכרת מסוג 2 שטופלו באינסולין. עם זאת, לא נצפתה עלייה בסיכון להיפוגליקמיה למרות ירידה משמעותית יותר ב-HbA1c בחולים שהשתמשו ב-CGM[39].
טכנולוגיה נוספת שנכנסה לשימוש היא טכנולוגית פלאש לניטור רמות הסוכר, הפועלת בסריקה ללא צורך בדקירה של האצבע וללא כיולים, אשר הוכחה כמורידה בצורה משמעותית את שיעור ההיפוגליקמיה בקרב מטופלים מבוגרים עם סוכרת מסוג 1 ברמת איזון טובה[40].
התאמת תרופות
חלק מאירועי ההיפוגליקמיה בסוכרת קשור לטיפול התרופתי עצמו, לכן חשוב להשתמש בתרופות עם סיכון נמוך להיפוגליקמיה.
מטפורמין, מעכבי 4-DPP, מעכבי SGLT2, אנלוגים של GLP-1 ופיוגליטזון כרוכים בסיכון נמוך להיפוגליקמיה בחולים עם סוכרת מסוג 2. לעומתם, תרופות ממשפחת הסולפונילאוריאה והמגלינטידים כרוכות בסיכון גבוה יותר להיפוגליקמיה[41], לכן מומלץ לשקול הורדת מינון או הפסקת התרופה ומעבר לטיפול אחר במקרים חוזרים של היפוגליקמיה, בתחילת המאה ה-21 הוביל המעבר לשימוש באנלוגים של אינסולין בזאלי ארוך טווח (כמו Levemir ו-Glargine U100) לירידה משמעותית באירועי ההיפוגליקמיה הלילית בהשוואה לאינסולין NPH[42][43], והחל מהעשור השני של המאה ה-21, האינסולינים הבזאליים ארוכי הטווח החדשים Glargine U300 (300 יחידות למיליליטר) ו-Degludec הובילו לירידה משמעותית נוספת בשיעור ההיפוגליקמיה הלילית בחולים עם סוכרת מסוג 1 וחולים עם סוכרת מסוג 2[44][45][46][47]. כמו כן, השימוש באנלוגים של אינסולין קצר טווח הביא לירידה משמעותית בשיעורי ההיפוגליקמיה הקשה בהשוואה לאינסולין הומני[48].
שילוב בין אינסולין בזאלי לאנלוג של 1-GLP במזרק אחד וביחס קבוע (Fixed Ratio Combination ,FRC), הראה שיפור משמעותי באיזון בחולים עם סוכרת מסוג 2 ללא עלייה בסיכון להיפוגליקמיה[49].
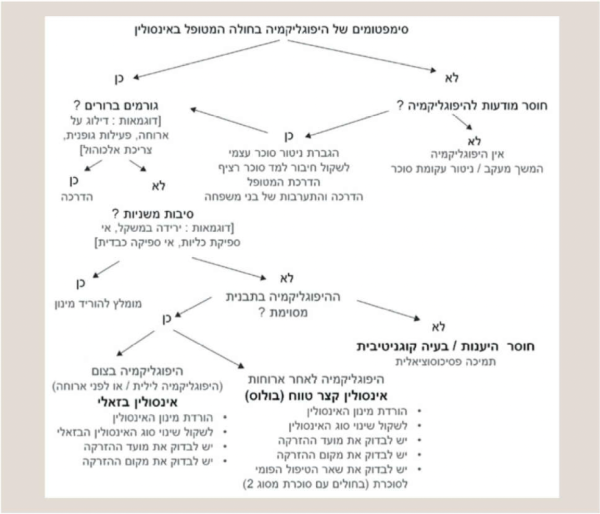
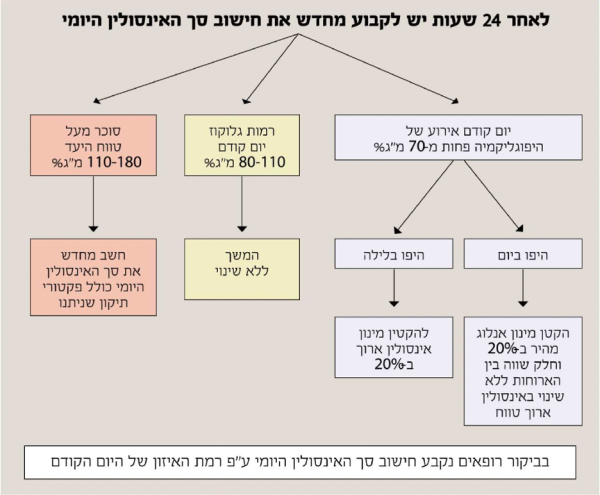
הגישה למניעת היפוגליקמיה בחולי סוכרת המטופלים באינסולין מפורטת בתמונה 4[50].
בעבודה משנת 2010 הודגם כי שימוש במשאבת אינסולין (Continuous Subcutaneous Insulin Infusion ,CSII) שיפר את סף המודעות להיפוגליקמיה בחולים עם סוכרת מסוג 1 שסבלו מאירועים חוזרים של היפוגליקמיה[51].
מטא-אנליזה משנת 2012 לא העלתה יתרון לשימוש במשאבה על פני משטר אינסולין מסוג Multiple Daily Insulin) MDI) בהפחתת אירועי ההיפוגליקמיה הקשה[52]. מטא-אנליזה נוספת הראתה יתרון קטן למשאבה בהורדת ה-HbA1c (0.2- אחוזים) ללא הבדל משמעותי באירועי היפוגליקמיה קשה בהשוואה לאינסולין במשטר MDI[53]. מטא-אנליזה קודמת הראתה שבהשוואה למשטר אינסולין MDI השימוש במשאבה הוריד את הסיכון להיפוגליקמיה, אך מסקנה זו התבססה על 3 עבודות מבוקרות שהשתמשו באינסולין NPH או Lente[52].
במחקר ASPIRE, שימוש במשאבת אינסולין המשלבת קריאת סוכר רציפה ומנגנון השהייה אוטומטי של הזלפת האינסולין בתגובה לערכי סוכר נמוכים הביא לירידה משמעותית באירועי ההיפוגליקמיה הלילית במטופלים עם סוכרת מסוג 1, ללא עלייה ב-HbA1c[54].
מחקר HypoCOMPaSS אשר כלל מטופלים עם סוכרת מסוג 1 והשווה בין קבוצת טיפול באינסולין MDI עם ניטור סוכר עצמי (SMBG) לבין קבוצת טיפול במשאבת אינסולין עם מד סוכר רציף (CGM), הראה ירידה באירועי היפוגליקמיה קשה ושיפור במודעות להיפוגליקמיה בצורה דומה בשתי הקבוצות, אך שביעות הרצון של המטופלים הייתה גבוהה יותר בקבוצת המשאבה[55].
מושקע מאמץ רב בבניית "הלבלב המלאכותי" - מערכת המשלבת העברת מידע אלחוטית בין מד סוכר רציף למשאבה האינסולין במעגל סגור, כך שהמשאבה תחשב את כמות האינסולין להזלפה בהתאם לרמת הסוכר שנמדדת. בסקירה סיסטמטית ומטא-אנליזה שפורסמה, הודגם כי שימוש בטכנולוגית "לבלב מלאכותי" מהווה טיפול יעיל ובטוח בחולים עם סוכרת מסוג 1 ומביא לשיפור באיזון הסוכר ולירידה באירועי ההיפוגליקמיה[56].
במקרים בודדים, הורידה השתלת איי לבלב את אירועי ההיפוגליקמיה ושיפרה את המודעות להיפוגליקמיה במטופלים עם סוכרת מסוג 1[57].
חשוב לזכור - היפוגליקמיה בסוכרת
- היפוגליקמיה היא סיבוך שכיח בחולים עם סוכרת, בעיקר באלה שמטופלים באינסולין, או בתרופות ממשפחת הסולפונילאוריאה או הגלינידים
- הסיכון להיפוגליקמיה בסוכרת עולה בנוכחות אי ספיקת כליות
- פגיעה במנגנוני ההגנה מפני היפוגליקמיה וחוסר מודעות להיפוגליקמיה מהווים גורמי סיכון עיקריים להיפוגליקמיה קשה
- אירועי היפוגליקמיה כרוכים בתחלואה גופנית ופסיכולוגית, ובמקרים קשים מאוד עלולים לגרום לתמותה
- החשש מהיפוגליקמיה מהווה בפני עצמו מחסום שפוגע ביכולת המטופל להגיע לאיזון טוב של הסוכרת
- על מנת למנוע היפוגליקמיה יש להשקיע מאמץ רב בהדרכה בנוגע לגורמי סיכון, סימנים מקדימים וטיפול בהיפוגליקמיה בשלב מוקדם, תוך כדי קביעת יעדי איזון מותאמים אישית
נספחים
ביבליוגרפיה
- ↑ Pedersen-Bjergaard U, Pramming S, Heller SR, et al. Severe hypoglycaemia in 1076 adult patients with type 1 diabetes: influ- ence of risk markers and selection. Diabetes Metab Res Rev 2004; 20:479-486
- ↑ Donnelly LA, Morris AD, Frier BM, et al.; DARTS/MEMO Collaboration. Frequency and predictors of hypoglycaemia in type 1 and insulin-treated type 2 diabetes: a populationbased study. Diabet Med 2005; 22:749-755
- ↑ UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). Lancet 1998; 352:854-865
- ↑ The Diabetes Control and Complications Trial Research Group. Hypoglycemia in the Diabetes Control and Complications Trial. Diabetes 1997; 46:271
- ↑ Gerstein HC, Miller ME, Byington RP, et al.; Action to Control Cardiovascular Risk in Diabetes Study Group. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008; 358:2545-2559
- ↑ Patel A, MacMahon S, Chalmers J, et al.; ADVANCE Collaborative Group. Intensive blood glucose control and vascular out- comes in patients with type 2 diabetes. N Engl J Med 2008; 358:2560-2572
- ↑ Duckworth W, Abraira C, Moritz T, et al.; VADT Investigators. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009; 360:129-139
- ↑ 8.0 8.1 8.2 8.3 8.4 8.5 Iqbal A, Heller S. Managing hypoglycaemia. Best Pract Res Clin Endocrinol Metab 2016; 30 (3), 413-430
- ↑ 9.0 9.1 MacLeod KM, Hepburn DA, Frier BM. Frequency and morbidity of severe hypoglycaemia in insulin-treated diabetic patients. Diabet Med J Br Diabet Assoc 1993;10(3):238-245
- ↑ 10.0 10.1 Ter Braak EW, Appelman AM, van de Laak M, et al. Clinical characteristics of type 1 diabetic patients with and without severe hypoglycemia. Diabetes Care 2000;23(10):1467-1471
- ↑ 11.0 11.1 Pedersen-Bjergaard U, Pramming S, Heller SR, et al. Severe hypoglycaemia in 1076 adult patients with type 1 diabetes: influence of risk markers and selection. Diabetes/Metab Res Rev. 20(6):479-486
- ↑ 12.0 12.1 UK Hypoglycaemia Study Group. Risk of hypoglycaemia in types 1 and 2 diabetes: effects of treatment modalities and their duration. Diabetologia 2007;50(6):l 140-1147
- ↑ 13.0 13.1 Kristensen PL, Hansen LS, Jespersen MJ, et al. Insulin analogues and severe hypoglycaemia in type 1 diabetes. Diabetes Res Clin Pract 2012;96(1):17-23
- ↑ Agiostratidou G, Anhalt H, Ball D, Blonde L, Gourgari E, Harriman KN, Kowalski AJ, Madden P, McAuliffe-Fogarty AH, McElwee-Malloy M, Peters A. Standardizing clinically meaningful outcome measures beyond HbAlc for type 1 diabetes: a consensus report of the American Association of Clinical Endocrinologists, the American Association of Diabetes Educators, the American Diabetes Association, the Endocrine Society, JDRF International, The Leona M. and Harry B. Helmsley Charitable Trust, the Pediatric Endocrine Society, and theTID Exchange. Diabetes Care. 2017 Dec 1;40(12):1622-30
- ↑ International Hypoglycaemia Study Group. Minimizing Hypoglycemia in Diabetes. Diabetes Care 2015; 38:1583-1591
- ↑ Melmed S, Polonsky K, Reed Larsen P, Kronenberg HM. Williams Textbook of Endocrinology 13th edition. 2016; Page 1584
- ↑ 17.0 17.1 Cryer PE. Diverse causes of hypoglycemia-associated autonomic failure in diabetes. New England Journal of Medicine. 2004; 350(22):2272-9
- ↑ Jacobson AM, Musen G, Ryan CM, et al. Diabetes Control and Complications Trial/Epidemiology of Diabetes Interventions and Complications Study Research Group. Longterm effect of diabetes and its treatment on cognitive function. N Engl J Med 2007;356:1842-1852
- ↑ Lin, A., Northam, E. A., Rankins, D., Werther, G. A., & Cameron, F. Neuropsychological profiles of young people with type 1 diabetes 12 yr after disease onset. Pediatric diabetes, 2010,11.4: 235-243
- ↑ 20.0 20.1 Yaffe, K., Falvey, C. M., Hamilton, N., Harris, T. B. et al. Association between hypoglycemia and dementia in a biracial cohort of older adults with diabetes mellitus. JAMA internal medicine 2013; 173(14), 1300-1306
- ↑ Goto A, Arah OA, Goto M, et al. Severe hypoglycaemia and cardiovascular disease: systematic review and metaanalysis with bias analysis. BMJ (Clin Res Ed) 2013;347
- ↑ Patterson CC, Dahlquist G, Harjutsalo V, et al. Early mortality in the EURODIAB population-based cohorts of type 1 diabetes diagnosed in childhood since 1989. Diabetologia. 2007; 50:2439-2442
- ↑ Skrivarhaug T, Bangstad HJ, Stene LC, et al. Long-term mortality in a nationwide cohort of childhood-onset type 1 diabetic patients in Norway. Diabetologia. 2006; 49:298-305
- ↑ Reno CM, Daphna-lken D, Chen YS, et al. Severe hypoglycemia induced lethal cardiac arrhythmias are mediated by sym- pathoadrenal activation. Diabetes. 2013; 62:3570-3581
- ↑ Amiel SA, Aschner P, Childs B, Cryer PE, de Galan BE, Frier BM, Gonder-Frederick L, Heller SR, Jones T, Khunti K, Leiter LA. Hypoglycaemia, cardiovascular disease, and mortality in diabetes: epidemiology, pathogenesis, and management. The Lancet Diabetes & Endocrinology. 2019 Mar 27
- ↑ Desouza CV, Bolli GB, Fonseca V. Hypoglycemia, diabetes ,and cardiovascular events. Diabetes Care 2010; 33:1389-94
- ↑ Yogev Y, Ben-Haroush A, Chen R, Rosenn B, Hod M, Langer O. Diurnal glycemic profile in obese and normal weight nondia- betic pregnant women. Am J Obstet Gynecol 2004; 191:949-953
- ↑ Ringholm L, Pedersen-Bjergaard U, Thorsteinsson B, Damm P, Mathiesen ER. Hypoglycaemia during pregnancy in women with Type 1 diabetes. Diabet Med 2012; 29:558-566
- ↑ RivielIo C, Mello G, Jovanovic LG. Breastfeeding and the basal insulin requirement in type 1 diabetic women. Endocr Pract 2009;15:187-193
- ↑ Joint British Diabetes Societies. The Hospital Management of Hypoglycaemia in Adults with Diabetes Mellitus, revised April 2021 Available at: https://abcd.care/sites/abcd.care/files/site_uploads/JBDS_01_Hypo_Guideline_FINAL_23042021_0.pdf (accessed April 2021)
- ↑ 31.0 31.1 Yale JF, Paty B, Senior PA. Hypoglycemia. Canadian journal of diabetes. 2018 Apr 1;42: S104-8
- ↑ American Diabetes Association. 7. Diabetes Technology: Standards of Medical Care in Diabetes-2021. Diabetes Care. 2021 Jan;44(Suppl 1): S85-99
- ↑ 33.0 33.1 American Diabetes Association. 6. Glycemic Targets: Standards of Medical Care in Diabetes—2021. Diabetes Care. 2021 Jan l;44(Supplement 1):S73-84
- ↑ Battelino T, Phillip M, Bratina N, Nimri R, Oskarsson P, Bolinder J. Effect of continuous glucose monitoring on hypoglycemia in type 1 diabetes. Diabetes Care 2011; 34:795-800
- ↑ Tamborlane WV, Beck RW, Bode BW, et al.; Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group. Continuous glucose monitoring and intensive treatment of type 1 diabetes. N Engl J Med 2008;359:1464-1476
- ↑ Beck RW, Hirsch IB, Laffel L, et al.; Juvenile Diabetes Research Foundation Continuous Glucose Monitoring Study Group. The effect of continuous glucose monitoring in well-controlled type 1 diabetes. Diabetes Care 2009; 32:1378- 1383
- ↑ 37.0 37.1 Heinemann L, Freckmann G, Ehrmann D, Faber-Heinemann G, Guerra S, Waldenmaier D, Hermanns N. Real-time continuous glucose monitoring in adults with type 1 diabetes and impaired hypoglycaemia awareness or severe hypoglycaemia treated with multiple daily insulin injections (HypoDE): a multicentre, randomised controlled trial.The Lancet. 2018 7;391(10128):1367- 77
- ↑ Beck RW, Riddlesworth T, Ruedy K, Ahmann A, Bergenstal R, Haller S, Kollman C, Kruger D, McGill JB, Polonsky W, Toschi E. Effect of continuous glucose monitoring on glycemic control in adults with type 1 diabetes using insulin injections: the DIAMOND randomized clinical trial. JAMA. 2017 Jan 24;317(4):371-8
- ↑ Dicembrini I, Mannucci E, Monami M, Pala L. Impact of technology on glycaemic control in type 2 diabetes: A meta-analysis of randomized trials on continuous glucose monitoring and continuous subcutaneous insulin infusion. Diabetes, Obesity and Metabolism. 2019;21(12):2619-25
- ↑ Bolinder J, Antuna R, Geelhoed-Duijvestijn P, Kroger J, Weitgasser R. Novel glucose-sensing technology and hypoglycae- mia in type 1 diabetes: a multicentre, non-masked, randomised controlled trial. The Lancet. 2016 5;388(10057):2254-63
- ↑ American Diabetes Association. 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Medical Care in Diabe- tes-2021. Diabetes Care. 2021 Jan;44(Suppl 1): 5111-124
- ↑ Monami, M., Marchionni, N., & Mannucci, E Long-acting insulin analogues versus NPH human insulin in type 2 diabetes: a meta-analysis. Diabetes research and clinical practice, 2008,81.2:184-189
- ↑ Monami M, Marchionni N, Mannucci E. Long-acting insulin analogues vs. NPH human insulin in type 1 diabetes meta-analy- sis. Diabetes Obes Metab 2009;! 1 (4):372-378
- ↑ Matsuhisa M, Koyama M, Cheng X, et al. New insulin glargine 300U/mL: glycemic control and hypoglycemia in Japanese people with T1DM (EDITIONJP1). Diabetes. 2014;63:LB22
- ↑ Yki-Jarvinen H, Bergenstal R, Ziemen M, et al. New insulin glargine 300 units/mL versus glargineTOO Units/mL in people with type 2 diabetes using oral agents and basal insulin: glucose control and hypoglycemia in a 6-month randomized con- trolled trial (EDITION2). Diabetes Care. 2014; 37:3235-3243
- ↑ Heller S, Buse J, Fisher M, et al. Insulin degludec, an ultra-long acting basal insulin, versus insulin glargine in basal-bolus treatment with meal-time insulin aspart in typeldiabetes (BEGIN Basal-Bolus Typel): a phase 3, randomised,open-label, treat- to-target non-inferiority trial.Lancet. 2012; 379:1489-1497
- ↑ Garber AJ, KingAB, DelPS, et al. Insulin degludec, an ultra-long acting basal insulin, versus insulin glargine in basal-bolus treatment with meal time insulin aspart in type 2 diabetes (BEGIN Basal-Bolus Type2): a phase 3, randomised, open-label, treat- to target on-inferiority trial. Lancet. 2012; 379:1498-1507
- ↑ Pedersen-Bjergaard U, Kristensen PL, Beck-Nielsen H, et al. Effect of insulin analogues on risk of severe hypoglycaemia in patients with type 1 diabetes prone to recurrent severe hypoglycaemia (HypoAna trial): a prospective, randomised, open-la- bel, blinded-endpoint crossover trial. Lancet Diabetes Endocrinol 2014;2(7):553-561
- ↑ Perreault L, Rodbard H, Valentine V, Johnson E. Optimizing Fixed-Ratio Combination Therapy in Type 2 Diabetes. Advances in therapy. 2019 Feb 1;36(2):265-77
- ↑ Blumer, I., & Clement, M.Type 2 Diabetes, Hypoglycemia, and Basal Insulins: Ongoing Challenges. Clinical Therapeutics, 2016 1;39(8):S1-1
- ↑ Gimenez M, Lara M, Conget I. Sustained efficacy of continuous subcutaneous insulin infusion in type 1 diabetes subjects with recurrent non-severe and severe hypoglycemia and hypoglycemia unawareness: a pilot study. Diabetes Technol Ther 2010;12(7):517-521
- ↑ 52.0 52.1 Pickup JC, Sutton AJ. Severe hypoglycaemia and glycaemic control in type 1 diabetes:metaanalysis of multiple daily insulin injections compared with continuous subcutaneous insulin infusion. Diabet Med 2008; 25:765-774
- ↑ Fatourechi MM, Kudva YC, Murad MH, Elamin MB, Tabini CC, Montori VM. Clinical review: Hypoglycemia with intensive in- sulin therapy: a systematic review and meta-analyses of randomized trials of continuous subcutaneous insulin infusion versus multiple daily injections. J Clin Endocrinol Metab 2009; 94:729-740
- ↑ Bergenstal RM, Klonoff DC, Garg SK, et al.; ASPIRE In-Home Study Group. Threshold-based insulin-pump interruption for reduction of hypoglycemia. N Engl J Med 2013; 369:224-232
- ↑ Little SA, Leelarathna L, Walkinshaw E, et al. Recovery of hypoglycemia awareness in long-standing type 1 diabetes: multi- center 2x2 factorial randomized controlled trial comparing insulin pump with multiple daily injections and continuous with conventional glucose self-monitoring (HypoCOMPaSS). Diabetes Care 2014;37(8):2114e22
- ↑ Bekiari E, Kitsios K, Thabit H, Tauschmann M, Athanasiadou E, Karagiannis T, Haidich AB, Hovorka R, Tsapas A. Artificial pan- creas treatment for outpatients with type 1 diabetes: systematic review and meta-analysis. bmj. 2018 Apr 18;361 :k1310
- ↑ Leitao, C. B., Tharavanij, T., Cure, P., Pileggi, A., Baidal, D. A., Ricordi, C., Alejandro, R. (2008). Restoration of hypoglycemia awareness after islet transplantation. Diabetes Care 2008;31(11):2113-2115
המידע שבדף זה נכתב על ידי
- ד"ר עפיף נח'לה, אנדוקרינולוג בכיר, המכון לאנדוקרינולוגיה סוכרת ומטבוליזם, רמב"ם - הקריה הרפואית לבריאות האדם, חיפה ומכבי שרותי בריאות
- פרופ׳ נעים שחאדה, מנהל מכון אנדוקרינולוגי, רמב"ם - הקריה הרפואית לבריאות האדם, חיפה
- פרופ׳ מיכה רפופורט, מנהל מחלקה פנימית ג׳ והשרות לסוכרת, המרכז הרפואי שמיר, צריפין


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק