המדריך לטיפול בסוכרת - כבד שומני - קשר לסוכרת מסוג 2 ודרכי טיפול - Fatty liver disease and type 2 diabetes - treatment methods
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| המדריך לטיפול בסוכרת | ||
|---|---|---|

| ||
| שם המחבר | ד"ר שירה זלבר-שגיא, ד"ר חני ישועה, פרופ' רן אורן | |
| שם הפרק | כבד השומני - הקשר לסוכרת מסוג 2 ודרכי טיפול | |
| מאת | המועצה הלאומית לסוכרת, משרד הבריאות |
|
| מועד הוצאה | 2013 | |
| מספר עמודים | 354 | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סוכרת, מחלת הכבד השומני
מחלת הכבד השומני שלא בגין צריכת אלכוהול הינה מחלת הכבד השכיחה ביותר בארצות המערב, כולל ישראל, עם המצאות המגיעה עד 30% באוכלוסיה הכללית[1]. המחלה מתאפיינת בהצטברות שומן בתאי הכבד (סטאטוזיס) בכמות החורגת מהכמות התקינה (שהינה עד 5%). השמנת יתר, היפרליפדמיה, תנגודת לאינסולין וסוכרת נמנים עם גורמי הסיכון העיקריים להופעת כבד שומני. בעוד שלפני מספר שנים נחשב הכבד השומני לממצא מקרי ללא משמעות קלינית, כיום ברור שכ-20%-10 מהסובלים מכבד שומני עלולים לפתח דלקת ופיברוזיס, מצב הנקרא NASH (Non-Alcoholic steato-Hepatitis) ומהם עלולים לפתח כ-5%-3 שחמת ואף הפטומה[2], [3], [4], [5].
בנוסף, כבד שומני נחשב כיום למרכיב הכבדי של הסינדרום המטבולי וכגורם סיכון מוקדם לסוכרת ולמחלת לב איסכמית.
הגורמים לכבד שומני
הגורמים ההתנהגותיים המעורבים בפתופיזיולוגיה של כבד שומני הם צריכת קלוריות מופרזת, הרכב תזונתי לקוי ואורח חיים יושבני. ברמה הביוכימית השחקנים העיקריים הם התנגודת לאינסולין, עלייה בשומן ויסצרלי ושינוי ביחס האדיפוציטוקינים עם עלייה ברמת הלפטין וירידה ברמת האדיפונקטין. הקשר החזק של NAFLD(Non Alcoholic Fatty Liver Disease) עם תנגודת לאינסולין ועם הסינדרום המטבולי תועד בהרחבה בספרות ויש ראיות לכך כי תנגודת לאינסולין קיימת גם בחולי NAFLD רזים ולא סוכרתיים[6], [7].
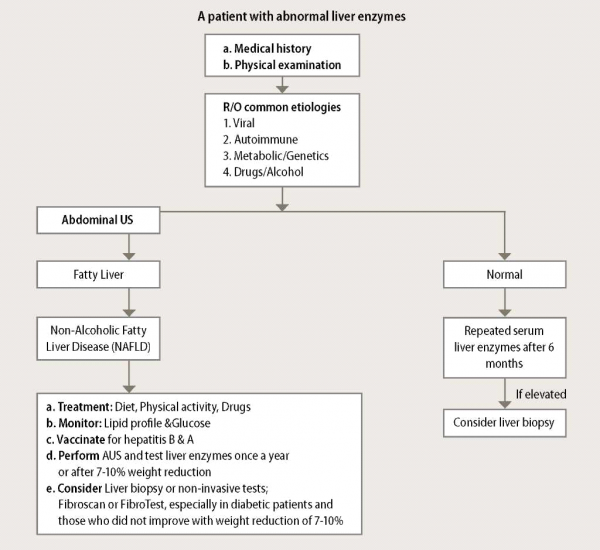
מאפיינים קליניים ואבחון של כבד שומני
רוב המקרים של כבד שומני מתגלים באקראי. מבחינת מעבדה, הפרעה באנזימי כבד מופיעה בכ-10% מהמטופלים עם כבד שומני ומתאפיינת בעליה קלה עד בינונית בטרנסאמינזות עם יחס AST/ALT של פחות מ-1 במקרים ללא פיברוזיס. תיתכן גם עלייה 2-GGT ובשכיחות נמוכה יותר גם בפוספטזה אלקלית. לא נמצא קשר בין רמת האנזימים לחומרת המחלה ההיסטולוגית[8].
במטופלים ללא הפרעה באנזימי כבד בהם התגלה כבד שומני באקראי בסונר והם אתסמינים מבחינת מחלות כבד וללא אנמנזה של צריכת אלכוהול מופרזת או נטילת תרופות היכולות לגרום לכבד שומני, ניתן להסיק שהסיבה לכבד שומני הינה מטבולית (קרי השמנת יתר, רמת סוכר גבוהה בצום, סכרת או דיסלפידמיה). במטופלים אלה אין מקום לבירור נוסף של הכבד עם הדמיה מתוחכמת יותר או ביופסיה. יש מקום לשקול לקיחת סרולוגיה להפטיטיס B C management of non-alcoholic[9]. אם קיימת הפרעה באנזימי כבד, האבחנה של כבד שומני תתבצע רק לאחר שלילת סיבות משניות אחרות להפרעה באנזימים כמקובל בספרות[10].
יש לשקול ביופסיה ב-2 מצבים, הראשון במטופלים בהם קיימת שאלה לגבי האבחנה -לדוגמא מטופלים עם הפרעה ניכרת באנזימים, עם טיטר גבוה של נוגדנים אוטואימוניים, או מטופלים ללא הפרעה מטבולית (רזה ,פרופיל שומנים תקין ,רמת סוכר תקינה). השני, במקרים בהם קיימת חשיבות קלינית להעריך את חומרת הפגיעה ההיסטולוגית בכבד. יש לציין שקיימים גם אמצעים לא חודרניים להעריך חומרת פגיעה כבדית כמו בדיקות דם מיוחדות ובדיקת פיברוסקאן[11].
יחסי הגומלין בין כבד שומני וסוכרת
גורמים המנבאים מעבר מסטאטוזיס פשוטה למצב דלקתי-פיברוטי בחולי כבד שומני לא אלכוהולי הינם: גיל מבוגר יותר, השמנת יתר, יחס ALT/AST גבוה מ-1 ונוכחות סוכרת[12]. Younossi מצא שכיחות גבוהה יותר של דלקת ופיברוזיס כבדי בחולים סוכרתיים עם כבד שומני, לעומת חולים ללא סוכרת עם כבד שומני. השכיחות של שחמת בחולים עם סוכרת וכבד שומני, הייתה 25%, לעומת 10% שכיחות של שחמת בחולים עם כבד שומני ללא סוכרת.
בנוסף, שיעורי התמותה מסיבות כבדיות היו גבוהים באופן משמעותי בחולי הסוכרת, לעומת חולים ללא סוכרת[13].
הסיבה לממצאים הקליניים וההיסטולוגים הקשים יותר בחולים סוכרתיים אינה ברורה, אך קשורה כנראה למצב דלקתי כרוני, עקה חמצונית ושחרור יתר של ציטוקינים הפטוטוקסיים. חולים עם סוכרת ומחלת כבד נמצאים גם בסיכון גבוה יותר להתפתחות סרטן כבד ראשוני[14].
יתרה מזאת, NAFLD הינו גורם סיכון לסיבוכים מטבוליים וסוכרת מסוג 2 [15] באופן עצמאי מגורמי סיכון ידועים אחרים. במטה אנליזה נראה כי כבד שומני מגביר את הסיכון למקרים חדשים של סוכרת פי 3.5[16]. ההסבר לכך הוא שהצטברות שומן בכבד מעכבת את הסיגנל לאינסולין בהפטוציטים וגורמת לתנגודת כבדית לאינסולין ולכן פוגעת בדיכוי ייצור גלוקוז אנדוגני (גלוקונאוגנזה).
כבד שומני כגורם סיכון למחלות לב
חשיבות כבד שומני בחולי סוכרת באה לידי ביטוי גם בהשלכות המטבוליות של כבד שומני על הגוף. מספר מחקרים אפידמיולוגים הראו כי כבד שומני הינו גורם סיכון עצמאי למחלה טרשתית בחולים עם סוכרת ובחולים ללא סוכרת. בסקר שכלל 3,166 מטופלים הסובלים מסוכרת, נמצאה שכיחות גבוהה יותר למחלת לב כלילית (26.6% לעומת 18.3%), מחלה צרברווסקולרית (20% לעומת 13%) ומחלת כלי דם היקפית (15.4% לעומת 10%) חולים הסובלים מסוכרת וכבד שומני לעומת חולים עם סוכרת בלבד[17]. במחקרים נוספים נמצאה עלייה בשכיחות פגיעה כלייתית ופגיעה עינית בחולי סוכרת עם כבד שומני לעומת חולי סוכרת ללא כבד שומני[18]. מחקרים נוספים תמכו בקשר בין כבד שומני להתפתחות מחלת לב. נראה כי פרופיל הליפידים הפרואתרוגני, הנפוץ בחולים עם כבד שומני, הוא אחד הגורמים האחראים לקשר למחלות לב. הסבר אפשרי לקשר בין כבד שומני לפרופיל לפידים אתרוגני הוא כי בתנגודת כבדית לאינסולין קיים ייצור כבדי מוגבר של טריגליצרידים וחלקיקי VLDL שמוביל באופן שניוני לרמות נמוכות של HDL ועלייה בצפיפות חלקיקי LDL-rn. הסברים נוספים לקשר בין כבד שומני ומחלות לב טמונים בכך שכבד שומני הינו מצב דלקתי תת קליני וכן בכך שכבד שומני מוביל להיפרגליקמיה ותנגודת לאינסולין. במטא-אנליזה נראה כי כבד שומני מגביר את הסיכון למקרים חדשים של מחלת לב פי 2[16].
טיפול
עיקר הטיפול מתמקד במניעה ובטיפול בגורמי הסיכון למחלה, כלומר: השמנה, תנגודת לאינסולין, היפררטריגליצרידמיה, איזון סוכרת או רמות גלוקוז מוגברות בצום (IFG) או מניעתם. וכן טיפול בגורמי הסיכון הנוספים למחלת לב כמו איזון כולסטרול אגרסיבי.
עד כה לא נמצא טיפול תרופתי שהוכח באופן חד משמעי במחקרים ושאומץ באופן גורף.
מאחר ששינוי אורח חיים הכולל ירידת משקל ופעילות גופנית נמצא יעיל בהפחתת גורמי הסיכון ל-NAFLD, הוא אומץ כטיפול המרכזי במחלה.
פעילות גופנית
ברוב המחקרים התצפיתיים נמצא קשר הפוך בין פעילות גופנית מדווחת או כושר קרדיו-רספירטורי לבין כמות שומן כבדי (2-CT או 2-MRS), באופן עצמאי מ-BMI[19], [20]. במחקר רחב היקף, דיווח עצמי על פעילות גופנית בעצימות גבוהה בלבד (כמו ריצה או שחייה) נמצאה כגורם מגן מפני NASH ופיברוזיס מתקדם בתקנון ל-BMI[21].
בשנים האחרונות נערכו כמה ניסויים קליניים, שהדגימו את השפעת אימון גופני מובנה על כבד שומני ואנזימי כבד. חולי NAFLD שקיבלו המלצה לפעילות גופנית אירובית (בעיקר הליכה) והוסיפו לפחות שעה בשבוע לפעילות היומית שלהם במשך שלושה חודשים, הורידו את רמות כל אנזימי הכבד (ALT, AST, GGT) באופן עצמאי משינוי במשקל[22]. בניסוי אחר נערכו אימוני אופניים 3 פעמים בשבוע במשך חודש שהובילו לירידה בשומן כבדי ב-21% ^MRS ללא שינוי במשקל או בדיאטה[23]. בשני ניסויים קליניים נוספים, האחד במתבגרים הסובלים מהשמנה[24] והשני בקשישים בריאים[25] נצפה שוב אפקט מיטיב של פעילות גופנית אירובית כאשר שניים עשר שבועות אימון הובילו לירידה בשומן בכ-35% מהשומן הכבדי. לאחרונה הודגם כי אימון התנגדות (מכשירים) בן 8 שבועות, 3 אימונים בשבוע, הוביל לירידת שומן בכבד ללא ירידת משקל[26].
תזונה
טיפול תזונתי מתבסס על הורדת כמות קלוריות (באנשים עם עודף משקל) ושינוי הרכב הדיאטה.
ירידה במשקל
קיימת הסכמה רחבה כי ירידת משקל מתונה של חצי קילו עד קילו בשבוע מסייעת בשיפור עד כדי רגרסיה מוחלטת של השומן בכבד, מסייעת ברגרסיה של דלקת ופיברוזיס, כמעט תמיד משפרת אנזימי כבד ולעיתים קרובות מביאה לנירמולם. בניסוי קליני בו נעשה שינוי באורחות חיים במשך שנה הודגם יחס מנה תגובה בין מידת ירידת המשקל ומידת הפחתה בשומן בכבד (2-MRS): ירידה של 5%-1 ממשקל הגוף הובילה לירידה של 33% מהשומן הכבדי בממוצע, ירידה של 10%-5 הובילה לירידת 65% שומן וירידת משקל של מעל 10% הובילה לירידת 80% מהשומן הכבדי[27].
בניסוי אחר שכלל אף הוא שינוי אורחות חיים במשך 12 חודשים, ירידת משקל של לפחות 7% מהמשקל ההתחלתי הובילה לשיפור היסטולוגי לא רק בשומן אלא גם בדלקת הכבדית (NASH histological activity score), אך לגבי פיברוזיס השינוי לא הגיע למובהקות סטטיסטית[28].
בניסוי אחר בו הושגה ירידת משקל של 10% בממוצע ממשקל הגוף, נצפה גם שיפור מובהק בפיברוזיס לאחר 6 חודשים. בכל המחקרים המוזכרים נעשתה דיאטה מתונה ומאוזנת לפי ההמלצות התזונתיות המקובלות ובשילוב עם פעילות גופנית מתונה[29]. בדף עמדה שפורסם לאחרונה על ידי האיגוד האירופאי לחקר הכבד, EASL, הומלצה ירידת משקל של 7% כטיפול ב-NAFLD/NASH[30].
שנוי הרכב הדיאטה
שינוי הרכב הדיאטה יכול לסייע בטיפול בכבד שומני גם ללא ירידת משקל. הודגם כי חולי NASH נוטים לאכול יותר שומן רווי וכולסטרול ופחות שומן בלתי רווי וסיבים, ויטמין C וטוקופרול[31]. בעבודה שנערכה בישראל נמצא כי חולי NAFLD צורכים באופן מובהק כמות גדולה יותר של משקאות קלים הממותקים בסוכר וכי צריכה מופרזת של בשר לסוגיו קשורה בסיכון מוגבר לכבד שומני, ללא קשר ל-BMI[32]. במספר עבודות הודגם כי חולים עם כבד שומני במשקל תקין צורכים יותר משקאות ממותקים לעומת ביקורות במשקל תקין וכי הקשר עצמאי מ-BMI[32]. יתירה מכך, במחקר רחב היקף הודגם כי צריכה יומית של משקאות מכילי פרוקטוז קשורה בסיכון מוגבר (פי 2.5) לפיברוזיס[33]. צריכת פרוקטוז מוגברת קשורה בסיכון להשמנה וסוכרת וידועה כמעודדת ליפוגנזה כבדית. לפיכך, נראה כי חולי NAFLD צריכים להגביל צריכת פרוקטוז או סירופ תירס עתיר פרוקטוז (High fructose corn syrup). הדרך הטובה ביותר לעשות זאת היא הגבלת צריכת משקאות קלים, מיצי פירות, מזון עשיר בסוכרוז (דו סוכר המורכב מגלוקוז ופרוקטוז) ומזון מעובד הממותק ב-Fructose corn syrup.
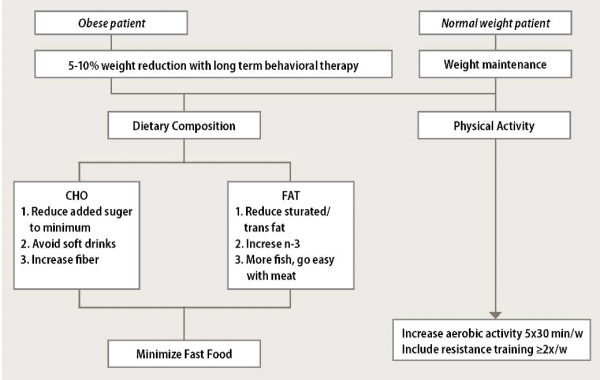
ההמלצות מבוססות הראיות לתזונה ופעילות גופנית בחולי NAFLD מסוכמות בגרף מספר 1.
ניתוחים בריאטריים
במטא-אנליזה נראה כי בעקבות ניתוח בריאטרי חל שיפור בכל המדדים ההיסטולוגיים של שומן, דלקת ופיברוזיס עד כדי רמיסיה מוחלטת, אך בסקירה של קוקרן נטען כי אין די ניסויים קליניים להערכת תועלת או נזק של ניתוחים בריאטריים כטיפול בחולי NASH. האיגוד האירופאי לחקר הכבד מסכם כי בחולים עם השמנה מורבידית יש לעודד ניתוחים בריאטריים בעיקר באלה עם NASH ופיברוזיס[30]. האיגוד האמריקאי לחקר הכבד מסכם כי אין קונטראינדיקציה לניתוח בריאטרי בחולי NAFLD או NASH, אך לגבי חולים שחמתיים אין די ריאיות לגבי בטיחות או יעילות הניתוח. וכן, מוקדם מידי להגדיר ניתוח בריאטרי כטיפול ספציפי ל-NASH [11].
אלכוהול וכבד שומני
להגדרת כבד שומני לא אלכוהולי יש לשלול ראשית צריכת אלכוהול נוכחית או מתמשכת של מעל 21 משקאות ממוצעים בשבוע לגבר ו-14 לאישה. חולי NAFLD צריכים להמנע מצריכת אלכוהול כבדה. למרות שקיימות ראיות שצריכה של פחות מכוס יין ביום קשורה בקשר הפוך לרמת אנזימי כבד ונזק היסטולוגי, אין מספיק מחקרים שעל פיהם ניתן לבסס המלצות לגבי שתיית אלכוהול במטופלים עם כבד שומני[11], [30].
תרופות אנטי סוכרתיות בשירות הכבד השומני
היות שבבסיס מנגנון הכבד השומני שאיננו על רקע אלכוהול קיימת עמידות לאינסולין, הרי שתרופות המורידות את התנגודת לאינסולין הינן מועמדות טבעיות לניסיון טיפולי במחלת הכבד השומני. מירב המחקרים בנושא מתמקדים במטפורמין (ביגואנידים) ובטיאזולידינדיונים.
ביגואנידים-מטפורמין
מטפורמין שייך למשפחת הביגואנידים והוא משפר את התנגודת הכבדית לאינסולין. מבחינת בטיחות השימוש מדובר בתרופה בטוחה, כאשר עד היום דווח על מקרה בודד של דלקת כבד חריפה בחולה עם סוכרת. התרופה לא ניתנת באי ספיקת כבד קשה, אי ספיקת לב קשה ובחולים עם הפרעה בתפקודי כליה.
במחקרים על בני אדם התוצאות שנויות במחלוקת מבחינת הורדת אנזימי כבד ומבחינת שיפור היסטולוגי[34]. נכון להיום אין המלצה להשתמש באופן שגרתי במטפורמין במטופלים עם כבד שומני ללא סוכרת.
גליטזונים-תיאזולידנידיונים (Thiazolidninediones)
הגליטזונים הינם קבוצת תרופות המעלות רגישות לאינסולין בתאי שומן פריפריים[5]. התרופות במשפחה זו פועלות כאגוניסטים של Peroxisone-Proliferator Activated Receptor-Gammappar-Y. התרופות הנמצאות היום בשוק הן רוזיגליטזון (Rosiglitazone) ופיוגליטזון (Pioglitazone).
- רוזיגליטזון
למרות שהתרופה גורמת לשיפור ברגישות לאינסולין וירידה של אנזימי כבד, כמות שומן בכבד ודלקת כבדית, לא נצפה שיפור בדרגת הצלקת בכבד בחולים עם כבד שומני עם או ללא סוכרת. הארכת משך הטיפול משנה לשלוש שנים לא שיפרה את התוצאות וסוכם כי ללא שינוי באורחות חיים הטיפול התרופתי לא יוביל לשנוי משמעותי[35]. עובדה זו רומזת שטיפול בעמידות לאינסולין אינו מספיק בחולים עם כבד שומני.
מקובל להיזהר במתן גליטזונים במטופלים סוכרתיים עם עלייה באנזימי כבד ואף קיימת התווית-נגד לטפול במטופלים עם טרנסאמינאזות מעל פי 3 מהערך העליון של הנורמה[36]. יש לציין שלאחרונה פוחת מאוד השימוש בתרופה והיא בשלבי הוצאה מהשוק עקב שאלות שעלו בקשר לבטיחותה הקרדיווסקולרית.
- פיוגליטזון
בניסוי קליני אקראי מבוקר רחב היקף שכלל מתן פיוגליטזון במינון של 30 מ"ג ליום לתקופה של 96 שבועות ל-247 מטופלים עם כבד שומני ללא סוכרת, נראתה ירידה ברמות אנזימי כבד ורמת שומן בכבד עם שיפור בחלק מהמרכיבים הדלקתיים ללא שיפור ברמת הפיברוזיס הכבדי. ההנחיה של איגוד הכבד האמריקאי היא לתת פיוגליטזון לחולים עם NASH שהוכח בביופסיה. יש להדגיש שרוב המחקרים שחקרו מתן פיוגליטזון בחולים עם NASH היו בחולים ללא סוכרת ובעלי טווחי זמן קצרים[37].
תרופות אנטי סוכרתיות אחרות - Exenatide) GLP-1 Agonist)
אקסנטיד הינו אגוניסט של קולטני 1-GLP ופעולתו העיקרית היא על שחרור אינסולין מתאי ביתא בלבלב. בעכברי מעבדה הוא הפחית כמות שומן בכבד ובניסוי קליני לא מבוקר בבני אדם שיפר רמות ALT [38], אך עדיין אין ראיות מספקות לתועלתו בטיפול בכבד שומני.
טיפולים תרופתיים אחרים
ויטמין E
מספר מחקרים בדקו לאחרונה השפעת ויטמין E במינונים גבוהים במטופלים עם כבד שומני ללא סוכרת. נמצא שתוספת ויטמין E קשור לירידה ברמת אנזימי כבד בחולים עם NASH, עם שיפור ברמת השומן בכבד ושיפור במדדי הדלקת ללא שיפור מדדי הצלקת. הבעיה היא שעצם השימוש בוויטמין E במינונים גבוהים שנוי במחלוקת עקב עדויות לגבי קשר בין צריכתו לעלייה בתמותה. נכון להיום ההמלצה של האגוד האמריקאי לחקר הכבד היא לתת ויטמין E במינון של 800 יחידות ליום בחולים לא סוכרתיים עם NASH שהוכח בביופסיה. אין המלצה למתן ויטמין E בחולים עם סוכרת וNASH[11].
אומגה 3
בחמישה ניסויים קליניים קטנים, רובם בהקצאה אקראית, בהם בדקו השפעת תוסף אומגה 3 במינון של 3-1 גרם ביום במשך 12-6 חודשים, נצפתה ירידת ALT ושיפור בכבד שומני כפי שנראה באולטרסאונד. ברוב המקרים לא נבדקה היסטולוגיות כבד ולכן לא ניתן ללמוד על שינוי ברמת הדלקת או הפיברוזיס.
נכון להיום, ההמלצה היא לתת אומגה 3 בחולים עם כבד שומני והיפרטריגלצרידמיה בלבד[11].
סטטינים
אין התווית נגד למתן סטטינים בחולים עם כבד שומני. הטיפול בדיסליפדמיה יינתן בהתאם לשקלול מכלול גורמי הסיכון למחלת לב של המטופל.
סיכום
הגישה הטיפולית בחולה הסוכרתי עם כבד שומני מתבססת על איתור וטיפול מיטבי במרכיבים נוספים של התסמונת המטבולית, איתור וטיפול בגורמי סיכון לבביים נוספים, הערכת חומרת המחלה הכבדית מבחינת נוכחות פיברוזיס, שחמת או הפטומה ע"י מעקב קבוע הכולל סונר ובדיקת אלפה פטו פרוטאין, טיפול בסטאטוזיס עצמו ע"י שינוי אורחות חיים וכמובן איזון הסוכרת עם העדפה למטפורמין וגליטזונים. ההמלצות מבוססות הראיות לתזונה ופעילות גופנית בחולי NAFLD מסוכמות בגרף מספר 2.
חשוב לזכור - הקשר בין כבד שומני לסוכרת מסוג 2 ודרכי טיפול
- שכיחות מחלת הכבד השומני שאינה בגין צריכת אלכוהול מגיעה עד 75% מכלל החולים הסוכרתיים.
- היארעות סוכרת באנשים עם כבד שומני גבוהה יותר מאשר באוכלוסייה דומה מבחינת גיל וגורמי סיכון מקובלים אחרים.
- סוכרת נחשבת כיום כגורם סיכון להופעת דלקת ופיברוזיס כבדי בחולים עם כבד שומני. השכיחות של שחמת בחולים עם כבד שומני וסוכרת הינה 25% לעומת 0%ו בחולים עם כבד שומני ללא סוכרת.
- הסיכוי של חולה סוכרת עם כבד שומני למות מכל סיבה שהיא היא פי 2.2 מאשר חולה סוכרתי ללא כבד שומני.
- עצם הנוכחות של כבד שומני בחולה סוכרת חושף אותו לסיכון מוגבר למחלת לב כלילית, ללא קשר למרכיבי הסינדרום המטבולי.
- סוכרת קשה יותר בחולים עם סוכרת וכבד שומני הן מבחינת הכבד והן מבחינת סיבוכים מאקרו ומיקרווסקולריים.
- כל הערכה של מטופל עם סוכרת וכבד שומני צריכה לכלול הערכה של הפגיעה הכבדית והערכה כללית של מצב קרדיומטבולי.
- שינוי באורחות חיים הוא אבן היסוד לטיפול בכבד שומני.
ביבליוגרפיה
- ↑ Zelber-Sagi S, Nitzan-Kaluski D, Halpern Z, Oren R. Prevalence of primary non-alcoholic fatty liver disease in a population-based study and its association with biochemical and anthropometric measures. Liver Int. 2006 Sep;26(7):856-63.
- ↑ Mendez-Sanchez N, Arrese M, Zamora-Valdes D, Uribe M. Current concepts in the pathogenesis of nonalcoholic fatty liver disease. Liver Int. 2007 May;27(4):423-33.
- ↑ Hashimoto E, Yatsuji S, Tobari M, Taniai M, Torii N, Tokushige K, et al. Hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. J Gastroenterol. 2009;44 Suppl 19:89-95.
- ↑ Matteoni CA, Younossi ZM, Gramlich T, Boparai N, Liu YC, McCullough AJ. Nonalcoholic fatty liver disease: a spectrum of clinical and pathological severity. Gastroenterology. 1999 Jun;116(6):1413-9.
- ↑ 5.0 5.1 Bugianesi E, Leone N, Vanni E, Marchesini G, Brunello F, Carucci P, et al. Expanding the natural history of nonalcoholic steato-hepatitis: from cryptogenic cirrhosis to hepatocellular carcinoma. Gastroenterology. 2002 Jul;123(1):134-40.
- ↑ Kim CH, Younossi ZM. Nonalcoholic fatty liver disease: a manifestation of the metabolic syndrome. Cleve Clin J Med. 2008 Oct;75(10):721-8.
- ↑ Marchesini G, Bugianesi E, Forlani G, Cerrelli F, Lenzi M, Manini R, et al. Nonalcoholic fatty liver, steatohepatitis, and the metabolic syndrome. Hepatology. 2003 Apr;37(4):917-23.
- ↑ Vernon G, Baranova A, Younossi ZM. Systematic review: the epidemiology and natural history of non-alcoholic fatty liver disease and non-alcoholic steatohepatitis in adults. Aliment Pharmacol Ther. Aug;34(3):274-85.
- ↑ Ramesh S, Sanyal AJ. Evaluation and management of non-alcoholic steatohepatitis. J Hepatol. 2005;42 Suppl(1):S2-12.
- ↑ Pratt DS, Kaplan MM. Evaluation of abnormal liver-enzyme results in asymptomatic patients. N Engl J Med. 2000 Apr 27;342(17):1266-71.
- ↑ 11.0 11.1 11.2 11.3 11.4 Chalasani N, Younossi Z, Lavine JE, Diehl AM, Brunt EM, Cusi K, et al. The diagnosis and management of non-alcoholic fatty liver disease: Practice Guideline by the American Association for the Study of Liver Diseases, American College of Gastroenter-ology, and the American Gastroenterological Association. Hepatology. 2012 Jun;55(6):2005-23.
- ↑ Angulo P, Keach JC, Batts KP, Lindor KD. Independent predictors of liver fibrosis in patients with nonalcoholic steatohepati-tis. Hepatology. 1999 Dec;30(6):1356-62.
- ↑ Younossi ZM, Gramlich T, Matteoni CA, Boparai N, McCullough AJ. Nonalcoholic fatty liver disease in patients with type 2 diabetes. Clin Gastroenterol Hepatol. 2004 Mar;2(3):262-5.
- ↑ Bugianesi E, Vanni E, Marchesini G. NASH and the risk of cirrhosis and hepatocellular carcinoma in type 2 diabetes. Curr Diab Rep. 2007 Jun;7(3):175-80.
- ↑ Fan JG, Li F, Cai XB, Peng YD, Ao QH, Gao Y. Effects of nonalcoholic fatty liver disease on the development of metabolic disorders. J Gastroenterol Hepatol. 2007 Jul;22(7):1086-91.
- ↑ 16.0 16.1 Musso G, Gambino R, Cassader M, Pagano G. Meta-analysis: natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of non-invasive tests for liver disease severity. Ann Med. 2011 Dec;43(8):617-49.
- ↑ Targher G, Bertolini L, Padovani R, Rodella S, Tessari R, Zenari L, et al. Prevalence of nonalcoholic fatty liver disease and its association with cardiovascular disease among type 2 diabetic patients. Diabetes Care. 2007 May;30(5):1212-8.
- ↑ Targher G, Bertolini L, Rodella S, Zoppini G, Lippi G, Day C, et al. Non-alcoholic fatty liver disease is independently associ¬ated with an increased prevalence of chronic kidney disease and proliferative/laser-treated retinopathy in type 2 diabetic patients. Diabetologia. 2008 Mar;51(3):444-50.
- ↑ Magkos F. Exercise and fat accumulation in the human liver. Curr Opin Lipidol. Dec;21(6):507-17.
- ↑ Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Zvibel I, Goldiner I, et al. Role of leisure-time physical activity in nonalcoholic fatty liver disease: a population-based study. Hepatology. 2008 Dec;48(6):1791-8.
- ↑ Kistler KD, Brunt EM, Clark JM, Diehl AM, Sallis JF, Schwimmer JB. Physical activity recommendations, exercise intensity, and histological severity of nonalcoholic fatty liver disease. Am J Gastroenterol. 2011 Mar;106(3):460-8; quiz 9.
- ↑ St George A, Bauman A, Johnston A, Farrell G, Chey T, George J. Independent effects of physical activity in patients with nonalcoholic fatty liver disease. Hepatology. 2009 Jul;50(1):68-76.
- ↑ Johnson NA, Sachinwalla T, Walton DW, Smith K, Armstrong A, Thompson MW, et al. Aerobic exercise training reduces hepatic and visceral lipids in obese individuals without weight loss. Hepatology. 2009 Oct;50(4):1105-12.
- ↑ van der Heijden GJ, Wang ZJ, Chu ZD, Sauer PJ, Haymond MW, Rodriguez LM, et al. A 12-week aerobic exercise program re¬duces hepatic fat accumulation and insulin resistance in obese, Hispanic adolescents. Obesity (Silver Spring). Feb;18(2):384-90.
- ↑ Finucane FM, Sharp SJ, Purslow LR, Horton K, Horton J, Savage DB, et al. The effects of aerobic exercise on metabolic risk, insulin sensitivity and intrahepatic lipid in healthy older people from the Hertfordshire Cohort Study: a randomised controlled trial. Diabetologia. Apr;53(4):624-31.
- ↑ Hallsworth K, Fattakhova G, Hollingsworth KG, Thoma C, Moore S, Taylor R, et al. Resistance exercise reduces liver fat and its mediators in non-alcoholic fatty liver disease independent of weight loss. Gut. Sep;60(9):1278-83.
- ↑ Lazo M, Solga SF, Horska A, Bonekamp S, Diehl AM, Brancati FL, et al. The Effect of a 12-Month Intensive Lifestyle Interven¬tion on Hepatic Steatosis in Adults with type 2 Diabetes. Diabetes Care. 2010 Jul 27.
- ↑ romrat K, Kleiner DE, Niemeier HM, Jackvony E, Kearns M, Wands JR, et al. Randomized controlled trial testing the effects of weight loss on nonalcoholic steatohepatitis. Hepatology. 2010 Jan;51(1):121-9.
- ↑ Vilar Gomez E, Rodriguez De Miranda A, Gra Oramas B, Arus Soler E, Llanio Navarro R, Calzadilla Bertot L, et al. Clinical trial: a nutritional supplement Viusid, in combination with diet and exercise, in patients with nonalcoholic fatty liver disease. Ali¬ment Pharmacol Ther. 2009 Nov 15;30(10):999-1009.
- ↑ 30.0 30.1 30.2 Ratziu V, Bellentani S, Cortez-Pinto H, Day C, Marchesini G. A position statement on NAFLD/NASH based on the EASL 2009 special conference. J Hepatol. 2010 Aug;53(2):372-84.
- ↑ Musso G, Gambino R, De Michieli F, Cassader M, Rizzetto M, Durazzo M, et al. Dietary habits and their relations to insulin resistance and postprandial lipemia in nonalcoholic steatohepatitis. Hepatology. 2003 Apr;37(4):909-16.
- ↑ 32.0 32.1 Zelber-Sagi S, Nitzan-Kaluski D, Goldsmith R, Webb M, Blendis L, Halpern Z, et al. Long term nutritional intake and the risk for non-alcoholic fatty liver disease (NAFLD): a population based study. J Hepatol. 2007 Nov;47(5):711-7.
- ↑ Abdelmalek MF, Suzuki A, Guy C, Unalp-Arida A, Colvin R, Johnson RJ, et al. Increased fructose consumption is associated with fibrosis severity in patients with nonalcoholic fatty liver disease. Hepatology. 2010 Jun;51(6):1961-71.
- ↑ הערה34
- ↑ Ratziu V, Giral P, Jacqueminet S, Charlotte F, Hartemann-Heurtier A, Serfaty L, et al. Rosiglitazone for nonalcoholic steato-hepatitis: one-year results of the randomized placebo-controlled Fatty Liver Improvement with Rosiglitazone Therapy (FLIRT) Trial. Gastroenterology. 2008 Jul;135(1):100-10.
- ↑ Chalasani N, Teal E, Hall SD. Effect of rosiglitazone on serum liver biochemistries in diabetic patients with normal and elevated baseline liver enzymes. Am J Gastroenterol. 2005 Jun;100(6):1317-21.
- ↑ Sanyal AJ, Chalasani N, Kowdley KV, McCullough A, Diehl AM, Bass NM, et al. Pioglitazone, vitamin E, or placebo for nonal¬coholic steatohepatitis. N Engl J Med. May 6;362(18):1675-85.
- ↑ Stein LL, Dong MH, Loomba R. Insulin sensitizers in nonalcoholic fatty liver disease and steatohepatitis: Current status. Adv Ther. 2009 Oct;26(10):893-907.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי
ד"ר שירה זלבר-שגיא, דיאטנית קלינית ואפידמיולוגית, המכון למחלות דרכי העיכול והכבד, המרכז הרפואי תל-אביב ובית הספר לבריאות הציבור, אוניברסיטת חיפה
ד"ר חני ישועה, המכון למחלות דרכי העיכול והכבד, המרכז הרפואי תל-אביב ושרותי בריאות כללית, המחלקה לרפואת משפחה, מחוז תל-אביב יפו
פרופ׳ רן אורן, המכון לגסטרואנטרולוגיה ומחלות כבד, המרכז הרפואי אוניברסיטאי הדסה, ירושלים'


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק