המדריך לטיפול בסוכרת - מטפורמין - היבטים חדשים בתרופה ותיקה - New aspects of metformin
המדריך לטיפול בסוכרת
מאת המועצה הלאומית לסוכרת, משרד הבריאות. עורכים מדעיים: ד"ר עופרי מוסנזון, פרופ׳ איתמר רז
| המדריך לטיפול בסוכרת | ||
|---|---|---|

| ||
| שם המחבר | ד"ר יוסי כהן | |
| שם הפרק | מטפורמין - היבטים חדשים בתרופה ותיקה | |
| עורך מדעי | פרופסור איתמר רז | |
| מאת | המועצה הלאומית לסוכרת, משרד הבריאות |
|
| מועד הוצאה | 2022 | |
| מספר עמודים | 614 | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – מטפורמין, טיפול תרופתי בסוכרת
התרופה Metformin מקובלת בתרופת קו ראשון בטיפול בסוכרת מסוג 2. מעמדה לא השתנה מאז המחצית השנייה של המאה ה-20, למרות פיתוחן של תרופות חשובות נוספות. הודות ליעילותה, בטיחותה ומחירה הזול היא בשימוש של כ-150 מיליון חולי סוכרת ברחבי העולם. מטפורמין משפרת את רמת הגליקמיה בסוכרת בעיקר על ידי דיכוי תהליך הניאוגלוקוגנזה בכבד והעלאת הרגישות לאינסולין ברקמות. למרות שנים רבות של מחקר, עדיין רב הנסתר על אופן פעולתה. קיימים חילוקי דעות ונושאים במחלוקת באשר למנגנון הפעולה, בעיקר בנוגע לתפקידו של האנזים AMPK (Activated Protein Kinase). מאמר זה יסקור בעיקר את התקדמות הידע הנוגע לפעילות התרופה כטיפול בסוכרת וכן את מקומה בטיפול במחלות נוספות.
מטפורמין - קו טיפולי ראשון בחולי סוכרת
מטפורמין הוכיחה עצמה לאורך תקופה ארוכה מאוד כיעילה בטיפול בסוכרת מסוג 2. ראשיתה כתרופה עממית. כבר בימי הביניים נחשב הצמח Galega officinalis (תמונה 1) ובשמו העברי "הלילך הצרפתי" (או "צער העיזים") לבעל תכונות אנטי-דיאבטיות. מחקר שנערך בשנת 1918 מצא שהחומר Guanidine הנמצא בצמח זה בשפע ורעיל לבני אדם, הוא בעל פעילות היפוגליקמית. בשנת 1929 הצליחו לייצר במעבדה על בסיס החומר האמור שתי תרכובות המכילות Dimethyl Biguanide שאינן רעילות, התרופות פנפורמין ומטפורמין. פנפורמק הראתה יעילות רבה יותר כתרופה אנטי-דיאבטית אך הוצאה משימוש בשנות ה-70 של המאה הקודמת בגלל היארעות מקרים של חמצת לקטית. לגבי מטפורמין, במשך 60 שנות שימוש בה נמצאה התרופה בטוחה עם תופעות לוואי מעטות שאינן חמורות, בעיקר במערכת העיכול. היארעות של חמצת לקטית משימוש בתרופה במינון המקובל היא תופעה יוצאת דופן, המוערכת ב-3 מקרים ל-100,000 מטופלים בשנה. מטפורמין היא התרופה היחידה המומלצת כקו ראשון לטיפול בסוכרת מסוג 2 על ידי האיגודים המקצועיים המובילים ברחבי העולם ובאוכלוסיות שונות. כמו כן התרופה היא בעלת פעילות סינרגטית משלימה עם מגוון תרופות נוספות לסוכרת ומאושרת לשילוב עם כל סוגי התרופות הקיימות, כולל אינסולין. כל התרופות האוראליות שפותחו מאז מפנה המאה ה-21 נבדקו במחקרים קליניים מבוקרים בשילוב מטפורמין והוכיחו העצמת יעילות לעומת יעילותן כתרופה יחידה. נמצאים שלובים מוכנים מראש במינון משתנה של מטפורמין עם Pioglitazone, תרופות ממשפחת 4-DPP (Depeptil Peptidase 4 Inhibitor) ותרופות ממשפחת SGLT2 (Sodium Glucose Transporter inhibitor). קיימים גם שילובים עם תרופות ממשפחת הסלפונילאוריאה. מקובל לשלב מטפורמין גם עם אינסולין בסיסי או בטיפול מורכב ולהוסיפו לתרופות ממשפחת 1-GLP (Glucagon Like Peptide 1).
מנגנון הפעילות
סוכרת מסוג 2 מהווה כ-90 אחוזים מכלל מקרי הסוכרת בעולם. יצור מוגבר של גלוקוז בכבד הוא מרכיב חשוב בפתוגנזה של המחלה והסיבה העיקרית לרמות סוכר גבוהות בצום בסוכרתיים מסוג זה. ניתן לקבוע כמעט בוודאות שהטיפול במטפורמין מדכא את ייצור הגלוקוז בכבד בתהליך הנאוגלוקוגנזה. במחקרים בחולי סוכרת מסוג 2 נמצא שמטפורמין מפחית את הפרשת הגלוקוז מהכבד בכ-37 אחוזים. מחקר אחר בסוכרתיים הראה ייצור כמעט כפול של גלוקוז בכבד בתהליך הנאוגלוקוגנזה[1] לעומת אנשים בריאים. מתן מטפורמין באותם נבדקים הפחית ב-33 אחוזים תהליך זה. מחקר בבעלי חיים, אחד מני רבים, הוכיח הפחתה של 60 אחוזים בייצור גלוקוז בכבד באמצעות מטפורמין. מחקרים אחרים שנעשו "In vivo" ובתרביות תאי כבד חזרו והוכיחו שעיקר פעילות המטפורמין היא בדיכוי תהליך הנאוגלוקוגנזה.
האם מטפורמין מדכא את יצור הגלוקוז בכבד דרך מנגנון הפעולה של AMPK
AMP-activated protein kinase הוא אנזים ממשפחת הקיאנז החיוני לתהליך ההומאוסטאזיס בתא במגוון רקמות כולל הכבד, המוח ושרירי השלד. מחקרים רבים שנערכו בשנים אחרונות הדגישו את פעולתו כמווסת עיקרי בפעילות התא בהיותו אחראי על האיזון האנרגטי של התאים בהתאם לשינויים בריכוזי Adenosine Mono Phosphate\Adenosine Di Phosphate) AMP\ADP) בהתחשב בכמות ה-ATP (Adenosine Tri Phosphate). ה-AMPK נכנס לפעולה כאשר הפעילות האנרגטית של התא פוחתת. בפעולתו הוא משחלף תהליכים אנאבוליים תלויי ATP לתהליכים קטבוליים יצרני ATP, על ידי זירוז בהחדרת הגלוקוז ושפעולו בתא בנוסף לחמצון של חומצות שומן, תוך סיוע לדיכוי היצור מחדש של הגלוקוז בכבד. היות שתהליך הנאוגלוקוגנזה הוא תהליך תלוי אנרגיה, דהיינו, לצורך סינתזה של מולקולת גלוקוז אחת מלקטט או פירובט נדרשות 4 מולקולות של ATP, הפחתה של רמת ה-ATP התוך תאי על ידי פעולת המטפורמין תגרום להאטת התהליך[2][3][4]. לאחר ספיגתה בתאי המעי מגיעה התרופה ישירות לכבד דרך המערכת הפורטלית, כך שבכבד ימצא ריכוז רב יותר של התרופה מאשר באיברים אחרים בגוף. התרופה אינה עוברת ביו-טרנספורמציה ומופרשת ברובה דרך הכליות.
פעילות המטפורמין באופן עקיף על ידי הגברת הרגישות לאינסולין ברקמת השריר והשומן
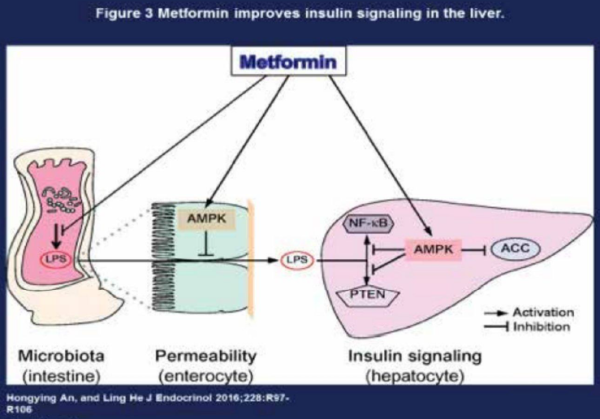
בנוסף לעיקר פעילות המטפורמין בכבד באמצעות דיכוי ייצור הגלוקוז, נמצא שלתרופה יש השפעה בהגברת הרגישות לאינסולין ברקמות השריר והשומן. האם תופעה זו נובעת באופן עקיף כתוצאה מהפחתת רמות סוכר הדם על ידי פעילותה בכבד, או שקיימים מנגנונים ישירים או עקיפים אחרים, לדוגמה: פעילות המטפורמין על הרכב החיידקים במעי (מיקרוביוטה). באדם שמן יש שוני בהרכב המיקרוביוטה במעי בהשוואה לאדם רזה[5]. במודלים של בעלי חיים נמצא קשר בין השמנה לבין הרכב החיידקים במעי. ייצור ליפו-פוליסאקרידים (רעלנים, Lipopolysaccharide ,LPS) במעי תלוי בהרכב המיקרוביוטה. כפי הנראה יש לחומרים אלה חשיבות במידת התנגודת לאינסולין[6][7]. מחקרים עדכניים בבעלי חיים הראו כי למטפורמין השפעה על הרכב החיידקים במעי וייצור LPS. בנוסף, התרופה משפיעה גם על הפעלת האנזים AMPK ברירית המעי. לאנזים יש חשיבות בהגנה על שלמות הרירית במעי ומניעת מעבר של רעלנים למחזור הדם.
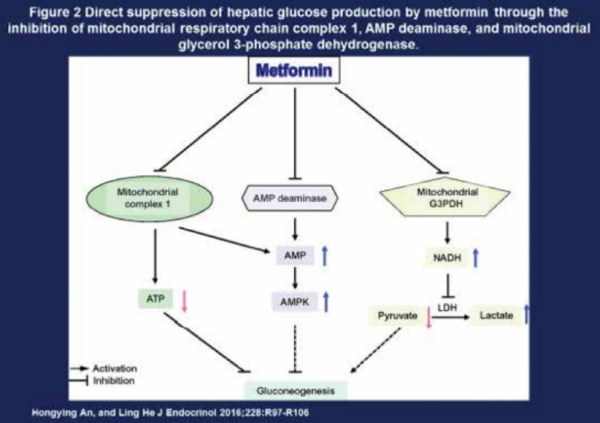
לסיכום: במינון המרבי של 2.5 גרם ליום, מטפורמין אמור לפעול במספר אתרים בגוף במנגנונים שונים באופן ישיר ועקיף ובסופו של תהליך להוריד את רמת הגליקמיה בחולי סוכרת מסוג 2. כתרופה פומית, מטפורמין תתחיל לפעול במעי בשינוי הרכב המיקרוביוטה והפעלת האנזים AMPK השומר על שלמות הרירית במעי ומניעת זליגת LPS למחזור הדם. הפחתה בכמות LPS במחזור הדם בעיקר במערכת הפורטלית ומכאן בכבד עשויה להפחית גם את התנגודת לפעולת האינסולין בכבד (תמונה 3) וברקמת השריר. בהגיעה לכבד, מעכבת התרופה את תהליך הנאוגלוקוגנזה באמצעות הפעלת האנזים AMPK בתאי הכבד. מנגנון נוסף שלא נידון בהרחבה הוא השפעת התרופה על רמת ATP במנגנון הדיכוי של שרשרת הנשימה המיטוכונדריאלית תוך שינוי היחס AMP\ATP, כך שפחות מולקולות של ATP נדרשות לנאוגלוקוגנזה[8], (תמונה 2). למרות כל הנאמר, מנגנון פעילות התרופה אינו נהיר דיו גם מסקירה של מחקרים רבים החל בתרביות תאים, בבעלי חיים ובבני אדם וחסרים עדיין המיקום המדויק אליו נקשרת התרופה לאנזים AMPK כמו גם פרטים מדויקים יותר לגבי אופן פעולתה בהפחתת התנגודת לאינסולין. קיימות ציפיות רבות להרחבת הידע בתחום זה בשנים הקרובות.
מקומה של התרופה בסוכרת מסוג 1
קיימות המלצות של מספר גופים מקצועיים לתוספת מטפורמין לסוכרתיים שמנים מסוג 1 במטרה לשפר את איזון הסוכרת ולצמצם את מינוני האינסולין ובכך לגרום לירידה במשקל. המלצות אלו מתבססות על מספר קטן של מחקרים קליניים. המחקר הנחשב לחשוב והמקיף העוסק בתוספת מטפורמין בסוכרת מסוג 1 למבוגרים שמנים הוא REMOVA (Reducing with Metformin Vascular Adverse lesion)[9][10]. המחקר בדק את השפעת התרופה על הגליקמיה והמשקל וניסה לאמוד סיכון קרדיווסקולרי. מחקר חשוב נוסף שבדק את יעילות התרופה הוא EXCHANGE. בשני המחקרים נמצאה ירידה מתונה ברמות HbA1c למשך זמן קצר. ההשפעה המטיבה פגה במעקב של 6 חודשים. במחקר REMOVL נמצאה ירידה מתונה ברמות ה-LDL כולסטרול ובמשקל במעקב של 3 שנים בסוכרתיים מסוג 1 שמנים בגילאי הביניים. ההשפעה הקרדיווסקולרית נבדקה באמצעות אומדן התעבות דופן בעורקי הצוואר (Carotid artery intima-media thickness). הבדיקה לא הראתה תוצאות חד משמעיות במטופלי מטפורמין. לדאבוננו לא ייתכנו מחקרי תוצאים כפי שנעשה בתרופות החדשות בסוכרת מסוג 2 בהיעדר עניין לתעשיית התרופות.
לסיכום: בחולי סוכרת מסוג 1 שמנים תוספת מטפורמין עשויה להפחית מינוני אינסולין במידת מה וייתכן שלבלום עלייה במשקל. יש לשקול תועלת מול תוספת תרופה שאינה נטולת תופעות לוואי.
מקומה של התרופה במחלות נוספות
השפעת התרופה על המערכת הקרדיווסקולרית
מחלות קרדיווסקולריות קשורות, ללא ספק, לסוכרת מסוג 2 ומהוות את הסיבה העיקרית לתחלואה ולתמותה במחלה זו. בטיחותן של התרופות לסוכרת בהקשר למערכת הקרדיווסקולרית מהווה את אחד המרכיבים החשובים בטיפול במחלה. מחקרים מרובי משתתפים, ארוכי טווח ועתירי ממון התנהלו ומתנהלים, בעיקר בעידודה וביוזמתה של תעשיית התרופות. מאז שנת 2008 מחויבות תרופות חדשות לסוכרת, על פי הוראת הגופים הרגולטורים, להוכיח בטיחות קרדיווסקולרית. במחקר UKPDS (UK Prospective Diabetes Study) ומחקרי המשך[11][9] נמצא שמטופלי מטפורמין (זרוע קטנה יחסית במחקר) הפחיתו באופן משמעותי - ב-36 אחוזים את סך כל התמותה וב-39 אחוזים את התמותה הקשורה מסיבוכי מחלת הסוכרת. נמצאה גם הפחתה משמעותית בהיארעות אוטם שריר הלב שנשמרה במעקב של 10 שנים, מחקרים נוספים אשרו את בטיחותה הקרדיווסקולרית של התרופה וחלקם הראו אף עליונות בהשוואה לתרופות אנטי-דיאבטיות אחרות. בעבר, אי ספיקת לב שימשה התווית-נגד לטיפול במטפורמין מחשש לחמצת לקטית אך המגמה התהפכה: התרופה מאושרת ואף מומלצת לחולי סוכרת הסובלים גם מאי ספיקת לב[12]. נדרשים מחקרים מבוקרים מול תרופות פומיות ממשפחות SGLT2 ו-DPP-4 כדי לאשר את בטיחותה ויתרונותיה הקרדיווסקולריים אך ספק רב אם אכן יתקיימו מחקרים מעין אלה בהיעדר עניין כלכלי לתעשיית התרופות.
השפעות אנטי נאופלסטיות של התרופה
תצפיות קליניות ואפידמיולוגיות תרמו להתעניינות רבה באשר להשפעתה של התרופה במניעה או בטיפול במחלת הסרטן. בשנת 2005 הוצגו לראשונה נתונים[13][14] מתוך מחקרים אפידמיולוגיים רטרוספקטיביים, שייחסו לסוכרתיים מטופלי מטפורמין היארעות פחותה של מחלת הסרטן לעומת מטופלים בתרופות אחרות. מחקרים נוספים הציגו נתונים דומים ולעומתם אחרים לא תמכו באותן מסקנות. הנושא שנוי במחלוקת בעיקר מהטעם שמדובר בעבודות פרמקו/אפידמיולוגיות רטרוספקטיביות בחולי סוכרת. בעבודות שנעשו "In vitro" נמצאה השפעה ממתנת על החלוקה המהירה של תאים סרטניים ממקור שונה. ההשפעה מיוחסת למנגנון הפעולה המוכר של התרופה, דהיינו, באמצעות הפעלת האנזים AMPK. בהיעדר מחקר קליני השוואתי של המטפורמין לעומת תרופות אחרות או בשילובה בפרוטוקולים טיפוליים קיימים, נכון להיום אין תשובות מוכחות והשפעתה החיובית במחלת הסרטן נותרת בגדר השערה.
השפעת התרופה בטיפול בתסמונת השחלות הפוליציסטיות (Poly-Cystic Ovary Syndrome)
תסמונת השחלות הפוליציסטיות היא הפרעה אנדוקרינולוגית שכיחה ביותר. שכיחותה מוערכת ב-4–8 אחוזים מהנשים. התרופה מטפורמין נתפסה באופן לוגי כטיפול ראוי במחלה, בעיקר כאמצעי לדיכוי היפר-אינסולינמיה שנחשבה בזמנו כגורם מרכזי בפתוגנזה של המחלה. מחקרים ראשוניים שנערכו בשנות ה-90 של המאה הקודמת הראו תוצאות מעודדות באשר ליעילות התרופה בהסדרת המחזור, הפחתת רמות האנדרוגנים בדם והפחתת משקל. בחלוף הזמן הותירו מחקרים קליניים מבוקרים את מעמדה כשנוי במחלוקת. נכון להיום, בעיקר בגלל ההטרוגניות הרבה של המחלה וחוסר אחידות באבחון, מטפורמין אינה מהווה תחליף לאורח חיים בריא בעיקר בנשים הסובלות גם מהשמנה המלווה את התסמונת[15][16]. באשר להשפעת התרופה על סיבוכים ארוכי טווח של המחלה, התפתחות סוכרת ומחלות לב וכלי דם בעיקר, אין מספיק מידע וידרשו מחקרים ארוכי טווח להוכיח זאת.
סיכום
לאחר כמעט 60 שנות ניסיון קליני בתרופה, יעילותה האנטי-דיאבטית אינה מוטלת בספק. בטיחותה ומחירה הזול מחזקים את מעמדה כתרופת הבחירה הראשונה לטיפול בסוכרת מסוג 2. מנגנון פעילותה בדיכוי תהליך הייצור מחדש של גלוקוז בכבד הובהר בצורה ברורה, מקומו של האנזים AMPK בתהליך זוכה לחיזוק רב במחקרים עדכניים ומנגנונים נוספים נמצאים בשלבים שונים של מחקר. בטיחותה הקרדיווסקולרית של התרופה עדיין אינה ברורה די הצורך בעיקר בהיעדר השוואתיות לדור החדש של התרופות שכבר עברו מחקרי תוצאים קרדיווסקולריים. השפעתה של התרופה במחלות נאופלסטיות מעוררת עניין רב, אך עדיין חסרת הוכחות.
השאלות שעדיין לא זכו למענה:
- מדוע התרופה מאבדת מיעילותה עם התמשכות המחלה?
- מדוע קיימים הבדלים משמעותיים ביעילותה בין חולים שונים?
- מהי השפעתה בשילוב התרופות החדשות לסוכרת לאורך זמן ומהם השילובים המומלצים יותר מבחינת יעילות, תופעות לוואי, יתרונות קרדיווסקולריים ואחרים?
- מהו הזמן הנכון להתערב בשילובי התרופה עם תרופות נוספות במהלך המחלה?
- האם נכון ורצוי להתחיל שימוש בתרופה כבר בשלב של טרום סוכרת, ואם כן מי החולה המתאים?
- האם המידע העדכני לגבי השפעת התרופה על חיידקי המעי הוא רלוונטי לשימוש קליני בחולי סוכרת ואולי אף במניעת המחלה?
- האם לתרופה יש השפעה מיטבה לאורך זמן על איזון הסוכרת, מניעת עלייה במשקל והסיבוכים הקרדיווסקולריים בסוכרתיים שמנים מסוג 1?
- מהו סף התפקוד של הכליות בו ניתן עדיין להשתמש בתרופה מבלי לסכן את המטופל בחמצת לקטית?
חשוב לזכור - מטפורמין: היבטים חדשים בתרופה ותיקה
- לתרופה מטפורמין יש 60 שנות ניסיון קליני. יעילותה האנטידיאבטית, בטיחותה ומחירה הזול מחזקים את מעמדה כתרופת הבחירה הראשונה לטיפול בסוכרת מסוג 2
- מנגנון פעולתה בדיכוי תהליך היצור מחדש של גלוקוז בכבד הובהר די הצורך ומתחזק ממחקר עדכני. שפעול האנזים AMPK זוכה לחיזוק רב במחקרים עדכניים, מנגנונים נוספים נמצאים בשלבים שונים של מחקר
- פעילות התרופה בהגברת הרגישות לאינסולין ברקמות השריר, השומן והכבד נקשרת גם לפעולתה על הרכב החיידקים במעי ובמעבר רעלנים דרך תאי המעי
- בטיחותה הקרדיווסקולרית של התרופה צברה די הוכחות, חסרה השוואה לדור החדש של התרופות שכבר עברו מחקרי תוצאים קרדיווסקולריים
- השפעתה של התרופה על מחלות נאו-פלסטיות עדיין חסרה הוכחה
ביבליוגרפיה
- ↑ Hundal RS, Krssak M, DufourS, Laurent D, Lebon V, Chandramouli V, Inzucchi SE, Schumann WC, Petersen KF, Landau BR, et al. Mechanism by which metformin reduces glucose production in type 2 diabetes. Diabetes. 2000;49:2063-2069.
- ↑ Cao J, Meng SM, Chang E, Beckwith-Fickas K, Xiong LS, Cole RN, Radovick S, Wondisford FE, He L. Low Concentrations of Metformin Suppress Glucose Production in Hepatocytes through AMP-activated Protein Kinase (AMPK) Journal of Biological Chemistry. 2014;289:20435-20446.
- ↑ Chen L, Jiao ZH, Zheng LS, Zhang YY, Xie ST, Wang ZX, Wu JW. Structural insight into the autoinhibition mechanism of AMP-activated protein kinase. Nature. 2009;459:1l46-U1139.
- ↑ Cheng JT, Huang CC, Liu IM, Tzeng TF, Chang CJ. Novel mechanism for plasma glucose-lowering action of metformin in streptozotocin-induced diabetic rats. Diabetes. 2006;55:819-825.
- ↑ Ley RE, Backhed F, Turnbaugh P, Lozupone CA, Knight RD, Gordon JI. Obesity alters gut microbial ecology. Proceedings of the National Academy of Sciences of the United States of America. 2005; 102:11070-11075.
- ↑ Cani PD, Amar J, Iglesias MA, Poggi M, Knauf C, Bastelica D, Neyrinck AM, Fava F, Tuohy KM, Chabo C, et al. Metabolic endo- toxemia initiates obesity and insulin resistance. Diabetes. 2007;56:1761-1766.
- ↑ Cani PD, Bibiloni R, Knauf C, Waget A, Neyrinck AM, Delzenne NM, Burcelin R. Changes in gut microbiota control metabolic endotoxemia-induced inflammation in high-fat diet-induced obesity and diabetes in mice. Diabetes. 2008;57:1470-1481.
- ↑ El-Mir MY, Nogueira V, Fontaine E, Averet N, Rigoulet M, Leverve X. Dimethylbiguanide inhibits cell respiration via an indirect effect targeted on the respiratory chain complex I. Journal of Biological Chemistry. 2000; 275:223-228.
- ↑ 9.0 9.1 Diabetes Care 1996; 19:182-183.
- ↑ Holman R Metformin as First Choice in oral Diabetes Treatment: the UKPDS experience. Journ Annu Diabetol Hotel Dieu 2007;13:13-20
- ↑ Turner RC, Cull CA, Holman RR. U.K. Prospective Diabetes Study
- ↑ Inzucchi SE, Bergenstal RM, Buse JB, Diamant M, Ferrannini E, Nauck M, Peters AL, Tsapas A, Wender R, Matthews DR. Man- agement of hyperglycaemia in type 2 diabetes: a patient-centered approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia. 2012; 55:1577-1596.
- ↑ Evans JMM, Donnelly LA, Emslie-Smith AM, Alessi DR, Morris AD. Metformin and reduced risk of cancer in diabetic patients. Br Med J. 2005; 330:1304-1305. [PubMed: 15849206]
- ↑ Inzucchi SE, Maggs DG, Spollett GR, Page SL, Rife FS, Walton V, Shulman Gl. Efficacy and metabolic effects of metformin and troglitazone in type II diabetes mellitus. New England Journal of Medicine. 1998; 338:867-872.
- ↑ Ding T, et al. BMJ Open 2016;6. doi:l0.1136/bmjopen-2016-012461
- ↑ Balen AH, Conway GS, Homburg R, et al. Polycystic ovary syndrome: a guide to clinical management. UK: Taylor & Francis, 2005.
- Creely SJ, McTernan PG, Kusminski CM, Fisher fM, Da Silva NF, Khanolkar M, Evans M, Harte AL, Kumar S. Lipopolysaccharide activates an innate immune system response in human adipose tissue in obesity and type 2 diabetes. Am J Physiol Endocrinol Metab. 2007;292:E740-747.
- Hardie DG, Ross FA, Hawley SA. AMPK: a nutrient and energy sensor that maintains energy homeostasis. Nature Reviews Molecular Cell Biology. 2012; 13:251-262.
- Inzucchi SE, Bergenstal RM, Buse JB, Diamant M, Ferrannini E, Nauck M, Peters AL,Tsapas A, Wender R, Matthews DR. Man- agement of hyperglycaemia in type 2 diabetes: a patient-centered approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia. 2012; 55:1577-1596.
- Landman GWD, Kleefstra N, van Hateren KJJ, Groenier KH, Gans ROB, Bilo HJG. Metformin Associated With Lower Cancer Mortality in Type 2 Diabetes - ZODIAC-16. Diabetes Care. 2010; 33:322-326.
- Ley RE, Turnbaugh PJ, Klein S, Gordon JI. Microbial ecology - Human gut microbes associated with obesity. Nature. 2006; 444:1022-1023.
- Inzucchi SE, Maggs DG, Spollett GR, Page SL, Rife FS, Walton V, Shulman GL Efficacy and metabolic effects of metformin and troglitazone in type II diabetes mellitus. New England Journal of Medicine. 1998; 338:867-872
- Petrie JR, Chaturvedi N, Ford I et al (2017) Metformin in adults with type 1 diabetes: design and methods of reducing with metfor-min vascular adverse lesions (REMOVAL): an international multicentre trial. Diabetes Obes Metab 19:509-516.
- Petrie JR, Chaturvedi N, Ford I et al (2017) Cardiovascular and metabolic effects of metformin in patients with type 1 diabe- tes (REMOVAL): a double-blind, randomised, placebo-controlled trial. Lancet Diabetes Endocrinol. doi:!0.10l6/S22l3-8.
המידע שבדף זה נכתב על ידי ד"ר יוסי כהן, מנהל מכון סוכרת, מכבי שירותי בריאות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק