הערכה מעבדתית והתנהלות בתרחיש של אריתרוציטוזיס (פוליציטמיה)
| מדריך בדיקות מעבדה | |
| הערכה מעבדתית והתנהלות בתרחיש של אריתרוציטוזיס (פוליציטמיה) | |
|---|---|
| מעבדה | המטולוגיה |
| תחום | התרחיש של polycytemia vera |
| יוצר הערך | פרופ' בן-עמי סלע |
פוליציטמיה הוא מצב בו ההמטוקריט ו/או רמת ההמוגלובין מוגברים בדם ההיקפי. מצב זה יכול להתרחש או כתוצאה מהגדלת מספר האריתרוציטים (פוליציטמיה מוחלטת) או כתוצאה מירידה בנפח הפלזמה (פוליציטמיה יחסית). הטיפול הדחוף במקרי פוליציטמיה (כגון צמיגות-יתר ויצירת פקקות) הוא בניקוז דם (phlebotomy), תהליך שיכול להתנהל באופן תקופתי וקבוע להורדת ההמטוקריט. תרופות המוגדרות כ-myelosuppressive, כגון hydroxyurea משמשות לעיתים בהתנהלות ארוכת-טווח של פוליציטמיה (Spivak ב-Blood משנת 2019).
פוליציטמיה מוחלטת: היצירה המוגברת של אריתרוציטים יכולה לנבוע מתהליך ראשוני במח העצם הידוע כתסמונת מיאלו-פרוליפרטיבית, או שהיא יכולה להופיע כתגובה לרמות חמצן נמוכות באופן כרוני, או לעיתים נדירות כתוצאה ממאירות. לחלופין, תוספת של אריתרוציטים יכולה להתרחש לאחר עירוי מנות-דם, או כתוצאה מסימום דם או blood doping (תהליך בלתי חוקי של הוצאת דם מגופו של אתלט והזרקתו מחדש לתוך הגוף לפני השתתפותו בתחרות ספורט), או בתרחיש של העוּבּר מבין תאומים המקבל את דמו מהעובר השני (מה שידוע כ-twin-to-twin transfusion syndrome).
פוליציטמיה ראשונית: סוג זה של פוליציטמיה נובע מגורמים אינטרינזיים המשפיעים על תאים קודמנים טרם הפיכתם לאריתרוציטים בשלים. מצבים של polycythemia vera (להלן PV), polycythemia rubra vera (להלן (PRV או תרחיש של erythemia, נובעים מאנומליות של מח העצם. לעיתים מוצאים יצירת יתר סימולטנית של אריתרוציטים ושל טסיות-דם. PV מוגדרת מחלה מיאלו-פרוליפרטיבית. תסמיניה כוללים כאבי-ראש ו-vertigo, ובבדיקה גופנית מתגלים טחול או כבד מוגדלים. לעיתים מטופלים עם PV סובלים מיתר לחץ-דם או מיצירת פקקות. הסמן המעבדתי הבולט ביותר הוא המטוקריט מוגדל (מעל 55%) שמוצאים ב-83% מהחולים (Wallach ב- Curr Med Diagn Treat משנת 2008). מוטציה סוֹמטית (לא מוּרשת) המוגדרת כ-V617F בגן JAK2, זוהתה ב-95% ממקרי PV. פוליציטמיה משפחתית ראשונית, הידועה גם כ- congenital polycythemia primary familial (להלן (PFCP, היא תרחיש תורשתי טב, בניגוד לשינויים המיאלו-פרוליפרטיביים שמוצאים ב-PV. במשפחות רבות, PFCP נגרם כתוצאה ממוטציה אוטוזומלית דומיננטית בגן EPOR המקודד לקולטן של erythropoietin. PFCP יכול לגרום לעלייה של עד 50% ביכולת נשיאת החמצן של הדם (Ang ב-Nat Genet משנת 2002).
פוליציטמיה שניונית: סוג זה של פוליציטמיה נגרם על ידי עליות טבעיות או מלאכותיות ביצירת erythropoietin הגורמות ליצירה מוגברת של אריתרוציטים. בפוליציטמיה שניונית יכולים למנות 6 עד 8 מיליון, ולעיתים אף 9 מיליון אריתרוציטים/ממ"ק. יש המכנים סוג זה של פוליציטמיה- "פיזיולוגית", והיא יכולה להיגרם מהסיבות הבאות:
- תלות בשהייה באזורים הרריים גבוהים (Altitude related)-הנגרמת מהסתגלות נורמלית למגורים או שהייה בגובה רב. אתלטים רבים מתאמנים בגבהים ליהנות מיתרון זה, מה שעלול להיחשב לצורה חוקית של doping. אכן ידועה התופעה של אתלטים אפריקניים החיים ומתאמנים בגבהים, ושליטתם בריצות הארוכות
- מצבים היפוקסיים - במחלת לב ציאנוטית כאשר ריכוזי החמצן בדם יורדים משמעותית, כתוצאה ממחלת ריאות היפוקסית כגון COPD או כתוצאה מתרחישים כרוניים את קוצר נשימה בשינה (sleep apnea).
- מצבים יאטרוגניים - מצבים כגון phlebotomy (הקזת דם)
- סיבות גנטיות - מצבים של מחלת המוגלובין שאינו "משחרר" חמצן כראוי, כגון Hb Chesapeake, שזיקתו לחמצן גדולה יותר מזו של המוגלובין תקין. כך פוחתת הובלת חמצן לכליות, מה שמביא ליצירה מוגברת של erythropoietin ולפוליציטמיה. המוגלובין Kempsey הוא בעל תכונות דומות, אך שני האחרונים אינם שכיחים.
פוליציטמיה יחסית: זהו מצב עם עלייה במספר האריתרוציטים בדם הנובע מירידה בנפח הדם (hypovolemia). מצב זה מתרחש על ידי ירידה בנוזלי הגוף כמו במצבי כוויה, התייבשות ועקה. מצב ספציפי של פוליציטמיה יחסית הוא תסמונת Gaisböck המתרחשת בעיקר בנשים מאוד שמנות בהן יתר לחץ-דם גורם לירידה בנפח הפלזמה וממילא לעלייה יחסית במספר האריתרוציטים.
מצבים בהם פוליציטמיה שניונית אינה נגרמת על ידי התאמה פיזיולוגית, והיא מתרחשת באופן בלתי תלוי בצרכים של הגוף, כוללים: ממאירויות כגון renal cell carcinoma או סרטן הכבד, מחלת von Hipple-Lindau ואי סדירות אנדוקרינית כגון פאוכרומוציטומה, אדנומה של האדרנל ותסמונת Cushing. מצב אחר הוא של אנשים שרמת הטסטוסטרון שלהם גבוהה כתוצאה משימוש בסטרואידים אנאבוליים, או ספורטאים העושים שימוש אסור ב-erythropoietin.
מצבים נוספים הם של שינויים בחישה של חמצן: מוטציות מורשות בשלושה גנים הגורמות להגברת היציבות של גורמים המשרים היפוקסיה, מה שמגביר יצירת erythropoietin ולאריתרופויזיס. ביניהם ניתן למנות פוליציטמיה ע"ש Chuvash שהיא צורה אוטוזומלית רצסיבית של אריתרופויאזיס שהיא אנדמית ברפובליקת Chuvash ברוסיה. מוטציה זו כרוכה בהומוזיגוטיות של מוטציית C598T בגן von Hipple-Lindau (להלן VHL) החיוני להרס הגורמים המשרים היפוקסיה בנוכחות חמצן (Perrotta וחב' ב-Blood משנת 2006). מקבצים של אנשים עם פוליציטמיה ע"ש Chuvash נמצאו גם באי האיטלקי Ischia הנמצא במפרץ נאפולי (Percy וחב' ב-Proc Natl Acad Sci USA משנת 2006). צורה אחרת היא PHD2 erythropoiesis שהיא הטרוזיגוטיות של מוטציות Loss-of-Function בגן PHD2 והן כרוכות באריתרופויאזה אוטוזומלית-דומיננטית והגברת הפעילות של הגורמים המשרים היפוקסיה (Percy וחב' ב-Blood משנת 2007, ו-Percy וחב' ב-N Eng J Med משנת 2008). עוד צורה היא של HIF2α erythropoiesis הנגרמת ממוטציות Gain-of-Function בגן HIF2α, וכרוכה באריתרופויאזה אוטוזומלית-דומיננטית (Gail וחב' ב-Blood משנת 2008), וביתר לחץ-דם ריאתי (Stefanini וחב' ב-Angiology משנת 1978).
המוטציה ב-JAK2
מוטציה בגן המקודד ל-Janus kinase 2 היא המקור הסביר ביותר לפתוגנזה של PV, כיוון ש-JAK2 מעורב ישירות באיתות התוך-תאי המלווה את החשיפה לציטוקינים להם רגישים תאי ה-progenitor של PV (על פי James וחב' ב-Nature משנת 2005). מוטציות ב-JAK2 מוצאים גם במחלות פרוליפרטיביות אחרות כגון תרומבוציטמיה ומיאלופיברוזיס אידיופתית. המוטציה V617F מובילה לאיתות קבוע של קולטני הציטוקינים הרלוונטיים (Kralovics וחב' ב-Blood משנת 2005, Levine וחב' ב-Cancer Cell משנת 2005, Guglielmelli וחב' ב-Hematologica משנת 2009, ו- Mustjoki וחב' ב-Leuk Res משנת 2009). מוטציה זו מופיעה בלמעלה מ-95% של אלה עם PV, וב-50-60% מאלה עם תרומבוציטמיה ומיאלופיברוזיס אידיופתית (Vannucchi ב-Hematologica משנת 2017). דימום ופקקת שכיחים במצבי PV כתוצאה מפגיעה במנגנונים המוסטאטיים מהסיבות הבאות:
- עלייה במספר האריתרוציטים
- עלייה במספר טסיות הדם
יש ממצאים על התפקיד של tissue factor ושל לויקוציטים פולי-מורפו-נוקלאריים (PMLs) כאשר פני הטסיות תורמים לריאקציות קואגולציה התלויות בפוספוליפידים. Tissue factor מסונתז על ידי לויקוציטים ורמת פקטור זה עולה באלה עם מחלה מיאלו-פרוליפרטיבית מה שעלול לתרום ליצירת פקקת.
היפר-הומוציסטינמיה גם הוא גורם סיכון לפקקת, ואף הוא שכיח באלה עם מחלה מיאלו-פרוליפרטיבית, ומופיע ב-56% מאלה עם PV. תסמונת von Willebrand נרכשת היא גורם מוכר לדימום באלה עם 12-15% מתוך אלה PV.
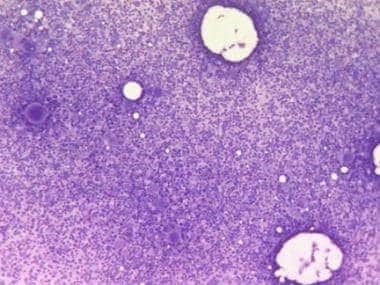
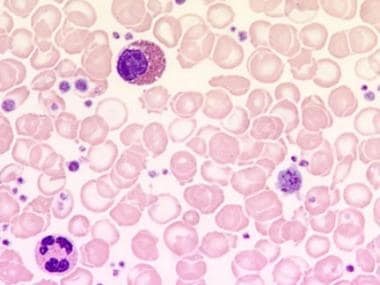
אם המוטציה V617F ב-JAK2 חסרה, אך רמת אריתרופויאטין נמוכה, בדיקת אקסונים 12 ו-13 של JAK2 חיונית ויכולה לסייע באבחון של PV ב-2-3% מאלה עם PV שהם שליליים למוטציה האמורה. מטופלים שנמצאים שליליים למוטציות ב-JAK2, ורמות אריתרפויאטין בהם נורמליות או אף גבוהות, הם בעלי אריתרוציטוזיס שניונית. בדיקת JAK2 מבוצעת במטופלים ללא סיבה ברורה ל-PV. בחינת בסיס של אריתרופויאזיס כוללת משטח-דם לבחינת אפשרות של מחלה מיאלו-פרוליפרטיבית כגון בזופיליה, בדיקת ferritin בנסיוב שכן חסר ברזל עלול למסך את דרגת האריתרוציטוזיס, ובדיקת פרופילים של כבד וכליות כדי לזהות מחלת כבד או כליות לא מאובחנת שעלולה לגרום לאריתרציטוזיס. אולטרה-סאונד של הבטן מבוצע לעיתים קרובות לגילוי טחול מוגדל, שמוצאים ב-2/3 מאלה עם PV, שכן לא תמיד ניתן לגלות טחול מוגדל על ידי מישוש (Messinezy וחב' ב-Br J Haematol משנת 1997). אם JAK2 מתקבל שלילי, מדידת אריתרופויאטין בנסיוב עשויה לעזור. רמת EPO נמוכה מצביעה על מחלת מח-עצם ראשונית, ומחייבת בדיקה של מוטציה באקסון 12 של JAK2, שמוצאים ב-2% מאלה עם PV.
פתו-פיזיולוגיה של PV
PV ותרומבוציטמיה הם סוגים שכיחים של מפגעים מיאלו-פרוליפרטיביים, כאשר פריצות-דרך עדכניות בהבנת האטיולוגיה המולקולרית של מפגעים אלה, לא היו מלוות בהערכה אפידמיולוגית מדויקת של שכיחותן. מחקר שנערך ב-Connecticut בשנת 2003 מצא 22 מקרים של PV ל-100,000 ב-Connecticut, ו-65,243 מקרי PV בכל ארצות הברית באותה שנה. ל-PV אין העדפה מגדרית, אם כי אחוז הגברים הלוקים בה גדול במעט ביחס לנשים. הגיל בו מתגלית המחלה באופן בולט יותר הוא 50–70 שנה, אך היא מופיעה גם באופן נדיר יותר גם בילדים צעירים.
Polycytemia vera או PV נובעת ממפגע פן-היפרפלסטי, נאופלסטי או ממאיר של מח העצם. בתרחיש מלווה גם על ידי עלייה מיאלואידית במספר הכדוריות הלבנות ומגקריוציטית במספר טסיות הדם, כאשר כל אלה נובעים משבט (clone) אנורמלי של תאי גזע המטו-פויאטיים, עם רגישות מוגברת לגורמי גדילה שונים לצורך בשלותם (Berlin ב-Semin Hematol משנת 1975, Landolfi ב-Curr Opin Hematol משנת 1998, ו-Streiff וחב' ב-Blood משנת 2002). התסמינים של PV הנובעים מירידה בהובלת חמצן בדם צמיג ו"בּוֹצי" כוללים כאבי ראש, תחושות טשטוש, ורטיגו, טנטון, הפרעות ראייה, תעוקת חזה (angina pectoris) וצליעה לסירוגין (intermittent claudication). סיבוכי דימום המופיעים ב-1% ממקרי PV, כוללים דימום מהנחיר או מחלל האף (epistaxis), דימומי חניכיים, דימום במערכת העיכול ו-ecchymosis (דֶּמֶם כִּתְמִי שהוא כתם דימום תת-עורי שקוטרו גדול מסנטימטר אחד). סיבוכים פקקתיים ב-1% ממקרי PV כוללים פקקת ורידית או עורקית הכרוכה בשבץ-מוחי, ותסחיף פקקתי. בדיקה פיזיקלית יכולה לאתר טחול מוגדל ב-75% ממקרי PV, כבד מוגדל ב-30% מהמקרים, יתר לחץ דם ו-plethora (גודש יתר; עודף של נוזלים בגוף, בעיקר של דם).
כאבי בטן עלולים להופיע ב-PV כתוצאה מכיב פפטי, כיוון ש-PV כרוכה ברמות היסטמין מוגברות, בחמציות מוגברת של הקיבה או אף בתסמונת Budd-Chiari (או פקקת בווריד שער הכבד) או בפקקת הווריד המזנטרי. איבוד משקל יכול לנבוע מתחושת שובע מוקדמת. תחושת גרד נובעת מהפרשה מוגברת של היסטמין ממספר מוגבר של בזופילים ותאי פיטום (mast cells) ועלולה להופיע -40% מאלה עם PV.
מח העצם של אלה עם PV מכיל תאי גזע תקינים, אך מכיל גם תאי גזע שבטיים אנומליים המפריעים או מדכאים את הגידול של תאי הגזע ובשלותם. ראיות מצביעות על כך שהאטיולוגיה של ה-panmyelosis נעוצה בשגשוג נאופלסטי בלתי סדיר. לויקוציטוזיס עלול להיות גורם סיכון לפקקת (Berk וחב' ב-Semin Hematol משנת 1986, Weinfeld וחב' ב-Eur J Hematol משנת 1994, ו-Fruchtman וחב' ב-Semin Hematol משנת 1997). בניסוי CYTO-PV נמצא שהסיכון לפקקת גדל במטופלים עם ספירת כדוריות-דם לבנות מעל 7,000 לויקוציטים/מיקרוליטר, כאשר מספרם הגיע ל-11,000 תאים למיקרוליטר ומעלה, הסיכון לפקקת גדל פי-3.9 (Barbui וחב' ב-Blood משנת 2015).
במשפחות רבות PFCP או Primary familial and congenital polycythemia, נגרם ממוטציות אוטוזומליות-דומיננטיות בגן המקודד לקולטן של אריתרופויאטין (EPOR). PFCP יכול לגרום לעלייה של עד 50% ביכולת נשיאת החמצן של הדם.
האבחון של PV
על פי ההנחיות המעודכנות של WHO משנת 2016, אבחון של PV דורש קיום של שלושת הקריטריונים העיקריים או לפחות שני קריטריונים עיקריים וקריטריון משני אחד (Arber וחב' ב-Blood משנת 2016): קריטריונים עיקריים על פי WHO כוללים:
- רמת המוגלובין גבוהה מ-17.5 גרם/דציליטר בגברים או מעל 16.5 גרם/דציליטר בנשים, או המטוקריט הגבוה מ-50% בגברים, או מעל 48% בנשים, או מסת אריתרוציטים הגבוהה ב-25% מעל הערך הנורמלי
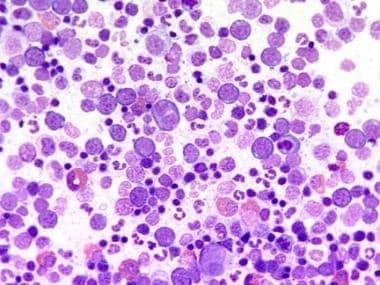
- ביופסיית מח עצם המראה תאיות-יתר (hypercellularity) ביחס לגיל הנבדק, עם גדילה מוגברת של שלוש שורות התאים (panmyelosis) הכוללת שגשוג מוגבר אריתרואידי, גרנולוציטי ומגקריוציטי עם מגקריוציטים פלאומורפיים בשלים
- נוכחות מוטציית JAK2V617F או מוטציה באקסון 12 של JAK2. הקריטריון המשני על פי WHO היא רמה נמוכה של EPO מתחת תחום הנורמה
מחקרים ציטוגנטיים מראים קריוטיפ לא נורמלי בתאי הפרוגניטור ההמאטופויאטיים בערך ב-34% ממקרי PV, בתלות באיזה שלב בוצעה הבדיקה. לפיכך, ב-20% המקרים מוצאים אנומליה ציטוגנטית בשלב מוקדם של אבחון המחלה, כאשר 10 שנים לאחר מכן מוצאים אנומליה זו ב-80% מהבדיקות. אנומליות גנטיות ב-PV הן כדלקמן: שֶמֶט (deletion) של 20q (ב-8.4% מהמקרים), שמט של 13q (ב-3%), trisomy של כרומוזום 8 (ב-7%), trisomy של כרומוזום 9 (ב-7%), trisomy של 1q (ב-4%), שמט של 5q או מונוזומיה 5 (ב-3%), שמט של 7q או מונוזומיה 7 (ב-1%). אנליזה של ביטוי גני בתאי +CD34 בדם ההיקפי של 19 מטופלים עם PV, מצאה מספר כפול של גנים משודרגים או מדוכאים גברים כמו גם בנשים. בהמשך מצאו אותם חוקרים 102 גנים עם רגולציה דיפרנציאלית שהיו תואמים בין גברים ונשים, ושניתן בעזרתם לחלק את המטופלים ל-2 קבוצות פנוטיפיות עם שוֹנוּת משמעותית במשך המחלה, תסמיניה והפרוגנוזה שלה (Spivak וחב' ב-N Eng J Med משנת 2014).
הקריטריונים לאבחון PV הוגדרו בשנות ה-70. עם הכנסת שיטת PCR המאפשרת גילוי מוטציה JAK2 V617F, הפכה שיטה זו לסמן המולקולרי-אבחוני הראשון של PV. בנוסף אישר WHO קריטריונים משניים כדלקמן:
רמות אריתרופויאטין מתחת לרף הנורמה המקובל. קריטריון שני (ביופסיה של מח עצם) לא נדרש במטופלים עם אריתרוציטוזיס מוחלטת ויציבה (בגברים המוגלובין מעל 18.5 גרם/ד"ל, והמטוקריט מעל 55.5%, ובנשים המוגלובין מעל 16.5 גרם/ד"ל, והמטוקריט מעל 49.5%) אם מתקיימים קריטריון 3 הראשי, או קריטריונים מינוריים. עם זאת, ביופסיה של מח העצם היא הדרך היחידה לזהות מיאלופיברוזיס התחלתית, שמוצאים ב-20% מהמטופלים, ויכולה להצביע על התקדמות מהירה יותר לכיוון של מיאלופיברוזיס גלויה. מוטציות ב-JAK2 מתרחשות ב-60% מאלה עם תרובוציטמיה מהותית, כמו גם מוטציות בקולטן לתרומבופויאטין, ובגן ל-calretculin (על פי Cabagnols וחב' ב-Blood משנת 2016). PV גם כן קשורה למוטציות ב-JAK2. PV "ממוסך" (masked PV) כולל דומיננטיות בגברים, היסטוריה יותר תכופה של אירועי פקקת עורקית ותרומבוציטוזיס, שיעורים גבוהים יותר משמעותית של התקדמות למיאלופיברוזיס וללויקמיה אקוטית, והישרדות נמוכה יותר (Barbui וחב' ב-Am J Haematol משנת 2014).
הנתונים המופיעים לעיתים קרובות ב-PV, אך אינם נדרשים לאבחון PV כוללים:
- תרומבוציטים של מעל 400 אלף/מיקרוליטר
- לויקוציטוזיס של מעל 12 אלף לויקוציטים/מיקרוליטר
- פעילות alkaline phosphatase בלויקוציטים שמעל 100 יח'/ליטר בהיעדר חום בהדבקה
ספירת תרומבוציטים של מעל 400 אלף /מיקרוליטר מופיעה בלמעלה מ-50% מאלה עם PV. ההפרשה של אשלגן לנסיוב הנגרמת על ידי צימות של תאים in vitro, יכולה ליצור תרחיש של pseudohyperkalemia בנסיוב, בעוד שרמת האשלגן האמיתית בנסיוב היא בתחום הנורמה, מה שמודגם על ידי היעדר שינויים ב-ECG. אי-סדירות מורפולוגית כוללת מציאות מאקרו-תרומבוציטים, ותרומבוציטים משוללי גרנולות. עלייה בספירת לויקוציטים מעל 12,000/מיקרוליטר, מופיעה בערך ב-60% מאלה עם PV. ספירה זו מורכבת בעיקר מנויטרופילים עם סטייה שמאלה, ומספר תאים לא בשלים. מצב מתון של בזופיליה מופיע ב-60% מהמטופלים, ורמתalkaline phosphatase בלויקוציטים מוגברת מופיעה ב-70% מאלה עם PV. ניתן להדגים תפקוד בלתי תקין של תרומבוציטים על ידי בחינת הצימות של תאים אלה בנוכחות אפינפרין, או של adenosine diphosphate או של קולאגן, אם כי זמן הדימום עשוי להיות תקין.
מהן התוצאות הקליניות של אריתרוציטוזיס? יש קשר מוגדר בין אריתרוציטוזיס לבין עלייה בצמיגות הדם, והסכנה לפקקת. לדוגמה, במעקב של 34 שנים במסגרת מחקר Framingham, נמצא קשר בין תחלואה ותמותה קרדיו-וסקולרית בקבוצת משתתפי הסקר עם נפח התאים הדחוסים הגבוה ביותר (Gagnon וחב' ב-Am Heart J משנת 1994). יחס הסיכון (OR) הרב-משתני המתואם לתחלואה קרדיו-וסקולרית היה 1.6 (P=0.0018) לגבי נשים, ו-1.29 (P=0.019) לגבי גברים, בקבוצת הגיל של 35–64 שנה. ההתנהלות עם אריתרציטוזיס חייבת לקחת בחשבון שהעלייה בנפח התאים הדחוסים יכולה להיות תגובה פיזיולוגית. לדוגמה, במחלת לב ציאנוטית, התגובה הפיזיולוגית להיפוקסיה היא עלייה בייצור אריתרוציטים להקל על העברת חמצן, ולפיכך טיפול באריתרוציטוזיס בתרחיש זה עלול להחמיר את העברת החמצן לרקמות, ולהגביר קשיי נשימה. תסמיני צמיגות-יתר הם כאבים בחזה ובבטן, כאבי שרירים וחולשה, עייפות, כאבי ראש, ראייה מטושטשת וכן תסמינים המרמזים ל-amaurosis fugax, נימוּל, האטה בפעילות מנטלית, ותחושת ירידה בהתאמה אישית (פּרְסוֹנָלִיזַצְיָה). אריתרוציטוזיס מתגלה לעיתים באופן מקרי, ויש צורך לחזור על ספירת הדם לוודא שלא מדובר באירוע חולף (הנמשך שבוע). יש לברר האם המטופל עם אריתרוציטוזיס מעשן או אלכוהוליסט, האם מטופל עם משתן דוגמת תיאזיד, צורך טסטוסטרון, או סטרואידים אנבוליים, או האם לוקה בהפרעות נשימה בשינה. חקירות התחלתיות כוללות ספירת דם כוללנית ((CBC ומשטח דם, רמות ברזל ופריטין, רמת אריתרופויאטין בדם, בירור אפשרות של מוטציה ב-JAK2, מדידת רוויון של חמצן, מקלון לבדיקת שתן, פרופיל תפקודי כבד וכליות. חקירות שניוניות כוללות אולטרה-סאונד של הבטן, צילום חזה, ותפקודי ריאות.
ההתנהלות באריתרוציטוזיס ראשונית
PV הוא מפגע לימפו-שגשוגי נדיר בו הסיכון לאירועי פקקת גדול ב-60% מאשר באוכלוסייה הכללית, אך הוא בדרך כלל מוגבל לאלה עם תרומבוציטוזיס (Barbui וחב' ב-Blood משנת 2009). המנגנון של המפגע אינו ברור לחלוטין, אך הוא עלול להיגרם על ידי מחלת von Willebrand נרכשת. מטופלים עם PV אמורים להיות במעקב על מנת לנטר סימני מחלה המתקדמת לשלב של מיאלופיברוזיס בו במח העצם מופיעות רצועות סיביות דחוסות של reticulin עם ציטופניה ששכיחותם בין 6-15% לאחר 15 שנות מעקב (Passamonti וחב' ב-Am J Med משנת 2004, ו- Gruppo Italiano Studio Policitemia ב-Ann Intern Med משנת 1995). הטיפול הציטו-רדוקטיבי המפחית את נפח התאים לאחר סרכוז כמו גם את מספרי הלויקוציטים וטסיות הדם, חיוני לאלה בסיכון גבוה לפקקת. הקזת דם (בדרך כלל 450 מ"ל להשגת המטוקריט הנמוך מ-45%, ביחד עם אספירין במינון נמוך הוא טיפול מקובל ב-PV. בשנת 2013 פרסמה קבוצת המחקר CYTO-PV תוצאות מחקר גדול ואקראי בה נמצא שאלה עם נפח דחוס של תאים הנמוך מ-0.45, היו בעלי שיעור תמותה קרדיו-וסקולרית או מאירוע פקקתי קטלני נמוך משמעותית מאשר באלה עם נפח תאים דחוסים של 0.45-0.50 (4.4% לעומת 10.9%) (Marchioli וחב' ב-N Eng J Med משנת 2012). מחקר ECLAP האקראי, מבוקר כנגד פלצבו וכפול סמיות שכלל 519 משתתפים, אישר את הבטיחות והיעילות של טיפול באספירין ב-PV (Landolfi וחב' באותו כתב-עת משנת 2004). ניסוי זה הראה שהטיפול באספירין בהשוואה לפלצבו, הפחית בממוצע ב-60% את הסיכון לאוטם שריר לב לא-קטלני, לשבץ מוחי לא קטלני, לתסחיף ריאתי, לפקקת ורידית ניכרת ולמוות קרדיו-וסקולרי, ללא עלייה משמעותית של אירועי דימום.
Hydroxyurea
מספר תכשירים ציטו-רדוקטיביים משמשים לטיפול ב-PV בסיכון גבוה, מתוכם busulfan ו-hydroxycarbanide (או hyroxyurea) הם בעלי רקע מוכר ומבוסס, ואילו תכשירים אחרים דוגמת מעכבי Janus kinase, הם בעלי רקע טיפולי קצר ועדיין לא מבוסס. טיפול קו-ראשון במטופלים מעל גיל 60 שנה הוא עם hydroxyurea שהוא מעכב של ribonucleotide reductase, (McMullin וחב' ב-Br J Haematol משנת 2005). קיימים חלוקי דעות בדבר האפשרות שטיפול ב-hydroxyurea עלול להוות פוטנציאל להופעת לויקמיה, אך מחקרים גדולים לא ביססו אפשרות זו ( Marchioli וחב' ב-J Clin Oncology משנת 2005, ו-Finazzi וחב' ב-Br J Haematol משנת 2000). עם זאת ידוע שלאחר זמן, הטיפול עם תכשירים ציטוטוקסיים עם פוטנציאל גרימת לויקמיה בשילוב עם hydroxyurea מגביר את הסיכון של התמרה ללויקמיה.
Hydroxyurea במינון התחלתי של 500 מיליגרם פעמיים ביום הוא התכשיר הציטו-רדוקטיבי השכיח ביותר. ניתן לטטר אותו על בסיס ספירות הדם. המטופלים העמידים לתכשיר זה או שאינם סבילים לפעילותו, ניתן להשתמש באינטרפרון-α שאינו טרטוגני בילדים או לויקמוגני. חלופה נוספת היא busulfan, הגורם לאלקילציה, ומאושר באירופה לשימוש בבני 65 שנה ומעלה בגין ה-leukemiagenicity הידועה שלו (Alvarez-Lerrán וחב' ב-Br J Haematol משנת 2014, ו-Nielsen ו- Hasselbalch ב-Am J Hematol משנת 2003). נמצא ש-137 מתוך 890 מטופלים עם PV (15.4%) הראו עמדות או אי-סבילות ל-hydroxyurea (Alvarez-Lerrán וחב' ב-Br J Haematol משנת 2016).
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק