חיסונים שאינם בשגרה בישראל - Non-routine vaccinations in Israel
הופניתם מהדף חיסונים בגיל ילדות - חיסונים שאינם בשגרת חיסונים בישראל לדף הנוכחי.
| חיסונים שאינם בשגרה בישראל | ||
|---|---|---|
| Non-routine vaccinations in Israel | ||

| ||
מודעה בריטית הקוראת להתחסן מפני דיפתריה
| ||
| יוצר הערך | ד"ר מיכאל דובלין ואושרית דובלין RN MA | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – חיסונים, חיסונים בגיל ילדות
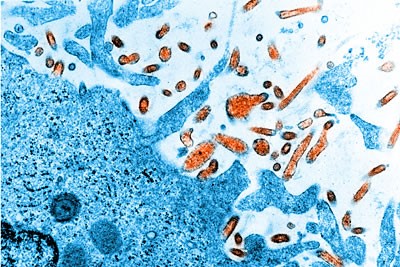
מחלת השפעת
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – שפעת
שפעת היא מחלה ויראלית (Viral, נגיפית) מדבקת והיא אולי מחלת החורף הקשה ביותר. בין 20-10 אחוזים מן הילדים בישראל חולים בשפעת מדי שנה. המחלה מערבת בעיקר את דרכי הנשימה העליונות (האף, ה"עץ" הברונכיאלי והריאות).
היסטוריה
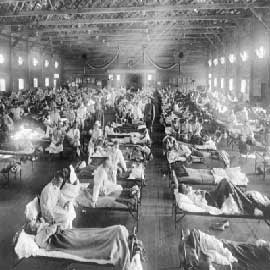
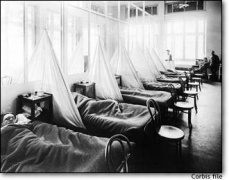
נגיפי השפעת מסוגים A, B עוברים באופן קבוע שינוי אנטיגני (Antigen) מסוג סחיפה. תהליך זה מתרחש באופן תדיר מעונה לעונה בה פורצת מחלת השפעת. שינוי אנטיגני מסוג העברה מתרחש באופן אקראי לחלוטין ובלתי צפוי שקשה להתכונן לו. וכאשר זה מתרחש, אוכלוסיות שלמות של אנשים, לעיתים מדובר בכלל האוכלוסייה ממש, נותרים ללא הגנה כל שהיא מול הנגיף, והתוצאות קטלניות. שינוי כזה מניב מגפה בסדר גודל עולמי הנקראת פנדמייה (Pandemic) ולא אפידמייה (Epidemic). במהלך המאה הנוכחית, אירעו שלוש פנדמיות של נגיף השפעת בשנים 1918, 1957 ו-1968. כל שנה כזאת גרמה לתמותה גבוהה עקב השפעת, ובפרט זאת של שנת 1918, שנה שבה התנהלה במקביל גם מלחמת העולם הראשונה שכל מספר חלליה לא מתקרב לזו של השפעת "הספרדית".
נתוני התמותה לפנדמיית השפעת מבהילים דיים. להלן הפירוט:
- 1919-18 "השפעת הספרדית" (H1N1)A גרמה למספר החללים הגבוה ביותר שגרם נגיף שפעת כלשהו. בערך חצי מיליון נספים בארצות הברית, וכ-20 מיליון בעולם כולו
- 1958-57 "השפעת האסייתית" (H2N2)A 70,000 מתים בארצות הברית בלבד
- 1969-68 "שפעת הונג קונג" (Hong Kong) (H3N2)A 34,000 מתים בארצות הברית בלבד
- התפרצותה של "שפעת הונג קונג" בשנים 68–1969 מציינת את תחילתו של עידן (H3N2)A, כאשר נגיף זה התגלה לראשונה, הוא אובחן על רקע השיפור שחל בתמותה החולים ביחס למוטציות (Mutations) הקודמות שלו. ישנן סיבות אפשריות העשויות להסביר את השיפור בהישרדות החולים. ראשית, הנגיף "האסייאתי" מסוג (H2N2)A עבר שינוי מסוג העברה והפך לנגיף המוכר לנו בשם שפעת הונג קונג" מסוג (H3N2)A. השינוי כפי שניתן להיווכח התרחש רק בחלבון Hemagglutinin כאשר החלבון Neuramindase נותר ללא שינוי, ולכן ניתן היה להסביר שלגוף הייתה בכל זאת הגנה מסוימת מפני המוטציה החדשה. הסבר שני לשיפור בשרידות החולים הוא שמוטציית שפעת עם אותו מבנה Hemagglutinin גרמה לשפעת בין השנים 1890 ולאורך השנים הראשונות של המאה. במצב שכזה, חולים שהיו בני 60 ואילך בשנת 1968 היו בעלי חסינות כלשהי כנגד נגיף השפעת, חסינות שנרכשה כנראה בתקופת חייהם כצעירים בסביבת המוטציה הנוכחית של השפעת.
ישנן עובדות הקשורות לנגיף השפעת שאינן ברורות די הצורך. למרות יחסי התמותה המשופרים של נגיף הונג קונג (H3N2)A, ממשיך נגיף זה להפיל חללים לאורך שנות פעילותו. במשך פעילותו של נגיף זה מאז שהתגלה, גרם (H3N2)A ל-400,000 מתים בארצות הברית בלבד, ו-90 אחוזים מבין אלה שייכים לאוכלוסיות הבוגרות. ולכן מבחינת פוטנציאל (Potential) הנזק של נגיף שפעת, (H3N2)A עדיין מהווה את המוקד לפגיעה חריפה ומסוכנת באוכלוסיות בוגרות או כרוניות.
- מגפת 1918 – תמונות מאותה תקופה
גם למוטציה (H1N1)A הקטלנית יש היסטוריה חשובה. לאחר הפנדמייה של שנת 19–1918 היא עברה באופן קבוע שינוי מסוג דריפט (הזזה), ובאופן עקיב גרמה למגיפות שפעת אבל לא בהיקף של שנת 19–1918. כאשר צצה השפעת האסיאתית (H2N2)A בשנת 1957, נעלם הנגיף מסוג (H1N1)A, ממש כמו שהוא עצמו נעלם כאשר התגלה נגיף "הונג קונג" (H3N2)A בשנת 1968. בשנת 1977 שוב הופיע הנגיף (H1N1)A שכונה "השפעת הרוסית" והתקשר לתוך (H3N2)A בהתלכדות תמידית, בינתיים. ובכל זאת הייתה לו השפעה מיוחדת, כי הנגיף של שנת 1977 היה זהה במבנהו לנגיף (H1N1)A שפעל בשנת 1950. לכן, רובם של האנשים שנולדו לפני שנת 1950 היו מחוסנים בפני הנגיף, והתפרצות השפעת מסוג (H1N1)A פגעה דווקא בצעירים יותר, לאמור בגילאים של 25 ומטה. העובדה שדווקא הבוגרים יותר מגלים חסינות לנגיף השפעת "הספרדי" האימתני מסביר בהתאם גם את השיפור שנצפה בהישרדות החולים. שהרי ממילא האוכלוסייה הבוגרת גם פגיעה יותר, ואם דווקא לה יש חסינות, ממילא משתפרים סיכויי השרידות של כלל האוכלוסייה בצורה דרמטית.
הידבקות
המחלה נקשרת לקור וחורף, אולם אין לה קשר ישיר לקור. ישנם מספר תאוריות באשר לתפוצתה הרבה של המחלה בעונת החורף. הסבר אפשרי אחד לתפוצתה הרבה בחורף נובע מהטעם הפשוט של חוסר אוורור במקומות הומי אדם. הסבר אחר הוא שטמפרטורות נמוכות גורמות לאוויר יבש יותר שמקשה על הגוף להיפטר מריכוזי הנגיף. ייתכן שגם ריבוי טיולים וביקורי קרובים בעונת החורף (במדינות המערב) מעודד את ההתפשטות. הסבר נוסף הוא שקור מחליש את מערכת החיסון של הגוף.
הנגיף גם מתקיים בקור לאורך זמן רב יותר על משטחים חשופים. ההידבקות עצמה במחלה נעשית באמצעות נגיפי המחלה המועברים בקלות רבה מאוד באמצעות האוויר, מה שהופך את המחלה למדבקת ביותר. ההידבקות בשפעת מתבצעת על ידי מעבר הנגיף אל דרכי הנשימה. שם הוא חודר לתוך תאי האפיתל שבדפנות דרכי הנשימה, לכל תא בנפרד. בתוך התאים משתכפל הנגיף בקצב מהיר ביותר ובתוך שעות אחדות נהרס התא, הנגיף מתפזר, חודר לתאים סמוכים וחוזר חלילה. התאים הנגועים מתים והמחלה מתקדמת עד שמערכת החיסון מדבירה את הנגיף או שהנגיף הורג את האדם.
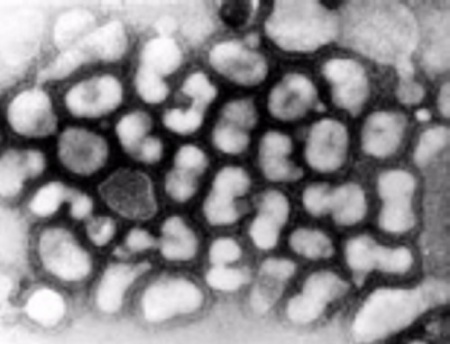
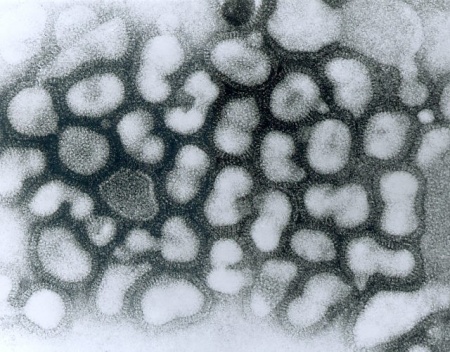
מבנה הנגיף
נגיף השפעת נראה כמו כדור העטוף ביתדות. היתדות עשויים מולקולות של החלבונים האנטיגנים Hemagglutinin (H) ו-Neuraminidase (N). כאשר יתדות אלה הממוקמים על פני חזית הנגיף באים במגע עם התא הבריא אליו נצמד הנגיף, הוא מפריש מייד נוגדנים הנלחמים בנגיף הפולש. היות שלנגיף יש קומבינציות שונות של יתדות כאלה על פניו, מפרישה המערכת החיסונית חומרים כנגד כל סוג נגיף שהיא מאתרת. יתרה מכך, המערכת החיסונית "מתעדת" את הנגיף שהתקיף את התא כך במקרה של זיהוי חוזר של תוקף דומה תוכל המערכת החיסונית להגיב מיידית על הפלישה.
מוליקולת (Molecule) ה-Hemagglutinin אינה יציבה ולכן היא משתנה כל הזמן ומחייבת גם את המערכת החיסונית להגיב על חותם הנגיף החדש. אבל כאמור כל עוד השינויים הם רק ביצירת עותקים זהים של Hemagglutinin מסוג הזזה קלה, עדיין שמורה למערכת החיסונית יכולת כלשהי להתגונן ורובם של נפגעי השפעת ישובו לאיתנם. אבל אם מתבצע שינוי ב-Hemagglutinin גופו, שינוי מסוג תנועה והחלפת מקום, אזי המצב מחמיר ועובר לכלל מגפה עולמית המכונה פנדמייה.
ישנם שלושה נגיפים שונים: Influenza A ,B ,C.
- הזנים A ו-B גורמים למחלה המערבת דרכי נשימה. הם מופיעים בכל חורף בדרגות משתנות.
- זנים אלו גורמים לצורה הקשה יותר של שפעת והמאמצים לחסן ולמנוע מתמקדים בזנים אלו. עם זאת, לזנים אלו יש יכולת השתנות, כך שכמעט בכל שנה מופיעה ואריאציה (Variation) מעט שונה של הנגיף ולא תמיד החיסון יעיל כנגד אותה צורה מתחדשת
- הזן C גורם למחלה קלה בדרכי הנשימה או שהוא חולף בצורה נטולת תסמינים. השפעתו על בריאות הציבור אינה כה רחבה והוא אינו מופיע בכל שנה
נגיף השפעת משתנה בתדירות גבוהה (עובר מוטציות רבות) וכך הוא מתחמק הן מן הזיכרון לטווח ארוך של מערכת החיסון משנים קודמות ולעיתים גם מן החיסון המיועד לאותה שנה ונועד לעצור את הזן החדש. תהליך ההדבקה והתחלואה די מובנה:
- אדם שנדבק בשפעת מפתח נוגדנים כנגד הנגיף
- הנגיף עובר מוטציה (שינוי צורה גדול או קטן)
- הנוגדנים כנגד הנגיף הקודם אינם מספקים הגנה כנגד הנגיף החדש
- מופיעה הדבקה מחדש בעונה הבאה
לעיתים המוטציה אינה מלאה והנוגדנים כנגד הנגיף הקודם מספקים הגנה כלשהי, מכיוון שהמוטציה אינה משנה את כל מרכיבי הנגיף המושפעים מהחיסון.
קיימים בעולם שני זנים של קבוצה A וזן אחד של קבוצה B האחראיים לתחלואה בעולם. תת-הקבוצות של נגיף מסוג A מסווגות על בסיס שני חלבוני הנגיף: Hemagglutinin ו-Neuraminidase.
לכן בעולם המדע מוכרים הזנים הפעילים כעת בתור– H1N1 ו-H3N2.
קליניקה
סימני המחלה מופיעים אצל החולה כ–48 שעות לאחר שנדבק מחולה שפעת אחר. היא מתחילה לרוב בצורה פתאומית על ידי צמרמורת, חום גבוה העולה עד 40 מעלות ואפילו יותר, כאבי ראש (מעל העיניים), שלשולים והקאות, כאבי גב ושרירים, בין הצלעות ובגפיים. הפנים אדומות והסומק מתפשט גם אל הצוואר והחזה. הפה יבש, הגרון כואב, האף בתחילה סתום, ולפעמים מדמם. קולו של החולה צרוד, בהתחלה מופיע שיעול קצר ויבש, ולאחר מכן הוא נעשה עוויתי – דמוי שיעול של שעלת. החם הגבוה נמשך 3–4 ימים. קורה שלאחר שהחם ירד ליום–יומיים, הוא שב ועולה ליומיים נוספים, מבלי שמהלך זה יבשר סיבוך במחלה.
כאשר לחולה יש חום הוא עייף, רדום לעיתים, והעייפות והתשישות נמשכות כמה ימים לאחר תם המחלה, גם באותם מקרים שהשפעת עוברת בצורה קלה.
תסמינים שכיחים
- חום, שעלול להיות גבוה
- כאב שרירים
- הרגשה כללית רעה "בכל הגוף"
- כאבי ראש
- שיעול, לרוב יבש (לא יצרני)
- כאבי גרון
- נזלת (בחלק מן המקרים)
- בחילה, לעיתים הקאה
- יציאות רכות
- חולשה ועייפות
משך המחלה הוא כשבוע במרבית האנשים, אבל החולשה והתשישות נמשכים עוד שבועות מספר.
כמו שניתן לראות רשימת הסימפטומים אינה ספציפית לשפעת. רק רופא הילדים יוכל למצות את ממצאי הבדיקה הגופנית וההיסטוריה שתוארה בפניו ולאבחן את המחלה.
שפעת לעומת הצטננות
אלו שתי מחלות שונות ונגרמות על ידי נגיפים שונים. ישנם כמה קווים משותפים אולם רב ההבדל על המשותף.
גם להצטננות ייתכנו סיבוכים (דלקות אוזניים, Sinusitis או דלקת ריאות) אולם כאשר היא מופיעה ללא סיבוכים הרי שזו מחלה קלה בהרבה. להלן מספר הבדלים:
| שפעת | הצטננות |
|---|---|
| חום גבוה | חום נמוך, או ללא חום כלל |
| כמעט תמיד קיימים כאבי ראש | כאבי ראש מופיעים לעיתים |
| נזלת מופיעה רק לעיתים | כמעט תמיד יש נזלת |
| לרוב אין התעטשויות | מתעטשים |
| שיעול יבש הולך ומחמיר | שיעול "נבחני" |
| לרוב כאבי שרירים | מעט כאבי שרירים |
| חולשה ותשישות למשך שבועות | מעט חולשה |
| כאבי גרון רק לפעמים | לרוב קיימים כאבי גרון |
| תשישות, לעיתים קיצונית | ירידה קלה ברמת האנרגיה הבסיסית |
חיסון לשפעת
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – חיסון לשפעת
התרכיב המקובל הוא תרכיב מומת בזריקה. התרכיב מכיל 3 זנים של שפעת, שמשתנים קצת מדי שנה. בכל השנים יש: H1N1, H3N2 ונציג של שפעת B. הזנים מגודלים בביצים ולכן מי שאלרגי לביצים לא מקבל את החיסון. מטפלים בנגיפים בפורמלין (Formaldehyde) כדי להרוג אותם. התרכיב הזה נקרא Whole vaccine. המרכיב השומני של התרכיב גורם לתופעות לוואי, בעיקר בילדים ולכן הוסיפו שלב נוסף ויצרו Split vaccine שזה אותו התרכיב, אבל ללא השומנים, אלא רק עם החלבונים.
Subunit vaccine – תרכיב שמכיל חלקים בלבד של הנגיף. מתן של תרכיב כזה בריריות לא גרם להופעה של חיסון. יש שני מרכזים למערכת החיסון הרירית – Peyer's patches ואתר נוסף באף. המטרה היא ליצור תרכיב שיעורר תגובה של המרכז באף.
אחת הסכנות בנגיף מוחלש – שחלוף גנטי (Genetic) עם נגיף רגיל.
CAR) Cold Adapted Reassortment) – פיתחו זן של הנגיף החי והמוחלש שמתרבה רק ב-32 מעלות. התרכיב הזה לא מגן נגד כל הסוגים. מכינים זנים רקומביננטיים (Recombinant) שכל גני ההתרבות שלהם מוחלשים, אבל NA ו-HA- שלהם הוא השולט. זה עדיין ניסיוני וזה נקרא CAR או CR. קבוצת היעד לתרכיב הזה היא חולים כרוניים קשים, חולים ללא מערכת חיסון ולצוות מטפל.
- FluMist חיסון דרך האף
מנהל התרופות והמזון האמריקאי אישר חיסון לשפעת הניתן דרך האף. החיסון משווק בארצות הברית בשם FluMist, והוא מכיל נגיפים מוחלשים של שפעת.
ה-FluMist מאושר למניעת שפעת כתוצאה מנגיפים מסוג A ו-B, והוא ניתן לגילאי 5 עד 49.
אצל ילדים בגילאי 5 עד 8 אשר מקבלים את החיסון בפעם הראשונה, החיסון ניתן בשתי מנות בהפרש של 6 שבועות לפחות. במתבגרים ובמבוגרים בגילאי 9 עד 49, נדרשת מנה אחת בלבד.
החיסון מכיל שלושה זנים נגיפיים (שניים מסוג A, ואחד מסוג B) אשר הומלצו לעונת השפעת של שנת 2003–2004. הנגיפים בחיסון חיים, אולם הם שונו כך שאינם יכולים לצמוח בטמפרטורת הגוף.
במחקרים קליניים רחבי היקף, FluMist הראה יעילות של 87 אחוזים במניעת שפעת בילדים, והפחית את הסיכון למחלה חמורה בליווי חום אצל מבוגרים.
החיסון אינו מתאים לשימוש במצבים הבאים: אנשים הסובלים מדיכוי מערכת החסון, חולי אסתמה (Asthma) או חולים אחרים עם בעיות במערכת הנשימה, גיל מתחת ל-5 או מעל 50, מחלות כרוניות אשר עלולות להגביר את הסיכון לשפעת חמורה, רגישות לביצים או לחיסון עצמו.
תופעות הלוואי כתוצאה משימוש בחיסון כוללות: הצטננות, נזלת, כאב גרון, ושיעול.
החיסון החדש מספק דרך נוספת למניעת שפעת, ומגביר את הזמינות של זריקות נגד שפעת המכילות נגיף מומת, עבור חולים הנמצאים בסיכון גבוה. יש לקוות שבקרוב יגיע חיסון זה גם לארץ.
את מי לחסן
- מבוגרים מעל גיל 65, אצלם סיבוכים יביאו לתחלואה משמעותי באם יחלו בשפעת
- חולים החוסים במוסדות, או שיש להם מחלת רקע כרונית
- כל ילד או מבוגר עם בעיית רקע ריאתית או לבבית ובכלל זה אסתמה, Cystic fibrosis, מחלת ריאות משנית לפגות (Bronchopulmonary Dysplasia ,BPD)
- כל ילד או מבוגר עם מחלה כרונית מן הרשימה הבאה: החולים במחלות מטבוליות (Metabolic) (כולל סוכרת), הפרעה כלייתית, דיכוי מערכת החיסון ( מולד, נרכש, או תרופתי), המוגלובינופתיות (Hemoglobinopathies) (אנמיות נרכשות או מולדות)
- ילדים בין הגילאים חצי שנה לגיל שמונה עשרה שנים הנוטלים אספירין באופן קבוע
- תינוקות בריאים בני 6–23 חודשים
- נשים הרות או בתקופת ההחלמה לאחר לידה
- עובדים בתחום הבריאות - רופאים, אחיות ואחרים המטפלים בחולים בסיכון גבוה בבתי-חולים ובקהילה (כגון ביחידות לטיפול נמרץ), בבתי חולים ומוסדות לחולים כרוניים או לקשישים, עובדי בתי- מרקחת וחדרי מיון. כמו כן צוותי שעת חירום כגון: עובד בתחום הפרא- רפואי (פרמדיק) וטכנאי רפואי. צוות רפואי ושאר מטפלים ומתנדבים הנכנסים לביקורי בית אצל אנשים בסיכון גבוה, וכן בני משפחה של האנשים בסיכון
- עובדים בבתי הבראה ועובדים הבאים במגע עם חולים בסיכון גבוה
- בני ביתם של חולים במחלה כרונית (ובכלל זה אחים/ אחיות של ילדים הנוטלים טיפול כימותרפי)
- אנשים הממלאים תפקידי מפתח כלשהם או מועסקים בשירותים קהילתיים חיוניים וכתוצאה מתחלואה גבוהה בקבוצה זאת עלולים להיווצר שיבושים בתפקוד השירותים לאוכלוסייה
- תיירים אשר מבקרים בארצות טרופיות בכל חודשי השנה או תיירים אשר מבקרים בארצות שבחצי הכדור הדרומי בין אפריל לספטמבר
- כל מי שמעוניין להפחית את הסיכון ללקות בשפעת
עיתוי
רצוי לחסן נגד שפעת כבר מתחילת חודש אוקטובר ומאוד מומלץ לא מאוחר מסוף נובמבר, אבל ניתן לחסן גם אחרי מועד זה.
הערה: יש לתכנן שילדים אשר לא חוסנו בעבר וזקוקים לשתי מנות תרכיב ברווח זמן של חודש ביניהן, יקבלו את המנה השנייה עד סוף נובמבר.
מתן בו-זמני של תרכיב שפעת ותרכיבים אחרים
ניתן לחסן בו-זמנית בתרכיב נגד שפעת עם חיסוני השיגרה בגיל הילדות או עם כל חיסון אחר (כגון נגד Pneumococcus בקבוצות סיכון אשר לא קיבלו חיסון זה בעבר).
מקום ההזרקה
יש להזריק את התרכיב לתוך השריר: באזור הדלטואיד למבוגרים ובחלק הקדמי- צדדי של הירך לתינוקות וילדים קטנים.
מינון
להלן לוח בו מצוין המינון לפי קבוצות גיל:
| גיל | מינון* | מספר מנות | סוג התרכיב |
|---|---|---|---|
| 35-6 חודשים | 1/2 מנה | 2-1 ** | מפוצל (split) *** בלבד |
| 8-3 שנים | 1 מנה | 2-1 ** | מפוצל (split) *** בלבד |
| 12-9 שנים | 1 מנה | 1 | מפוצל (split) *** בלבד |
| 13 שנים ומעלה | 1 מנה | 1 | רגיל או מפוצל |
(*) הכמות למנה מפורטת בדף ההסבר המלווה את אריזת התרכיב. נמצאים בשוק מזרקים חד-מנתיים/לשימוש בילדים. כמו כן, על חלק מהמזרקים המיועדים למבוגרים קיים ציון חצי מנה
(**) 2 מנות מומלצות לילדים אשר מתחסנים נגד שפעת בפעם הראשונה בחייהם. מומלץ על רווח זמן של 4 שבועות בין המנות
(***) ילדים מתחת לגיל 13 שנים, ובמיוחד ילדים בגילאים 6 חודשים עד 3 שנים, עלולים להגיב בתופעות רעילות (לרבות התכווצויות מלוות חום) לתרכיב שפעת רגיל, המוכן מנגיף שפעת שלם. תרכיב השפעת מהטיפוס המפוצל (Split) מלווה בפחות תופעות לואי מאשר תרכיב המוכן מנגיף שלם, לכן, בגילאים אלה מומלץ מתן תרכיב מפוצל, בהרכב ובמינון זהים למינון התרכיב הרגיל (ראה בעלון התרכיב). בתרכיב המפוצל, הנגיפים עברו טיפול כימי להקטנת רמת המרכיבים העלולים לגרום לחום. תרכיבים אלו מופיעים תחת שמות כגון: "Split" "subvirion” “purified-surface antigen” “sub-unit” “disrupted”
תופעות לוואי וסיבוכים
מפני שתרכיב השפעת מכיל נגיפים מומתים, הוא אינו יכול לגרום לשפעת. הופעת זיהום נשימתי סמוך לקבלת החיסון פירושו שהתרכיב ניתן בתקופת הדגירה של השפעת, או שהמחלה נגרמה על ידי מחולל אחר. התגובות לאחר מתן תרכיב שפעת הן נדירות.
תגובות מקומיות של אודם, נפיחות, רגישות במשך 1–2 ימים, מופיעות בפחות משליש ממקבלי החיסון.
תופעות רעילות כגון חום, מצב כללי רע, כאבי שרירים ותופעות כלליות אחרות מופיעות 12-6 שעות לאחר הזרקת התרכיב ונמשכות יום או יומיים. תופעות אלה שכיחות במיוחד אצל אלו שלא היו חשופים בעבר לאנטיגנים של זני השפעת אשר בתרכיב (כגון ילדים).
על מנת להפחית החום אצל ילדים יש להשתמש בתרכיב מפוצל.
תופעות אלרגיות המופיעות מיד לאחר הזרקת התרכיב הן נדירות ביותר: Urticaria, Angioedema, קשיים נשימתיים, או הלם אנפילקטי (Anaphylaxis). תופעות אלה נובעות מרגישות-יתר למרכיבים מסוימים בתרכיב, במיוחד לחלבון ביצה. אנשים הידועים כבעלי רגישות מסוג IgE (Immunoglobulin E) לחלבון ביצה, כולל אנשים עם תופעות של אסתמה תעסוקתית או תופעות אלרגיות אחרות על רקע חשיפה תעסוקתית לחלבון ביצה, נמצאים בסיכון גבוה יותר לפתח תגובות לאחר חיסון נגד שפעת. התרכיבים נגד שפעת הנמצאים בשימוש, למרות היותם מוכנים על ביצים מופרות, הם מטוהרים מאוד, ולכן נדירות למדי תופעות אלרגיות לאחר קבלתם.
סיבוכים נוירולוגיים
מאז 1976 (כשניתן חיסון שפעת מזן החזירים), לא נרשמה עליה בשכיחות תסמונת Guillain-Barre קשור למתן תרכיב שפעת מזנים אחרים.
הוראות נגד ואזהרות
אין לתת את החיסון לאנשים אשר סובלים ממחלת חום בשלב החריף.
אין לתת תרכיב נגד שפעת לאנשים עם סיפור של תגובה קודמת חמורה לתרכיב או עם תולדות של רגישות-יתר מסוג אנפילקטי לחלבון ביצה בלי להתייעץ עם רופא המטפל.
בקבוצה זאת נכללים אלו אשר אחרי אכילת ביצה מפתחים נפיחות בשפתיים או בלשון, בצקת כללית, קשיים נשימתיים או אבוד הכרה.
הטיפול התרופתי בשפעת
השימוש בתרופות למניעה מומלץ במקרים הבאים:
- התפרצות שפעת בעיקר במוסד בו מתגוררים אנשים בסיכון גבוה, ובמיוחד כאשר יש ספק לגבי יעילות התרכיב עקב שינויים אנטיגניים בנגיף. יש להתחיל במתן הטיפול בהקדם האפשרי, כשיש חשד להתפרצות, לכל דיירי המוסד (כולל אלה שקיבלו חיסון נגד שפעת בעונה הקודמת) ולהמשיך בטיפול לאורך כל תקופת ההתפרצות ועוד שבוע אחד לאחר סיומה
- אנשים בסיכון גבוה שחוסנו באיחור כאשר פעילות השפעת כבר החלה בקהילה. התרופות אינן מונעות יצירת נוגדנים לנגיף השפעת ומומלץ לתת במשך שבועיים נוספים לאחר מתן התרכיב (עד להתפתחות החסינות)
- השלמת ההגנה של אנשים אשר קיבלו חיסון נגד שפעת וידועים כמדוכאי חסינות. אין מידע על פעולות הדדיות עם תרופות נגד זיהום HIV (Human Immunodeficiency Virus)
- אנשים הידועים כרגישים לחלבון ביצה ועלולים לפתח תופעות אנפילקטיות לחיסון
- ניתן להשתמש בתרופות הנזכרות למעלה גם לטיפול באנשים מבוגרים בריאים הלוקים במחלה החשודה לשפעת בעת פעילות שפעת בקהילה, במטרה למנוע אצלם את סיבוכי המחלה וצמצום משך המחלה. את התרופה יש לתת תוך 24–48 שעות מתחילת המחלה ולהמשיך עוד 48 שעות לאחר העלמות סימניה
- הטיפול יקבע על ידי רופא הילדים בהתבסס על
- גיל הילד/ה, מצב הבריאות הכללי וההיסטוריה הרפואית
- מפושטות המחלה וחומרתה
- מידת ההיענות והסבילות של הילד/ה לטיפול תרופתי
- הצפי לגבי מהלך המחלה מעת המפגש במרפאה
- העדפות המשפחה והילד/ה
- הטיפול יכלול לרוב
- תרופות המפחיתות כאב ומורידות חום (יש להימנע משימוש באספירין)
- טיפול נוגד גודש לאף במקרי נזלת
- מנוחה
- שתייה מרובה
- טיפול ספציפי במקרים מיוחדים
במאגר חברות התרופות והממסד הרפואי בעולם נמצאות 4 תרופות לטיפול או למניעה של הדבקות בנגיף ה-Influenza: שתי תרופות הוותיקות יותר שאושרו לשימוש עוד בשנת 1993; Amantadine ו-Rimantadine (Flumadine), שייכות למשפחת תרופות המפריעות לנגיף שחדר לתא הפונדקאי בשלב העירום שלו, דהינו אותו שלב מאבד נגיף את המעטפת החיצונית שלו (Uncoating) וחומצת הגרעין שלו מתחילה את תהליך שכפולה ליצירת נגיפי-בת רבים. שתי תרופות אלה יעילות רק כנגד הנגיף Influenza A2, הזן ה"אסייתי" (Asian), על ידי שהן נקשרות לחלבון הנגיפי M2, ובכך מפריעות להסרת מעטפת הנגיף לאחר חדירתו לתא. אך השימוש בשתי תרופות אלה מוגבל הן בשל מספר תופעות לוואי רעלניות ובפרט השפעתן על מערכת העצבים, וכן כיוון שהנגיפים המטופלים בתרופות אלה פיתחו עד מהרה עמידות כנגדן, והסתבר שהזנים העמידים שהם יציבים מבחינה גנטית ועלולים להיות מועברים בהדבקות מאדם לשני, והם פתוגניים (Pathogen) באותה מידה כמו נגיף הבר, וגרוע מכך הם יכולים להמשיך והתרבות ולהיות מופרשים בנוזלי גוף של אותם מטופלים עם מערכת חיסונית פגומה או מוחלשת ובכך להפוך למקור מתמשך של הדבקות עם זן נגיפים עמיד לתרופות אלה. ההופעה של עמידות בנגיפים המטופלים בשתי תרופות ממשפחת ה-Adamantanes, מגבילה אם כן את יעילות השימוש בהן.
שתי התרופות האחרות, העומדות מתחילת המאה ה-21, בחזית המאבק בנגיף ה-Influenza הן Zanamivir (Relenza) ו-Oseltamivir (Tamiflu) פועלות למעשה כמעכבות את פעולת האנזים Neuraminidase, ובכך מפריעות לשחרור נגיפי שפעת מהתאים המודבקים, ובכך נמנעת התפשטות הנגיף והמחלה בדרכי הריאות. כיוון שההתרבות של נגיף השפעת בצינור הנשימה מגיעה לשיאה בין 24 ל-72 שעות מהופעת המחלה, שתי התרופות האחרונות הפועלות בשלב התרבות הנגיף, צריכות להינתן מוקדם ככל האפשר. בניגוד לשתי תרופות הוותיקות, התרופות מהדור החדש שהן יקרות בהרבה מקודמותיהן, מעכבות Neuraminidase, אינן גורמות לתופעות לוואי רעלניות ואינם מעודדות יצירת נגיפי-שפעת עמידים להן. אך החשוב מכל היא תכונת שתי התרופות האחרונות לגלות יעילות כנגד כל זני נגיף השפעת בכך שהן מעכבות פעילות אנזים העומדת ביסוד ההדבקה וההתפשטות של כל נגיפי Influenza. תכשיר Relenza מגיע בצורת אבקה המוחדרת בעזרת משאף, ואילו Tamiflu כטבליות לבליעה. גם יעילות הטיפול בשתי תרופות אלה רבה יותר ככל שמקדימים בו.
ניסוי משנת 2003 עם Tamiflu בקרב 1,426 חולי שפעת הראה שכאשר הטיפול החל 12 שעות מתחילת התסמינים קיצר את מהלך המחלה ביותר משלושה ימים, ולעומתו טיפול באותה תרופה שהחל בין 36–48 שעות מתחילת התסמינים הראה יעילות מופחתת בהרבה. מה יעילותן של שתי התרופות האחרונות בהפחתת סבל או אף תמותה בקרב קשישים? סקירה של ניסויים קליניים שנערכו לפני שנת 2002 בקרב קשישים מעל גיל 65 שנה או אלה עם מצבים קליניים כרוניים, הראו כי Relenza הפחיתה את פרק הזמן עד להיעלמות התסמינים ביומיים, אם כי Tamiflu היה יעיל פחות ובממוצע קיצר את הזמן מתחילת הטיפול בו עד להתפוגגות התסמינים בחצי יום בלבד. ומה באשר לילדים? כאן דווקא מתהפכות היוצרות לגבי יעילות שתי התרופות האמורות: ניסוי קליני ב-471 ילדים בני 5 עד 12 שנה בהם ניתן הטיפול ב-Relenza, בין 36 עד 48 שעות מתחילת התסמינים, נמצא שתרופה זו קצרה את משך התסמינים ביום אחד בממוצע. לעומתה, טיפול ב-695 ילדים בגיל 1 עד 12 שנים ב-Tamiflu שהחל באותו פרק זמן מתחילת התסמינים כמו במקרה של Relenza, הביא לקיצור מהלך המחלה ב-1.5 ימים בממוצע. מה שמרשים יותר, שהטיפול בילדים עם שפעת ב-Tamiflu הפחית ב-44 אחוזים את התרחשות דלקת חריפה של האוזן התיכונה שהיא סיבוך שכיח בילדים עם שפעת.
מינונים
המינון בטיפול מלא בשפעת:
Amantadine - 100 מיליגרמים פעמיים ביום למשך 10 ימים.
Rimantadine - 100 מיליגרמים פעמיים ביום למשך 10 ימים.
Oseltamivir - 75 מיליגרמים פעמיים ביום למשך 5 ימים.
- נתונים על יעילות התרופות השונות ובטיחות השימוש בהן
| קריטריון/תרופה | Amantadine | Rimantadine | Oseltamivir |
|---|---|---|---|
| יעילות נגד שפעת A (באחוזים) | 90-70 | 90-70 | 90-70 |
| יעילות נגד שפעת B (באחוזים) | אין | אין | 90-70 |
| התפתחות של עמידות הנגיף לתרופה | מהירה | מהירה | איטית, אם בכלל |
| הפסקת התרופה עקב תופעות לוואי (באחוזים) | 11 (חלקן קשות) | 6 | 2 |
| חיי מדף | 5 שנים | 5 שנים | 10 שנים |
| השפעת הטיפול | קיצור המחלה ביום | קיצור המחלה ביום | קיצור המחלה ביום |
| הפחתת התחלואה – מניעה לפני חשיפה (באחוזים) | 63 | 63 | 71 |
| הפחתת התחלואה – מניעה לאחר חשיפה (באחוזים) | 63 | 63 | 83 |
אמצעי זהירות
בשל מגוון תופעות הלוואי של התרופות האנטי-נגיפיות, יש להתייעץ עם מומחה למחלות זיהומיות לפני השימוש, הן לגבי בחירת התרופה והן לגבי המינון, ובכל מקרה יש לעיין בעלון היצרן.
תופעות לוואי של Amantadine: בחילה, סחרחורת, חוסר שינה, עצבנות, קשיי ריכוז. תופעות אלו ואחרות עלולות להופיע במיוחד אצל בני-אדם אשר סובלים ממחלות כרוניות, במיוחד קשישים, לכן נחוץ מעקב מיוחד לגבי אנשים אלה.
תופעות לוואי של Oseltamivir: בחילות והקאות.
זהירות מיוחדת דרושה כאשר הטיפול ניתן לאנשים הסובלים מליקויים בתפקודי הכליות, הכבד, מהתקפים אפילפטיים (Epilepsy) או נלקח בו-זמנית עם תרופות הפועלות על מערכת העצבים המרכזית. במצבים אלה יש לשקול הקטנת המינון ולהפסיק את הטיפול מיד עם הופעת תגובות חריגות.
לא מומלץ לנשים בהיריון ולמניקות.
סיכום שפעת
המלצת ארגון רופאי הילדים בישראל היא חד משמעית בעד חיסון כל ילד מגיל חצי שנה. אין ספק כי ככל שיהיו יותר ילדים מחוסנים הרי שהסיכוי להתפתחות מגפות כלל ארציות קטן יותר. לפי דעת הכותב יש לחייב כל ילד/אדם הלומד במוסד חינוכי מפעוטון ועד אוניברסיטה להתחסן לשפעת בטרם כניסתו לכותלי המוסד הלימודי (כפי שמקובל בארצות הברית וקנדה).
שפעת העופות והקשר לשפעת
שפעת העופות (Avian influenza) היא סוג של שפעת נגיפית התוקפת עופות. לשפעת העופות שני זנים עיקריים: זן שאינו אלים (H9N2) וזן אלים (H5N1).
התגלו כמה עשרות הידבקויות וגם תמותה של בני אדם במחלה בדרום מזרח אסיה. כמו כן התגלו מוטציות רבות של הנגיף (לא כאלו שמועברות לבני אדם). החשש הכבד הוא שהנגיף הקטלני יעבור מוטציה שתקנה לו כושר הדבקה מהיר, בדומה לנגיף השפעת האנושי הנפוץ, ובכך יביא למגפה עולמית. לנגיף זה לא נמצאה תרופה שהוכחה כיעילה. קיימת הערכה שהתרופה "Tamiflu", הנמצאת בשימוש כנגד שפעת רגילה, יכולה להפחית את נזקו של הנגיף על האדם, אם כי לא לחסן מפניו.
- סיבות להתפרצות המגפה במזרח אסיה
- גידול בעלי חיים (עופות, חזירים) בערוב ובצמידות למגורי אדם
- שווקי עופות חיים מפותחים
- צמיחה מהירה בגידול העופות האינטנסיבי
- יצוא מפותח (הברחה של עופות)
- שימוש בתרכיבים ברמת איכות נמוכה (סין, אינדונזיה)
- רמת דיווח וניטור נמוכה
- הסתרת מידע מכוונת מטעם השלטונות (אירועים החלו במחצית הראשונה של 2003)
- חוסר ניסיון בטיפול באירועים דומים
- מחסור באמצעים כלכליים ומערכות פיצוי לחקלאים
סין ידועה מזה שנים רבות, כמקור להפצת נגיף השפעת. נראה שמקור הנגיף הוא דרום סין.
בדיקות רצף של הנגיף שבודד מברווזים שהוברחו לטייוואן מסין ב–22.01.03, מצאו התאמה לנגיף שבודד מחולים בוייטנאם.
מרבית בני האדם שנדבקו היו במגע ישיר עם עופות חולים, אך ישנם גם דיווחים שלא הוכחו על בני משפחה שנדבקו זה מזה. שפעת העופות תוקפת בעיקר בני אדם צעירים; כ-70 אחוזים מאלו שנדבקו במחלה היו מתחת לגיל 20.
התסמינים הקליניים של בני אדם שחלו בשפעת העופות (H5N1) דומים לאלו של בני האדם שחולים בשפעת האנושית הרגילה (H3N2). מתברר, כי הנגיף H5N1 הקטלני מעביר מטען גנטי בינו ובין אחד ממיני נגיף השפעת הרגילה, ויוצר מוטציה קטלנית הגורמת למוות בהדבקתו את האדם.
במחקרים שבוצעו על עכברים גילו החוקרים שזנים חדשים של שפעת העופות שהוזרקו לעכברים הפכו לקטלניים יותר.
נגיף שפעת העופות H5N1 התגלה לראשונה בשנת 1961 בדרום אפריקה. הפעם הראשונה שבה אובחנה הדבקה של בני אדם על ידי מוטציה (Mutation) של הנגיף הייתה בשנת 1997 בהונג קונג, כששמונה-עשר בני אדם נדבקו במחלה ושישה מהם מתו. בתחילת שנת 2003 חלו בסין שלושה בני משפחה אחת ושניים מהם מתו. בהמשך התגלו סימני המחלה אצל בני אדם בטייוואן (Taiwan), וייטנאם (Vietnam), דרום קוריאה (South Korea), יפן (Japan), תאילנד (Thailand), קמבודיה (Cambodia), לאוס (Laos), אינדונזיה (Indonesia) ופקיסטן (Pakistan). מתוך 120 בני אדם שחלו במחלה, מתו 60.
בסוף שנת 2005 התגלו בטורקיה( Turkey), רומניה (Romaina), ורוסיה (Russia) התפרצויות של שפעת העופות בעופות, בעקבות נדידת עופות מהמזרח הרחוק, בנוסף נפוצו ידיעות על התפשטות המחלה ליוון שהתבררו כלא נכונות, שלטונות הבריאות בעולם נערכו למניעת הידבקות המונית של בני אדם במחלה. התפשטות זו של המחלה הביאה את ללחץ חזק על חברת "Roche", יצרנית תרופת Tamiflu, להתיר ייצור של התרופה על ידי חברות אחרות וזאת על מנת להגדיל את הייצור לאחר שהחברה מסרה כי לא תוכל לטפל בכל ההזמנות שהוזמנו ברגע האחרון למרות שהחברה הציע לממשלות להזמין אותן באמצע שנות ה-90, החברה נכנעה לבסוף ללחץ ובסוף אוקטובר 2005 החלה במשא ומתן עם חברות תרופות אחרות בנושא. במקביל החלו להתעורר פקפוקים בנושא יעילות התרופה לגבי הזן שעלול לעבור מוטציה אולם המצב בנושא זה עדיין איננו ברור.
החשש בישראל הוא שעופות נודדים שחונים חניית ביניים בשמורת החולה ובמקומות אחרים עלולים להעביר את המחלה לישראל.
לא ברור לאן פניה של המגפה ואם נכונה לנו בעתיד מגפה עולמית או לא. בעד מגפה עולמית העובדה שמדובר בנגיף שטרם תקף בני אדם ועל כן מערכת החיסון שלנו עדיין לא למדה כיצד להתגונן מפני נגיף זה. נגד - העובדה שעד היום לא קרה דבר. החששות שהובעו על ידי ארגון הבריאות העולמית ממגפה קשה של שפעת העופות נובע מקרבה ניכרת בין שפעת העופות שתקפה בדרום אסיה לנגיף השפעת הספרדית. החשש הוא כי נגיף השפעת הספרדית שתקף גם את העופות יעבור שינוי גנטי וכך יתקוף בחזרה בני אדם אשר לא יהיו מחוסנים כלפי הנגיף "המשופר". ההסתברות הסטטיסטית ששינוי כזה בנגיף יקרה בתקופה הקרובה הוא די גבוה. ועל פי מודלים מתמטיים חושב כי אם לא תהייה הכנה מוקדמת כנגד הנגיף הנזכר למעלה הרי שצפויים להיפגע כ-150 מיליון איש ברחבי העולם תוך שנה אחת.
ארגון הבריאות העולמי דרש מישראל להצטייד במלאי תרופות כנגד השפעת שיספיקו לטיפול בכל אוכלוסיית ישראל.
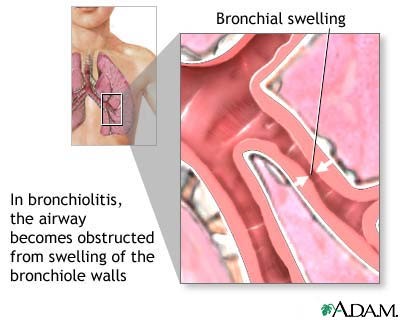
Respiratory Syncytial Virus – הגורם ל-Bronchiolitis
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – ברונכיוליטיס
Bronchiolitis היא מחלה של דרכי הנשימה העליונות והתחתונות. מדובר במחלה עונתית נגיפית מגפתית. הגורם המחולל השכיח ביותר למחלה הוא נגיף ה-Respiratory Syncytial Virus (RSV). הגורמים הנוספים הם נגיף השפעת נגיף ה-Parainfluenza. רוב ילדי העולם נדבקים במחלה זו בשנות חייהם הראשונות. לרוב מדובר במחלה בינונית בחומרתה שביטוייה הם כשל שפעת הנמשכת כשבוע ימים. לעיתים המחלה יכולה להתבטא בחומרה גדולה יותר ואז היא דומה יותר לשילוב שבין שפעת + אסתמה + דלקת ראות בגוף שגילו לא עולה בדרך כלל על גיל חצי שנה. במקרים כאילה מחלה זו יכולה להמשך בין 10 ימים לשבועיים ויכולה בהחלט לסכן חיים. בתצורתה הקשה מחלה זו יכולה לגרום לאי ספיקה נשימתית, הפסקות נשימה עד מוות.
כ-20 אחוזים מכלל אשפוזי החורף בילדים מקורם בנגיף זה.
נגיף ה-RSV שייך למשפחת ה- Para-myxo-viridea. לנגיף שני חלבונים עקריים על הקופסית שלו האחד שמו F - חלבון הגורם לאיחוי והחדרת המטען הגנטי לתא המאחסן והשני G הגורם להצמדה לתא המאחסן.
הנגיף גורם ליצירת תאי ענק מרובי גרעינים ברקמת תאי הרירית של הגוף המארח.
קיימים שני תת-מינים של הנגיף A – שאחראי על הזיהומים החמורים יותר ו-B האחראי על 80 אחוזים מכלל ההדבקות והוא הזן הפחות אלים.
גוף האדם יודע ליצור נוגדנים כנגד החלבונים G ו-F ומכאן החיסון הטבעי המתפתח לאחר הזיהום. התפתחות נוגדנים כנגד חלבון F מקנה חסינות מלאה בעוד שנוגדנים כנגד חלבון G מקנים לנו חסינות חלקית בלבד. החיסון הסביל שניתן לתינוקות הוא נוגדן ספציפי כנגד חלבון F דבר המקנה חסינות זמנית מלאה כנגד הנגיף.
מקורות הדבקה בנגיף
ערך מורחב – זיהום בנגיף ה-RSV infection - RSV
ההדבקה מתבצעת על ידי מגע יד מזוהמת בהפרשות מתינוק אחר. לא מדובר על הדבקה טיפתית. שרשרת הדבקה זו הניתנת לעצירה על ידי שטיפת ידיים ובפגיות בארץ ובעולם מקובל שימוש בכפפות חד פעמיות ומגני פנים וחלוקים למניעת הדבקת הפגים.
הדגירה במחלה קצרה ונמשכת בדרך כלל כיומיים בלבד ומרגע זה התינוק כבר מדביק אחרים.
הנגיף מדביק את התינוק מייד עם כניסתו לפה והוא מופרש מילד מודבק מכל נוזלי הגוף. הנגיף מופרש כ 5 ימים מרגע ההדבקה ועד 3 שבועות מתחילת המחלה. למעשה בגן ילדים שאליו הובא תינוק אחד עם RSV ידביק תוך כיממה אחת את רוב התינוקות בגן כאשר המטפלות הן הווקטור למחלה.
כמחצית מהצוות המטפל/מורים/גננות ידבקו באותה הדבקה. שליש מהילדים ומהצוות שנדבק יסבלו גם מזיהומים נוספים חיידקיים שהם סיבוך שכיח למחלה זו (בעיקר דלקות אוזניים וריאות).
אפידמיולוגיה
המגפות בנגיף זה הן רחבות תחלואה ונמשכות כ-3 חודשים. התחלואה עונתית ומתרחשת בין החודשים ינואר ועד אפריל. הפגיעה באוכלוסייה רחבה מאוד וכל שכבות הגילאים יכולות להיפגע. עד גיל שנתיים רוב האוכלוסייה כבר נפגעת מנגיף זה. רוב הפגיעות הקשות מתרחשות בתינוקות מתחת לגיל שנה והפגיעה הקשה ביותר היא בפגים.
בכל חורף כ-15–20 אחוזים מכלל אשפוזי הילדים מתחת לגיל שנתיים מקורם בהדבקה בנגיף זה.
מבחינה סטטיסטית קיימת שונות מובהקת בין שכבות האוכלוסייה. בשכבות סוציואקונומיות נמוכות שיעור האשפוזים גבוה פי 5 מאשר בשכבות החזקות יותר. הנתון הזה נכון גם בישראל ומודגש הרבה יותר בארצות הברית שם שיעור האשפוזים בשכבות חלשות מגיע לפי 10 מאשר בשכבות החזקות (צפיפות דיור, מספר ילדים בבית ורמת הכנסה נמוכה היו המנבאים החזקים ביותר לאשפוז בשל RSV).
בנים מאושפזים פי 2 מאשר בנות – למרות תחלואה זהה בחומרתה בשני המינים.
- הגורמים האתיולוגיים ל-Bronchiolitis
- RSV – 75 אחוזים
- נגיף ה-Parainfluenza - 7 אחוזים
- Influenza B - 10-7 אחוזים
- Adenovirus – 3 אחוזים
- Mycoplasma – 2-1 אחוזים
- Pneumovirus – אחוז אחד
גורמי הסיכון לאשפוז
- משקל לידה נמוך – מתחת ל 2,200 גרם
- פגות – מתחת ל-28 שבועות היריון
- שכבה סוציו-אקונומית נמוכה
- עישון של ההורים
- העדר יניקה
- ביקור במעון או גן ילדים
- בנים פי 2 מבנות
קליניקה
המחלה מתחילה כהצטננות רגילה המלווה בשיעול נזלת וחום. לאחר כיומיים מתחילת המחלה מתחיל שיעול עמוק יותר ומתחילים להופיע צפצופים וחרחורים על פני הראות. מופיעים התקפי שיעולים הנשמעים כהתקפי אסתמה קשה. התינוקות מתקשים באכילה, שתייה ויניקה.
חלק מהתינוקות מפתחים בזמן אכילה קוצר נשימה והכחלה סביב לפה. לעיתים מופיעים סימנים של מצוקה נשימתית מתגברת הכוללים פעילות שרירים מוגברת של בית החזה (רתיעות), נשימת כנפי אף ואף הפסקות נשימה בעיקר בשינה – דבר הצריך להדליק נורה אדומה אצל ההורים. המחלה נרפית מעצמה וברוב המקרים הקלים יותר לאחר כ-7 עד 10 ימים של חום ושיעול מתחיל תהליך החלמה הדרגתי הכולל את ירידת החולים והפסקה הדרגתית של השיעולים.
חלק מהילדים ימשיכו להשתעל עוד מספר חודשים לאחר תום המחלה ואצל חלקם תתפתח אסתמה כרונית.
התהליך בריאות
מקור הפגיעה הריאתית בבצקת המתפתחת בדפנות העץ הברונכיאלי (Bronchial) וזאת בשל הסננת הנגיף לאזור. התאים הפגועים מהנגיף נושרים לתוך חלל העץ הברונכיאלי ומתווספים להפרשות הסמיכות המופרשות מהברונכים הפגועים. כל ההפרשות הנל הופכות להיות יותר ויותר סמיכות וצמיגות ומפריעות מאוד בנשימה. בשלב הזה מופעלת מערכת החיסון שלנו המושכת בצורה כימית כמות גדולה של לימפוציטים (Lymphocytes) המוסיפים לבצקת הכללית.
הבצקות וההפרשות יוצרות חסימות חלקיות או מלאות של דרכי האוויר הקטנים בריאה ונוצרים חללי אוויר גדולים הלכודים בריאה והחלקה הריאה עוברת תמט בשל חוסר אוורור.
הריאה מאבדקת חלק גדול מהאלסטיות שלה ומיכולתה לשמש כמכשיר כהעברת חמצן לרקמות ולשחרור פחמן דו-חמצני – מכאן ה-Hypoxemia (חוסר חמצן בקרמות).
המצב יכול להיות קל ולהסתדר על ידי מערכת החיסון של הגוף הפוגעת בנגיף ולאחר תקופה של מספר ימים מתקנת את הנזקים. המצב יכול להגיע לאי ספיקה נשימתית המצריכה הנשמה בלחץ חיובי לשם פתיחת דרכי הנשימה המוצרים והמודלקים.
אוכלוסיית הסובלים ממחלת ריאה בסיסית כגון: אסתמה קשה, מחלה היאלינית (Hyaline) של פגות, חולי CF (Cystic Fibrosis) הם ילדים המועדים להיפגע קשות מנגיף זה.
ילדים הסובלים ממחלות לב קשות או מחלות מטבוליות קשות גם כן מועדים להפגע קשה יותר מנגיף זה.
אבחנה
ברוב המקרים רואים בבדיקה תינוק קטן הסובל מחום גבוה וברוב המקרים גם ממצוקה נשימתית ניכרת.
האבחון הוא קליני בדרך כלל ניתן לשמוע על פני הראות ציפצופים אקספירטוריים ואינספירטוריים – דהיינו הן בשאיפה והן בנשיפה. בחלק מהמקרים ניתן לשמוע חירחורים עדינים על פני בסיסי הריאות וכן קולות המזכירים נייר פרגמנט מקומט (קרפיטציות, Crackles). ברוב המקרים מוצאים נשימה מהירה עם שימוש ניכר בשרירי בית החזה לנשימה וכן תנועה של כנפי האף המצביעים על מצוקה נשימתית. מצוקה נשימתית קשה יותר ניתן לראות על ידי כיחלון סביב השפתיים, כיחלון באצבעות ורתיעות בין צלעיות. כל הנזכרים למעלה יכולים להצביע על מעורבות של חלק גדול מהריאות בתהליך דלקתי רחב.
בדיקת ריווי חמצן בדם שהיא בדיקה פשוטה מאוד בעזרת מתמר קטן המצוי בכל מרפאה יכולה לתת התוויה מיידית לגבי מצבו האמיתי של הילד/תינוק. ריווי חמצן שיורד מ-92 אחוזים משמעו פגיעה בינונית ברקמת הריאה ומתחת ל-85–90 אחוזים יש להפנות את התינוק באופן מיידי לבית חולים.
בדיקות עזר העומדות לרשות הרופא: צילום חזה בו ניתן לראות תמונה אופיינית מאוד למחלה זו.
בספירת דם ניתן לראות לעיתים עליה של מספר הכדוריות הלבנות - מצביע על תהליך דלקתי ממקור זיהומי.
בבתי החולים בחדרי מיון קיימים תבחינים ספציפיים אותם מספק משרד הבריאות שנועדו לאיתור מהיר של הנגיף מהפרשות. התבחין אמין מאוד והתשובה מתקבלת מיידית. תבחינים אלה נמצאים רק במרכזים רפואיים ובחדרי מיון ולא במרפאות הקהילה (מחיר).
אסתמה לאחר Bronchiolitis
אין ספק כי קיים קשר סטטיסטי בין תחלואה ב-RSV בגיל צעיר והופעת אסתמה. מאות מחקרים נכתבו על נושא זה ולא קיימת תמימות דעים לגבי הדרך בה נגרמת מחלת ריאות כרונית לאחר זיהום נגיפי זה.
לעיתים לאחר סיום המחלה יש צורך במתן טיפול מונע עם סטרואידים (Steroids) בשאיפה או עם חוסמי לויקוטריאנים (Leukotrienes) לשם טיפול בהתקפי קוצר הנשימה.
טיפול
הטיפול בעיקרו הוא טיפול תומך וכולל מתן חמצן בשעת הצורך, אינהלציות של מרחיבי סימפונות, סטרואידים ואנטיביוטיקה בזמן הדבקה חיידקית משנית.
בתינוקות מתחת לגיל שנה מקובל לתת סטרואידים בשאיפה בעזרת מכשיר אינהלצייה. שני התכשירים המצויים בשוק Budicort respules ו-Flixotide nebules. לתכשירים אילו השפעה יחסית קטנה על הקליניקה ורב הוויכוח על הצורך במתן טיפול בסטרואידים למחלה זו.
רוב התינוקות הקטנים מצריכים השגחה בבית חולים תחת ניטור של ריווי חמצן בדם.
הפסקות נשימה הן אחת הבעיות הקשות איתן חייבים להתמודד במהירות ולכן בדרך כלל נוטים לאשפז תינוקות קטנים החולים ב-Bronchiolitis לשם ניטור הפסקות נשימה תחת השגחה רפואית בבית חולים.
חיסון
למרות ניסיונות ארוכי שנים לייצר חיסון פעיל יעיל הרי שחיסון כזה עדיין לא קיים בשוק.
החיסון היחידי הקיים הוא חיסון סביל שהוא נוגדן ספציפי אותו ניתן לתת כמניעה בטרם מתחילה עונת המחלה.
על פי קריטריונים שנקבעו על ידי משרד הבריאות החיסון הסביל ניתן רק לקבוצות אוכלוסייה בסיכון גבוה מאוד – פגים קטנים שנולדו מתחת ל-28 שבועות היריון. זו קבוצת הגיל אותה מכסה סל הבריאות (מחירו העדכני של החיסון הוא כ-1900 שקלים חדשים לפג).
ניתן לרכוש את החיסון באופן פרטי – מחירו באופן פרטי גבוה בהרבה ויכול להגיע ל-3000 דולרים לילד.
החיסון, שאושר לשימוש ב-1999 ומשווק בישראל על ידי חברת Abbott, הוא חיסון סביל, המכיל נוגדנים בדומה לאלה שיילוד בשל מקבל באופן טבעי מאמו, ופעיל כ-30 יום. זיהומי ה-RSV מופיעים לרוב בתקופת החורף; מתן זריקה חודשית של החיסון בתקופה זו מפחית את הסיכון ללקות במחלה ב-80-55 אחוזים, ומפחית את הסיכון לאשפוז בשל הנגיף ב-60 אחוזים.
החיסון הוכנס לסל הבריאות בישראל ב-2001, אך בשל עלותו הגבוהה - כ-35 אלף שקלים לפג לטיפול מלא - הוחלט לתת אותו רק לפגים שנולדו עד שבוע 28 כולל, ושלא הגיעו לגיל שישה חודשים לפני מועד מתן החיסון הראשון. עוד מקבלים אותו פגים החולים במחלת ריאות כרונית ותינוקות עם מומי לב מולדים.
החל מממועד כתיבת מאמר זה (2006) הוחלט שהחיסון יינתן על ידי קופות החולים, ולא בבתי החולים, כפי שהיה נהוג.
אוכלוסיות הנמצאות בסיכון – התוויות לחיסון
פגים ותינוקות עם מחלת ריאות כרונית חשופים יותר לזיהומים בדרכי הנשימה התחתונות, אשר עשויים להוביל לאשפוז. אוכלוסייה זו עשויה גם לסבול מהשפעות ארוכות טווח של התחלואה, כגון אסתמה. אצל פגים הריאות ומערכת החיסון אינן מפותחות. כמו כן, פגים אינם מקבלים מהאם נוגדנים כנגד RSV, שכן עיקר הנוגדנים עוברים מהשבוע ה-35 להיריון. מכאן שפגים נמצאים בקבוצת סיכון, והמחלה עלולה להסתבך אצלם, תוך כדי שהיא עוברת לדרכי הנשימה התחתונות, עד כדי אשפוז בטיפול נמרץ הכולל הנשמה מלאכותית ובמקרים קיצוניים גם למוות. נגיף ה-RSV הוא הגורם הנפוץ ביותר לאשפוז חוזר של פגים.
Palivizumab (Abbosynagis) הוא טיפול למניעת זיהום נגיף RSV. מדובר בחיסון סביל המכיל נוגדנים מוכנים. החיסון הוא תוצר של הנדסה גנטית מגורם אנושי ברובו. הטיפול נמצא בסל הבריאות ומיועד לפגים שנולדו עד שבוע 28, שהשתחררו מבית החולים וטרם מלאה להם חצי שנה. כמו כן, פגים עם מחלת ראות כרונית, עד גיל שנה או שנתיים אם הם תלויי חמצן, זכאים לקבל את הטיפול. בשנה שעברה חוסנו 330 פגים. הטיפול המניעתי ניתן בזריקה חודשית במשך 5 החודשים בהם הנגיף פעיל (נובמבר עד מרץ). בזריקה מוזרק נוגדן ספציפי לנגיף.
על פי המלצות של האקדמיה האמריקאית לרפואת ילדים יש לחסן פגים שנולדו עד שבוע 28 וטרם מלאה להם שנה, פגים שנולדו בשבוע 29–32 וטרם מלאה להם חצי שנה ופגים שנולדו בשבוע 33–35 שטרם מלאה להם חצי שנה ויש להם 2 גורמי סיכון (כגון: אחים קטנים בבית, הורה מעשן ועוד). החיסון מפחית ב-80-55 אחוזים מהאשפוזים הקשורים ל-RSV אצל פגים ומפחית עד כ-57 אחוזים שיעור האשפוזים במחלקה לטיפול נמרץ.
הגנה ביתית כנגד RSV
יש מספר צעדים שהורים יכולים לנקוט כדי לעזור להפחית את הסיכון לזיהום בשל נגיף RSV:
- רחיצת ידיים תכופה של מי שבא במגע עם התינוק
- העברת מוצרי היגיינה משומשים לפח סגור (קיימים פחים אטומים)
- ניקוי וחיטוי של צעצועי התינוק, במיוחד אם ילד אחר שיחק בהם
- שימוש בחדרי שינה נפרדים לתינוקות וילדים בגיל בית הספר במידת האפשר
- הימנעות משהות במעון יום
- שמירת מרחק בין התינוק לבין אדם עם תסמינים של צינון
- הימנעות מעישון בסביבת התינוק/להימנע מעישון בבית
- הימנעות משהות במקומות הומי אדם
לסיכום
מדובר במחלת ילדים הדומה מאוד בהתנהגותה לשפעת קשה שהמחולל העיקרי שלה הוא ה-RSV. רוב הילדים עוברים מחלת חום זו ללא בעיות מיוחדות. הבעיות העקריות במחלה זו היא בשכבת הילדים מתחת לגיל שנה ובפגים. בשתי הקבוצות מחלה זו יכולה להיות קשה מאוד ואף קטלנית. מחלה זו אחראית לחלק לא מבוטל מאשפוזי התינוקות כל שנה בחודשי החורף. ניתן למנוע מחלה זו בקבוצות הגיל הבעייתיות על ידי חיסון סביל וזאת בזמן מגפות. מחירו של החיסון גבוה מאוד. עדיין אין בנמצא חיסון פעיל למחלה זו.
מנינגוקוק (Meningococcus) - Neisseria meningitides
מנינגוקוק ידוע כ"החיידק האלים"
הקדמה
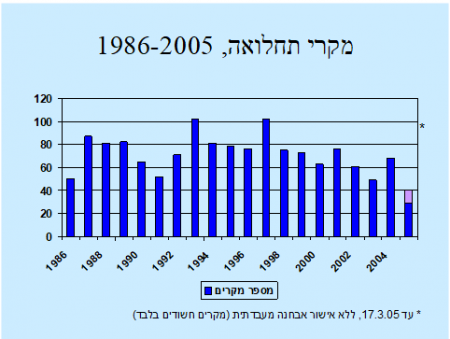
התחלואה בחיידק זה חוזרת לכותרות מידי מספר שנים בשל התפרצויות מקומיות ותוצאתן ההרסנית באותו אזור. בשנות התשעים היינו עדים להתפרצויות קשות באזור הצפון אז נפגעו בו זמנית מספר רב של ילדים בבריכת שחייה באחד הקיבוצים בצפון, לאחר מכן התפשטה המחלה לעיר נהרייה ונמצאה גם במספר כפרים הסמוכים לעיר זו. אחוזי התמותה בשנים אלו עמד על למעלה מ-75 אחוזים ב-24 השעות הראשונות לחשיפה לחיידק.
החיידק בודד וזוהה סופית בשנת 1887. מאותה תקופה מעמיד חיידק זה אתגר קשה בפני הרפואה המודרנית המצליחה לפגוע בחיידק זה רק לאחר חדירתו לגוף על ידי מתן תכשירים אנטיביוטיים יעילים אך לא קיים חיסון יעיל למחלה זו.
שמו המלא של החיידק הוא Neisseria meningitides והוא חיידק עגול וקטן שאינו נצבע בצביעה מיוחדת לחיידקים הנראית צביעת גרם (Gram stain) (מכאן שהחיידק גרם שלילי). עד היום נמצאו 13 זנים שונים של חיידק זה המכונים על פי אותיות. הזנים נבדלים האחד מהשני על פי צורת המעטפת הרב סוכרתית משולבת החלבון שלהם (למעשה על פי חלקי המעטפת המוצגים כלפי חוץ). באימונולוגיה (Immunology) מודרנית אנו משתמשים בצורות הסוכרתיות הנזכרות למעלה לשם יצירת חיסונים ספציפיים כלפי אותם חיידקים.
הזן מסוג B הוא הקשה ביותר ל"טיפול אימונולוגי" (חיסוני) וזאת בשל צורת מעטפת המקשה מאוד על יצירת חיסון. חיידק זה הוא החיידק התוקף ילדים בישראל ובחלק מהמקרים גורם למותם.
החיידק וגוף האדם
החיידק נמצא בבני אדם בלבד ולא בבעלי חיים – זאת אומרת שהאדם הוא המעביר היחידי של החיידק בטבע וגם בית הגידול היחידי של החיידק. מכך עולה כי חלק מהאוכלוסייה הבריאה חייבת לשאת את החיידק באופן קבוע אחרת החיידק היה נעלם מהעולם. אכן כ-5 אחוזים מכלל האוכלוסייה הבריאה נושאית חיידק זה בלוע (בתקופה ללא מגפות) ובתקופת מגפות גדולות שכיחות החיידק הנישא בלוע של ילד בריא לחלוטין יכול להגיע אפילו ל-30 אחוזים מכלל הילדים עד גיל שנתיים. מעניין הוא כי רוב הנשאים הם בוגרים – דהיינו מעל גיל 18 שנים ורוב החולים הם תינוקות – מתחת לגיל שנתיים.
החיידק חודר דרך מערכת הנשימה בהדבקה טיפתית (בדומה לרוב החיידקים). החיידק מתיישב ומתרבה בלוע האדם. סיכויי החדירה של החיידק את רקמות הלוע בהם הוא יושב והגעה למחזור הדם הוא נמוך מאוד בשל היותו חיידק שהגוף מצליח ברוב המקרים לפגוע בו המהירות בכל ניסיון חדירה.
בחלק מאוד קטן מהילדים (אשר לנו כרופאים לא ברור מי מהילדים חשוף יותר ולמה) מתרחשת העברה לדם שם מייצר החיידק מחלה קשה מאוד ולמעשה הופך להיות אלים וטורף. לא ברור מדוע הופך החיידק לאלים אך ברור כי בזמן מגפות אלימותו משתנה בייחוד של זן B (האלים יותר) שהופך תוך שעות ממצב של נשא למצב של מחלה קשה המסכנת חיים.
לכל שאר הילדים הנושאים את החיידק בלוע ולא מתפתחת מחלה פולשנית הרי שתוך מספר ימים יתחילו להיווצר נוגדנים כנגד החיידק ותוך מספר שבועות בודד יהיה הגוף מחוסן לחלוטין בפני החיידק. היות שרוב הנדבקים הם תינוקות עלתה השאלה מתי יורדת כמות הנוגדנים שקבלו מאמם והאם קיימת התאמה לכך במועד ההדבקה. אכן נמצא כי לרוב התינוקות שנולדים חיסון מלא כנגד החיידק שמועבר להם דרך השלייה או בהנקה. בין חצי שנה לגיל שנתיים מתחילה ירידה הדרגתית של החיסון האימהי ומתחילה להיווצר חסינות נרכשת (ראו ערך מערכת החיסון הנרכשת בתחילת הספר). החסינות הנרכשת מקורה בחשיפות אקראיות לחיידק שלא בזמן מגפה בזמן שאלימותו נמוכה יחסות ואז לגוף יש מספיק זמן לייצר נוגדנים המגנים עלינו בזמן הופעת המגפות. נראה כי לכל אותם ילדים שנפגעו מהחיידק בצורה אלימה כל כך לא היו מספיק נוגדנים שהיו אמורים להירכש מוקדם יותר או שמערכת החיסון של אותם ילדים הייתה ירודה יותר (מצב סוציואקונומי ירוד עם רמת תברואה נמוכה). חיידק זה יודע לפגוע לא רק בזמן מגיפות ואף יודע לפגוע סביב השנה באופן אקראי כאשר הוא פוגש מאכסן שלא מצליח לפתח נוגדנים כלפיו.
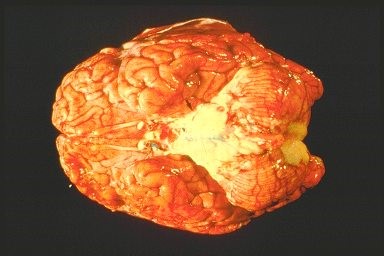
בשל התפתחות של רפואה מונעת יעילה מאוד דלקות של העוצבה (קרום המוח) הפכו לדבר נדיר ורוב התוקפים הם נגיפים שלא גורמים נזק קבוע למוח. לחיידק זה (שאין דרך כרגע לחסן בפני זן B שלו מקום חשוב מאוד ביצירת נזקים קבועים במוח בשל גרימת מחלה פחות אלימה ממנינגוקוקסמיה (דלקת המועברת דרך הדם) והיא דלקת קרום המוח.
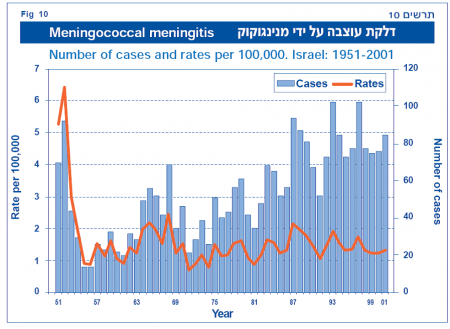
אפידמיולוגיה
בישראל, כ-1,500 איש מתדרדרים מדי שנה למצב של אלח דם (Sepsis) חמור ומבין המקרים כ-50-30 אחוזים מסתיימים במוות (בארצות הברית כ-750,000 מדי שנה). מתוך קבוצה זו בין 60-40 סובלים מאלח דם על רקע פלישה של מנינגוקוק אלים וכל השאר מחיידקים אחרים.
אלח דם חמור הוא זיהום כללי אשר גורם לכשל מערכות וידוע בקרב רופאי היחידות לטיפול נמרץ כגורם העיקרי לתמותה של חולים המאושפזים במחלקות לטיפול נמרץ בבתי חולים.
מספר גורמים מהווים זרז להחמרת הזיהום עד למצב של אלח דם חמור: טראומה שלאחר ניתוחים וטיפולים חודרניים, עמידות של סוגי חיידקים לאנטיביוטיקה, כוויות, תאונות דרכים או מחלות כגון סרטן ודלקת ריאות, כל אלה מחלישים את מערכת החיסון של הגוף. מהירות טיפול היא גורם מכריע בטיפול באלח דם חמור. ידועים מקרים רבים על קושי בזיהוי ואבחון המצב הקליני אשר מוביל למוות מהיר של המטופל. אמצעי הטיפול המקובלים כוללים טיפול בזיהום על ידי מתן אנטיביוטיקה וטיפול תומך לאיבר (מערכת) שנפגע.
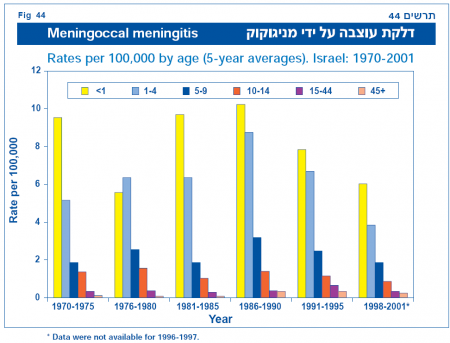
המחלה פוגעת בכל חודשי השנה אך קיימת נטייה לתחלואת יתר בעיקר בחודשי האביב המוקדמים (אפריל–מאי). יותר מ-50 אחוזים מכלל הנפגעים הם ילדים הקטנים מגיל שנתיים. גיל הנפגעים יורד מאוד בזמן מגפות גדולות כאשר אז הזנים הפחות אלימים דווקא שולטים (בעיקר זן A). זן A היווה את הזן השולט במגפות הגדולות לפני מלחמת העולם השנייה אך כמעט נעלם לחלוטין לאחריה.
ההנחה האפידמיולוגית היא כי שינוי חד במצב הסוציואקונומי ושיפורו ב-50 השנים האחרונות עם שיפור ניכר במערכת התברואה בעולם המתועש תרמו במידה ניכרת לירידה ניכרת במספר המגפות.
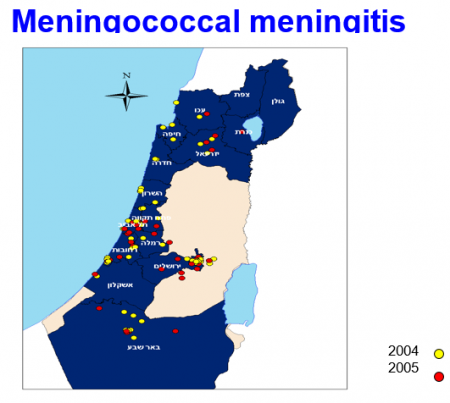
כ-80 אחוזים מכלל ההדבקות בעולם נגרמים על ידי 5 זנים A, B, C, Y ,W135. באירופה שולטים הזנים B ו-C ואחראים לרוב ההדבקות. באסיה ואפריקה רוב ההדבקות מקורן בזנים A,C. בישראל הזנים השולטים הם B ו-Y המהווים את רוב ההדבקות החדשות.
אפריקה היא האזור הגאוגרפי הסובל ביותר מחיידק המניגוקוק האזור המוכה מכונה "חגורת המנינגיטיס" ומשתרע מאתיופיה במזרח ועד לסנגל במערב. באזור זה שכיח הזן A. שכיחות התחלואה באזור זה גדולה פי 100 מאירופה וארצות הברית אחת ל-10 שנים לערך מתחוללת באפריקה מגפה שמעלה את שכיחות התחלואה ל-1000 מקרים לכל 100,000 תושבים. שכיחות התמותה מתחלואה בחיידק באזור זה עומדת על 20 אחוזים.
סוג B פעיל יותר בחורף ואחראי על המקרים המפוזרים והתפרצויות קטנות. הסוג W135 נפוץ מאוד בעולי רגל המקיימים את מצוות החאג' וכל שנה מספר לא מבוטל של עולים לרגל נחשפים לחיידק זה ומתים בזמן החאג'. בישראל נהוג לחסן את כל עולי הרגל למכה.
קליניקה
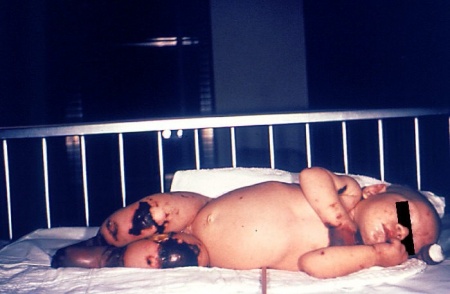
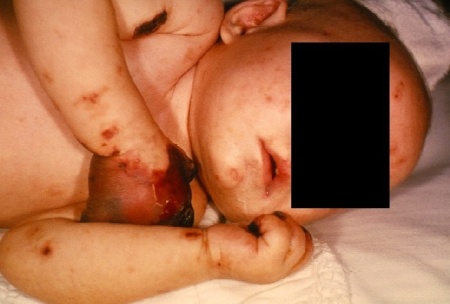
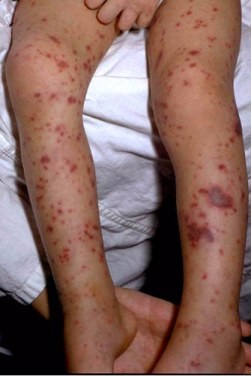
מקור הבעיה הוא במהפך של חיידק נוח ועדין להיות אלים ופולשני ומעבר שלו לתוך מערכת הדם תוך כדי חציית כל המחסומים בדרכו מהלוע. חיידק אלים כזה גורם למחלה קשה מאוד המכונה Meningococcemia הגורמת לאלח דם וזריעה של החיידק לכל אברי הגוף. בשל זריעה מפושטת זו נפגעים רוב אברי הגוף בו זמנית : ראות, מוח, אוזניים, מפרקים, לב, מעי ובלוטות יותרת הכליה. אפילו שרירים ורקמות העור הם אברי מטרה. אין אבר בגוף שלא יכול להיפגע מהחיידק ולכן המחלה מאופיינת בקריסת מערכות מהירה ביותר.
אבחון מחלה זו בשלביה המוקדמים הוא קשה במיוחד ודורש ניסיון רב כיון שלמעשה היא אינה שונה בצורה משמעותית ממגוון מחלות אחרות כמו שפעת או הצטננות רגילה המלווה בחום.
תחילה גורם המנינגוקוק לתסמינים שונים במערכת הנשימה העליונה: נזלת, שיעול קל המלווים בחום גבוה על אלה עשויה להתלוות פריחה כתמית אדומה-כחלחלה על פני העור, שאינה נעלמת בנגיעה קלה. המנינגוקוק עלול לגרום גם לפגיעה במערכת העצבים, עד לירידה במצב ההכרה ופרכוסים.
הנזק נוצר מפגיעה בכלי הדם דרכם הוא עובר–ביציאתו החוצה מכלי הדם הוא יוצר קרישי דם בשל נזק לתאים הנקראים תאי אנדותל (Endothelium) המרכיבים את כלי הדם. פגיעה רב מערכתית כזו בשל ירידה באספקת הדם לרוב אברי הגוף גורמת לקריסה מהירה ולירידה חדה בלחץ הדם.
מלה קשה זו מסתיימת במוות ב-50-15 אחוזים מהחולים כתלות במדינה (במדינת ישראל כ-10 אחוזים תמותה לעומת 50 אחוזים בשנות השמונים). גם כאן חלק גדול מהחולים ב-Meningococcemia חובלים רק ממחלה קלה ורק לחלק קטן מחלה דרמטית וקשה מאוד. לאבחון מצב זה יש צורך בצפייה ישירה של החיידק בדם וזיהוי אנטיגני שלו בצביעות מיוחדות. הבדיקות מבוצעות דרך מחלקת טיפול נמרץ.
מחלה קלה יותר יחסית נצפית אצל כל אלה שהתסמין הראשון שלהם היה התפתחות של דלקת קרום המוח. בחולים אילו המחלה מתחילה בדרך כלל בצורה פתאומית עם כאבי ראש, חום גבוה ובהמשך מופיעים סימני דלק קרום המח הכוללים קשיון עורף, בחילות והקאות. בילדים צעירים מאוד סימני דלקת קרום המח לא אופייניים וכוללים מרפס בולט ופועם, אי שקט ועצבנות, הכרה מעורפלת והתנהגות שאינה מאפיינת אותו. גם כאן ב-75 אחוזים מהמקרים ניתן לבודד בתרבית דם חיידקים. בחולים אילו ניתן לזהות את החיידק בנוזל השדרה בבדיקה המכונה LP (Lumbar Puncture) (ניקור נוזל השידרה).
דלקת ריאות מתחוללת ב-20 אחוזים מהחולים אך דלקת זו די מעטה בתסמינים ממוקדים וקל מאוד לא לזהות אותה בתחילת המחלה.
למעשה הפעולות בחדר המיון די קבועות - בחדר המיון תעברו בדיקת רופא, לאחריה במידת הצורך יבוצע הליך הקרוי "בירור Sepsis מלא" הכולל בדיקות דם, בדיקת שתן, ובדיקת נוזל שדרה – על ידי ניקור מותני לשם איתור החיידקים. בחשד לזיהום בחיידק, לאחר מכן מועברים כל הילדים לאשפוז במחלקה בחדר מבודד או לטיפול נמרץ בזמן אבחון של Meningococcemia, והילד יקבל טיפול אנטיביוטי לתוך הוריד למשך מספר ימים, עד לקבלת תשובה סופית מהמעבדה על סוג החיידק המדויק שצמח בתרבית שנלקחה.
זיהוי החיידק
בחולים החשודים נלקחות תרביות הן מהדם והן מנוזל עמוד-השדרה. תרביות אילו מודגרות בתנאים הנוחים להתרבות החיידק ואם הוא אכן קיים בנוזלים הללו ניתן לזהות אותו בדגימות, לאחר כיומיים.
קיימות בדיקות ישירות לזיהוי הנקראות אימונופלורסצנטיות (Immunofluorescence) – בדיקות אילו מבוצעות מיידית לאחר צפייה ישירה בחיידקים בדם וזאת על מנת לקבל את סוגו המדויק של זן החיידק והערכת הטיפול על פי אלימות החיידק.
מידת הקטלנות של החיידק
בכל העולם המערבי אחוזי התמותה נעים סביב 10 אחוזים - וזאת בעשור השני של המאה ה-21. למרות שיפור ניכר בטכנולוגיה ובטיפול התרופתי הרי שלא חל שום שינוי באחוזי התמותה בעשור זה. נמצאו שינויים קלים בקשר בין גיל החולה לתמותה אך השינויים לא משמעותיים מבחינה סטטיסטית גלובלית.
סיבוכים מהמחלה נפוצים – כ-25 אחוזים מכלל הנפגעים מסיימים עם חסר כלשהו – פגיעה בשמיעה, חסרי עור, נזקים לגפיים, שרירים ועצמות.
טיפול במגעים קרובים
היות שהסיכוי ללקות במחלה לאנשים שבאו במגע קרוב עם חולה ב-Meningococcemia הוא פי 500 מאשר שאר האוכלוסייה הרי שמקובל לטפל בכל הנחשפים.
הטיפול כולל טיפול אנטיביוטי רחב טווח בזריקה לקטנים ובכדור לבוגרים.
מקובל לחסן את כל המגעים הקרובים בחיסון פעיל (במקרה ומדובר במחנות צבא או בתי ספר גדולים).
מניעה וחיסון
עיקר תפקידו של משרד הבריאות הוא ביצירת סגר על אזור נגוע וטיפול אנטיביוטי לכל המגעים הקרובים של החולה. ניראה כי תברואה טובה ומצב בריאות טובה של כלל האוכלוסייה יכולים למנוע חלק ניכר מהמעבר המהיר של החיידק מאדם לאדם ולהקטין את הפיזור הארצי שלו (טיפול ברמה לאומית). תפקידו של משרד הבריאות בחיסון אוכלוסיות ספציפיות של חולים כרוניים הסובלים מהמחלות הבאות או במצבים מיוחדים:
- חולים שעברו כריתת טחול
- חולים עם הפרעה בתפקוד הטחול כגון אנמיה חרמשית (Sickle cell anemia)
- אנשים חסרי טחול מלידה
- חולים המיועדים לעבור כריתת טחול, מתן החיסון לפני כריתת הטחול
- חולים עם חסרים מסוימים במרכיבי המשלים (נקבע על ידיי בדיקות אימונולוגיות מיוחדות במחלקה לאימונולוגיה)
- לחולים עם חסרים במערכת החיסון מסיבות שונות [מחלות של מערכת החיסון וחולי איידס ( AIDS, Acquired Immune Deficiency Syndrome)]
- תיירים לארצות בהן המחלה אנדמית או בהתפרצות עונתית
- חיסון בזמן התפרצות נקודתית של אוכלוסייה בסיכון להדבקה ישירה (בית ספר לאחר הדבקה של אחד הילדים, מחנות צבא וכדומה)
החיסונים הקיימים בישראל הם Mencevax AC, Mencevax ACWY.
החיסונים ניתנים בזריקה תוך שרירית במינון של 0.5 מיליליטר בכל הגילאים. אין הבדל במינון לעומת גיל.
החיסון אסור לחולים הידוע שרגישים לחיסונים, ולחלבון. החיסון מאושר למתן בהיריון רק כאשר שנה התוויה מיוחדת – סיכוי גבוה להדבקה. אישור לחיסון בהיריון חייב להגיע ממומחה בזיהומים או ממשרד הבריאות המחוזי.
תופעות הלוואי מהחיסון מעטות וכוללות נפיחות מקומית, כאב מקומי ואף חום שיכול להתפתח ב 24 השעות הראשונות לאחר החיסון. לא נצפו תופעות לוואי קשות יותר.
טיפול במנינגוקוק
הטיפול המיידי הוא אנטיביוטיקה תוך ורידית כאשר רוב זני המנינגוקוק מגיבים ל-Ceftriaxone
תוך ורידי (Cephalosporine דור III). מתן סטרואידים תוך ורידי הוא חלק מאלגוריתם הטיפול במחלה.
כל החולים מאושפזים במחלקות טיפול נמרץ ללא קשר למצבם תוך כדי מתן נוזלים תוך ורידי וניטור קבוע אחר כל מערכות הגוף.
התרופה Drotrecogin alfa (Xigris), היא תרופה ראשונה מסוגה לטיפול באלח דם חמור, בשל מחירה הגבוה ניתנת רק במקרים מעטים, למרות היותה תרופה מצילת חיים. מדובר בטיפול הניתן בהזרקה תוך ורידית למשך 96 שעות ומפחיתה את הסיכון למוות ב-30 אחוזים. Xigris, מהווה נקודת מפנה בטיפול. מדובר בטיפול לטיפול באלח דם חמור. מדובר ב- Protein C פעיל. התרופה פועלת על 3 מערכות בו זמנית ומיוצרת בטכנולוגיה של ביולוגיה מולקולרית והנדסה גנטית.
סיכום מנינגוקוק
כל התסמינים זהים למחלת חום רגילה וחום כשלעצמו הוא תסמין שכיח אצל תינוקות וילדים, ולפיכך אין צורך בכל עליית חום בטיפול רפואי, שכן ברוב המקרים המדובר בדלקת נגיפית החולפת מאליה. אם בנוסף לחום הגבוה הילד ישנוני, מסרב לאכול, ומופיעה על פני העור תפרחת בצורת כתמים אדומים – כחלחלים שאינה נעלמת למשך שניות לאחר לחיצה קלה באצבעות על המקום, או במקרה של הופעת פרכוסים או חוסר הכרה, יש לפנות לרופא או לחדר מיון מיידית.
אכן יש לגלות ערנות לזיהוי הסימנים שהוצגו למעלה ולהחיש את החולה לקבלת טיפול רפואי. אך למרות ההד התקשורתי והחרדה הרבה עדיין מדובר במחלה נדירה ובחיידק מוכר כך שהפחד מחיידק זה הוא ברוב המקרים מוגזם ונטול בסיס הגיוני.
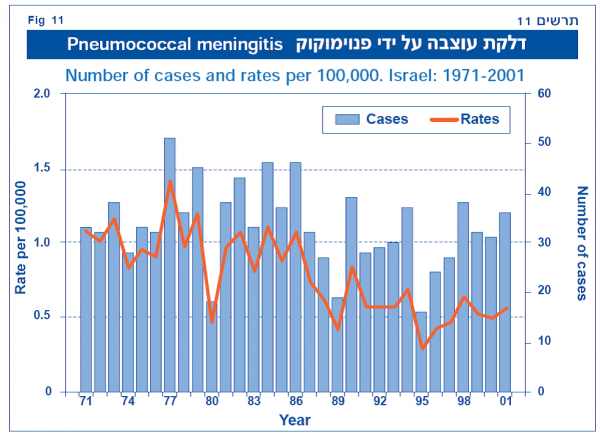
(התרשימים נלקחו מנתוני משרד הבריאות)
פנאומוקוק – דלקת ראות חיידקית/דלקת עוצבה חיידקית
הפגיעה מחיידק הפנאומוקוקוס (Pneumococcus), יכולה לגרום למגוון שלם של מחלות שפגיעתן רעה. המועדים לפורענות הם מבוגרים מגיל 65 ואילך, אלכוהוליסטים, חולי איידס, חולי סרטן, חולים במחלות ריאה, סוכרת ואי ספיקה כילייתית.
החיידק עלול לגרום לדלקות ריאה, אלח דם ולדלקת קרום המוח. אחד מכל 20 חולי דלקת ריאה עלול למות מהמחלה. 2 מכל 10 נפגעים באלח דם ו-3 מחולי דלקת קרום המוח, נפטרים מהזיהום החיידקי.
אם בעבר, Penicillin היה טיפול יעיל וטוב, התפתחו זנים יציבים לטיפול ולכן המניעה על ידי חיסון, היא דרך הטיפול המועדפת.
חיסון נגד חיידק הפנוימוקוקוס
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – חיסון נגד חיידק הפנוימוקוקוס
החיסון מכיל אנטיגנים (חלבונים מעוררי יצירת נוגדנים) מהקופסית הרב-סוכרית של כל אחד מ-23 הזנים של החיידק האחראים למרבית התחלואים ממנו.
3-2 שבועות מהחיסון, מרבית האנשים מפתחים תנגודת לחיידק.
קשישים ותינוקות ולעיתים חולים במחלות ממושכות, עלולים שלא לפתח חסינות.
יעילות החיסון נעה בין 60 אחוזים ל-85 אחוזים.
החיסון ניתן מעל גיל שנתיים, בהזרקה תת-עורית או תוך שרירית, יש להימנע מהזרקה תוך-עורית או תוך ורידית. בדרך כלל מספיקה מנת חיסון אחת, למעט אלו המועדים לפורענות, שיש לחזור ולחסנם במנה נוספת:
- מבוגרים שחוסנו מתחת לגיל 65 יקבלו מנת חיסון שנייה, 5 שנים לאחר מכן
- ילדים מתחת לגיל 10 מומלץ לחזור ולחסן לאחר 3 שנים
- ילדים מעל גיל 10, כמו המבוגרים
התכשירים שבשימוש בישראל: Pneumo 23 ,Pneumovax 23. התכשירים נקנים בבתי המרקחת של קופות החולים עם מרשם מהרופא המטפל.
אוכלוסיית יעד לחיסון
- מבוגרים מגיל 65 ואילך
- אדם מעל גיל שנתיים הסובל ממחלת לב כרונית, אנמיה חרמשית, אלכוהוליזם, דליפת נוזל השדרה, מחלת כרוניות של דרכי הנשימה והריאות (אסתמה), סוכרת או שחמת (Cirrhosis של הכבד)
- אדם מעל גיל שנתיים הסובל מכשל חיסוני (חוסר יכולת של מערכת החיסון להתמודד עם חיידקים), כגון: מחלת Hodgkin, אי ספיקה כילייתית, תסמונת נפרוטית (Nephrotic syndrome), חסר טחול, לאחר השתלת איברים, לימפומה (Lymphoma), לוקמיה (Leukemia), מיאלומה נפוצה (Multiple myeloma) או איידס
- אדם מעל גיל שנתיים הנוטל תרופות המחלישות את המערכת החיסונית, כגון: סטרואידים, הקרנות, טיפולים כימותרפיים (Chemotherapy)
תופעות לוואי מהחיסון
עד 50 אחוזים מהמקרים מופיעים אודם ורגישות מקומיים באזור ההזרקה. לעיתים יש תופעות כלליות של חום, כאבי שרירים, פריחה ותגובות רגישות יתר.
אין לחסן אנשים הרגישים למרכיבי החיסון או נשים בהיריון (למעט מצב של סיכון גבוה).
חיסון מוצמד כנגד פנאומוקוקים Prevenar
החיסון Prevenar, הוכנס לשימוש בשנת 2006. חיסון זה ניתן לתת מתחת לגיל שנתיים והוא ניתן בחלק ממדינות העולם בשגרת החיסונים עם החיסון המחומש. חיסון זה יעיל יותר מ-Pneumo 23/Pneumovax 23. על פי מדיניות משרד הבריאות חיסון זה אינו מוכנס לחיסון האוכלוסייה כולה. החיסון הקיים ניתן רק לאוכלוסייה בסיכון גבוה. יתרון החיסון היא בהצמדתו לחלבון (חיסון מוצמד) חיסון זה מסוגל ליצור זיכרון חיסוני קבוע כנגד פנאומוקוקים מזנים רבים כולל אלה הגורמים למנינגיטיס ודלקת ראות.
יעילות החיסון החדש גבוהה במיוחד במניעה של הדבקה במשפחה בדלקות לוע ואוזניים – בייחוד מונע את הזנים הפולשניים. החיסון מכסה כ-40 אחוזים מכלל הפנאומוקוקים המוכרים.
בטיחות החיסון גבוהה ותופעות הלוואי הבודדות כוללות חום ותופעות לוואי מקומיות של נפיחות חום וכאב במקום ההזרקה.
החיסון ניתן עם חיסוני השגרה ומצורף לחיסון Hib (Haemophilus Influenzae type B). מספר המנות המומלץ תלוי בגיל. מתחת לגיל 6 חודשים; 4 מנות המחולקות עם חיסוני השגרה. בין גיל חצי שנה ועד שנה 3 מנות בהפרש של חודשיים לפחות בין כל מנה. בין גיל שנה ועד גיל שנתיים שתי מנות בלבד. ומעל גיל שנתיים מנה אחת בלבד.
התרופה נכנסה לסל הבריאות בשנת 2006 וניתנת לילדים החל מגיל 8 שבועות ועד גיל 59 חודשים, אשר משתייכים לקבוצות סיכון הבאות:
- הפרעות בפעילות הטחול [אנטומיות (Anatomical) או תפקודיות], כגון כריתת טחול, חוסר טחול מולד, אנמיה חרמשית וכדומה
- ליקויים חיסוניים עקב:
- מחלות ממאירות, כגון לוקמיה ולימפומה
- טיפול מדכא חסינות [כגון הקרנות, חומרים ציטוטוקסיים (Cytotoxic)]
- זיהום HIV
- כל מצב רפואי אחר, המלווה בליקויים של מערכת החיסון
- השתלת איברים, שתל קוכליארי (Cochlear) ומח עצם
- דליפות נוזל חוט שדרה עם סיכון לדלקת עוצבה חוזרת
- אי ספיקת כליות כרונית, תסמונת נפרוטית, טיפול בדיאליזה (Dialysis)
שחפת – Tuberculosis (TB)
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – שחפת
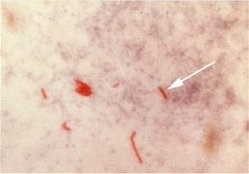
מחולל המחלה הוא מתג השחפת Mycobactericum Tuberculosis, שנתגלה על ידי הרופא הגרמני Robert Koch בשנת 1882. מתג (Bacilli) זה חי גם בבקר וגם באדם. לאדם הוא מעביר את המחלה על ידי רסיסי רוק, ולעומת זאת לבקר הוא מעביר את המחלה על ידי שתיית חלב נגוע.
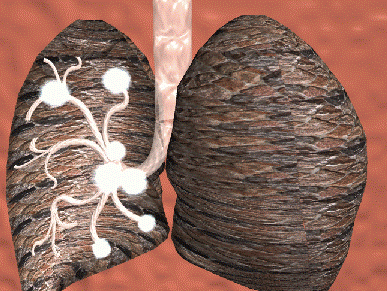
השחפת היא מחלה מידבקת קשה. בעבר הייתה זו מחלה אנושה, אך התמותה כתוצאה ממנה, היא מועטה. כמו כן, בעבר המחלה הייתה נפוצה בעיקר בקרב הנשים, אך היום היא מרובה יותר בקרב הגברים. כאשר מוקד שחפתי נוצר בתוך חלל טבעי וריק, נוצרת מחילה שדרכה עלולים לצאת מתגים נוספים לאיברים שונים בגוף. הסיבוכים השכיחים יותר הם במערכת הלימפה, בכליות, בעצמות ובמחזור הדם.
חיידקי השחפת מתפשטים בקלות כשהם נישאים באידי הרוק באוויר. תרחיף חיידקים זה, יכול להישאר באוויר זמן ארוך. המגע הראשוני בין חיידק השחפת לאדם נגרם מזיהום טיפתי מחולה שחפת הנשאף לדרכי הנשימה. חיידק השחפת נישא בתוך חלקיק של לכלוך או אבק דרך מערות האף, יחד עם האוויר הנשאף. החיידק עובר מהאף אל דרכי הנשימה, משם יורד במורד קנה הנשימה, אל הראות. האוויר מזוהם בחיידקים ממלא את חלל הריאה. אם חיידק זה לא נקטל מיד על ידי מקרופאג'ים (Macrophages) הנמצאים ברקמות. הוא יתרבה בתוכם. ובמקביל תתפתח תגובה חיסונית תאית, ורגישות יתר מאוחרת. עקב פעילות של המקרופאג'ים והלימפוציטים יתהווה נמק גבינתי מקומי שבו חיידקי השחפת אינם יכולים להתחלק.
חיידקי השחפת יכולים להישאר רדומים במשך שנים במצב זה כגרנולומה (Granuloma). התוצאה היא השתלטות הגוף על הזיהום הראשוני ופיתוח חיסון מפני זיהום נוסף. אך אם יש ירידה בתפקוד מערכת החיסון, החיידקים הכלואים בתוך הדופן מתחילים להיות פעילים ולהתרבות. כשהחיידקים הופכים פעילים הם מתרבים ומתפשטים בדרכי הנשימה. על ידי עיטוש ושיעול ידביק חולה זה (שהוא עתה חולה פעיל) את המצויים בסביבתו. במצב זה יש התפרצות של מחלת השחפת. שחפת היא מחלה קשה ולעיתים אף קטלנית. מחלת השחפת פוגעת בראות ובאיברים אחרים. סימניה הקליניים הם עייפות אובדן תיאבון ומשקל, חום נמוך, הזעת לילה כאבי פרקים שיעול יבש המתפתח לשיעול ליחתי ודמי.
למחלת השחפת עלולות להיות תגובות אלרגניות, בעיקר בגלל הרעל שמייצר המתג, כגון גבשושיות שחפת (Tuberculum).
- ישנם כמה סוגים נוספים של מתגי שחפת
- מיקובקטריום תוך תאי (Mycobactericum Intracellular). המצטיין ביציבות ניכרת נגד תרופות
- מיקובקטריום קנזסי (Mycobactericum Kansasii
היסטוריה של מחלת השחפת
ההיסטוריה של מחלת השחפת מתחילה בימי קדם, ומקורה כנראה בביות הבקר. נתגלו שרידי גופות בני אדם קדמונים (מסביבות שנת 4000 לפני הספירה) שסבלו משחפת. נמצאו גם מומיות מצריות (מסביבות 3000-2400 לפני הספירה), עם גבשושיות המאובחנות כגבשושיות שחפת. התייחסויות מצד סופרים והיסטוריונים, וגם מכתובות קיר קדומות מגילות, מראות שגם בהודו המחלה הייתה נפוצה מסביבות שנת 2000 לפני הספירה. כמו כן, באותה התקופה היא הגיעה גם לאמריקה הצפונית ואמריקה הדרומית. כמה צורות של המחלה היו קרוב לוודאי ידועות ליוונים הקדמונים. Hippocrates, הרופא היווני הקדום, מזהה את שחפת הריאות כמחלה נפוצה באותה התקופה, ורוב הזמן - גם קטלנית.
מכיוון שהמחלה מתאפיינת בתסמינים רבים, לא זיהו אותה כמחלה אחידה עד לשנת 1820 בערך, ולמעשה - עד שנת 1839 כלל לא קראו לה שחפת.
בית ההבראה (Sanatorium) הראשון לחולי שחפת הוקם בפולין בשנת 1859. שנים אחריו הוקם מוסד דומה בארצות הברית בשנת 1885.
גורם השחפת נתגלה על ידי Robert Koch שפרסם את תגליתו ב-24 במרץ 1882, וקיבל על ממצאיו פרס נובל לרפואה לשנת 1905. Koch גילה כי הבקר נדבק בשחפת על ידי חלב נגוע ובני האדם נדבקים דרך רסיסי רוק. גורם ההידבקות מידי חלב נגוע סולק באמצעות תהליך הפסטור. Robert Koch הכריז בשנת 1890 ברבים שתמצית Glycerin (שמן מתוק ושקוף המשמש לרפואה, לייצור מזון ולתעשיות שונות אחרות) יכולה לשמש כ"תרופה" לשחפת. הוא קרא ל"תרופה" זו בשם Tuberculin.
ההצלחה האמיתית הראשונה בחיסון ונטרול השחפת התרחשה בשנת 1906 על ידי Camille Guérin ו-Albert Calmette כאשר הם החלישו מתגי שחפת של בקר, ועל ידי זה פיתחו תרופה לבקר. לאחר מכן, והצליחו השניים להרכיב תרופה, שבני אדם השתמשו בה לראשונה בצרפת, ב-18 ביולי, שנת 1921.
מחלת השחפת מיקדה את עניין הציבור במאה ה-19 ובתחילת המאה ה-20, כמחלה נפוצה באזורים העירוניים העניים. בשנת 1815 אחד מכל ארבעה מקרי מוות באנגליה נבע משחפת; בשנת 1918, עדיין אחד מכל שישה ממקרי המוות בצרפת היה כתוצאה מהמחלה. לאחר שהוכח בשנות ה-80 של המאה ה-19 שמחלת השחפת היא מדבקת, היא הוכרזה כמחלה שיש להודיע עליה בבריטניה; עניים שנדבקו במחלה "עודדו" להיכנס לבתי הבראה, שדמו ברובם לבית כלא. למרות התועלת של האוויר הצח והעמל שבבתי ההבראה, 75 אחוזים מהחולים בשחפת שהיו בבתי ההבראה השונים, נפטרו במהלך חמש שנים.
התקיימו מבצעים למניעת יריקה במקומות ציבוריים, שכן המחלה מועברת ברוק, ולשימוש במרקקות - כלים מיוחדים אליהן ניתן היה לירוק. שיפור בבריאות הציבור הביא לצמצום מקרי המוות כתוצאה ממחלת השחפת, וזה עוד לפני המצאת האנטיביוטיקה. באירופה, כמות האנשים שמתו משחפת ירדה מ-500 לכל 100,000 אנשים בשנת 1850 ל-50 אנשים מכל 100,000 בשנת 1950. אך העבודה לא תמה, וכך למשל הפרויקט הראשון של מועצת המחקר הרפואית הבריטית שהוקמה ב-1913 עסק במחלה.
רק בשנת 1946, כאשר פותחה התרופה האנטיביוטית Streptomycin, נוצר טיפול יעיל לריפוי המחלה. ובשנת 1952 התגלתה גם יעילותו של ה-Isoniazide כתרופה אנטי-שחפתית יעילה.
למחלת השחפת מיוחסים מספרי פטירות גדולים יותר מאלו המיוחסים למחלת איידס, מלריה (Malaria) ומחלות טרופיות (Tropical) יחדיו, כאשר 300 אלף מתוכם הם ילדים. כל שנייה נדבק עוד אדם ברחבי העולם משחפת, שהיא המחלה המידבקת הקטלנית ביותר בעולם, והיא אחראית ל-25 אחוזים מכלל הפטירות ממחלות הניתנות למניעה במדינות המתפתחות. 1.7 מיליארדי בני-אדם בעולם מודבקים היום עם חיידק השחפת שהם למעלה מרבע מאוכלוסיית העולם. אדם הנושא את חיידק השחפת, ללא סימני מחלה או שאף אינו מודע לכך, שאינו מטופל תרופתית, ידביק עשרה עד חמישה-עשר איש בסביבתו הקרובה מדי שנה. שחפת שהייתה בקו ירידה במדינות מזרח אירופה משך 40 שנה, מרימה שם היום ראשה ומספרי הנדבקים בה בעליה מתמדת. ארבעים אחוז מנשאי הנגיףHIV בעולם מודבקים בחיידק השחפת, ולמעשה החיידק מהווה את גורם המוות של כ-1/3 מנשאי נגיף האיידס בעולם הנפטרים ישירות מסיבוכי השחפת.
אך חיידק השחפת התגלה כקשה לריפוי, ותוך שינוי מתמיד של הרכבו הגנטי, פיתח עמידות לתרופות אלה או לחלקן. בהמשך הוכנסו תרופות חדשות למלחמה בחיידק: Pyrazinamide וכן Rifampicin שהוכנס לשימוש בשנת 1967, הביאו לירידה מסוימת בשעורי הנדבקים בחיידק, אם כי יש המייחסים את הירידה בתחלואה לשיפור תנאי המגורים וההיגיינה בעולם. דווקא כיוון שהמחלה נחשבה כמחלתם של חלכאים ועניים בעולם השלישי, חברות התרופות המובילות איבדו עניין בפיתוח תרופות חדישות נגד שחפת, שכן ההערכות הכלכליות לא היו אופטימיות, והמחלה נחשבה לנכחדת בארצות המתועשות-העשירות. אך מבחינה גלובאלית, אין כזכור גבולות בין מדינות מתפתחות למפותחות, ובעידן של תיירות מערבית מפותחת למדינות אסיה ואפריקה, חיידקי השחפת נישאו במהירות מקצה העולם ועד קצהו, מהלך שעות ספורות.
וכך קרה, שהמחלה שדעכה במערב, החלה לנסוק במהלך שנות ה-90 של המאה הקודמת. בצרפת למשל, בה כונתה שחפת ה"מגפה הלבנה", והיא הוזכרה שם במונחים נוסטלגיים, זוהו בשנת 1993 כ-10 אלפי מקרים חדשים של המחלה, וכמאה איש מתים ממנה בצרפת בעשור האחרון, מדי שנה. מספר מקרי שחפת באנגליה עולה בהתמדה ב-15 השנים האחרונות, ובמספר אזורים שם שעורי השחפת דומים לאלה שבהודו. לא פלא אפוא שההתייחסות לחיידק זה היא כאל "פצצת זמן רפואית". הבעיה העיקרית היא בכך שכ-50 מיליון איש המודבקים בחיידק השחפת בעולם, נושאים חיידק שפיתח עמידות למכלול התרופות האנטיביוטיות שפעם היו יעילות כנגדו. למעשה חזרנו עם חיידק השחפת לנקודת המוצא: מספר המתים בעולם מהמחלה דומה לזה ששרר בשנת 1882, כאשר Koch גילה את החיידק. אם אמנם 1.7 מיליארדי איש בעולם, או 27 אחוזים מהאנושות נושאים חיידק זה, כיצד ייתכן שרק 3 מיליונים מתים מדי שנה? מסתבר כי 90 אחוזים מהמודבקים בחיידק אינם מפתחים מחלה, כיוון שמערכת החיסון שלהם מונעת את "התלקחות" החיידק בגוף, במנעה את התרבותו. אך במדינות תת-הסהרה באפריקה (Sub-Saharan Africa), באסיה, מזרח אירופה ודרום אמריקה בהם שעורי הנשאות של נגיף HIV ומחלת איידס הגיעו לממדים מבהילים, זוכה חיידק השחפת לעדנה.
ואמנם נגיף HIV המשמיד לימפוציטים מסוג CD4+ תאי מפתח בחיסון התאי, מסייע להתפרצותו של חיידק השחפת ובמדינות, צמד קטלני זה של נגיף וחיידק עושה שמות באוכלוסייה שם. כיוון שחיידק השחפת תוקף בדרך כלל אנשים צעירים בטווח הגילים 15 עד 45 שנה, מהווה הדבר מהלומה קשה למדינות המתפתחות המתבססות על כוח עבודה פיזי-צעיר. חשוב לציין, שטיפול תרופתי בנשאי חיידק השחפת, לפני שפרצה בהם המחלה, הוא זול להפליא, ומדובר בתרופות שעלותן אינה עולה בממוצע על 13 דולרים לאדם. כן נמצא שהיחס: עלוּת-יעילוּת של הטיפול בנשאי חיידק השחפת היא מהגבוהות ביותר בין כל סוגי הטיפולים התרופתיים, בדומה למשל לטיפול במחלת שלשולים בילדים בשתיית תמיסה למניעת התייבשותם. לכן כה קריטי לגלות את האוכלוסייה שנדבקה במתג השחפת, ולטפל בה בשלב מוקדם לפני הגיעה לדרגת מחלה שהטיפול בה קשה אם בכלל אפשרי.
המבדק לזיהוי חיידק שחפת סמוי פותח כאמור לפני למעלה מ-120 שנים על ידי Koch, והוא נחשב למבדק האבחוני הוותיק ביותר ברפואה. למרות מגבלותיו הידועות של מבחן העור הידוע כתבחין Tuberculin, לא הייתה לו חלופה אמינה. וכך משך למעלה ממאה שנים נשתמרה שיטת אבחון שרגישותה והספציפיות שלה לא היו מהגבוהות, וכך הוחמצו לבטח אינספור מקרים, או אף ניתנו טיפולים תרופתיים לכאלה שלא היו כלל זקוקים להם. בתבחין Tuberculin מזריקים אל תוך תת העור תמצית של חומר המופרש בתרבית גידולו של חיידק השחפת, ותמצית זו מכילה מעל-200 אנטיגנים האופייניים לחיידק זה. באנשים הרגישים לחיידק, תתפתח על פני העור באזור ההזרקה, תגובת רגישות-יתר אופיינית תוך הופעת נפיחות ואדמומיות תוך 2–3 ימים, כאשר נפיחות העור מעבר לממדים מסוימים נחשבת כתגובה "חיובית". אך מגבלות שיטה זו רבות: אנשים שהיו מודבקים בעבר בחיידקי Mycobacterium סביבתיים בלתי-אלימים, יגיבו אף הם באופן חיובי למבחן העור, ולעומתם אנשים המודבקים באופן סמוי עם חיידק השחפת ואינם מגיבים למבחן זה בגלל פגם או "חולשה" של מערכת החיסון בהם.
כך למשל אנשים החיוביים לנגיף HIV, מושתלי איברים שונים המטופלים ב-Cyclosporine להחליש את מערכת החיסון למניעת דחיית השתל, אנשים חולי סרטן המקבלים טיפול כימי וקרינתי, או כאלה עם דלקת מפרקים שיגרונתית (Rheumatoid arthritis) המטופלים בתרופות נוגדות TNF (Tumor Necrosis Factor). למגינת הלב, דווקא כל אלה שצוינו, הם בדרגת סיכון גבוהה יותר להידבק החיידק השחפת, בגלל חולשת מערכת החיסון בהם, אך אלה גם יגיבו באופן מוגבל אם בכלל לתבחין ה-Tuberculin. קשה מאוד גם להעריך באופן סטנדרטי את עוצמת תגובת העור. ואי הנוחות הכרוכה בביקור מעבדה נוסף לאחר יומיים-שלושה, עם האפשרות להתפתחות שלפוחית מכאיבה, או אף צלקת קבועה.
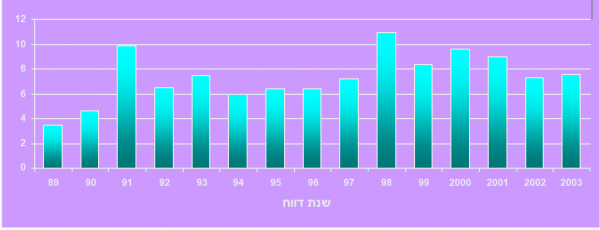
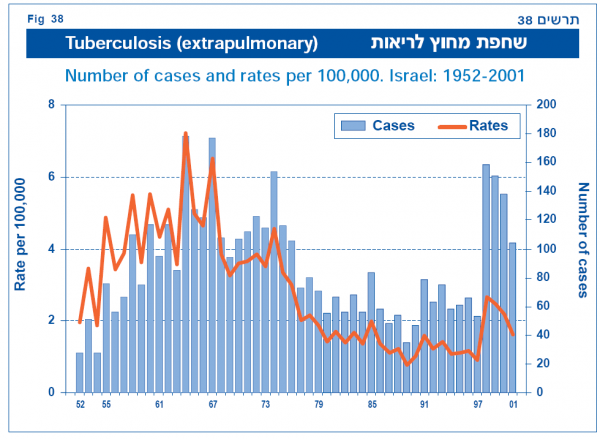
שכיחות השחפת בישראל
בישראל נמצאו בשנת 2003 כ-550 חולים חדשים הסובלים משחפת.
אבחון השחפת
תבחין Tuberculin
ערך מורחב – תבחין טוברקולין בשיטת המנטו - (Tuberculin test (mantoux
תבחין ה-Tuberculin ידוע גם בשם מבחן מנטו (Mantoux) יכול לזהות את מרבית החולים 6–8 שבועות לאחר חשיפתם לחיידק השחפת.
- למי מבצעים תבחין Tuberculin?
- אנשים הנמצאים במגע יום יומי עם חולי שחפת פעילה
- חולים בעלי תסמינים של שחפת כגון: שעול ממושך, חום, אובדן משקל, הזעת לילה, עייפות כרונית או אובדן תיאבון
- אנשים בעלי חסינות ירודה כגון חולי איידס
- ביצוע התבחין
מזריקים כמות קטנה של חומר חלבוני בלתי מזיק של חיידק השחפת - PPD (Protein Purified Derivative) בהזרקה תת-עורית. התגובה בעור נבדקת 48–72 שעות לאחר ההזרקה.
- משמעות העדר תגובה בעור
- האדם הנבדק לא נחשף לחיידק השחפת
- הבדיקה נעשתה קרוב מידי למועד החשיפה או החשד להדבקה ויש לחזור עליה לאחר 3 חודשים
- תגובה חיסונית ירודה למרות הדבקה
- משמעות תגובה חיובית לתבחין
תגובה חיובית משמעותה הופעת אודם בקוטר מסוים באזור ההזרקה. כאשר האודם מתחת ל-5 מילימטרים המבחן נחשב כשלילי (אין חשיפה לחיידק). כאשר קוטר הפריחה מעל ל-10 מילימטרים התבחין חיובי. תבחין חיובי מעיד על המצאות חיידק השחפת בגוף. המצאות החיידק בגוף אינה מעידה על מחלה פעילה.
- מציאת חיידקיי שחפת באדם בריא - הכיצד?
כאשר החיידק חודר לגוף ומעורר תגובה חיסונית כנגדו המתבטאת בין השאר ביצירת "חומה" המבודדת אותו מהתפשטות לרקמות שונות. החיידק מצוי בגוף בצורה בלתי פעילה ולכן האדם אינו חולה. תבחין ה-Tuberculin יהיה חיובי במצב זה. אדם שקיבל חיסון כנגד שחפת יראה תבחין Tuberculin חיובי למרות שאינו חולה.
- תבחין מנטו חיובי - השלכות
- תבחין שלילי – אין צורך בנקיטת פעולה
- תבחין חיובי – יש לבצע צילום חזה
- תבחין חיובי בנוכחות צילום חזה חיובי יש להניח שהחיידק קיים בצורה בלתי פעילה. בתלות הגיל יש לטפל על מנת למנוע מחלה בעתיד
- צילום חזה תקין אך יש תסמינים המחשידים לשחפת –יש לבצע מבחנים נוספים
- צילום חזה אינו תקין –יש לוודא האם מדובר בשחפת או במחלה אחרת
- תופעות לוואי לתבחין
נדירות, כאשר אדם חולה בשחפת הוא עלול לפתח תגובות עור מוגזמות.
תבחין Clinispot TB
בתבחין זה נספרים לימפוציטים T מדמו של הנבדק, המפרישים את החומר Interferon Gamma כאשר מביאים אותם במגע עם אנטיגנים ספציפיים ביותר לחיידק השחפת Micobacterium tuberculosis. נוכחות תאי T כאלה, מעידה על הדבקה בחיידק זה, גם אם אין עדות קלינית של מחלה פעילה. לביצוע המבדק נוטלים מעט דם ורידי, מפרידים את תאי הדם הלבנים מן הכדוריות האדומות, ומדגירים את התאים הלבנים עם אנטיגן חיידק השחפת, בתוך בארות של פלטות ELISA(Enzyme-Linked Immunosorbent Assay). אם אמנם תאי T הם של אדם מודבק בחיידק, הם משופעלים על ידי אנטיגן השחפת ומפרישים בתגובה Interferon Gamma. חומר מופרש אחרון זה מזוהה על ידי נוגדנים ספציפיים ל-Interferon Gamma, ואת נוגדנים אלה ניתן להעריך באופן כמותי על ידי סמן כימי צבוע. תבחין Clinispot-TB זה מראה רגישות גבוהה בהרבה בהשוואה לתבחין ה-Tuberculin העורי, גם באנשים בעלי מערכת חיסונית מוחלשת, ואלה שתבחין ה-Tuberculin בהם פוענח כשלילי. האנטיגן החלבוני המאוד ספציפי ל-Mycobacterium Tuberculosis השחפתי מקודד על ידי אזור בגנום (Genom) של חיידק זה הידוע כ-RD-1, שאינו מופיע בחיידקים אחרים ממשפחת ה-Mycobacteria (M), כמו למשל M. Bovis או החיידק התוקף עופות M. Avium.
המבדק נוסה ב-15 ניסויים נפרדים על סך של מעל 3,000 נבדקים ב-11 מדינות, ונמצא באופן שאין מובהק ממנו כעדיף על תבחין ה-Tuberculin העורי, גם בחולי שחפת סמויים עם מערכת חיסון פגומה ביותר וכן בילדים מודבקים, בהם השיעור של מבחן עור "שלילי" גבוה יחסית. גם בנבדקים מודבקים ללא מחלה ריאתית רגישות המבדק החדש הייתה של 96 אחוזים, כאשר באותם נבדקים רגישות מבחן העור הייתה רק 69 אחוזים. ב-Zambia, בה אחוז גבוה במיוחד של חולי איידס מודבקים גם בחיידק השחפת, מקום שם רגישות מבחן העור אינה עולה על 30 אחוזים בגלל הכשל החיסוני החריף, תבחין Clinispot-TB הראה רגישות של 92 אחוזים.
במקרה שהתפרסם בבריטניה, בה תלמיד נגוע בשחפת שהה תקופה ארוכה בקרבה לעשרות רבות של תלמידים אחרים, נתן המבדק החדש תוצאות מרשימות בדִיוּקָן כאשר נבדקו בו 535 תלמידי בית הספר האמור. לעומת זאת תבחין העור החמיץ אחוז גבוה של תלמידים שבדיעבד נמצאו כנגועים בחיידק. כעת מתוכנן סקר המוני בקרב אוכלוסיית יעד שסיכוייה להידבק בחיידק גבוהים יחסית כגון אנשי צוות רפואי וסיעודי בבתי אבות או במוסדות לחולי-נפש, בקרב מהגרים ממדינות עם אחוז גבוה של נגיעוּת בשחפת, אנשי צבא, אסירים וסוהרים, ועוד. המבדק החדש מבוסס כאמור על נטילת דם פשוטה, בניגוד לצורך שהיה קיים עד היום להוכחה ישירה של נוכחות חיידק שחפת חי המצוי בתפליטי חומר מהריאות שלא קל להשיג, לא כל שכן לבודד מתוכם חיידק פעיל. אין כל ספק שהמבדק החדש יחולל מהפכה ושיפור ביכולת לגלות מקרי שחפת סמויים קדם-קליניים, שרב הסיכוי לטפל בהם באנטיביוטיקה מתאימה ולהכחיד בהם את חיידק השחפת. ומי יודע אולי זו תחילתו של עידן חדש במלחמה שתנהל האנושות בחיידק קטלני כל כך, והוא אף ערמומי ביכולת ההדבקה "השקטה" שלו.
חיסון נגד חיידק השחפת
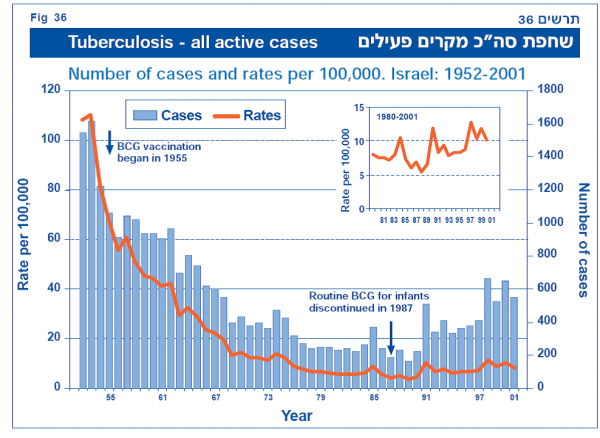
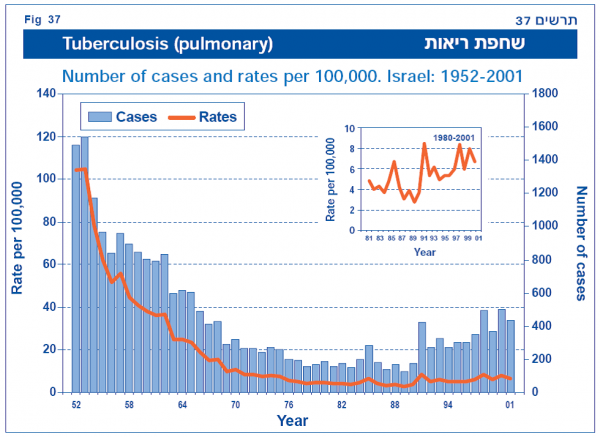
ערך מורחב – חיסון ב.ק.ג - BCG
ניתן לחסן נגד חיידק השחפת באמצעות חיסון ב-Bacille Calmette Guerin) BCG) כדי לגרום ליצירת זיהום ראשוני מחיידק מוחלש, ובכך למנוע הדבקה בחיידק האלים. ה-BCG הוא חיסון באמצעות זן שחפת פרות שהוחלש מעבדתית. בטיחותו ויעילותו של החיסון שנויים במחלוקת למרות עשרות שנות שימוש.
החיסרון הגדול של החיסון: הופך את מקבליו לבעלי תבחין Tuberculin חיובי.
- החיסון אינו מאפשר שימוש בתבחין ה-Tuberculin כאמצעי לסריקה ואיתור חולים
- אין לחסן אנשים בעלי תבחין Tuberculin חיובי מחשש להתלקחות מחלה רדומה
- תופעות לוואי
כחודש לאחר מתן החיסון יכולים להופיע באזור ההזרקה אודם, נפיחות והגדלת בלוטות הלימפה (Lymph nodes) האזוריות (היווצרות קומפלקס ראשוני). תופעת לוואי נדירה היא התפתחות מורסה באזור ההזרקה. יש לבצע מעקב אך לרוב אין מטפלים בה. הטיפול הוא באמצעות חבישה מקומית והרטבות קרות. ניתן בדרך כלל לראות באזור המורסה סינוס (Sinus) מפריש. ההפרשה היא סרוטית (Serous) דמוית מוגלה אך אין הדבר מחייב טיפול אנטיביוטי אלא במקרה של זיהום חיידקי אחר, במקרה זה, מקובל לקחת תרבית מהנוזל.
DOTS - הריפוי לכולם
- הטיפול התרופתי נקבע על ידי הרופא במרכז למחלות שחפת/מרכז למחלות ריאה
- יש לקחת את הטיפול באופן סדיר ומלא (לפחות 6 חודשים) בהשגחה ישירה (DOTS, Directly Observed Therapy Short Course)
- כל הפסקה או אי השלמת טיפול עשויה לגרום להישנות המחלה ואף להתפתחות זנים עמידים לתרופות
- החולה מגיע למעקב במרכז לשחפת, אחת לחודש, לבדיקת רופא, בדיקת אחות ובדיקות נוספות
הטיפול בחולי שחפת הוא בשיטת טיפול בהשגחה ישירה: DOT
טיפול בהשגחה ישירה מתבצע באמצעות מערך של משגיחים.
משגיח - אדם המכיר את החולה, לא מבני משפחתו, והביע הסכמתו להיות אחראי על מתן הטיפול באופן קבוע ומוסכם על החולה, על מרכז השחפת ועל נציג לשכת הבריאות. על פי רוב הטיפול ניתן על ידי אחיות קופת החולים.
המשגיח (נותן הטיפול) מקבל את פרטי המטופל ואופן הטיפול בעל-פה ובכתב.
התרופות נשלחות למשגיח על ידי שליח בצרוף דף הנחיות הטיפול, חתום על ידי רופא המלש”ח ודף חתימות.
דף ההנחיות ודף החתימות מתויקים בקלסר המיועד לחולי שחפת בלבד.
המטופל בולע את התרופות בנוכחות המשגיח, המשגיח מאשר בציון שמו המלא בדף החתימות, את לקיחת התרופה על ידי המטופל בכל יום. כל זאת רק לאחר שראה כי המטופל בלע את כל התרופות.
- אירועים המחייבים דיווח מיידי של המשגיח למלש”ח
- דיווח של המטופל על תופעות לוואי
- קושי בנטילת התרופות
- אי הגעת המטופל לקבלת טיפול במועד שנקבע
שחפת טיפול מונע
- למי שמוגדר כמגע הדוק של חולה שחפת פעילה ומדבקת, מומלץ לתת טיפול מונע, מכאן החשיבות בקביעה ברורה מי הוא המגע ההדוק מתוך כלל המגעים של חולה שחפת
- הטיפול ממושך, שישה חודשים, בגלל אופיים של חיידקי השחפת המתרבים באופן איטי מאוד. הטיפול התרופתי פעיל נגד החיידקים רק בשלב ההתרבות
- טיפול מונע לקטין עד גיל 18 שנים יינתן בהשגחה ישירה -DOT ולא על ידי בני משפחתו
(הגרפים נלקחו מנתוני משרד הבריאות)
כלבת
ערך מורחב – כלבת - Rabies
כלבת היא מחלה נגיפית קטלנית התוקפת את מערכת העצבים.
המחלה תוקפת לא רק את גזע הכלביים, כפי ששמה עלול לרמז, אלא את כל היונקים, כולל האדם. הגורם למחלה הוא נגיף המועבר לרוב בנשיכה מבעל חיים נגוע לבעל חיים אחר. מגע עם רוק הוא דרך ההדבקה המשמעותית ביותר, לרוב דרך נשיכה אך ייתכן שגם במעבר דרך מגע רוק עם העין, האף או הפה. הנגיף מגיע ממקום הנשיכה אל המוח דרך תאי העצב המובילים אליו.
בטבע קיים מאגר של נגיף הכלבת בעיקר בתנים, זאבים, שועלים, חולדות ועטלפים, ובעלי חיים נגועים עלולים לשמש כווקטורים המעבירים את הנגיף ולהדביק גם בני אדם הבאים עימם במגע.
נגיף הכלבת הוא נגיף RNA (RiboNucleic Acid) חד-גדילי מקבוצת Rhabdoviriae וצורתו דמוית קליע. הוא לא מגיע למוח דרך מחזור הדם אלא דרך סיבי עצב קרועים, על כן הוא קשה יותר לאבחון. הנגיף מתקדם במעלה מערכת העצבים אל המוח. כל עוד הוא לא הגיע למוח, בעל החיים נקרא נשא. קצב התקדמות הנגיף במערכת העצבים הוא כסנטימטר ליום. קצב התפרצות המחלה תלוי במיקום הנשיכה. הנגיף נקשר לתאי המטרה ככל הנראה באמצעות הקולטן ל-Acetylcholine - הממלא תפקיד מפתח בהעברת אותות מן העצב אל השריר.
מהלך המחלה ותסמיניה
אל מערכת העצבים המרכזית מגיע הנגיף תוך כדי נדידה דרך האקסונים (Axons) המובילים אליה, ושם תוקף אזורים במוח הגדול האחראים להיבטים מסוימים של ההתנהגות (המערכת הלימבית, Limbic system). כדי להתרבות זקוק הנגיף לרקמת מוח של יונק. מרגע שהנגיף הגיע למוח, המחלה מתפרצת והמוות הבלתי-נמנע מגיע תוך עשרה ימים. כשהנגיף מגיע לתא במוח הוא חודר אליו ומזריק את החומר הגנטי שלו לתא, ובכך אוכף על התא לייצר נגיפים נוספים. הנגיפים פורצים החוצה ומדביקים תאים נוספים תוך הרס התא שיצר אותם. כתוצאה מכך ישנו תהליך התמוססות של אזורים שלמים במוח היונק במה שנקרא "נמק גבינתי" (בדומה לגבינה שווייצרית). התוצאה היא שיטיון (Dementia).
אחד הסימנים הראשונים של המחלה הוא שינוי התנהגותי. לדוגמה: כלב ידידותי הופך לתוקפני, ולהפך. חיות בר נזהרות בדרך כלל מבני אדם; אם חיית בר ניגשת לבני אדם מיוזמתה, היא עלולה להיות נגועה במחלה. ככל שמתקדמת המחלה, חלק מהנגיפים יורדים דרך עצבי הפנים ומגיעים לבלוטות הרוק. זה הרגע בו הקורבן מתחיל להדביק באמצעות הרוק (לדוגמה, דרך נשיכה). בשלב הבא, הנגיף יורד לכיוון שרירי הבליעה. התוצאה היא שהוא ימנע מלבלוע ולכן הרוק יוצא החוצה וישנו ריור מוגבר. מאחר שמאוד כואב לו לבלוע, הוא ימנע מלשתות מים למרות הצמא. לאחר מכן מתחיל להתפתח שיתוק בכל רחבי הגוף, שיתוק שרירי הנשימה ומוות.
שני סוגי תגובות מאפיינים את המחלה: סוג אחד הוא תגובה סוערת המאופיינת בריצה בלתי מבוקרת למרחקים ארוכים, בתוקפנות רבה, בנגיסה בעצמים שונים ובאובדן כושר השיפוט. סוג התגובה השני רגוע למדי ומלווה בדיכאון, שיתוק והתנהגות מוזרה.
חיסון לכלבת
הכלבת מוגדרת בספר השיאים של גינס כמחלה הקטלנית ביותר; אחוזי התמותה מרגע ההתפרצות מגיעים לכדי 100 אחוזים (למעשה קיימות מחלות רבות בעלות תמותה ודאית, אך רובן אינן זיהומיות כי אם תורשתיות). את הכלבת ניתן לעצור עוד לפני התפרצותה, זאת באמצעות חיסון.
את החיסון לכלבת פיתח Louis Pasteur, אבי המיקרוביולוגיה (Microbiology). בשנת 1880 מצא Pasteur כי הגורם למחלה אינו חיידק. הוא החל לערוך ניסויים בכלבים נגועים על ידי תרביות מוחלשות של הנגיף. בהתאם לאמצעים של אותם ימים, היה בודק Pasteur את השפעת החיסון על ידי ארנבונים חיים שהיה מכניס לכלוב הכלב. באחת הפעמים הבחין כי הכלב בו טיפל מיאן לתקוף את הארנבת כהרגלו. פסטר הסיק מכך כי תרכיב החיסון, אחד מני רבים שהכין, הוא אשר לו נזקק. יעילותו של החיסון הוכחה כאשר בשנת 1884 הובא לביתו של Pasteur ילד שננשך על ידי כלב משוטט בתשעה מקומות. בעוד Pasteur מזריק לו את החיסון הניסיוני שלו, נאסף סביב הבית קהל זועם שהמטיר נאצות כלפי Pasteur וגידף את ניסוייו, אולם כעבור ימים אחדים ניצלו חייו של הילד.
בשנת 1903 זיהה נֶגְרִי את גורם המחלה ואף תיאר גופיפים תוך-תאיים אופייניים במוחם של בני אדם ובעלי חיים נגועים. מאז קרויים אלה גופיפי Negri ועד ימינו מהווה נוכחותם בבדיקה שלאחר המוות את שיטת האבחנה לפגיעת הכלבת.
אפידמיולוגיה
הכלבת היא המחלה היחידה בעולם כולו שיש נגדה חקיקה נפרדת. כל השירותים הווטרינרים בעולם התפתחו ראשית כל במטרה להתמודד עם מחלת הכלבת ורק בהמשך החלו לעסוק גם בבעיות אחרות. בשנת 1995 חוקק בישראל חוק הכלבת שהחליף את פקודת הכלבת הוותיקה יותר מימי המנדט הבריטי. לפי החוק חייב כל כלב בן 3 חודשים בחיסון. חיסון הכלבת תקף בכלב לשלוש שנים, אולם החוק מחייב לחסן כל שנה. החוק מחייב כרגע לחסן רק כלבים.
אדם שננשך בישראל מגיע ללשכת הבריאות המחוזית ושם תזריק לו האחות תרכיב חיסוני חמש פעמים בכתפו בפרקי זמן ההולכים וגדלים, בכמות ההולכת וגדלה בכל פעם. באם ננשך קרוב לראשו, קיימת סכנה רבה יותר לחלות במהרה מאשר במקום מרוחק מן הראש כמו בכף הרגל. הטיפול הזה ניתן רק במסגרת משרד הבריאות ולא בקופות החולים.
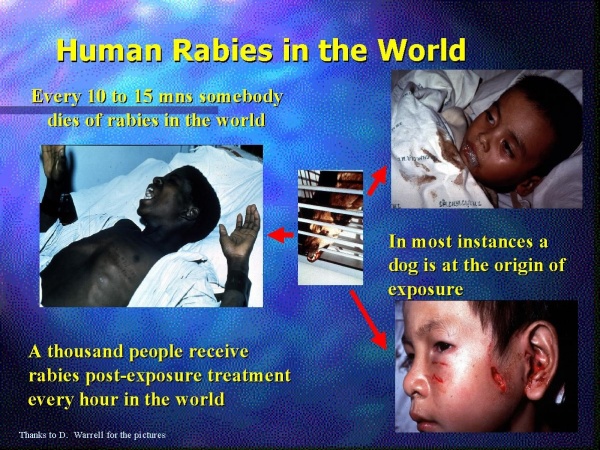
בכל שנה מתים ברחבי העולם בין 40,000 ו-70,000 אנשים מכלבת, כ-90 אחוזים מהם באסיה. כ-6 מיליון אנשים ברחבי העולם מקבלים בכל שנה חיסון לאחר חשש להדבקה.
חיות בית, כולל כלבים, מחויבות לקבל חיסון למחלה כבר בהיותן גורים. חיות בר מקבלות חיסון באמצעות פיתיונות מזון. בעבר ניסה משרד החקלאות לפתור את בעיית הכלבת על ידי הדברת תנים, שועלים וכלבי בר. בדיעבד ידוע עתה כי נגרמה הרעלה משנית שהמיתה עופות דורסים רבים שאוכלוסייתם לא התאוששה.
אוכלוסייה העלולה לחלות בכלבת
כל יונק עלול להיפגע מהכלבת, אולם באזורנו נפגעים ממנה בעיקר בעלי חיים משלושה סוגים:
- חיות בית כמו כלבים וחתולים
- בהמות כמו פרות, צאן וסוסים
- חיות בר כמו שועלים, תנים, זאבים, נמיות וגיריות
כלבת במכרסמים ובעטלפים היא נדירה ובישראל לא אובחנו מקרים כאלה. המאגר העיקרי בישראל לנגיף הכלבת הוא בשועלים והם מפיצי המחלה העיקריים.
קליניקה
הכלבת מופיעה במגוון צורות. בימי המחלה הראשונים חל שינוי בהתנהגות בעל החיים. חיות ידידותיות הופכות לתוקפניות, וגם להפך. בהמשך ניכרת התרחבות אישונים, החיות לוקות בטירוף, נעות למרחקים ונושכות בדרך כל דבר: חפצים דוממים, בעלי חיים אחרים ובני אדם. בהמשך מופיע שיתוק שרירים הפוגע בבית הבליעה, גורם לשינוי הקול ולהופעת ריר וקצף בפה. בשלב הסופי החולים אינם מגיבים לגירויים ולוקים בהתכווצויות ובשיתוק.
חיית בר, שהופכת ידידותית ואינה חוששת להתקרב לבני אדם, חשודה מאוד בכלבת.
עזרה ראשונה ואיתור חיה פוגעת
חובה לשטוף מיד וביסודיות את מקום הנשיכה במים ובסבון, ולאחר מכן לחטא בכוהל או בתמיסת יוד. בהמשך יש לפנות את הננשך לתחנת מגן דוד אדום, מרפאת קופת-חולים, חדר מיון או רופא פרטי.
חשוב לאתר ולזהות את בעל החיים שנשך לפני שיברח מן המקום, וכן לאתר את בעליו כדי שניתן יהיה להכניס את הנושך להסגר תצפית למשך 10 ימים במקרה הצורך. התצפית מאפשרת לרופא להחליט על דרך הטיפול בנשוך. יש לדווח למשרד הבריאות על כל מקרה של חשש לכלבת.
הסגר קיים רק לגבי כלבים וחתולים. חיות בר, מומתות עם תפיסתן ומובאות לבדיקת כלבת במעבדה לפתולוגיה במכון הווטרינרי בבית דגן. גם בעל חיים שמת טרם הסגרתו – מועבר לבדיקה וטרינרית ברשות המקומית.
מניעת כלבת
כל כלב מגיל שלושה חודשים חייב בחיסון שנתי נגד כלבת, שניתן בנפרד מכל חיסון אחר. כמו כן נעשות פעולות לאיסוף כלבים משוטטים. יציאת כלבים לרשות הרבים מותרת רק כשלפיהם מחסום והם מובלים ברצועה. לפי הרשאת החוק, מותר להשמיד כל כלב המהלך לבדו גם אם הוא מחוסן לכאורה.
החוק מחייב להמית כלבים בלתי מחוסנים המהווים סכנה להדבקה ולהפצה של המחלה לכלבים אחרים או לבני אדם.
בנוסף, נעשה ניסיון לדילול טורפי בר המשמשים מאגר חשיפה לנגיף הכלבת וכן נעשים ניסיונות בהטמעת חיסון נגד כלבת בחיות בר בשיטת פיזור פיתיונות המכילים תרכיב.
מחלת הכלבת בישראל
במהלך תשע שנותיה הראשונות של המדינה, בין השנים 1957-1948, מתו בישראל 23 בני אדם ממחלת הכלבת. מאז שהוחל בשנת 1958 בפעולות מניעה מיוחדות של השירותים הווטרינריים, אשר כללו שילוב של חיסון חובה בכלבים והדברת בעלי-חיים משוטטים, אירעו 4 מקרי הינגעות נוספים, כולם לפני שנת 1971. שניים מהם בתחומי הקו הירוק, ושניים אחרים מיד לאחר מלחמת ששת הימים בשטחים.
כעבור 15 שנים ללא מקרי כלבת באדם, במשך שנה בין חודש דצמבר ב-1996 לחודש דצמבר ב-1997 נפטרו ממחלת הכלבת שלושה בני אדם שלא קבלו טיפול הולם בזמן. חייל ברמת הגולן, ילדה מקלנסווה וגבר מהכפר ג'דיידה שליד עכו אשר ננשכו על ידי חיות לא מזוהות בעת שנתם בלילה.
כל שלושת המקרים אובחנו כחיוביים בבדיקות שנעשו במעבדות המכון הווטרינרי בבית דגן, בדגימות הרוק שנלקחו בעודם בחיים בעזרת שיטה ביומולקולרית: Nested RT-PCR (Reverse Transcription-Polymerase Chain Reaction).
בשנת 2003 נפטרה מכלבת אישה שננשכה על ידי חתול באזור ירוחם. אף במקרה זה לא ניתן טיפול מונע אחרי הנשיכה.
על פי נתוני משרד הבריאות, בשנת 1997 הגיעו ההוצאות הישירות שנבעו מטיפול בבני אדם לאחר חשיפה ל 16 מיליון שקלים חדשים.
עובדות אלה וההשלכות הכלכליות על המשק החקלאי עמדו בפני וועדת הכלכלה של הכנסת שהחליטה בישיבתה בתאריך ה-06.01.1989, על הקמת מטה לאומי למאבק בכלבת. במטה מיוצגים משרדי הבריאות, החקלאות, איכות הסביבה, הביטחון, הפנים, החינוך והאוצר בשיתוף נציגי השלטון המקומי וצה"ל. המלצתו העיקרית של המטה, הייתה להתחיל בפרויקט חיסון אוראלי של חיות בר כמקובל ברוב ארצות אירופה וצפון אמריקה.
השלב הראשון במימוש פרויקט זה, הוא בדיקת היתכנות השימוש בשיטת החיסון הפומי לחיסון תנים ושועלים בישראל. העבודה נחלקה לשנים, חלק אחד בוצע בשבי ואילו השני בשדה.
הבדיקה בשבי הראתה כי שני סוגי התרכיבים שנבדקו יעילים לחיסון התנים כנגד הכלבת. לאור תוצאות עבודות במדינות אחרות, ניתן היה לוותר על בדיקת היעילות בחיסון שועלים.
בניסוי השדה שנערך באזור כרמיאל בשטח של כ–450 קילומטר רבוע, נמצא כי באוכלוסיות השועלים והתנים, מאפשר השימוש בשיטה זו, לחסן שיעור אוכלוסייה ברמה המקובלת כמספיקה לעצירת התפרצות המחלה.
שכיחות מקרי הכלבת באזור כרמיאל ירדה לאפס ומאז 1999 ועד 2003 לא נתגלו בו כל מקרה נוסף של כלבת.
לאור התוצאות החיוביות, הורחב אזור החיסון ל-5000 קילומטר רבוע הכוללים את שטחה הצפוני של המדינה מגבול הצפון והגולן ועד למרכז.
הירידה בשכיחות מקרי הכלבת הצביעה על יעילות השיטה אף אחר הרחבת האזור. מנגד הופיעו התפרצויות כלבת באזורי המרכז והדרום שלא חוסנו. עקב כך, התקבלה בשנת 2002 החלטת ממשלה על מימון הפרויקט והרחבת היקפו. תקציב הפרויקט עומד על 6.3 מיליון שקלים חדשים לשנה, המוקצים למשך שלוש שנים 2003–2005.
בעקבות כך, הגיע היקף הפרויקט ב-2003 ללמעלה מ־15000 קילומטר רבוע.
עקב המצב הפוליטי, לא יצא אל הפועל פרויקט חיסון בשיתוף פעולה אזורי שתוכנן לשנת 2001 ואשר אמור היה לכלול את מצרים, ירדן הרשות הפלשתינאית וישראל. עבודה במתכונת אזורית, היא למעשה הדרך היחידה שבכוחה להבטיח ביעור של המחלה. המימון לפרויקט זה ניתן על ידי הקהילה האירופית ורק המצב פוליטי מנע את מימוש התקציב. כולם מקווים שבעתיד תצא לפועל תוכנית זו, שבלעדיה לא ניתן יהא להגיע להדברת הכלבת באזורי ירושלים, לאורך קו התפר ובבקעת הירדן.
קדחת צהובה
קדחת צהובה (Yellow fever) היא מחלה הנגרמת על ידי נגיפים הנישאים באמצעות יתושים. המחלה אופיינית בעיקר לאזורים טרופיים ותת-טרופיים (Sub-tropical).
הנגיף הגורם למחלה מתרבה בעיקר בתוך תאי הכבד בתוך כדי הרס שלהם. בין סימני המחלה: דימומים, כולל דימום מהקיבה, צהבת, כאבי ראש, בחילות, צמרמורת וחום גבוה.
היסטוריה
בתחילת המאה ה-19, צבא של 40 אלף איש שנשלח על ידי Napoleon ל-Haiti כדי לדכא את המהפכה ההאיטית (Haiti) לעצמאות חוסל על ידי הקדחת הצהובה (כולל מפקד המשלחת, שהיה גיסו של Napoleon). יש היסטוריונים המאמינים ש-Haiti הייתה עתידה להיות נקודת התחלה לפלישה לארצות הברית דרך Louisiana (שהייתה אז בשליטה צרפתית).
בנוסף הניסיון הראשון לבניית תעלת Panama (על ידי חברה צרפתית) נכשל בחלקו בגלל הקדחת הצהובה שטבחה בעובדים. החיסון לקדחת פותח לראשונה במהלך הניסיון השני לבניית התעלה (על ידי האמריקנים).
מניעה
קיים חיסון לקדחת צהובה שנותן לילדים מגיל 10 ומבוגרים הגנה מפני הדבקות במחלה כשהם מגיעים לאזורים נגועים. דוחי יתושים, ביגוד מגן ורשתות על הבתים אינם תמיד מספיקים למניעת הידבקות. באזורים נגועים הדברת יתושים הוכיחה את עצמה כדרך יעילה לצמצם את מספר ההידבקות במחלה.
קדחת צהובה היא אחת מהמחלות היחידות שמדינות מסוימות מציבות דרישה שמטיילים לאזור נגוע חייבים לקבל חיסון לפני כן. במדינות אלה יש לרוב תקנות שמחייבות בידוד אנשים שהגיעו לאזור נגוע ללא תיעוד שקיבלו חיסון לקדחת צהובה. זאת מכיוון שאחד ממעבירי המחלה, יתוש ה-Aedes, קיים גם באזורים טרופיים אחרים בעולם (שבהם אין קדחת צהובה) וישנו פוטנציאל להתפרצות המחלה אם תובא לשם.
אין תרופה למחלה אשר עלולה להיות קטלנית בעיקר למי שמערכת החיסון שלו חלשה; ולכן החיסון חשוב ביותר. החיסון נקרא Yellow Fever Vaccine וניתן בזריקה אחת. הוא מגן עליך במשך עשר שנים. יש להתחסן לפחות עשרה ימים לפני היציאה.
הטיפול הקיים מטפל בתסמינים בלבד. עירוי נוזלים כדי לטפל בלחץ דם נמוך ועירויי דם נחוצים במרבית המקרים החמורים. קורבן עם חום זקוק להרבה מנוחה, אוויר צח, והרבה נוזלים.
התוויות נגד לחיסון
אם הייתה תגובה אלרגית קשה לחיסון בעבר.
החיסון מכיל נגיף חי מוחלש, ולפיכך לא יכולים להתחסן בו אנשים הלוקים בהפרעות של מערכת החיסון: חולי סרטן, מטופלים בכימותרפיה או סטרואידים וכן נשים בהיריון ונשאי HIV.
- לאחר החיסון - האם ומתי כדאי לדאוג לגבי הופעה של תופעות לוואי, ומה הסימנים שצריכים להדליק "אור אדום"?
בכל מקרה של אלרגיה חריפה המתבטאת בנפיחות סביב אזור ההזרקה, או אם מופיעים התסמינים הבאים (אחד או יותר): פריחה, קשיים בנשימה, צפצופים בנשימה, תחושה של נפיחות בגרון – יש להגיע מייד ובדחיפות לקבלת עזרה רפואית. גם אם מתפתח לאחר החיסון חום גבוה, או אם חלים שינויים קיצוניים בהתנהגות – יש לפנות במהירות לקבלת עזרה רפואית.
סלמונלוזיס (Salmonella Typhi)
סלמונלה (Salmonella, S) היא שמה של משפחה גדולה המונה קצת למעלה מ-2,300 סוגים של חיידקי גרם (Gram) שליליים, אשר כעשרה אחוזים מהם עלולים לפגוע בבני אדם. חיידקי הסלמונלה שהתגלו לראשונה במעי חזיר בשנת 1885 על ידי הווטרינר האמריקאי Daniel Salmon, מחולקים לסוגים, מינים ותת-מינים.
בדרך כלל חיים החיידקים במערכת עיכול של בעלי חיים שונים, כולל חיות בעלות דם קר. סוגי החיידקים השונים נקבעים לפי האנטיגנים המאפיינים אותם.
ניתן גם לחלק את החיידקים לשתי קבוצות: האחת – לה שייכים חיידקים החיים בגופו של פונדקאי עיקרי אחד כמו Salmonella Typhi ו-Salmonella Paratyphi במעי של בני אדם, או כמו חיידקי Salmonella Typhimurium העשויים לשכון בפונדקאים שונים.
חיידקי הסלמונלה עשויים לשרוד חודשים ארוכים גם כשאינם מצויים במעיים של בעל חי ובלבד שהתנאים בסביבה, יתאימו מבחינת מצע מזון, טמפרטורות, לחות וכדומה. מלבד גופם של פונדקאים, עשויים החיידקים לשרוד גם באדמה ובמים. בגוף עשויים החיידקים לחיות בסביבה בין תאית וגם בתוך התאים עצמם. יש להם שוטונים אשר מלבד אפשרות התנועה שהם מעניקים לחיידק, הם מאפשרים לו לחדור לתוך תאים ולשרוד אפילו בתוך פאגוציטים (Phagocytes) (תאים בלעניים של מערכת החיסון, שנשלחים לבלוע ולחסל את הסלמונלה). למעשה יש אף באפשרות חיידקי הסלמונלה לגרום לתאים אלה של מערכת החיסון להתאבד בתהליך הקרוי Apoptosis (מבטאים רק אות P אחת). ולכן ניתן בתאוריה, להשתמש בסלמונלה כדי להתמודד עם תאים סרטניים.
למרות שטווח הטמפרטורות שבהן חיידקי הסלמונלה פעילים, נע בדרך כלל מעשר ועד שישים מעלות, היא גם מתחת לעשר מעלות הם אינם מתים, אלא הופכים לנבגים שעשויים לשרוד אפילו בטמפרטורות קיפאון. נבגים אלה יהפכו שוב לחיידקים פעילים כשתתחמם האווירה. חיידקים העשויים לחיות במקום שיש בו אויר כמו גם במקום שאין בו אויר. למרות שחיידקי הסלמונלה עלולים להיות אלימים במיוחד בטמפרטורה של 37 מעלות צלזיוס (Celcius) ובמקום שאין בו חמצן, מספר חיידקים קטן אינו גורם בדרך כלל למחלה.
מערכת החיסון של האדם משתלטת ומחסלת אותם על נקלה, בעיקר בעזרת נוגדנים. בדרך כלל תהיה צואה – הזיהום העיקרי שממנו ניתן להידבק. ואילו החדירה לגוף, תיעשה בדרך כלל דרך הפה ומשם דרך הקיבה אל המעי. שלמרות רגישותם הרבה לחומצה, מצליחים החיידקים לשרוד את החומצה המלחית החזקה שבקיבה, בשל יכולתם להיצמד זה לזה וליצור מיקרו מושבות, כשהחיידקים החיצוניים מגנים על אלה שבפנים. כמו כן ניתן להיפגע גם דרך המערכת הלימפטית, כשהחיידק חודר לקשרי הלימפה בצוואר. אפשרויות הידבקות נוספות הן על ידי שאיפת החיידק לדרכי הנשימה, או אפילו מגע ידיים מזוהמות בלחמיות העיניים.
לאחר ההידבקות עלולים חיידקי הסלמונלה לגרום לאדם למחלות קשות כמו: אלח דם, דלקת מעיים, Paratyphi ו-Typhi. מחלות שעלולות להסתיים במוות אצל אדם בעל מערכת חיסון חלשה ובעיקר אצל חולים במחלות כרוניות, תינוקות וזקנים.
כשמגיע החיידק אל המעיים הוא נצמד לרירית באזורים שונים ובעיקר במעי הדק, מתחיל לאכול מסביבתו, חודר לתאים והורס את ה-Brush border, שהוא מערך צפוף של סיסים זעירים הבולטים מעל לפני שטח המעי ומאפשרים את ספיגת המזון. כשמגיעים לאזור ההדבקה בו מצויים תאי מערכת החיסון – נויטרופילים ומונוציטים הלוחמים בחיידקים מזיקים, מתחיל שלב התגובה הדלקתית ונפתחת מלחמה. אולם לרוע המזל, מסתבר שחיידקי הסלמונלה מסוגלים לשרוד בתוך התאים המונוציטים אשר בלעו אותם על ידי נטרול האנזימים (Enzymes) המעכלים חיידקים שנבלעו.
למעשה הם עושים שימוש בתאי מערכת החיסון ככלי תעבורה להגיע אל מערכת הלימפה, ומשם לאיברים נוספים כמו הכבד והטחול, בתוך כדי פגיעה רב-מערכתית שעלולה לגרום למוות. המחלה עלולה לסכן חיים, בין היתר בגין איבוד נוזלים ומינרלים חיוניים, וכן בגלל פגיעה במאזן החומצות והבסיסים בגוף. עם זאת, בני אדם בעלי מערכת חיסון חזקה, ישרדו את הסלמונלה גם ללא כל טיפול. בין היתר מכיוון שמערכת חיסון חזקה מייצרת גם נוגדנים מיוחדים המנטרלים את החיידקים.
חרף העובדה שחיידקי הסלמונלה מפרישים רעלנים, תהיה הסיבה העיקרית למחלה, דווקא התרבות חיידקים במעי. ולכן תתפתח המחלה באיטיות והתהליך יימשך בממוצע בין 12 ל-48 שעות, ועשוי לארוך גם 72 שעות ואפילו עד עשרה ימים. את הסימן המיידי להרעלת סלמונלה ניתן למצוא בהתקפי בחילות שמלווים בכאבי בטן עוויתיים ובשלשול מימי (מלווה בריר או בדם). השלשול מתרחש ככל הנראה, עקב פעילות תאי מערכת החיסון – הנויטרופילים, וכן בגלל פגיעת הרעלנים שמפרישים החיידקים באזורים שונים במעי, אשר בהם נעשית ספיגת רכיבי המזון. בשלשול ניתן למצוא גם כמות רבה של חיידקים המופרשים מהגוף. אולם הפרשה מסיבית זו הולכת ומידלדלת, ומספר החיידקים המפורשים בצואה יורד לאחר כמה ימים בצורה חדה. מלבד הסימנים הרשומים לעיל, יהיו מבין סימני המחלה גם חוסר תיאבון, הקאות, חום גבוה, כאבי ראש ודיכאון.
החיסון יעיל כנגד המחלה פותח כבר בשלהי המאה ה-19. החיסון הזה נוצר מחיידק מומת והיה יעיל ב-50 עד 80 אחוזים מהמחוסנים במניעת תחלואה למשך 12 שנים. לחיסון זה היו תופעות הלוואי רבות מקומיות שנמצאו בחמישים אחוזים מהמחוסנים.
בשנות השמונים פותח חיסון המבוסס על חיידק מוחלש הנלקח דרך הפה (Ty21a).
חיסון זה הוא החיסון המומלץ עבור מטיילים לאזורים בהם החיידק פעיל. ההוראה על מתן החיסון ניתנת על פי משרד הבריאות במרפאות המטיילים על פי יעד הנסיעה.
החיסון נלקח ב-4 מנות במשך שבוע (יום כן ויום לא) ומותר לשימוש החל מגיל 6.
בתחילת המאה ה-21 פותחו חיסונים נוספים פעילים שמקורם בחלבונים ממעטפת החיידק. חיסונים אילו מותרים כבר מגיל שנתיים והרושם הוא שיעילותם היא גבוהה ותופעות הלוואי שלהם קלות הרבה יותר מהחיסונים הקודמים. גם חיסונים אלו ניתנים רק על פי הוראת משרד הבריאות במרפאות למטיילים.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק