מיאלומה נפוצה - טיפולים חדשים - 2017 - MM, new treatments
הופניתם מהדף טיפולים חדשים במיאלומה נפוצה - נכון ל-2016 לדף הנוכחי.
| מיאלומה נפוצה - טיפולים חדשים (2017) | ||
|---|---|---|
| (MM, new treatments (2017 | ||
| 250px | ||
צילום מיקרוסקופי של פלסמציטומה, המקבילה ההיסטולוגית של מיאלומה נפוצה
| ||
| שמות נוספים | מיאלומה נפוצה - מחלה ותיקה עם טיפולים חדשים | |
| ICD-10 | Chapter C 90.0 | |
| ICD-9 | 203.0 | |
| MeSH | D009101 | |
| יוצר הערך | ד"ר הילה מגן | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מיאלומה נפוצה
מיאלומה נפוצה היא ממאירות של תאי הפלזמה הממוקמים במח העצם, המאופיינת בשגשוג חד שבטי (מונוקלונלי) של תאי פלזמה המפרישים במרבית החולים חלבון מסוג מסוים (החלבון המונוקלונלי/החד שבטי) לדם ו/או לשתן. המחלה מהווה כ־1 אחוז מסך הממאירויות וכ־10 אחוזים מהממאירויות ההמטולוגיות[1]
בישראל מאובחנים 400–500 חולים חדשים מדי שנה. ביטויי המחלה כוללים: פגיעה בעצמות השלד על ידי נגעים הורסי עצם, פגיעה כלייתית ופגיעה בתפקוד המערכת החיסונית היכולה להתבטא בשכיחות מוגברת של זיהומים.
קיימת שונות רבה בין חולי מיאלומה, הן בביטויים המביאים לאבחנה והן בתגובה לטיפול, הנובעת ככל הנראה ממורכבות המחלה ומהמטען הגנטי אותו היא נושאת.
הטיפול במיאלומה נפוצה
במאה ה-21 חלה התקדמות משמעותית בטיפול במיאלומה הודות לפיתוח ואישור תרופות חדשות, בעלות מנגנוני פעילות שונים, המכוונות לפגיעה בתאי הפלזמה ובסביבתם התומכת. פיתוחים אלה הרחיבו את אפשרויות הטיפול במחלה שהיו מצומצמות בעיקר לטיפול בשילוב סטרואידים ותרופות כימותרפיות מקבוצת ה-Alkylator agents, שאינן סלקטיביות לפגיעה בתאי הפלזמה. התרופות החדשות משמשות לטיפול בחולי מיאלומה מקו הטיפול הראשון ולאורך קווי הטיפול המתקדמים עם התקדמות המחלה.
למרות שבמרבית החולים המחלה עדיין אינה ברת ריפוי, חלק גדול מהחולים חווה שיפור מתמשך בתוחלת החיים ובאיכותם עם תקופות של מחלה שקטה (רמיסיות). התקדמות זו בטיפול הובילה לשיפור משמעותי בהישרדות הממוצעת של חולי המיאלומה (Median overall survival) אשר נעה בין שש לעשר שנים ותלויה בגיל החולה, במחלות רקע נלוות ובמאפייני המחלה השונים.
להלן קבוצות התרופות מקובלות כטיפול במיאלומה נפוצה:
אלקלטורים (Melphalan and Cytoxan) - תרופות כימותרפיות שעדיין יעילות בטיפול במיאלומה. ה-Melphalan טוקסי יותר ומשמש בעיקר לטיפול במינון גבוה במסגרת השתלת מח עצם עצמית. ה-Cytoxan מקובל בשילוב עם התרופות המתקדמות בקווי הטיפול השונים.
סטרואידים (Dexamethasone, Prednisone) - מהווים חלק במרבית הטיפולים ובשילובי התרופות השונים הניתנים. Dexamethasone הוא התכשיר היעיל ביותר כאשר ניתן כמונותרפי (לא במצבים שכיחים משמש כתרופה בודדת).
IMiDs - Immunomodulatory agents - תכשירים הפועלים במספר מנגנונים, הכוללים:
- הרג ישיר של תאי המיאלומה במספר מנגנונים הכוללים עצירה בחלוקת התאים והפרעה באינטראקציה בין תאי הגידול לסביבתם, החיונית להמשך שגשוגם
- פעילות אימונומודולטורית שבה משופעלים תאים ציטוטוקסיים (Natural killers) ומעוכבים תאים אחרים - תהליך המסתיים בפגיעה והרג תאי מיאלומה
- פעילות אנטיאנגיוגנטית הפוגעת ביצירת כלי דם החיוניים להמשך התפתחות ושגשוג תאי הגידול
Thalidomide - תרופה המוכרת משנות ה־50, פותחה כטיפול להקלה על בחילות בהיריון והטיפול בה הופסק כעבור זמן קצר. ב־1999 נוסה טיפול בתלידומיד בחולי מיאלומה שלא הגיבו לטיפולים קודמים ובשליש נראתה תגובה לטיפול. מאז אושרה יעילות התרופה במחקרים נוספים והיא נוספה כמרכיב חשוב בטיפול במיאלומה ואושרה לטיפול במיאלומה על ידי ה-FDA (Food and Drug Administration) במאי 2006.
Revlimid) Lenalidomide) - דור שני של IMiDs, פוטנטי יותר ופחות טוקסי מתלידומיד. הוכנס לסל התרופות בישראל לטיפול במיאלומה בשנת 2011. בדומה לתלידומיד, מתקשר לעלייה בשיעור אירועי קרישיות יתר ורידית, בעיקר במתן בשילוב סטרואידים ועל כן השימוש בתרופה זו מצריך טיפול מניעתי לקרישי דם. עלול לגרום לירידה בספירות הדם, דבר המצריך ניטור קבוע של ספירות הדם והפחתת מינון כאשר נצפית ירידה משמעותית בספירות. ב־2017 אושר על ידי ה-FDA כטיפול אחזקתי לחולי מיאלומה נפוצה לאחר השתלת מח עצם עצמית.
Pomalyst) Pomalidomide) - דור שלישי של IMiDs, הודגם במספר מחקרים כפוטנטי מאוד הן כטיפול יחיד והן במשלב עם תרופות נוספות, אף בחלק מהחולים שמחלתם הייתה עמידה לטיפול בתלידומיד וברבלימיד. התרופה אושרה על ידי ה-FDA ב-2013 כטיפול במחלה מתקדמת ואושרה על ידי סל התרופות בישראל משנת 2014 כטיפול קו שלישי לחולים שמחלתם נשנתה לאחר קווי טיפול שכללו מעכב פרוטאוזום ו-IMiDs מדורות קודמים.
מעכבי הפרוטאוזום (Proteasome Inhibitors - PI’s) - פרוטאוזומים מהווים קומפלקס אנזימטי בתאים הפועל בפירוק חלבונים פגומים לחומצות אמינו ומאפשר לתא ביצוע מחזור ליצירת חלבונים חדשים. תאי הפלזמה תלויים בפרוטאוזום בשל כמות החלבון הרב המיוצרת בהם. מעכבי הפרוטאוזום פוגעים בהישרדות תאי הפלזמה על ידי עצירת פירוק החלבונים בתא. חלבונים אלה מצטברים באופן רעיל בתא, תהליך הגורם בסופו למות התא בתהליך אפופטוטי.
Veicade) Bortezomib) - דור ראשון במעכבי הפרוטאוזום שאושר לטיפול. פועל על ידי עיכוב הפיך של הפרוטאוזום בתא. יעיל במרבית החולים בשילוב כטיפול קו ראשון. בזכות פעילותו המהירה מסוגל להביא לשיפור משמעותי עד להתנרמלות התפקוד הכלייתי בחולי מיאלומה הסובלים מאי ספיקת כליות חריפה על רקע מסת מחלה גבוהה, כאשר ניתן בשלב מוקדם. הטיפול ב-Bortezomib מאושר בישראל כטיפול קו ראשון למיאלומה נפוצה החל משנת 2011.
Kyprolis) Carfilzomib) - דור שני של מעכבי הפרוטאוזום. ניתן תוך ורידית והוכח כיעיל אף בחולים שמחלתם נשנתה תחת טיפול ב-Bortezomib. פועל על ידי עיכוב הפרוטאוזום באופן בלתי הפיך. מאושר בישראל משנת 2014 כטיפול קו שלישי ומשנת 2017 מאושר במסגרת טיפול קו שני בשילוב עם Lenalidomide עבור חולים המוגדרים כבעלי מחלה בסיכון גבוה.
Ninlaro) Ixazomib) - מהווה את התכשיר הראשון מקבוצת מעכבי הפרוטאוזום הניתן פומית. משנת 2017 מאושר בישראל כטיפול קו שני בשילוב עם Carfilzomib עבור חולים המוגדרים כבעלי מחלה בסיכון גבוה.
NP1 0052] Marizomib] - דור שני של מעכבי הפרוטאוזום מעכב את שלושת האתרים הקטליטיים בפרוטאוזום באופן בלתי הפיך, נבדק עדיין במחקרים קליניים.
ONX-0912] Oprozomib] - דומה במבנהו לקרפילזומיב, מעכב באופן בלתי הפיך את הפרוטאוזום וניתן פומית. נבדק עדיין במחקרים קליניים.
מעכבי היסטון דאציטילז, Histone DACIs) Histone Deacetylase inhibitors) - דאצטילזות הם אנזימים המתמחים בסילוק קבוצות אצטיל מחלבונים שונים בתא. דאצטילזות מבוטאים ביתר בתאי סרטן, כולל בתאי מיאלומה. עיכובם גורם לשינויים במבנה הכרומטין בתא אשר מביא לעצירה בהבשלה ולמוות תאי (אפופטוזיס תאי). מתן מספר תרופות מקבוצה זו לא הדגים תוצאות מרשימות כאשר ניתנו כטיפול יחיד, אולם בשילוב עם מעכבי הפרוטאוזום ועם תרופות נוספות הביאו לשיפור בשיעורי התגובה.
Vorinostat - שילוב טיפול זה עם Lenalidomide + Dexamethasone ועם Bortezomib + Dexamethasone לחולים עם מחלה מתלקחת או עמידה הביא לשיפור התגובה עם פרופיל תופעות לוואי נסבל[2][3].
Panobinostat - התכשיר הראשון מקבוצת ה-HDAC שאושר על ידי ה-FDA בפברואר 2015 לטיפול בחולי מיאלומה שמחלתם נשנתה לאחר לפחות שני קווי טיפול קודמים שכללו Bortezomib ו-IMiD. האישור ניתן לאחר קבלת תוצאות מחקר ה־1 Panorama שבו טופלו חולי מיאלומה שמחלתם נשנתה ב: Bortezomib + Dexamethasone -/+ Panobinostat. בחולים שטופלו ב-Panobinostat נראתה עלייה בהישרדות ללא מחלה (PFS - Progression Free Survival) בכ-4 חודשים לעומת אלה שלא טופלו בו[4].
Monoclonal Antibodies - MAbs:
Emliciti) Elotuzumab) - נוגדן מונוקלונלי הומני כנגד 7-SLAMF - חלבון הנמצא על פני תאי המיאלומה ועל פני ה- NK - Natural Killer cells. היקשרות הנוגדן לשני סוגי התאים גורמת לשפעולם תאי ה-NK כנגד תאי המיאלומה. במחקר רנדומלי פאזה שלישית, ה-ELOQUENT2 טופלו חולי מיאלומה שמחלתם נשנתה כעבור 1–3 קווי טיפול בשילוב Revlimid + Dexamethasone -/+ Elotuzumab. לאחר 3 שנים נראתה ירידה של 27 אחוזים בסיכון להתקדמות/למוות בחולים שטופלו גם ב-Elotuzumab ועיכוב ב־14 חודשים בממוצע עד לטיפול הבא לעומת החולים שטופלו ברבלימיד ודקסמטזון בלבד. אותה תגובה הושגה גם בקבוצת החולים שהיו בעלי שינויים ציטוגנטיים בעלי פרוגנוזה גרועה שטופלו ב-Elotuzumab. תופעות הלוואי בקבוצת ב-Elotuzumab היו מוגברות מינימלית ביחס לקבוצת הביקורת וכללו תגובות לעירוי, בחילה, חולשה, כאב ראש ועליית חום, ברובן בעת העירוי הראשון וניתנות למניעה על ידי סטרואידים ואנטי היסטמינים הניתנים לפני העירוי[5]. בעקבות תוצאות אלו אושר התכשיר על ידי ה-FDA בנובמבר 2015 לטיפול בשילוב עם Revlimid + Dexamethasone בחולי מיאלומה שמחלתם נשנתה כעבור 1–3 קווי טיפול קודמים.
Darzalex) Daratumumab) - נוגדן מונוקלונלי הומני מסוג IgG1k הנקשר ל-CD38, סמן המבוטא על פני תאי המיאלומה באפיניות גבוהה[6] וכן מבוטא על פי תת-אוכלוסיות של תאי B ו-T רגולטוריים, תאים סופרסוריים הנגזרים מהשורה המיאלואידית וכן על פני תאים/רקמות לא המטופואיטיות[7][8]. היקשרות הנוגדן לתאי המיאלומה גורמת להשמדתם במספר מנגנוני פעולה המתווכים אימונית כמפורט בציור 1.
הטיפול ב-Daratumumab נבדק בתחילה כמתן כתכשיר בודד (Monotherapy) בחולים עם מחלה שהתלקחה ו/או הייתה עמידה לטיפולים קודמים שכללו מעכב פרוטאזום ואימיד. ההישרדות הממוצעת ללא התקדמות מחלה (Median progression-free survival) הייתה 5.6 חודשים (8.1 ,4.2 :95% CI) ו־65 אחוזים מהחולים שהגיבו (CI 95%: 28, 86) נשארו בהפוגה 12 חודשים.
בהמשך נבדק הטיפול ב-Daratumumab (SIRIUS study) בסדרה רב מרכזית בה ניתן הטיפול לחולי מיאלומה שטופלו בלפחות 3 קווי טיפול קודמים, כולל מעכב פרוטאזום ואימיד, או שהיו עמידים לשניהם. מ-106 חולים, ב-31 נראתה תגובה - ב-3 sCR (Stringent Complete Response), ב-10 VGPR (Very Good Partial Response), וב-18 PR (Partial Response). הזמן הממוצע לתגובה הראשונה היה 1 חודש (נע בין 5.6-0.9 חודשים). משך התגובה הממוצע היה 7.4 חודשים (נע בין 5.6-0.9 חודשים) והישרדות ללא התקדמות (PFS) 3.7 חודשים (4.6-2.8 :95% CI). סך ההישרדות ל־12 חודשים היה 64.8 אחוזים (75.5-51.2 :95% CI) ובהמשך ההישרדות הממוצעת הייתה 17.5 חודשים (95% CI 13-7 - not estimable). הטיפול נסבל היטב והראה תוצאות מעודדות לגבי יעילותו כטיפול בודד אף בחולים לאחר קווי טיפול רבים עם מחלה עמידה.
בהתבסס על תוצאות סדרות אלו אושר הטיפול ב-Daratumumab בנובמבר 2015 על ידי ה-FDA עבור חולי מיאלומה שמחלתם נשנתה לאחר לפחות 3 קווי טיפול קודמים, והיה לנוגדן המונוקלונלי הראשון שאושר לטיפול בחולי מיאלומה. בשמו המסחרי Darzalex, מיוצר ומשווק בישראל על ידי חברת יאנסן.
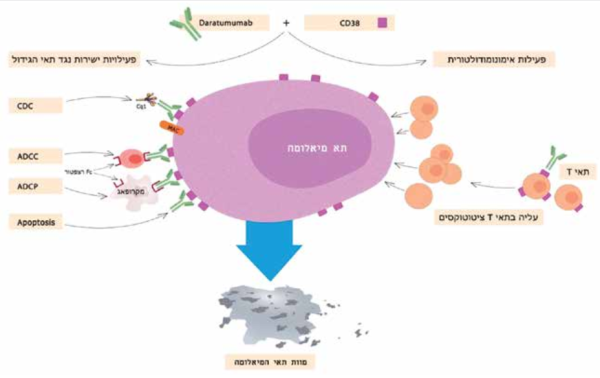
Complement-dependent cytotoxicity) CDC) - ציטוטוקסיות התלויה בהפעלת מערכת המשלים. קשירת רצפטור Fc של ה־daratumumab לחלבון ה־ C1q מביאה להפעלת מערכת המשלים הגורמת בסיומה ליצירת קבוצת מבנים - (membrane attack complex (MAC הגורמים לניקוב תאי הגידול ולהשמדתם.
ADCC - (Antibody-dependent cellular cytotoxicity) - ציטוטוקסיות תאית התלויה בנוגדן. שפעול תאי Natural killers על ידי קשירת ה־ daratumumab ל־Fc רצפטור, גורם לשחרור פרפורין, גרנזימים (granzymes), טומור נקרוזיס פקטור (TNF) וליגנדים נוספים הגורמים לליזיס והרג משמעותי של תאי המיאלומה.
ADCP (Antibody-dependent cell-mediated phagocytosis) - פאגוציטוזיס מתווך תאית כתלות בנוגדן. קשירת ה־daratumumab ל־Fc רצפטור שעל פני המקרופאג גורמת לשפעולו ומאפשרת תהליך בליעת תאי המיאלומה.
Apoptosis - הפעלת מנגנוני השמדה עצמית של התאים.
פעילויות אימונומודולטוריות: היקשרות רצפטור Fc של ה־ daratumumab ל־CD38 שעל פני תאי Tגורמת לשפעולם ולעלייה בתאי T ציטוטוקסיים ועוזרים (cytotoxic & helpers) התוקפים ישירות את תאי המיאלומה ותורמים להשמדתם. בנוסף יכול ה־ daratumumab לגרום לירידה בתאים האימונוסופרסיביים ולשינוי במיקרו-סביבת הגידול התורמים גם לפגיעה בתאי המיאלומה
עם הדגמת יעילות התרופה במתן כתרופה בודדת הוחל בבדיקת שילובה עם תרופות נוספות ולאחר סדרות פאזה 1/2 שהראו תוצאות מעודדות נבדק שילובה בסדרות הבאות:
POLLUX - סדרה רנדומלית, פאזה 3 שבה השווה מתן Daratumumab בשילוב DRd - Lenalidomide/Dexamethasone, לעומת Rd - Lenalidomide/Dexamethasone בחולים שמחלתם התלקחה או הייתה עמידה (RRMM - Relapsed/Refractory Multiple Myeloma). כל החולים לאחר קו טיפול 1 לפחות וללא עמידות לרבלימיד. בקבוצת ה-DRd טופלו 286 חולים לעומת 283 ב-RD. ההישרדות ללא מחלה כעבור 12 חודשים הייתה 83 אחוזים בקבוצת ה-DRd לעומת 60 אחוזים בקבוצת ה-Rd ו-78 אחוזים לעומת 52 אחוזים כעבור 18 חודשים. יעילות ה-DRd על פי ה-DR נצפתה בכל תת-קבוצות החולים. שיעורי ההפוגה המלאה [CR/sCR] הוכפלו בקבוצת ה-DRd לעומת ה-DR ושיעור ה-MRD הוכפל פי ארבעה בקבוצה זו. סך ההישרדות כעבור 18 חודשים הייתה 86 אחוזים בקבוצת ה-DRd לעומת 76 אחוזים בקבוצת ה-Rd. סדרה זו הראתה פרופיל חיובי עבור היתרון לעומת הסיכון בשילוב Daratumumab עם Lenalidomide/Dexamethasone והעלתה את האפשרות לשילוב קומבינציה זו כאחת מאפשרויות הטיפול המקובלות עבור חולים אלו.
CASTOR study - סדרה רנדומלית, פאזה 3 שבה השווה מתן Daratumumab בשילוב DVD) Velcade-Dexamethasone) לעומת DV) Velcade-Dexamethasone) בחולים שמחלתם התלקחה או הייתה עמידה (RRMM) ושלא היו עמידים ל-Velcade. לזרוע ה-Daratumumab גויסו 251 חולים לעומת 247 חולים בזרוע השנייה. ה-Primary endpoint היה הישרדות ללא התקדמות מחלה (PFS). כעבור 12 חודשי טיפול ההישרדות ללא התקדמות נראתה ב-60.7 אחוזים בזרוע ה-DVd לעומת 26.9 אחוזים בזרוע ה-VD והמחקר הופסק מוקדם מהמתוכנן לאור היתרון משמעותי שנראה בשילוב הטיפול עם Daratumumab [7].
לאור תוצאות מחקרים אלה אישר ה-FDA בנובמבר 2016 טיפול ב-Darzalex בשילוב עם Lenalidomide and Dexamethasone, or Bortezomib and Dexamethasone לטיפול בחולי מיאלומה נפוצה אשר טופלו בקו טיפול קודם 1 לפחות.
תוצאות ביניים ממחקר פאזה 3, ה-ALCYONE study אשר גייס 706 חולי מיאלומה שטופלו במסגרת קו ראשון ב-Velcade-Melphalan Prednisone (VMP) +/- Darzalex, הראה ששילוב Darzalex צמצם הסיכון להתקדמות/למוות ב־50 אחוזים בהשוואה לטיפול ב-VMP, וההישרדות הממוצעת ללא מחלה (PFS) עדיין לא ניתנת להערכה, בהשוואה ל-18.1 חודשים בחולים שטופלו ב-VMP בלבד.
Darzalex - תופעות לוואי
תופעות הלוואי השכיחות של Darzalex כוללות: תגובות הקשורות לעירוי (Infusion Related Reactions - IRRs) - חולשה, עליית חום, קוצר נשימה, שיעול, נזלת/הרגשת גודש באף, בחילה, כאב ראש. שכיחות התגובות הקשורות לעירוי דווחה בעד 71 אחוזים מהחולים, כאשר ברובן היו קלות, בחומרה שנעה בין 1–2 Grade ברוב המכריע של החולים. מרבית התגובות התרחשו במהלך העירוי הראשון עם ירידה ניכרת בהמשך. מתן טיפול מונע לפני הטיפול ואחריו צמצם משמעותית התגובות לעירוי. הטיפול המומלץ כשעה לפני העירוי כולל כדור Acamol (1,000-650 מיליגרם), אנטי-היסטמין (Diphenhydramine 50-25 מיליגרם פומי או תוך ורידי, או שווה ערך שלו) וסטרואידים (Methylprednisolone 100 מיליגרם תוך ורידי ב-2 העירויים הראשונים ומהשלישי ניתן לרדת ל-60 מיליגרם). ביומיים לאחר העירוי יש לתת מדי יום סטרואיד (Methylprednisolone 20 מיליגרם פומי).
תיתכן ירידה בספירת הדם העלולה להעלות הסיכון לזיהומים ולדימומים.
Darzalex - שונות
מאחר ש-Daratumumab הוא נוגדן מונוקלונלי הומני הוא יכול להיות מאותר כפס השקעה מונוקלונלי בבדיקת האימונופיקסציה באזור הגאמה (γ-region) ובכך עלול למסך מצב של תגובה מלאה (שבה לא נראה מקטע באימונופיקסציה).
בבדיקת DIRA (Daratumumab IFE Reflex Assay) מבוצעת אינקובציה של סרום של החולה לאחר טיפול ב-Daratumumab עם נוגדן מונוקלונלי Anti-idiotype. ה-Daratumumab הנקשר לנוגדן נודד מאזור ה-gamma ובכך ניתן להסיר המיסוך העלול להיגרם על ידי ה-Daratumumab ולהבהיר האם מקורו של פס ההשקעה ב-Daratumumab או בשארית קלון תאי הפלזמה של החולה[9]. יש לדווח למעבדה לפני התחלת טיפול ב-Daratumumab כדי שידעו להפעיל בדיקה זו בעת הצורך.
הצלבת דם - CD38 מבוטא באופן חלש על פני כדוריות דם אדומות. Daratumumab הנקשר לכדוריות האדומות עלול לגרום לתוצאה חיובית שגויה (False positive results) בבדיקת Indirect Antiglobulin Test (Indirect Coombs test), אך לא בבדיקת האנטיגנים המג'וריים (ABO/RhD).
קיימות מספר אפשרויות למניעת אפקט מעבדתי זה המפריע בהצלבת הדם:
DTT) Dithiothreitol) - דנטורציה של האפיטופים של CD38 על פני הכדוריות המונעת קשירת Daratumumab.
נוגדנים מונוקלונליים Anti-idiotype ו-Soluble CD38 המונעים קשירת Daratumumab לכדוריות האדומות.
בדיקת גנוטיפ לביסוס ההתאמה (אם החולה קיבל עירוי דם ב־3 החודשים הקודמים).
לא נצפתה המוליזה משמעותית בחולים שטופלו ב-Daratumumab ולא נצפו תגובות לעירויים בחולים אלה. יש לדווח לבנק הדם על חולה המתחיל טיפול ב-Daratumumab[10][11].
לסיכום, חלה התקדמות בטיפול בחולי מיאלומה נפוצה הודות לפיתוח ואישור תרופות חדשות, בעלות מנגנוני פעולה שונים, ועם אפשרות לשלבן באופן סינרגיסטי אשר הביא לשיפור בהישרדות ללא מחלה (Progression free survival) ובהישרדות הכללית (Overall survival).
מחקרים הבודקים את שילוב התרופות החדשות יחד עם השתלה עצמית צפויים להביא לשיפור נוסף עם צפי אף לריפוי בכ-15 אחוזים מהחולים[1]. תרופות נוספות, חלקן פיתוחים מתקדמים של תרופות קיימות ואחרות בעלות מנגנוני פעולה שונים, נמצאות בשלבי פיתוח מתקדמים.
קיימת הכרה בשנים האחרונות בהטרוגניות המחלה, המתבטאת בקיום תאים בעלי שונות גנטית כבר באבחנה, המכתיבים את ביטויי המחלה, תגובה לטיפול ואת הפרוגנוזה[12]. עם הבנה טובה יותר של ההטרוגניות המחלה יחד עם הרחבה משמעותית באופציות הטיפוליות הפך הטיפול במיאלומה למורכב ומאתגר יותר, עם שיפור בהישרדות הנראה ב-15 השנים האחרונות יחד עם התלקחויות מחלה עמידה למספר עולה של קווי טיפול קודמים.
שיתוף גובר של חולים במסגרת מחקרים קליניים יכול לעזור במציאת משלבי טיפול שיהיו יעילים ופחות רעילים הן לחולים חדשים והן לחולים שמחלתם נשנתה/עמידה לטיפול. טיפול משולב בתרופות בעלות מנגנוני פעולה שונים, שיהיה מבוסס בעתיד על סמנים המנבאים תגובה לטיפול, ייתכן שישפר משמעותית את שיעורי התגובה לטיפול, את שיעורי ההישרדות ואף את שיעורי הריפוי במחלה זו.
ביבליוגרפיה
- ↑ 1.0 1.1 Philippe Moreau: How I treat myeloma with new agents. Blood 2017 130:1507-1513.
- ↑ D S Siegel at all: Vorinostat in combination with lenalidomide and dexamethasone in patients with relapsed or refractory multiple myeloma. Blood Cancer Journal (2014) 4, e182.
- ↑ Dimopoulos M at all: Vorinostat or placebo in combination with bortezomib in patients with multiple myeloma (VANTAGE 088): a multicentre, randomised, double-blind study. Lancet Oncol. 2013 Oct; 14(11):1129-40.
- ↑ San Miguel JF at all: Phase Ib study of panobinostat and bortezomib in relapsed or relapsed and refractory multiple myeloma. J Clin Oncol 2013; 31. .
- ↑ Sagar Lonial, at all: Elotuzumab Therapy for Relapsed or Refractory Multiple Myeloma. N Engl J Med 2015;373:621-31
- ↑ Lonial S, Weiss B, Usmani S, et al. Daratumumab monotherapy in patients with treatment-refractory multiple myeloma (SIRIUS): an open-label, randomised, phase 2 trial. Lancet. 2016; 387(10027):1551-1560.
- ↑ 7.0 7.1 Usmani S, et al. Clinical efficacy of daratumumab monotherapy in patients with heavily pretreated relapsed or refractory multiple myeloma. Blood 2016 Jul 7; 128(1):37-44.
- ↑ Palumbo A, et al. Daratumumab, Bortezomib and Dexamethasone for Multiple Myeloma. N Engl J Med 2016; 375:754-766.
- ↑ tten HG, et al. Interference of daratumumab in monitoring multiple myeloma patients using serum immunofixation electrophoresis can be abrogated using the daratumumab IFE reflex assay (DIRA). Clin Chem Lab Med. 2016 Jun 1; 54(6):1105-9.
- ↑ Chapuy et al. Transfusion. 2015; 55(6 Pt 2):1545-54.
- ↑ Oostendorp et al. Transfusion. 2015; 55(6 Pt 2):1555-62.
- ↑ Rajkumar SV. Myeloma today: Disease definitions and treatment advances. Am J Hematol.2016;91(1):90-100.
המידע שבדף זה נכתב על ידי ד"ר הילה מגן, מנהלת שירות מיאלומה נפוצה, המרכז הרפואי רבין, בית החולים בילינסון, פתח תקוה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק