טכניקת LAM לזיהוי חיידק השחפת
| מדריך בדיקות מעבדה | |
| טכניקת LAM לזיהוי חיידק השחפת | |
|---|---|
| מעבדה | כימיה בשתן, אימונולוגיה בשתן |
| תחום | שחפת (tuberculosis). |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – שחפת
מבוא
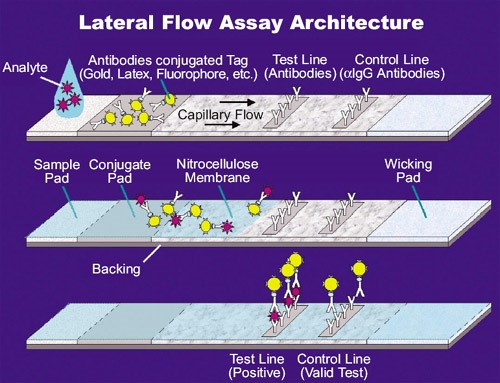
בארצות הברית בערך 13 מיליון אנשים סובלים מהדבקה סמויה של שחפת, המוגדרים כאלה שנדבקו על ידי Mycobacterium tuberculosis ללא תסמינים ואינם מגיעים לשלב של שחפת גלויה. ללא טיפול, כ-5 עד 10% מאלה עם מערכת חיסון תקינה ייפתחו שחפת גלויה במהלך חייהם (Sterling וחב' ב-MMWR Recomm Rep משנת 2020). שחפת גורמת מדי שנה ל-1.5 מיליון מקרי מוות בעולם, ונותרה הסיבה המובילה לפטירות כקרב נשאי HIV. האבחון של שחפת מהווה מפתח למלחמה במחלה, אם כי הירידה במספר האבחונים בסוף העשור השני של המאה ה-21 ותחילת העשור השלישי מיוחסת למחויבות העצומה של מערכות הבריאות בעולם למאבק בפנדמיה של COVID-19 שהגבירה בהרבה את מספר הפטירות משחפת. הפיתוח של בדיקות המסוגלות לאבחן שחפת במדגמים שאינם רוק, מאפשר טיפול דחוף המתחיל ביום האבחון, ולכן הוא כה חיוני בבקרה ובשליטה על מחלה זו. בדיקת point-of-care הראשונה הניתנת לביצוע שקיבלה את אישור WHO, הייתה ערכת Alere-B LAM של חברת Abbott, המבוססת על זיהוי בשתן של האנטיגן lipoarabinomannan (להלן LAM) של החיידק M. tuberculosis. השימוש בדגימת שתן הוא בעל יתרון שכן 14 עד 63% מחולי שחפת שמחלתם קשה אינם מסוגלים לתת דגימת רוק (Lawn וחב' ב-BMC Med משנת 2017, ו-Huerga וחב' ב-BMC Med משנת 2019). ערכת AlereLAM הגדילה את יכולת האבחון של שחפת (Drain וחב' ב-Sci Rep משנת 2016, Bjerrum וחב' ב-BMC Infect Dis משנת 2015, ו-Florida וחב' ב-Clin Infect Dis משנת 2017).
בשנת 2016, כוח המשימה האמריקני למניעת מחלות (להלן USPSTF) המליץ על בדיקת סקר של כל האמריקאים בני 18 שנה ומעלה המצויים בסיכון לשחפת סמויה, לעבור בדיקת דם כגון הפרשה של אינטרפרון-γ או בדיקת טוברקולין בעור. אלה המצויים בסיכון לשחפת סמויה, גרים באזורים אנדמיים לשחפת, וכן אלה עם מערכת חיסון פגועה, או אלה המקבלים תרופות לדיכוי מערכת החיסון, כגון אנטגוניסטים של TNF, או מקבלים קורטיקו-סטרואידים דוגמת פרדניזולון באופן סיסטמי במינון של 15 מיליגרם ליום, או אלה המטופלים עם ציקלוספורין באופן כרוני לאחר השתלת איבר. לאחר וידוא של שחפת פעילה מתחילים מידית בטיפול.
ביצוע בדיקות AlereLAM ו-FujiLAM הפחית את התמותה בקרב מאושפזים (Peter וחב' ב-Lancet משנת 2016, ו-Gupta-Wright וחב' באותו כתב עת משנת 2018), כאשר בדיקות אלה והתקבלו יפה על ידי אנשי המעבדה (Mathabire-Rucker וחב' ב-Globe Health Action משנת 2019). לערכה זו יש גם עלות-יעילות טובה (Shah וחב' ב-AIDS משנת 2013, Sun וחב' ב-Int J Tuberc Lung Disease משנת 2013, ו-Reddy וחב' ב-Lancet Globe Health משנת 2019). במטה-אנליזה נמצא שהרגישות של AlereLAM במטופלים עם תסמיני שחפת היא 42% (כאשר הרגישות היא של 45% באלה עם ספירת CD4 הנמוכה מ-200 תאים/ממ"ק, 16% באלה עם ספירת CD4 הגבוהה מ-200 תאים/ממ"ק, ו-29% במטופלים אמבולטוריים), וספציפיות של 92% (על פי Bjerrum וחב' ב-Cochrane Database Syst Rev משנת 2019). WHO ממליץ ש-AlereLAM ישמש לאבחון שחפת במטופלים עם HIV ותסמינים של שחפת, כמו גם במטופלים עם מערכת חיסון פגועה באופן חמור או באלה עם ספירת CD4 נמוכה מ-100 תאים/ממ"ק.
ערכת Fujifilm SILVAMP TB LAM היא ערכה חדשה לבדיקת point-of-care בשתן המסוגלת לגלות ריכוזי LAM נמוכים יותר בהשוואה לערכת AlereLAM תוך שימוש בנוגדנים חד-שבטיים בעלי זיקה גבוהה מאוד לאפיטופים של LAM. שני מחקרים נערכו בדרום אפריקה ובגאנה לקביעת הדיוק האבחוני של FijiLAM במטופלים נשאי HIV, ובהם התגלתה רגישות גבוהה יותר מאשר בערכת AlereLAM בדגימות שתן קפואות, (70% לעומת 42% בדרום אפריקה, ו-78% לעומת 53% בגאנה) אם כי הספציפיות של FujiLAM הייתה מעט נמוכה יותר מאשר זו של AlereLAM: (91% לעומת 95% בדרום אפריקה לעומת 89% לעומת 96% בגאנה) (Broger וחב' ב-Lancet Infect Dis משנת 2019, ו-Bjerrum וחב' ב-Open Forum Infect Dis משנת 2019). מחקר רטרוספטיבי בניגריה, ומחקר פרוספקטיבי בזמביה במטופלים עם HIV הניבו תוצאות דומות (Comella-Del-Barrio וחב' ב-J Clin Med משנת 2021, ו-Muyoyeta וחב' ב-Eur Respir J משנת 2021).
מחקר של Huerga וחב' ב-Lancet מינואר 2023 בחן את הדיוק של בדיקת FujiLAM במטופלים עם HIV וסיכון גבוה של שחפת בארבע מדינות של תת-סהרה (אוגנדה, קניה, מוזמביק ודרום אפריקה), ותוצאותיו כדלקמן: המחקר שיתף 1,575 נשאי HIV (מתוכם 823 נשים) בני 15 שנה ומעלה, עם תסמינים של שחפת ללא תלות במספר תאי CD4 (קבוצה א'), מטופלים א-תסמיניים עם מחלת HIV מתקדמת בשלב III ו-IV עם ספירת CD4 נמוכה מ-200 תאים/ממ"ק (קבוצה ב'). כל משתתפי המחקר עברו צילומי-X של החזה ובדיקת דם, והתבקשו לתת דגימת שתן ו-2 דגימות רוק בהם בוצעו בדיקות בשיטת FujiLAM ובשיטת AlereLAM, כמו גם ספירת תאי CD4 ותרבית הרוק לחיידק M. tuberculosis. בקבוצה א' נכללו 1,031 משתתפים, ובקבוצה ב' 544 משתתפים. שחפת אושרה מיקרוביולוגית ב-96 משתתפים מקבוצה א' (9.4%), וב-18 משתתפים מקבוצה ב' (3.3%). נמצא שרגישות שיטת FujiLAM לאבחון שחפת הייתה 60%, וזו של שיטת AlereLAM הייתה 40%. בקרב נבדקים עם ספירות CD4 הנמוכות מ-200 תאים/ממ"ק, הרגישות של FujiLAM נקבעה כ-69%, ואילו זו של אלה עם ספירות CD4 הגבוהות מ-200 תאים לממ"ק הייתה 52%. בנבדקים עם למעלה מ-200 תאי CD4 לממ"ק, הרגישות של שיטת FujiLAM הייתה 47%, לעומת 24% בשיטת AlereLAM. הספציפיות של שיטת FujiLAM הייתה 87%, לעומת 86% בשיטת AlereLAM.
הפיזיולוגיה של lipoarabinomannan
אנטיגן זה (להלן LAM) הוא גליקוליפיד וגורם וירולנטי הכרוך ב-Mycobacterium tuberculosis שתפקידו העיקרי לנטרל מקרופאגים ולקלוט רדיקלים חמצוניים. האינאקטיבציה של מקרופאגים מקלה על התפשטות החיידק באזורי גוף שונים, וההרס של רדיקלים חומציים מאפשר את הישרדות החיידק, כיוון שרדיקלים מחמצנים חופשיים הם מנגנון חשוב המסייע לגוף להשמיד חיידקים פולשים. LAM הוא למעשה lipoglycan המהווה חלק עיקרי בדופן החיידק. הוא משמש גם כ-modulin עם פעילות אימונו-רגולטורית ונוגדת-דלקת. תכונות אלו מקלות על החיידק להישרד בגוף, על ידי פגיעה בתנגודת הגופנית ובהחלשת התגובה החיסונית של הגוף כנגד החיידק (Guerardel וחב' ב-J Biol Chem משנת 2003). מנגנונים אלה כוללים את עיכוב השגשוג של תאי T והחלשת יכולת ההשמדה של החיידקים על ידי מקרופאגים. דרך החלשת התגובה של אינטרפרון-γ (Knutson וחב' ב-J Biol Chem משנת 1998). תפקידים נוספים של LAM כוללים כנראה את הנטרול של הרדיקלים החמצוניים החופשיים שיוצרים מקרופאגים ועיכוב של protein kinase C.
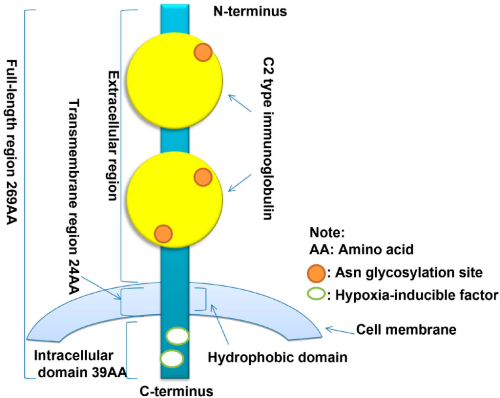
המבנה של LAM
LAM מסונתז על ידי הוספת שיירי mannose ל-phosphoinositol על ידי רצף של מנוזיל-טרנספראזות ליצור PIMs ו-lipomannan (להלן LM) (Kordulakova וחב' ב-J Biol Chem משנת 2002, Lea-Smith וחב' באותו כתב-עת משנת 2008, ו-Morita וחב' באותו כתב-עת משנת 2006). PIM ו-LM עוברים קישור עם arabinan ליצירת LAM (Gueradel וחב' ב-J Biol Chem משנת 2002). ל-LAM יש שלושה מקטעים מבניים הכוללים עוגן של glycosylphosphatidyl הקושר את המולקולה הזאת לדופן התא, מגרעין של D-mannan המשמש כשלד קרבוהידרטי, ומ-D-arabinan טרמינלי. מספר גדול של הסתעפויות צדדיות של arabinofuranosyl מהשלד של mannose (על פי Maiti וחב' ב-J Biol Chem משנת 2001). מודיפיקציות קו-ולנטיות של ה-D-arabinan הטרמינלי הן שיוצרות מבנים רבים של LAM המאפשרים הישרדות של החיידק בתוך הפונדקאי. מסווגים את מולקולות LAM לשלושה סוגים עיקריים:
- ManLAM: מולקולת LAM שעברה מנוזליציה מאופיינת על ידי שיירי mannosyl באזור ה-D-arabinan הטרמינלי. סוג זה של LAM נמצא בעיקר בסוגי מיקובקטריום יותר פתוגניים כ- M. leprae ו-M. bovis. נמצא ש-ManLam היא מולקולה אנטי-דלקתית, המעכבת את יצירת TNF-α ו-IL-12 על ידי תאים דנדריטים באדם כמו גם על ידי מקרופאגים אנושיים in vitro, והיא גם מאפננת (גורמת למודולציה) אפופטוזיס במקרופאגים המושרה על ידי M. tuberculosis על ידי קישורה לקולטני mannose, על פני מקרופאגים (Gilleron וחב' ב-J Biol Chem משנת 1997). הוצעו מנגנונים רבים להסביר את אופן התפקוד של ManLAM: שפעול על ידי ManLAM של מסלול PI3K מספיק לגרות פוספורילציה של Bad, חלבון השייך למשפחת Bcl-2. דה-פוספורילציה של Bad גורמת לו לסייע לאפופטוזיס, והשפעול של Bad מסייע להישרדות תאים. ManLAM עשוי גם לשפעל ישירות את SHP-1, שהוא phosphotyrosine phosphatase המווסת באופן שלילי מסלולים הקשורים לפעילות אינטרפרון-גמה ואינסולין. אחרי השפעול, מולקולת SHP-1 נודדת מהציטופלזמה לממברנת התא. על ידי שפעול של פוספטאזה, LAM מסוגל לעכב במונוציטים פוספורילציה של טירוזין, המושרית על ידי LPS ואינטרפרון-γ. עיכוב יצירת TNF-α פוגע בפעילות של מולקולה הנחוצה ליצירת גרנולומות כנגד M. tuberculosis וחיונית לפעילות של מקרופאגים כנגד חיידק השחפת, על ידי יצירת NO. השפעול על ידי LAM של SHP-1 פועל גם לדה-אקטיבציה של IL-12, ציטוקין החיוני בעמידות הטבעית (innate) להדבקות עם חיידק השחפת. LAM משפעל תאי natural killer המייצרים אינטרפרון-γ המשפעלים מקרופאגים.
- PILAM:{כ}} LAMs עם phosphoinositol בקצותיהם, מופיעים לרוב בזנים לא פתוגניים של מיקובקטריום כולל M. smegmatis . בניגוד ל-ManLAMs הרי ש-PILAMs מעודדים דלקת. CD14 שהוא קולטן המופיע על פני מקרופאגים, פועל ביחד עם toll-like receptor 2 (להלן TLR2) שהוא הקולטן של PILAM (Yu וחב' ב-J Immunol משנת 1998). קישור PILAM לקולטן משפעל קסקדה של איתותים תוך-תאיים המשפעלים גורמי שעתוק המאתחלים שעתוק של גנים מקודדים לציטוקינים מעודדי דלקת. בכך משופעלים TNF-alfa, וכן IL-8 ו-IL-12 ונגרם אפופטוזיס של מקרופאגים (Vignal וחב' ב-J Immunol משנת 2003).
- AraLAM: מספר מינים של מיקובקטריום בעל קצב גידול מהיר כגון M. chelonae, מכילים LAMs החסרים מבני mannose ו-phosphoinositol. סוג זה של LAM מאופיין על ידי שרשראות צדדיות של 1.3-mannosyl במקום 1,2-mannosyl שמוצאים במיני מיקובקטריום אחרים. צורות אלה נחשבות פוטנטיות יותר מאשר ManLAM המכיל mannose בהשריית תפקודים הכרוכים בשפעול של מקרופאגים. בנוסף לעידוד של גנים מוקדמים כגון c-fos ,KC ו-AraLAM .JE משרה את השעתוק של mRNA ליצירת ציטוקינים (כגון TNF-α ,IL-1β ,IL-1α ,IL-6 ,IL-8 ו-IL-10 המיוצרים באופן אופייני על ידי מקרופאגים. פרוטו-אונקוגנים כ-c-fos ו-c-myc פועלים בוויסות של שעתוק גנים, בעוד ש-JE ו-KC הם ציטוקינים פפטידיים המשמשים כגריינים כימיים של מונוציטים וניטרופילים (Roach וחב' ב-J Immunol משנת 1993). שפעול של TNF-α מחיש התבטאות פתולוגית של המחלה, כגון נמק רקמתי ונזק עצבי (Barnes וחב' ב-Infect Immun משנת 1992). שיירי O-acyl של arabinomannan עלולים להיות אחראיים לפעילות TNF הגורמת לתסמיני שחפת כגון חום, איבוד משקל, ונמק (Moreno וחב' ב-Clin Exp Immunol משנת 1989). עם זאת, נוכחות ManLAM מפחיתה את פעילות AraLAM תוך דיכוי מערכת החיסון.
מחקר של Peter וחב' ב-PLoS One משנת 2013 בחן עת הערך המוסף של בדיקת LAM בשתן עם ערכת strip test (Determine-TB) לאבחון מאושפזים עם שחפת שהם נשאי HIV עם מערכת חיסונית מדוכאת. במחקר זה שותפו 281 מאושפזים נשאי HIV החשודים לשחפת, שנבדקו בשיטת LAM strip בשתן. 116 מתוך 281 הנבדקים זוהו כנדבקים ודאיים בשחפת, בעוד ש-71 מהנבדקים הוגדרו כנדבקים אפשריים בשחפת. 39 מתוך 187 הנבדקים (21%) שנמצאו חיוביים בבדיקת LAM, שהוגדרו כנדבקי שחפת ודאיים או סבירים, הוחמצו בבדיקות אמפיריות מוקדמות, ומתוך 39 נבדקים חיוביים אלה, 25 נבדקים (64%) הוחמצו בבדיקה מיקרוסקופית של משטח דם. לפיכך, 25 מתוך 187 הנבדקים (13.4%) של מודבקים ודאיים או סבירים בשחפת, שהיו מוחמצים בשיטות בדיקה אחרות והטיפול כנגד שחפת בהם היה מתעכב, זוהו בעזרת LAM strip test. נבדקים מטופלים בשיטת LAM שהוחמצו בשיטות בדיקה אחרות, היו בעלי ספירה ממוצעת נמוכה יותר של תאי CD4 (p=0.008) בעלי ממוצע חומרת מחלה גבוה יותר ((p=0.001 ובעלי רמות גבוהות יותר של urea (p=0.002), בהשוואה למטופלים עם תוצאת LAM שלילית שטופלו אמפירית קודם לכן.
רוב המחקרים דווחו שבדיקת AlereLAM התקבלה חיובית כבר בניסיון הבדיקה הראשון בעוד שתוצאות שלא ניתנו לאינטרפרטציה (פחות מ-1%) התקבלו רק ב-3 מחקרים (Chan וחב' ב-Am Am J Respir Crit Care Med משנת 2000, Doublier וחב' ב-AIDS משנת 2007, ו-Rechman ו-Hershfield ב-Tuberculosis משנת 2000). תוצאות מחקרים רבים סוכמו כדלקמן: במאושפזים רגישות השיטה 52% והספציפיות שלה 87%. בנבדקים אלקטיביים במרפאות-חוץ הרגישות שלה 29% והספציפיות 96%. כללית, בנבדקים בקטגוריות שונות רגישות השיטה 42% והספציפיות 91%.
לאבחון של שחפת במבוגרים חיוביים ל-HIV ללא קשר לסימנים ותסמינים של שחפת, הדיוק האבחוני של AlereLAM הוא כדלקמן: בנבדקים מאושפזים הרגישות 62% והספציפיות 84%. בנבדקים אלקטיביים במרפאות-חוץ הרגישות 31% והספציפיות 95%. בנבדקים בקטגוריות שונות רגישות השיטה 35% והספציפיות 95%. לאבחון של שחפת במבוגרים עם מחלת HIV מתקדמת, ללא קשר לסימנים ותסמינים של שחפת, הדיוק האבחוני של בדיקת AlereLAM הוא כדלקמן: במאושפזים עם ספירת תאי CD4 נמוכה מ-200 תאים לממ"ק, רגישות השיטה 64% והספציפיות שלה 82%. בנבדקים אמבולטוריים במרפאות-חוץ עם ספירת CD4 נמוכה מ-200 תאים לממ"ק, רגישות השיטה 21% והספציפיות שלה 96%. בנבדקים בקטגוריות שונות עם מספר תאי CD4 נמוך מ-200, רגישות השיטה 26% והספציפיות שלה 96%. במאושפזים עם ספירת CD4 נמוכה 100, רגישות השיטה 57% והספציפיות שלה 90%. בנבדקים אמבולטוריים עם מספר תאי CD4 נמוך מ-100, רגישות השיטה 40% והספציפיות שלה 87%. בנבדקים בקטגוריות שונות עם מספר תאי CD4 נמוך מ-100, רגישות השיטה 47%, והספציפיות שלה 90%. לאבחון של שחפת בילדים חיוביים ל-HIV, הדיוק האבחוני של בדיקת AlereLAM היא כדלקמן: רגישות השיטה 47% והספציפיות שלה 90%. השימוש בטכניקת AlereLAM חוסכת 15 פטירות לכל 1,000 מטופלים (Whiting וחב' ב-BMC Med Res Methodol משנת 2003).
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק