כימוקין ליגנד 9 - Chemokine ligand 9
הופניתם מהדף כימוקין ליגנד 9 לדף הנוכחי.
| מדריך בדיקות מעבדה | |
| כימוקין ליגנד 9 | |
|---|---|
| Chemokine ligand 9 | |
| שמות אחרים | CXCL9, MK ,Humig ,MIG ,YB9 ו- crg-10. |
| מעבדה | כימיה בדם |
| תחום | כימוקין המשחק תפקיד חשוב במחלות סרטניות, בדלקות, ובמערכת החיסון. |
| יוצר הערך | פרופ' בן-עמי סלע |
כימוקינים
כימוקינים או ציטוקינים כימוטקטיים, הם משפחה של ציטוקינים קטנים או חלבוני איתות המופרשים על ידי תאים וגורמים לתנועה כיוונית של לויקוציטים, כמו גם לסוגי תאים אחרים, כולל תאי אנדותל ואפיתל. בנוסף הם בעלי תפקיד מרכזי בהפעלת תגובות חיסוניות של המארח, כימוקינים חשובים לתהליכים ביולוגיים, כולל מורפוגנזה וריפוי פצעים, כמו גם בפתוגנזה של מחלות כמו סרטן.
כימוקינים מסווגים לארבע תת-משפחות עיקריות: CXC, CC, CX3C ו-C.
CXCL9
כימוקין ליגנד 9 (CXCL9) הוא ציטוקין קטן השייך למשפחת הכימוקינים CXC, הידוע גם כמונוקין המושרה על ידי גמא אינטרפרון (MIG). CXCL9 הוא אחד הכימוקינים אשר ממלא תפקיד בגרימת כימוטקסיס, קידום התמיינות וכפל של לויקוציטים, וגורם לפריקת רקמות.
תפקיד CXCL9
התפקיד העיקרי של CXCL9 הוא לגייס תאי חיסון ספציפיים לאזורים של פציעה, הדבקה, או מחלה. הוא משמש כ-chemoattractant, לגיוס סוגים אחדים של תאים לבנים, בעיקר תאי T ותאים שהם Natural Killer (להלן NK). תאים מסתובבים תמיד בצירקולציה, אך CXCL9 מספק את האיתות הספציפי הקובע לתאים היכן לעצור ולפעול. תאי T ו-NK מכילים קולטן על פניהם הקרוי CXCR3. כאשר CXCL9 נמצא ברקמה, הוא נקשר לקולטני XCR3 שעל תאי החיסון, תוך גירוי של קסקדה של איתותים פנימיים המדריכים את התאים לנוע לקראת המקור של CXCL9.
גירויים ליצירת CXCL9
הכימוקין CXCL9 אינו נוצר באופן רצוף, ונוכחותו מצביעה על כך שתגובה חיסונית ספציפית עומדת להתרחש. הגירוי הראשוני ליצירת CXCL9, היא מולקולת אינטרפרון-גאמא (IFN-γ), המשתחררת על ידי תאי חיסון כגון T או NK, כאשר אלה מבחינים בסיכונים כגון נגיפים או תאים סרטניים. כאשר IFN-γ עובר צירקלציה ונקשר לתאים שונים בגוף, כולל תאי עור, פיברובלסטים ומקרופאגים, הוא מסמן להם להתחיל לייצר ולהפריש CXCL9. תהליך זה מייצר לולאה של משוב חיובי. ההופעה ההתחלתית של תאי חיסון מעטים מגרה את IFN-γ, מה שגורם לרקמות מקומיות לייצר CXCL9. ייצור זה מגייס יותר תאי T ותאי NK לאזור המדובר, מה שמגביר את התגובה החיסונית. היכולת של CXCL9 לזמן תאי חיסון היא תועלתית במספר מצבים אך מזיקה במצבים אחרים. בתגובה בריאה, CXCL9 מסייע להילחם בהדבקות ובסרטן. במהלך הדבקה נגיפית, לדוגמה, תאים מודבקים מגרים את ההפרשה של IFN-γ, מה שמוביל ליצירה של CXCL9 המגייסת תאי T לגלות ולהשמיד את התאים המוחשדים. תפקוד זה הוא גם תועלתי באונקולוגיה. סוגי סרטן רבים מוחדרים על ידי תאי חיסון, ו-CXCL9 מסייע לכוון תאי T ישירות למיקרו-סביבה של הגידול הסרטני ולהתקיף את תאי הסרטן. רמות גבוהות של CXCL9 בתוך גידול כרוכות בפרוגנוזה טובה יותר. מאידך גיסא, התפקוד של גיוס תאים על ידי CXCL9 עלול להזיק כאשר מערכת החיסון אינה מכוונת היטב. במחלות אוטו-אימוניות כגון rheumatoid arthritis או טרשת נפוצה, CXCL9 נוצר לרוב באזורים נגועים, כגון המפרקים או המוח, בהם הוא מגייס תאי T ופוגע ברקמה בריאה, תוך שהוא גורם לדלקת ולנזק. תהליך מזיק דומה מתרחש בעת דחיית שתל. מערכת החיסון של מקבל השתל מזהה אותו כזר ופוגע בו. CXCL9 הוא מרכיב בתהליך הדחייה של השתל, תוך גיוס תאי T המתקיפים את השתל.
אימפליקציות תרפויטיות
האופי הכפול של CXCL9 הוביל למחקר בצורך למניפולציה שלו לתועלת תרפויטית. האיסטרטגיות הראשוניות כורכות חסימה של CXCL9 או עידוד פעילותו בתלות במחלה. במצבים כגון מחלות אוטו-אימוניות או בדחיית שתל, המטרה היא לעכב את CXCL9. חוקרים מפתחים תרופות, כולל נוגדנים חד-שבטיים, לנטרל את CXCL9 כדי למנוע ממנו התקשרות לקולטן CXCR3. גישה אחרת כרוכה ביצירת מעכבים קטנים לחסום את הקולטן CXCR3 עצמו, כדי למנוע מתאי T תגובה ל-CXCL9. תרפיות אלו מכוונות למנוע את הנדידה של תאי חיסון לרקמות רגישות, ועל ידי כך להפחית דלקת ונזק. היפוכו של דבר, בטיפול בסרטן, המטרה היא לעודד את השפעותיו של CXCL9. כיוון שרמות גבוהות יותר של CXCL9 בתוך גידולים משפרות את תוצאי המחלה, חוקרים מפתחים שיטות להגביר ישירות את יצירת CXCL9 בתוך הגידול. זה עשוי לכרוך תרפיות המעודדות הפרשת IFN-γ במיקרו-סביבה של הגידול, או אפילו החדרה ישירה של CXCL9 לגידול. המטרה היא לעודד את הגיוס של תאי T הפוגעים בתאים הסרטניים. יש חוקרים המתייחסים לכימוקין זה תחת השם monokine induced by γ-interferon (להלן MIG). חלבון זה הוא חלק מהמעקב של הגוף והתגובה לתאי הסרטן.
CXCL9 או Chemokine (C-X-C motif) ligand 9 השייך למשפחת הכימוקינים CXC. הכימוקין CXCL9 משחק תפקיד בכימוטקסיס, ובעידוד התמיינות ושגשוג של לויקוציטים ובגרימת extravasation או מצב של דליפת דם מכלי הדם לרקמה המקיפה אותו (Tokunaga וחב' ב- Cancer Treat Rev משנת 2018). כימוקין זה דומה לשני כימוקינים CXC הידועים כ-CXCL10 ו-CXCL11, שהגנים המקודדים אותם ממוקמים בסמוך לגן של CXCL9 על כרומוזום 4 באדם באתר 76.0-76.01 או בכרומוזום 5 בעכבר באתר 92.47 – 92.48 (Lee ו-Farber ב-Cytogenet Cell Genet משנת 1996, ו-O'Donovan באותו כתב עת משנת 1999). כל שלושת הכימוקינים, CXCL9 CXCL10 ו-CXCL11 מפעילים את התפקודים הכימוטקטיים שלהם על ידי תגובה עם הקולטן הכימוקיני CXCR3 (Tensen וחב' ב-J Investig Dermatol משנת 1999).
המבנה של CXCL9 מאופיין על ידי אזור N-טרמינלי קצר וגמיש, וליבה המיוצבת על ידי שני קשרים די-סולפידיים, שלושה beta-strands אנטי-מקבילים ו-C-טרמינל במבנה של alpha-helix (Valdés וחב' ב-Front Immunol משנת 2024). המבנה השלישוני המשומר מספק יציבות כמו גם את הגמישות המבנית החיונית בטרמינלים N ו-C מה שמאפשר אינטראקציות יעילות עם הקולטן שלו, CXCR3, ומקדם העברת סיגנל החיונית לנדידה של תאי החיסון ושפעולם. הליבה משומרת ביותר בין הכימוקינים מסוג CXC, בעוד שווריאציות באזורי הלולאה תורמות להבדלים בקישור לקולטן ולספציפיות התפקודית.
תפקוד
הפולריזציה של Th1 גם כן משפעלת את תאי החיסון בתגובתם ל-IFN-γ (Schoenborn ו-Wilson ב-Adv Immunol משנת 2007). לימפוציטים המסתננים לתוך הגידול הם מפתח לתוצאים הקליניים ולניבוי של התגובה למעכבי checkpoint (Fernandez-Poma וחב' ב-Cancer Res משנת 2017). מחקרים in vivo מציעים שליבת CXCL9 משחקת תפקיד טומורוגני בשגשוג ובגרורתיות, ועל ידי כך מסייעים להסננה לימפוציטית לאזורי הגידול ולדיכוי הגידול הסרטני (Gorbachev וחב' ב-J Immunol משנת 2007).
אפנון (מודולציה של החיסון)
בהתמיינות של תאי חיסון, מספר דיווחים מצביעים על כך ש-CXCL9 מעודד את הפולריזציה של T helper 1 (להלן Th1) דרך CXCR3 (ללZohar וחב' ב-J Clin Invest משנת 2014). במודל in vivo הדגימו Zohar וחב' ש-CXCL9 הגביר את השעתוק של T-beta- ו-RORγ, מה שמביא לפולריזציה של תאי Foxp3− type 1 regulatory (Tr1) או של תאי Th17 שמקורם בתאי T נאיביים דרך הזרחון של STAT4, STST1 ו-STAT5. מספר מחקרים הראו שמקרופאגים הכרוכים בגידול סרטני (להלן TAMs) הם בעלי השפעות מודולטוריות במיקרו-סביבה של הגידול, עם הציר CXCL9/CXCR3 המשפיע על הפולריזציה של TAM. למעשה, TAMs יכולים להפגין השפעות מנוגדות: מקרופאגים M1 מסייעים לפעילות האנטי-סרטנית, בעוד שמקרופאגים M2 מסייעים להתפתחות הגידול. נמצא שעכברים החסרים CXCR3 הראו יצירה מוגברת של IL-4 ופולריזציה של M2 במודל של סרטן השד, מלווים על ידי הפחתה בחיסון הטבעי (innate) ובתגובה האנטי סרטנית המתווכת על ידי תאים (Oghumu וחב' ב-Immunology משנת 2014).
באשר לשפעול של תאי חיסון, CXCL9 מעודד את הפולריזציה של Th1 ואת השפעול שלו, מה שמוביל ליצירה של IFN-γ, TNF-α ו-IL-2, ובכך מגביר את החסינות האנטי-סרטנית, על ידי שפעול של לימפוציטי-T ציטו-טוקסיים, של תאי NK ושל מקרופאגים (Mosser ו-Edwards ב-Nature Rev Immunol משנת 2008). בנוסף, לולאת השפעול החיסוני התלויה ב-IFN-γ ומעודדת הפרשה של CXCL9. נמצא שסיגנל אוטוקריני של CXCL9/CXCR3 בתאי סרטן מעודד שגשוג תאים אלה, אנגיוגנזה וגרורתיות.
רגולציה של checkpoint חיסוני
היחס בין הציר CXCL9/CXCR3 לבין המסלול של PD-L1/PD-1 חשוב ברגולציה החיסונית. הביטוי של programmed cell death protein 1 (או PD-1) גדל בתאי T בתוך הגידול, בהשוואה לתאי T בדם ההיקפי. נמצא שהתרפיה anti-PD-1 לא רק מגבירה את הרגרסיה של הגידול בתיווך תאי-T, אלא גם מגדילה את הביטוי של IFN-γ בתאים של מח העצם (Peng וחב' ב-Cancer Rs משנת 2012). בנוסף, טיפול עם נוגדן anti-CTLA4 הביא להגברת הרגולציה של הצי CXCL9/CXCR3 בטיפול בנגעי מלנומה במטופלים שהראו תגובה קלינית מועילה לטיפול עם ipilimumab (Ji וחב' ב- Cancer Immunol Immunother משנת 2012).
המשמעות הקלינית
CXCL10, CXCL9 ו-CXCL11 נמצאו סמנים ביולוגיים להתפתחות של אי-ספיקת לב ופגיעה בתפקוד של חדר הלב השמאלי, מה שמדגים קשר פתו-פיזיולוגי בין הרמות של כימוקינים אלה לבין התפתחות של פגיעה לבבית (Altara וחב' ב-PLoS One משנת 2015). כמו כן CXCL9 נמצא כרוך כסמן באבחון של הדבקות Q fever (ללJensen וחב' ב-BMC Infectious Diseases משנת 2017). CXCL9 זוהה גם כסמן של תרפיית adoptive T cell transfer במלנומה גרורתית (Bedognetti וחב' ב-Br J Caner משנת 2013).
תפקיד של חברי משפחת CXCL במחלות שונות
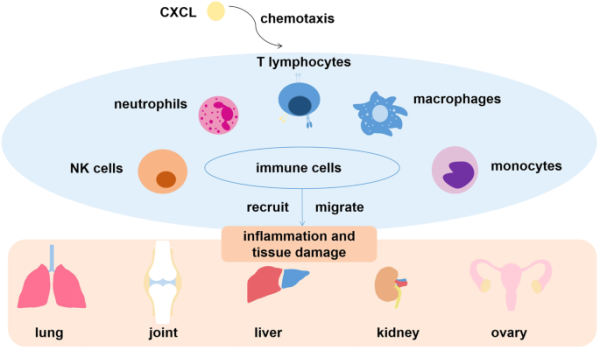
כימוקינים מסוג CXC יכולים לגייס ולשגר קטגוריות שונות של תאי חיסון, יכולים לווסת התנהגויות פתולוגיות של גידולים סרטניים כגון שגשוג, חודרנות וגרורתיות, ויכולים לשפעל אנגיוגנזה. CXCLs הם תת-משפחה של הכימוקינים, חיוני בתפקודים האחרונים, כולל הגיוס של תאי החיסון ומעורבות בתהליך הפתולוגי של הממאירות. הוכח שה-CXCLs קשורים במידה רבה בסוגי סרטן רבים כגון סרטן השד, ריאות, קיבה, מעי גס, שחלות, לבלב, מלנומה, הפאטומה. CXCLs משתתפים במחלות דלקתיות באיברים ורקמות שונים כגון ארטריטיס, לופוס, COPD, הפאטיטיס. הוכח ש-cxcls שולטים על דלקת דרך נדידת לויקוציטים הכוללים נויטרופילים, מונוציטים ומקרופאגים, על ידי שפעול של מסלולי איתות שונים כגון STAT3 ו-NF-κB, ובכך מאיצים את התפתחות הסרטן. התפקוד של CXCLs נעזר באינטראקציה עם קולטנים הקשורים ל-G protein על פני תאים (Miller ו-Mayo ב-Int J Mol Sci משנת 2017). בהתאם להבדלים ב-motif המשומר של ציסטאין הקרוב ל-N-טרמינל שלהם, כימוקינים מחולקים ל-4 קבוצות: CXCL ,CCL, XCL ו-CX3CL (Hughes ו-Nibbs ב-FEBS J משנת 2018). משפחת CXCL היא אחת המרכזיות בין הכימוקינים, והמולקולות הקטנות של משפחה זו מופרשות על ידי תאי סרטן, לויקוציטים, פיברובלסטים, תאי אנדותל, ותאי אפיתל.
המבנה והתפקוד של משפחת CXCL
CXCL1, ידוע כאונקוגן הקשור לגדילה, יכול להיות מבוטא בתאי חיסון ובנוירונים. תפקידו העיקרי הוא לגייס אימונוציטים, בעיקר נויטרופילים (Jiang וחב' ב-Int Immunopharmacology משנת 2023). CXCL2 גם הוא אונקוגן הקשור בגדילה, המיוצר על ידי מונוציטים ומקרופאגים משופעלים. הוא גורם לכימוטקסיס של נויטרופילים. CXCL3 גם הוא גורם כימוטקטי של נויטרופילים. CXCL4 הידוע גם כ-platelet factor 4, הוא חלבון קטן המשוחרר מטסיות משופעלות. CXCL5 ידוע גם כ-epithelial activating neutrophil protein, משחק תפקיד במערכת החיסון במצבי דלקת. CXCL6 הידוע גם כ-granulocyte chemotactic protein 2, הוא מגיב-כימו של נויטרופילים דרך הקולטנים CXCR1 ו-CXCR2. הוא קשור לחודרנות של תאים, לאפופטוזיס ולשגשוג תאים (Wang וחב' ב-Cancer Biol Ther משנת 2021). CXCL7, הידוע גם כ-neutrophil activating peptide 2, מופרש מתאים מונוציטים ומקרופאגים ובכך מסייע להתקדמות הסרטן (Wang וחב' ב-Cell Death Dis משנת 2021, ו-Yan וחב' ב-Cancer Lett מאותה שנה). CXCL8 מופרש על ידי מקרופאגים ותאי אפיתל, הוא גורם אנגיוגני פעיל כמו גם גורם המסייע לדלקות ונוטל חלק בהתפתחות הסרטן, כולל שינויים במיקרו-סביבה הסרטנית (Fousek וחב' ב-Pharm Ther משנת 2021). לכימוקינים CXCL10 ,CXCL9 ו-CXCL11 יש אותו קולטן-CXCR3. הם מופרשים על ידי לויקוציטים, מקרופאגים, תאי סרטן ופיברובלסטים. הם יכולים להיות מושרים על ידי אינטרפרון לגיוס של תאי Th, תאי T ותאי NK לפעול כאנטי-הדבקות ואנטי תאים סרטניים (Dillemans וחב' ב-Cell Mol Life Sci משנת 2023). הכימוקין CXCL12 הידוע כ-stem cell-derived factor 1, הוא בעל תכונות אנגיוגניות, ומווסת התקדמות סרטן. CXCL13 המבוטא על ידי תאי סטרומה ומקרופאגים, הוא chemoattractant יעיל של תאי B (Hoellwerth וחב' ב-Life משנת 2023). הוא משחק גם תפקיד בהתפתחות סרטן. CXCL14 הוא כימוקין משומר ביותר ובעל תפקיד בהסננה של תאי חיסון, במוביליזציה ובבשלות של תאים דנדריטים. CXCL14 שמקורו מתאים שונים משפיע על התפתחות בדרכים שונות: כאשר הוא מופרש מפיברובלסטים הוא מעודד התפתחות סרטן, אך כאשר הוא מופרש מתאי אפיתל, הוא דווקא מעכב את התפתחות הסרטן (Gowhari-Shabgah וחב' ב-Int Immunopharmacol משנת 2021). CXCL16 הוא כימוקין המבוטא בכבד, בריאות ובכליות. הוא מגייס תאי NK להגן בעיקר כנגד גידולים סרטניים (Korbecki וחב' ב-Cancer Res משנת 2021). CXCL17 מיוצר על ידי האפיתל של דרכי האוויר, ומייצר השפחות חיוביות אך גם פתולוגיות בסוגי סרטן שונים. הוא chemoattractant של מונוציטים ומקרופאגים. הוא משתתף בגיוס תאים מיאלואידים, ומעכב מיקרו-אורגניזמים פתולוגיים וכן מעכב אנגיוגנזה בסרטן (Hashemi ו-Khorramdelazad ב-J Cell Commun Signal משנת 2022).
תפקידי משפחת CXCL בסרטן
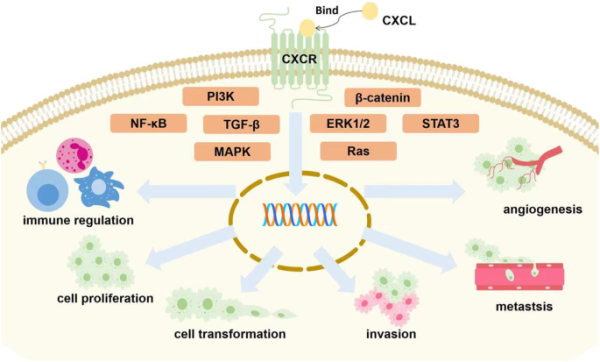
רוב הכימוקינים מסוג CXCL נקשרים לקולטנים וכרוכים בצמיחה של גידולים על ידי שפעול של מסלולים שונים של איתות כגון STAT3, Zhuo) NF-κB וחב' ב-Biol Direct משנת 2022), Ras, MAPK, P13K, TGF-β, β-catenin, ו-ERK1/2. הכימוקין משפיע על השגשוג, החודרנות, הנדידה, והממאירות של תאים סרטניים, כמו גם על בקרת החסינות, והאנגיוגנזה של הגידול.
הוראות לביצוע הבדיקה
את הדם יש להכניס למבחנת ספירת-דם (EDTA, פקק סגלגל). תוך 8 שעות מנטילת הדם יש לסרכז את המבחנה ולאחר הסרכוז יש להעביר את נוזל הפלזמה העליון למבחנת פלסטיק ולהקפיא מיד לצורך העברה למעבדה כנוזל קפוא. הדגימה הקפואה יציבה למשך 180 יום.
שיטת הבדיקה: Automated microfluidics immunoassay.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק