לויקואנצפלופתיה רב מוקדית מתקדמת - Progressive multifocal leukoencephalopathy
הופניתם מהדף לויקואנצפלופתיה רב מוקדית מתקדמת לדף הנוכחי.
| לויקואנצפלופתיה רב מוקדית מתקדמת | ||
|---|---|---|
| Progressive multifocal leukoencephalopathy | ||
| ICD-10 | Chapter A 81.2 | |
| ICD-9 | 046.3 | |
| MeSH | D007968 | |
| יוצר הערך | ד"ר מירב טשורני | |
לויקואנצפלופתיה רב מוקדית מתקדמת (PML, Progressive Multifocal Leukoencephalopathy) היא מחלה דמיאלנטיבית (Demyelinative) קטלנית ונדירה של מערכת העצבים המרכזית. המחלה נגרמת כתוצאה מראקטיבציה (Reactivation) של Polyomavirus JC (JCV) באוליגודנדרוציטים (Oligodendrocytes) הגורמת לנזק ליטי, ולדמיאלניזציה משנית של החומר הלבן במערכת העצבים המרכזית (תמונה 1). ישנו טיפול מסוים כנגד הנגיף ועם זאת, היות שהראקטיבציה היא באסוציאציה למערכת חיסונית חלשה, הטיפול העיקרי הוא חיזוק מערכת החיסון התאית בחולים.
אפידמיולוגיה
אתיולוגיה
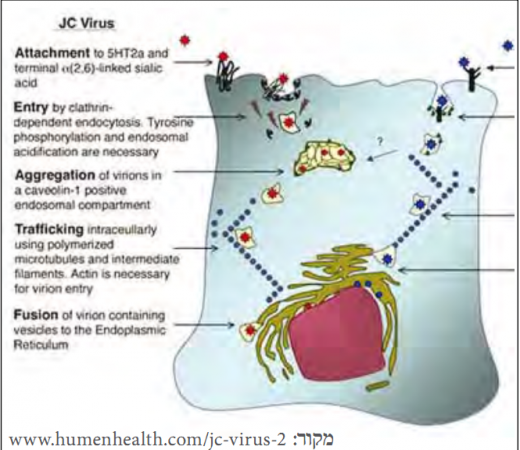
נגיף JC קרוי על שמו של מטופל בשם John Cunningham שאובחן עם PML. הנגיף שייך למשפחת DNA polyomavirus. לנגיף 3 חלבוני קפסיד היוצרים 8 פנוטיפים שונים כאשר פנוטיפ מספר 2 נמצא בנוזל השדרה או ברקמת המוח בחולה עם PML (תמונה 2). בני האדם הם מאחסנים בלעדיים של הנגיף והוא מצוי בצורתו הלטנטית ב-75 אחוז מהאוכלוסייה הכללית עקב זיהום ראשוני על ידי שאיפת הנגיף למערכת הנשימה. הנגיף נקשר לרצפטורים (2,6) Sialic acid α ול-HT2a-5 המצויים על פני תאים ברקמה הלימפואידית (שקדים), מח עצם ותאי פלזמה, אפיתל כליה, אוליגודנדרוציטים ואסטרוציטים (Astrocytes) המשמשים לו כרזרבואר בצורתו הלטנטית (תמונה 3). לכן, נוכחות PCR (Polymerase Chain Reaction) חיובי ל-JCV בבדיקות בשתן (עד 25 אחוז מהאוכלוסיה הכללית) אינה מהווה עדות למחלה פעילה.
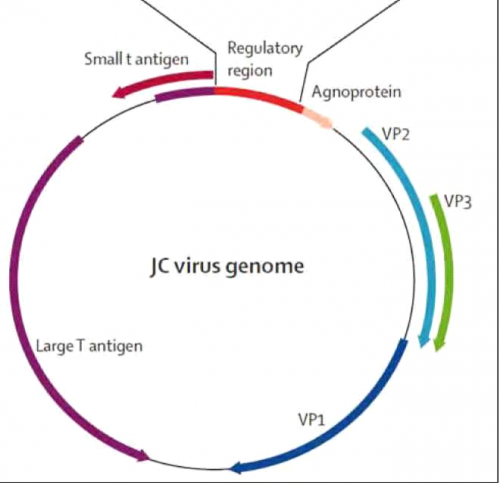
אם קיימת מערכת חיסון תאית ירודה, הנגיף עובר ריאקטיבציה באוליגודנדרוציטים וגורם לדמיאלניזציה במערכת העצבים המרכזית. על כן, PCR חיובי ל-JCV בנוזל השדרה מעיד על מחלה. התגובה החיסונית ההומורלית אינה מספקת למניעת ראקטיבציה ועל כן, נחוצה תגובה תאית למניעת ראקטיבציה של JCV[1],[2].
ראקטיבציה של JCV עלולה להתרחש באוכלוסיה עם מערכת חיסון תאית ירודה - חולי HIV (Human Immunodeficiency Virus), מחלה לימפופרוליפרטיבית או מושתלים המטופלים בתכשירים מונעי דחית שתל.
תוארו מספר מקרי PML במטופלים בנוגדנים מונוקלונליים כגון Efalizumab Raptiva לחולי פסוריאזיס, Mabthera (Rituximab) לחולי לימפומה וכן Tysabri (Natalizumab) לחולי טרשת נפוצה. עם זאת קשה לבודד את תפקיד התרופות המונוקלונליות כפתוגנזה אפשרית ל-PML כיוון שרוב החולים טופלו בעבר באימונוסופרסיה (Immunosuppression) על רקע מחלתם הבסיסית.
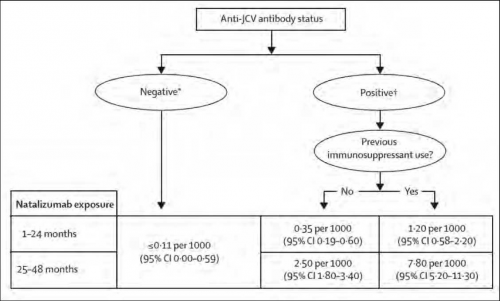
הארעות הופעת PML במטופלי Tysabri עומדת על 1.5 ל-1,000 מטופלים. תוארו מספר מאפייני מטופלים העלולים לפתח PML בסבירות גבוהה[3] (תמונה 6) והם:
- מערכת חיסון תאית חלשה (HIV, מושתלים ובעלי מחלות לימפופרוליפרטיביות)
- טיפול קודם באימונוסופרסיה
- טיפול ממושך ב-Tysabri (מעל 25 טיפולים)
- JCV חיובי בתחילת הטיפול
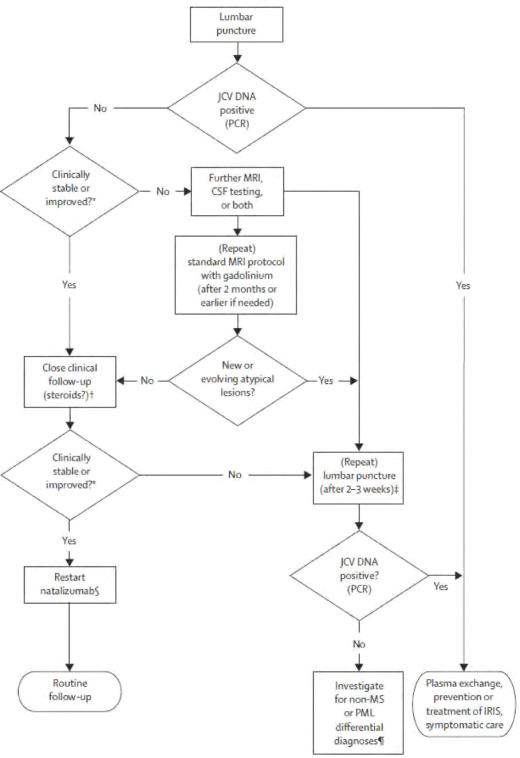
בשל תוצאות מחקרים אלה נבנה אלגוריתם ניהול חולה טרשת נפוצה המטופל ב-Tysabri כמתואר בתמונה 7. בהפסקת הטיפול ב-Tysabri, בהופעת PML, יש לזכור כי זמן מחצית החיים של התרופה הוא 3 חודשים. לאור זאת, יש הנעזרים בפלזמה פרזיס (Plasmapheresis) על מנת לזרז את סילוקה מהמחזור ויש לכך מחיר: IRIS (Immune Reconstitution Inflammatory Syndrome) כתוצאה מהחלמה מהירה מדי של מערכת החיסון התאית.
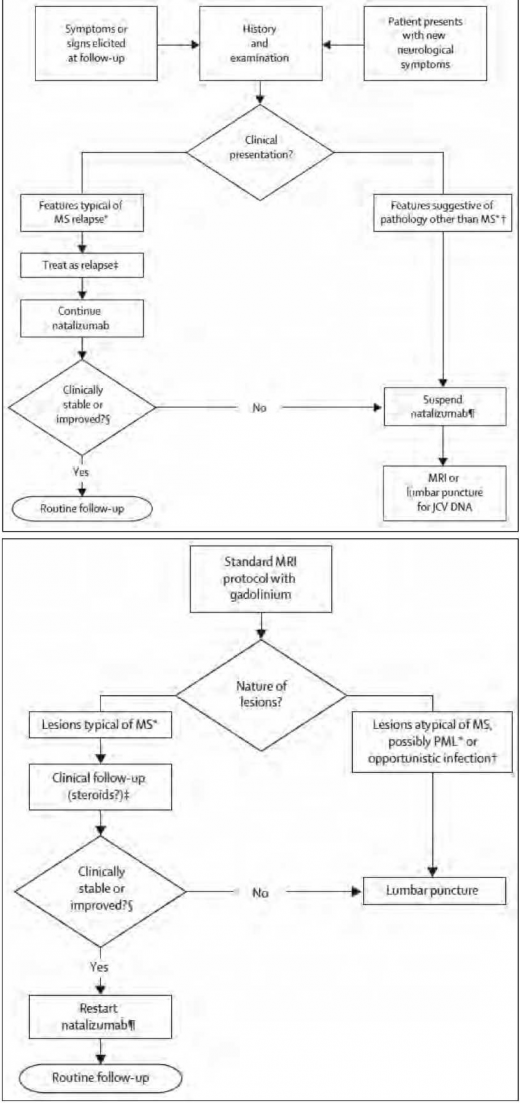
קליניקה
הפגיעה הקלינית תתבטא בעיקר בירידה קוגניטיבית, אולם בשל הנטיה לפגיעה בצומת החומר האפור-לבן במוח ניתן יהיה לראות גם אפזיה, פגיעה בקואורדינציה, פגיעה בראיה ופרכוסים. בניגוד למחלות דמיאלנטיביות אחרות (טרשת נפוצה וכדומה), ב-PML עצבי הראיה וחוט השדרה בדרך כלל שמורים.
וירוס JC יכול לפגוע לא רק בחומר הלבן במוח אלא גם בחומר האפור בצרבלום ובקורטקס הצרברלי, כמו גם בקרומי המוח[1]:
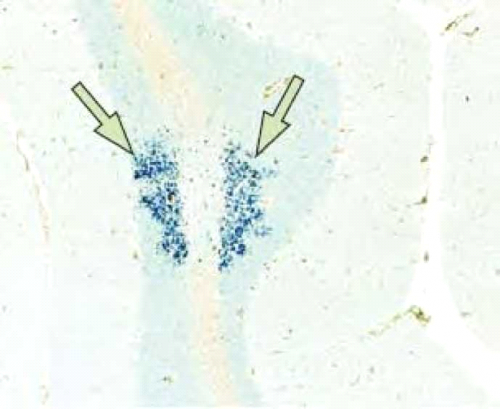
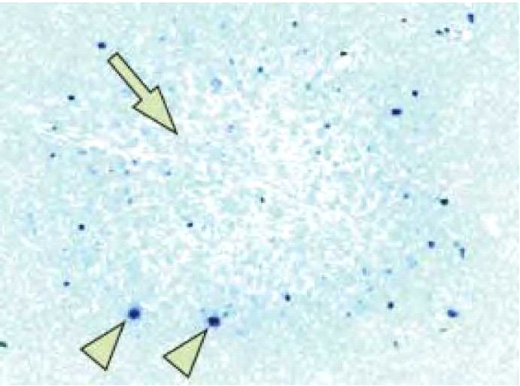
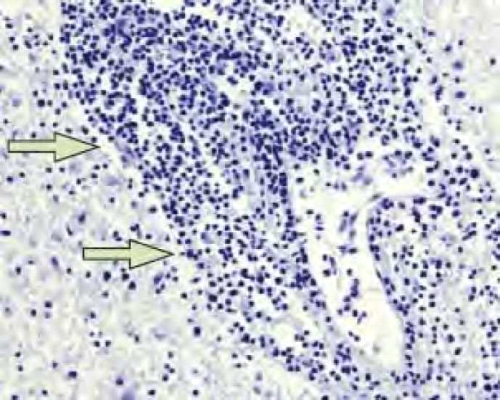
- Granule cell neuronopathy - הנגיף גורם לליזיס של תאי Granule בצרבלום (לעומת תאי גליה ב-PML) המביא לאטרופיה צרבלרית והתבטאות קלינית של דיסארתריה, הליכה אטקטית וחוסר קואורדינציה (תמונה 4).
- אנצפלופתיה (Encephalopathy) - זיהום ליטי פולמיננטי של נוירונים קורטיקלים פירמידליים[4]. מנגנוני פתופיזיולוגיה אפשריים: התקדמות הוירוס מהצומת אפור-לבן לחומר האפור או פנוטיפ של וירוס JC, שתוקף ישירות את החומר האפור.
- דלקת קרום המוח (Meningitis) - תוארו מספר מקרים של חולים עם סימנים מנינגיאליים בנוכחות וירוס JC בנוזל השדרה, ללא מעורבות רקמת המוח.
אבחנה
בהדמיה מוחית נוכל לראות נגעים מפושטים מפוזרים בחומר הלבן (סמוך לצומת האפור-לבן) ללא בצקת או סימני לחץ (בניגוד למחלות דמיאלנטיביות אחרות כגון טרשת נפוצה). תיתכן מעורבות גרעיני בסיס או תלמוס המכילים סיבי מיאלין. בבדיקת תהודה מגנטית (MRI, Magnetic Resonance Imaging) הנגעים יהיו היפראינטנסים ב-FLAIR ו-T2 והיפואינטנסים ב-T1.
טיפול
אין טיפול ספציפי כנגד נגיף ה-JC. תוארו מספר תרופות בהקשר לטיפול בנגיף, כגון Mirtazapine בהיותה חסם רצפטור סרוטונרגי (5-HT2a) המונעת את קשירת הנגיף לתאים כמו גם Chlorpromazine בהיותו מעכב Clathrin החיוני לאנדוציטוזיס (Endocytosis) של הנגיף לתוך התא. קיימות תרופות נוספות הנמצאת בשלבי מחקר מבוקרים שונים כגון Lariam (Mefloquine) (אנטי מלריה) - Cytarabine (כימותרפיה) המעכבים רפליקציה ויראלית ו-2-IL שמטרתה חיזוק מערכת החיסון התאית.
עיקר הטיפול ב-PML הוא החזרת עטרה ליושנה, הווה אומר, להחזיר את התגובה החיסונית התאית לשליטה על נגיף JC על ידי מתן HAART (Highly Active Anti Retro-viral Therapy) בחולי HIV ובאלה שאינם חולי איידס (ממאירות לימפופרוליפרטיבית או מושתלים), החזרת התגובה החיסונית התאית על ידי הפסקת התרופות מדכאות החיסון.
Immune Reconstitution Inflammatory Syndrome
בצורה פרדוקסלית, עם הפסקת הטיפול הכימותרפי או התחלת הטיפול ב-HAART, מערכת החיסון "המשתקמת" יכולה לגרום דווקא להחמרה קלינית, תופעה הידועה בשם IRIS (Immune Reconstitution Inflammatory Syndrome). בשל היווצרות תגובה תאית אנטי-דלקתית סביב הנגע הדמיאלנטיבי ופגיעה ב-BBB (Brain Blood Barrier) (תמונה 5) נוצרת בצקת סביב הנגע עם סימני לחץ והאדרה, וזאת בניגוד לנגע PML קלאסי שהינו ללא סימני בצקת ואינו עובר האדרה. IRIS יכול להופיע בין שבוע עד שנה לאחר התחלת הטיפול ב-HAART או הפסקת הטיפול הכימותרפי.
קיימים מחקרים התומכים במתן טיפול בסטרואידים להפחתת התגובה התאית האנטי דלקתית הסוערת לשם שיפור הפרוגנוזה[5],[6]. במטופלי HAART יש להמשיך את הטיפול האנטי רטרו-ויראלי ולא להפסיקו וזאת כדי להימנע מיצירת מוטציות HIV עמידות לטיפול.
פרוגנוזה
נוכחות תאי CD-8 T ספציפיים כנגד JCV היא סמן פרוגנוסטי טוב ומעלה את שיעור year survival-1 מ-46 אחוז ל-76 אחוז[7]. גם האדרה מוחית בחולים משמשת פקטור פרוגנוסטי טוב בהיותה עדות עקיפה למערכת חיסון תאית פעילה[7]; year survival-1 של 83 אחוז לעומת 39 אחוז בחולי PML בהם הנגעים לא עוברים האדרה.
מתן HAART בחולי HIV העלה את שיעור Year survival-1 מ-PML מ-10 אחוז ל-50 אחוז.
דגלים אדומים
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 1.3 1.4 Tan CH, Koralnik IJ, Lancet Neurology, 2010; 9,425
- ↑ Jilek S, Jaquiery E, Hirsch HH et al., Lancet Neurol¬ogy, 2010; 9,566
- ↑ 3.0 3.1 3.2 Kappos L, Bates D, Edan G et al., Lancet Neurology, 2011; 10, 745
- ↑ Wu'thrich C, Dang X, Westmoreland S et al., Ann Neurol, 2009;65,742
- ↑ Berger JR, Neurology, 2009; 72,1454
- ↑ Tan K, Roda R, Ostrow L et al., Neurology, 2009;72,1458
- ↑ 7.0 7.1 Marzocchetti A, Tompkins T, Clifford DB, et al., Neu¬rology, 2009;73,1551
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר מירב טשורני, המחלקה לנוירולוגיה, המרכז הרפואי תל אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק