לישמניאזיס של העור בישראל - Cutaneous Leishmaniasis in Israel
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| לישמניאזיס של העור בישראל | ||
|---|---|---|
| ' | ||
| ||
| יוצר הערך | גב' יעל גלזר, דר' דן גנדקו, דר' לאור אורשן, דר' איזבלה קרקיס, דר' רועי סינגר, דר' אמיליה אניס | |
לישמניאזיס היא מחלה זואונוסית הנגרמת ע"י טפילים חד תאיים מהמין לישמניה (Leishmania). טפילי הלישמניה מתפתחים בתאי מערכת החיסון של חולייתנים ומועברים בעקיצה על ידי נקבת זבוב החול המכונה הוקטור של המחלה.
נהוג לסווג את הלישמניאזיס לפי ביטויה הקליניים לשלוש קבוצות עיקריות:
- לישמניאזיס של העור (cutaneous leishmaniasis), בה הטפילים נשארים באזור העקיצה המדביקה וגורמים לחבורה מקומית;
- לישמניאזיס של האיברים הפנימיים (visceral leishmaniasis), בה הטפילים מתרבים ברקמות פנימיות כולל הכבד והטחול, ומתפתחת מחלה סיסטמית העלולה להסתיים במוות ללא טיפול מתאים;
- לישמניאזיס של הריריות (mucocutaneous leishmaniasis), בה הטפילים נודדים לרקמות הריריות של האף והלוע וגורמים להרס נרחב של הרקמות ודפורמציה.
מקובלת חלוקה נוספת של המחלות בהתאם לאקולוגיה של מעגל ההעברה:
- לישמניאזיס זואונוטית - מעגל העברה של הטפילים מתקיים בין זבובי החול ובין בעלי חיים המשמשים כחיות מאגר, וההדבקה של בני אדם היא אקראית ואינה חשובה להמשך העברת הטפיל.
- לישמניאזיס אנתרופונוטית - האדם הוא המאחסן העיקרי והטפילים מועברים על ידי זבובי החול מאדם לאדם. מעגל העברה זואונוטי נפוץ באזורים כפריים ופתוחים ובשולי ערים. מעגל העברה אנתרופונוטי מצוי בד"כ במרכזים עירוניים המיושבים בצפיפות. כל אחד מהטיפוסים הקליניים של המחלות יכול להיות מועבר במעגל זואונוטי או אנתרופונוטי.
לישמניאזיס היא מחלה אנדמית ביותר מ- 80 מדינות ברחבי העולם ואחת מתשע המחלות הזיהומיות הנפוצות ביותר בעולם. כ- 20 מיני לישמניה ידועים כגורמים למחלות בבני אדם. מעריכים שמדי שנה ישנם בין 1.5 - 2 מיליון חולים חדשים במחלה[1]. נתוני ארגון הבריאות העולמי מצביעים על עלייה בתחלואה ההומאנית והתפשטות של מחלות הלישמניאזיס לאזורים חדשים. התחלואה אינה יציבה ומתבטאת בתנודתיות לא סינכרונית. גורמים טבעיים, תנועת אוכלוסייה ופיתוח נחשבים לגורמים משמעותיים המשפיעים על ההתפרצויות ועל התפשטות המחלות לאזורים חדשים.
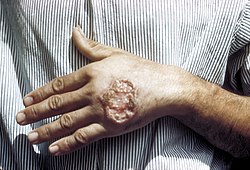
לישמניאזיס של העור היא הצורה השכיחה ביותר של המחלה ומצויה ברבות ממדינות אגן הים התיכון ואסיה כמו: ישראל, ירדן, לוב וטוניסיה. על פי רוב, המחלה מתחילה כקשריר או נגע במקום העקיצה אשר גדל, מפתח קרום ובסופו של דבר הופך לכיב. אבולוציית המחלה ממושכת ונעה בין 3-18 חודשים עד לריפוי. תקופת הדגירה של המחלה נמשכת בד"כ בין שבועיים למספר חודשים [2]. בסוף תהליך הריפוי עשויות להישאר צלקות. אף שהמחלה אינה גורמת לתמותה, עלולים להיגרם ממנה סיבוכים תפקודיים ו/או קוסמטיים בשיעור של עד ל- 1% [3] , [4]. עיכוב באבחון המחלה ובתחילת מתן טיפול מתאים עלולים לגרום סבל נוסף לחולים. אדם שחלה בלישמניאזיס של העור הוא מחוסן למין הטפיל שגרם לה. מחלה זו מהווה מטרד ועד היום לא נמצאו פתרונות יעילים כולל חיסון, למניעתה [5].
לישמניאזיס של העור בישראל
לישמניאזיס של העור היא אנדמית בארץ ומחייבת הודעה פרטנית החל משנת 1949. המחלה מוכרת גם בשמות "שושנת יריחו" ו"חבורת יריחו". אין חובה לאשר מעבדתית כל מקרה מחלה מדווח ואין הבחנה בין מקרים חשודים המזוהים בד"כ בבדיקה סרולוגית, לבין מקרים וודאיים, המאושרים מעבדתית. לכן, הן מקרים חשודים והן מקרים וודאיים נספרים כמקרי תחלואה במחלה. שיטת הדיווח הנהוגה בישראל היא סבילה ובדומה למדינות אחרות, ידוע שקיים תת-דיווח של המחלה. היות ולאורך השנים לא נעשו שינויים בשיטת הדיווח או בהגדרת המקרה של המחלה, מניחים שניטור התחלואה בשיטה זו משקף את מגמות התחלואה האמיתיות ומאפשר לזהות התפרצויות בזמן אמת.
בישראל מחלות הלישמניאזיס של העור הן זואונוזות. מחוללי המחלה הם הטפיל (.Leishmania (L major המועבר על ידי זבוב החול מהמין Phlebotomus (P.) papatasi והטפיל L. tropica המועבר על ידי זבובי החול מהמינים P. sergenti ו- P. arabicus. פסמון המדבר ומריון המדבר נחשבים לחיות המאגר העיקריות ל- L. major בעוד ששפנים הם חיות המאגר המרכזיות ל- L. tropica. טכנולוגיות מולקולאריות מאפשרות כיום לזהות את מין הלישמניה הן בדגימות של חולים, הן בזבובי החול והן בחיות המאגר.
העברה אנדמית של הטפיל L. tropica קיימת סביב הכנרת, באזור גב ההר ביהודה ובשומרון, מרכז הגליל ובקעת כנרת. העברה אנדמית של הטפיל L. major קיימת בבקעת בית שאן, הנגב המערבי, הר הנגב והערבה.
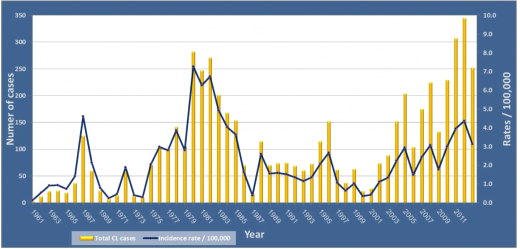
במבט היסטורי על שיעורי התחלואה המדווחים לאגף לאפידמיולוגיה (תרשים 1), ניתן לראות שעד סוף המאה ה- 20, שיעורי התחלואה נעו במחזוריות של כעשר שנים. תקופות שבהן שיעורי המחלה היו גבוהים נצפו ב:
- 1965-1969 עם שיא של מקרים ב- 1967; ככל הנראה בעקבות מלחמת ששת הימים, כתוצאה מחשיפה של אנשים לא מחוסנים לאזורים גיאוגרפיים האנדמיים למחלה.
- 1975-1986 עם שיא בשנים 1980-1982; ככל הנראה משקף את המשך העלייה במספר הישובים החדשים שהוקמו ממערב לעמק הירדן לכיוון ירושלים.
- 1988-1996 עם שיא בשנים 1988 ו- 1995-1996 .
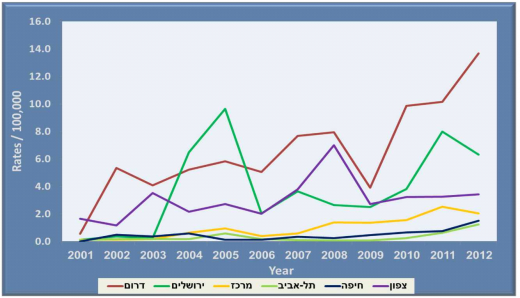
בעשור האחרון, מרבית מקרי התחלואה דווחו מאזור הנגב, הידוע כאנדמי לזן לישמניה מיגו'ר (תרשים 2). בנוסף, היו מספר התפרצויות במוקדים חדשים: ב- 2003 התפרצות בכנרת, ב-2004-05 במעלה אדומים (נפת ירושלים), ב- 2007-08 בשדה אליהו (נפת עפולה) וב- 2012 באופקים (מחוז דרום).
שיעורי היארעות המחלה ל- 100,000 תושבים עלו מ- 1.3 ב- 2003 ל- 4.3 ב- 2012 ככל הנראה כתוצאה מהתפשטות המחלה ליישובים חדשים, שינויים במערכות אקולוגיות כתוצאה מפיתוח, שינויים דמוגרפיים ושינויים בשימושי קרקע אשר גרמו ליצירת תנאי מחייה מטיבים ביחס לתנאי הסובב בבית הגידול הטבעי וליצירת בתי גידול מלאכותיים רבים לזבובי חול ולחיות המאגר לטפיל הלישמניה. הרחבת יישובים קיימים והקמת יישובים חדשים מצמצמים מרחקים בין הישובים, ומאיצים ככל הנראה את קצב התפשטות המחלה למקומות חדשים בארץ.
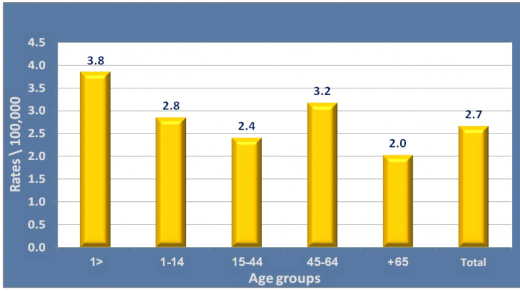
שיעורי ההיארעות הגבוהים ביותר של המחלה דווחו בד"כ בקרב תינוקות עד גיל שנה (תרשים 3), ככל הנראה בעקבות חשיפה ראשונה לטפיל. יחד עם זאת, מרבית מקרי התחלואה השנתיים מדווחים ע"י קבוצת גיל 15-44, ככל הנראה כתוצאה מחשיפה תעסוקתית הכוללת שעות מרובות בחוץ עקב טיולי טבע באזורים השונים מהמקום המגורים.
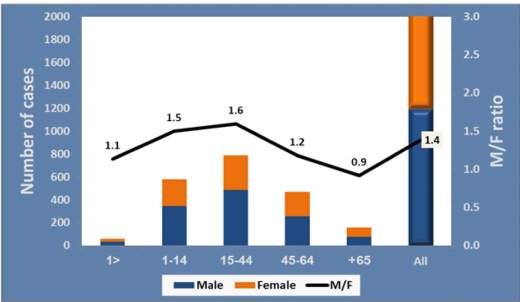
המחלה שכיחה יותר בקרב גברים, למעט אצל מבוגרים מגילאי 65 ומעלה (תרשים 4).
התמודדות עם המחלה
בשנים האחרונות נצפית הופעה של המחלה במוקדי תחלואה חדשים. למרות מאמצים רבים של אנשי מקצוע ומחקר בארץ ועולם, וחרף השקעה ניכרת של משאבים כספיים בנושא בקנה מידה עולמי, לא נמצא עדיין פתרון שורש מבוסס עובדות למניעת המחלה ולהפחתת התחלואה.
לכן, באוגוסט 2012 הממשלה החליטה להטיל על השר להגנת הסביבה בתיאום עם משרד הבריאות, משרד הביטחון, משרד הפנים ורשות הטבע והגנים, לבחון את דרכי ההתמודדות להפחתת מפגעי הלישמניה בישראל (החלטת ממשלה חכ/296) [6].
בעקבות זאת, הוחל בתכנית פעולה לשלוש שנים, הכוללת, בין היתר: ביצוע פעולות הסברה לציבור בישובים נבחרים וביצוע פעולות ניסיוניות סביבתיות להפחתת ההעברה של לישמניה באמצעות זבובי חול מחיות מאגר לבני אדם. כמו כן, יבוצעו ניטור והערכה של מידת ההצלחה של הפעולות הניסיוניות, מחקרים לקידום הידע על דרכי העברת המחלה ומציאת אמצעים יעילים להפחתת מפגעי הלישמניה [6]. אחד מן המחקרים שאושרו למימון ע"י המשרד להגנת הסביבה, יבוצע ע"י אוניברסיטת בן-גוריון, בשיתוף עם האגף לאפידמיולוגיה במשרד הבריאות במטרה לזהות אזורים סביבתיים עם סיכון מוגבר לחשיפה ללישמניאזיס של העור בעזרת מידע על החולים במחלה, המדווחים לאגף לאפידמיולוגיה מכל הארץ.
דגלים אדומים
ביבליוגרפיה
- ↑ WHO. The world health report 2004. Changing history. Geneva:WHO, 2004.
- ↑ Piscopo T V, Azzopardi CM. Leishmaniasis. Postgrad Med J. 2007 February; 83(976): 649-657.
- ↑ L. Heymann D. Control of Communicable Diseases Manual. 19th Edition, 2008.
- ↑ Bari AU. Clinical spectrum of cutaneous leishmaniasis: an overview from Pakistan. Dermatol Online J. 2012 Feb 15;18(2):4.
- ↑ Raman VS, Duthie MS, Fox CB, Matlashewski G, Reed SG. Adjuvants for Leishmania vaccines: from models to clinical application. Front Immunol. 2012;3:144. doi: 10.3389/fimmu.2012.00144. Epub 2012 Jun 11.
- ↑ 6.0 6.1 http://www.sviva.gov.il
קישורים חיצוניים
המידע שבדף זה נכתב על ידי גב' יעל גלזר - האגף לאפידמיולוגיה, דר' דן גנדקו - האגף לאפידמיולוגיה, דר' לאור אורשן - המעבדה האנטומולוגית, דר' איזבלה קרקיס - האגף לאפידמיולוגיה, דר' רועי סינגר - האגף לאפידמיולוגיה, דר' אמיליה אניס - האגף לאפידמיולוגיה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק