מחלת קרוהן - Crohn's disease
הופניתם מהדף מחלה ע"ש קרוהן לדף הנוכחי.
| מחלת קרוהן | ||
|---|---|---|
| Crohn's disease | ||
| 250px | ||
The three most common sites of intestinal involvement in Crohn's disease are
ileal, ileocolic and colonic
| ||
| ICD-10 | Chapter K 50. | |
| ICD-9 | 555 | |
| MeSH | D003424 | |
| יוצר הערך | ד"ר ערן ישראלי תת פרק 'טיפול ביולוגי' עודכן על ידי ד"ר אורית קרני-רחקוביץ' בפברואר 2017 |
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מחלות מעי דלקתיות
מחלת קרוהן (Crohn's disease) ודלקת כיבית של המעי הגס (Ulcerative colitis) מהוות את שתי הצורות העיקריות של מחלת המעי הדלקתית (Inflammatory Bowel Disease). מחלות אלו מאופיינות בקיום של דלקת כרונית או התקפית בדרכי העיכול, הנוצרת על ידי שפעול אידיופטי (Idiopathic) של מערכת החיסון.
הדלקת במחלת קרוהן יכולה לערב כל אחד מהחלקים של מערכת העיכול (מחלל הפה ועד לפי הטבעת), אך ברוב החולים המעורבות הדלקתית היא בקצה המעי הדק (Terminal ileum) ובמעי הגס המקורב. במרבית המקרים הדלקת אינה רציפה, וניתן לראות מוקדים דלקתיים לצד אזורים תקינים לאורך דופן המעי. הדלקת יכולה לערב את כל שכבות דופן המעי – מהרירית ועד לסרוזה. בהתאם לכך, עלולים להופיע סיבוכים שונים - כגון היצרות חלל המעי, מורסה תוך-בטנית, או היווצרות נצורים (Fistulae) בין לולאות מעי סמוכות או מלולאת מעי דלקתית לאיברים סמוכים [שלפוחית השתן, הלדן (Vagina), או דופן הבטן].
התסמינים השכיחים במחלה כוללים שלשול, כאבי בטן וירידה במשקל. כמו כן, ישנה מעורבות ספציפית של איברים מחוץ למערכת העיכול - כולל הפרקים, העור והעיניים. האטיולוגיה של המחלה אינה ברורה במלואה. קיים טיפול יעיל למניעת התסמינים והסיבוכים, אך לא קיים טיפול המביא לריפוי מוחלט של המחלה.
אפידמיולוגיה
שכיחות גבוהה יותר של המחלה נצפית בארצות מתועשות ובאוכלוסייה ברמה סוציואקונומית גבוהה, בהשוואה למדינות מתפתחות. עוד בשנות ה-60 נצפה יחס הפוך בין שכיחות המחלה לשיעור תמותת התינוקות (כמדד לרמה הסוציואקונומית) באזורים גיאוגרפיים שונים על פני כדור הארץ. בצפון אמריקה ובאירופה נצפה סולם עולה של שכיחות מדרום לצפון - שכיחות גבוהה יותר של המחלה תוארה באזורים הצפוניים של היבשת ביחס לאזורים הדרומיים.
בהתאם לשונות הגיאוגרפית המתוארת לעיל בארה"ב (ארצות הברית) ובאירופה, ההיארעות השנתית באוכלוסיה מתואמת לגיל ל-105 (Annual incidence) נעה בין 0.9 (דרום אירופה) ל-14 (סקנדינביה, ארה"ב). שכיחות המחלה באסיה נמוכה (0.5/105 - יפן וקוריאה), ובדרום אמריקה ובאפריקה נדירה.
שינוי בהיארעות המחלה נצפה לא רק בהתאם לאזור הגיאוגרפי, אלא גם לאורך ציר הזמן. בעשורים האחרונים ישנה עלייה דרמטית בהיארעות המחלה בארצות מתפתחות (כדוגמת קוריאה הדרומית), לעומת עלייה מתונה יותר או ללא שינוי בהיארעות באירופה ובארה"ב. ייתכן וחלק מהעלייה בהיארעות בארצות המתפתחות נובע מהתקדמות הרפואה ושיטות האבחון. יחד עם זאת, ההיארעות של דלקת כיבית של המעי הגס באותו פרק זמן לא עלתה משמעותית, ומדובר בשיטות אבחון דומות. כך, שלפחות חלק מהעלייה בהיארעות המחלה היא אמיתית. היארעות המחלה (Prevalence) בארה"ב מוערכת בכ-201 ל-105 במבוגרים, ו-43 ל-105 בילדים ובמתבגרים עד גיל 20.
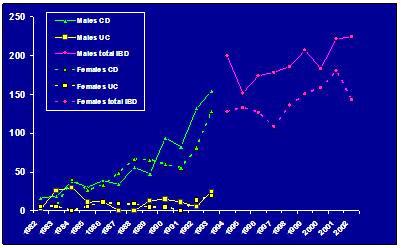
אין נתונים מדויקים לגבי שכיחות המחלה בישראל, אך ישנם מספר מחקרים שבוצעו בקרב אוכלוסיות נבחרות (כגון אוכלוסיות הקיבוצים והמושבים בצפון הארץ). במחקר שכלל נתונים לגבי כלל המתגייסים לצה"ל (צבא ההגנה לישראל) (גרף מספר 1) ניתן לראות כי ההימצאות של מחלת קרוהן בקרב בני נוער עד גיל 17 עלתה פי שלושה מתחילת שנות ה-80 ועד אמצע שנות ה-90, בעוד ששכיחותה של הדלקת הכיבית של המעי הגס נשארה יציבה לאורך השנים.
ניתן לאבחן את מחלת קרוהן בכל גיל (מינקות ועד לגיל הקשיש)- חציון הגיל בעת האבחנה הינו 30. יחד עם זאת, ישנם שני שיאים להופעת המחלה: בין 15 ל- 30 שנים וכן בעשור השביעי לחיים.
אטיולוגיה
האטיולוגיה של המחלה אינה ידועה, אך על פי התיאוריה המקובלת מדובר בפעילות דלקתית שמקורה בשפעול כרוני של מערכת החיסון כנגד מרכיבים (שטרם זוהו) בדופן או בחלל המעי. הרקע הגנטי (Genetic), כמו גם גורמים סביבתיים שונים - בעלי השפעה משמעותית על רמת הסיכון לפתח את המחלה אצל פרט מסוים, וכמו כן על תזמון הופעתה.
שפעול מערכת החיסון
דופן המעי התקין מכיל צפיפות גבוהה של תאים חד-גרעיניים בעלי פעילות דלקתית פיזיולוגית, היוצרת מצב של ריסון או סבילות כנגד האנטיגנים המרובים המצויים בחלל המעי – שמקורם מהתזונה או מהפלורה (Flora) הטבעית. במחלת קרוהן, ישנה עדות לשפעול ממושך של מערכת החיסון, מה שיוצר נזק דלקתי בדופן המעי. לא ברור אם הטריגר לשפעול מערכת החיסון הינו מיקרואורגניזם פתוגני (Pathogenic microorganism) שטרם זוהה, או אבדן של אותה סבילות חיסונית הקיימת במצב תקין במערכת העיכול.
מספר מחקרים הדגימו קשר נסיבתי בין נוכחות מיקרואורגניזמים מסויימים (Mycobacterium paratuberculosis, וירוס החצבת, ו-Paramyxovirus) למחלת קרוהן. יחד עם זאת, העדות לנוכחות מחוללים אלו בקרב החולים אינה חד-משמעית בהשוואה לאוכלוסייה הבריאה. במקרה של M. paratuberculosis, מתן טיפול אמפירי כנגד המחולל לא הניב תוצאות משמעותיות במיגור המחלה.
ממודלים של המחלה בבעלי חיים ניתן ללמוד כי נוכחות חיידקי המעיים חיונית לקיום הפעילות הדלקתית הכרונית. בחולי קרוהן ישנה עדות לתגובתיות יתר של הלימפוציטים מסוג T (T Lymphocytes) לפלורה של המעיים, כמו גם הופעה של נוגדנים המכוונים כנגד מרכיבים של הפלורה הטבעית - כדוגמת E.coli outer membrane protein(OmP-C), Flagellin ו- Saccharomyces cerevisea.
עדיין לא ברור עם הפעילות הדלקתית במחלה נובעת מפגיעה בתפקוד מערכת החיסון הראשונית הלא ספציפית (Innate), מהפעלה לא מבוקרת של מערכת החיסון ההסתגלותית (Adaptive), או מפגיעה משולבת בשתי המערכות. במודלים בבעלי חיים וכן בבני אדם נמצאו מספר מנגנונים המביאים בסופו של דבר לביטוי משותף של המחלה בדופן המעי:
- מוטציה בגן (Gene mutation)-NOD2/CARD15 - הודגמה בקרב 30-20 אחוזים מהחולים. החלבון המקודד מבוטא במונוציטים (Monocytes) ובתאי Paneth, ומהווה חיישן תוך תאי לזיהוי Peptidoglycan חיידקי. הפגיעה בתפקוד החלבון מובילה לפגיעה בתגובה האנטי-בקטריאלית (Anti-bacterial) ופגיעה בהפרשת Defensins, כלומר, יוצרת פגיעה במערכת החיסון הראשונית. ייתכן ופגיעה זו מביאה באופן משני לשפעול בלתי מבוקר של מערכת החיסון ההסתגלותית
- פגיעה במנגנון ה-Autophagy - מנגנון קדום זה משמש לפירוק חלבונים מזיקים בתא. מדובר ביצירת שלפוחיות המצופות בקרום מממברנת (Membrane) התא המעבירות את תוכנן ישירות לליזוזומים (Lysosomes). הפגיעה במנגנון קשורה במוטציות מסויימות:
- מוטציה בגן ATG16L1 - מגינה מפני המחלה
- שינוי בביטוי הגן IRGM (בעל חשיבות בעמידות בפני חיידקים תוך-תאיים כגון Listeria ו-Toxoplasma) – מגביר את הסיכון למחלה
- מוטציות בקולטן ל-Interleukin-23 (IL) - Interleukin-23 מופרש על ידי תאים דנדריטים (Dendritic) ומקרופאגים (Macrophages) בתגובה למיקרואורגניזמים שונים. בתגובה להפרשתו, לימפוציטים מסוג CD4+ מקבלים פנוטיפ (Phenotype) של תאים מסוג Th-17, המהווים תא אפקטורי (Effector cell) חשוב בתהליך הדלקתי. מוטציות שונות בקולטן ל-IL-23, מגינות מפני המחלה או מגבירות את הסיכון להתפתחותה
- פגיעה בלימפוציטים המבקרים את פעילות מערכת החיסון ההסתגלותית – Treg (Regulatory T cells)
- פגיעה בתפקוד תאי האפיתל (Epithelial cells) במעי במניעת החדירה של מיקוראורגניזמים (Barrier function)
גנטיקה
העדות למעורבות גנטית במחלה קיימת כבר מתצפיות מוקדמות של ריכוז חולים בתוך משפחות. הסיכון של קרוב משפחה מדרגה ראשונה של חולה קרוהן לפתח את המחלה גבוה פי 15-14 לעומת הסיכון בקרב האוכלוסייה הכללית.
במחקרי תאומים, ההתאמה בין תאומים מונוזיגוטיים (Monozygotic twins) של הופעת המחלה מגיעה ל-67 אחוזים, בעוד ההתאמה של דלקת כיבית של המעי הגס מגיעה ל-20 אחוזים בלבד. הסיכון להופעת המחלה גבוה פי 4-2 בקרב יהודים אשכנזים לעומת אוכלוסייה שאינה יהודית המתגוררת באותו אזור גיאוגרפי.
עם תחילת השימוש בשיטות מיפוי מודרניות של הגנום (Genome) האנושי, מחלת קרוהן היתה הראשונה בה הצליחו לבצע מחקרים מבוססי Genome-wide association. מחקרים אלו אפשרו לבדוק מאות אלפי סמנים גנטיים בעת ובעונה אחת, תוך השוואה בין החולים לבין האוכלוסייה שאינה סובלת מהמחלה. כל זאת, ללא צורך בהשערה מוקדמת לגבי מיקום הגנים החשודים. עד היום נמצאו יותר מ-30 סמנים גנטיים הקשורים למחלה. חלק מהגנים מגבירים את הסיכון גם לדלקת כיבית של המעי הגס, וחלקים ספציפיים למחלת קרוהן.
הדוגמה הראשונה לגן מסוג זה זוהתה בשנת 2001, וידועה כגן 15NOD2/CARD. בגן זה נמצאו 3 מוטציות עיקריות באוכלוסייה האירופאית ובאוכלוסיית צפון אמריקה. קיום של אחת המוטציות בשני האללים (Alleles) מגביר את הסיכון להופעת המחלה פי 17.5 לעומת האוכלוסייה הכללית, ואילו הטרוזיגוט (Heterozygous) נמצא בסיכון מוגבר פי 2.5. כמו כן, נמצא קשר בין קיום המוטציות להופעה של המחלה בגיל מוקדם יותר, וליצירת חסימות במעי הדק.
יחד עם זאת, רק 30-20 אחוזים מחולי קרוהן נושאים את המוטציה, ויש מספר גדול של אנשים בריאים הנושאים את המוטציה ללא ביטוי של המחלה (חדירות המוטציה המחושבת קטנה מ-1 אחוז). מכאן ניתן להסיק כי ישנה חשיבות רבה לגורמים הסביבתיים המשפיעים על הופעת המחלה.
גורמים סביבתיים
העלייה בשכיחות המחלה בעשורים האחרונים, והקשר בין ההיארעות לרמה הסוציואקונומית מרמזים על חשיבותם של הגורמים הסביבתיים. ייתכן וההסבר טמון בתיאוריית ההיגיינה, המקשרת בין חשיפה מועטה למיקרואורגניזמים לא-פתוגניים בילדות (כגון תולעים וחיידקים ממקור מעיים של בעלי חיים) לסיכון מוגבר להופעת המחלה. על פי תיאוריה זו, חשיפה מוקדמת למחוללים אלו חשובה להתפתחות מערכת הבקרה של מערכת החיסון (ובעיקרה להבשלה של תאי T רגולטורים, Treg). במחקר שנערך בישראל בקרב מתגייסים נמצא כי גדילה בסביבה כפרית מורידה את הסיכון להופעת המחלה פי 2.2 לעומת גדילה בסביבה עירונית. כמו כן, אותו מחקר הדגים כי מספר גדול של אחים במשפחה (המעלה את צפיפות המגורים) מהווה גורם מגן מפני הופעת המחלה.
מרבית המחקרים הדגימו כי הנקה מהווה גורם מגן מפני הופעת המחלה. הגורמים המגבירים את הסיכון למחלה על פי המחקרים כוללים שימוש בתרופות ממשפחת ה-NSAIDs, שימוש בגלולות למניעת הריון, ועישון. לא נמצא קשר חד משמעי לתזונה (צריכה מוגברת של סוכרים פשוטים ומיעוט בצריכת פירות וירקות). מספר מחקרים הדגימו קשר בין זמן הופעת המחלה לזיהומי מעיים שהתרחשו לאחרונה ונגרמו על ידי מיקרואורגניזמים פתוגניים. ייתכן והקשר בין כל גורמי הסיכון שהוזכרו הינו השפעתם על הפלורה של המעיים, ותגובתיות מערכת החיסון כנגדה.
למרות טענותיהם של החולים בדבר הקשר בין ההופעה הראשונית של המחלה למצבי לחץ נפשי, קשר שכזה לא הוכח בצורה מחקרית. יחד עם זאת, ייתכן וקיים קשר בין לחץ נפשי לבין הופעת התקפים חוזרים של המחלה.
קליניקה
מיקום המחלה
שליש עד מחצית מהחולים סובלים ממעורבות דלקתית הן של ה-Ileum והן של המעי הגס (המחלה נוטה להופיע ב-Ileum המרוחק והמעי הגס המקורב). כשליש מהחולים סובלים ממעורבות המעי הדק בלבד (בדרך כלל ב-Ileum), והיתר ממעורבות של המעי הגס בלבד.
מעורבות משמעותית של המעי הדק המקורב, כמו גם של הקיבה והתריסריון, פחות שכיחה - ובדרך כלל מלווה מעורבות של המעי הדק המרוחק. על פי רוב, הפעילות הדלקתית לאורך המעי אינה רציפה, ועם הזמן עשויים להופיע אזורים חדשים המעורבים במחלה.
תסמינים במערכת העיכול
קיימת שונות גדולה של התמונה הקלינית בין החולים - התלויה במיקום המחלה לאורך המעי, חומרת הדלקת, הופעת סיבוכים במערכת העיכול ומעורבות של איברים נוספים.
התסמין המרכזי במחלה הוא כאב בטן. הכאב יכול לנבוע מהדלקת, מנוכחות של מורסה תוך-בטנית, או משנית לחסימה. מאפייני הכאב יהיו בהתאם למנגנון– התקפי ועוויתי, או ממושך וחמור. לעתים התסמינים מופיעים בעצמה נמוכה, בצורה התקפית, ולאורך זמן ממושך. במקרים אלו ייתכן עיכוב (של חודשים) בקביעת האבחנה.
תסמינים אופייניים נוספים כוללים שלשול ותלונות מערכתיות - הכוללות חום, חולשה וירידה במשקל. דמם רקטלי (Rectal bleeding) ו-Tenesmus הינם נדירים (בהשוואה לדלקת כיבית של המעי הגס), לאור העובדה שברוב המקרים הרקטום (Rectum) אינו מעורב בדלקת.
הופעה קלינית שכיחה נוספת (המופיעה בקרב 35-15 אחוזים מהחולים) היא מחלה פריאנלית (אשר עשויה להקדים את ההסתמנות במעי ברבע מהמקרים). ביטויי המחלה הפריאנלית כוללים כיבים, קפלי עור גדולים ורגישים, פיסורה אנלית (Fissura ani), והופעה של נצורים העלולות להיחסם ולגרום להיווצרות מורסה מקומית.
| תסמין/סימן | מנגנון |
|---|---|
| שלשול |
|
| כאבי בטן |
|
| ירידה במשקל ותת-תזונה |
|
| חום |
|
| אנמיה |
|
תסמינים מחוץ למערכת העיכול
תסמינים מחוץ למערכת העיכול מופיעים בקרב 25-6 אחוזים מהחולים. שכיחותם גבוהה יותר בקרב החולים הסובלים ממעורבות של המעי הגס.
מעורבות מערכת השרירים והשלד
- התאלות (Clubbing) של אצבעות הידיים
- מעורבות מפרקים פריפריים (20-16 אחוזים מהחולים) – ישנו קשר בין הופעה של כאבים או נוקשות במפרקים להתקף של המחלה במעי. המעורבות בדרך כלל אסימטרית ונודדת. נדיר שגורמת לדפורמציה של המפרק.
- מעורבות המפרקים הגדולים (10-3 אחוזים מהחולים) - ישנו קשר בין ספונדיליטיס ל-HLA-B27. כמו כן, ישנה שכיחות מוגברת של דלקת עצה וכסל (Sacroiliitis) דו-צדדית
- Osteoporosis (60-30 אחוזים מהחולים) - משנית לטיפול ממושך בסטרואידים (Steroids) או הפרעה בספיגת סידן וויטמין D.
- Wegener's granulomatosis - נדירה.
- Amyloidosis - נדיר.
מעורבות עורית
Pyoderma gangrenosum - מופיעה ללא קשר לפעילות המחלה במעי.
- Erythema nodosum - שכיחה יותר בנשים. יש קשר למעורבות המפרקים, ולפעילות המחלה במעי.
מעורבות עינית
מופיעה בקרב 6 אחוזים מהחולים.
- Scleritis ו-Episcleritis - יש קשר בין הופעתן לפעילות המחלה במעי
- Uveitis - מתבטאת בכאבי ראש, כאבי עיניים, דמעת, טשטוש ראייה ו-Photophobia. נובעת ממעורבות דלקתית של הלשכה הקדמית
מעורבות הכבד ודרכי המרה
עלייה בשכיחות אבנים בכיס המרה - למעלה מ-25 אחוזים מהחולים סובלים ממחלה זו.
- עלייה אסימפטומטית ברמות אנזימי הכבד
- דלקת ראשונית צלקתית של דרכי המרה (Primary sclerosing cholangitis) - נדירה יותר בקרב חולי קרוהן לעומת חולי דלקת כיבית של המעי הגס, אך עשויה להופיע בקרב 4 אחוזים מהחולים
מעורבות דרכי השתן והמין
עלייה בשכיחות אבנים בדרכי השתן - העלייה היא בשכיחות אבני Oxalate וחומצה אורית (Uric acid) בלבד. ה-Steatorrhea המופיעה במחלה גורמת לעלייה ברמת חומצות השומן החופשיות במעי. חומצות אלו קושרות סידן, ומוירות רמה גבוהה של Oxalate חופשי הנספג לדם. אבני חומצה אורית נוצרות בשל התייבשות חוזרת ומצב היפרמטבולי המאפיינים את הדלקת.
מעורבות מערכת הקרישה
נטייה לקרישיות יתר - עשויה לבוא לידי ביטוי בתסחיפים קרישתיים ורידיים בעיקר, ועורקיים במקרים נדירים. מנגנון ההיווצרות קשור בכך שהדלקת גורמת ל-Thrombocytosis ולעלייה ברמות Fibrinogen, Factor V, Factor VIII וחסר ב-Antithrombin III ו-Protein S.
צורות הביטוי של המחלה
על פי חלוקה גסה, ישנן שלוש צורות ביטוי קליניות של המחלה:
- ביטוי פיסטולרי-אגרסיבי (Fistular-aggressive): הופעת הופעת נצורים בין שתי לולאות מעי או בין לולאת מעי לאיברים סמוכים, מורסות תוך-בטניות ונצורים בפי הטבעת.
- ביטוי פיברוטי-חסימתי (Fibrotic-obstructive): הצטלקויות בדופן המעי הגורמות להיצרות החלל ולחסימות מעי.
- ביטוי דלקתי: מעורבות דלקתית מערכתית, המתבטאת בחום, אנמיה של מחלה כרונית, ועלייה בערכי CRP (C Reactive Protein) או שקיעת הדם.
יחד עם זאת, לעתים קרובות קיימת חפיפה בין הביטויים השונים אצל אותו חולה – לדוגמא: קיום בו בעת של היצרות המעי ונצור לפני איזור החסימה.
- הגורמים המשפיעים על צורת הביטוי
- גורמים גנטיים - מוטציה ב-NOD2 (Nucleotide-binding Oligomerization Domain-containing protein 2) מגבירה את הסבירות לביטוי חסימתי
- פרופיל סרולוגי (Serologic profile)- קיום נוגדנים כנגד מרכיב ה-mannan בשמר Saccharomyces cerevisiae (Anti-Saccharomyces Cerevisiae Antibodies, ASCA) מגביר את הסיכוי למעורבות המעי הדק. קיום נוגדן Anti-CBir1 (Anti-flagellin) מגביר את הסיכוי לביטוי פיסטולרי או חסימתי
אבחנה
לא ניתן לאבחן את המחלה על סמך מאפיין בודד. יש צורך בצירוף של נתונים קליניים, מעבדתיים, אנדוסקופיים, היסטולוגיים, והדמייתיים.
אנמנזה
יש להתעכב על משך התסמינים, נסיעות לחוץ לארץ לאחרונה, שימוש בתרופות ושינויים בתזונה. אנמנזה משפחתית עשויה להעלות את החשד לקיום המחלה. חשוב לברר קיום של תסמינים מחוץ למערכת העיכול, ירידה במשקל או חום.
בדיקה גופנית
חשוב להתרכז בסימנים בבדיקת הבטן העשויים להעיד על חסימת מעי, נוכחות מסה דלקתית או מורסה. בדיקה רקטלית יכולה להדגים קיום של מחלה פריאנלית אופיינית.
בדיקות מעבדה
בדרך כלל ישנה עלייה ברמות מדדי דלקת שונים, כולל CRP, שקיעת דם, Thrombocytosis ואנמיה. Leukocytosis עם סטייה שמאלה עשויה לרמז על סיבוך זיהומי. יש לכלול בדיקת צואה לתרבית ומשטח צואה למיקרוסקופ, וכמו כן לבדוק נוכחות של טוקסין Clostridium difficile במקרים מסויימים.
שימוש במדדים סרולוגיים שמור בעיקר להבדלה בין מחלת קרוהן לדלקת כיבית של המעי הגס. רגישותה של בדיקת ASCA למחלת קרוהן נעה בין 60-40 אחוזים, עם סגוליות גבוהה (תיתכן בדיקה חיובית גם בחולי Celiac, או בקרב קרובי משפחה של חולים ללא מחלה פעילה). ניתן להיעזר בבדיקת הסרולוגיה במידה והיא חיובית. היעדר נוגדן ל-ASCA אינו שולל קיום האבחנה.
בדיקות הדמיה
הדמיה של המעי הדק מבוצעת באמצעות בדיקת CT (Computed Tomography) או MR Enterography (Magnetic Resonance Enterography). הממצאים המוקדמים האופייניים כוללים כיבים ועיבוי של דופן המעי, או הרחבה של ה- Valvulae conniventes. בצקת ושינוי שומני בדופן יתבטאו בהרחבה של המרווח בין לולאות המעי. בשלבים מאוחרים ניתן לראות תמונת אבני מרצפת (Cobblestones), הופעה של סינוס או נצור מלולאות המעי, או היצרות של לולאות.
מיפוי עם לויקוציטים יכול להוות בדיקת עזר במקרים של מחלה דלקתית עם מיעוט סימנים ב-Enterography.
שימוש ב-Ultrasound (על-שמע) שמור לבירור סיבות אחרות לכאבי בטן (דרכי מרה או סיבות גינקולוגיות), אך ישנם מרכזים נבחרים שפיתחו שיטות רגישות לבדיקת שינויים בלולאות המעי באמצעות Ultrasound.
קולונוסקופיה מהווה בדיקה ישירה המאפשרת להתבונן בדופן המעי וגם לקחת ביופסיות. הממצאים האופייניים כוללים כיבים אפטיים (Aphthous ulcerations), בצקת ברירית, ותמונה דמוית "אבני מרצפת" המכילה איי רירית מעי תקינה בין אזורים דלקתיים ולעתים מחוסרי רירית. בשלבים מאוחרים ניתן לזהות היצרות של חלל המעי, או פתח של נצור לתוך דופן המעי. במרבית המקרים אין מעורבות של הרקטום, וקיימת מעורבות סגמנטרית של הדלקת לאורך המעי.
בכל מקרה של חשד למחלת קרוהן יש לשאוף לבצע אינטובציה (Intubation) של ה-Ileum. במקרים בהם יש חשד למעורבות מעי דק שלא נצפה בבדיקות הנזכרות, יש מקום לבצע בדיקה באמצעות וידאו-קפסולה (Video Capsule Endoscopy) – אך יש לקחת בחשבון את הרגישות הגבוהה והסגוליות הנמוכה יחסית של בדיקה זו בזיהוי ממצאים ברירית המעי הדק.
טיפול
לא ידוע על טיפול תרופתי או כירורגי המרפא את המחלה. השאיפה היא להביא למצב של הפוגה ממושכת, המאפשרת היעלמות של התסמינים ,שיפור איכות החיים ומניעת סיבוכים (כגון הצורך בניתוחים או אשפוזים). מחקרים מהשנים האחרונות הדגימו כי ריפוי מוקדם של רירית המעי במהלך המחלה יעיל למניעת התלקחויות וסיבוכים עתידיים. יחד עם זאת, לאור העובדה שמדובר בטיפול ממושך, בעת התאמת הטיפול המונע יש לקחת בחשבון את תופעות הלוואי והיכולת לשמור על יעילות הטיפול לטווח הארוך.
Aminosalicylates-5 (ASA-5)
Salazopyrin (Sulfasalazine) ותרופות מקבוצת ה-(ASA-5), הודגמו כבעלות יעילות מתונה בטיפול במחלת קרוהן קלה עד בינונית המערבת את המעי הגס. לעומת זאת, לא הודגמה יעילות מובהקת בטיפול במחלה המערבת את המעי הדק או כטיפול מונע. רוב תופעות הלוואי של Sulfasalazine קשורות במרכיב ה-Sulfapyridine של התרופה, ואינן קיימות בתכשירי ה-(ASA-5) הנוספים. יתרונה של Sulfasalazine הוא בהשפעתה המיטיבה על הפרקים המעורבים.
טיפול אנטיביוטי
טיפול אנטיביוטי נדרש כאשר מופיעים סיבוכים זיהומיים של המחלה. יש מעט עדויות מחקריות לגבי יעילותו בטיפול במחלה פריאנלית, נצורים או מחלה דלקתית במעי.
Metronidazole יעילה לטיפול בנצור פריאנלי, ובעלת יעילות מתונה במניעת חזרה של המחלה באזור ההשקה לאחר כריתה ניתוחית. יחד עם זאת, טיפול ממושך ב-Metronidazole גורם לתופעות לוואי, והפסקת הטיפול כרוכה בשכיחות גבוהה של חזרת הנצור.
Ciprofloxacin יעילה לריפוי נצור פריאנלי, והטיפול בה כרוך בפחות תופעות לוואי לעומת טיפול ב-Metronidazole. מספר עבודות הדגימו את יעילותה של Ciprofloxacin גם במקרים של התלקחות קלה עד בינונית של המחלה הדלקתית במעי - עם יעילות דומה לטיפול ב-ASA-5 או בסטרואידים למשך 12 שבועות.
טיפול בסטרואידים
למרות תופעות הלוואי, לסטרואידים יש עדיין תפקיד מרכזי בטיפול בהתלקחות חריפה של המחלה. במחלה בדרגה קלה עד בינונית שאינה מגיבה לטיפול ראשוני, או בהתלקחות קשה - נהוג לטפל ב-Prednisone במינון של 60-40 מ"ג ליום, עם ירידה הדרגתית במינון תוך 6-4 שבועות. שיעור התגובה הצפוי לטיפול נע בין 90-80 אחוזים, והתגובה לטיפול מהירה (תוך כשלושה שבועות). לחולים במצב קשה נהוג לתת טיפול בסטרואידים דרך הוריד, כדוגמת Hydrocortisone במינון של 100 מ"ג כל 8 שעות.
אין עדויות ליעילותם של סטרואידים במניעה, ואין עדות שהטיפול מביא לריפוי הרירית. כמו כן, קיימות תופעות לוואי רבות בשימוש ארוך טווח. עד 50 אחוזים מהחולים מפתחים תלות בטיפול בסטרואידים, עם חזרה של התסמינים תוך ירידה במינון. מתוך ניסיון למנוע את תופעות הלוואי המערכתיות, פותח השימוש ב-Budesonide. ההיקשרות (Affinity) של Budesonide לקולטן ה-Glucocorticoid גבוהה מזו של Prednisone, והיא עוברת מטבוליזם (Metabolism) מהיר במעבר ראשוני בכבד. כמו כן, פותחה תרכובת המביאה לשחרור של התרופה ב-Illium המרוחק והמעי הגס הימני. תרופה זו, במינון של 9 מ"ג ליום, יעילה יותר מ-ASA-5 מבחינת שיעור ההפוגה, אך פחות יעילה מ-Prednisone. ניתן להשתמש בתרופה באותו מינון גם למניעה, לטווח של שנה ללא תופעות לוואי משמעותיות.
Thiopurines
קבוצה זו כוללת את ה-Azathioprine ו-Puri-Nethol (Mercaptopurine-6). מטהאנליזה (Meta-analysis) הדגימה כי תרופות אלו יעילות בהשגת הפוגה ב-54 אחוזים מהמטופלים, ויעילות בהפסקת התלות בטיפול בסטרואידים. התרופות יעילות גם כטיפול מונע ולשמירה על הפוגה ממושכת (עד 67 אחוזים לאחר שנה). בניגוד לסטרואידים, טיפול ב-Thiopurines עשוי להביא לריפוי של הרירית. המינון המקובל של Azathioprine הוא 2.5 מ"ג/ק"ג/יום, ושל Mercaptopurine-6 הוא 1.5 מ"ג/ק"ג/יום.
המטבוליזם של התרופות ידוע היטב - אנזים (Enzyme) מרכזי בתהליך הוא ThioPurine MethylTransferase (TPMT). אחד מכל 300 אנשים באוכלוסייה הומוזיגוטי למוטציה (Homozygous Mutation) שגורמת לאינאקטיבציה (Inactivation) של האנזים. במקרה זה, נטילת התרופה תביא ליצירת כמות רעילה של המטבוליט Thioguanine-6 (TG-6), ולהתפתחות Leukopenia קשה. להטרוזיגוטים למוטציה (Heterozygous Mutation) (כ-11 אחוזים מהאוכלוסייה) תהיה רמה מוגברת של TG-6, ויידרש מינון נמוך יותר של התרופה לצורך השגת יעילות טיפולית. ניתן לנטר את רמת ה-TG-6 כמדד ליעילות הטיפול כאשר אין תגובה, על מנת להבדיל בין חוסר היענות לטיפול לבין רמת פעילות גבוהה של TPMT. בקבוצה האחרונה, רמות ה-TG-6 תהיינה נמוכות, תוך הצטברות של מטבוליט אחר- Methyl MercaptoPurine-6 (MMP-6). במקרה זה, ניתן יהיה לשפר את יעילות הטיפול על ידי מתן זהיר של Allopurinol והורדת מינון התרופה.
חסרונן של תרופות אלו הוא הזמן עד להשגת תגובה טיפולית, העומד על 12-8 שבועות טיפול לפחות. תופעות לוואי חמורות של הטיפול כוללות דלקת חריפה של הלבלב ב-7-3 אחוזים מהחולים, ותגובות אלרגיות ב-2 אחוזים. ניתן לראות עלייה מתונה ברמות אנזימי הכבד בקרב עד 9 אחוזים מהחולים. כמו כן, יש לנטר את ספירת הדם שבוע לאחר התחלת טיפול או כל שינוי במינון, וכן אחת ל-3 חודשים בכל משך מתן התרופה.
תרופות אלו, במיוחד בשילוב עם סטרואידים או טיפול ביולוגי, מגבירות את הסיכון לזיהומים [כולל זיהום ב-CMV (CytoMegaloVirus)]. כמו כן, טיפול ממושך ככל הנראה מגביר את הסיכון ל-Lymphoma, אך חשוב לזכור שלחולים עם מחלות מעי דלקתיות ישנו סיכון מוגבר ללימפומה ברקע - ללא קשר לטיפול התרופתי. הסיכון האבסולוטי לפתח לימפומה הינו נמוך, ולא צריך להוות שיקול להימנעות מטיפול תרופתי שימנע הופעה של סיבוכים ארוכי טווח.
Methotrexate
Methotrexate יעילה לטיפול במחלה פעילה, כמו גם לשימור הפוגה. המינון המקובל הוא 25 מ"ג אחת לשבוע בזריקה תוך-שרירית, או תת-עורית. גם מתן פומי עשוי להיות יעיל, אך ספיגת התרופה אינה עקבית - במיוחד בחולים עם מחלה פעילה במעי הדק.
Methotrexate מהווה אנטגוניסט של פולאט, אך תוספת חומצה פולית (Folic acid) לטיפול תמנע הופעה של סטומטיטיס ובחילות מבלי להשפיע על יעילות התרופה. הסיבוך הפוטנציאלי הקשה ביותר של הטיפול הוא פיברוזיס (Fibrosis) בכבד. בחולי Psoriasis, נהוג לבצע ביופסיית כבד לאחר מתן מינון מצטבר של 1.5 גרם של התרופה. למרות זאת, שיעור ההופעה של פיברוזיס כבדי בקרב חולים עם מחלת מעי דלקתית הוא נמוך יותר, מסיבה שאינה ידועה.
שילוב של Methotrexate עם תרופות המכילות סולפה או עם Thiopurines עלול לגרום להחמרה קשה של Leukopenia. כמו כן, תופעת לוואי נדירה אך מסכנת חיים היא Interstitial pneumonitis, שיכולה להופיע באופן הדרגתי עם תסמינים של שיעול וקוצר נשימה. מצב זה דורש הפסקה מיידית של הטיפול התרופתי, ומתן טיפול בסטרואידים.
Methotrexate היא תרופה טרטוגנית (Teratogenic), וכמו כן רעילה לזרע. גברים המטופלים בתרופה צריכים להפסיק את הטיפול לפחות 3 חודשים טרם ניסיונות כניסה להריון. Methotrexate נחשבת לחלופה טובה לטיפול ב-Thiopurines בקרב חולים שאינם מגיבים לטיפול או מפתחים תופעות לוואי קשות.
טיפול ביולוגי
- נוגדי TNF (Tumor Necrosis Factor)
התרופה הראשונה שפותחה מקבוצה זו של נוגדי TNF היא Remicade (Infliximab) - נוגדן כימרי מונוקלונלי (Chimeric monoclonal antibody). טיפול במינון תוך-ורידי של 5 מ"ג/ק"ג הביא לתגובה בקרב 81 אחוזים מהחולים תוך 4 שבועות. משך הזמן עד לתגובה היה שבועיים במרבית החולים. מקובל לתת קורס השראה של התרופה בשבועות 2,0, ו-6, ולאחר מכן טיפול אחזקתי מדי 8 שבועות. התרופה יעילה גם לריפוי נצורים לעור בכ-70 אחוזים מהמקרים.
בהמשך אושרה לשימוש תרופה נוספות ממשפחה זו - Humira (Adalimumab). Adalimumab היא נוגדן מונוקלונלי ממקור אנושי (Human monoclonal antibody) (IgG1, Immunoglobulin G subclass 1), וניתנת בזריקות תת-עוריות. טיפול ההשראה ניתן אחת לשבועיים במינון של 160 מ"ג, 80 מ"ג ו-40 מ"ג , וטיפול האחזקה ניתן במינון של 40 מ"ג אחת לשבועיים.
בארה"ב אושר בשנת 2013 הטיפול בתרופה נוספת מהמשפחה, Certolizumab pegol (Cimzia). תרופה זו מכילה Fab fragment של נוגדן אנושי כנגד TNF, המצופה ב-Polyethylene-glycogen. התרופה ניתנת במינון של 400 מ"ג תת-עורית בשבועות 2,0 ו-4 ולאחר מכן מדי 4 שבועות.
יעילות הטיפול לטווח קצר נעה סביב 60 אחוזים עבור כל אחת מהתרופות. כ-40 אחוזים מהחולים שומרים על הפוגה לאחר שנה. שילוב של תרופה ביולוגית עם Thipurines מעלה את שיעור ההפוגה לאחר שנה. מחקר SONIC הדגים שיעור הפוגה של 57 אחוזים בטיפול משולב, לעומת 44 אחוזים בטיפול ב-Infliximab בלבד ו-31 אחוזים בטיפול ב-Azathioprine בלבד).
תופעות הלוואי כוללות תגובה מקומית במקום ההזרקה, או תגובה לעירוי. כ-13 אחוזים מהחולים המטופלים ב-Infliximab או בתרופות אחרות מהמשפחה מפתחים נוגדנים עצמיים כנגד התרופה. פיתוח הנוגדנים עלול לגרום להופעת תגובות אלרגיות, ובמקביל להפחית את היעילות הטיפולית. מתן קבוע של התרופות (בניגוד למתן תקופתי), כמו גם שילוב עם תיופורינים או Methotrexate, מפחית את הסיכון ליצירת נוגדנים כנגד התרופה.
כאשר יעילות התרופה יורדת עקב יצירת נוגדנים, ניתן להגדיל את מינון התרופה או את תדירות המתן, או להחליף את הטיפול לנוגד-TNF אחר. בשימוש בתרופה אחרת מאותה משפחה, צפויה הפחתה של יעילות הטיפול לעומת חולה נאיבי לתרופה. נוגדנים מסוג ANA יופיעו בקרב עד 50 אחוזים מהמטופלים לאחר שנתיים, וב-30 אחוזים מהחולים יופיעו גם נוגדנים מסוג anti-dsDNA. לעומת זאת, התפתחות של זאבת (Lupus) משנית לטיפול התרופתי היא נדירה.
הטיפול בנוגדי-TNF, במיוחד כאשר ניתן בשילוב עם Thipurines וסטרואידים, מגביר את הסיכון לזיהומים. לעומת זאת, זיהומים מסכני חיים יופיעו ב-4-2 אחוזים מהמקרים בלבד. אין לטפל בנוגדי-TNF בחולים הסובלים מזיהום פעיל או מורסה פריאנלית (Perianal abscess) שלא נוקזה. הסיכון לזיהום גבוה יותר בקרב חולים שטופלו בסטרואידים, לעומת חולים שטופלו ב-Thipurines או ב-Methotrexate - ויש לנקוט בזהירות תוך ניטור קפדני של החולים בעת מתן טיפול משולב שכזה.
לפני תחילת הטיפול, יש לבצע בדיקה לגילוי מוקדם של שחפת לטנטית בכל החולים באמצעות בדיקת מנטו (Tuberculin test, Mantoux) וצילום חזה. חולים עם עדות לזיהום לטנטי (Latent) חייבים לקבל טיפול כנגד שחפת למשך 6 חודשים טרם תחילת הטיפול בתרופה. כמו כן, נוגדי-TNF עלולים לגרום לשפעול מחדש של דלקת כבד נגיפית מסוג B, ועל כן יש לשקול טיפול מונע בנשאים או לבצע ניטור הדוק [כולל החולים עם נוגדן anti-HBc IgG (anti-hepatitis B core immunoglobulin) חיובי בלבד].
טיפול בנוגדי-TNF בשילוב עם תיופורינים מגביר את הסיכון ללימפומה פי שישה, אך הסיכון האבסולוטי להתפתחות המחלה קטן. ישנם דיווחים על מספר מקרים של לימפומה מסוג הפטוספלני שאינה מגיבה לטיפול בקרב חולים צעירים (רובם גברים) שקיבלו טיפול משולב שכזה.
מחקרים מראים כי Infliximab יכולה לחדור את השליה בטרימסטר השלישי להריון, ויש לשקול הפסקה של התרופה בחולות יציבות בטרימסטר השלישי. יחד עם זאת, יש עדויות מצטברות לפיהן אין עלייה בשיעור המומים המולדים בעת מתן הטיפול בכל שלבי ההריון.
מחקר שבוצע על ידי D'Hans וחבריו הדגים כי טיפול משולב בנוגדי-TNF ו-Thipurines בשלב מוקדם של המחלה מגביר את שיעור ההפוגה לאחר שנה, לעומת טיפול מדורג בסטרואידים, Thipurines ונוגדי-TNF (62 אחוזים לעומת 42 אחוזים). כמו כן, שיעור ריפוי הרירית לאחר שנתיים היה גבוה יותר בקרב החולים שקיבלו את הטיפול המשולב, והם לא סבלו מתלות בטיפול בסטרואידים. לאור זאת, בחולים עם מחלה אגרסיבית הנוטה לגרום לסיבוכים מקובל לשקול מתן טיפול אימונומודולטורי (Immunomodulator) מוקדם, עם או בלי תוספת נוגדי-TNF.
עדיין לא ברור מהם המדדים המנבאים מהלך מחלה מסובך. על פי מחקרים שבוצעו לאחרונה - גיל צעיר בעת הופעת המחלה (פחות מ-40), מחלה חסימתית, צורך בטיפול מוקדם בסטרואידים ומחלה פריאנלית מנבאים מהלך מחלה מסובך. בחולים אלו יש לשקול טיפול מוקדם בתיופורינים, עם או בלי תוספת של נוגדי-TNF. כמו כן, חולים עם מחלה פיסטולרית מורכבת ייהנו מטיפול מוקדם בנוגדי-TNF.
מצד שני, כשליש מהחולים עם מחלת קרוהן צפויים להיכנס להפוגה ממושכת ללא סיבוכים, גם ללא טיפול בנוגדי- TNF או ב-Thipurines. כמו כן, אחוז לא מבוטל של חולים יפתחו עמידות לטיפול בנוגדי-TNF עם הזמן, עקב יצירת נוגדנים עצמיים. על כן, עדיין לא מקובל לטפל בנוגדי-TNF בכל חולה קרוהן המצוי בשלבים המוקדמים של המחלה.
- Anti-integrin antibodies
- Natalizumab
Tysabri (Natalizumab) היא נוגדן אנושי מונוקלונלי (חד שבטי) כנגד Integrin 4, המעכב את קשירת הלויקוציטים לאנדותל בכלי הדם ואת נדידתם לרקמה הדלקתית. התרופה ניתנת דרך הוריד במינון של 300 מ"ג מדי 4 שבועות. התרופה יעילה לטיפול במחלה חריפה. בקרב המגיבים, לאחר שנה של טיפול 61 אחוזים נשארו בהפוגה.
במסגרת המחקר הקליני ENACT, תופעת הלוואי המסוכנת של תרופה זו - מחלה נוירולוגית ניוונית מתקדמת Progressive Multifocal Leukoencephalopathy, (PML) – הופיעה בחולה אחד בלבד. המחלה נגרמת כתוצאה משפעול של נגיף ה-JC (John Cunningham virus) במוח. לאור זאת, התרופה נמצאת בשימוש רק באותם חולים שלא מגיבים לטיפול בנוגדי-TNF. מאז המחקר בוצע מעקב אחר כל החולים שקיבלו את התרופה, ולא היו דיווחים נוספים של המחלה בקרב חולים עם קרוהן.
- Vedolizumab
Entyvio (Vedolizumab) היא נוגדן אנושי מונוקלונלי כנגד Integrin 4. התרופה יעילה לטיפול במחלה פעילה בחומרה בינונית וקשה; לטיפול בחולים עם תגובה חלקית, חוסר תגובה או אי סבילות לטיפול קונבנציונאלי (Conventional) או עם נוגדי TNF. התרופה אושרה לשימוש בארץ באפריל 2015.
במחקר הקליני GEMINI הושגה הפוגה ב-53 אחוזים ו-39 אחוזים מהחולים שטופלו במשך 8 שבועות ו-4 שבועות בהתאמה. היארעות הפוגה גבוהה יותר (57 אחוזים ו-43 אחוזים בהתאמה) נרשמה בחולים שהיו נאיבים (Naïve) לטיפול עם נוגדי TNF לעומת חולים על כשלון קודם לטיפול בנוגדי TNF(48 אחוזים ו-29 אחוזים בהתאמה)[1].
- Anti-IL-12/23 antibodies
- Ustekinumab
Stelara (Ustekinumab), נוגדן אנושי מונוקלונלי IgG1k אשר מדכא את הפעילות הביולוגית של IL-12 (Interleukin-12) ו- IL-23 (Interleukin-23) על ידי דיכוי הקולטנים לציטוקינים אלו על תאי ה-T, תאי Natural killer ותאים מציגי אנטיגנים (Antigen presenting cells).
במחקר קליני של Sandborn וחבריו נמצא כי טיפול אחזקתי ב-Ustekinumab לעומת טיפול בפלצבו השיג שיעורים גבוהים יותר של הפוגה קלינית (41.7 אחוזים לעומת 27.4 אחוזים) ותגובה (Response) (69.4 אחוזים לעומת 42.5 אחוזים) בשבוע 22. זיהומים חמורים נצפו בשבעה חולים (6 תחת Ustekinumab) במהלך ה-Induction ו-11 חולים (4 תחת Ustekinumab) במהלך הטיפול האחזקתי. Basal-cell carcinoma התפתחה בחולה אחד שטופל ב-Ustekinumab [2].
חולים עם מחלה בינונית-קשה עם תנגודת לטיפול בנוגדי TNF הדגימו תגובה מוגברת לטיפול ב-Ustekinumab בשלב ה-Induction לעומת פלצבו. חולים עם תגובה ראשונית ל-Ustekinumab הדגימו תגובה מוגברת משמעותית והפוגה תחת טיפול ב-Ustekinumab כטיפול אחזקתי [2].
התרופה אושרה לשימוש על ידי ה- FDA (Food and Drug Administration) בארה"ב בספטמבר 2016 לשימוש במבוגרים החולים במחלה בחומרה בינונית עד קשה ואשר הטיפול הקונבנציונאלי בה כשל (סטרואידים, תרופות מדכאות מערכת חיסון או נוגדי TNF) [2].
טיפול ניתוחי
הטיפול הניתוחי הוא טיפול בלתי נפרד במחלה. בעבר, עד 75 אחוזים מהחולים נזקקו לניתוח לאחר 20 שנות מחלה. בשל חזרה של הדלקת לאזור ההשקה הניתוחית, הטכניקות הניתוחיות המודרניות מסתמכות על שימור המעי. לעתים קרובות בוחרים לבצע Stricturoplasty במקום כריתה של המעי.
ההתוויות לניתוח כוללות את הסיבוכים השונים של המחלה: מורסה תוך-בטנית, נצור שאינו מגיב לטיפול תרופתי, או היצרות פיברוטית הגורמת לתלונות חסימתיות. לעתים אין ברירה אלא לנתח חולים עם מחלה דלקתית שאינה מגיבה לטיפול תרופתי. בילדים לעתים נדרש ניתוח על מנת למנוע פיגור בגדילה.
פרוגנוזה
דגלים אדומים
ביבליוגרפיה
- ↑ Vedolizumab as induction and maintenance therapy for ulcerative colitis. Feagan BG, Rutgeerts P, Sands BE, Hanauer S, Colombel JF, Sandborn WJ, Van Assche G, Axler J, Kim HJ, Danese S, Fox I, Milch C, Sankoh S, Wyant T, Xu J, Parikh A. N Engl J Med. 2013 Aug 22;369(8):699-710.
- ↑ 2.0 2.1 2.2 Ustekinumab induction and maintenance therapy in refractory Crohn's disease. Sandborn WJ, Gasink C, Gao LL, Blank MA, Johanns J, Guzzo C, Sands BE, Hanauer SB, Targan S, Rutgeerts P, Ghosh S, de Villiers WJ, Panaccione R, Greenberg G, Schreiber S, Lichtiger S, Feagan BG. (CERTIFI Study Group). N Engl J Med. 2012 Oct 18;367(16):1519-28. doi: 10.1056/NEJMoa1203572.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר ערן ישראלי, מנהל המרכז למחלות מעי דלקתיות, המכון לגסטרואנטרולוגיה ומחלות כבד, המרכז האוניברסיטאי הדסה, ירושלים


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק