מיגור האיידס בישראל עד 2030 - נייר עמדה - AIDS eradication in israel until 2030
הופניתם מהדף מיגור האיידס בישראל לדף הנוכחי.
|
| |
|---|---|
| מיגור האיידס בישראל עד 2030 | |

| |
הסרט האדום הפך לסמל המאבק העולמי במחלת האיידס
| |
| האיגוד המפרסם |
|
| קישור | באתר הר"י |
| תאריך פרסום | מרץ 2023 |
| יוצר הערך | ראו הוכן על ידי |
| ניירות עמדה מתפרסמים ככלי עזר לרופא/ה ואינם באים במקום שיקול דעתו/ה בכל מצב נתון. כל הכתוב בלשון זכר מתייחס לשני המגדרים. | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – HIV - נגיף הכשל החיסוני האנושי
מיגור איידס בישראל עד שנת 2030 - ראשי פרקים
מטרת מסמך זה להציע קווים כללים לתוכנית מיגור איידס (AIDS, Acquired ImmunoDeficiency Syndrome) בישראל 2030, ברוח הסטנדרטים הבינלאומיים ובהתאם לתשתית מערכת הבריאות הישראלית.
המסמך מבוסס על מדיניות ה-"95-95-95", על פיה 95 אחוזים מהנשאים יאובחנו, 95 אחוזים מהמאובחנים יקבלו טיפול מתאים לאורך זמן ו-95 אחוזים מהנשאים המטופלים יגיעו לרמת עומס נגיפי בלתי בלתי מדיד בדם (Undetectable)[1]. מטרת מסמך זה להתוות אסטרטגיה כללית למעבר מהכלת הנגיף למיגורו.
ראשית יוצג רקע כללי, ולאחריו הרחבה על מטרות התכנית, הפערים הקיימים בישראל, וכן על טיפול באוכלוסיות מיוחדות. לבסוף, יוצגו מסקנותינו.
השותפים לתוכנית יכללו את איגוד רופאי בריאות הציבור, החברה הישראלית לכשל חיסוני נרכש, החברה הישראלית לרפואה להט"בית (לסביות, הומואים, טרנסג'נדרים וביסקסואלים), הוועד למלחמה באיידס.
הגופים הבאים השתתפו בניסוח התוכנית וחיבור המסמך:
- איגוד רופאי בריאות הציבור
- החברה הישראלית לכשל חיסוני נרכש - איידס
איידס בישראל 2022
רקע
בהינתן היענות סדירה לטיפול באופן קבוע לאורך חיי המטופל, זיהום ב-HIV הפך למחלה כרונית והאנשים החיים עם הנגיף זוכים לתוחלת חיים כמעט זהה לאוכלוסייה הכללית. הטיפול הקיים לנשאי HIV (Human Immunodeficiency Virus) יעיל ביותר, מיוחסות לו תופעות לוואי מעטות, והוא מביא למצב שבו העומס הנגיפי בדם אינו מדיד (מצב המוגדר Undetectable); במצב זה, הנשא המטופל באופן רציף וקפדני אינו יכול להעביר את הנגיף ביחסי מין לא מוגנים[2][3][4][5][6][7][8][9]. בנוסף, מוצעים טיפולים מונעים יעילים ביותר במקרה של חשיפה לנגיף או לפניה:
PrEP) Pre-Exposure Prophylaxis) - שימוש בתכשיר המכיל שילוב תרופות שהוכח כיעיל בהפחתת הסיכון להידבקות ב-HIV בשיעורים של מעל ל-90 אחוזים. תכשירים חדשים, כגון Cabotegravir[9], אף הוכחו כיעילים יותר מהטיפול הפומי הקיים. התכשירים מיועדים למניעת הדבקה באנשים החשופים פוטנציאלית לנגיף (גברים המקיימים יחסי מין עם גברים ללא שימוש בקונדום, בני/ות זוג של נשאים המסרבים טיפול, אנשים העוסקים בזנות, משתמשים בסמים בהזרקה)[10][11][12][13][14][15].
PEP) Post-Exposure Prophylaxis) - שימוש בתכשירים אנטי-רטרו ויראליים (AntiRetroviral Therapy ,ART) למניעת הדבקה לאחר חשיפה, אם ניתנים תוך 72 שעות לאחר החשיפה[15][16][17][18]. בנוסף, קיימות אסטרטגיות מניעה בהתאם לדרכי ההעברה - שימוש בקונדומים (למניעה העברה ביחסי מין)[19][20], שימוש במחטים חד פעמיות וסקירת מוצרי דם (למניעת העברה עקב חשיפה לדם נגוע). מלבד מניעה ראשונית, נעשים מאמצים לזהות את הנגיף בשלב מוקדם, בדרך כלל על ידי עידוד בדיקות בקרב אוכלוסיות בסיכון ובסקירת נשים הרות בכדי למנוע העברה אנכית[4][5][6][7][8][21][22][23].
מבחינה רפואית, ניכר שיפור והתקדמות של הטיפול הרפואי המוצע לאנשים החיים עם הנגיף, כתוצאה מכך, תוחלת החיים של נשאים מטופלים מתקרבת לממוצע באוכלוסייה הכללית. בנוסף לעלייה באורך החיים, הטיפולים התרופתיים המוצעים והעתידיים מאפשרים לנשאים החיים עם הנגיף איכות חיים טובה לאורך זמן והגנה על הבאים איתם במגע מיני לא מוגן. עם זאת, למרות הטיפול הרפואי המתקדם והכיסוי הביטוחי הקיים בישראל, נראה כי הירידה בשיעורי הנשאות מתונה ולא עולה בקנה אחד עם האפשרויות הטיפוליות והחינוכיות הקיימות בישראל ובעולם[24]. מגמה זו נובעת מהיעדר תוכנית לאומית סדורה למיגור והעלאת מודעות ל-HIV[25]. יש לשפר את ההנגשה ל-PrEP וכן, את ההכשרה לרופאים הרושמים את הטיפול. יש לשפר את תהליך מתן הטיפול המונע לאחר חשיפה (PEP), שניתן רק במרכזי האיידס בבתי החולים. חלק מהאוכלוסייה שנמצאת בסיכון להדבקה ב-HIV לא נבדק או ממעט להיבדק. גורמי רפואה מדווחים על מקרים של אבחון מאוחר, במקרים לא מעטים, כאשר מתפתחת מחלה וזאת עקב חוסר מודעות ציבורית, מיעוט הפניות לבדיקה על ידי רופאים[25][26]. בלי בקשה ישירה מהמטופל, רופאים רבים לא יכללו את הבדיקה בבירור עבור מטופל שלא נמצא בקבוצת סיכון. לבסוף, מהגרים חסרי מעמד מוגבלים בנגישות מוגבלת לטיפול. מעבר לחשש להחמרת המצב הבריאותי של החולים הלא מטופלים, הם עלולים להביא להדבקה חדשה בקרב אחרים. המידע על נשאות, אבחון וטיפול ב-HIV בישראל מוגבל רק לפרטי מידע מסוימים, הרחבת הנגישות למידע דמוגרפי על הנשאים יכולה לאפשר עבודה ממוקדת ויעילה יותר למיגור. על כן, ניתן להצביע על פערים בתחום התכנון הלאומי וכן המודעות והחינוך בציבור הכללי, בקבוצת הסיכון ובציבור הרפואי[25][27][28].
מטרות התוכנית
זיהוי 95 אחוזים מהנשאים
זיהוי מוקדם מאפשר לנשא לפנות לטיפול ואגב כך להקטין את העומס הנגיפי. כמו כן, הנשא המאובחן מודע לאפשרות שהוא עלול להעביר את הזיהום למגעים מיניים או לשותפים להזרקת סמים ומונחה לנקוט באמצעי זהירות מתאימים. לשם כך, יש צורך בשיפור הסיקור, והפנייה לטיפול מוקדם ככל האפשר.
קיימות שתי שיטות אבחון עיקריות: אבחנה בבדיקת דם משולבת של נוגדנים ואנטיגן מדור רביעי ואבחנה באמצעות בדיקות מהירות.
בארצות הברית ההמלצה העדכנית היא לבדיקת HIV לפחות פעם אחת בחיים לכלל האוכלוסייה ללא תלות בגורמי סיכון, בין גיל 15–65, לנשים בהיריון בכל היריון, ובאנשים עם גורמי סיכון - אחת לשנה או אפילו יותר מזה[2][3][21][22][23][29][30]. ברוב מדינות אירופה סיקור נשים בהיריון הוא אוניברסלי ובנוסף, נעשה סיקור על פי קבוצות סיכון והנגשת הבדיקות לקהילה ולכלל האוכלוסייה. בשנת 2015 יצא נייר עמדה משותף של האיגוד הישראלי למחלות זיהומיות, איגוד רופאי המשפחה, איגוד הניאונטולוגים, החברה לרפואת אם ועובר והאיגוד לרפואת נשים ומיילדות הממליץ על בדיקת HIV לכל אישה בתכנון או בתחילת כל היריון[31]. משרד הבריאות הוציא נוהל שממליץ להציע בדיקת HIV לכל אישה בהיריון[32].
בדיקות לגילוי הנגיף בישראל נעשות רק על ידי גורמים מאושרים לכך, ואין שימוש בערכות לגילוי עצמי. יתירה על כך, היעדר הנחיה סדורה ומודעות בקרב הציבור הרפואי מביאה למיעוט הפניות לבדיקות אבחון, כיוון שרופאים רבים נמנעים מהפנייה של מטופלים שלא שייכים לקבוצות הסיכון הקלאסיות. תת-אבחון עלול להוביל לאבחנה מאוחרת, כאשר כבר מופיעים סימנים קליניים.
מטרתנו היא להגביר מצד אחד, ולמקד מצד שני, את מאמצי האבחון בישראל. מכיוון שאבחנות רבות מבוצעות במסגרות של קופת חולים בעוד הטיפול בנשאים מתבצע בבתי החולים נוצר פער בין האבחון לבין ההנגשה לטיפול. יש ליצור מנגנון המפשט את הקישור בין האבחנה למרפאת ה-HIV המטפלת. בנוסף, יש להגביר את מאמצי היישוג ולעודד נגישות בדיקות במסגרות שונות הנותנות מענה הולם לאוכלוסיות שונות[33].
טיפול ב-95 אחוזים מהנשאים
בעבר קווי הטיפול היו שמרניים והתייחסו גם לספירות תאי CD4 בהחלטה על התחלת טיפול.
נכון למועד כתיבת נייר זה, מקובל לטפל ולעקוב בכל שלבי המחלה, מוקדם ככל האפשר וקרוב ככל שניתן לרגע האבחנה[5][6].
Treatment as prevention - הטיפול האנטי- רטרו ויראלי (תכשיר נוגד נגיפי) הוכח ביעילותו למניעת הדבקה, וידוע כי נשא שהעומס הנגיפי בדמו הוא בלתי מדיד במשך חצי שנה, לא ידביק את השותפים ליחסי המין הבלתי מוגנים[4][5][6][7][8]. על מנת להבטיח שכל הנשאים יהיו מטופלים ותחת מעקב רפואי, יש לשפר את המנגנון ליצירת הקשר המוקדם עם כל מי שמאובחן כנשא או כחולה, על מנת למסור הודעה לגבי הנשאות, לאתר מגעים לא מוגנים ולהתחיל טיפול מוקדם, ככל האפשר, על מנת למנוע הדבקות נוספות. המעקב אחרי המטופלים מתבצע במרכזי האיידס על ידי צוותים מולטידיסיפלינאריים הכוללים רופאים/אות, אחים/אחיות, מגשרות תרבותיות לעדה האתיופית, עובדים/ות סוציאליות ופסיכיאטר/ית (האחרונים רק במיעוט מן המרכזים). על מנת לשפר את ההיענות לטיפול יש ליצור מנגנון פסיכו סוציאלי מותאם תרבותית לאוכלוסיות שונות (יוצאי מזרח אירופה, מגזר ערבי) בדומה למה שקיים לאוכלוסיית יוצאי אתיופיה. בהתאם, יש צורך במעקב מגעים יעיל וסדור, בתוכנית מוגדרת.
הגישה לטיפולים מונעי הדבקה לפני חשיפה מוגבלת עקב בעיות הנגשת ההכשרה לרופאים המעוניינים לרשום את הטיפול, בעיקר בערי הפריפריה. טיפול מונע הדבקה אחרי חשיפה ניתן לקבל בבתי חולים בלבד, מה שגורם לתהליך מסורבל. יש להכשיר מרכזים בקהילה שיהיו אחראים על מתן הטיפול המונע לאחר חשיפה.
הגעה לעומס ויראלי לא מדיד ב-95 אחוזים מהנשאים המטופלים
הגעה לעומס נגיפי לא מדיד דורשת היענות מיטבית לטיפול באופן עקבי ובר-קיימא לאורך כל חיי המטופל[5][6]. על כן, יש לשקול שני היבטים ברמה הפרטנית והרמה הארגונית:
- מעקב ושימור של אנשים בטיפול - על מנת למנוע נשירה של מטופלים ממעקב והפסקות טיפול שמשמעותם היא התפתחות של עמידות הנגיף לתרופות והדבקות, יש לוודא מעקב במרכזי האיידס פעם בחצי שנה. יש להקים מנגנון לאיתור נשאים וחולים המחמיצים ביקורים. לפיכך, יש לעבות את רכזי הטיפול הקיימים באנשי מקצוע שיכולים לענות באופן הוליסטי על המצוקות העולות מהטיפול לאורך חיי הנשא - מגשרים, פסיכולוגים ועובדים סוציאליים
- ניטור תוצאים ונקודות כשל - יש צורך בהקמת מנגנון אינהרנטי חסוי לשיתוף מידע ארצי לבדיקת תוצאות cascade of care על לאתר נקודות חולשה ולוודא עמידה ביעדים. איסוף נתונים ארצי נרחב והנגשתם יאפשר לאתר גם מגמות חדשות של הדבקות ב-HIV
עקב נושא חיסיון מידע רפואי נתוני מעקב וטיפול במרפאות HIV לא מקושרות לרפואת הקהילה. במקביל הנתונים הקליניים והמעבדתיים מקופת החולים לרוב אינם זמינים לרופאי מרפאות ה-HIV. כך רופא/ת הקהילה לא מקבל מידע על המעקב והטיפול הרפואי מה שמקשה על שימור מטופלים במסגרות טיפוליות.
מניעה של HIV מתבססת על הגברת המודעות לדרכי ההדבקה בנגיף ולדרכים להימנע מהדבקה, טכנולוגיות למניעת הדבקה, אבחנה מוקדמת וטיפול מוקדם ומעקב צמוד אחרי היענות לטיפול. בנוסף למטרות הנזכרות למעלה מניעת הדבקה מורכבת מחינוך ומטכנולוגיות, כאשר עיקר מאמצי המניעה מתמקדים באוכלוסיות הסיכון ופחות באוכלוסייה הרחבה. קיימות דרכים שונות למניעת הידבקות החל מחינוך ומיניות בטוחה, סיקור מוצרי דם, שימוש בקונדום, שימוש ב-PrEP וב-PEP, ומניעת העברה אנכית. עמדתנו תומכת בשילוב אמצעים שונים למניעת הדבקה כיוון שקצב ההדבקות בקרב גברים שמקיימים יחסי מין עם גברים לא ירדה באופן מספק, וכן עדיין יש הדבקות באוכלוסיות שאינן מוגדרות בסיכון גבוה. נראה כי לאמצעים חינוכיים המותאמים לכל האוכלוסיות תהיה השפעה חיובית במניעת הדבקה. ככל שמאמצי המניעה החינוכיים יהיו משמעותיים יותר, הצורך בהשקעת משאבים בטיפול צפוי לרדת. מאמצי המודעות והחינוך לא רק מוכיחים את עצמם מבחינת יעילות, מדובר באמצעי בעל יחס עלות-תועלת חיובי לאורך זמן במיגור HIV.
לרופא הקהילה יש תפקיד מרכזי בהצלחת הטיפול. המטופלים חשופים למחלות מגוונות כמו כל מטופל אחר. על מנת שתהיה נגישות והיענות גבוהה יש למצוא מנגנון שיאפשר לקיחות בדיקות בקהילה, כאשר הבדיקות הוירולוגיות יועברו למעבדות בתי החולים המתמקצעות בתחום. כך ימנעו ביקורים מיותרים בבתי החולים, כאשר המטופלים יגיעו למרכזי האיידס לבדיקה פעמיים בשנה עם תוצאות הבדיקות. הדבר יעלה את היענות המטופלים והשגת המטרות.
מנגנון ושיתופי פעולה בין מרכזי האיידס, רפואת הקהילה ולשכות הבריאות עשויים להביא להעלאת ההיענות לאבחון ולטיפול.
פערים, אתגרים ויעדים בישראל
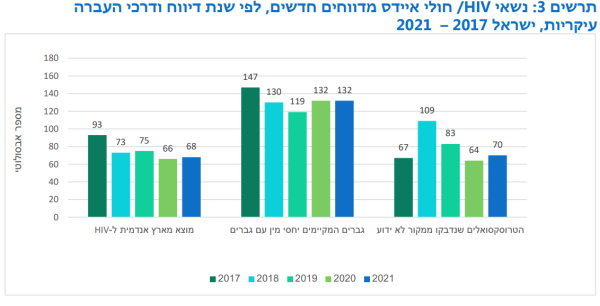
החל מ-1981 ועד סוף 2020 תועדו בישראל 10,791 מקרים חדשים של נשאי HIV וחולי איידס, מתוכם כ-16.4 אחוזים התקדמו למצב קליני ומעבדתי של מחלת האיידס. בין השנים האלו דווחו כ-1,683 מקרי תמותה. בישראל חיים (נכון למועד כתיבת נייר זה) 7,851 נשאים רשומים. בשנת 2020 דווח על 362 מקרים חדשים. השיעור המדווח בישראל נחשב נמוך ביחס למדינות העולם המערבי. עם זאת, קיימים פערים גדולים בין אוכלוסיות שונות בישראל. ויש חוסר בהעברת מידע אפידמיולוגי באשר לאוכלוסיות השונות[24][4][5].
בעבר נעשה ניסיון למקד את הסיקור בקבוצות סיכון, בעיקר לאור הסטיגמה שכרוכה במחלה וחוסר הענות לבדיקות. משרד הבריאות פרסם נוהל הממליץ לכל אישה בהיריון להיבדק ל-HIV[32]. הטמעת הנוהל בקרב רופאי הנשים והמשפחה וכן מידע לציבור הרחב יוכלו להביא לגילוי מוקדם וצמצום העברות אנכיות.
אוכלוסיות מיוחדות
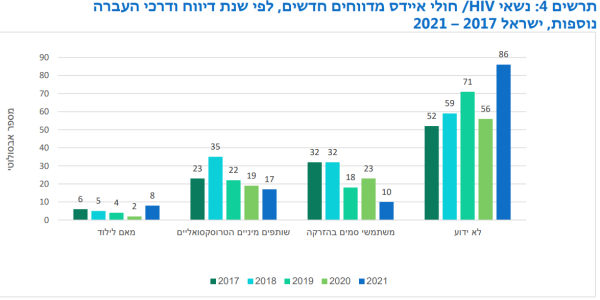
ישנן אוכלוסיות שנמצאות בסיכון מוגבר להדבקה. בין אוכלוסיות אלו: אנשים העוסקים בזנות, גברים המקיימים יחסי מין עם גברים, מהגרים מאזורים אנדמיים לנגיף ומשתמשים בסמים בהזרקה[25][34]. עבור אוכלוסיות אלו יש להבין את התנאים הייחודיים להן ולפעול בהתאם.
טיפול בחסרי מעמד
אזרחים ישראלים זכאים לקבלת טיפול מרגע אבחנתם, וניתנת להם גישה נוחה וזמינה יחסית לבדיקות וטיפול עדכני ללא תשלום. עם זאת, רק חלק מחסרי המעמד האזרחי בישראל, המהווים נתח משמעותי בהדבקות החדשות בישראל זה שנים רבות, זכאים לטיפול ולמעקב. למעשה מהגרים מארצות אנדמיות נמצאים בקבוצת סיכון, ובקבוצה זו יש תת-אוכלוסייה של מהגרים חסרי מעמד, אשר חווים קשיים בגישה לאבחון ולטיפול[25]. לכך שני חסמים עיקריים:
- חלקם מגיעים לישראל עם זיהום קיים ועל כן הוא נחשב "מצב רפואי קודם" ואינו מכוסה על ידי הביטוחים הפרטיים; בנוסף, גם אם ההדבקה התקיימה בישראל וכוסתה על ידי הביטוח, שינוי מעסיק וקטיעת הרצף הביטוחי תביא להחרגתה. כך, גם בעלי ביטוח פרטי בפועל לא זוכים לטיפול זמין ועקבי. כמו כן, הפסקת רצף עבודה מביאה להפסקת ביטוח רפואי על ידי המעסיק
- בישראל מוצעת "התוכנית הלאומית למניעת HIV וטיפול במהגרים נשאי HIV חסרי ביטוח רפואי". תוכנית זו מציעה טיפול תרופתי ומעקב. עם זאת, אחד מהקריטריונים להכללה הוא ספירת CD4 נמוכה מ-500 תאים למיקרוליטר. קריטריון זה אינה עולה בקנה אחד עם המלצות ארגון הבריאות העולמי או עם האינטרס הציבורי בישראל - שכן חולה לא מטופל מהווה פוטנציאל הדבקה. מכיוון שקריטריון להכללה בתוכנית הוא שהות של לפחות 6 חודשים בישראל, נשאים שהגיעו תחת טיפול תרופתי ממדינת המוצא שלהם, נאלצים להפסיק טיפול למשך לפחות לחצי שנה; דבר המסכן אותם בהתפתחות של עמידות, ועלול לגרום להדבקה של פרטנרים מיניים בתקופת ההפסקה. "התוכנית הלאומית למניעת HIV וטיפול במהגרים נשאי HIV חסרי ביטוח רפואי" מעניקה בדיקות מעקב מוגבלות מאוד (פעם בשנה CD4 ועומס נגיפי) וכן תכשירים תרופתיים ספורים. קיים קושי במקרים של מטופלים החווים תופעות לוואי, מטופלים בתכשירים עם אפשרות לתגובות בין תרופתיות במסגרת הטיפול שניתן בתוכנית או מפתחים עמידות כנגד הטיפול התרופתי[35]
טיפול בגברים המקיימים יחסי מין עם גברים
המאמצים החינוכיים והעלאת המודעות בקרב גברים המקיימים יחסי מין עם גברים עלו יפה ומסתמנת התמתנות בקצב ההדבקה על אף עלייה קלה בשנה האחרונה. לפי עבודה שהתפרסמה, שיעור הנשאות ל-HIV בקרב גברים המקיימים יחסי מין עם גברים מוערך כ-0.7 האחוז ובתל אביב כאחוז אחד[36].
עם זאת, עדיין מדובר באוכלוסייה שעלולה לסבול מתיוג שלילי, וחשופה להדבקה עקב ריבוי יחסי מין, פרקטיקות מיניות שמעלות את הסיכון להידבקות, שימוש בסמים משבשי תודעה במהלך קיום יחסי מין[37]. התמקדות יתירה יש לבצע בתוך תת-אוכלוסיות בקרב גברים המקיימים יחסי מין עם גברים שפחות חשופים למידע ועלולים להתמודד עם מחסומים בפנייה לאבחון (חרדים, פלסטינים, אנשים על הקשת הטראנסית ועוד). קהילות אלו ממעטות להיבדק והנגישות שלהן לטיפולים מונעים הפחתתה.
אנשים העוסקים בזנות
קיום יחסי מין עם שותפים רבים מעלה את הסיכון להידבקות במחלות מין באופן כללי ובנגיף האיידס. חלק מהאנשים העוסקים בזנות משתמשים בסמים, אינם נמצאים בקשר קבוע עם גורמי בריאות ורווחה וסובלים מתחלואה כפולה. משכך, ההיענות שלהם להמלצות לשמירה על בריאות, ובכלל זה על שימוש באמצעי הגנה בפני הידבקות בנגיף מוגבלים.
צעדים ליישום - מסקנות
נקודות מפתח
- ייתכן שקיים תת-אבחון בישראל
- הגישה לטיפול בחסרי המעמד נופל באיכותו מזה של אוכלוסייה מבוטחת
- מניעת הדבקה מיטבית מבוססת על העקרונות הבאים:
- הסברה והעלאת מודעות
- עידוד והנגשת בדיקות ואבחון בשלב מוקדם
- הפנייה מהירה של הנשאים לטיפול ולמעקב רפואי
- השגת עומס נגיפי בלתי מדיד בר-קיימא בקרב נשאים
- עידוד קבוצות סיכון להשתמש בטיפול לפני חשיפה
- ביצוע חקירות אפידמיולוגיות לזיהוי החשופים לנגיף
המלצות
- הגדרת צוותי עבודה שיהיו אחראים ליישום הנושאים השונים בתוכנית
- העלאת מודעות למחלה ולדרכי ההדבקה והמניעה בכל המגזרים. בנוסף, העלאת המודעות לאבחון וסוגי הטיפול והמניעה השונים בקרב צוותים רפואיים
- פעילות חינוך פורמלית (בתוך בתי ספר) וכן לא פורמלית (במרכזי נוער, מרכזי בילוי וכדומה) בקרב בני נוער מותאמות לאוכלוסייה הכללית ולקבוצות סיכון. יתירה על כך, יש לפעול להעלאת המודעות בציבור הכללי ולהפחתת הסטיגמה על נשאים
- הרחבת שירותים קהילתיים מחוץ לקופות החולים המעניקים סיקור והסברה וכן הגברת הנגישות לקונדומים, לטיפול לפני חשיפה ולמזרקים חד פעמיים לאוכלוסיות בסיכון
- הסדרת מנגנון לאיתור מאובחנים וקישורם למרכזי טיפול, איתור חולים שנושרים ממעקב והשלמת חקירות אפידמיולוגיות
- הרחבת שירותי הרפואה הייעודיים לנשאים ללא ביטוח רפואי
- מיסוד מאגר נתונים לאומי בלתי מזוהה הכולל מידע דמוגרפי, אפידמיולוגי, קליני ומעבדתי
- שיתוף פעולה עם סוכנויות ממשלתיות וארגוני חברה אזרחית
- הידוק שיתוף הפעולה בין מרפאות האיידס לרופאי הקהילה
למען יישום תוכנית זאת אנו סבורים כי יש להקים מנהלת עם בעלי תפקידים בשכר שיפעלו ליישומה.
הוכן על ידי
- ד"ר דן טורנר
- ד"ר חן מוסקוביץ
- ד"ר הילה אלינב
- ד"ר שרון רייספלד
- ד"ר גל וגנר קולסקו
- ד"ר יאן מיסקין
- פרופסור גליה רהב
- פרופסור מרטין אליס
- פרופסור חגי לוין
- פרופסור נדב דוידוביץ
- פרופסור זהר מור
- מר עידן ברק
ביבליוגרפיה
- ↑ Understanding Fast Track, UNAIDS 2015
- ↑ 2.0 2.1 Rodger, A. J., Cambiano, V., Bruun, T., Vernazza, P., Collins, S., Degen, O.,... & Pechenot, V. (2019). Risk of HIV transmission through condomless sex in serodifferent gay couples with the HIV-positive partner taking suppressive antiretroviral therapy (PARTNER): final results of a multicentre, prospective, observational study. The Lancet, 393)10189(, 2428-2438.
- ↑ 3.0 3.1 Rodger, A., Bruun, T., Weait, M., Vernazza, P., Collins, S., Estrada, V.,... & Lundgren, J. (2012). Partners of people on ART-a New Evaluation of the Risks (The PARTNER study): design and methods. BMC public health, 12(1), 1-6.
- ↑ 4.0 4.1 4.2 4.3 Owens, D. K., Davidson, K. W., Krist, A. H., Barry, M. J., Cabana, M., Caughey, A. B.,... & US Preventive Services Task Force. (2019). Screening for HIV infection: US preventive services task force recommendation statement. Jama, 321(23), 2326-2336.
- ↑ 5.0 5.1 5.2 5.3 5.4 5.5 Cohen, M. S., Chen, Y. Q., McCauley, M., Gamble, T., Hosseinipour, M. C., Kumarasamy, N.,... & Fleming, T. R. (2016). Antiretroviral therapy for the prevention of HIV-1 transmission. New England Journal of Medicine, 375(9), 830-839.
- ↑ 6.0 6.1 6.2 6.3 6.4 Clinical Guidelines-Clinical info HIV, <https://aidsinfo.nih.gov/guidelines> (2019).
- ↑ 7.0 7.1 7.2 EACS guidelines Version 10.0, <https://www.eacsociety.org/files/2019_guidelines-10.0_final.pdf> (2019).
- ↑ 8.0 8.1 8.2 Cohen, M. S., Chen, Y. Q., McCauley, M., Gamble, T., Hosseinipour, M. C., Kumarasamy, N.,... & Fleming, T. R. (2011). Prevention of HIV-1 infection with early antiretroviral therapy. New England journal of medicine, 365(6), 493-505.
- ↑ 9.0 9.1 Insight Start Study Group. (2015). Initiation of antiretroviral therapy in early asymptomatic HIV infection. New England Journal of Medicine, 373(9), 795-807.
- ↑ Kirby, T. (2020). Cabotegravir, a new option for PrEP. The Lancet Infectious Diseases, 20(7), 781.
- ↑ Molina, J. M., Capitant, C., Spire, B., Pialoux, G., Cotte, L., Charreau, I.,... & Delfraissy, J. F. (2015). On-demand preexposure prophylaxis in men at high risk for HIV-1 infection. N Engl J Med, 373, 2237-2246.
- ↑ Grohskopf, L. A., Chillag, K. L., Gvetadze, R., Liu, A. Y., Thompson, M., Mayer, K. H.,... & Buchbinder, S. P. (2013). Randomized trial of clinical safety of daily oral tenofovir disoproxil fumarate among HIV-uninfected men who have sex with men in the United States. JAIDS Journal of Acquired Immune Deficiency Syndromes, 64(1), 79-86.
- ↑ Grulich, A. E., Guy, R., Amin, J., Jin, F., Selvey, C., Holden, J.,... & Parkhill, N. (2018). Population-level effectiveness of rapid, targeted, high-coverage roll-out of HIV pre-exposure prophylaxis in men who have sex with men: the EPIC-NSW prospective cohort study. The lancet HIV, 5(11), e629-e637.
- ↑ Powell, V. E., Gibas, K. M., DuBow, J., & Krakower, D. S. (2019). Update on HIV preexposure prophylaxis: Effectiveness, drug resistance, and risk compensation. Current infectious disease reports, 21(8), 1-8.
- ↑ 15.0 15.1 Cardo, D. M., Culver, D. H., Ciesielski, C. A., Srivastava, P. U., Marcus, R., Abiteboul, D.,... & Centers for Disease Control and Prevention Needlestick Surveillance Group. (1997). A case-control study of HIV seroconversion in health care workers after percutaneous exposure. New England Journal of Medicine, 337(21), 1485-1490.
- ↑ Do, A. N., Ciesielski, C. A., Metler, R. P., Hammett, T. A., Li, J., & Fleming, P. L. (2003). Occupationally acquired human immunodeficiency virus (HIV) infection: national case surveillance data during 20 years of the HIV epidemic in the United States. Infection Control & Hospital Epidemiology, 24(2), 86-96.
- ↑ Panlilio, A. L., Cardo, D. M., Grohskopf, L. A., Heneine, W., & Ross, C. S. (2005(. Updated US Public Health Service guidelines for the management of occupational exposures to HIV and recommendations for postexposure prophylaxis. Morbidity and Mortality Weekly Report: Recommendations and Reports, 54(9), 1-CE.
- ↑ Leshin, D., Olshtain-Pops, K., Moses, A., & Elinav, H. (2019). Limited awareness of the effective timing of HIV post-exposure prophylaxis among people with high-risk exposure to HIV. European Journal of Clinical Microbiology & Infectious Diseases, 38(4), 779-784.
- ↑ Weller, S. C., & Davis-Beaty, K. (2002). Condom effectiveness in reducing heterosexual HIV transmission. Cochrane database of systematic reviews, (1).
- ↑ Giannou, F. K., Tsiara, C. G., Nikolopoulos, G. K., Talias, M., Benetou, V., Kantzanou, M.,... & Hatzakis, A. (2016). Condom effectiveness in reducing heterosexual HIV transmission: a systematic review and meta-analysis of studies on HIV serodiscordant couples. Expert review of pharmacoeconomics & outcomes research, 16(4), 489-499.
- ↑ 21.0 21.1 Briand, N., Jasseron, C., Sibiude, J., Azria, E., Pollet, J., Hammou, Y.,... & Mandelbrot, L. (2013). Cesarean section for HIV-infected women in the combination antiretroviral therapies era, 2000-2010. American Journal of Obstetrics and Gynecology, 209(4), 335-e1.
- ↑ 22.0 22.1 Mandelbrot, L., Tubiana, R., Le Chenadec, J., Dollfus, C., Faye, A., Pannier, E.,... & Veber, F. (2015). No perinatal HIV-1 transmission from women with effective antiretroviral therapy starting before conception. Clinical Infectious Diseases, 61(11), 1715-1725.
- ↑ 23.0 23.1 Townsend, C. L., Cortina-Borja, M., Peckham, C. S., de Ruiter, A., Lyall, H., & Tookey, P. A. (2008). Low rates of mother-to-child transmission of HIV following effective pregnancy interventions in the United Kingdom and Ireland, 2000-2006. Aids, 22(8), 973-981.
- ↑ 24.0 24.1 משרד הבריאות, דו"ח אפידמיולוגי תקופתי 1981-2020
- ↑ 25.0 25.1 25.2 25.3 25.4 הועד למלחמה באיידס, סוגיות במיגור HIV בישראל 2022
- ↑ Levy, I., Maor, Y., Mahroum, N., Olmer, L., Wieder, A., Litchevski, V.,... & Rahav, G. (2016). Missed opportunities for earlier diagnosis of HIV in patients who presented with advanced HIV disease: a retrospective cohort study. BMJ open, 6(11), e012721.
- ↑ Chemtob, D., Gandacu, D., Mor, Z., Grotto, I., Anis, E., & Rosenberg, E. (2017). A national strategic plan for reducing the burden of sexually transmitted infections in Israel by the year 2025. Israel journal of health policy research, 6(1), 1-10.
- ↑ Chowers, D. M., Chemtob, D., Mor, O., Levy, I., Elbrit, D., Elinav, H.,... & Turner, D. (2018, November). 572. Cascade of HIV Care of Newly Diagnosed Citizens in Israel 2011-2015: A Population-Based Cohort Study. In Open Forum Infectious Diseases (Vol. 5, No. Suppl 1, pp. S211-S212). Oxford University Press.
- ↑ Zhou, Z., Meyers, K., Li, X., Chen, Q., Qian, H., Lao, Y.,... & Ho, D. D. (2010). Prevention of mother-to-child transmission of HIV-1 using highly active antiretroviral therapy in rural Yunnan, China. JAIDS Journal of Acquired Immune Deficiency Syndromes, 53, S15-S22.
- ↑ Siegfried, N., van der Merwe, L., Brocklehurst, P., & Sint, T. T. (2011). Antiretrovirals for reducing the risk of mother-to-child transmission of HIV infection. Cochrane database of systematic reviews, (7).
- ↑ איגוד הניאונטולוגים בישראל, נייר עמדה בנושא בדיקות HIV בהיריון, 2015.
- ↑ 32.0 32.1 משרד הבריאות, אבחון מוקדם של האישה בגיל הפוריות הנושאת HIV והטיפול בה, 2022
- ↑ Israel Journal of Health Policy Research Community Vs. hospital HIV testing sites in Jerusalem, Israel - who’s tested and who’s at risk? 18 May 2020
- ↑ Katchman, E., Ben-Ami, R., Savyon, M., Chemtob, D., Avidor, B., Wasserman, A.,... & Turner, D. (2017). Successful control of a large outbreak of HIV infection associated with injection of cathinone derivatives in Tel Aviv, Israel. Clinical Microbiology and Infection, 23(5), 336-e5.
- ↑ התוכנית הלאומית למניעת HIV וטיפול במהגרים נשאי HIV חסרי ביטוח רפואי - חוזר משרד הבריאות
- ↑ Mor, Z., & Davidovich, U. (2016). Same-sex sexual attraction, behavior, and practices of Jewish men in Israel and the association with HIV prevalence. AIDS care, 28(sup1), 64-67.
- ↑ Lin, S. Y., Lachowsky, N. J., Hull, M., Rich, A., Cui, Z., Sereda, P.,... & Moore, D. M. (2016). Awareness and use of nonoccupational post-exposure prophylaxis among men who have sex with men in Vancouver, Canada. HIV medicine, 17(9), 662-673.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק