נוגדנים כנגד ממברנת הבסיס - Anti basement membrane antibodies
| מדריך בדיקות מעבדה | |
| נוגדנים כנגד ממברנת הבסיס | |
|---|---|
| Anti basement membrane antibodies | |
| שמות אחרים | נוגדנים ל-GBM |
| מעבדה | אימונולוגיה בדם |
| תחום | מחלת פקעיות הכליה או בועיות האוויר בריאות, ותסמונת Goodpasture בהתרחשות של 2 המפגעים גם יחד |
| טווח ערכים תקין | חסר מוחלט או כמעט מוחלט של נוגדני אנטי-GBM מסוג IgG. במדידה כמותית לא יותר מ-5units/ml |
| יוצר הערך | פרופ' בן-עמי סלע |
מחלה עם הופעת נוגדנים עצמיים כנגד ממברנת הבסיס, נגרמת על ידי נוגדנים המגיבים עם שרשרת אלפא-3 הבלתי קולאגנית במולקולת קולאגן type IV שגודלה 28,000 דלטון. נוגדנים עצמיים אלה מגיבים כנגד אנטיגן זה המופיע בממברנת הבסיס בפקעיות הכליה (GBM) וכן בממברנת הבסיס של בועיות האוויר (alveoli) בריאה. התקשרות הנוגדן לאנטיגן האמור, גורמת לקשירה של משלים, והפעלה של תאי-חיסון עם הרס של תאים. מדובר בהפעלת הקומפלקס C5-9 של המשלים, הידוע כ- membrane attack complex הנקשר לממברנת התאים וגורם להם נזק מהיר על ידי חירור (perforation) של הממברנה.
התסמינים הקליניים הנובעים מקישור נוגדנים אלה, יכולים להתבטא במגוון של חומרה החל ממעורבות כלייתית קלה וכלה בהתדרדרות מהירה של גלומרולו-נפריטיס, וכשל סופני של הכליות. דלקת זו כוללת פרוליפרציה ונזק כלייתי חמור, כאשר מקטעי Fc של הנוגדן העצמי מפעילים מקרופאגים, נויטרופילים, תאי NK, בנוסף להפעלה של ADCC או antibody-dependent cell mediated cytotoxicity, על ידי תאי NK, ומתרחשת הפעלה של פּרפוֹרינים ההורסים תאים תוך דקות.
לעתים, יש נטייה להתייחסות בנשימה אחת למחלת anti-GBM ולמחלת Goodpasture, אך יודגש שמחלת Anti-GBM במובנה המקורי מתייחסת יותר לנזק הכלייתי, בעוד שמחלת Goodpasture מתייחסת להתרחשות הקלינית בה יש מעורבות של גלומרולו-נפריטיס או של שטפי-דם ריאתיים, או שניהם. יש כמובן לסייג שהתסמינים הכלייתיים והריאתיים יכולים להתרחש במפגעים שונים, כגון במקרה של נוכחות נוגדנים ל-ANCA, כמו גם ב-vasculitis ובמפגעים אוטו-אימוניים נוספים. לכן חיונית הדגמת נוגדנים ל-GBM בנסיוב, בניסיון לאבחן מחלת Goodpasture. ב-60-70% מבין המטופלים עם מחלת anti-GBM, יש מעורבות של הכליות וכן של הריאות, ואלה מוגדרים כלוקים בתסמונת Goodpasture. לעומתם, ב-20-40% עם מעורבות בלעדית של הכליות ואלה מוגדרים כלוקים בגרסה הכלייתית של מחלת anti-GBM.
פתופיזיולוגיה
קולאגן type IV הוא מבנה פולימרי, שהבסיס המונומרי התלת-גדילי (triple helix) שלו, מורכב מ-3 שרשרות אלפא (אלפא-3, אלפא-4 ואלפא-5). כל שרשרת מאופיינת על ידי מקטע קולאגני ארוך בו משולבים מדי פעם רצפים קצרים לא-קולאגניים, על ידי קצה N-טרמינאלי לא קולאגני, וכן על ידי מקטע לא קולאגני ארוך בקצה ה-C טרמינאלי הידוע כ-NC1. אנטיגן Goodpasture הוא מקטע הקצה ה-C טרמינאלי הלא-קןלאגני של שרשרת אלפא-3 של קולאגן type IV או כפי שנהוג לסמנו-α-3[IV]NC1. מקטע זה מגיב עם המקטעים הלא-קולאגניים של שרשרות אלפא-4 ואלפא-5, ליצירה של מבנה תלת-גדילי הידוע כ-protomer שעובר דימריזציה ליצירה של מבנה הֶקסָמֶרי מקושר על ידי קשרי צילוב מרובים. היצירה של המבנה המשולב אלפא-3-אלפא-4-אלפא-5 (type IV), חיונית לפעילות ממברנת הבסיס.
נוגדנים כנגד GBM הם כמעט בלעדית נוגדנים מסוג IgG. היעד העיקרי של נוגדנים אלה, הם 2 אזורים סמוכים במקטע NC1 של שרשרת אלפא-3 של קולאגן type IV. אזורים אלה שסימונם EA ו-EB מכונים Goodpasture epitopes, ומיקומם המדויק הוא ברצפי חומצות אמינו 17-31 וכן 127-141, בהתאמה. נוגדני אנטי GBM, יכולים לאתר לחוד את 2 האפיטופים הללו.
אך דברים מורכבים יותר: מחקר מדוקדק של האפיטופים של Goodpasture, העלה שלמעשה קיימים 2 סוגי hexamres: קיים M-hexamer איתו מגיב הנוגדן העצמי ולעומתו ישנו גם D-hexamer שהוא קריפטי יותר ואינו נגיש לנוגדן העצמי. בפועל, יש יותר הקסמרים מסוג D, בהם קיימים קשרי צילוב בין מקטעי NC1 שהופך את האחרונים לדימרים של NC1, מה שמסייע לאופי הקריפטי של האפיטופים של Goodpature, לעומת ההקסמרים מסוג M, שהם פחות נפוצים, השומרים על אופיים המונומרי, באופן שחושף את האפיטופ NC1 להגבה עם הנוגדנים העצמיים בעיתות דלקת והתלקחות המחלה. לכן, הבדלים בין אנשים שונים הלוקים בתסמונת Goodpasture, בהרכב המונומרי/דימרי של של האפיטופ alpha-3(IV)NC1 בממברנת הבסיס של בועיות הריאה שלהם, יכולה להסביר מדוע בחלקם לא מתפתחת מחלת ריאה.
כמו בכל מחלה אוטו-אימונית אחרת, עמידות לא מלאה של מנגנוני חיסון מרכזיים ל-α-3(IV)NC1 משחקת תפקיד במחלת anti-GBM. מקטע אנטיגני זה בא לביטוי בבלוטת ההֶרֶת (טימוס), אלא שתאי +CD4 מתחמקים מהכחדה על ידי הטימוס, ומשתתפים באופן פעיל במחלת anti-GBM. גם בבני אדם בריאים יש טיטר נמוך של נוגדנים כנגד α-3(IV)NC1, כמו גם תגובת אנטי-α-3(IV)NC1 חלשה של תאי T נאיביים. יתרה מכך, ייתן למצוא בחלק מהמקרים בנסיוב של אלה עם מחלת אנטי-GBM, טיטר נמוך של נוגדנים עצמיים כנגד מרכיבים אחרים של GBM, כגון מקטע NC1 של שרשרות קולאגן אחרות. לא ברור עדיין, האם נוגדנים נוספים אלה הם בעלי משמעות פתוגנית, או שהם מייצגים בסך הכול epi-phenomenon.
ייתכן שבפתוגנזה של מחלת אנטי-GBM, משחקת תפקיד גם תגובה חיסונית תאית במנגנון של delayed-type hypersensitivity. ישנם נתונים ניסויים חזקים המרמזים לכך שיש לתאי T תפקיד בלתי ישיר בעידוד יצירתם של נוגדנים כנגד GBM בתאי B, וכן יש ראיות שתאי T יכולים בעצמם לגרום נזק לפקעיות הכליה ולבועיות האוויר בריאות. מנגד, יש עדויות לכך שתאי T מסוג +CD25, עשויים להפחית את הנזק הגלומרולארי.
ראוי לציין ששרשרת α-3 type IV של קולאגן מופיעה גם בממברנת הבסיס של רקמות אחרות (פרט לגלומרולי ולבועיות הריאה) כגון בעיניים, באשכים, ב-choriod plexus ובשבלול האוזן הפנימית (cochlea), ואף-על-פי-כן רקמות אלה אינן נחשפות למחלה דמוית אנטי-GBM. נראה שהמבנה המיוחד של הקפילארות בפקעיות הכליה ובבועיות האוויר בריאות, מאפשר לנוגדנים הללו נגישות והגבה עם ממברנת הבסיס שלהן באופן ייחודי.
למחלת anti-GBM יש נטייה להופיע יותר באביב או בתחילת הקיץ, כאשר רוב הלוקים בה מראים תסמיני מחלה סיסטמית או מעורבות של נפריטיס חדה או מעורבות ריאתית, אם כי יש תת-קבוצה בה באים לביטוי כל שלושת התסמינים האלה. המעורבות הריאתית יכולה להתבטא שנים אחדות לפני המעורבות הכלייתית, אך היא יכולה להופיע גם לאחר הופעת התסמינים הכלייתיים.
אפידמיולוגיה
בארה"ב מחלת Goodpasture מאובחנת ב-1 מתוך מיליון אנשים מדי שנה. במבוגרים, מחלת anti-GBM אחראית בערך ל- 5% מכלל המקרים של גלומרולו-נפריטיס, והיא מאובחנת ב-1-2% מביופסיות הכליה המבוצעות. גלומרולו-נפריטיס על רקע anti-GBM, אחראית ל-20% מכלל המקרים של גלומרולו-נפריטיס המתקדמת מהר במבוגרים, ולפחות מ-10% מכלל מקרים אלה בילדים.
מחלת הנוגדנים כנגד GBM מופיעה במגזרים אתניים שונים, אך שכיחה יותר באוכלוסיות לבנות. על פי דיווחים מצטברים, 83% מכלל המקרים מתרחשים בקרב לבנים. מחלה אוטו-אימונית זו שכיחה יותר בקרב גברים ביחס של 3:1 לעומת נשים. היא יכולה להופיע בגילאים השונים, ויש לה פיזור גילים דו-שיאי, כאשר השיא ראשון של הופעת המחלה הוא בסביבות גיל 30, והתרחשות אחרת מגיעה לשיאה בגיל 60 שנה. כאשר המחלה באה לביטוי בגיל המאוחר יותר, יש לה נטייה להתבטא יותר בנשים מאשר בגברים. הדיווח המוקדם ביותר בספרות של אבחון מחלת אנטי-GBM היה בתינוקת בת 11 חודשים.
מחוללי מחלת anti-GBM
פרט לעובדת היותה מחלה אוטו-אימונית, לא ברורה האטיולוגיה שלה, אם כי מספר גורמים תורמים להופעתה.
- גריינים של מעורבות פולמונארית כוללים הדבקות וזיהומים של מערכת הנשימה (שפעת) עם אפשרות של cross-reactivity, או שאיפת רעלנים כגון מרכיבי עשן סיגריות, תרסיסי שיער, CO, אדי שריפת דלק, או הידרו-פחממנים (עובדי תחנות דלק) הגורמים לשיבוש מערכת החיסון.
- גורמים הכרוכים בהתבטאות כלייתית הם נזקי כליה מאי-ספיקה, גלומרולו-נפריטיס ממברנאלית, וייתכן אף גירוי הנגרם על גלי-הלם הנוצרים בפרוצדורות של ריסוק אבנים על ידי ליתוטריפסיה (אם כי רק 4 מקרים אחרונים כאלה דווחו עד כה מתוך מיליוני פרוצדורות כאלה המתבצעות ברחבי העולם).
- במטופלים עם תסמונת Alport אין מוצאים אפיטופים של Goodpasture. לכן, השתלת כליה מתורם בריא למטופל עם תסמונת Alport, מביא להחדרת אפיטופים אלה כאנטיגן חדש "זר". לכן, כמחצית מהלוקים בתסמונת Alport מושתלי הכליות, מפתחים נוגדנים כנגד GBM, אם כי רק מיעוט מתוכם ידחו את הכליה המושתלת מסיבה זו.
בחלק מאלה עם תסמונת Alport, זיקה ותכונות הקישור של נוגדנים ל-GBM אל האפיטופים הרלוונטיים, חלשות משמעותית מאלה שמוצאים בצורה הראשונית ה"קלאסית" של מחלת anti-GBM. הבדל זה נובע משינויים בהתבטאות האנטיגנית שונה של שרשרות אלפא שונות בממברנת הבסיס, וזו גם הסיבה שהביטוי הקליני של מחלת בחולי Alport מושתלי כליה, מתון יותר מזה המתפתח בצורה הראשונית של תסמונת Goodpasture. זו גם הסיבה שחולי Alport עם כשל סופני של הכליה הם מועמדים ראויים להשתלת כליה. - הרגישות הדיפרנציאלית בבני-אדם למחלת anti-GBM כרוכה בצורה חזקה ל-MHC II או class II major histocompatability complex. בנוסף, מחלת Anti-GBM כרוכה בחוזקה עם HLA-DR-W15 haplotype, בעיקר עם האלל DRB1-1501, שמוצאים בלמעלה מ-80% מהמטופלים עם מחלת anti-GBM. יתרה מכך, הגנה חזקה מהתבטאות מחלה זו נגרמת בביטוי של האלל DRB1-0701, באופן שלמטופלים בהם יש הורשה של 2 האללים DRB1-1501 ו-DRB1-0701, יש סיכון להתבטאות המחלה שאינו גדול יותר מאשר לפרטים באוכלוסייה הכללית. יש לציין שמטופלים עם הפלוטיפ HLA-B7, נוטים להיות עם צורה יותר חמורה של גלומרולו-נפריטיס.
אבחנה מבדלת של מחלת anti-GBM
להלן תסמונות שיכולות להיות כרוכות במחלת anti-GBM, ואשר נוכחותם מצדיקה ביצוע בדיקה למציאות נוגדנים כנגד GBM: נפריטיס, פנאומוניה, SLE, תסמונת Goodpasture, הידבקות בחיידק legionella, אוטם ריאתי, ברונכיטיס (כרונית או חדה), תסמונת APLA, גלומרולו-נפריטיס בתר-סטרפטקוקאלית חדה, סקלרוזיס סיסטמי, שחפת, וסקוליטיס ותרומבו-פלביטיס, גרנולומטוזיס ע"ש Wegener.
תסמינים של מחלה סיסטמית כוללים לעתים פרקי חום לא-גבוה, חולשה, כאבי ראש, כאבים בחזה, אנורקסיה, בחילה, הקאות, איבוד משקל, אנמיה על רקע איבוד-דם, עייפות.
תסמינים של מעורבות כליות כוללים המאטוריה, ירידה בנפח השתן (oliguria), בצקת, טכיקרדיה, קצב נשימה מהיר, יתר לחץ-דם, אוושה ריאתית, בצקת גומתית (pitting edema). בחולים עם uremia יכולים להתבטא חיוורון, ריח נשימה מיוחד, רעידות בכל הגוף או רעד בלתי נשלט בכפות הידיים (asterixis), סימנים נוירולוגים ממוקדים, שינויים במצב הנפשי, פרכוסים.
תסמינים של מעורבות פולמונארית יכולים לכלול קוצר נשימה, כאבים בחזה, שיעול ממושך שעלול להיות דמי (hemoptysis), ליחה עם רצועות דם, מצוקה נשימתית לדרגותיה עד לכשל נשימתי חמור, חיוורון, טכיקארדיה, עד כדי הלם.
בחולים עם מחלת אנטי-GBM שהם גם חיוביים ל-ANCA, מוצאים לעתים פריחה עורית מלווה בגרד, וכאבי פרקים.
מבחנים מעבדתיים
נוכחות נוגדנים ספציפיים ל-GBM בפלזמה
נוכחות נוגדנים אלה פתוגנומונית למחלה. מציאותם נעשית בדרך כלל בשיטת ELISA, בה האנטיגן המשמש מצע לבדיקה הוא human alpha-3 (type IV collagen) NC1 antigen, שיכול להיות טבעי או רקומביננטי. הספציפיות של הנוגדן לאנטיגן זה יכולה להיות מאוששת על ידי Western blotting. תוצאות false positive נמצאות בפחות מ-5% מהמקרים, וייתכן למצוא אותם במאובחנים עם תסמונת Alport לאחר שעברו השתלת כליה. בפחות מ-1% מהמקרים תהיה תגובה false positive כתוצאה מנוכחות נוגדנים כנגד שרשרות אחרות של קולאגן type IV.
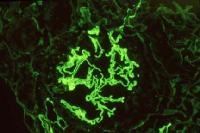
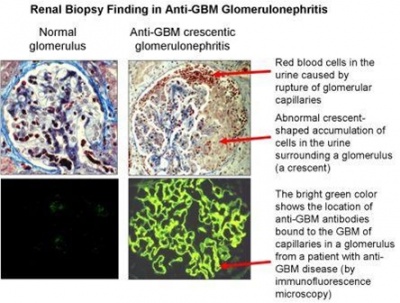
לעתים נדירות מבצעים בדיקה אימונו-היסטוכימית בלתי-ישירה על ידי הדגרה של רקמת כליה תקינה עם הנסיוב של הנבדק, וצביעת המשך עם נוגדן מסחרי ל-IgG מסומן על ידי סמן פלואורסצנטי. קבלת צביעה חיובית היא אבחונית (ראה תמונות), אם כי תוצאות שליליות-כזובות יכולות להתקבל ב-10-40% מהנבדקים.
2 תמונות: צביעה אימונו פלואורסצנטית, ותמונה עם הכותרת Renal biopsy finding of Anti-GBM
בדיקות כימיות של תפקודי כליה
תפקודי הכליה יכולים להתקבל תקינים אך גם להתדרדר במהירות תוך תקופה של שבועות עד חודשים. הכפלה של רמת קראטינין בפלזמה וירידה של GFR כדי מחצית תוך 3 חודשים, היא ראייה לגלומרולו-נפריטיס מתקדמת במהירות. אי-סדירות של האלקטרוליטים בדם, כגון היפונתרמיה, היפרקלמיה, היפרפוספטמיה ואצידמיה, יכולים להתקבל במחלה מתקדמת.
בשתן יכולים למצוא מיקרו- או מאקרו-המאטוריה. בבדיקת שתן כללית (Urinalysis), ניתן למצוא מיקרוסקופית משקעי שתן ממקור כלייתי, עם כדוריות דם אדומות דיסמורפיות, וכן מקבצים (casts) של כדוריות אלה. תיתכן גם פרוטאינוריה.
בספירת דם כללית (CBC), ניתן לגלות אנמיה מיקרוציטית היפוכרומית כתוצאה מחסר ברזל. כמו כן תיתכן תרומבוציטופניה מתונה. רמת המשלים (C3) נמוכה ב-30-80% מהמטופלים בגיל הילדות.
ליחה
מציאות של מקרופאגים עמוסים בהֶמוסידרין, היא אינדיקציה לשטפי דם בריאות.
צילום רנטגן
צילום רנטגן של בית החזה עשוי להידרש לגילוי אפשרי של שטפי-דם או דלקת ריאות. כמו כן עשויה להתבצע ברונכוסקופיה ותרבית, להערכה מלאה של הסיבה לשטפי הדם הריאתים.
בדיקת ANCA או antineutrophilic cytoplasmic antibodies
ANCA הם נוגדנים עצמיים המכוונים כנגד מרכיבים של הגרנולות הראשוניות בנויטרופילים, ובליזוזומים מכילי-פראוקסידאזה במונוציטים. בדיקת ANCA מתקבלת חיובית ב-35% מנבדקים עם מחלת anti-GBM, אם כי קיים מתאם הפוך בין הטיטר של של נוגדנים ל-ANCA ונוגדנים ל-GBM. הגילוי של נוגדנים ל-ANCA רלוונטי במחלת anti-GBM, שכן מטופלים עם נוגדני ANCA יגיבו טוב יותר לטיפול התרופתי.
מלבד הערך הפרוגנוסטי של של מציאות נוגדני-ANCA במחלת אנטי-GBM, ל-ANCA יש משמעות אבחונית חשובה כסמן ל-vasculitis של כלי-דם קטנים, כמו ב-Wegener granulomatosis, בפוליאנג'יטיס מיקרוסקופית, ובתסמונת Churg-Straus, וכן בצורות אחדות של וסקוליטיס מושרה על ידי תרופות כגון thiouracil. מצבים אחרונים אלה נכללים באבחנה המבדלת של מחלת anti-GBM. לכן, מטופלים עם גלומרולו-נפריטיס חדה, עם או ללא שטפי דם ריאתיים, נבדקים באופן שגרתי לנוכחות ANCA.
פרוצדורות היסטולוגיות
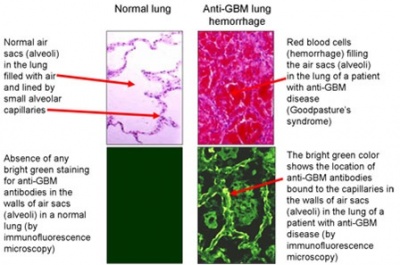
נוכחות ברורה של נוגדנים ל-GBM בפלזמה מייתרת ביצוע של ביופסיה כלייתית. בשלב הפעיל של המחלה, נראית במיקרוסקופ אור פרוליפרציה של ריבוי תאים וסהרונים (crescents) בפקעיות הכליה. במקרים מתקדמים של המחלה, נראים סהרונים בתצורה יותר סיבית מאשר תאית, וניתן לראות יש מעורבות טובּולו-אינטרסטיציאלית ניכרת יותר (אטרופיה טובולארית, הסננה אינטרסטיציאלית, פיברוזיס). בריאות ניתן למצוא שטפי דם בתוך בועיות האוויר (alveoli), וכן משקעי ברזל. וסקוליטיס בכליות או בריאות אינה שכיחה, אך יכולה להימצא במטופלים שהם חיוביים ל-ANCA.
במיקרוסקופיה פלואורסצנטית עם נוגדנים פלואורסצנטיים כנגד IgG, הממצא של צביעה לינארית של משקעי IgG לאורכן של הקפילארות הגלומרולאריות , וכן לעתים צביעה ליניארית דומה לאורך האבוביות, נחשבת פתוגנומונית. ישנם רק עוד 2 תרחישים כלייתיים הכרוכים בצביעה לינארית של IgG בפקעיות: נפרופתיה סוכרתית ו-fibrillary glomerulonephritis.
ניתן כמו כן במחלת anti-GBM למצוא משקעים נקודתיים או משקעים לינאריים מקוטעים של IgG לאורך ממברנת הבסיס בבועיות הריאה (alveolar basement membrane). במיקרוסקופ אלקטרוני ניתן לראות שברים תכופים ב-GBM.
פרוצדורות טיפוליות
- הרחקת נוגדנים ל-GBM מהצירקולציה על ידי פלזמה-פרזיס, כאשר מספר הטיפולים יכול לנוע בין 5-14 בפרק זמן של 14-21 יום.
- מניעה של יצירה עתידית של נוגדנים ל-GBM על ידי immunosuppression: רוב המטופלים מקבלים מנה גדולה של מתיל-פרדניסולון בעירוי ורידי משך 3 ימים. סטרואיד זה מדכא במהירות את מערכת החיסון ומונע יצירת נוגדנים נוספים ל-GBM. המשך הטיפול בסטרואיד הוא בטיפול פומי שיכול להימשך עד 3 חודשים, בהתאם לתגובה התרופתית. תכשיר נוסף לדיכוי יצירת נוגדנים ל-GBM, הוא ציקלופוספאמיד (שם מותג Cytoxan). הטיפול זה יכול להינתן או באופן פומי, או בעירוי תוך-ורידי אחת לחודש. הטיפול להרחקת נוגדנים ל-GBM חיוני בעיקר לפני ההליך של השלת כליה, ומומלץ ש-6 חודשים לפני ההשתלה יטופלו אלה עם הכשל הכלייתי הסופני, למנוע מצב בו נוגדנים קיימים כנגד ממברנת הבסיס יפגעו בכליה המושתלת.
- גישה פרופילקטית בהימנעות מחשיפה לגורמי סיכון פוטנציאליים כמו רעלנים וכימיקאלים שהוזכרו למעלה, מעישון, וחיסונים עונתיים למניעת שפעת.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק