נוגדנים לנגיף הפטיטיס - Antibodies to hepatitis - C
| מדריך בדיקות מעבדה | |
| נוגדנים לנגיף הפטיטיס C | |
|---|---|
| Antibodies to hepatitis C | |
| מעבדה | סרולוגיה בדם |
| תחום | תחלואת כבד, מחלות נגיפיות של הכבד |
| טווח ערכים תקין | שלילי |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – הפטיטיס
מטרת הבדיקה
אבחון הסיבה לדלקת כבד חריפה או כרונית, ואבחון נשאי הנגיף הפטיטיס C כמו גם זיהום של מנות דם הנועדות לעירוי בנגיף. בדיקה זו מתבצעת בעובדי מערכת הבריאות, ובחולי כליה המתחילים טיפולי דיאליזה.
בסיס פיזיולוגי
הנגיף הגורם לדלקת הכבד הנגיפית מסוג C (להלן HCV) ממשפחת ה-Flaviviradae הוא אחד הגורמים העיקריים למחלת כבד כרונית בעולם, ועל פי הערכות שונות נגועים בו בין 120 ל-300 מיליוני אנשים. כאשר המחלה אינה מתגלה או מטופלת היא עלולה להתפתח בשלבים למצב של לייפת הכבד (פיברוזיס), לצמקת או שחמת הכבד (צירוזיס), לכּשֶל כבדי ואף לקרצינומה של הכבד (הֶפּאטוֹמָה). בניגוד לדלקת הכבד הנגיפית מסוג B, ההידבקות ב-HCV אינה מוגבלת בעיקר למדינות המתפתחות, כאשר במדינה כבריטניה מעריכים ש- 0.7% מהאוכלוסייה בשנת 2000 הייתה מודבקת בנגיף זה. ההידבקות ב-HCV והתפשטותו מתבצעת כמעט באופן מוחלט על ידי מגע ישיר בדם. כ-15% מכלל האנשים הנגועים בהפאטיטיס C במדינות צפון אירופה עדיין שייכים לדור שהודבק בעירויי דם במהלך שנות ה-70 וה-80 עד שנת 1992, עוד לפני שנעשה סינון קפדני ובדיקה של דגימות הדם הנתרם לנוכחות הנגיף HCV שהרי זה התגלה רק בשנת 1989. נוכחות הנגיף בבנקי הדם החל משנת 1992 התאפשרה לאחר בידוד ואפיון הנגיף ע"י חברת הביוטכנולוגיה Chiron Corp.
שיעור ההידבקות בעירוי דם של מנות-דם נגועות בנגיף פחת עד כדי 0.04% מכלל העירויים. כ-74% מכלל ההדבקות בנגיף כיום הם על ידי שימוש משותף של מזרקים על ידי מכורים לסמים. העברת הנגיף מאישה מודבקת בו בשעת הריונה ליילוד פחות שכיחה אך עדיין מהווה כמחצית האחוז מכלל ההדבקות באוכלוסייה. העברת הנגיף HCV במגע מיני מתרחשת אם כי אינה שכיחה, ופחות מ-5% מכלל בני הזוג קבועים נדבקים בנגיף בדרך זו. סקירה של 1,500 בריטים מודבקים בנגיף HCV העלתה ש-51 מתוכם או 3.4%, נדבקו כתוצאה מקעקוע עורי (tattoo), אחוז מפתיע ומדאיג לאור הפופולאריות הגואה של פולחן חברתי זה.
בגלל האופי הבלתי-תסמיני של הידבקות ב-HCV, לעתים שנים רבות ממועד ההידבקות בנגיף, חיונית גישה כלל אוכלוסייתית של סריקה של דגימות דם לגילוי הנגיף. דווקא בהפאטיטיס C בשלב פעיל של התרחשות תהליך דלקתי בכבד, אחד הסמנים המעבדתיים המובהקים ביותר לתפקודי כבד, האנזים ALT מוגבר ברמתו בבדיקת הדם השִגרתית רק במהלך כחודש בתחילת תקופת ההדבקה, מה שעלול להקשות על זיהוי של פעילות כבד חריגה. נגיף HCV נחשב עד היום לנגיף "מתעתע" בכך שהוא עלול להדביק מבלי להשאיר רישומו שנים רבות, אם בכלל. זו גם אחת הסיבות לגילויו המאוחר יחסית על ידי Choo בשנת 1989, אם כי כבר ב-1975 נכתב המאמר הראשון בו התנבא Alter על מציאות נגיף העלול לגרום לדלקת כבד כרונית , ואז הוא הוגדר בדרך השלילה כנגיף Non-A, non-B, כלומר נגיף הפאטיטיס שאינו אחד משני הנגיפים שהיו ידועים אז, מסוג A ו-B.
אמנם מהלך ההדבקה ב-HCV אינו צפוי מראש: ב-15% מהמקרים הנגיף מנוטרל לחלוטין באופן שלא יגרום בעתיד לתופעות קליניות כלשהן, אם כי ב-85% מהמקרים מתפתחת הדבקה כרונית. כדי להמחיש את האופי הכרוני של הדבקה זו, יצוין שחולפות בממוצע 30 שנה מזמן ההדבקה בנגיף עד להופעת צמֶקֶת כבדית. הגורמים העיקריים הכרוכים בסכנה מוגברת למחלת הכבד מ-HCV הם גיל שמעל 40 שנה, צריכה מרובה של אלכוהול ומין זכר. במסלול האיטי של הנזק הכבדי המתהווה על ידי נגיף זה, מופיע אחר מספר שנים בקצב איטי עד מתון מצב של ליֶיפֶת הכבד (hepatic fibrosis), ורק כ-35 עד 50% מכלל אלה שהגיעו לשלב לייפת הכבד מגיעים בהמשך המסלול לשלב צמקת הכבד. בין 5 עד 15% המקרים מתפתח לשלב של החמרה נוספת של צמקת הכבד או בהופעת שאת סרטנית של הכבד (הפאטומה). צמקת הכבד כתוצאה מהידבקות ב-HCV, מהווה כיום את הסיבה הנפוצה ביותר להשתלת כבד ברוב הארצות.
אוכלוסיות הנחשדות לסיכון מוגבר להדבקה ב-HCV בהן מומלצת בדיקת סקר לזיהוי ההדבקה:
- מי שקיבל תרומת דם או דם ומוצריו, או מי שעבר השתלת איברים לפני 1992.
- תרומת איבר להשתלה (כבד, כליה, לב או ריאות) מתורם שנדבק בעבר.
- שימוש באותו המזרק ע"י משתמשי סמים, כאשר אחד המשתמשים נדבק בעבר בנגיף.
- טיפולי דיאליזה במשך תקופה ארוכה (מערכת הדיאליזה עלולה להזדהם בביה"ח עם הזמן בנגיף, כתוצאה מטיפול בחולה שנדבק בעבר).
- פציעה מקרית ממזרק מזוהם, לה חשופים צוותים רפואיים ועובדי מעבדות רפואיות.
- מגע מיני עם בן/ בת זוג נשאי הנגיף.
- הידבקות יילודים תוך כדי הלידה לאמהות שהן נשאיות של הנגיף.
- חולים ונשאים של איידס.
- חולי המופיליה אשר קבלו עירוי גורמי קרישה לפני 1987.
- אנשים שחיו באזורים בהם שכיחות ההדבקה והנשאות של נגיף הפטיטיס C הייתה גבוהה.
- רקע של קעקועי-גוף או piercing.
- אלה עם אנזימי כבד או תפקודי כבד מוגברים ללא סיבה אחרת.
אבחון
השלב המעבדתי הראשון לאחר ששוללים מחלות כבד אחרות, הוא הניסיון לאתר בנסיוב הנבדק נוגדנים המגיבים עם אנטיגנים חלבוניים של הנגיף בשיטת ELISA. מבדק מעבדתי מאוד רגיש וסגולי הוא במציאת עותקים של חומצת הגרעין של הנגיף RNA בדם המתבצע בשיטה המאוד רגישה של PCR או polymerase chain reaction, ושיטה זו מאפשרת הן לזהות הדבקה בנגיף, וכן מצביעה על כמות הנגיף השְאֵרי בדם במהלך הטיפול האנטי-נגיפי. בהתאם לתוצאות שני מבדקים אלה, נקבע המשך המעקב: אם ה-PCR נמצא חיובי, בלי כל קשר לתוצאות מבחני המעבדה לתפקודי הכבד, תתבצע ביופסיה של הכבד להערכת דרגת הפיברוזה שלו, ואת תוצאות ביופסיה זו מבטאים בסולם ע"ש Knodell. אם תוצאת הביופסיה מתונה יחסית (מתחת לדרגה 6 בסולם Knodell), ממשיכים בשגרה של בדיקת מעבדה לתפקודי הכבד אחת ל-3 חודשים, בעיקר בבדיקת פעילות האנזים גאמה-גלוטמיל-טרנספראזה. כן מומלץ לחזור על הביופסיה מקץ שנתיים אם יש החמרה בתסמינים קליניים או אם רמת האנזים ALT הדם עלתה פי-שתיים מרמתו ההתחלתית.
הגנום של HCV שגודלו 9.0kb מקודד לפחות ל-10 חלבונים הכוללים את חלבון ליבת ה-nucleocapsid הידוע גם כ-core protein, חלבוני מעטפת הנגיף E1 ו-E2, החלבונים NS3 ,NS4A ,NS4B ,NS5A ,NS5B המרכיבים את האנזים הנגיפי RNA polymerase, והחלבונים NS2 ו-NS3 המייצגים את אנזימי protease/helicase של הנגיף.
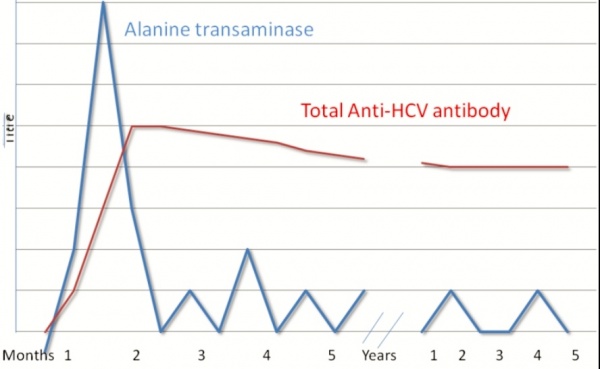
אבחון הפטיטיס C לעתים נדירות מתאפשר בשלב האקוטי של המחלה, הן כיוון שברוב המכריע של המקרים אין כל תסמיני מחלה בשלב זה, והאבחון אף מאתגר בשלב הכרוני של ההדבקה עם HCV, בהיעדר תסמינים או כיוון שתסמינים כאלה אינם ספציפיים עד להתפתחות מחלת כבד של ממש, לעתים עשרות שנים מההדבקה המקורית. האבחון המעבדתי מתחיל בטסטים סרולוגיים בנסיון לאפיין נוגדנים ל-HCV. נוגדנים אלה בדרך כלל לא יופיעו לפני 8 שבועות מההדבקה, אם כי טווח הופעתם ייתכן בין 4-10 שבועות מההדבקה, לעומת הגילוי של RNA נגיפי כבר 2-3 שבועות מהחשיפה לנגיף. בפאזה הכרונית של הדבקת הנגיף, רמות RNA נגיפי הן די קבועות, בעוד שרמת IgG כנגד HCV ממשיכה לעלות בהדרגה באופן מתון, בעוד שרמת האנזים הכבדי ALT המגיעה לשיאה בפאזה החריפה של ההדבקה דועכת לאחר מכן באופן בולט בפאזת ההדבקה הכרונית, ועולה שוב לערכים משמעותיים בשלבים מתקדמים של ההדבקה כאשר מחלת הכבד פורצת.
אבחון הדבקה ב-HCV מבוסס על גילוי בנסיוב של נוגדנים מסוג IgG כנגד הנגיף. בגלל ריבוי תוצאות חיוביות-כזובות (false positive) בטסטים המקובלים לגילוי נוגדנים אלה, יש לאשש תוצאה חיובית של נוגדנים לנגיף או על ידי מבחן RIBA או recombinant immunoblot assay או על ידי מדידה של RNA של הנגיף. תוצאה חיובית של נוגדנים לנגיף אינה יכולה להבדיל בין הדבקות ישנות או טריות. נוכחות RNA נגיפי בדם היא ראייה מקובלת להדבקה נוכחית. הנוגדנים כנגד הנגיף מכוונים כנגד החלבונים NS3, NS4, NS5 ואזור הליבה (core). שימוש בחלבוני HCV רקומביננטים מאפשר במבדקים של ELISA מה"דור השלישי", להגיע לרגישות של 97%, בטווח של 6-8 שבועות מההדבקה, אם כי מבדקים בשיטת chemiluminescence הם בעלי רגישות דומה אך ספציפיות משופרת. בדרך כלל מקובל שמבדקי ELISA מה"דור שלישי" מאוד ספציפיים, ואם תוצאת מבדק כזה חיובית, הסבירות להדבקה עם HCV במועד כלשהו גדולה מ-99%.
נתונים מצטברים מראים שנוגדנים לנגיף יכולים להתגלות ב-80% מהנבדקים תוך 15 שבועות מההדבקה, בלמעלה מ-90% מהנבדקים תוך 5 חודשים לאחר החשיפה לנגיף, ובלמעלה מ-97% מהמקרים תוך 6 חודשים מההדבקה. בסך הכול, למבדק הנוגדנים ל-HCV יש ערך ניבוי חיובי חזק להערכת החשיפה לנגיף, אך הוא עלול להחמיץ נבדקים שעדיין לא פיתחו נוגדנים לנגיף (seroconversion), או כאלה בהם רמת הנוגדנים נמוכה מתחת לסף הגילוי שלהם. כמו כן, נבדקים שנדבקו ב-HCV אלא שמערכת החיסון שלהם פגועה, עלולים לא לפתח כלל נוגדנים לנגיף. לכן, חיוני שילוב של המבדק להערכת RNA נגיפי, במקרים שבדיקת הנוגדנים מתקבלת שלילית, אך החשש להדבקה ב-HCV גבוה, לדוגמה כאשר מתקבלות תוצאות מוגברות של תפקודי כבד במי שמוגדר בסיכון להדבקה זו.
מבדק RIBA מיושם כדי לאשר תוצאות חיוביות של מבדק נוכחות נוגדנים בשיטת ELISA, וזאת למרות ששיטת PCR לגילוי RNA נגיפי הפכה להיות שכיחה במעבדות קליניות רבות. שיטת RIBA עדיין שימושית לגלות תוצאות חיוביות-כזובות של ELISA באתם נבדקים מעטים בהם מערכת החיסון הרחיקה את הנגיף, אך עדיין נותרו בדמם נוגדנים לנגיף. ה-FDA אישר את מבדק RIBA באותם מקרים בהם מבחני ELISA או chemilumenescence מתקבלים חיוביים, שכן מבדק RIBA מגלה נוכחות נוגדנים כנגד 4 חלבוני הנגיף שצוינו לעיל, שעברו ספיחה לממברנת ניטרוצלולוזה המשמשת למבדק immunoblot. תוצאת מבדק RIBA נחשבת חיובית, אם שניים או יותר מארבעת האנטיגנים האמורים מזוהים בו. אם רק אנטיגן אחד מזוהה במבדק RIBA, נחשבת התוצאה בלתי ודאית. אם אף לא אחד מהאנטיגנים האלה מזוהים תיחשב התוצאה שלילית בהחלט. הספציפיות של מבדק זה מאוד גבוהה, אך הרגישות שלו נמוכה מזו של מבחן ELISA או שיטת ה-chemilumenescence לגילוי הנוגדנים.
בגלל המגבלה שתוצאה חיובית של נוגדנים ל-HCV אינה יכולה לתת מידע על סטאטוס "גיל" ההדבקה, חיונית הבדיקה המולקולארית להערכת נוכחות חומצת גרעין נגיפית. מבדק זה יכול להיעשות בשיטת PCR (תגובת שרשרת פולימראזה), או בשיטת TMA או reversed transcriptase-PCR transcription mediated amplification, או בשיטת b-DNA או branched DNA, יכולות לגלות לא רק את מציאות הנגיף, אלא למדוד את כמות חלקיקי הנגיף הנמצאים בדם. כימות רמת הנגיף בדם חיונית בניטור התגובה לטיפול על ידי אינטרפרון, אך אין לה יכולת להעריך את חומרת המחלה או את הסבירות להתקדמותה. אם טיפול תרופתי מביא לתגובה מבוקשת, הגדרת "sustained virologic response" מתייחסת למצב בו לא ניתן לגלות כלל RNA נגיפי בתום תקופת טיפול ו-6 חודשים לאחר הפסקת טיפול זה.
בשנת 2008 אישר ה-FDA לשימוש 2 שיטות נוספות של RT-PCR לגילוי RNA נגיפי: שיטת Roche שיש לה סף גילוי של 50IU/ml של RNA בפלזמה, ושיטת Versant HCV RNA qualitative assay, עם סף רגישות משופר עוד יותר של 10IU/ml. השדרוג של שיטות גילוי הנוגדנים ל-HCV בשיטות ELISA ו-RIBA נמשך: שתי שיטות אלה מ"הדור השני", עשו שימוש באנטיגנים הנגיפיים C100-3, C200, C22 ו-C33C, בעוד שבקיטים של ה"דור השלישי", משמשים במבחני ELISA ו-RIBA האנטיגנים C22, C33 ,C100 ו-NS5.
אחר זיהוי חיובי של נוגדנים ל-HCV, ובדיקת העומס הנגיפי (viral load) יש לשקול ביצוע בדיקה לסיווג הנגיף, HCV genotyping. זאת על מנת להעריך לאיזה מ-6 תת הסוגים הידועים שייך הנגיף, שכן קביעת סוג הנגיף עשויה לסייע בהערכת התגובה שלו לטיפול המבוסס על אינטרפרון, וכן על המשך הצפוי של טיפול זה המבוסס על אינטרפרון אלפא ו-ribavirin. גנוטיפים I (השכיח ביותר) ו-IV מגיבים טוב יותר לטיפולים אלה מאשר גנוטיפים II ו-III.
שיטות כמותיות להערכת רמת RNA נגיפי: כיום קיימת שיטת להערכה כמותית של חומצת הגרעין הנגיפית, בטכניקת b-DNA-based method, שפיתחה חברת Roche על מכשיר Amplicor COBAS, גרסה 2.0. אזור היעד לאמפליפיקציה של ה-RNA הנגיפי, נמצא בתוך מקטע '5-UTR של הגנום הנגיפי המשומר היטב בכול 6 הגנוטיפים המוכרים של הנגיף.
השיטות האיכותיות או הכמותיות להערכת ה-RNA load הנגיפי, שימושיות בהערכה האם קיים מצב של חלקיקי נגיף בדם (viremia), בעיקר בנבדקים שנחשפו לנגיף ממש לאחרונה. שיטות אלה רגישות יותר משיטת ה-ELISA השגרתית, שהרי היא תגלה נבדקים עם חשיפה טרייה לנגיף 1-3 שבועות ממועד החשיפה. לעומת זאת, תשובה שלילית במבדק המולקולארי משמעותה שההדבקה התפוגגה או שההדבקה פעילה בתוך הכבד, אך אין שחרור של חלקיקי נגיף לזרם הדם בעת ביצוע המבדק.
פענוח תוצאות הבדיקה
| פענוח | HCV RNA | Anti-HCV (RIBA) | Anti-HCV (ELISA/EIA) |
|---|---|---|---|
| חוסר הדבקה | שלילי | שלילי | שלילי |
| הדבקת נגיף בעיצומה | חיובי | חיובי | חיובי |
| הדבקה בעבר או בהווה | שלילי | חיובי | חיובי |
| אין הדבקה, ממצא כוזב של ELISA | שלילי | שלילי | חיובי |
| ממצאים לא ברורים: יש לחזור על הבדיקות | שלילי | בלתי ודאי | חיובי |
| הדבקה טרייה עם הנגיף, או הדבקה כרונית בנבדק עם מערכת חיסון פגועה, שלא מסוגל לייצר נוגדנים כראוי |
חיובי | שלילי | שלילי |
הוראות לביצוע הבדיקה
אין צורך בהכנות מיוחדות או בצום. נוטלים דם במבחנה כימית (פקק אדום או צהוב), ולאחר הפרדת הנסיוב הדגימה יציבה לצורך הבדיקה למשך 7ימים בטמפרטורת החדר, או לחודשים אחדים בקירור או הקפאה למינוס 20 מעלות. חיסון נגד שפעת בסמוך לבדיקת הנוגדנים ל-HCV, עלול לתת תשובה חיובית מוגברת באופן כזוב.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק