סקרטין - Secretin
| מדריך בדיקות מעבדה | |
| סקרטין | |
|---|---|
| Secretin | |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | הערכת תפקוד בלוטת הלבלב, ומפגעי מעי |
| טווח ערכים תקין | 12-75 פיקוגרם/מ"ל |
| יוצר הערך | פרופ' בן-עמי סלע |
רקע היסטורי
בשנות ה-90 של המאה ה-19 הבחין הפיזיולוג הרוסי הנודע Pavlov בעובדה שהפרשות בלוטת הלבלב נשלטות על ידי מנגנון כפול: הן על ידי העצב התועה (vagus) וכן על ידי גירוי המגיע מרירית המעי לאחר שזו נחשפת לחומר חומצי המתרוקן מהקיבה לתריסריון. אך אסכולת Pavlov דגלה בהערכה שהגירוי שמקורו מחומר חומצי בתריסריון, מפעיל רפלקס של מערכת העצבים ההיקפית, וזו מקשרת בין רירית המעי ללבלב.
בשנת 1902 עסקו במחקר William Bayliss ו-Ernest Starling כיצד מערכת העצבים שולטת על התהליך של עיכול המזון. היה ידוע כבר לפני 100 שנה שבלוטת הלבלב מפרישה מיצים מעכלים בתגובה למעבר החומר הנוזלי למחצה (chime) המכיל את בליל המזון במעברו דרך השוער הפילורי של הקיבה בדרכו לתריסריון. שני חוקרים אלה מצאו (על ידי ניתוק כל העצבים המובילים ללבלב בחיות הניסוי) שהפרשת מיצי הלבלב למעשה אינה נשלטת על ידי מערכת העצבים. הם קבעו שחומר המופרש על ידי שכבת החיפוי במעי הוא שמעודד את הלבלב לאחר מעברו לבלוטה זו בזרם הדם. שני חוקרים אלה טבעו את המונח Secretin, והוא היה למעשה החומר ה"כימי השליח" הראשון שהתגלה. בשנת 1905 הגדיר Bayliss את secretin כהורמון, ואגב גם המושג הורמון נטבע לראשונה על ידי חוקר זה. Bayliss ו-Starling הראו שהורמון זה הוא ווסת מרכזי של הפרשות הלבלב, ומעודד הפרשה של נוזל מימי פנקראטי עשיר בבי-קרבונאט שנועד לנטרל את החומצות המופרשות מהתאים הפרייטאליים (parietal) בקיבה במעברן במעי הדק.
המבנה של secretin
עברו כ-60 שנה מאז גילוי secretin עד ש-Mutt ניקה לראשונה את ההורמון הזה ממקור חזיר, וקבע את רצף חומצות האמינו שלו (Acta Chem Scand, 1961). יצירת נוגדנים כנגד secretin אפשרה ל-Schaffalitzky ול-Fahrebkrug להוכיח את העלייה החדה ברמת secretin בדם לאחר החדרת חומצה לתריסריון, וכן לנטרל בניסויים בכלבים את השפעת ההורמון בשנת 1981 על ידי Gardner ו-Jensen.
החלבון הזה מסונתז במקור כקודמן (precursor) הכולל 120 חומצות אמינו המכונה prosecretin. צורה מוקדמת זו מכילה בקצה ה-N טרמינאלי שלה פפטיד איתות (signal peptide), ולאחריו מקטע מרווח (spacer), לאחריו הרצף בן 27 חומצות אמינו שיהווה בדיעבד את מולקולת secretin הבשלה (שיירים 28-54), ולאחריה בקצה ה-C טרמינאלי רצף של 72 חומצות אמינו.
לאחר ביקוע פרוטאוליטי להסרת ה-signal peptide וה-spacer, כמו גם של הקצה ה-C טרמינאלי, מתקבלת מולקולה בשלה של secretin בעלת 27 חומצות אמינו, שהמשקל המולקולארי שלה 3,055 דלטון. המולקולה מכילה חלק גדילי (helical) קצר בין חומצות אמינו 5 ו-13. רצף חומצות האמינו של secretin הוא כדלקמן:
H-His-Ser-Asp-Gly-Thr-Phe-Thr-Ser-Glu-Leu-Ser-Arg-Leu-Arg-Asp-Ser-Ala-Arg-Leu-Gln-Arg-Leu-Leu-Gln-Gly-Leu-Val-NH2.
רצף חומצות אמינו זה הוא בעל דמיון לזה של גלוקאגון, VIP או vasoactive intestinal peptide ול-GIP או gastric inhibitory peptide. ארבע עשרה חומצות אמינו מתוך ה-27, נמצאות באותו מקום בדיוק כמו בגלוקאגון, 7 חומצות אמינו נמצאות באותו מקום כמו ב-VIP ו-10 חומצות אמינו נמצאות בדיוק במקום בו הן מופיעות ב-GIP. אופיינית ל-secretin חומצת אמינו valine בקצה ה-C טרמינאלי שעברה אמידציה.
הקולטן ל-secretin
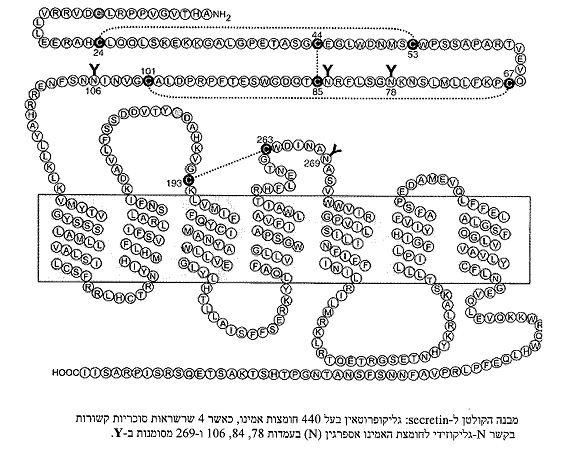
הגן המקודד לקולטן ל-secretin קרוי SCTR. המחקרים המקוריים על אופי הקולטן ל-secretin, החלו כבר בסוף שנות ה-70 במקביל במעבדותיהם של Gardner ו-Jensen, וכן באלה של Rosselin ושל Robberecht. הם מצאו שהקולטן הוא גליקופרוטאין בעל 440 חומצות אמינו, המצומד לאנזים adenylate cyclase בעזרת חלבון G אוליגומרי, וכן שקולטן זה מצוי באיברים רבים כגון במוח, שחלות, ריאות, לב, מעי גס, כליות, קיבה, כבד, וכמובן בלבלב. הקולטן הראשון ששובט היה זה אליו שנקשר secretin של חולדה, ולאחריו Patel וחב' כמו גם Jiang וחב' וכן Chow וחב', פרסמו בשנת 1995 ב-Mol Pharmacol וב-Biochem Biophys Res Commun על שיבוט קולטני secretin באדם. הקולטן האחרון, הוא טרנס-ממברנאלי שחולף דרך ממברנת התא 7 פעמים (ראה תרשים) הלוך וחזור, והוא מורכב מ"זנב" N-טרמינאלי תוץ-תאי ארוך, שלוש לולאות חוץ תאיות, ושלוש לולאות תוך תאיות, וכן הוא מכיל שרשרת הידרופובית C-טרמינאלית ציטופלזמית קצרה.
Miller וקבוצתו כמו גם Robberecht וחב', הראו שהקצה ה-N טרמינאלי החוץ-תאי של הקולטן הוא שאחראי לקשירת secretin, ו-Pang הדגים באופן אלגנטי שנקודת הגליקוזילציה של חומצת האמינו בעמדה 78 מהקצה ה-N טרמינאלי קריטית לקישור ההורמון. בשנת 1996 הראו Holtmann וחב' ב-J Biol Chem, שהקצה ה-C טרמינאלי בציטופלזמה קשור לדה-סנסיטיזציה של הקולטן ל-secretin על ידי זרחון המתבצע בעזרת receptor kinase הכרוך בחלבון G. בשנת 1998 הדגים Ulrich שבלבלב הקולטן ל-secretin מופיע הן בתאים האצינריים (acinar) וכן בתאים התוך-צינוריים (ductal).
עבודות עם עכברי knock-out שהונדסו גנטית באופן שהם אינם מסוגלים לבטא כלל את הקולטן ל-secretin, בחנו את המשמעות הסיסטמית של פגם זה. בשנת 2007 הדגימו Chu וחב', שעכברים אלה פיתחו polydipsia ו-polyuria שהיו כרוכים עם ביטוי כלייתי מופחת של Aquaporin 2 ושל Aquaporin 4, החלבונים המסייעים לחדירת מים לתאים, וכן נמצאו בעכברים אלה שינויים מורפולוגיים גלומרולאריים וטובולאריים, עם הפרעה לספיגה מחדש של מים בכליות. לעומת המחקר האחרון, מצאו Nishijima וחב' בשנת 2006, שעכברים החסרים קולטן ל-secretinממשיכים בתפקוד פיזיולוגי סביר והם אף פוריים, אם כי ניכרת בהם פגיעה בסינפסות בהיפוקאמפוס, וממילא עכברים אלה הראו שינויים בהתנהגות חברתית ובקוגניציה.
תפקידיו הפיזיולוגיים של secretin
בשנת 1970 הראו Mutt וחב' ש-secretin מיוצר על ידי תאי S ברירית של התריסריון, הממוקמים בקריפטות של Lieberkuhn. באדם, חלבון זה מקודד על ידי הגן SCT. בשנת 1998 הראו Chang וחב' במאמר ב-Amer J Physiol, במערכת in vitro שהפרשת secretin על ידי התאים המייצרים אותו במעי, יכולה להיות מושפעת על ידי נוירופפטידים כמו bombesin ,VIP ,gelanin ,gastric releasing polypeptide, ו-PACAP או pituitary adennykate cyclase-activating polypeptide.
בשנת 1992 הראו Wheeler וחב' שהגן ל-secretin מבוטא באופן זמני וחולף גם בתאי β מייצרי אינסולין באיי הפנקריאס המתפתחים, בנוסף לביטויו בתאי מעי. כמו כן secretin מיוצר גם בשורות תאי β, ואף נמצא שגן זה מבוטא גם באיברים אחרים כולל טחול, אשכים, ואף במספר אזורים במוח כפי שדווחו Whitmore בשנת 2000 ו-Welch וחב' ב-2004.
שחרור secretin לדם וללומן של המעי יגבר כאשר ה-pH בתריסריון הוא בין 2.5-4.0, בתלות בבעל החיים. הפרשת secretin מוגברת גם על ידי תוצרי פירוק חלבונים. גורמים נוספים הקשורים להפרשת secretin הם מלחי מרה, וחומצות שומניות. הפרשת ההורמון מעוכבת על ידי אנטגוניסטים לקולטן של H2, החוסמים פעילות היסטאמין על התאים הפרייאטליים בקיבה, ומפחיתים בכך את הפרשת חומצות קיבה. אב-טיפוס לתכשירים אלה הוא cimetidine הידוע בשם המותג Tagamet, וכן rantidine המוכר בשם Zantac.
Secretin מעודד גם הפרשה מכיס המרה על ידי הגברה של תעלות המים של aquaporin-1 הממברנה של תאי האפיתל של צינורות המרה, ה-cholangiocytes. בשנת 2006 הופיעה סקירתו של Chu בה הוא מתאר את הפעילויות הפלאוטרופיות המגוונות של secretin בבלוטת יותרת הכליה, במערכת הקרדיו-וסקולארית, במערכות העצבים המרכזית וההיקפית, בוושט, במחזור הרבייה הנשי, במעיים, בכליות, בכבד, בריאות, במערכת הרבייה הזכרית, בקיבה וכמובן בלבלב.
ההורמון secretin פועל על ידי הגברת ריכוז ביקרבונאט בבלוטת הלבלב. במרכז בלוטה זו יש תאים אצינריים המכילים על פני הממברנה קולטנים ל-secretin. בהיקשר ההורמון לקולטניו, הוא משרה פעילות adenylate cyclase ליצירת c-AMP מ-ATP. תוצר ריאקציה זו הוא קריטי בהעברת איתותים תוך תאיים, והוא ידוע גם בהגברת רמת קרבונאט בתא, ובשמירה על השגשוג של הלבלב ותמיכה בו. secretin מגביר הפרשת מים וביקרבונאט בתריסריון כדי לשמש buffer לנוזל החומצי המגיע מהקיבה. לאותה מטרה secretin מגביר הפרשת מים וביקרבונאט גם מהבלוטות ע"ש Brunner בתריסריון.
בנוסף, secretin מגביר את השפעתו של ההורמון cholecystokinin להשפיע על הפרשה של אנזימי עיכול מכיס המרה ומבלוטת הלבלב. כמו כן secretinמפחית רמת גלוקוזה בדם על ידי הגברת הפרשת אינסולין מהלבלב. בנוסף secretin מעודד הפרשת האנזים פפסין מתאי chief, להגברת פירוק חלבונים מהמזון, וכן הפרשת גלוקאגון, סומטוסטטין ופוליפפטיד פנקראטי.
אוסמורגולציה
רק בשנת 2007 התגלה ש-secretin משחק תפקיד בוויסות האוסמולריות בדם, על ידי השפעותיו על ההיפותלאמוס, ההיפופיזה ועל הכליות. למרות שהורמון זה מביא לשחרור gastrin במקרים של gastrinoma, הוא מפחית הפרשת חומצה מהקיבה על ידי עיכוב הפרשת gastrin מתאי G בקיבה. פעילות זו מסייעת לנטרל מעט את חומציות התריסריון, והדבר חיוני בעיקר לאנזימים עיכוליים אחרים המופרשים מבלוטת הלבלב כמו עמילאזה וליפאזה, הפועלים באופן אופטימאלי ב-pH מעט בסיסי. הייתה אף השערה שאי-סדירות בהפרשת secretin עשויה להסביר את הפגע הידוע כ-type D syndrome of inappropriate anti-diuretic hormone hypersecretion או SIADH. במטופלים אלה, אמנם יש הפרשה תקינה של vasopressin ואף תגובה תקינה לפעילותו, אך יש אי-סדירות בפעילות הכליות ובחלק מהמקרים טרנסלוקציה של aquaporin 2.
ההורמון secretin כנוירופפטיד
הביטוי המובהק של secretin באוכלוסיות ייחודיות של נוירונים בתוך המוחון (cerebellum) ובקליפת המוח, והביטוי של הקולטן של הורמון זה בכל רחבי המוח, מצביע על כך ש-secretin הוא גם נוירופפטיד. נמצא -secretin מעודד השפעה מעכבת של תאי Basket על פעילות GABA, במוחון, בהיפוקמפוס ובקליפת המוח. הורמון זה מעודד הפרשת cAMP, ומעודד הנצה של נויריטים בתרביות תאים הלקוחים מתעלת השדרה, והוא אף קשור למודולציה של תהליכי ניוון ומות נוירונים מוטוריים בעמוד השדרה.
ראיות לכך ש-secretin עשוי לפעול כנוירוטרנסמיטור, באות ממספר מחקרים. לדוגמה, Karelson וחב' הראו בשנת 1995 ב-Neuropeptides, ש-secretin מעודד ספציפית את האנזים adenylate cyclase בהיפותלאמוס ובהיפוקאמפוס. בנוסף, Banks וחב' הראו ב-2002 ב-J Pharmacol Exp Ther, ש-secretin מסומן רדיואקטיבית חדר דרך מחסום דם-מוח, והגיע לאזורי מוח שונים אך בעיקר להיפותלאמוס ולהיפוקאמפוס. Gouler וחב' הראו ב-2003 ב-Neuroscience, שעירוי תוך-ורידי של secretin עודד שפעול של c-Fos בעמיגדלה המרכזית בחולדות. Nussdorfer וחב' הראו בשנת 2000 ב-Peptides, ש-secretin מעכב את ההפרשה של ACTH, ולעומת זאת מעודד הפרשה של סומטוסטטין מסינפטוזומים במעי של חולדות על פי Kurjak וחב' ב-1996 ב-Eur J Pharmacol.
הזרקה ישירה של secretin לתוך חדרי המוח, עודדה בחולדות הפרשת אקסוקרינית של הלבלב, על פי Conter וחב' ב-1996 ב-Surgery, וכן דוח על ידי Yung וחב' בשנת 2001 ב-J Neurosci, ש-secretin מעודד מעבר של GABA מתאי Purkinje למוחון בחולדות.
כאמור, secretin וכן הקולטן שלו, באים לביטוי במגוון נוירונים בהיפוקמפוס ובאונה האחורית של בלוטת יותרת המוח. secretin מצוי לאורך הציר ההיפותלמוסי-נוירו-היפּופיזאלי ומעודד השפעת vasopressin בהיפותלאמוס והפרשתו מהאונה האחורית של ההיפופיזה, כאשר זו בסופו של תהליך משפיעה על הכליות לווסת את ההומאוסטאזיס של מים בגוף. secretin פועל גם כגורם נוירו-הפרשתי, והוא עצמו מופרש מהאונה האחורית של ההיפופיזה בתנאים של יתר-אוסמולריות בפלזמה, וכך הוא יכול לפעול ישירות על הכליות.
Secretin כמו גם הקולטן שלו מופיעים בגרעינים מבודדים בהיפותאלמוס, כולל הגרעין הפארא-ונטריקולארי וה-arcuate nucleus, שידועים כאזורי מוח חיוניים לוויסות הומאוסטאזיס של האנרגיה בגוף. נמצא שהזרקת secretin לעכברים מפחיתה בהם את צריכת המזון, מה שמצביע על פעילות אנורקטית של ההורמון. פעילות secretin בהקשר זה מתווכת על ידי מערכת ה-melanocortin המרכזית.
היבטים קליניים של secretin
יצוין שאין כל מחלה ספציפית הכרוכה בהפרשת יתר או בחסר הפרשה של secretin. מבחינה אבחונית נעשה שימוש נרחב בהורמון זה לבחינת תפקוד בלוטת הלבלב, במקרים של מפגעי הבלוטה בעיקר בפנקראטיטיס כרונית. בשנים האחרונות יש נטייה לשלב מדידת רמות secretin לזיהוי ממאירות בלבלב. Secretin משמש גם בהקשר של בדיקות בלתי חודרניות בנוסח magnetic resonance cholangio-pancreatography. מבחן secretin stimulationנמצא שימושי לגילוי גסטרינומות בבלוטת הלבלב או אף באזורים חוץ-פנקראטיים כפי שמצא Isenberg עוד בשנת 1972 ב-Gastroenterology. כמו כן הראו Takasu וחב', במאמר משנת 1998 ב-J Gastroenterol, שהזרקת secretin לתוך העורק יכולה להיות שימושית בגלוי גסטרינומה בשכבה התת-רירית של התריסריון.
פתו-פיזיולוגיה של secretin
תרחיש של רמת secrein נמוכה בנסיוב, מופיע בשני מפגעים, דהינו במטופלים עם achlorhydia ובמחלת צליאק במבוגרים. גם במקרים של אנמיה ממאירה (pernicious anemia) מוצאים hyposecretinemia. במטופלים קשישים בדרך כלל עם achlorhydia, תכולת secretin בתאים ברירית המעי היא תקינה, וניתן לעודד הפרשת secretin על ידי שתיית משקאות חומציים כמו מיץ תפוזים. במקרה של מחלת צליאק במבוגרים, האטרופיה של רירית החלק העליון של המעי הדק, גורמת לאבדן תאים מייצרי secretin, ובתרחיש זה ניתן לתקן את ה-hyposecretinemiaרק לאחר רה-גנרציה של שכבת הרירית במעבר למזון נטול-גלוטן. במחקר של Nyhlin וחב' מ-1999 בכתב העת Amyloid, נמצא שרמות secretin וכן זו של gstrin inhibitory polyprtide בתריסריון היה נמוכות, ונמצאו במתאם עם תרחיש של familial amyloidotic polyneuropathy.
בניגוד לכך, רמות מוגברות של secretin מוצאים במטופלים עם תסמונת Zollinger-Ellison, באלה עם כיב בתריסריון, באלה עם הפרשת יתר של חומצות קיבה, בתקופות רעב, בסוכרת, באלה עם כשל כליות, או במטופלים עם גידולים אנדוקריניים מפרישי secretin, שבאים לביטוי בשלשולים מימיים כפי שדיווחו לראשונה Schmitt וחב' בשנת 1975 ב-Gastroenterology. תאים מייצרי secretin נמצאו גם בגידול של מטופל עם small cell carcinoma של הוושט, כפי שדיווחו Nagashima וחב' ב-Dig Dis Sci ב-1999.
מבחן גירוי secretin או Secretin stimulation test
מבחן זה מיועדת לבחון את התפקוד העיכולי של בלוטת הלבלב, בדרך כלל במטופלים עם פנקראטיטיס כרונית, cystic fibrosis, או ממאירות הבלוטה. במבדק נבדקת תגובת הלבלב ל-secretin אקסוגני, על ידי החדרת צינורית דרך האף, הוושט, הקיבה עד הגיעה לתריסריון. בשלב זה, ייעשה עירוי תוך-ורידי של secretin, והנוזל הפנקראטי המופרש בתגובה לעירוי secretin נאסף על ידי הצינורית המוחדרת תוך 1-2 שעות. לצורך המבדק יש להיות בצום מלא של 12 שעות, כולל שתיית מים.
תכשיר מקובל של secretin למבחנים השונים של מתן הורמון אקסוגני הוא תכשיר Secretin-Ferring הוא מוצר טבעי ממקור חזיר, עם פוטנציאל של לא פחות מ-3,000 יחידות קליניות (CU) לכל מיליגרם של פפטיד. תכשיר זה מכיל בכל כמוסה 75 יחידות פעילות קליניות (CU) בצורת הורמון אבקתי מטוהר, 1 מיליגרם של L-ציסטאין-HCl, ו-20 מיליגרם של מניטול. לאחר רה-קונסטיטוציה ב-7.5 מ"ל saline, כל מיליליטר מכיל 10CU של secretin, לעירוי תוך ורידי. יחידת פעילות סטנדרטית המשמשת לגבי Secretin-Ferring היא "היחידה הקלינית" שהוגדרה על ידי Jorpes ו-Mutt בשנת 1966.
ההפרשה הפנקראטית בתגובה ל-secretin באנשים בריאים בהשוואה לזו של מטופלים עם פנקראטיטיס מבוטאת בטבלה הבאה (על פי (1972, Gutierrez and Baron):
| גברים בריאים | גברים עם פנקראטיטיס כרונית | |
|---|---|---|
| נפח ההפרשה מהלבלב (מ"ל/ק"ג/שעה) | 3.6±0.8 | 1.1±0.6 |
| ריכוז HCO3 בהפרשת הלבלב (mEq/L) | 114±20 | 71±33 |
| קצב הפרשת HCO (mEq/Kg/hr) | 0.436±0.141 | 0.105±0.093 |
תגובת הפרשה של פחות מ-2.0 מ"ל/ק"ג/שעה, ריכוז ביקרבונאט של פחות מ-90 mEq לליטר, וקצב הפרשת ביקרבונאט של פחות מ- 0.2 mEq/Kg/hrמזוהים עם תפקוד פנקרטאי פגום.
מטופלים הסובלים מפנקראיטיטיס חריפה אינם אמורים להיות מטופלים ב-Secretin-Ferring לצורך מבדק זה דע שההתקף יחלוף. מטופלים שעברו vagotomy, או שהם מקבלים טיפול אנטי-כולינרגי בעת בחינת השפעת secretin, או אלה עם מחלת מעי דלקתית (IBD), עלולים להגיב בצורה פחותה במבדק גירוי secretin. לעומת זאת, בנבדקים הסובלים ממחלת כבד אלכוהולית או אחרת, מוצאים לעתים נפחי הפרשת נוזל פנקראטי הגבוהים מאשר באנשים בריאים, מה שעלול למסך את המציאות של מחלת לבלב. יש להקפיד במקרה של מטופלים עם אסתמה או כאלה עם היסטוריה של atopic allergy, בהם יש חשש לתגובה אלרגית ל-secretin, לגלות זהירות-יתר: במקרים אלה יש לתת עירוי מקדמי של 0.1-1.0CU, ואם לא נצפית כל תגובה אלרגית לאחר דקה אחת, ניתן להמשיך בעירוי במינון המומלץ באיטיות למשך 1-2 דקות.
עירוי ורידי של Secretin-Ferring מעודד הפרשת גסטרין בנבדקים עם גסטרינומה, לעומת אי-שינוי או שינוי קל ביותר ברמת גסטרין כתגובה למתן secretin באנשים בריאים. לעומת זאת, מתן תכשיר secretin זה למטופלים עם מחלת כיב בתריסריון, יכולה לגרום לירידה קלה ברמת גסטרין בנסיוב.
בטיחות ותופעות לוואי לטיפול ב-secretin
הורמון זה ניתן כתרופת מרשם הניתנת בעירוי תוך-ורידי לאורך 1-2 דקות הנחשב בטוח אם הוא ניתן באופן מושכל. בארה"ב ילדים טופלו ב-secretinבמתן טרנס-דרמאלי, תוך שימוש ב-DMSO המוסף לאזור בעור בו נמרחה אבקת secretin, אך גם כג'ל או כתמסיך (lotion), או במדבקות עוריות. כמו ניתן secretin כטבליות או כפתילות (suppositories).
תופעות לוואי מוכרות של secretin כוללות הסמקה בפנים, בצוואר או בחזה. תופעות פחות מוכרות הן הקאות, שלשולים, הופעת קרישי דם, חולשה, חום, וקצב לב מוחש. יתר המטופלים חווים ריקאציה אלרגית כאדמומיות העור, חרלת (סרפדת, hives), ולעתים מאוד נדירות אף הלם אנפילקטי.
מבחן secretin-CCK
מבחן זה הוא שילוב של מבחן גירוי עם secretin ומבחן גירוי עם cholecystokinin, כאשר המבחן המשולב נועד להעריך את התפקוד הן של בלוטת הלבלב והן של כיס המרה. עירוי תוך-ורידי של cholecystokinin (הורמון המופרש על ידי תאי APUD ברירית המעי הדק הקריבני), מגרה את הלבלב להפריש אנזימי עיכול (עמילאזה, טריפסין וליפאזה). אנזימים מופרשים אלה נאספים על ידי צנתר הממוקם בתריסריון וכמותם נמדדת. אך cholecystokinin גם מעודד את זרימת המרה וגורם לכיס המרה להתכווץ וקובע אם כיס המרה מתרוקן באופן ראוי. הורמון אחרון זה גם משפיע על שריר השוער (sphincter) של הוושט וכן על ה-sphincter of Oddi על ידי הגברת התנועתיות בקיבה ובמעיים. הריכוז וקצב הפרשת ביקרבונאט במבחן secretin-CCK, דומה למה שמוצאים במבחן הסטנדרטי של גירוי-secretin.
הגילוי של SRP או secretin-releasing peptide
בשנת 1990 פרסמו Li וחב' ב-J Clin Invest, שהפרשת secretin המושרית על ידי חומציות המעי, מתווכת על ידי גורם נוסף, SRP או פפטיד המסייע להפרשת secretin. פפטיד זה התגלה בנוזל פרפוזיה של תוכן מעי חומצי, שנאסף בחולדות, ואופיין כבעל משקל מולקולארי קטן מ-10,000 דלטון. בהמשך בודד SRP ממקור כלבים ומשקלו המולקולארי נקבע כנמוך מ-4,000 דלטון, אם כי בשנת 1999 פרסמו Chang וחב' בכתב העת Pancreas, מאמר הרבה יותר מפורט ומהימן כדלקמן:
אף הם בחנו נוזל לבלבי ממקור כלבים, וניקו מתוכו שני SRPs במשקל מולקולארי זהה של 14,000 דלטון, שכונו SRF-1 ו-SRF-2. רצף של 31 חומצות האמינו בקצה ה-N טרמינאלי של SRF-1 היה זהה לרצף של האנזים PLA2 או pancreatic phosphplipase A2 ממקור כלבים. בנוסף, לפרקציה SRF-2 הייתה הומולוגיה של 71% עם האנזים PLA2. פרקציות SRF מכלבים בדומה לאנזים הפנקראטי PLA2 ממקור חזיר, השרו הפרשה של secretin מהתאים המייצרים אותו במערכת in vitro, תוך שהם משפעלים חדירת סידן לתאים אלה וכן משרים את פעילות האנזים PKC (או protein kinase C).
יתרה מכך, כאשר הדגירו תרכיז של פרפוזיה חומצית מהקיבה (CAP או concentrated acid perfusate) עם נוגדנים כנגד האנזים PLA2, איבדה תמיסת CAP זו את יכולתה להשרות הפרשת secretin בחולדות. יחד עם זאת, שכאשר החדירו אינפוזיה של PLA2 מנוקה ממקור חזיר, לא ניתן היה לקבל בחולדות הפרשת secretin, ונראה שהאנזים PLA2 כשלעצמו אינו מספיק לגרום להפרשת ההורמון על ידי תאי S, ונחוץ גורם נוסף שיסייע לו.
Secretin ו-PDD כולל autism
הקשר ההיפותטי מעי-מוח בתחום מפגעי אוטיזם הביא לגל של שימוש בהורמון זה לטיפול במפגעים האמורים, אם כי אין כל מידע רפואי מוסמך המסייע לגישה זו. כמו במקרים לא מעטים לגבי תכשירים או תרופות ששמם עלה בעבר בהקשר של off-label שיש בהם לכאורה בשורה במפגע זה או אחר, כך מסתמן בשלב זה הטיפול ב-secretin ב-pervasive developmental disorder בכלל ואוטיזם בפרט. הסאגה האחרונה החלה בשנת 1996 כאשר ילד אמריקני בשם Parker Beck הלוקה ב-PDD טופל ב-secretin לברור הסיבה לבעיות גסטרואנטראליות שלו, כאשר מייד לאחר טיפול זה העידה האם על כך שהילד החל לבטא לראשונה מלים וקשר העין שלו שופר. ב-1998 פרסם Horvath ב-J Assoc Acad Minor Phys, על שיפור בכישורים החברתיים והלשוניים של ילדים עם מפגעי הספקטרום האוטיסטי לאחר טיפול ב-secretin.
כמקובל במדינה כארה"ב החשיפה וההד התקשורתי-טלוויזיוני לעדות האם היה עצום, והדרישה חסרת התקדים ל-secretin גרמה למניית חברת Ferring יצרנית ההורמון, לנסיקה חסרת תקדים. בנוסף, חסר חריף במלאי secretin שנוצר כתוצאה מביקוש היסטרי, הביא מספר מעבדות לייצור גרסה של הורמון סינטתי, כאשר חברת Repligen רכשה ב-2001 את הפטנט ליצור זה. חברת Repligen השלימה ניסויי phase 2 במהלך שנת 2001, בהם בחנה 3 מינונים של secretin או פלצבו ב-126 ילדים אוטיסטים בגיל 3-6 שנים, כאשר ב-64 ילדים במדגם זה נרשם לכאורה שיפור בתפקוד החברתי, בכלל התסמינים והגברה של הבנת הנאמר או הכתוב (שפה רצפטיבית).
נכון להיום השימוש ב-secretin באוטיזם שנוי במחלוקת. מצד אחד, היו דיווחים על שיפורים במטופלים בתפקודי קיבה ומעי, וביכולות חברתיות, שפתיות והתנהגותיות כבר לאחר עירוי חד פעמי של secretin. אך רוב העדויות אינן מצביעות על טיפול זה כמשפר אוטיזם או PDD באופן כללי, הן לאחר טיפול אחד או בעקבות טיפולים חוזרים. ה-FDA לא נתן אישור לשימוש ב-secretin בלוקים באוטיזם. קיים חשש "תיאורטי" שעירויים חוזרים של ההורמון עלול לגרות את מערכת החיסון של הילד לתגובה עצמונית של "תקיפת" ה-secretin האנדוגני או את קולטניו, מה שעלול לגרום לבעיה קלינית חמורה.
הוראות לביצוע הבדיקה
הדם נאסף במבחנת הפארין (פקק ירוק) ויש לסרכז תוך 30 דקות מנטילת הדם בצנטריפוגה מקוררת, ולאחריה יש להקפיא מיד את הפלזמה המופרדת.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק