סרטן ממוין של בלוטת המגן - הנחיה קלינית - Differentiated thyroid carcinoma
הופניתם מהדף סרטן ממוין של בלוטת המגן - הנחיה קלינית לדף הנוכחי.
|
| ||
|---|---|---|
| הטיפול בסרטן ממוין של בלוטת המגן | ||
| 250px | ||
| הוועדה המקצועית | האגודה הישראלית לאנדוקרינולוגיה, בשיתוף: איגוד הכירורגים בישראל, איגוד רופאי אף אוזן גרון וכירורגיה של ראש צוואר, האיגוד לרפואה גרעינית, האיגוד הישראלי לאונקולוגיה קלינית ורדיותרפיה | |
| תחום | אונקולוגיה, כירורגיה | |
| קישור | באתר ההסתדרות הרפואית | |
| תאריך פרסום | 2008 | |
| הנחיות קליניות מתפרסמות ככלי עזר לרופא/ה ואינן באות במקום שיקול דעתו/ה בכל מצב נתון | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן בלוטת התריס
סרטן ממויין של בלוטת המגן אינו נמנה עם הממאירויות האלימות ביותר. עם זאת, יש לו פוטנציאל לפגיעה קשה באיכות החיים ובתוחלת החיים. ניתן לקבוע, שלטיפול "נכון" בסרטן של בלוטת המגן, יש השפעה משמעותית על מהלך המחלה. סוד ההצלחה בטיפול בסרטן ממויין של בלוטת המגן הוא בהקפדה על עקרונות מוכחים של איבחון, טיפול ומעקב. מטרת ההנחיות הקליניות לטיפול בסרטן ממויין של בלוטת המגן, להציג בפני הקהיליה הרפואית בישראל את העקרונות המשותפים, הרחבים, של הסכמה לגבי הגישה לחולים עם סרטן ממויין של בלוטת המגן, להציג חלופות ומחלוקות לגיטימיות (Legitimate), במקום שישנן. לגשר בין מומחים מדיסציפליניות (Disciplines) שונות המטפלים בחולים: רופאי משפחה, מנתחים, מומחים ברפואה גרעינית, אונקולוגים (Oncologists), פתולוגים (Pathologists) ומומחים בהדמיה, להקטין ככל הניתן את מוקדי אי-הבהירות, שצצים ועולים מדי פעם, ולהציע בסיס משותף ורחב, שיאפשר טיפול יעיל וטוב בחולים, בתנאים הקיימים בישראל. כמו כן, ראינו לנכון להציע שיטות ואמצעים, שנדרשים לצורך שיפור הטיפול ואיכותו, על-מנת שיכללו בעתיד בסל שירותי הבריאות בישראל.
מבוא
סרטן ממוין של בלוטת המגן אינו בין השאתות השכיחות באוכלוסייה, ובדרך כלל איננו שאת אלימה במיוחד. כאשר החולים מטופלים "נכון", התמותה נמוכה מאד, עד אפסית. עם זאת, בישראל, כמו גם במקומות אחרים בעולם, ניכרת במשך השנים עליה בשיעור המאובחנים בסרטן בלוטת המגן[1]. הסיבה לכך אינה ברורה, ונוטים ליחס זאת לשיפור באמצעי האיבחון, עליה ניכרת בשימוש בבדיקת הסונר של הצוואר, והתייחסות קפדנית יותר לקשרים קטנים בבלוטת המגן, אשר בעבר לא היו מגיעים לשלב של איבחון אנטומי-היסטולוגי (Anatomical histological). לא יפלא, איפה, שיש המטילים ספק במשמעותם הקלינית של קשרים קטנים בבלוטת המגן, גם אם הם מוגדרים "ממאירים" בבדיקה ציטולוגית (Cytology).
העקרונות הבסיסיים של המעקב והטיפול נקבעו, ברובם, לפני זמן רב ולא השתנו באופן מהותי במרוצת השנים. הם מבוססים על שימור תכונות סגוליות של ריקמת המקור: תגובתיות ה-TSH (Thyroid Stimulating Hormone), קליטת יוד בתאים וייצור תירוגלובולין (Thyroglobulin). אפשרויות התימרון בין שיטות טיפול שונות מוגבלת למדי. עם זאת, התבססו מוסכמות מסוימות, הקשורות להיקף הניתוח בהסרה של סרטן ממוין של בלוטת המגן, ואופן השימוש בתירוגלובולין כסמן אונקוגני (Oncogenic marker). הצטברו נתונים חדשים בקשר ליעילות השימוש במיפוי כל גופי לאחר מתן יוד רדיואקטיבי (Radioactive Iodine), בדיקה סונר של הצוואר, סריקה באמצעות Fluorodeoxyglucose) FDG 18) ושימוש ב-TSH רקומביננטי (Recombinant) (להלן rhTSH), במעקב הבתר-ניתוחי של המטופלים.
הדגש על טיפול "נכון" משתקף היטב בפרק המבוא להנחיות הטיפוליות בסרטן בלוטת המגן, שפורסמו על ידי Royal College of Physicians-1 British Thyroid Association, שמצאו, שתוחלת החיים של חולי סרטן בלוטת המגן בבריטניה נמוכה משמעותית בהשוואה למדינות מערב-אירופה האחרות. הנחתם, במשתמע, הייתה, שהבעיה נובעת מאופן הטיפול, הלא מיטבי, שניתן לחולים, וכי פרסום הנחיות קליניות עשוי לשפר את המצב[2]. טיפול ראשוני "נכון" הוכח כמקטין שיעורי הישנות ותמותה בחולים עם סרטן ממוין של בלוטת המגן[3][4].
מרבית הידע המצוי לגבי מעקב וטיפול בסרטן ממוין של בלוטת המגן מתבסס על מחקרים שמטרת הסיום שלהם אינה, מדידת תחלואה בעלת משמעות קלינית או תמותה, כי אם מטרות סיום משניות, כגון הופעת סמן אונקוגני או איתור הישנויות בבדיקת הדמיה זו או אחרת, שהקשר ביניהן לבין מידת התחלואה המשמעותית והתמותה מהמחלה אינו חד-משמעי. לעובדה זו יש, בלי ספק, השפעה על הבדלי השקפה וגישה בין מומחים שונים ולמידת האגרסיביות שהם מיישמים, ואליה הם מטיפים, במעקב ובטיפול.
בפרסום המסמך הנוכחי, שמה לה האגודה הישראלית לאנדוקרינולוגיה למטרה ליצור מכנה משותף רחב ככל האפשר בין מומחים מדיסציפלינות שונות המטפלים בחולים: רופאי משפחה, מנתחים, מומחים ברפואה גרעינית, אונקולוגית, פתולוגים ומומחים בהדמיה; להקטין ככל האפשר את מוקדי אי-הבהירות, שצצים ועולים מדי פעם (כמו, למשל, לגבי רמת המטרה של TSH תוך כדי מתן תירוקסין (Thyroxin) או לגבי סוג אמצעי המעקב ותדירות השימוש בהם), לשקף את עיקרי ההבדלים הלגיטימיים, בגישתם של מומחים שונים באשר לטיפול בסרטן ממוין של בלוטת המגן, להתוות את תחומי המקובל והרצוי ולהציע בסיס משותף ורחב, שיאפשר טיפול יעיל וטוב בחולים בתנאים הקיימים בישראל. מטרה מרכזית לא פחות, להציע שיטות ואמצעים שנדרשים לצורך שיפור הטיפול ואיכותו על-מנת שיכללו בעתיד בסל שירותי הבריאות בישראל.
לצורך כתיבת מסמך זה הקימה האגודה הישראלית לאנדוקרינולוגיה ועדה, שהורכבה מנשיא האגודה ומאנדוקרינולוגים בכירים בעלי ניסיון ועניין בתחום הטיפול בסרטן בלוטת המגן, המועסקים במוסדות רפואיים שונים ברחבי ישראל. חברי הוועדה משקפים מגוון דעות וגישות מעשיות ביחס למעקב ולטיפול. בראש הוועדה עמד נשיא האגודה הישראלית לאנדוקרינולוגיה ולצידו שני חברים אשר ריכזו את עבודת הוועדה. יתר חברי הוועדה שימשו יושבי-ראש של תת-ועדות, שבהן שותפו נציגים של איגודים מדעיים נוספים הנוטלים חלק בטיפול בחולים עם סרטן ממוין של בלוטת המגן [איגודי הכירורגים, אא"ג (אף אוזן וגרון), רפואה גרעינית ואונקולוגיה]. חברי תת-הוועדות סקרו את הספרות הרלוונטית, השתמשו בניסיונם ועיבדו הנחיות בנושאים השונים, תוך התייחסות למצוי ולרצוי ומבלי להתנתק מהיבטים מעשיים הקשורים לתפקוד מערכת הבריאות בארץ.
אפידמיולוגיה של סרטן בלוטת המגן
שיעור היארעות סרטן בלוטת המגן הוא, בארצות שונות, בין 2.0 ל-3.8 חולים ל-100,000 תושבים, ושכיחה יותר בנשים (ביחס של כ-1:3). סרטן בלוטת המגן שכיח יותר באזורים אנדמיים (Endemic) לחסר יוד. בישראל מגיע שיעור המקרים המאובחנים של סרטן בלוטת המגן בנשים ל-12.4 ל-100,000 ובגברים, 3.7 ל-100,000 (מתוקנן לגיל, ב-2001). הסיבה לשיעור הגבוה, יחסית לעולם, של איבחון סרטן בלוטת המגן בישראל אינה ברורה. בישראל (1), כמו במקומות אחרים בעולם[5][6], נצפתה מגמת עליה בשיעור האיבחונים במהלך 20 השנים האחרונות, כאשר ממדי מסת הגידול הראשוני המאותר הולכים וקטנים, ומבלי שנצפה שינוי משמעותי בשיעורי התמותה.
קיים פער בין שיעור ההיארעות הנמוך של סרטן בלוטת התריס עם ביטוי קליני לעומת הימצאותו [בדרך כלל במימדים מיקרוסקופיים (Microscopic)] בבדיקות היסטולוגיות שלאחר המוות, ב-2–20 אחוזים (ויותר!) מאוכלוסיית הנבדקים (לפחות פי 100 יותר מאשר הביטוי הקליני). שיעור התמותה השנתית מסרטן בלוטת המגן נמוך מאד, כ-5 מקרים למיליון תושבים (על פי סקר צפון אמריקאי), והוא לא עלה במקביל לעליה בשיעורי האבחון[5][7].
מיון סוגי סרטן בלוטת המגן
המיון הראשוני של הסוגים ההיסטולוגיים של סרטן בלוטת המגן מבחין בין סרטן פפילרי (Papillary) ופוליקולרי (Follicular), שמקורם בתאי האפיתל הזקיקי של הבלוטה, משמרים חלק מתכונות תאי המקור, ונחשבים כסרטן "ממוין" (Differentiated), לבין סרטן מדולרי (Medullary), שמקורו בתאים הפארא-פוליקולריים (Parafollicular) של בלוטת המגן [תאים מייצרי קלציטונין (Calcitonin)]. במקרים נדירים הסרטן הוא מסוג אנאפלסטי (Anaplastic) [שגם מקורו המשוער מתאים אפיתליאליים (Epithelial) של זקיקי בלוטת המגן, אך אינו משמר את תכונות תאי המקור], לימפומה (Lymphoma) של בלוטת המגן וסוגים נדירים נוספים.
הדיון במסמך זה מוגבל לסוגי הסרטן הממוין של בלוטת המגן.
כ-80 אחוזים מכלל מקרי סרטן בלוטת המגן נמנים עם סרטן פפילרי של הבלוטה. מרביתם של יתר המקרים הם של סרטן פוליקולרי או סרטן מסוג מעורב: פפילרי-פוליקולרי, אשר לגבי כולם תחזית השרידות מצוינת בדרך כלל (בכפוף לתנאי הפתיחה ולקבלת טיפול ומעקב מתאימים)[4]. קיימים תת-סוגים היסטולוגים, נדירים יחסית, שמסמנים מהלך אלים יותר: Tall (columnar)-cell, Insular, שתופסים עמדת ביניים בין סוגי הסרטן הממוין לסרטן האנפלסטי.
גורמי-סיכון לסרטן בלוטת המגן
הסיכון ללקות בסרטן בלוטת המגן גבוה יותר במי שנחשפו לקרינה מייננת לאזור הראש (טיפול בגזזת למשל) או הצוואר [תולדות של הקרנה לקשריות הלימפה (Lymph nodes), שקריים וכדומה].
היארעות משפחתית של סרטן בלוטת המגן אופיינית לסרטן מסוג מדולרי (שאינו נמנה עם סוגי הסרטן הממוין), אך ידועה גם הופעה משפחתית, נדירה יחסית, שקשורה לסרטן פפילרי[8][9]. סרטן מדולרי של בלוטת המגן מופיע בשכיחות גבוהה יותר בחולים הסובלים מתסמונת שאתות אנדוקריניות רב-מערכתית מסוג 2 (Multiple Endocrine Neoplasia, MEN-2), אך גם סרטן בלוטת המגן ממוין תואר בקשר עם MEN-1- MEN-2A.
קיים סיכון יתר לסרטן ממוין של בלוטת המגן בחולים הלוקים בתסמונות אונקוגניות (Oncogenic) [פוליפוזיס משפחתי של המעי (Familial polyposis), תסמונות אנדוקריניות רב-מערכתיות, תסמונת Gaidner, תסמונת Cowden, וכדומה). הקשר עם שאתות ממאירות אחרות קיים גם במהופך: קיימת היארעות גבוהה מהצפוי של סוגי סרטן ראשוני אחר בחולים עם סרטן בלוטת המגן [10][11].
סיכון-יתר לסרטן בלוטת המגן מדווח בחולים עם מחלות שונות של בלוטת המגן: לאחר מחלת Graves, מחלת Hashimoto (במקרה זה, קיים סיכון-יתר ללקות בסרטן ממוין וכן בלימפומה ראשונית של בלוטת המגן), וכן במי שחיים באזורים אנדמיים (Endemic) לחוסר יוד. מנתונים עדכניים עולה, ששיעור היארעות מקרי סרטן בלוטת המגן במי שלוקים במחלה רב-קשרית של בלוטת המגן דומה לזה שבאוכלוסיית המטופלים עם קשר בודד[12].
מאפיינים פרוגנוסטיים (Prognostic) של סרטן ממוין של בלוטת המגן
סרטן ממוין של בלוטת המגן מקנה תחזית טובה מבחינת שיעורי הישנות, תחלואה ותמותה, אך עם זאת, זוהו מספר מאפיינים קליניים המרמזים על מהלך אלים יותר:
- מין החולה: התחזית בגברים נחשבת טובה פחות, אך קביעה זו שנויה במחלוקת
- גיל בעת האיבחון: הסיכון להישנות ומוות עולה כאשר האבחנה של סרטן ממוין של בלוטת המגן נקבעת לאחר גיל 40–45
- מאפיינים היסטולוגיים: Tall (Columnar)-cells, Insular, Hurthle cell מסמנים תחזית טובה פחות
- מאפיינים ציטוגנטיים (Cytogenetic): נוכחות מוטציה בגן (Gene mutation) BRAF למשל, קשורה למהלך אלים יותר
- ממדי הגידול הראשוני ומידת התפשטותו בעת האבחנה: התחזית טובה פחות ככל שהגידול הראשוני גדול וככל שקיימת התפשטות מחוץ לתחומי בלוטת המגן, קיימות גרורות בקשרי לימפה אזוריים וקיימות גרורות מרוחקות.
דרוג (Staging) המחלה ורמת הסיכון
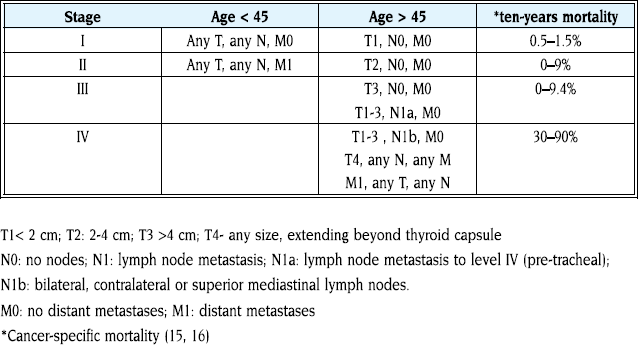
קיימות שיטות אחדות לחיזוי רמת/שיעור הסיכון של חולים בסרטן ממוין של בלוטת המגן. המכנה המשותף של שיטות הדירוג השונות מתייחס להחמרת התחזית אחרי גיל 40–45, ככל שמסת הגידול הראשוני גדולה וככל שהגידול מפושט[13]. השיטה הנפוצה ביותר היא זו של דירוג לפי (TNM (primary Tumor, regional Nodes, distant Metastases, שפותחה ומקודמת, על ידי ה-American joint Committee on Cancer. להלן תמצית שיטת הדרוג[14]:
קשריות בלוטת התריס וסוגיית הגילוי מוקדם של סרטן
עיבוד איבחוני של קשרים בבלוטת המגן קשור קשר הדוק לנושא הכללי של גילוי מוקדם של סרטן, גם אם במרבית המקרים מדובר בגילוי אקראי של קשרים בבלוטת התריס, ולא בחיפוש מכוון. המטרה העיקרית של גילוי מוקדם של סרטן היא לזהות תהליך גידולי בשלב אסימפטומטי (Asymptomatic), כדי להקטין תחלואה ותמותה עתידיים מסיבה הקשורה במחלה שאת גילויה המוקדם מבקשים להשיג.
לא בכל מקרה יש לתוכנית של גילוי מוקדם יתרון מוכח. מחקרים בנושא הגילוי המוקדם נתונים להטיות מסוגים שונים, אשר נוטות להציג יתרון מדומה לקבוצת המחקר על פני קבוצת הביקורת, המורכבת מכאלו שאינם נחשפים לטכנולוגית הגילוי מוקדם. הטיות אלו עלולות להסוות, במקרים קיצוניים, נזקים הנגרמים עקב התהליך האיבחוני. כעיקרון, תוכניות לגילוי מוקדם יעילות ביחס לגידולים בעלי קצב הכפלה מתון. בגידולים בעלי קצב הכפלה מהיר פרק הזמן הקצר שבין הגילוי המוקדם לבין המועד המשוער של הופעת תסמינים, אינו מקנה יתרון לגילוי מוקדם. גילוי מוקדם של גידולים בעלי זמן הכפלה איטי מאד אינו מקנה יתרון (לפחות באשר לשיעורי התמותה הסגולית מהגידול) באשר הם עשויים להישאר אסימפטומתיים למשך כל תוחלת החיים של הנבדק או לא-מזיקים-בפועל גם אחרי גילויים התסמיני (תוחלת החיים עשויה להיות מושפעת מסיבות בלתי תלויות בגידול הנסקר). במקרה זה גילוי של ממצא חשוד כסרטני נחשב "איבחון-יתר׳׳ (Overdiagnosis). קיימת הסכמה בקשר לתועלת של גילוי מוקדם של סרטן צוואר הרחם, המעי הגס וייתכן גם ביחס לסרטן השד. קיימים חילוקי דעות ביחס ליתרון של גילוי מוקדם של סרטן הריאה.
מכיוון שתוכניות לגילוי מוקדם של סרטן מיושמות, בדרך כלל, על אוכלוסייה בריאה, יש לתת את הדעת ולמנוע נזק כתוצאה מתהליך הגילוי המוקדם. יש לוודא, שהטיפול הניתן בעקבות הגילוי המוקדם מקטין במידה מובהקת את שיעורי התחלואה והתמותה מהגידול, בהשוואה להתחלת טיפול בגידול לאחר הופעת תסמיני המחלה. הנזקים שיכולים להיגרם עקב יישום תוכנית לגילוי מוקדם של סרטן כוללים חרדת הנבדק מפני האפשרות שהמחלה אכן תתגלה, תופעות לוואי כתוצאה מההליך האיבחוני עצמו, תופעות לוואי כתוצאה מבדיקות משלימות, ובחולים שאובחנו כסובלים מהמחלה: תופעות לוואי מטיפול מומלץ או מטיפול שמתגלה בדיעבד כמיותר.
לפי שעה, אין בנמצא נתונים ישירים לגבי תועלת אפשרית הקשורה בגילוי מוקדם של סרטן ממוין של בלוטת המגן (המהווה את רוב מנינם של מקרי סרטן בלוטת המגן). ראוי לתת את הדעת, שהשיפוד באמצעי ההדמיה, הגדיל בעשורים האחרונים את היכולת לזהות קשרים קטנים בבלוטת המגן, ולעליה ניכרת במספר הקשרים המתגלים באקראי. קשרים בבלוטת המגן נצפים בעד כדי 60 אחוזים מבני האוכלוסייה הבוגרת (ובעיקר בנשים מבוגרות)[15]. אמנם קיימים סוגים אלימים של סרטן בלוטת המגן, אך הם מהווים מיעוט, ושיעור גילויים לא עלה בעקבות השימוש בשיטות הדמיה רגישות. העלייה הניכרת בגילוי מוקדי סרטן קטנים, לא לוותה בשינוי בשיעורי התמותה מסרטן בלוטת המגן[4]. כמו כן, יש לתת את הדעת לעובדה, שקשרים המתאימים להגדרה של סרטן ממוין של בלוטת המגן המתגלים באחוז ניכר (עד 35 אחוזים) מבלוטות המגן הנבדקות לאחר המוות, במי שנפטרו מסיבות שאינן קשורות בסרטן בלוטת המגן[16], מרמזים להתנהגותם הביולוגית השפירה של רבים ממוקדי הסרטן הקטנים.
התייחסות למטופל עם ממצא אקראי של קשר, או קשרים, בבלוטת המגן ומידת הפעלתנות בבירור, צריכה להביא בחשבון את אי-הוודאות הקיימת ביחס ליחס תועלת/נזק שבגילוי מוקדם של סרטן בלוטת המגן, וצריכה להתחשב בגורמי הסיכון הסגוליים של המטופל ותוחלת חייו הצפויה.
הטיפול בחולים עם סרטן ממוין של בלוטת המגן
הפשטות היחסית בגישה האיבחונית והטיפולית לסרטן ממוין של בלוטת המגן, והתחזית הטובה (בהשוואה לשאתות ממאירות אחרות), עלולה ליצור את הרושם שמדובר במחלה קלה. חברי הוועדה מבקשים להדגיש שקיימים סיכונים הכרוכים בטיפול לא-מיומן (תת-טיפול כמו גם טיפול-יתר) הקשורים בהיעדר ידע סגולי ו/או ניסיון, בעיקר בהקשר של מקרים החורגים מהביטוי או המהלך הרגיל. חברי הוועדה מאוחדים בהמלצה, שכדי להשיג תוצאות מיטביות בטיפול בחולים עם סרטן ממוין של בלוטת המגן, הטיפול צריך להינתן במרכזים עם ניסיון רב-מקצועי מצטבר באיבחון ובטיפול במחלה, ובפיקוח רופאים מנוסים ומעודכנים בחידושים הקשורים לשיטות האיבחון, הטיפול והמעקב במחלה.
מבנה המסמך
פרקי המסמך הדנים באיבחון, בטיפול הראשוני ובמעקב מלווים בתרשימי זרימה. השלבים המכריעים בתרשימי הזרימה ממוספרים, והקורא מופנה להסברים המופיעים בפיסקאות הממוספרות במספור תואם בפרק הנלווה. הפרק הנלווה מכיל הרחבה של ההנחיות, הדגשים, ופירוט נושאים של אי-הסכמה. בסוף המסמך מופיעות המלצות המופנות למוסדות נותני השירות והרשויות הרגולטוריות.
אבחון סרטן בלוטת התריס, עימד טרום־ניתוחי, דירוג המחלה (Staging) ורמת הסיכון
תהליך האיבחון של סרטן בלוטת המגן מתחיל, בדרך כלל, בגילוי של קשר בבלוטה ואפיונו. הקשר עשוי להתגלות על ידי המטופל או מקורביו, בגלל "נפיחות" בצוואר, סימפטומטולוגיה (Symptomatology) צווארית [כגון, תחושת מלאות, קושי בבליעה, צרידות, סטרידור (Stridor), לימפאדנופתיה (Lymphadenopathy)], או כממצא לוואי של בדיקת הדמיה של הצוואר שלא כוונה מלכתחילה לחיפוש ממצאים בבלוטת המגן. ההתייחסות לקשר בבלוטת המגן אינה תלויה באופן גילויו (סימפטומטי או מקרי). שיעור ההיארעות של ממאירות בקשריות קטנות של בלוטת המגן זהה לזו בקשרים גדולים, אך קיים מתאם בין ממדיו של קשר ממאיר לבין הסיכון לסיבוכים (הישנות, תמותה) בטווח הארוך, כמו כן ישנם רמזים שקשריות ממאירות קטנות עשויות להציג התנהגות ביולוגית "שפירה" (ולא להתבטא כממאירות קלינית), כך שניתן להתייחס לקשריות קטנות בגישה שמרנית תוך מעקב זהיר. לא קיימת אחידות דעים לגבי הגבול העליון של ממדי קשרית נתונה המצריך גישה פעלתנית יותר (האזכורים בספרות נעים בין קוטר שמעל 1 סנטימטר, 2.5 סנטימטרים ועד ל-4 סנטימטרים). בהמלצות הנוכחיות נבחר הגבול של 1 סנטימטר, והתייחסות למאפיינים סונוגרפיים (Sonographic).
הערכת גורמי סיכון, בדיקה גופנית והערכת הממצא בהדמיה סונרית
- גורמי הסיכון להמצאות ממאירות בבלוטת המגן כוללים
- חשיפה לקרינה טיפולית ממוקדת (בעיקר קרינה לאזור הראש או הצוואר) או קרינה מפוזרת [כגון לאחר תאונה גרעינית, אסון צ׳רנוביל (Chernobyl)]
- תולדות משפחה של ממאירות בלוטת המגן
- תולדות של תסמונת ממאירות תורשתית (,Familial polyposis, Gardner's syndrome, Cowden's Disease, 2-MEN)
- ממצאים קליניים המעלים את הסיכוי להמצאות ממאירות בלוטת המגן
- קשר נוקשה ו/או לא נייד בבלוטת המגן
- גידול מהיר בממדי הקשר (במהלך שבועות או חודשים אחדים)
- מין זכר
- צרידות (כתוצאה משיתוק מיתרי הקול)
- ממצאים סונוגרפיים המחשידים לממאירות בקשרית בבלוטת המגן
רשימת המאפיינים הסונוגרפיים המחשידים לממאירות כוללת:
- היפואקוגניות (Hypoechogenicity)
- גבולות בלתי סדירים
- מיקרוקלציפיקציות (Microcalcification)
- ווסקולריות (Vascularity) תוך-קשרית (בניגוד לווסקולריות בהיקף הקשר)
- נוכחות קישריות לימפה חשודות[17]
- פרמטרים (Parameters) המחשידים להסננה גרורתית של קשריות לימפה
- שיבוש המבנה הסונוגרפי התקין
- הדיות הטרוגנית (Heterogenic)
- המצאות קלציפיקציות
- אזורים ציסטיים (Cystic)
- מבנה מעוגל לעומת מבנה אובאלי של בלוטות תקינות או תגובתיות. יש לתת את הדעת, שהדיווחים בספרות באשר לכושר הניבוי החיובי - (Positive piedictive value) מצביעים על ערכים שאינם גבוהים מאד (בממוצע כ-60 אחוזים) והשונות גדולה מאד. הסגוליות של כל אחד מהסימנים הסונוגרפיים בנפרד נמוך יחסית אך ככל שמספר הסימנים המחשידים לממאירות גדול, עולה דיוק הבדיקה[17]. הדיוק האבחנתי של בדיקת US (Ultrasound) תלויה במידה רבה מאד בניסיונו ובמיומנותו של הבודק
- ממצאים נוספים הקשורים להמצאות ממאירות בלוטת המגן
המצאות מוקד קולט במיפוי PET-FDG (Positron Emission Tomography-Fluorodeoxyglucose) מעלה את הסיכון לממאירות, אך הבדיקה אינה סגולית לממאירות. קשרים אוטונומיים (Autonomic), שאינם חשודים לממאירות, עשויים להסתמן בבדיקת PET וניתן לזהותם ככאלה באמצעות בדיקת תפקוד בלוטת המגן ומיפוי של הבלוטה. באשר לקשרים שאינם אוטונומיים, הגישה זהה לזאת שבקשריות שהתגלו באמצעים אחרים[18].
קשרים בבלוטת המגן עשויים להתגלות במיפוי פראתירואיד (Parathyroid) באמצעות Sestamibi. גם במקרה שכזה קיימים דיווחים שהממצא מעלה את הסיכון לממאירות, ויש לבררו על-פי תרשים הזרימה.
תפקוד בלוטת המגן, קלציטונין בנסיוב
בדיקת TSH חיונית לצורך הערכת פעילות בלוטת המגן והערכת האפשרות של פעילות אוטונומית של הקשר שבבירור. הסיכון לממאירות בקשר פעיל("חם") נמוכה מאד. בחולים עם מחלת גרייבס ('Graves) וקשר בבלוטת המגן קיים סיכון לממאירות שהוא גבוה יחסית. בחולים עם TSH נמוך (מתחת לגבול התחתון של תחום התקין) ניתן לבצע מיפוי בלוטת המגן על מנת להגדיר את אופי הקליטה; קליטה ממוקדת בקשר או קליטה דיפוזית עם קליטה נמוכה בקשר. קליטה ממוקדת בקשר מגדירה אותו כבעל פעילות אוטונומית ("חם"). קליטה דיפוזית וקשר "קר" מעוררת חשד לאפשרות של ממאירות בנוכחות מחלת גרייבס. בדיקה ציטולוגית עשויה לסייע באפיון כל קשר כשפיר או ממאיר, ללא תלות במידת תפקודו[19].
ממספר מחקרים עולה, שבדיקת קלציטונין (Calcitonin) בנסיוב עשויה לסייע לאיבחון של סרטן מדולרי של בלוטת המגן[20], אך אין תמימות דעים לגבי חיוניותה כבדיקת סקירה. הבדיקה עשויה להיות יעילה במקומות שבהם קיימת באוכלוסייה שכיחות גבוהה יחסית של סרטן מדולרי, שאינו שכיח בישראל. חברי הוועדה מאוחדים בדעה שבדיקת קלציטונין אינה צריכה להיות חלק מהבירור השיגרתי בישראל, אך יש לבצעה במקרים בהם קיימת סבירות לסרטן מדולרי (תולדות משפחה של סרטן מדולרי, 2־MEN). הבדיקה הציטולוגית, המהווה מרכיב מרכזי באפיון של קשרי בלוטת המגן, מאפשרת לאפיין ככזה גם סרטן מדולרי של בלוטת המגן.
בדיקות תירוגלובולין (Thyroglobulin). נוגדני בלוטת המגן בנסיוב אינן תורמות להערכה הקלינית של הסיכון לממאירות בחולים עם קשרים בבלוטת המגן.
זפק רב קשרי
ריבוי הקשרים בזפק רב-קשרי יוצר בעיה אבחנתית. ככלל, הסיכון לממאירות בחולה עם קשר יחיד דומה לזה בחולה עם זפק רב קשרי. הסיכון לממאירות בקשר נתון נמוך יותר ככל שמספר הקשרים בזפק רב יותר, עובדה המקשה על איתורו של הקשר הממאיר שבזפק, אם קיים קשר כזה בזפק נתון. כאשר קיים קשר ממאיר בזפק רב-קשרי, קיים סיכוי של כ-70 אחוזים שהממאירות תמצא בקשר הגדול, אך ככל שמספר הקשרים בזפק עולה, גובר הסיכוי שהממאירות תמצא בקשר שאינו הגדול ביותר. רק בכ-40 אחוזים מהמקרים בהם הזפק מכיל 4 קשרים או יותר הממאירות תמצא בקשר הגדול ביותר, לעומת כ-85 אחוזים מהמקרים שבהם הזפק מכיל שני קשרים בלבד[12]. יש לשאוף לדגום כל אחד מהקשרים לצורך בדיקה ציטולוגית. עם זאת, ניתן להתמקד בקשרים הגדולים ביותר, אלו המסתמנים כ"קרים" במיפוי, ולהסתייע בהנחיית US לאיתור קשרים בעלי מאפיינים סונוגרפיים (Sonographic) חשודים.
מיפוי בלוטת המגן
ברוב המכריע של המקרים אין הבדל עקרוני בין מיפוי באמצעות טכנציום (Technetium), שביצועו פשוט ומהיר, למיפוי באמצעות יוד רדיואקטיבי. עם זאת, יש לתת את הדעת שבאחוז נמוך (כ-5 אחוזים מהחולים) שבהם נמצא קשר "חם" בבדיקת טכנציום, אין התאמה עם הממצאים במיפוי באמצעות יוד רדיואקטיבי (שמראה שהקשר "קר"), כתוצאה מלמדת יוד (במנגנון שלוכד גם טכנציום) ופגם בתהליך האורגניפיקציה שלו (Organification) [21]. הסיכוי לממאירות בקשרים עם הפרעה באורגניפיקציה עשוי להגיע לכ-30 אחוזים. בנוסף, קיימים מקרים נדירים שבהם סרטן בלוטת המגן מציג פעילות אוטונומית. בכל מקרה של ספק לגבי מהות הקשר ניתן להיעזר בבדיקה ציטולוגית.
הבדיקה הציטולוגית
הבדיקה הציטולוגית היא האמצעי המדויק והחשוב ביותר לצורך הבחנה בין קשרים שפירים וממאירים של בלוטת המגן. הדיקור צריך להעשות על ידי מי שמיומן בביצוע הבדיקה. הבדיקה צריכה להעשות כאשר החולה שוכב, רצוי לאלחש את העור באחור הדיקור ולבצע לפחות 3–4 דיקורים. מבצע מיומן יכול לזהות דגימה טובה בעין, אך כאשר התנאים מאפשרים, רצויה נוכחות ציטולוג באתר הבדיקה לצורך צביעה מהירה, וכדי להבטיח שהמשטחים מכילים חומר מתאים לאבחנה. בתיאום עם הציטולוג יש לשלוח את המחטים וחומר שטיפה מהמחטים לצורך שיקוע Cell blocks. במקרה של קשר שנמוש בקלות, ניתן לבצע את הדיקור בהנחיה באמצעות מישוש. כאשר הקשר אינו נמוש בקלות או שאינו נמוש כלל, יש לבצע את הבדיקה בהנחיה של US.
במגבלות הבדיקה, התשובה עשויה להיות אחת מ-5 הגדרות:
- שפיר (Benign)
- ממאיר (Malignant)
- חשוד לממאירות (Suspicious for malignancy)
- נגע פוליקולרי (Indeterminate, follicular lesion)
- חומר לא מספיק לאבחנה (Inadequate). הבדיקה הציטולוגית מסוגלת לאבחן סרטן פפילרי ולהבדילו מסרטן מדולרי. הבדיקה הציטולוגית אינה מסוגלת להבחין בין אדנומה (Adenoma) פוליקולרית לקרצינומה (Carcinoma) פוליקולרית.
חולים עם קשרים המוגדרים "ממאיר" או "חשוד לממאירות" מופנים לכריתה ניתוחית של הקשר (ראו "טיפול ראשוני"), וכן נגעים פוליקולריים "קרים" במיפוי. במקרה של נגע פוליקולרי "חם" במיפוי, ניתן לבחור באפשרות של מעקב, שכן הסיכוי לממאירות בקשר "חם" נמוך מאד. כאשר החומר אינו מספיק לאבחנה, ניתן לחזור על הדיקור ו/או להסתייע בהנחיה אולטראסונית (סונר)[14][22].
מעקב אחר קשרים, שהוגדרו כשפירים ולא נותחו
לנוכח מגבלות הטבועות הן בבדיקה הציטולוגית, ובעיקר בבדיקת ה-US, במקרים בהם הבירור שולל את הצורך המיידי בטיפול ניתוחי, רצוי להמשיך במעקב קליני ו/או סונוגרפי. לנוכח קצב הגדילה האיטי של מרבית ממאירויות בלוטת המגן, פרקי הזמן למעקב יכולים להתפרש על מספר חודשים (כ-6 חודשים למעקב הראשון) ואם אין עדות לגדילה משמעותית של הקשר, ניתן להרחיב את טווח המעקב עד שנה (ויותר). הסיכון לממאירות בקשר שאובחן שפיר בבדיקה ציטולוגית, נמוך ביותר, אך במקרה של ספק ניתן לחזור על הבדיקה[14].
קביעת הדירוג ורמת הסיכון (Staging) טרום־ניתוחי
משהועלה חשד ציטולוגי או קליני לאפשרות של סרטן בלוטת המגן והוחלט על הפניית החולה לטיפול ניתוחי, מומלץ לבצע דירוג סיכון קליני-הדמייתי, שכולל בדיקה גופנית, וסריקת US של הצוואר במטרה לזהות מראש קשריות לימפה חשודות. אם קיים חשד להתפשטות מקומית נרחבת של הגידול יש לשקול הדמיה של הצוואר והמדיאסטינום (Mediastinum) באמצעות CT ללא חומר ניגוד (כדי למנוע עיכוב לאפשרות של טיפול עתידי ביוד רדיואקטיבי) או Magnetic resonance imaging) MRI). [14].
- נושאים שבמחלוקת
- שימוש ב-US לצורך דיקור קשרים בבלוטת המגן:
חברי הוועדה אינם מאוחדים בדעתם בנושא זה, הן מטעמים ענייניים והן לנוכח הזמינות המוגבלת של דיקור מונחה US, ובלבד שביצוע הבדיקה יהיה בידי מי שמיומן בכך. עם זאת, קיימת הסכמה לגבי הצורך בדיקור מונחה US במקרים בהם הקשרים חשודים ולא נמושים ובמקרים בהם האבחנה הציטולוגית לאחר דיקור מונחה מישוש אינה חד-משמעית - תוצאה ציטולוגית אבחנתית לאחר דיקור מונחה מישוש בלבד:
חברי הוועדה אינם מאוחדים בדעתם בנושא זה, הן מטעמים ענייניים והן לנוכח הזמינות המוגבלת של דיקור מונחה US, ובלבד שביצוע הבדיקה יהיה בידי מי שמיומן בכך. עם זאת, קיימת הסכמה לגבי הצורך בדיקור מונחה US במקרים בהם הקשרים חשודים ולא נמושים ובמקרים בהם האבחנה הציטולוגית לאחר דיקור מונחה מישוש אינה חד-משמעית - התוויה לניתוח לאחר אבחנה ציטולוגית לא אבחנתית, או של נגע "פוליקולרי":
לא קיימת הסכמה גורפת לגבי צורך בהפניה מיידית לניתוח, או רק אם הנגע אינו "חם" במיפוי. הגישות האפשריות כוללות: הפניה לניתוח של כל נגע פוליקולרי "קר", דיקור חוזר של הקשר לאחר פרק זמן של מספר חודשים, מעקב US אחר ממדי הקשר. בכל מקרה של החלטה על מעקב קליני-סונוגרפי, יש להקפיד שהמעקב יהיה הדוק וזהיר. במקרה שמתעורר ספק במהלך המעקב, יש להעדיף הפניה לניתוח - מידת הפעלתנות בבירור קישריות קטנות:
לא קיימת הסכמה לגבי מידת הפעלתנות בבירור קישריות קטנות (פחות מ-1~ סנטימטר) המתגלות "במקרה" (מוגדרות גם כ׳׳מיקרו-קרצינומה׳׳). הארעות מחלה קשרית של בלוטת המגן שכיחה מאד, עד כ-60 אחוזים מהאוכלוסייה המבוגרת. יש מי שסבורים שהתכונות הציטו-מורפולוגיות אינן סגוליות דיין ושלפחות חלק מהנגעים המדגימים תכונות ציטו-מורפולוגיות החשודות כממאירות אינן כאלה. מאידך גיסא, ידוע על מהלך ביולוגי אלים הקשור במיקרו-קרצינומות של בלוטת המגן. לא קיימת בנמצא המלצה, לסריקה של האוכלוסייה לגילוי של קשריות בבלוטת המגן. אין בנמצא נתונים הרומזים לתחלואה או תמותה עודפת כתוצאה מהשהיית הטיפול הכירורגי בקשריות ממאירות קטנות. ביצוע בירור מעמיק של קשריות קטנות המתגלות באקראי מעלה, לכאורה, סוגיה אתית לגבי קשריות המצויות באוכלוסייה ואשר אינן מתגלות. גישה אפשרית: עיבוד פעלתני, באמצעות דיקור מונחה US של קשרים קטנים בחולים עם גורמי סיכון לסרטן בלוטת המגן או כלפי קשרים בעלי מיקבץ של מאפיינים סונוגרפיים חשודים. במקרים אחרים, ניתן להסתפק במעקב קליני וסונוגרפי למשך מספר שנים
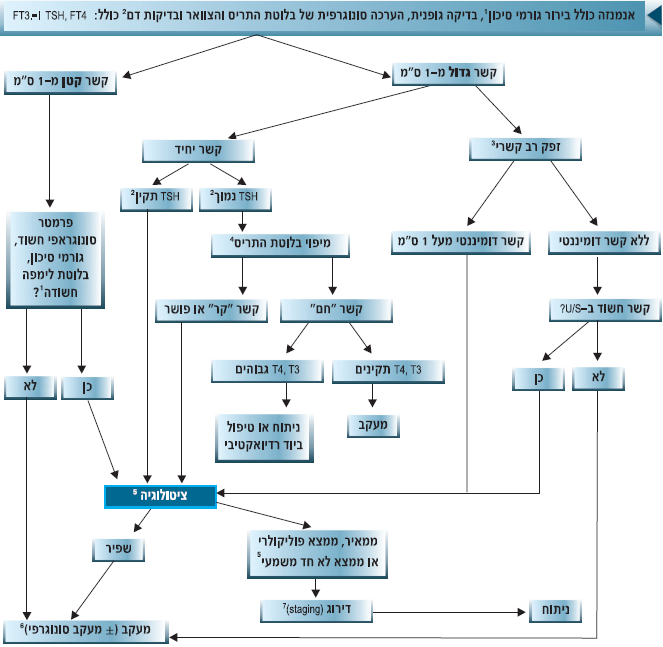
תרשים זרימה מספר 1: אבחון, עיבוד טרום ניתוחי וקביעת דרגת סיכון לסרטן ממוין של בלוטת התריס
הטיפול הראשוני בסרטן ממוין של בלוטת המגן
מטרת הטיפול הראשוני לסלק, ככל האפשר, את כל מסת הגידול (או את רובה המכריע), לנוכח השכיחות הגבוהה יחסית של ריבוי מוקדים מיקרוסקופיים, ועל מנת לאפשר שימוש בתירוגלובולין כסמן אונקולוגי. מטרה נוספת של הטיפול הראשוני, למעט במקרים מיוחדים, כפי שיפורט להלן, היא גם לסלק ולהשמיד את יתרת הריקמה התקינה לכאורה, של בלוטת המגן באמצעות טיפול משלים ביוד רדיואקטיבי. לבסוף, על מנת לבטל את ההשפעה מעוררת הגדילה של TSH על תאים ממקור בלוטת המגן, נדרש דיכוי של רמת TSH אל מתחת לתחום הנחשב "תקיף באמצעות התאמה של מינון תירוקסין (Thyroxin).
אופי הטיפול מוכתב במידה רבה על ידי מידת הסיכון להישנות. מקובל למיין את המטופלים לקבוצת סיכון.
קבוצת סיכון נמוך: ללא עדות לגרורות מקומיות (במיטת בלוטת המגן, בצוואר ובאיברים סמוכים -קנה, ושט) או גרורות מרוחקות, כל מסת הגידול הנראית לעין הוסרה, ללא הסננה לכלי דם, ללא צורה היסטולוגית אלימה (ראה מבוא), קליטת יוד רדיואקטיבי במיטת בלוטת המגן בלבד במיפוי הכל גופי (Whole Body Scan ,WBS) הראשון.
קבוצת סיכון גבוה: חולים שבהם נמצא אחד או יותר מהבאים: גידול הראשוני בקוטר גדול מ-4 סנטימטרים, פלישת הגידול הראשוני לכלי דם ו/או לסביבה, היסטולוגיה אלימה יחסית (כולל קרצינומה פוליקולרית), כריתה לא-שלימה של הגידול, גרורות מקומיות או מרוחקות.
היקף הניתוח לכריתת בלוטת המגן
מרבית החולים מנותחים לאחר שנקבעה אבחנה טרום-ניתוחית ודאית או שנקבע חשד לסרטן בלוטת המגן. הניתוח המומלץ במקרים אלו הוא כריתה מלאה, או כמעט מלאה, של בלוטת המגן. ניתוח זה נדרש כאשר קוטר הגידול הראשוני גדול מ-1 סנטימיטר, כאשר מצויות קשריות באונה השנייה של בלוטת המגן, ישנם גורמי-סיכון סגוליים (כגון, תולדות של הקרנה לראש-צוואר, תולדות של ממאירות בבלוטת המגן בקרובי משפחה מדרגה ראשונה, תסמונות של גידולים מרובים), כאשר קיימת התפשטות מקומית או גרורות מרוחקות. קיימת הצדקה לכריתה מלאה או כמעט מלאה גם בחולים בגיל שמעל 45 שנה, נוכח מהלך אלים יחסית ושכיחות-יתר של הישנות הגידול בקבוצת גיל זו[23].
ניתן להסתפק בניתוח חלקי [כריתת אונה ואיסטמוס (Isthmus)] בחולים עם גידול חד-מוקדי בקוטר הקטן מ-1 סנטימטר, בהיעדר גורמי סיכון סגוליים (כנזכר לעיל), בהיעדר קשריות באונה הנגדית של בלוטת המגן ו/או קשריות לימפה צוואריות חשודות כנגועות. כאשר האבחנה של סרטן בלוטת המגן ידועה או נחשדת מראש, רצוי לשתף את החולה ולהתחשב ברצונו לגבי היקף הניתוח[24].
השלמת כריתת בלוטת המגן לאחר כריתה חלקית (Completion thyroidectomy)
היה ובוצעה כריתה חלקית של בלוטת המגן ובסופו של דבר אובחן הגידול כממאיר, מומלץ על השלמת הכריתה, בניתוח חוזר, פרט למקרים המקיימים את התנאים המאפשרים כריתה חלקית (ראה לעיל).
הרחבת הניתוח למדורי בלוטות הלימפה
ביתור (Dissection) של מדורי קשריות הלימפה האזוריות מומלץ כאשר בדיקות ההדמיה הטרום-ניתוחיות מרמזות על מעורבותן של קשריות לימפה. ביתור של Central compartments מומלצת כאשר הגידול רב-מוקדי, פורץ מחוץ לקופסית או שקיימים ממצאים תוך-ניתוחיים המחשידים לאפשרות של התפשטות לימפתית (קשריות לימפה מוגדלות).
- גישה ניתוחית בגידולים המערבים את ה-Recurrent laryngeal nerved
יש להעריך את תנועתיות מיתרי הקול טרם הניתוח. אם קיים שיתוק מיתרי הקול אין מניעה לכרות את העצב בצד של מיתר הקול המשותק. אם לא קיימת הפרעה טרום-ניתוחית בתנועת מיתרי הקול, יש לנסות לשמר את העצב ולקלף את הגידול שסביבו.
- גישה ניתוחית בגידולים החודרים לקנה ו/או לושט
במקרים בהם מזוהה הסננה של הגידול לקנה הנשימה ו/או לושט, מומלץ לבצע "גילוח"("Shaving") של ריקמת הגידולית מעל הקנה ו/או הושט, ולהרחיק את מירב הריקמה הגידולית.
השלמת הטיפול הראשוני: טיפול ביוד רדיואקטיבי
כל החולים בהם אובחן סרטן ממויין של בלוטת המגן, שעברו כריתה מלאה או כמעט מלאה, מועמדים להשלמת טיפול באמצעות יוד רדיואקטיבי. הטיפול ניתן תוך גירוי באמצעות TSH (ראה להלן). סמוך לפני מתן היוד הרדיואקטיבי, רצוי לבדוק רמת תירוגלובולין בנסיוב לנוכח רמזים לקיומו של מתאם בין רמת תירוגלובולין בנסיוב לאחר הניתוח למידת הסיכון להישנות, וכן כייל נוגדנים לתירוגלובולין.
המינון המקובל של יוד הרדיואקטיבי (1131) הוא 100 מיליקירי (Millicurie). מינון זה ניתן בכל המקרים בהם הגידול מוגבל לבלוטת המגן. בחולים בהם אובחנה התפשטות הגידול לקישריות לימפה אזוריות מינון היוד הרדיואקטיבי המומלץ הוא 150 מיליקירי, וכאשר קיימת עדות להימצאות גרורות מרוחקות המינון המומלץ הוא 200 מיליקירי (ראה גם "נושאים שבמחלוקת").
לפני מתן המנה הטיפולית של יוד רדיואקטיבי, יש להעריך את ממדי שארית בלוטת המגן. הדבר נעשה באמצעות בדיקת קליטה במינון נמוך של יוד רדיואקטיבי או באמצעות מיפוי טכנציום. יש להימנע ממיפוי אבחנתי במינונים של 2–10 מיליקירי של 1131, כפי שהיה מקובל בעבר, בשל חשש מהימום -Stunning- ופגיעה ביעילות המנה הטיפולית של היוד הרדיואקטיבי. מטרת הבדיקה להתריע מפני מינון גבוה של יוד רדיואקטיבי כאשר קיימת שארית גדולה של בלוטת המגן לאחר הניתוח, אשר עשויה להגיב ב-Thyroiditis. כאשר מתגלה שארית גדולה, נדרש שיקול לגבי המשך טיפול, כאשר האפשרויות הן ניתוח להשלמת כריתת הבלוטה, או טיפול ביוד רדיואקטיבי בשני שלבים: מינון ראשוני נמוך (בדרך כלל כ-30 מיליקירי) שמטרתו להשמיד את שארית הבלוטה, ולאחר 6–12 חודשים, השלמת טיפול במינון של 100 מיליקירי, או יותר.
גירוי באמצעות TSH לצורך חיסול שאריות רקמת שארית הבלוטה (Ablation) באמצעות יוד רדיואקטיבי
על מנת לאפשר קליטה מיטבית של יוד רדיואקטיבי יש צורך בגירוי באמצעות ריכוזים גבוהים של TSH. מומלץ ומקובל להעלות את ריכוז TSH לרמת מטרה שמעל 30 מילי יחידות/מיליליטר. לאחר ניתוח כריתת הגידול הראשוני ניתן לנקוט בהימנעות ממתן של הטיפול בהורמון בלוטת המגן למשך 2–3 שבועות, ולכל היותר 4 שבועות (אם מסיבות לוגיסטיות הטיפול מתמהמה, ניתן להתחיל במתן מינון תחליפי של תירוקסין, ולהפסיקו כ-3 שבועות לפני מועד הטיפול המתוכנן), או להשתמש בגירוי באמצעות TSH רקומביננטי (rhTSH). שתי השיטות נמצאו יעילות במידה דומה[25][26]. הסתמנה עליה בהיקף השימוש ב-rhTSH לצורך חיסול של שארית בלוטת המגן, מכיוון שאינו מצריך להביא את המטופל למצב של תת-רמה של הורמון בלוטת המגן ולמנוע אי-נוחות הכרוכה בכך. השימוש ב-rhTSH לצורך חיסול שארית בלוטת המגן מאושר לשימוש על ידי הרשויות בארצות הברית ובאירופה, אך נכון למועד פרסום מסמך זה לא אושר בישראל, והשימוש בו מצריך אישור באמצעות טופס 29ג׳, כמוגדר בחוק. מניסיונם של חלק מחברי הוועדה ושל אחרים עולה, שהימנעות קצרה ממתן תירוקסין (3-2 שבועות) אינה כרוכה באי-נוחות משמעותית[27].[28], ועלותה נמוכה בהרבה מזו של שימוש ב-rhTSH.
השימוש ב-rhTSH לצורך הכנה לטיפול ביוד רדיואקטיבי הוא החלופה הבטוחה והעדיפה במטופלים שאינם יכולים להגיע לרמת מטרה של TSH (כגון, מחלת ההיפותלמוס או יותרת המח) או בכאלה שלגביהם קיימת חשיבות לשמור על איזון מטבולי או למנוע מצב של תת-תריסיות (Hypothyroidism) [כגון, מחלת לב קשה או גרורות באתרים קריטיים (Critical)].
- טיפול ראשון ביוד רדיואקטיבי כאשר רמת TSH בנסיוב אינה מגיעה לרמת המטרה (30 מילי יחידות/מיליליטר)
לרוב, TSH לא יגיע לרמת המטרה בשל שארית גדולה ומתפקדת של ריקמת בלוטת המגן [לעיתים נדירות, כאשר הגידול מפריש הורמוני תירואיד (Thyroid) או כאשר לחולה מחלה היפופיזרית (Hypophyseal) או היפותלמית (Hypothalamic) המפריעה להפרשת TSH]. אם, מסיבות שונות אין רצון או שלא קיימת אפשרות להשלים את הכריתה, ניתן להשמיד את שארית הבלוטה בשלבים, באמצעות יוד רדיואקטיבי במינון 30–60 מיליקירי, ובמידת הצורך השלמת הטיפול במינון של 100 מיליקירי, או יותר, כעבור 6–12 חודשים.
- מיפוי כל גופי לאחר הטיפול ביוד רדיואקטיבי
8-5 ימים לאחר מתן המנה הטיפולית של יוד רדיואקטיבי יש לבצע מיפוי כל גופי (WBS), לאיתור מוקדי קליטה יודופיליים כביטוי לקיום מחלה שאריתית קולטת יוד באזור הצוואר או מחוצה לו (גרורות מרוחקות).
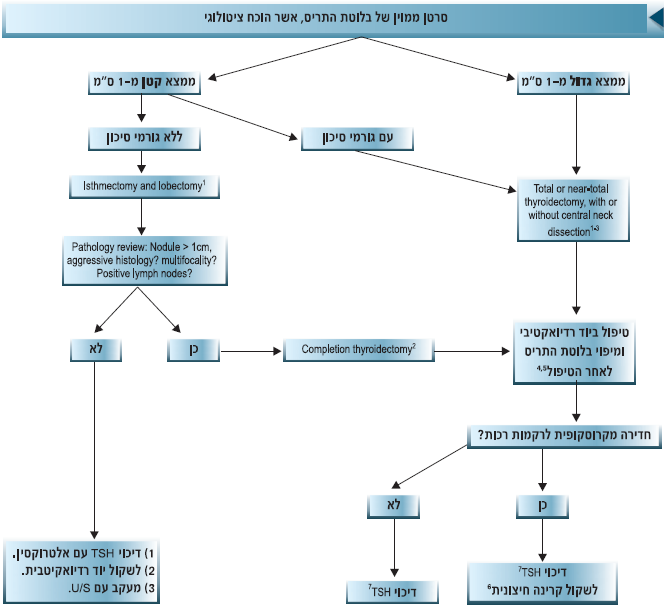
תרשים זרימה מספר 2: טיפול ראשוני בסרטן ממוין של בלוטת התריס
טיפול בקרינה חיצונית כחלק מהטיפול הראשוני בחולה
השימוש בקרינה חיצונית בחולים עם סרטן ממוין של בלוטת המגן אינו נפוץ. ניתן להשתמש באמצעי זה בחולים בהם מזוהה התפשטות מקומית נרחבת של הגידול עם חדירה לקנה ו/או לושט, לאחר טיפול ביוד רדיואקטיבי, כנזכר לעיל. יעילותם של תכשירים כימותרפיים בטיפול בסרטן ממוין של בלוטת המגן מוגבלת, והשימוש בהם מוגבל למקרים ייחודיים.
טיפול תחלפי ודיכוי TSH באמצעות תירוקסין
לאחר מתן הטיפול ביוד רדיואקטיבי, יש להתחיל בטיפול בתכשיר תירוקסין פומי. מטרת הטיפול, דיכוי רמת TSH בנסיוב לרמת מטרה הנמוכה מ-0.1 מילי יחידות/ליטר. רמת מטרה זו חיונית במיוחד בחולים בדרגת סיכון גבוהה. בחולים בדרגת סיכון נמוכה, ניתן להסתפק ברמת מטרה של TSH שבין 0.5-0.1 מילי יחידות/ליטר.
- נושאים שבמחלוקת
- מינון יוד רדיואקטיבי לצורך הטיפול הראשון שלאחר הניתוח:
קיימים דיווחים על יעילות דומה בהשוואה בין מינונים של 30 ל-100 מיליקירי. נטית חברי הוועדה לתמוך במינון של 100 מיליקירי, וביתר תוקף בחולים בגיל 45 ויותר או גיל 18 ופחות, בחולים עם גורמי סיכון סגוליים לסרטן בלוטת המגן או עם צורות היסטולוגיות הנוטות להתנהגות ביולוגית אלימה[29] - השלמת כריתה בגידולים בקוטר 1–2 סנטימטרים:
יש הגורסים שניתן לשקול, בשיתוף עם החולה, הימנעות מניתוח משלים בהיעדר גורמי סיכון נוספים, ולסלק את יתרת ריקמת הבלוטה באמצעות יוד רדיואקטיבי, ובמיוחד כאשר האבחנה הפתולוגית היא קרצינומה פוליקולרית[30] - טיפול ביוד רדיואקטיבי בחולים עם מחלה מדרגה 1 (לפי TMN):
יש הגורסים שהטיפול ביוד רדיואקטיבי בחולים בדרגת הסיכון הנמוכה אינו תורם למניעת הישנות[30]
המעקב אחר חולים עם סרטן ממוין של בלוטת המגן
מעקב אחר חולים שאובחנו כסובלים מסרטן ממוין של בלוטת המגן מתבסס על בדיקה תקופתית של תירוגלובולין בנסיוב והדמיה אולטראסונית (סונרית) של הצוואר (US). בעבר התבסס המעקב גם על מיפוי כל-גופי באמצעות יוד רדיואקטיבי, אמצעי שנמצא יעיל פחות משיטות חדשות שהוכנסו לשימוש. תירוגלובולין משמש סמן אונקולוגי רק בחולים שניתן להניח שאין בגופם שאריות של ריקמה ממקור בלוטת המגן (לאחר כריתה שלימה של בלוטת המגן וטיפול במינון גבוה של יוד רדיואקטיבי). ניתן לבדוק תירוגלובולין תוך כדי דיכוי חלקי של TSH באמצעות טיפול בתירוקסין (Tg-on), אך ניתן לשפר במידה רבה את יכולת הגילוי על ידי בדיקת תירוגלובולין על ידי גירוי באמצעות TSH, אשר מגביר את הפעילות המטבולית של תאים ממקור בלוטת המגן, ובמקביל גם את הייצור וההפרשה של תירוגלובולין. ניתן להשיג גירוי באמצעות TSH על ידי הפסקה זמנית של הטיפול בתירוקסין (Tg-off), או על ידי הזרקת TSH רקומביננטי (rhTSH). השיפור שחל בכושר ההפרדה של הבדיקה האולטראסונית והזמינות של rhTSH הרחיבה את הגמישות בגישה למעקב אחר חולי סרטן ממוין של בלוטת המגן.
קביעת דרגת הסיכון
דרגת הסיכון מכתיבה במידה רבה את אופי המעקב. השיטות השונות לקביעת רמת הסיכון (ראה מבוא) מתבססות במידה זו או אחרת על ממדי הגידול הראשוני ומידת התפשטותו, מעורבות מערכת הלימפה האחורית, קיומן של גרורות מרוחקות, גיל החולה והמיון ההיסטולוגי של הגידול. שיטות אלה נוצרו במקורן לצורך ניבוי הסיכון לתמותה בעוד שהצרכים הקליניים המעשיים מכתיבים התבססות על גורמי סיכון להישנות הגידול. לצורך התאמת המעקב והטיפול מקובל למיין את החולים לקבוצת סיכון:
קבוצת סיכון נמוך: ללא עדות לגרורות מקומיות (במיטת בלוטת המגן, בצוואר ובאיברים סמוכים: (קנה, ושט) או גרורות מרוחקות, כל מסת הגידול הנראית לעין הוסרה, ללא הסננה לכלי דם, ללא צורה היסטולוגית אלימה (ראה מבוא), קליטת יוד רדיואקטיבי במיטת בלוטת המגן בלבד במיפוי הכל גופי (WBS) אחרי הטיפול הראשון ביוד רדיואקטיבי.
קבוצת סיכון גבוה: כוללת חולים שבהם נמצא אחד או יותר מהבאים: גידול הראשוני בקוטר גדול מ-4 סנטימטרים, פלישת הגידול הראשוני לכלי דם ו/או לסביבה, היסטולוגיה אלימה יחסית (כולל קרצינומה פוליקולרית), כריתה לא-שלימה של הגידול, גרורות מקומיות או מרוחקות, קליטה מחוץ למיטת בלוטת המגן ב-WBS אחרי הטיפול הראשון ביוד רדיואקטיבי. שיוך המטופל לקבוצת סיכון עשויה להשתנות בהתאם לנסיבות ולממצאים המתגלים במהלך המעקב.
הטיפול בתירוקסין
לאחר כריתה שלימה של בלוטת המגן וטיפול ראשון ביוד רדיואקטיבי (ראה "טיפול ראשוני") כל החולים מטופלים בתירוקסין לצורך דיכוי רמת TSH .TSH הוא גורם מעודד גדילה מוכח בתאי אפיתל של בלוטת המגן וקיים ביסוס מחקרי המוכיח שיעור נמוך יותר של הישנות בחולים המטופלים במינון מדכא של תירוקסין (25). מידת הדיכוי ההתחלתית המומלצת בכל החולים היא פחות מ-0.1 מילי יחידות/ליטר, למעט אלו עם גידולים מיקרוסקופיים, בהם ניתן להסתפק במידה פחותה של דיכוי, בתחום 0.5-0.1 מילי יחידות/ליטר[14][24][31].
בדיקת תירוגלובולין
בדיקת תירוגלובולין בנסיוב תוך גירוי של TSH מומלצת לביצוע סמוך לתום השנה הראשונה שלאחר הטיפול הראשון (ניתוח ויוד רדיואקטיבי) אם רמת תירוגלובולין בזמן טיפול בתירוקסין (Tg-on) אינה גבוהה[32]. הבדיקה ניתנת לביצוע באחד משני אופנים: א. הפסקת טיפול באלטרוקסין (בדרך כלל ניתן להגיע לרמת מטרה של 30<TSH מילי יחידות/ליטר תוך 14–21 יום)[33][34][35]. ב. באמצעות הזרקה של rhTSH (37). רמת הסף לתגובה חיובית היא תירוגלובולין > 2 ננוגרם/מילילטר (לתוצאה זו רגישות של 100 אחוזים ומגולחת של כ-90 אחוזים)[32]. לא קיים הבדל מהותי בין מדדי יעילות הבדיקה המתקבלים לאחר הפסקת טיפול בתירוקסין לאלו המתקבלים באמצעות הזרקה של rhTSH [36]. גירוי באמצעות rhTSH נוח יותר לחלק מהמטופלים אך עלותו גבוהה מאד. השימוש ב-rhTSH לצורך מעקב מאושר על ידי משרד הבריאות בישראל, אך נכון למועד כתיבת מסמך זה אינו כלול בסל שירותי הבריאות, ואין אחידות במידה ההשתתפות של קופות החולים בעלות התכשיר. גירוי באמצעות rhTSH אינו האמצעי המומלץ באלו מהמטופלים שלהם הפרעות בתפקוד היפופיזרי וקושי להגיע לרמת המטרה של TSH ובמטופלים שלגביהם מעבר למצב היפותירואידי עלול לפגוע בבריאותם (כגון חולים עם מחלת לב קשה).
השיטה המעבדתית הנפוצה ביותר למדידת רמת תירוגלובולין בנסיוב, המשמשת את מרבית המעבדות בארץ, היא שיטה אימונורדיומטרית (Immunoradiometric). לשיטה זו מספר מגבלות, שחשוב להביאן בחשבון בכלל השיקולים לקביעת מצב החולה[37]:
א) הרגישות הפונקציונלית של הבדיקה (הריכוז הנמוך ביותר של החומר הנבדק שבבדיקות חוזרות מספק מקדם שונות הקטן מ-20 אחוזים) היא סביב 0.9 ננוגרם/מיליליטר, כאשר הרגישות האנליטית (הריכוז הנמוך של חומר נבדק ביותר שנקבע על ידי ערכת הבדיקה כשונה מאפס) מגיעה ל-0.2 ננוגרם/מיליליטר. המשמעות המעשית של ההבדל בין הרגישות האנליטית לרגישות הפונקציונלית היא בכך, שניתן ליחס משמעות מוגבלת להבדלים החלים ברמת תירוגלובולין בין בדיקות שתוצאתן מצויה מתחת לסף הרגישות הפונקציונלית. עם זאת, כל רמה מדידה של תירוגלובולין בריכוז שמעל לסף הרגישות האנליטית עשויה להעיד על מציאות ריקמה ממקור בלוטת המגן, ועליה עקבית, לאורך זמן, של רמת תירוגלובולין, גם אם היא בתחום שמתחת לסף הרגישות הפונקציונלית, צריכה לעורר ערנות לאפשרות של הישנות פעילה
ב) קיימת שונות ניכרת בין התוצאות המתקבלות על ידי ערכות בדיקה שונות. על מנת להקטין את השונות, רצוי שבדיקת תירוגלובולין תערך באמצעות ערכה שהותאמה לתקנים עדכניים (457-CRM) ותלווה, במקביל, בבדיקה לנוכחות נוגדנים כנגד תירוגלובולין (ראה להלן). כמו כן, רצוי שהמעקב לאורך זמן בחולה נתון יעשה באותה מעבדה ובאמצעות ערכה זהה
ג) נוכחותם של נוגדנים בנסיוב כנגד תירוגלובולין (Anti-Tg antibodies) עלולה להפריע למדידת רמת תירוגלובולין (בבדיקות הרדיומטריות נוכחות נוגדנים גורמת, בדרך כלל, לקריאה נמוכה יותר של רמת תירוגלובולין, כלומר מקטינה את רגישות הבדיקה). (ראה להלן המלצה לגישה לחולה עם כייל גבוה של נוגדנים בנסיוב כנגד תירוגלובולין). ערכות שונות לבדיקת נוגדנים כנגד תירוגלובולין עשויות להגיב באופן שונה לנוכחות נוגדנים כנגד תירוגלובולין בחולה נתון [ככל הנראה בגלל הטרוגניות מבנית שקיימת בין נוגדנים כנגד תירוגלובולין, ומסגוליות שונה של ערמת בדיקה שונות כלפי האפיטופים הדומיננטיים (Dominant epitopes) בנוגדנים אלו][38]. לכן, יש להביא בחשבון, שכייל שלילי לנוכחות נוגדים כנגד תירוגלובולין אינו שולל לחלוטין נוכחות הנוגדנים, ועם כל זאת, בדיקות ניצולת (recovery) של תירוגלובולין בערכה, אינן מומלצות[37].
בדיקת סונר (US) של הצוואר
בדיקת סונר של הצוואר נמצאה יעילה מאד לצורך איתור מסות גידוליות בצוואר, לרבות בקשריות לימפה (המאפיינים הסונוגרפיים של קשריות מוסננות פורטו בפרק האיבחון).
רצוי לבצע את מדידת תירוגלובולין תוך גירוי TSH ואת בדיקת הסונר של הצוואר במקביל, סמוך לתום השנה הראשונה שלאחר הטיפול הראשוני. ההערכה המשולבת של הבדיקה הסונרית ותירוגלובולין תוך גירוי TSH מקנה רגישות של כ-95 אחוזים וערך ניבוי שלילי שנושק ל-100 אחוזים[39]. הדיוק האבחנתי של בדיקת US תלויה במידה רבה מאד בניסיונו ובמיומנותו של הבודק, ואין להקיש בהכרח מהממצאים בספרות הרפואית לגבי התוצאות בחיי היומיום. על מנת להגיע ליעילות מיטבית, הבדיקה והפיענוח צריכים להעשות בו זמנית, על ידי רופא שמיומן בבדיקה.
מיפוי כל גופי ביוד רדיואקטיבי (WBS)
הרגישות האבחנתית הגבוהה של שילוב של בדיקת תירוגלובולין תחת גרוי TSH ו-US של הצוואר עולה במידה רבה על זו של המיפוי הכל גופי ומייתרת אותו[40][41][42]. הרגישות האבחנתית של WBS במינון נמוך (4-2 מיליקירי) של 1131, נמוכה גם בהשוואה למיפוי כל גופי לאחר מינון טיפולי[43]. עם זאת, יש להקפיד לבצע מיפוי כל גופי בטווח של 5–10 ימים אחרי כל מתן של מנה טיפולית של יוד רדיואקטיבי.
רמה גבולית גבוהה של תירוגלובולין (10-2 ננוגרם/מילילטר) לאחר גירוי TSH
רמת סף של תירוגלובולין בנסיוב בגובה 2 ננוגרם/מילילטר אינה מהווה, כשלעצמה, התוויה לטיפול חוזר ביוד רדיואקטיבי, שכן במספר לא מבוטל של מטופלים עם רמת תירוגלובולין בנסיוב שבין 2–10 ננוגרם/מילילטר לא ניתן לאתר גידול פעיל (בחלקם רמת תירוגלובולין יורדת עצמונית במהלך המעקב, בדרך כלל תוך שנתיים לאחר הטיפול הראשוני). יש להתייחס למגמה עקבית של עליה ברמת תירוגלובולין בהתוויה אפשרית לטיפול ביוד רדיואקטיבי[40].
במטופלים המוגדרים ברמת סיכון גבוהה ועם תירוגלובולין גבולי גבוה, קיימת התוויה לטיפול חוזר ביוד רדיואקטיבי. אין לבצע מיפוי כל גופי מקדים במקרים אלו בגלל רגישותו הנמוכה בהשוואה למיפוי כל גופי לאחר טיפול ובגלל חשש מהימום (Stunning) של תאי הגידול כתוצאה מחשיפה מוקדמת ליוד רדיואקטיבי[24][32].
רמת תירוגלובולין גבוהה מ-10 ננוגרם/מילילטר מהווה התוויה לטיפול חוזר ביוד רדיואקטיבי, גם בהיעדר עדות הדמייתית לשארית גידול. מיפוי כל גופי לאחר הטיפול עשוי לסייע באיתור שארית הגידול. אם שארית הגידול נותרת בעינה לאחר הטיפול ביוד רדיואקטיבי ואם אינה ניתנת להסרה ניתוחית, יש לחזור על טיפול ביוד רדיואקטיבי עד להשמדת הגידול או עד שיחדל להגיב לטיפול[32][44]
45). בקביעת ההתויה למינון מצטבר גבוה של יוד רדיואקטיבי, יש לשקול את יחס התועלת של טיפול ביוד רדיואקטיבי (בעיקר במינון מצטבר שמעל 600 מיליקירי) אל מול תופעות לוואי של הטיפול ביוד רדיואקטיבי, שכוללות עליה תלוית-מינון בסיכון להופעה של ממאירות ראשונית נוספת, קסרוסטומיה, ויובש לחמיות[45][46].
שארית גידול שאינו קולט יוד רדיואקטיבי
גידולים מאבדים לעיתים את הכושר לרכז יוד ובמקביל עולה הפעילות המטבולית המתבטאת בעלייה בניצול גלוקוזה (Glucose). בחולים עם תירוגלובולין גבוה ללא עדות לקליטת יוד רדיואקטיבי במיפוי כל גופי, רצוי לבצע בדיקת PET-CT באמצעות deoxyglucose־FDG) F18). ניתן לשפר את רגישות בדיקת PET-CT על ידי גירוי באמצעות TSH (הפסקה זמנית של טיפול בתירוקסין או מתן rhTSH[47][48].
המעקב והטיפול בתירוקסין בטווח הארוך
במטופלים ברמת סיכון נמוכה ניתן לעקוב בתדירות של אחת ל-6 חודשים, ובהמשך אחת לשנה. המעקב יכלול בדיקת TSH, תירוגלובולין בנסיוב תוך דיכוי (Tg-on) וכייל נוגדנים כנגד תירוגלובולין.
קיים מתאם בין דיכוי ממושך של TSH להופעה של הפרעות-קצב לב על-חדריות, החמרה של מחלת לב איסכמית וירידה במסת העצם. רמת המטרה של TSH במטופלים ברמת סיכון נמוכה היא 0.5-0.1 מילי יחידות/ליטר. במטופלים ברמת סיכון גבוהה, רמת המטרה נמוכה מ-0.1 מילי יחידות/ליטר, למשך 3–5 שנים אחרי השגת הפוגה (העדר עדות לקיום שארית גידול), אך יש להימנע מהופעת סימנים קליניים של תירוטוקסיקוזיס (רמת FT4 צפויה להיות גבוהה במקצת במי שמטופלים בתירוקסין בכדורים. רמת T3 צריכה להישמר בתחום התקין)[14][24][31].
מקרים "מיוחדים"
- נוכחות כייל חיובי של נוגדנים כנגד תירוגלובולין
כאמור לעיל, נוגדנים כנגד תירוגלובולין מפריעים לקביעת רמת תירוגלובולין בנסיוב. כאשר שיטת הבדיקה של תירוגלובולין היא אימונורדיומטרית (המקובלת במרבית המעבדות בארץ), נוכחות נוגדנים גורמת לקריאה נמוכה שגוייה של רמת תירוגלובולין (בשיטת רדיואימונואסיי הנוגדנים גורמים בדרך כלל לקריאה גבוהה שגויה). בנוכחות נוגדנים כנגד תירוגלובולין ניתן לבסס את המעקב על US של הצוואר ומיפוי כל גופי עם יוד רדיואקטיבי (ובמקרים נבחרים, PET-CT). מיל חיובי קבוע של נוגדנים כנגד תירוגלובולין עלול, כשלעצמו, להוות סמן בלתי תלוי לנוכחות שארית גידול. בהיעדר שארית ריקמת ממקור בלוטת המגן (ריקמה תקינה או גידולית), המיל קטן בהדרגה עד להעלמות, תוך כשנתיים מהטיפול הראשוני[49].
- למטופל עם תולדות של קשר קטן מ-1 ס"מ שטופל בכריתה חלקית של בלוטת המגן, ללא טיפול ביוד רדיואקטיבי
ניתן טיפול בתירוקסין (רמת מטרה 0.5-0.1 מילי יחידות/ליטר). מעקב באמצעות us של הצוואר בלבד. השלמת כריתת בלוטת המגן כאשר מתעורר חשד להישנות גידול בבלוטת המגן[14][24][31].
- נושאים שבמחלוקת
- תדירות ואופי המעקב: לא קיימת הסכמה בספרות לגבי משך, תדירות ואופי המעקב (ביצוע בדיקות חוזרות של תירוגלובולין תחת גירוי, US) של מטופלים ברמת סיכון נמוכה וללא עדות להישנות. ככלל מעקב ממושך וצמוד משפר את סיכויי ההישרדות. עם זאת, במטופלים ברמת סיכון נמוכה ועל בסיס פרטני, ייתכן שניתן להסתפק במרווחי מעקב גדולים מבלי לפגוע בסיטייהם. לדעת חברי הוועדה, לנוכח העובדה שהישנויות עלולות להתגלות גם בטווח של שנים רבות לאחר טיפול ראשוני שהוגדר "מוצלח", רצוי לשמר, ללא הגבלת זמן, תדירות מסוימת של מעקב (אחת לשנה-שנתיים) גם בחולים שלכאורה נקיים מגידול. לא קיימת הסכמה בספרות לגבי הצורך לחזור על בדיקת תירוגלובולין תחת גירוי TSH, מעבר לבדיקה המבוצעת סמוך לתום השנה הראשונה שלאחר הטיפול הראשוני, במטופלים שבהם לא נמצא ריכוז מדיד של תירוגלובולין בבדיקה תוך גירוי בתום השנה הראשונה. מחקר שפורסם ב-2008 מרמז שהתועלת בבדיקות חוזרות קטנה במקרים בהם הבדיקה הראשונה העלתה ממצאים שליליים[50]
- רמה גבולית-גבוהה של תירוגלובולין בנסיוב במטופלים המוגדרים ברמת סיכון נמוכה: לכאורה, רמת תירוגלובולין גבולית-גבוהה עשויה להצביע על נוכחות שארית גידול או הישנות ומכת זה לשנות את הערכת דרגת הסיכון של המטופל. מאידך גיסא, במקרים רבים רמת תירוגלובולין יורדת עצמונית במשך הזמן. הגישות האפשריות כוללות מעקב צמוד וחזרה על טיפול ביוד רדיואקטיבי לנוכח המשך עלית רמת תירוגלובולין או טיפול מיידי ביוד רדיואקטיבי וסיווג מחודש של רמת הסיכון על-פי תוצאות המיפוי הכל-גופי שלאחר הטיפול
- המינון המצטבר המרבי האפשרי של יוד רדיואקטיבי: לא קיימת הסכמה באשר למגבלה במינון המצטבר המרבי של יוד רדיואקטיבי. יש לתת את הדעת לכך שמעונים גבוהים של יוד רדיואקטיבי כרוכים בתופעות לוואי (יובש רירית הפה והלחמיות) ובעליה אפשרית בסיכון להופעת ממאירות ראשונית נוספת[10][11][46]
- שיפור דרגת התמיינותם של גידולים שאינם קולטים יוד, באמצעות רטינואידים: לא קיימת אחידות דעים בקשר לתועלת הקלינית בניסיון לשפר את דרגת התמיינותם של גידולים שאינם קולטים יוד, באמצעות רטינואידים (Cis-Retinoicacid, Roaccutane-13)[51]
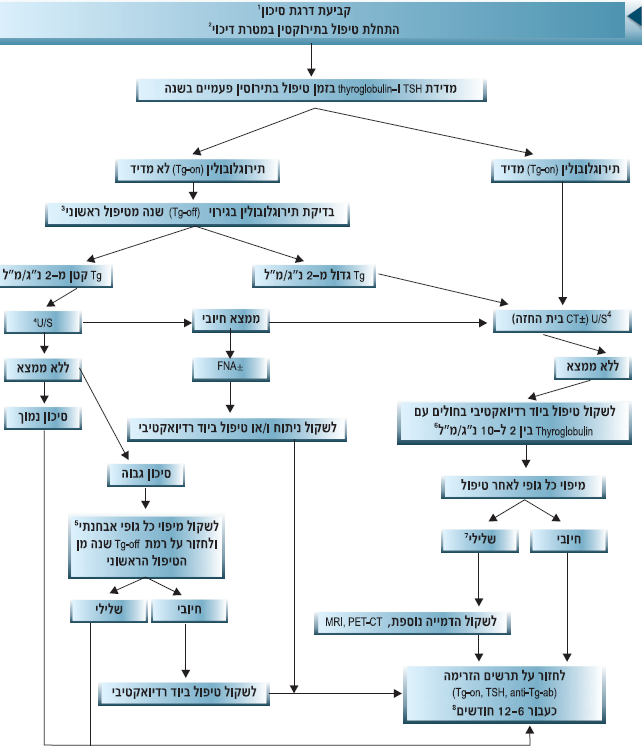
תרשים זרימה מספר 3: מעקב ארוך טווח אחר חולה עם סרטן ממוין של בלוטת התריס
טיפול בהישנות של סרטן ממוין של בלוטת המגן
מרבית ההישנויות של סרטן ממוין של בלוטת המגן הן מקומיות בצוואר. ההארעות של גרורות מרוחקות נעה בין 5–20 אחוזים מהחולים, והן מאותתת בעיקר בריאות ובשלה איבחון מוקדם של הישנות סרטן בלוטת המגן עשוי להוביל להחלמה או להארכה משמעותית של השרידות, בעיקר כאשר הממצא נתיח או קולט יוד רדיואקטיבי. בחולים עם הישנות בצוואר ניתן להגיע להפוגה ב-2/3 מהמקרים ובחולים עם גרורות מרוחקות בכ-1/3 מהמקרים. שיעורים גבוהים של הפוגה מושגים במתאם הפוך לממדי המסה הגידולית[52][53][54][55].
העיקרון המנחה בטיפול בהישנות סרטן ממוין של בלוטת המגן הוא כריתה כירורגית של מסות משמעותיות, או כאלה המאיימות על איברים חיוניים, השלמת טיפול באמצעות יוד רדיואקטיבי ובמקרים מיוחדים קרינה חיצונית ו/או טיפול כימותרפי. בתום כל סדרת טיפול, חוזרים לשיגרת מעקב באמצעות תירוגלובולין בנסיוב ואמצעי הדמיה המותאמים לאתרי הפיזור הגרורתי בחולה הנתון (ראו "המעקב אחר חולים עם סרטן ממוין של בלוטת המגן").
הישנות מקומית במיטת בלוטת המגן או בצוואר
הטיפול המומלץ בחולה עם הישנות המאותרת למיטת בלוטת המגן או לקשריות לימפה צוואריות, הוא כריתה ניתוחית של המסה הגידולית ו/או של קשריות הלימפה הנגועות. התפשטות הגידול והסתננותו לאיברי הצוואר עשויה להצריך כריתה של הקנה או הושט. קישריות לימפה נגועות המזוהות בבדיקה סונרית (US) ניתן לסמן סמוך לניתוח באמצעות מחטי עיגון (Hook needles). לאחר הניתוח יש לשקול טיפול חוזר במינון גבוה של יוד רדיואקטיבי.
גרורות בריאות
גרורות בריאות מופיעות לרוב בפיזור מיליארי, רב-מוקדי, והטיפול הנבחר הוא באמצעות יוד רדיואקטיבי. במקרים נדירים יחסית, שבהם מתגלה גרורה ריאתית בודדת, או כאשר גרורה ריאתית אחת גדלה במהירות, בשעה שגרורות אחרות יציבות, ניתן לשקול כריתה ניתוחית[52][53][54][55]. בטיפול בגדורות מפוזרות בריאות יש להביא בחשבון סיכון של לייפת (פיברוזיס, Fibrosis) ריאתית ולתכנן את מינון היוד בהתאם.
גרורות במדיאסטינום
הטיפול בגדורות במדיאסטינום הוא באמצעות ניתוח ו/או יוד רדיואקטיבי. ניתן לטפל באמצעות קרינה חיצונית בגדורות שאינן קולטות יוד ואינן זמינות לכריתה ניתוחית.
גרורות בשלד
הטיפול בגדורות בשלד חייב להינתן במרכז המשלב את דיסציפלינות השונות שעשויות לקחת חלק בטיפול. הטיפול הראשוני בגדורות בשלד הוא באמצעות יוד רדיואקטיבי. יש לשקול כריתה ניתוחית של גרורות בעצמות הארוכות או באגן, כאשר נפחן גדול וקיים סיכון לשבר פתולוגי ו/או כאשר הגרורות אינן קולטות יוד רדיואקטיבי וקיימת גישה ניתוחית נוחה. ניתן לטפל באמצעות קרינה חיצונית בגדורות שאינן קולטות יוד ואינן זמינות לכריתה ניתוחית[56][57][58][33]. כאשר נבחר טיפול משולב, סדר הטיפולים (קרינה, ניתוח, יוד רדיואקטיבי) נקבע בבכל מקרה לגופו, על פי הנסיבות הפרטניות.
- גרורות בעמוד השדרה
כאשר גרורות של סרטן ממוין של בלוטת המגן בחוליות עמוד השדרה מאיימות על חוט השדרה, יש לשקול כריתה כירורגית, עם או בלי אמבוליזציה מקדימה. ניתן לטפל באמצעות קרינה חיצונית בגדורות שאינן קולטות יוד ואינן זמינות לכריתה ניתוחית. יש מקום לשקול טיפול במינון גבוה של גלוקוקורטיקואידים במקרים בהם קיימת אפשרות של לחץ על חוט השדרה כתוצאה מבצקת סביב הגרורות.
- טיפול בביפוספונטים
ביפוספונטים, בדרך כלל במתן תוך-ורידי, עשויים להקל על כאב הנגרם בגלל גרורות בשלד, שאינן מגיבות לטיפול ביוד רדיואקטיבי[56][57][58][33][59]. הניסיון במחלות ממאירות אחרות מראה, שטיפול בביפוספונטים (Bisphosphonates) עשוי להקטין הופעה של גרורות בשלד ולהגביל התפתחותן של גרורות קיימות.
גרורות במח
כריתה ניתוחית אפשרית במקרים נדירים של גרורות בודדות במת. ניתן לטפל באמצעות קרינה חיצונית בגדורות שאינן קולטות יוד ואינן זמינות לכריתה ניתוחית[60]. יש מקום לשקול טיפול במינון גבוה של גלוקוקורטיקואידים במקרים בהם קיימת אפשרות של נזק נוירולוגי כתוצאה מבצקת סביב הגרורות.
טיפול ביוד רדיואקטיבי
הטיפול המקובל בגדורות של סרטן ממוין של בלוטת המגן שאינן נגישות לטיפול כירורגי הוא באמצעות מינון גבוה של יוד רדיואקטיבי (1131). לא מומלץ לבצע מיפוי במינון אבחנתי של 1131 לפני מתן הטיפול ביוד רדיואקטיבי. המיפוי באמצעות מינון אבחנתי (נמוך יחסית) של יוד רדיואקטיבי אינו רגיש דיו לזיהוי כל מוקדי הגרורות והוא עלול להפחית את קליטת היוד הרדיואקטיבי בשלב הטיפול (כתוצאה מ-Tumor stunning).
מיפוי כל-גופי (WBS) המבוצע 4–10 ימים לאחר מתן הטיפול ביוד רדיואקטיבי מספק מידע על היקף המחלה, על תגובה לטיפול קודם (הישארות או העלמות מוקדי מחלה קודמים) וכושר קליטת היוד של הגרורות (נתון הנשקל לצורך החלטה על טיפולים נוספים).
ניתן לגרום לעלייה ברמת ה-TSH מעל 30milli-International Units/Litre באמצעות הפסקת הטיפול בהורמון בלוטת המגן למשך כ-3 שבועות. הנתונים לגבי שימוש ב-rhTSH לצורך טיפול בגדורות עדיין מצומצמים[61]), והשימוש rhTSHo לצורך טיפול בגדורות לא אושר עדיין לאינדיקציה (Indication) הזו. אי-לכך, עד לפרסום נתונים המוכיחים את יעילות הגישה, אין להמליץ על שימוש ב-rhTSH לצורך הכנה לטיפול ביוד רדיואקטיבי בחולים עם גרורות, למעט מקרים בהם לא קיימת חלופה בטוחה אחרת: מטופלים שלהם הפרעות בתפקוד היפופיזרי וקושי להגיע לרמת המטרה של TSH ומטופלים בהם מעבר למצב היפותירואידי עלול לפגוע בבריאותם (כגון חולים עם מחלת לב קשה).
- מינון הטיפול ביוד רדיואקטיבי (1131)
- המינון המומלץ לטיפול בהישנות מקומית בצוואר ו/או גרורות בבלוטות לימפה צוואריות שאינן ניתנות לכריתה כירורגית (או לאחר כריתה כירורגית) הוא 150 - 200 מיליקירי [7.4-5.5 GBq (Gigabecquerel)]. ישנם מרכזים, לא רבים, בעולם שבהם ניתנים מינונים גבוהים יותר לאחר דוסימטריה, לצורך אבטחת הגבלת מינון הקרינה ללשד העצם ולרקמת הריאה
- בחולים עם גרורות מרוחקות, המינון המומלץ של יוד רדיואקטיבי הוא 200 מיליקירי (7.4 GBq). ניתן לחזור על הטיפול ביוד רדיואקטיבי כעבור 4–6 חודשים או יותר, על פי הערכה קלינית לתגובה לטיפול קודם ועל-פי קצב התקדמות המחלה. לא נקבעה תקרת מינון מרבי מצטבר שניתן לתת במקרים של הישנות וההחלטה על הגדלת המינון המצטבר צריכה להתבסס על הערכת קצב התקדמות המחלה, יעילותם של טיפולים קודמים ביוד רדיואקטיבי, אלטרנטיבות טיפוליות ותשומת לב לתופעות לוואי כתוצאה ממיגון מצטבר גבוה של יוד רדיואקטיבי, כולל אפשרות של עליה בהארעות ממאירויות ראשוניות נוספות[46]. במקרים של פיזור גרורתי נרחב בריאות, יש לתת את הדעת לסיכון אפשרי של לייפת (פיברוזיס) ריאתית בעקבות טיפול במינון גבוה של יוד רדיואקטיבי, ויש לתכנן את מינון היוד הרדיואקטיבי, על-מנת למנוע נזקי קרינה לריקמה ריאתית תקינה
טיפול בקרינה חיצונית (External-beam irradiation)
הטיפול בקרינה חיצונית ניתן לעיתים רחוקות יחסית בחולים עם סרטן ממוין של בלוטת המגן. הטיפול עשוי להפחית, ככל הנראה, הישנות מקומית בחולים עם סיכון גבוה להישנות בגלל מחלה שיורית בצוואר, כאשר טיפול ניתוחי נוסף אינו אפשרי. יש לתכנן את הטיפול בקפידה, תוך שימוש ב-D-3 Conformal planning techniques על מנת למנוע מיילופתיה (Myelopathy) כתוצאה מחשיפה לקרינה של חוט השדרה. הטיפול בקרינה חיצונית אינו בא במקום טיפול ביוד רדיואקטיבי, ובדרך כלל מתווסף אליו.
- התוויות לטיפול בקרינה חיצונית
- גידולים שאינם ניתנים לכריתה כירורגית ושאינם קולטים יוד רדיואקטיבי
- שארית ניכרת של גידול ועדות ברורה להתפשטות מקומית ניכרת בצוואר בזמן ניתוח, בעיקר כאשר הגידול אינו קולט יוד רדיואקטיבי[62][63]
- טיפול משכך (פליאטיבי, Palliative) בגדורות בלתי-נתיחות בשלד, במדיאסטינום, במוח, בעמוד השדרה ובאתרים אחרים
כימותרפיה משככת (פליאטיבית)
הטיפול הכמותרפי אינו נחוץ ואינו יעיל במרבית החולים. הוא ניתן כמפלט אחרון ובררני לחולים עם מחלה סופנית, סימפטומטית, שאינה ניתנת לשליטה באמצעות ניתוח, יוד רדיואקטיבי או קרינה חיצונית. שימוש בשילובים המקובלים, הכוללים Doxorubicin ו-Cisplatin, מקנים תגובה חלקית ב-10–20 אחוזים מהמטופלים[64][65][66][67][68].
טיפול משכך (פליאטיבי)
הטיפול נחוץ בקבוצה קטנה מאוד של חולים, עם מחלה חוזרת, סופנית. הטיפול כולל שיכוך כאבים יעיל (שילוב של תרופות וטיפול קרינתי לגרורות לשלד), טיפול בסטרידור וחרדת חנק באמצעות טיפול תרופתי או טיפול כירורגי פליאטיבי (פיום קנה). השיטות לטיפול משכך מותאמות באופן פרטני, בהתאם לנסיבות.
- נושאים שבמחלוקת
- טיפול בליתיום קרבונאט (Lithium carbonate) לפני טיפול ביוד רדיואקטיבי: לא קיימת הסכמה בספרות לגבי היעילות של הטיפול בליתיום קרבונאט (שנועד לעכב את שיחדור היוד מהתאים ולהגביר את יעילות הטיפול ביוד רדיואקטיבי) במקרים של הישנויות שאינן קולטות יוד או שקולטות יוד ביעילות נמוכה[69]
- רה-דיפרנציאציה (Redifferentiation) באמצעות רטינואידים: לא קיימת אחידות דעים בספרות בקשר לתועלת הקלינית בניסיון לשפר את דרגת התמיינותם של גידולים שאינם קולטים יוד, באמצעות רטינואידים (Cis-Retinoicacid, Roaccutane-13)[51][70]
- סדר הטיפול בטיפולים משולבים: לא קיימת הסכמה בספרות לגבי סדר הטיפולים, יוד לפני קרינה חיצונית, או להפך. הרושם שהתקבל מסקירת הספרות הוא, שבמקרים בהם הוחלט על טיפול משולב, יוד רדיואקטיבי וקרינה חיצונית, מתן היוד הרדיואקטיבי קודם לקרינה החיצונית
נספח - המלצת יושבי ראש איגוד רופאי אף אוזן גרון והאיגוד הכירורגי לבי הרחבת הניתוח למדורי בלוטת הלימפה
בסרטן ממוין של בלוטת המגן שבהם קיימת מחלה גרורתית בבלוטות לימפה צוואריות יש לבצע ביתור (דיסקציה) צווארי סלקטיבי על מנת לכרות את בלוטות הלימפה הנגועות ואת אלה שבסיכון.
כאשר קיימת מחלה גרורתית בצוואר הקידמי, הפאראטראכאלי (Paratracheal), יש לבצע ביתור צווארי פאראטראכאלי/פרהטראכאלי (Pretracheal) (אזור מספר VI), שגבולו העליון - עצם הלשון, וגבולו התחתון - הכניסה למיצר (מדיאסטינום, Mediastinum), גבולותיו הצדדיים של אזור זה הם עורקי הקרוטיס (Carotid) דו-צידית.
כאשר קיימת מחלה גרורתית בצוואר הצידי (תחנות IV-II) יש לבצע כריתה צווארית הכוללת את שלושת האזורים הללו כמקשה אחת Antero-lateral neck dissection או (Selective neck dissection of levels II-IV), תוך שמירה על הוריד היוגולרי (Jugular), עורק הקרוטיס, הפלקסוס הבראכיאלי (Brachial plexus), עצבי גולגולת XII-X ועצב הפרניקוס (Phrenic) לשריר מפנה הראש.
כאשר קיימת מחלה גרורתית בצוואר האחורי (תחנה V). הכריתה צריכה לכלול גם את התחנה הנזכרת מעלה בנוסף ל-3 התחנות היוגולריות שצויינו (Selective neck dissection II-V).
האזור התת לסתי (Level I) מעורב במקרים נדירים על ידי סרטן גרורתי ממקור בלוטת המגן ולכן הוא איננו נכלל בדרך כלל בכריתה הצווארית.
לא מומלצת כריתה של בלוטות בודדות העועות במחלה גרורתית ממקור בלוטת המגן(Berry picking). טכניקה זו איננה מקובלת כיום בטיפול הניתוחי בסרטן גרורתי ממוין של בלוטת המגן.
הכנה לטיפול ביוד רדיואקטיבי
מתן יוד רדיואקטיבי מצריך היערכות הכוללת הזמנת החומר ואספקתו, תשומת-לב למגבלות באשר לכמות החומר הרדיואקטיבי המוזמן ושיריון של חדר-בידוד, למשך מספר שעות עד מספר ימים. במציאות הקיימת, נוצר לעיתים קרובות מצב, בו לא ניתן לטפל ביוד רדיואקטיבי בטווח של שבועות ספורים לאחר הניתוח. במקרה שכזה, יש להתחיל טיפול בתירוקסין, במינון תחליפי, או ציטומל (Cytomel) (Liothyronine) (T3).
לקראת טיפול ביוד רדיואקטיבי יש להפסיק את הטיפול בתירוקסין (או ציטומל) (בדרך כלל ניתן להסתפק ב-3-2 שבועות הפסקה על-מנת להשיג רמת מטרה של TSH של 30 מילי יחידות/ליטר ויותר) [28],[35]. במקביל להפסקת הטיפול בתירוקסין, רצוי להגביל את צריכת היוד באמצעות תזונה דלת יוד [הגבלת מוצרי חלב, מולטיוויטמינים (Multivitamins), ביצים, מלח מועשר ביוד, תכשירים של אצות-ים, פיחת ים, דגי-ים, מוצרי סויה, מוצרים המכילים צבע מאכל אדום, תפוחי-אדמה שאינם קלופים]. במידה שהטיפול ביוד רדיואקטיבי ניתן תוך גירוי באמצעות TSH רקומביננטי, אין צורך להפסיק טיפול בהורמוני תירואיד. עם זאת, יש להקפיד על תזונה דלת יוד.
הנחיות משרד הבריאות קובעות, שהבידור המתחייב לאחר טיפול במינון גבוה של יוד רדיואקטיבי יכול להתבצע בביתו של המטופל אם קיימים תנאים המאפשרים זאת. יש לברר מראש באם התנאים בביתו של המטופל מאפשרים בידוד ביתי על פי ההנחיות, בתיאום עם היחידה האחראית על בטיחות קרינה.
לפני טיפול ביוד רדיואקטיבי יש לוודא ספירת דם תקינה ותקינות התפקוד הכליתי. ליקוי בתפקוד הכליתי מחייב הפחתת מינון היוד הרדיואקטיבי (אשר מתפנה ברובו באמצעות הכליות). בגברים, מינון מצטבר גבוה של יוד רדיואקטיבי עלול לגרום לירידה, לפחות זמנית, בספירת הזרע. כאשר נושא הפוריות עומד על הפרק וצפוי מינון מצטבר של יוד רדיואקטיבי שמעל 200 מיליקירי (22.2 GBq), רצוי להעלות לדיון אפשרות של הקפאת זרע.
המלצות
- קביעת תבנית לתשובת פיענוח בדיקה סונרית של בלוטת המגן, עם התייחסות פרטנית לפרמטרים היכולים לסייע להגדרת מידת הסיכון לממאירות
- קביעת תבנית לתשובת פיענוח ממצאים ציטולוגיים של קשרים של בלוטת המגן
- הכשרת רופאים הנוטלים חלק מרכזי באבחון ומעקב של מטופלים עם קשרים בבלוטת המגן בשימוש במכשירי US, בפיענוח בדיקות ובביצוע דיקורים בהנחיה סונרית. הטמעת מכשירי US כחלק מהסטנדרד הטיפולי במרפאות המטפלות בחולים עם קשרים בבלוטת המגן (בדומה לשימוש שנעשה בבדיקה על-קולית על ידי מיילדים ורופאי נשים)
- הכללה בסל השירותים של מתן rhTSH לצורך אבחנה וטיפול ביוד רדיואקטיבי [44] למטופלים שאינם יכולים להגיע לרמת מטרה של TSH [כגון, מחלת ההיפותלמוס (Hypothalamus) או יותרת המח] וכאלה שלגביהם קיימת חשיבות לשמור על אחון מטבולי (Metabolic) או למנוע מצב של תת-תריסיות (כגון, במטופלים עם מחלת לב קשה או גרורות באתרים קריטיים)
ביבליוגרפיה
- ↑ Lubina A, Cohen 0, Barchana M et al. Time trends of incidence rates of thyroid cancer in Israel: what might explain the sharp increase. Thyroid. 2006; 16: 1033-1040
- ↑ Guidelines for the management of thyroid cancer in adults. 2002
- ↑ Benbassat CA, Mechlis-Frish S, Hirsch D. Clinicopathological characteristics and long-term outcome in patients with distant metastases from differentiated thyroid cancer. World J Surg. 2006; 30: 1088-1095
- ↑ 4.0 4.1 4.2 Mazzaferri EL, Jhiang SM. Long-term impact of initial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med. 1994; 97: 418-428
- ↑ 5.0 5.1 Davies L, Welch HG. Increasing incidence of thyroid cancer in the United States, 1973-2002. JAMA 2006; 295: 2164-2167
- ↑ Trimboli P, Ulisse S, Graziano FM et al. Trend in thyroid carcinoma size, age at diagnosis, and histology in a retrospective study of 500 cases diagnosed over 20 years. Thyroid. 2006; 16: 1151¬1155
- ↑ GPacini F, De Groot LJ. Thyroid cancer. Thyroid disease manager
- ↑ Fagin JA. Familial nonmedullaiy thyroid carcinoma-the case for genetic susceptibility. J Clin Endocrinol Metab. 1997; 82: 342-344
- ↑ Malchoff CD, Malchoff DM. Familial papillary thyroid carcinoma. Cancer Treat Res. 2004; 122: 381-387
- ↑ 10.0 10.1 Bhattachaiyya N, Chien W. Risk of second primary malignancy after radioactive iodine treatment for differentiated thyroid carcinoma. Ann Otol Rhinol Laryngol. 2006; 115: 607-610
- ↑ 11.0 11.1 Verkooijen RB, Smit JW, Romijn JA, Stokkel MP. The incidence of second primary tumors in thyroid cancer patients is increased, but not related to treatment of thyroid cancer. Eur J Endocrinol. 2006; 155: 801-806
- ↑ 12.0 12.1 Frates MC, Benson CB, Doubilet PM et al. Prevalence and distribution of carcinoma in patients with solitary and multiple thyroid nodules on sonography. J Clin Endocrinol Metab. 2006; 91:3411-3417
- ↑ Shaha AR. TNM classification of thyroid carcinoma. World J Surg. 2007; 31: 879-887
- ↑ 14.0 14.1 14.2 14.3 14.4 14.5 14.6 Cooper DS, Doherty GM, Haugen BR et al. Management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2006; 16: 109-142
- ↑ Tan GH, Gharib H. Thyroid incidentalomas: management approaches to nonpalpable nodules discovered incidentally on thyroid imaging. Ann Intern Med. 1997; 126: 226-231
- ↑ Kovacs GL, Gonda G, Vadasz G et al. Epidemiology of thyroid microcarcinoma found in autopsy series conducted in areas of different iodine intake. Thyroid. 2005; 15: 152-157
- ↑ 17.0 17.1 Frates MC, Benson CB, Charboneau JW et al. Management of thyroid nodules detected at US: Society of Radiologists in Ultrasound consensus conference statement. Radiology. 2005; 237: 794¬800
- ↑ Nam SY, Roh JL, Kim JS, Lee JH, Choi SH, Kim SY. Focal uptake of (18)F-fluorodeoxyglucose by thyroid in patients with nonthyroidal head and neck cancers. Clin Endocrinol (Oxf). 2007; 67: 135¬139
- ↑ Liel Y. The yield of adequate and conclusive fine-needle aspiration results in thyroid nodules is uniform across functional and goiter types. Thyroid. 1999; 9: 25-28
- ↑ Elisei R, Bottici V, Luchetti F et al. Impact of routine measurement of serum calcitonin on the diagnosis and outcome of medullary thyroid cancen experience in 10,864 patients with nodular thyroid disorders. J Clin Endocrinol Metab. 2004; 89: 163-168
- ↑ Reschini E, Ferrari C, Castellani M et al. The trapping-only nodules of the thyroid gland: prevalence study. Thyroid. 2006; 16: 757-762
- ↑ Carmeci C, Jeffrey RB, McDougall IR, Nowels KW, Weigel RJ. Ultrasound-guided fine-needle aspiration biopsy of thyroid masses. Thyroid. 1998; 8: 283-289
- ↑ Cooper DS. Thyroxine suppression therapy for benign nodular disease. J Clin Endocrinol Metab. 1995; 80: 331-334
- ↑ 24.0 24.1 24.2 24.3 24.4 Pacini F, Schlumberger M, Dralle H, Elisei R, Smit JW, Wiersinga W. European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium. Eur J Endocrinol. 2006; 154: 787-803
- ↑ Barbara D, Boni G. Radioiodine ablation of post-surgical thyroid remnants after preparation with recombinant human TSH: why, how and when. Eur J Surg Oncol. 2007; 33: 535-540
- ↑ Pacini F, Molinaro E, Castagna MG et al. Ablation of thyroid residues with 30 mCi (131)1: a comparison in thyroid cancer patients prepared with recombinant human TSH or thyroid hormone withdrawal. J Clin Endocrinol Metab. 2002; 87: 4063-4068
- ↑ Golger A, Fridman TR, Eski S, Witterick IJ, Freeman JL, Walfish PG. Three-week thyroxine withdrawal thyroglobulin stimulation screening test to detect low-risk residual/recurrent well-differentiated thyroid carcinoma. J Endocrinol Invest. 2003; 26: 1023-1031
- ↑ 28.0 28.1 Liel Y. Preparation for radioactive iodine administration in differentiated thyroid cancer patients. Clin Endocrinol (Oxf). 2002; 57: 523-527
- ↑ Hackshaw A, Harmer C, Mallick U, Haq M, Franklyn JA. 1311 activity for remnant ablation in patients with differentiated thyroid cancen A systematic review. J Clin Endocrinol Metab. 2007; 92: 28-38
- ↑ 30.0 30.1 Jonklaas J, Sarlis NJ, Litofsky D et al. Outcomes of patients with differentiated thyroid carcinoma following initial therapy. Thyroid. 2006; 16: 1229-1242
- ↑ 31.0 31.1 31.2 Cooper DS, Specker B, Ho M et al. Thyrotropin suppression and disease progression in patients with differentiated thyroid cancen results from the National Thyroid Cancer Treatment Cooperative Registry. Thyroid. 1998; 8: 737-744
- ↑ 32.0 32.1 32.2 32.3 Mazzaferri EL, Robbins RJ, Spencer CA et al. A consensus report of the role of serum thyroglobulin as a monitoring method for low-risk patients with papillary thyroid carcinoma. J Clin Endocrinol Metab. 2003; 88: 1433-1441
- ↑ 33.0 33.1 33.2 JZettinig G, Fueger BJ, Passler C et al. Long-term follow-up of patients with bone metastases from differentiated thyroid carcinoma - surgery or conventional therapy? Clin Endocrinol (Oxf). 2002; 56: 377-382.
- ↑ Davids T, Witterick IJ, Eski S, Walfish PG, Freeman JL. Three-week thyroxine withdrawal: a thyroid-specific quality of life study. Laryngoscope. 2006; 116: 250-253
- ↑ 35.0 35.1 Serhal DI, Nasrallah MP, Arafah BM. Rapid rise in serum thyrotropin concentrations after thyroidectomy or withdrawal of suppressive thyroxine therapy in preparation for radioactive iodine administration to patients with differentiated thyroid cancer. J Clin Endocrinol Metab. 2004; 89: 3285-3289
- ↑ Robbins RJ, Robbins AK. Clinical review 156: Recombinant human thyrotropin and thyroid cancer management. J Clin Endocrinol Metab. 2003; 88: 1933-1938
- ↑ 37.0 37.1 Baloch Z, Carayon P, Conte-Devolx B et al. Laboratory medicine practice guidelines. Laboratory support for the diagnosis and monitoring of thyroid disease. Thyroid. 2003; 13: 3-126
- ↑ Spencer CA, Bergoglio LM, Kazarosyan M, Fatemi S, LoPresti JS. Clinical impact of thyroglobulin (Tg) and Tg autoantibody method differences on the management of patients with differentiated thyroid carcinomas. J Clin Endocrinol Metab. 2005; 90: 5566-5575
- ↑ Torlontano M, Attard M, Crocetti U et al. Follow-up of low risk patients with papillary thyroid cancer: role of neck ultrasonography in detecting lymph node metastases. J Clin Endocrinol Metab. 2004; 89: 3402-3407
- ↑ 40.0 40.1 Cailleux AF, Baudin E, Travagli JP, Ricard M, Schlumberger M. Is diagnostic iodine-131 scanning useful after total thyroid ablation for differentiated thyroid cancer? J Clin Endocrinol Metab. 2000; 85: 175-178
- ↑ Papini E, Guglielmi R, Bianchini A et al. Risk of malignancy in nonpalpable thyroid nodules: predictive value of ultrasound and color-Doppler features. J Clin Endocrinol Metab. 2002; 87: 1941¬1946
- ↑ Robbins RJ, Chon JT, Fleisher M, Larson SM, Turtle RM. Is the serum thyroglobulin response to recombinant human thyrotropin sufficient, by itself, to monitor for residual thyroid carcinoma? J Clin Endocrinol Metab. 2002; 87: 3242-3247
- ↑ Pacini F, Agate L, Elisei R et al. Outcome of differentiated thyroid cancer with detectable serum Tg and negative diagnostic (131)1 whole body scan: comparison of patients treated with high (131)1 activities versus untreated patients. J Clin Endocrinol Metab. 2001; 86: 4092-4097
- ↑ 44.0 44.1 Pacini F, Ladenson PW, Schlumberger M et al. Radioiodine ablation of thyroid remnants after preparation with recombinant human thyrotropin in differentiated thyroid carcinoma: results of an international, randomized, controlled study. J Clin Endocrinol Metab. 2006; 91: 926-932
- ↑ Durante C, Haddy N, Baudin E et al. Long-term outcome of 444 patients with distant metastases from papillary and follicular thyroid carcinoma: benefits and limits of radioiodine therapy. J Clin Endocrinol Metab. 2006; 91: 2892-2899
- ↑ 46.0 46.1 46.2 Rubino C, de Vathaire F, Dottorini ME et al. Second primary malignancies in thyroid cancer patients. Br J Cancer. 2003; 89: 1638-1644
- ↑ Chin BB, Patel P, Cohade C, Ewertz M, Wahl R, Ladenson P. Recombinant human thyrotropin stimulation of fluoro-D-glucose positron emission tomography uptake in well-differentiated thyroid carcinoma. J Clin Endocrinol Metab. 2004; 89: 91-95
- ↑ Robbins RJ, Wan Q, Grewal RK et al. Real-time prognosis for metastatic thyroid carcinoma based on 2-[18F]fluoro-2-deoxy-D-glucose-positron emission tomography scanning. J Clin Endocrinol Metab. 2006; 91: 498-505
- ↑ Chiovato L, Latrofa F, Braverman LE et al. Disappearance of humoral thyroid autoimmunity after complete removal of thyroid antigens. Ann Intern Med. 2003; 139: 346-351
- ↑ Castagna MG, Brilli L, Pilli T et al. Limited Value of Repeat Recombinant Human Thyrotropin (rhTSH)-Stimulated Thyroglobulin Testing in Differentiated Thyroid Carcinoma Patients with Previous Negative rhTSH-Stimulated Thyroglobulin and Undetectable Basal Serum Thyroglobulin Levels. J Clin Endocrinol Metab. 2008; 93: 76-81
- ↑ 51.0 51.1 Liu YY, Stokkel MP, Pereira AM et al. Bexarotene increases uptake of radioiodide in metastases of differentiated thyroid carcinoma. Eur J Endocrinol. 2006; 154: 525-531
- ↑ 52.0 52.1 Beierwaltes WH, Nishiyama RH, Thompson NW, Copp JE, Kubo A. Survival time and "cure" in papillary and follicular thyroid carcinoma with distant metastases: statistics following University of Michigan therapy. J Nucl Med. 1982; 23: 561-568
- ↑ 53.0 53.1 Bemier MO, Leenhardt L, Hoang C et al. Survival and therapeutic modalities in patients with bone metastases of differentiated thyroid carcinomas. J Clin Endocrinol Metab. 2001; 86: 1568-1573
- ↑ 54.0 54.1 Leeper RD. The effect of 1311 therapy on survival of patients with metastatic papillary or follicular thyroid carcinoma. J Clin Endocrinol Metab. 1973; 36: 1143-1152
- ↑ 55.0 55.1 Pacini F, Cetani F, Miccoli P et al. Outcome of 309 patients with metastatic differentiated thyroid carcinoma treated with radioiodine. World J Surg. 1994; 18: 600-604
- ↑ 56.0 56.1 Marcocci C, Pacini F, Elisei R et al. Clinical and biologic behavior of bone metastases from differentiated thyroid carcinoma. Surgery. 1989; 106: 960-966
- ↑ 57.0 57.1 Pittas AG, Adler M, Fazzari M et al. Bone metastases from thyroid carcinoma: clinical characteristics and prognostic variables in one hundred forty-six patients. Thyroid. 2000; 10: 261-268
- ↑ 58.0 58.1 Schneider AB, Ron E. Carcinoma of follicular epithelium. In: Braverman LE, Utiger RD, eds. Philadelphia: Lippincott-Raven Publishers; 1996; 902-909
- ↑ Vitale G, Fonderico F, Martignetti A et al. Pamidronate improves the quality of life and induces clinical remission of bone metastases in patients with thyroid cancer. Br J Cancer. 2001; 84: 1586-1590
- ↑ McWilliams RR, Giannini C, Hay ID, Atkinson JL, Stafford SL, Buckner JC. Management of brain metastases from thyroid carcinoma: a study of 16 pathologically confirmed cases over 25 years. Cancer. 2003; 98: 356-362
- ↑ Lippi F, Capezzone M, Angelini F et al. Radioiodine treatment of metastatic differentiated thyroid cancer in patients on L-thyroxine, using recombinant human TSH. Eur J Endocrinol. 2001; 144: 5-11
- ↑ Ford D, Giridharan S, McConkey C et al. External beam radiotherapy in the management of differentiated thyroid cancer. Clin Oncol (R Coll Radiol). 2003; 15: 337-341
- ↑ Mazzarotto R, Cesaro MG, Lora O, Rubello D, Casara D, Sotti G. The role of external beam radiotherapy in the management of differentiated thyroid cancer. Biomed Pharmacother. 2000; 54: 345-349
- ↑ Braga-Basaria M, Ringel MD. Clinical review 158: Beyond radioiodine: a review of potential new therapeutic approaches for thyroid cancer. J Clin Endocrinol Metab. 2003; 88: 1947-1960
- ↑ Droz JP, Schlumberger M, Rougier P, Ghosn M, Gardet P, Parmentier C. Chemotherapy in metastatic nonanaplastic thyroid cancen experience at the Institut Gustave-Roussy. Tumori. 1990; 76:480-483
- ↑ Haugen BR. Management of the patient with progressive radioiodine non-responsive disease. Semin Surg Oncol. 1999; 16: 34-41
- ↑ Pacini F, Vitti P, Martino E et al. Treatment of refractory thyroid cancer with adriamycin. Drugs Under Experimental and Clinical Research. 1984; 10: 911 «916
- ↑ Santini F, Bottici V, Elisei R et al. Cytotoxic effects of carboplatinum and epirubicin in the setting of an elevated serum thyrotropin for advanced poorly differentiated thyroid cancer. J Clin Endocrinol Metab. 2002; 87: 4160-4165
- ↑ JLiu YY, van der Pluijm G, Karperien M et al. Lithium as adjuvant to radioiodine therapy in differentiated thyroid carcinoma: clinical and in vitro studies. Clin Endocrinol (Oxf). 2006; 64: 617-624.
- ↑ Simon D, Korber C, Krausch M et al. Clinical impact of retinoids in redifferentiation therapy of advanced thyroid cancen final results of a pilot study. Eur J Nucl Med Mol Imaging. 2002; 29: 775¬782


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק