סרטן ערמונית גרורתי - טיפול מכוון מטרה באמצעות לוטיציום PSMA
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| Lutetium PSMA - טיפול חדשני מכוון מטרה בסרטן ערמונית גרורתי | ||
|---|---|---|
| ' | ||

| ||
| יוצר הערך | ד"ר אביבית פאר | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן הערמונית
סרטן הערמונית הוא הסרטן השכיח ביותר בגברים ישראלים וגורם המוות הרביעי במספר בגברים. בישראל יש, נכון ל-2023, כ־15 אלף חולים בסרטן הערמונית ומדי שנה נוספים כ־2,500 חולים חדשים, מתוכם 10 אחוזים עד 15 אחוזים שנמצאים כבר בשלב גרורתי.
לארגז הכלים הטיפולי בסרטן ערמונית מתקדם, נוספו תרופות שונות המשפרות את הישרדות החולים, לצד שיפור במדדי המחלה כולל איכות חיים. זאת באמצעות טיפולים הורמונליים מהדור החדש, טיפולים כימותרפיים למחלה עמידה וכן טיפול המבוסס גישה של Theranostics ברפואה גרעינית, אשר הולך ומתפתח.
Theranostics, שפירושה אבחון משולב טיפולים (Therapy + Diagnostics) המבוססים על אותה מטרה מולקולרית ברפואה גרעינית, היא גישה מוכרת ומאושרת לטיפול במספר ממאירויות, כדוגמת יוד רדיואקטיבי בסרטן בלוטת התריס, טיפול בלימפומה, בגידולים נירואנדוקרינים וברדיום בסרטן ערמונית המוגבל לעצמות (תמונה מספר 1).
טיפול בלוטיציום PSMA
טיפול בלוטיציום PSMA הוא איזוטופ (חומר רדיואקטיבי) 177-Lu, הנושא עימו פפטיד, הנקשר לחלבון PSMA (Prostate Specific Membrane Antigen) שקיים על גבי תאי סרטן הערמונית. חלבון זה עולה בביטוי שלו עד פי 1,000 בתאי סרטן ערמונית והופך את המטרה האבחנתית והטיפולית לאטרקטיבית לאחר האבחון המקדים בהדמיית PET-PSMA לזיהוי אתרי הגרורות.
LU-PSMA (PLUVICTO) מאושר לשימוש בגידולים "PSMA Positive" ובכך הופך אותו לסוג של רפואה מדויקת ומתואמת אישית בסרטן ערמונית גרורתי.
הלוטיציום מוזרק למחזור הדם ומתנייד בגוף ללא הפרעה עד שהוא מגיע לתאים המבטאים pSMA ופוגע בהם באופן ממוקד באמצעות קרינה בטא בעוצמה בינונית בטווח של 2 מילימטר, המשתחררת בתא ומובילה לפגיעה בתאי הגידול תוך שמירה על הסביבה התקינה (תמונה 2).

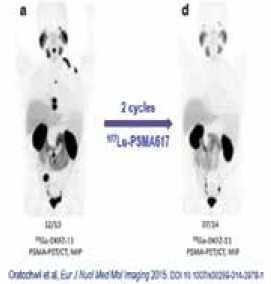
החל משנת 2015 החלו להתפרסם מחקרים רטרוספקטיביים ופרוספקטיביים התומכים ביעילות גישה זאת בטיפול בסרטן ערמונית גרורתי עמיד לסירוס בחולים שמיצו טיפולים מקובלים, או לא מועמדים להמשך טיפול כדוגמת כימותרפיה נוספת. החלוץ בתחום, ד"ר הופמן באוסטרליה, הדגים שיפור רדיולוגי בהתקדמות המחלה (rPFS - radiologic Progression Free Survival) וירידה ב-PSA (Prostate Specific Antigen) של 50 אחוזים ומעלה במטופלים שקיבלו טיפול זה[1]. עבודות רבות פורסמו בטיפול בודד והדגימו הן בטיחות והן יעילות של הטיפול במחלה מתקדמת (תמונה מספר 3).
בישראל, אחרי שהטיפול החל להתבסס באוסטרליה ובגרמניה, ניתן טיפול בלוטציום כטיפול חמלה החל משנת 2017 על בסיס טיפול חמלה פרטני, והניסיון של הטיפול בישראל פורסם בעיתונות המקצועית[2]. מרבית המחקרים מדגימים תגובה ביוכימית, בכ-40 אחוזים עד 50 אחוזים מהמטופלים והישרדות חציונית של כ-14-10 חודשים תחת טיפול זה. חולים שטרם קיבלו כימותרפיה מדגימים תגובות עמוקות יותר הן מבחינת ירידת PSA והן בהישרדות חציונית של מעל שנתיים.
למרות המידע החיובי של מחקרים אלה, בהם זרוע בודדת של טיפול, לא היה בעבר מידע לגבי יעילות הטיפול בהשוואה לטיפולים מקובלים בחולים אלה. שני מחקרים רנדומליים פורסמו והדגימו יתרון של טיפול זה אל מול טיפול כימותרפי וכן אל מול טיפול הורמונלי בודד.
במחקר TheraP שהוביל ד"ר הופמן[3] ב-200 חולים נבחן טיפול בלוטציום אל מול טיפול כימותרפי מקובל בקו מתקדם בקבזיטקסל, בחולים עם מחלה מתקדמת עמידה לסירוס לאחר טיפול בטקסוטר וטיפול הורמונלי. החולים עברו גם PET-FDG (Positron Emission Tomography - Fluorodeoxyglucose) לשלול חוסר התאמה בקליטות בגרורות בין PET-PSMA ל-FDG, המנבאת תגובה נמוכה יותר לטיפול.
מחקר זה הראה יתרון מהותי לטיפול בלוטציום PSMA בתגובת PSA (66 אחוזים לעומת 33 אחוזים), ופחות רעילות בדרגה 3/4, 35 אחוזים לעומת 54 אחוזים. מחקר זה לא הדגים יתרון בהישרדות של החולים, אך זה לא היווה End point עיקרי במחקר (לא תוכנן להדגים יתרון הישרדותי), בשל מספר חולים קטן וכן מאחר שלחולים בזרוע הביקורת ניתנה אפשרות לקבל טיפול בלוטציום בהתקדמות מחלה, כך שמספר לא מבוטל של חולים בזרוע הביקורת, קיבלה בסופו של דבר את טיפול המחקר.
במרץ 2022 ה-FDA (Food and Drug Administration) אישר את הטיפול בלוטציום Pluvicto) PSMA) בהתבסס על הניסוי הבינלאומי הגדול והאקראי שלב 3 VISION, בהובלת ד"ר מייקל מוריס[4]. מחקר זה הראה כי Lu-PSMA מאריך חיים, מפחית את התקדמות המחלה ושומר על איכות חיים. מטופלים שטופלו ב-Lu-PSMA בתוספת טיפול סטנדרטי הכולל טיפול הורמונלי, חיו ארבעה חודשים יותר בממוצע לעומת מטופלים שטופלו בטיפול סטנדרטי בלבד (15.3 לעומת 11.3 חודשים). גם הזמן עד להחמרת המחלה בסריקות היה ארוך יותר בממוצע של 5.3 חודשים (8.7 לעומת 3.4 חודשים). תגובת PSA הייתה 46 אחוזים לעומת 7 אחוזים בזרוע הביקורת ושיעור תגובה הדמייתית, Response Rate, עמד על 30 אחוזים לעומת 2 אחוזים לטובת לוטציום. הטיפול נסבל היטב, תופעות לוואי כגון ירידות בספירות הדם, יובש בפה ובחילות, היו שכיחות יותר בזרוע Lu-PSMA. פרופיל בטיחות דומה פורסם במחקרים נוספים וכך טיפול זה הוא בטוח במטופלים מתקדמים גם בגיל מבוגר.
פרסום נוסף של מחקר VISIONS תמך גם בשיפור במדדי איכות חיים תחת טיפול בלוטציום (PLUViCTo)[5]. מחקרים נוספים רטרוספקטיביים תומכים מבחינת בטיחות המטופל במתן טיפול זה גם לאחר טיפול קודם ברדיום 223[6].
סיכום
הטיפול בלוטציום PsMA ניתן במחלקת רפואה גרעינית דרך הווריד במינון של 7.4GBq (Giga-Becquerel), אחת לשישה שבועות. מספר מחזורי הטיפול נקבע על פי התגובה לטיפול ועד שישה טיפולים בסך הכל. לאחר הטיפול מתבצעת סריקה המראה באופן ברור את אופן הפיזור של החומר בכל הגוף וקליטתו באתרי המחלה.
עם אישור זה, טיפול ממוקד PsMA הופך לסוג הטיפול החדש ביותר בסרטן הערמונית. בשלב זה הפופולריות של טיפול זה עולה במהרה מחוץ לישראל. בישראל נצבר ניסיון בטיפול במאות חולים.
טיפול מאושר בלוטציום PSMA הוגש לסל התרופות 2024 בישראל, בהתוויה למטופלים מבוגרים עם סרטן ערמונית גרורתי עמיד לסירוס וחיובי ל-PSMA, שטופלו עם מעכבי מסלול הקולטן לאנדרוגן ושעברו כימותרפיה מבוססת טקסן או שאינם מתאימים מבחינה רפואית לטיפול בטקסנים.
ביבליוגרפיה
- ↑ Hofman MS, Violet J, Hicks RJ, et al. [177 Lu]-PSMA-617 radionuclide treatment in patients with metastatic castration-resistant prostate cancer (LuPSMA trial): a single-centre, single-arm, phase 2 study. Lancet Oncol. 2018;19(6):825-833.
- ↑ Leibowitz R, Davidson T, Gadot M, et al. A retrospective analysis of the safety and activity ofLutetium-177- prostate-specific membrane antigen radionuclide treatment in older patients with metastatic castration¬resistant prostate cancer. Oncologist 2020;25(9): 787-792.
- ↑ Hofman MS, Emmett L, Sandhu S, et al. [177Lu] Lu-PSMA-617 versus cabazitaxel in patients with metastatic castration-resistant prostate cancer (TheraP): a randomised, open-label, phase 2 trial .Lancet 2021 397(10276):797-804. https://doi.org/10.1016/S0140- 6736(21)00237-3.
- ↑ Sartor O, de Bono J, Chi KN, et al. Lutetium-177- PSMA-617 for metastatic castration-resistant prostate cancer. N Engl J Med 2021; 385: 1091-103.
- ↑ Karim Fizazi, et al. Health-related quality of life and pain outcomes with [177Lu] Lu-PSMA-617 plus standard of care versus standard of care in patients with metastatic castration-resistant prostate cancer (VISION): a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2023; 24: 597-610.
- ↑ RALU: Time interval between 223Ra and 177Lu-PSMA therapy and clinical outcomes in patients with mCRPC. K. Rahbar ASCO 2023 Abstract 73.
המידע שבדף זה נכתב על ידי ד"ר אביבית פאר, רופאה בכירה באגף האונקולוגי, אחראית מרפאת גידולי דרכי השתן ומנהלת המחקרים הקליניים באגף, המרכז הרפואי רמב"ם
PLU-ART-09.23 oct-2023


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק