סרטן שד גרורתי - טיפולים חדשניים - Metastatic breast cancer - new treatments
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| סרטן שד גרורתי - טיפולים חדשניים | ||
|---|---|---|
| Metastatic breast cancer - new treatments | ||
| שמות נוספים | סרטן שד גרורתי - טיפולים ביולוגיים וכימיים חדשניים לטיפול | |
| יוצר הערך | ד"ר לריסה ריבו | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן השד
סרטו השד היא המחלה הממארת השכיחה ביותר בישראל ובעולם המערבי. בישראל, כ-4,000 נשים מאובחנות מדי שנה כחולות בסרטן השד ואחת מכל שמונה נשים עלולה לחלות במחלה. במדינות מפותחות, רוב מקרי סרטן השד מתגלים בשלבים מוקדמים. ככל שהמחלה מאובחנת בשלב מוקדם, סיכויי הריפוי גבוהים יותר. מסתמן כי מספר הנשים אשר מחלימות מסרטן השד עולה בהתמדה בזכות הגילוי המוקדם ובזכות שיפור דרכי הטיפול והגברת המודעות הנרחבת בארץ. בכ-5% מהנשים מופיעה מחלה מפושטת בגילוי הראשוני.
קיימים סוגים שונים של סרטן השד. במאמר זה נתרכז בסרטן שד גרורתי עם ביטוי יתר של HER2 (Human Epidermal Growth Factor Receptor 2).
רקע על סרטן שד מסוג HER2 חיובי
אחת מחמש נשים החולות בסרטן שד, תחלנה בסוג מסוים הנקרא סרטן שד מסוג HER2 חיובי. מדובר בסרטן מסוג אגרסיבי, כאשר אבחון הביטוי ביתר של HER2 נעשה בשלב הביופסיה הנלקחת מהגידול. לאבחון השפעה מכרעת על סוג הטיפול שיינתן, על איכות חיי החולות ועל הסיכוי להארכת חיים.
HER2 הוא קולטן המצוי באופן נורמלי על פני התא ולו תפקיד חשוב בבקרה על גדילתם וחלוקתם של תאים תקינים. בתא נורמלי ניתן למצוא אותו בכמויות קטנות יחסית. בגידולים סרטניים מסוימים יש ביטוי יתר של HER2, המוגדר בבדיקה כ- HER2 חיובי, שגורם לגדילה בלתי מבוקרת של התאים ולהתפתחות מואצת של תאים סרטניים. כאמור, נשים עם סרטן שד המאובחנות עם רמות גבוהות של HER2, סובלות ממחלה אלימה במיוחד של סרטן שד עם פרוגנוזה גרועה וסיכוי גדול להתפתחות גרורות מרוחקות. בשנים האחרונות פותחו טיפולים חדשים, ביניהן טיפול מוכוון מטרה (Targeted therapy), הקשורים לביטוי יתר של HER2.
טיפול מוכוון מטרה (Targeted therapy)
Herceptin (Trastuzumab)
השימוש ב- Herceptin לסרטן שד גרורתי מקובל מזה שנים רבות. Herceptin הינו נוגדן חד שבטי מואנש (Humanized monoclonal antibodies), אשר מכוון באופן ספציפי נגד הקולטן HER2 ומהווה את בסיס הטיפול לנשים עם סרטן שד מסוג HER2 חיובי. התרופה ניתנת בהזרקה תוך ורידית. התרופה פועלת בארבעה מנגנוני פעולה שונים:
- עיכוב שגשוג התא דרך קולטן HER2.
- עיכוב יצירת כלי דם חדשים (Angiogenesis), המוביל לירידה בקוטר ונפח כלי הדם של הגידול, ירידה בצפיפות כלי-הדם סביבו וירידה בנדידת תאי האנדותל.
- הפעלה של המערכת האוטואימונית כנגד התאים הסרטניים (מגביר גיוס של תאי מערכת החיסון להרג התא הסרטני).
- מניעת חיתוך החלק החוץ-תאי של קולטן HER2 והיווצרות היחידה הפוטנטית p95.
Herceptin בשילוב עם כימותרפיה
טיפול ב- Herceptin בשילוב עם כימותרפיה יאריך את חיי המטופלות ויעניק להן כתשעה חודשים נוספים ביחס לטיפול המקובל בכימותרפיה בלבד. בסרטן שד הנמצא בשלב מוקדם, לאחר ניתוח לכריתת הגידול, נהוג להוסיף טיפול משלים (Adjuvant). במחקר שפורסם בכתב העת The New England journal of Medicine ב-2011, נבדקה הוספת מתן Herceptin למשך שנה לאחר סיום הטיפול הכימי המונע. במחקר השתתפו 3,222 נשים עם סרטן שד משלב מוקדם מסוג HER2 חיובי אשר עברו ניתוח לכריתת הגדול הראשוני. החולות טופלו בכימותרפיה או בכימותרפיה בתוספת Herceptin. הוכח כי מתן Herceptin למשך שנה משפר את ההישרדות הכללית והזמן עד להישנות המחלה לעומת טיפול כימותרפי בלבד. הטיפול המשלים עם Herceptin למשך שנה הפך לטיפול המקובל גם בקרב חולות עם סרטן שד HER2 חיובי הנמצא בשלב מוקדם.
Herceptin במתן תת-עורי
לאחרונה נמצאת בפיתוח ובתהליכי רישום גם צורת מתן חדשה Herceptin תת-עורי (Herceptin SC - Herceptin Subcutaneous). מדובר באותה תרופה עם אותו מרכיב פעיל (Trastuzumab), אם כי שילובו עם האנזים היאלורונידאז (Hyaluronidase) רקומביננטי, מאפשר את מתן התרופה בזריקה תת-עורית. אנזים זה מחקה את פעילותו של היאלורונידאז הפועל באופן טבעי בגוף, ומפרק באופן זמני והפיך את החומצה ההיאלורונית (Hyaluronic acid), המהווה חלק מהשכבה התת-עורית (ביחד עם סיבי הקולגן). טכנולוגיה זו מאפשרת מתן נפח גדול יותר של נוזלים ובמקרה של Herceptin מתאפשר מתן של 5 מיליליטר בזריקה תת עורית. Herceptin SC ניתן במינון קבוע של 600 מ"ג עם משך הזרקה של 5 דקות, ללא צורך במנת העמסה (Loading dose) וללא צורך בהכנה רוקחית. התרופה נבדקה במחקר שלב III בשילוב עם טיפול כימי והראתה יעילות דומה לטיפול תוך ורידי.
Kadcyla (T-DM1 - Trastuzumab Emtansine)
Kadcyla מיועדת לטיפול בחולות עם סרטן שד חיובי ל-HER2. התרופה היא מולקולה חדשה מסוג נוגדן מצומד לתרופה כימותרפית (ADC -(Antibody drug conjugate). ה-ADCs שייכים לקבוצה תרפויטית חדשה המשלבת תרופה ציטוטוקסית (Cytotoxic drug) הקשורה בקשר קוולנטי לנוגדן מכוון מטרה. בזכות מבנה זה, ה- ADCs מפחיתים חשיפה מערכתית לציטוטוקסיות ומשפרים את האינדקס התרפויטי של התרופה.
Kadcyla, ובשמה הגנרי המקוצר T-DM1, מורכבת מ:
- Herceptin (Trastuzumab)
- מקשר יציב (Stable linker) ייחודי בשם MCC (MCC - 4-[N-maleimidomethyl] cyclohexane-1-carboxylate)
- ציטוטוקסיקה פוטנטית בשם DM1 (Derivative of Maytansine).
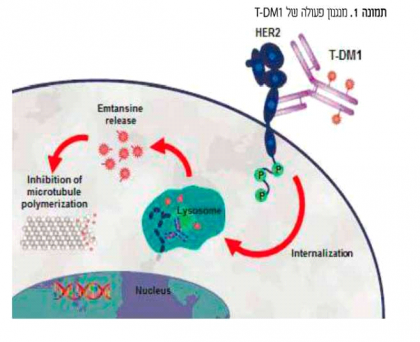
כהוצאה ממנגנון פעולתה הייחודי, Kadcyla, מאפשרת שחרור תוך תאי בררני של כימותרפיה פוטנטית בתאים סרטניים שמבטאים ביתר HER2. היקשרות התרופה ל- HER2 על פני שטח תא הגידול (בעזרת המרכיב Herceptin) מובילה לבליעה תאית (Endocytosis) של הקומפלקס אל תוך תא הגידול. עם השלמת התהליך, הקומפלקס עובר פירוק בליזוזום תוך שחרור תוך תאי של המטבוליט הציטוטקסי (תמונה 1).
התרופה נבדקה במחקר בשם EMILIA study, אשר כלל 980 נשים עם מחלה גרורתית וביטוי יתר של HER2. החולות נחשפו קודם לטיפול ב- Herceptin ומחלתן התקדמה. החולות חולקו באופן אקראי לשתי קבוצות:
- קבוצה אחת קיבלה טיפול ב-Kadcyla.
- הקבוצה השנייה קיבלה טיפול כימותרפי מקובל המשלב Tykerb (Lapatinib) עם Xeloda (Capecitabine).
תוצאות המחקר הוכיחו הבדל משמעותי סטטיסטית משך הזמן עד התקדמות המחלה בקבוצה שקיבלה טיפול T-DMI היה ארוך יותר לעומת קבוצת הביקורת (9.6 חד' לעומת 6.4 חד' בהתאמה). כמו כן יותר חולות בקבוצה של T-DMI השיגו רמיסיה של המחלה (43.6% לעומת 30.8%). ההישרדות החציונית הכללית בקבוצת T-DMI הייתה 30.9 חודשים לעומת קבוצת הביקורת: 25.1 חודשים.
(Perjeta (Pertuzumab
Pertuzumab התרופה (Perjeta (pertuzumab הינה נוגדן חד שיבטי מואנש הנקשר לקולטן HER2, והיא הראשונה מקבוצה חדשה של תרופות: HER2 Dimerisation inhibitors. באופן כללי, כאשר שני קולטנים ממשפחת HER עוברים דימריזציה, מופעלים מסלולים תוך-תאיים המובילים לפרוליפרציה של התאים הסרטניים.
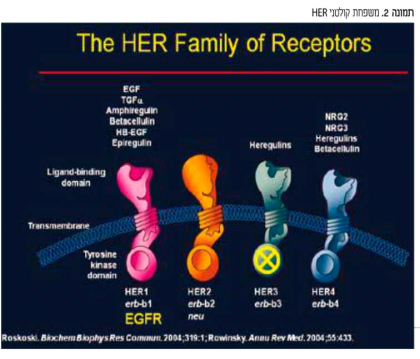
משפחת חלבוני HER מורכבת מ-4 רצפטורים טרנס-ממברנלים (מסוג Tyrosinekinase). חלבוני 1,3,4 HER הם קולטנים תלויי ליגנד: כאשר הליגנד נקשר אליהם המבנה המרחבי של הקולטן משתנה וכך מתאפשרת הדימריזציה לקולטן אחר ממשפחה HER. לעומת זאת, קולטן HER2 אינו תלוי ליגנד, הוא נמצא במבנה מרחבי פתוח ותמיד זמין לעבור דימריזציה, ולכן הוא הפרטנר המועדף ליצירת דימרים עם קולטני HER האחרים(תמונה 2).
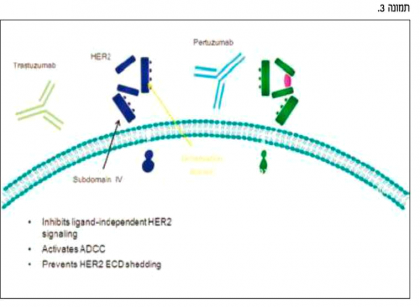
Perjeta נקשרת לאתר אחר על-גבי אותו קולטן HER2, אתר ספציפי שאחראי לדמריזציה, ומונעת את היצמדותו לקולטנים אחרים ממשפחת HER. במנגנון זה, Perjeta מונעת, בין היתר, את יצירת הצמד HER2-HER3, שנמצא כצמד האונקוגני הפוטנטי ביותר בסרטן שד וכך מונעת הפעלת שני מסלולים תוך תאיים האחראים לשגשוג הגדול ולהישרדותו. עיכוב שני מסלולים אלה מביא לפגיעה בפעילותו של התא הסרטני.
כמו-כן, Perjeta מגבירה גיוס תאי מערכת החיסון להרג התא הסרטני (ADCC).
ל-Perjeta יש מנגנון פעולה משלים להרספטין ולמעשה טיפול משולב של שניהם מאפשר חסימה מקיפה יותר של מסלולי האיתות התוך תאיים של משפחת HER ובכך דיכוי יעיל יותר של הגידול הסרטני (ציור 3).
Perjeta נבדקה במחקר (CLEOPATRA), המחקר כלל 808 נשים עם מחלה גרורתית וביטוי יתד של HER2, החולות לא קיבלו טיפול קודם בהרספטין. החולות חולקו באופן אקראי ל־2 קבוצות. קבוצה אחת קיבלה טיפול בהרספטין + פרטוזומב + טקסוטר וקבוצה שנייה קיבלה טיפול בהרספטין + טקסוטר. תוצאות המחקר הראו כי הזמן עד התקדמות המחלה בקבוצה שקיבלה טיפול בהרספטין + פרטהומב + טקסוטר היה ארוך יותר לעומת קבוצת הביקורת (18.5 חד' לעומת 12.4 חד'). כמו כן יותר חולות בקבוצה הרספטין + פרטוזומב + טקסוטר הגיבו לטיפול (80% לעומת 70%). לגט ההישרדות הכללית עדין אין נתונים.
לסיכום
הנתונים בספרות מצביעים על התקדמות בטיפולים ביולוגיים נוגדי HER2 בחולות סרטן שד משלב גרורתי ומשלב מוקדם; מתן הסרפטין אדג׳ובנטי משפר שיעורי ריפוי של חולות בסרטן שד מוקדם, לגבי מחלה גרורתית - הטיפולים הביולוגיים מעלים את יעילות הטיפולים הכימותרפיים וזאת מבלי להוסיף רעילות באופן משמעותי. טיפולים ביולוגיים בשלוב עם טיפולים כימותרפיים מאריכים חיים ומשפרים איכות חיים, בחולות עם סרטן שד גרורתי עם ביטוי יתר של HER2.
(Haiaven (eribulin
Haiaven מבוססת על סנתוז של חומר פעל שנמצא לפני שנים בספוג ים שחור יפני.
פיתוח התרופה מחזיר לבמה תהליכים שחלקם נזנחו על יד חברות התרופות, במסגרתם נמצאו חומרים פעילים שמקורם בצמחים והפכו לתרופות. במקרה הנוכחי קיים בספוגים חומר פעיל שהראה פעילות אנטי סרטנית באמצעות פעילות המונעת את התחלקות התא. מכיוון שכמות החומר בספוגים הייתה קטנה, החוקרים עבדו במשך שנים על מנת לייצר מולקולה סינתטית זהה למקורית והיא זו הנמצאת כיום בתרופה.
(Halaven (Eribuim הינה כימותרפיה המשמשת לטיפול בסרטן שד מתקדם או גרורתי לאחר טיפול בשני משטרי טיפול אחרים שאיבדו את האפקטיביות שלהם. יעילותה ובטיחותה של Halaven הודגמו במחקר בו השתתפו 762 נשים חולות בסרטן שד גרורתי שטופלו בעבר בשני משטרי טיפול קודמים. הנשים חולקו לקבלת Halaven או טיפול כימותרפי אחר (תרופה בודדת). תוצאות המחקר הראו כי Halaven האריכה באופן מובהק את חייהן של המטופלות בה בהשוואה לאורך חייהן של המטופלות בקבוצה הביקורת.
הטיפול ניתן רק פעמיים בלבד, ביום הראשון והשמיני, במהלך מחזור טיפול של 21 יום.
מתן העירוי נמשך כ-15 דקות בלבד ואינו דורש שימוש באנטי-היסטמינים או סטרואידים.
הטיפול נסבל היטב ונמצא יעיל בקוים מתקדמים של טיפול בסרטן שד גרורתי.
ביבליוגרפיה
- Tzahar E, Waterman H, Chen X, Levkowltz G, Karunagaran D, Lavi S, et al. A hierarchical network of interreceptor interac¬tions determines signal transduction by Neu differentiation factor/neuregulin and epidermal growth factor. Mol Cell Biol 1996;16:5276-5287.
- Citri A, Skaria KB, Yarden Y.The deaf and the dumb: the biol-0gyofErbB-2and ErbB-3. Exp Cell Res 2003;284:54-65.
- Clynes RA, Towers TL, Presta LG, Ravetch JV. Inhibitory Fc re¬ceptors modu late in vivo cytotoxicity against tumor targets. Nat Med 2000; 6:443-446.
- Gennari R, Menard S, Fagnoni F, Ponchio L, Scelsi M, Tagli-abue E, Castiglioni F, Villani L, Magalotti C, Gibelli N, Oliviero B, Ballardini B, Da Prada G, Zambelli A, Costa A. Pilot study of the mechanism of action of preoperative Trastuzumab in patients with primary operable breast tumors overexpressing HER2. Clin Cancer Res 2004; 10:5650-5655.
- Arnould L, Gelly M, Penault-Llorca F, Benoit L, Bonnetain F, Migeon C, Cabaret V, Fermeaux V, Bertheau P, Gamier J, Jeannin JF, Coudert B. Trastuzumab-based treat¬ment of HER2-positive breast cancer: an antibody-dependent cellular cytotoxicity mechanism? J Cancer 2006; 94; 259-267.
- Chari RV. Targeted cancer therapy: conferring specificity to cytotoxic drugs. Acc Chem Res. 2008;41:98-107.
- Lewis Phillips GD, Li G, Dugger DL, et al. Targeting HER2-positive breast can¬cer with trastuzumab-DM1, an antibody-cytotoxic drug conjugate. Cancer Res. 2008;68:9280-9290.
- Junttila TT, Li G, Parsons K, Phillips GL, Sliwkowski MX.Trastuzumab-DM1 (T-DMI) retains all the mechanisms of action of Trastuzumab and efficiently inhibits growth of lapatinib insensitive breast cancer. Breast Cancer Res Treat. 2011;128:347-356.
- Slamon DJ, Leyland-Jones B, Shak S, Fuchs H, Paton V, Bajamonde A, Fleming T, Eiermann W, Wolter J, Pegram M, Baselga J, Norton L, Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2. N Engl J Med. 2001 Mar 15;344(11):783-92.
1. Slamon D, Eiermann W, Robert N, Pienkowski T, Martin M, Press M, Mackey J, Glaspy J, Chan A, Pawlicki M, Pinter T, Valero V, Liu MC, Sauter G, von Minckwitz G, Visco F, See V, Buyse M, Bendahmane B, Tabah-Fisch I, Lindsay MA, Riva A, Crown J; Breast Cancer International Research Group. Adjuvant Trastuzumab in HER2-positive breast cancer. N Engl J Med. 2011 Oct6;365(14]:1273-83
קישורים חיצוניים
- הטיפול ההורמונלי בסרטן השד, TheMEDICAL
המידע שבדף זה נכתב על ידי ד"ר לריסה ריבו, רופאה בכירה, המערך האונקולוגי, המרכז הרפואי ת"א


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק