סרטן שלפוחית השתן - טיפול בטכנולוגית סינרגו - Bladder cancer - treatment with synergo technology
| סרטן שלפוחית השתן - טיפול בטכנולוגית סינרגו | ||
|---|---|---|
| Bladder cancer - treatment with synergo technology | ||
| יוצר הערך | ד"ר שראל הלחמי, ד"ר גיא הידש, פרופ' עופר נתיב 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן במערכת השתן
סרטן שלפוחית השתן הוא הממאירות הרביעית בשכיחותה בגבר והשמינית באישה.
מדי שנה בארצות הברית מתגלים כ-60,000-75,000 מקרים חדשים לשנה, ובישראל בין כ-1,000 ל-1,500 מקרים. שיעור הגידול במספר החולים הלוקים בסרטן השלפוחית עולה באופן קבוע בכ-0.8% לשנה [1]. רוב הלוקים במחלה סובלים מסרטן שלפוחית לא חודרני, המטופל של ידי כריתה אנדוסקופית (Endoscopic) של הנגע. עם זאת, למרות כריתה שלמה, עד 70% מהחולים יסבלו מהישנות של הנגע בשלפוחית, וכ-10%-15% יסבלו מהתקדמות של שלב המחלה.
טיפול תרופתי משלים לאחר כריתה
בשל הנטייה הגבוהה להישנות, טיפול משלים תוך-שלפוחיתי לאחר כריתת הנגע השטחי הוא הכרחי בשיעור ניכר של המטופלים. תרופת הבחירה לטיפול המשלים היא חיידקי שחפת מוחלשים - הגורמים לתגובה חיסונית מקומית, לתקיפה ולחיסול תאי הסרטן בדופן כיס השתן. למרות יעילותה הרבה, יש ל-Immucyst מספר חסרונות: חולים עם שחפת, חולים במחלת כבד וכאלו הסובלים מהפרעה בתפקוד מערכת החיסון, או המטופלים בתרופות המדכאות את מערכת החיסון, אינם יכולים לקבל טיפול בתרופה. 30%-40% מהמטופלים יסבלו מכישלון של הטיפול ותופיע אצלם הישנות של המחלה וכ-5%-10% נוספים יסבלו מתופעות לוואי לתרופה זו, וגם בקבוצה זו תידרש החלפת טיפול משלים. לחולה המטופל ב-Immucyst יש סיכוי גבוה עד 80%-90% ללקות בתופעות לוואי קלות עד בינוניות ועד 5% עשויים לסבול מתופעות לוואי חמורות.
אחת התרופות היעילות יחסית לטיפול משלים תוך-שלפוחיתי היא Mitomycin C. התרופה היא חומר מאלקל (Alkylating agent) והיא מעכבת בניה של דנ"א (DNA, Deoxyribonucleic Acid). חדירת תרופה לרקמת השלפוחית תלויה במספר משתנים: ריכוז התרופה בכיס השתן, עובי האורותל (Urothelium) ומקדמי הפעפוע של הרקמה, כל זאת בהתאם לחוק פיק. בריכוז טיפולי מיטבי, Mitomycin C עשויה לחדור לדופן השלפוחית עד לעומק של כ-500 מיקרון, כלומר עד למחצית עובייה של הלמינה פרופריה (Lamina propria) בשלפוחית תקינה. באזור גידולי, כמות הצמתים ההדוקים הבין תאיים (Tight junctions) שבין התאים פחותה, לכן הרקמה יותר חדירה וחדירת הכימותרפיה היא טובה יותר בהשוואה לרקמה בריאה.
מספר רב של מחקרים הדגימו, כי טיפול משלים ב-Mitomycin C מקטין את שיעור הישנות הגידול מ-70% לכ-40%-50%, שיעור נחות יותר לעומת ה-Immucyst. בשל גודל המולקולה, 334 קילו דלתון, ספיגתה נמוכה ושיעור תופעות הלוואי הוא נמוך. בהשוואה ל-Immucyst, כמעט ואין תיאור של תופעות לוואי חמורות. לאור היעילות הטובה והיעדר תופעות הלוואי, חיפשו החוקרים דרך להגביר את יעילות התרופה תוך שימור המתאר הבטיחותי.
טיפול בתרמותרפיה (Thermotherapy)
ההשפעה הראשונית של יתר-חום (Hyperthermia) טיפולי (43-45 מעלות צלזיוס) על רקמה בריאה, הוא עלייה בפעפוע של כלי הדם ושיפור בחמצון הרקמה הבריאה והממארת. אומנם לתוצא זה אין השפעה נוגדת סרטן ישירה, אך באופן זה הרקמה הגידולית עשויה להיות רגישה יותר לטיפולים נוגדי סרטן נוספים, כגון: כימותרפיה וקרינה. יתר-חום ממושך או חום גבוה עשוי לגרום לקריסת מערכת כלי הדם של הנגע בשל פקקת ושטפי דם[2]. תוצא נוסף של החימום על הרקמה הגידולית הוא שינוי במאזן החומצי-בסיסי, עם עלייה ברמת החומציות של הרקמה הגידולית, שאינה מופיעה ברקמה הבריאה[3]. כמו כן, בחימום ממושך של כ- 30-60 דקות, יתר-חום גורם ישירות לתמותה של תאי גידול.
ואן דר הידן וחבריו[4] הדגימו כי יתר-חום כשלעצמו מעכב שגשוג של גידולי שלפוחית. יתרה מכך, בנגעים שבהם נמצא חלבון P53 תשני (Mutant), טיפול ביתר-חום הפחית משמעותית את רמות החלבון הלא תקין. חלבון זה מיוצר על ידי גן מעכב סרטן, ותשניות גורמות לאיבוד היכולת המעכבת.
דיאנס וחבריה הדגימו עלייה בפעילות נוגדת סרטן של תאים לבנים מסוג תאי הרג טבעי (Natural killers), בעקבות יתר-חום [5].
טיפול בטכנולוגית סינרגו: כימו-תרמותרפיה לסרטן שלפוחית לא חודרני
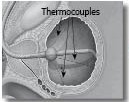
מערכת הסינרגו (תמונות 2-1) מאפשרת טיפול תוך-שלפוחיתי ב-Mitomycin C, תוך כדי חימום רקמת השלפוחית, על ידי אנרגיית גלי רדיו (RF, Radiofrequency). חימום בשיטה זו מאפשר שליטה מדויקת על חום הרקמה, ולכן ניתן למנוע נזקים של חימום יתר. החום ברקמה מפוזר באופן שווה, ולכן התוצא הטיפולי אחיד בכל דופנות השלפוחית. חימום באמצעות גלי רדיו יעיל יותר מחימום של נוזל השטיפה, למשל. כדי לחמם את שלפוחית השתן ל-42 מעלות צלזיוס, על נוזל השטיפה להיות חם יותר מ-50 מעלות, חום העלול לגרום נזק לרקמות. נוסף על כך, דעיכת החום היא מהירה וגם אם הנוזל במרכז השלפוחית יהיה במעלות הללו, דפנות השלפוחית יתחממו עד לחום של 37-41 מעלות בלבד ואלו הן מעלות שאינן טיפוליות (תמונה 3).
השילוב של חימום דופן השלפוחית עם שטיפה בכימותרפיה, מאפשרת פעפוע טוב יותר של Mitomycin C לרקמה, והשגת ריכוזים טיפוליים גבוהים יותר ברקמה, באותו מינון טיפולי.
התוצא הטיפולי של Mitomycin C נגרם בשל קשירת המולקולה לסליל הדנ"א. כדי להיות זמינה לקשר זה, על מולקולת Mitomycin C לעבור חמישה שינויים במבנה המרחבי שלה, התגובה הכימית היא תלוית חום, ובעקבות יתר-החום יש האצה בקצב התגובה ובזמינות המולקולה הפעילה (תמונה 4).
השילוב של כימו-תרמותרפיה יעיל יותר ממתן Mitomycin C בלבד. טיפול זה הוא קו שני יעיל, לחולים שסבלו מהישנות למרות טיפול ב-Immucyst. מספר מחקרים מראים יעילות דומה של השילוב, בהשוואה לטיפול ב-Immucyst. השיעור והחומרה של תופעות הלוואי הם נמוכים, בהשוואה לטיפול תוך-שלפוחיתי ב-Immucyst.
- תוצאות מחקרים
מושקוביץ וחבריו[6] השתמשו בכימו-תרמותרפיה, ב-22 חולים עם נגעים שלפוחיתיים לא חודרניים , שסבלו מהישנויות חוזרות של הגידול למרות טיפול קודם ב- Immucyst (59%, 13/22), Mitomycin C (32%, 7/22) ובתרופות נוספות. לנוכח ההישנות החוזרת, שלב המחלה, ודרגת התמיינות הנגעים, חולים אלו הוגדרו כבעלי סיכון בינוני עד גבוה להישנות ולהתקדמות. בתקופת מעקב ממוצעת של 9.6 חודשים, היו 20 חולים (91%) חופשיים ממחלה. הישנות הגידול אובחנה בשני חולים בלבד לאחר כ-14 חודש בממוצע.
קולומבו וחבריו[7] השוו טיפול כימותרפי תוך-שלפוחיתי (41 מטופלים) לטיפול כימו-תרמותרפי (42 מטופלים) במחקר אקראי (Random) מבוקר. המחקר הדגים את היתרון בטיפול המשולב, ושיעור ההישנות הכולל במטופלים בכימותרפיה היה 58%, לעומת 17% בקבוצת הטיפול המשולב.
גופרית וחבריו[8] בדקו את יעילות הטיפול המשולב, בחולים עם נגע לא פולשני מתקדם: 40 חולים היו בשלב T1G3, 11 בשלב TaG3 ו-3 עם CIS (Carcinoma In Situ). בזמן חציון של כ-15 חודש, באף אחד מן החולים לא הייתה התקדמות בשלב המחלה, בחולים שבהם ניתן טיפול מניעתי (24 מטופלים) בתקופת זמן ממוצעת של כ-35 חודש, 15 חולים (כ-62.5%) לא סבלו מהישנות של הנגע. קבוצה של כ-28 חולים קיבלה טיפול צריבתי (Ablation), וב-21 (75%) מהם הייתה נסיגה של הנגע. בתקופת מעקב ממוצעת של 20 חודש לא הייתה ב-80% מהם הישנות.
הלחמי וחבריו בדקו את שיעור ההישנות והתקדמות המחלה, ב-56 חולים עם סרטן לא חודרני מתקדם בשלב T1G3. 26 מטופלים בקבוצה זו סבלו מהישנות, לאחר כישלון טיפולי ב-Immucyst. 51 מטופלים סיימו את המעקב, ובזמן מעקב ממוצע של כ-20 חודש, רק ב-33% (17 מטופלים) הופיעה הישנות הגידול. זמן ממוצע להופעת ההישנות היה כ-9 חדשים. מכלל החולים שבהם הופיעה הישנות, ב-4 הייתה התקדמות של הנגע לשלב חודרני. החולים שבהם נכשל טיפול ב-Immucyst, נהנו משיעור חופשי מהישנות, כמו יתר המטופלים, והפרוגנוזה שלהם לא הייתה גרועה יותר.
תופעות לוואי
תופעות הלוואי הקשורות ל-Mitomycin C אינן רבות בהשוואה ל-Immucyst, והן כוללות בעיקר רגישות יתר וגרד, ושיעורן נמוך מאוד. תופעות הקשורות לדיכוי מח העצם אינן קיימות, מאחר שעקב גודל המולקולה אין ספיגה של Mitomycin C לדם ברמות מדכאות מח עצם.
פרוני וחבריו[9] בדקו אם תוספת תרמותרפיה משפיעה על ספיגת Mitomycin C לנסיוב. הרמות בנסיוב לאחר מתן 80 מ"ג (מיליגרם) Mitomycin C, במשולב עם יתר-חום, הגיעו ל-69 ננוגרם למיליליטר בלבד. הרמה המזערית (Minimal) של Mitomycin C בנסיוב, הדרושה לקבלת תוצא מדכא מח עצם, היא 400 ננוגרם למיליליטר.
עיקר תופעות הלוואי קשורות לאי נוחות בזמן הטיפול, הן בשל הצורך לשאת צנתר למשך כל זמן השטיפה והן בשל אי הנוחות שביתר-החום. שיעור תופעות הלוואי הגורם למטופל להפסיק את הטיפול הוא נמוך ובסדרות שונות שיעור הנשירה עומד על כ-5%-9%.
ביבליוגרפיה
- ↑ Jemal A, Siegel R, Ward E, et al. Cancer statistics, 2008. CA Cancer J Clin 2008;58(2):71-96
- ↑ Emami B, Song CW. Physiological mechanisms in hyperthermia: a review. Int J Radiat Oncol Biol Phys 1984;10:2289-295
- ↑ Horsman MR. Tissue physiology and the response to heat. Int J Hyperthermia 2006;22(3):197-203
- ↑ van der Heijden AG, Jansen CF, Verhaegh G, et al. The effect of hyperthermia on mitomycin-C induced cytotoxicity in four human bladder cancer cell lines. Eur Urol 2004;46(5):670-674
- ↑ Dayanc BE, Beachy SH, Ostberg JR, et al. Dissecting the role of hyperthermia in natural killer cell mediated anti-tumor responses. Int J Hyperthermia 2008;24(1):41-56
- ↑ Moskovitz B, Meyer G, Kravtzov A, et al. Thermo-chemotherapy for intermediate or high-risk recurrent superficial bladder cancer patients. Ann Oncol 2005;16(4):585-589
- ↑ Colombo R, Da Pozzo LF, Salonia A, et al. Multicentric study comparing intravesical chemotherapy alone and with local microwave hyperthermia for prophylaxis of recurrence of superficial transitional cell carcinoma. J Clin Oncol 2003;21(23):4270-4276
- ↑ Gofrit ON, Shapiro A, Pode D, et al. Combined local bladder hyperthermia and intravesical chemotherapy for the treatment of high-grade superficial bladder cancer. Urology 2004;63(3):466-471
- ↑ Paroni R, Salonia A, Lev A, et al. Effect of local hyperthermia of the bladder on Mitomycin C pharmacokinetics during intravesical chemotherapy for the treatment of superficial transitional cell carcinoma. Br J Clin Pharmacol 2001;52(3):273-278
קישורים חיצוניים
- כימו-תרמותרפיה לסרטן השלפוחית: סינרגו, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר שראל הלחמי, פרופ' עופר נתיב - המחלקה לאורולוגיה, מרכז רפואי בני ציון, והפקולטה לרפואה, חיפה, ד"ר גיא הידש - מרכז רפואי הדסה, ירושלים


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק