פוספו-פרוקטו-קינאז - Phosphofructokinase
| מדריך בדיקות מעבדה | |
| פוספו-פרוקטו-קינאז | |
|---|---|
| Phosphofructokinase | |
| שמות אחרים | PFK |
| |
| מעבדה | כימיה בדם |
| תחום | מעגל הגליקוליזה. |
| טווח ערכים תקין | בגיל מעל 12 חודשים 5.8-10.9 יחידות/גרם המוגלובין. ערכי ייחוס לא נקבעו מתחת גיל 12 חודשים. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
בחינה של תפקוד האנזים פוספו-פרוקטו-קינאז במהלך הגליקוליזה. מחקר גנטי של משפחות עם חסר phosphofructokinase; הערכת נבדקים המגיבים בחומרה לפעילות גופנית עצימה או עם מיופתיה; הערכת אנשים עם אנמיה המוליטית לא-ספרוציטית שהם Coombs שליליים.
תפקוד
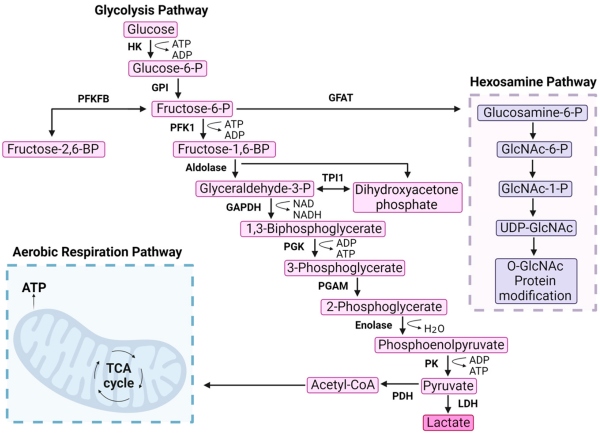
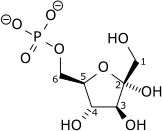
אנזים זה מזרחן fructose 6-phosphate בגליקוליזה. הטרנספר המקוטלז על ידי האנזים של קבוצת פוספוריל מ-ATP היא ריאקציה חשובה במספר ניכר של הליכים ביולוגיים (Hellinga ו-Evans ב-Nature משנת 1987). PFK מקטלז את הזרחון של fructose-6-phosphate ל-fructose-1,6-bisphosphate, שהוא צעד מפתח רגולטורי של המסלול הגליקוליטי (Wegener ו-Krause ב-Biochem Soc Transact משנת 2002, ו-Raben וחב' ב-Am J Hum Genet משנת 1995). האנזים מעוכב אלוסטרית על ידי ATP ומשופעל אלוסטרית על ידי AMP, מה שמצביע על כך שהצרכים האנרגטיים של התא מתמלאים כאשר מתקיים בו המסלול הגליקוליטי (Garrett ו-Grisham ב-Arch Biochem Biophys משנת 2012). האנזים PFK מתקיים כהומוטטרמר בחיידקים ובאדם (כאשר כל מונומר מכיל שני מקטעים דומים), וכאוקטומר בשמרים (בהם יש 4 מקטעי אלפא-PFK1, ו-4 מקטעי בטא (PFK2), כאשר האחרונים שבהם בדומה למונומרים של יונקים, מכילים 2 מקטעים דומים). חלבון זה יכול להשתמש במודל של morpheein לרגולציה אלוסטרית. ל-PFK יש בערך 300 חומצות אמינו לאורכו, ומחקרים מבניים של האנזים בחיידקים הראו שהוא מורכב משתי אונות דומות (alpha/beta): אחת מהן מעורבת בקישור של ATP, והאחרת משמשת מקום לקישור למצע ולאתר האלוטרי (אתר קישור רגולטורי שונה מהאתר הפעיל, אך משפיע על פעילות האנזים). תת-היחידות הטטרמריות הזהות, הן בעלות 2 קונפורמציות שונות: במצב "סגור", יון מגנזיום מגשר בין קבוצות הפוספוריל של תוצרי האנזים (ADP ו-fructose-1,6-bisphosphate); ואילו במצב "הפתוח" יון המגנזיום נקשר רק ל-ADP (Shirakihara ו-Evans ב-J Mol Biol משנת 1988), כאשר שני התוצרים מרוחקים זה מזה. הריאקציה ההפוכה מקוטלזת על ידי האנזים fructose-1,6-bisphosphatase.
משפחת ה-PFK
האנזים PFK שייך למשפחת ה-phosphofructokinase B (להלן PfkB) של קינאזות סוכרים (Park ו-Gupta ב-Cell Mol Life Sci משנת 2008). חברים אחרים במשפחה זו (הידועה גם כמשפחת Ribokinase) כוללים ribokinase (להלן RK), adenosine kinase (להלן AK), inosine kinase ו-1phosphofructokinase (Bork וחב' ב-Prot Sci משנת 1993). החברים של משפחת PfkB/RK מזוהים על ידי הנוכחות של שלושה motifs עם רצפים משומרים (Maj וחב' ב-Biochemistry משנת 2002). המבנים של אחדים ממשפחת החלבונים Pfk נקבעו במספר אורגניזמים, והפעילות האנזימטית של משפחה זו מראה תלות בנוכחות של יונים פנט-וולנטיים (Sigrell וחב' ב-Structure משנת 1998). PFK מצא בגרסאות איזופורמיות בשריר שלד, בכבד, ובטסיות, מה שמאפשר ביטוי ותפקוד רקמתי ספציפי. נמצא באדם שמספר שורות תאים סרטניים הגבירו את הקצב הגליקוליטי בקורלציה עם הגברת הכמות של PFKL (Sola-Penna וחב' ב-IUBMB Life משנת 2010, ו-Ausina וחב' ב-Biomed Pharmacother משנת 2018). ישנם שני אנזימים שונים של PFK באדם:
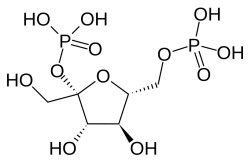
- הסוג phosphofructokinase 1 עושה שימוש במצע fructose-6-phsphate ליצירה של fructose-1,6-bisphosphate תוך טרנספר של קבוצת פוספאט מ-ATP ל-F-6-P ליצירה של ADP
- הסוג phosphofructokinase 2 עושה שימוש באותו מצע ליצירה של fructose-2,6-bisphosphate
האנזים PFK-1 נמצא בציטוזול של כמעט כל התאים. הוא קובע כיצד תאים מנצלים גלוקוז ליצירת אנרגיה. PFK-1 הוא חלבון גדול השייך לקבוצת הטרנספראז של אנזימים. תפקידו הראשוני הוא לווסת את קצב הגליקוליזה המייצרת אנרגיה, שהוא המסלול לנשימה אארובית ואנארובית.
גליקוליזה הוא המסלול המטבולי ההופך גלוקוז לפירובט, תוך יצירת כמות קטנה של אנרגיה תאית. שלב ה-rate limiting step בגליקוליזה: ריאקציה זו נחשבת "צעד מותנה" של הגליקוליזה כיוון שהוא בלתי הפיך, תחת מצב תאי נורמלי. ברגע שנוצר fructose-1,6-bisphosphate, הוא מתועל באופן כמעט אקסקלוסיבי לכיוון הצעדים הנותרים של המסלול הגליקוליטי. לפני צעד זה, מולקולת גלוקוז ההתחלתית יכולה להיות מופנית למסלולים אחרים, כגון מסלול ה-pentose phosphate או לכיוון סינתזה של גליקוגן. כיוון שריאקציית ה-PFK-1 היא השלב הבלתי-הפיך הראשון בגליקוליזה, הוא קובע את המהירות של כל התהליך הגליקוליטי. אנזים זה פועל כצוואר מטבולי, הקובע כיצד גלוקוז מנוצל ליצירת אנרגיה.
מנגנוני בקרה אלוסטרית
PK-1 הוא אתר ראשוני לרגולציה של גליקוליזה ביונקים, כאשר רגישותו מבוקרת באופן אלוסטרי. לאנזים ישנם מספר אתרי קישור השונים מהאתר הפעיל העיקרי שלו, מה שמאפשר למולקולות קטנות לפעול כסיגנלים מטבוליים, שיכולים לעכב או לשפעל את האנזים. הסיגנלים המונטוריים הראשוניים של PFK-1 הם הסטאטוס האנרגטי של התא, המשתקפים ביחס של ATP לבין תוצרי השבירה שלו, ADP ו-AMP. כאשר מאגרי האנרגיה התאיים גבוהים, ה-ATP המוגבר נקשר לאתר הרגולטורי ב-PFK-1 ופועל כמעכב אלוסטרי. קישור זה משנה את פעילות האנזים לפאזה של פעילות נמוכה, תוך הפחתת הזיקה שלו למצע, fructose-6-phosphate, מה שמאט את הגליקוליזה. גם ציטראט שהוא תוצר ביניים מוקדם של מעגל החומצה הציטרית, מעכב את PFK-1, תוך איתות שלתא יש מספיק נתוני בנייה. לעומת זאת, כאשר התא מנצל אנרגיה במהירות, ATP הופך ל-ADP ולאחר מכן ל-AMP. ריכוז גבוה של AMP פועל כמשפעל אלוסטרי, המסכל את ההשפעה המעכבת של ATP. כיוון שרמות AMP משתנות באופן דרמטי, ירידה קלה ב-ATP גורמת לעלייה גדולה ב-AMP, תוך סימון של צורך דחוף ביצירת אנרגיה. Fructose-2,6-bisphosphate, מולקולה שאינה חלק מהמסלול הגליקוליטי עצמו, היא משפעל אלוסטרי של PFK-1, תוך הגברת הזיקה של האנזים ל-F-6-P, וביטול העיכוב על ידי ATP. הריכוז התאי של fructose-2,6-bisphosphate, מבוקר על ידי אנזים אחר דו-תפקודי הידוע כ-PFK-2/FBPase-2. האנזים הרגולטורי האחרון קושר את פעילות PFK-1 לסיגנלים הורמונליים, כגון אינסולין וגלוקגון, מה שגורם לקואורדינציה של המסלול עם הצרכים הכלליים של הגוף, בעיקר בכבד.
ההשפעה של PFK-1 על מפגעים מטבוליים
בגלל העמדה של האנזים כמרכיב בקרה חשוב של גליקוליזה, הדיס-רגולציה של PFK-1 קשורה למספר מצבי מחלה. בסרטן, הרבה תאים סרטניים מפגינים את מה שידוע כ-Warburg Effect, תוך שהם נסמכים בחוזקה על גליקוליזה כמקור אנרגיה גם עם אספקה מתאימה של חמצן. השינוי המטבולי נתמך על ידי רגולציה מוגברת של אנזימים גליקוליטיים, כולל איזופורמים ספציפיים של PFK-1, המסייעים לספיגה של גלוקוז רב ולהמרתו ללקטאט. לדוגמה, תת-היחידה PFK-1 מהסוג הנוצר בכבד, לעיתים מבוטאת ביתר בגידולים, מה שמחיש את המטבוליזם הגליקוליטי החוץ לשגשוג אונקוגני. אי היכולת לפעול על גלוקוז גורמת להצטברות של תוצרי ביניים גליקוליטיים, מה שמוביל להצטברות אנומלית של גליקוגן ברקמת שריר. חסר חלקי של אריתרוציטים שכיח אף הוא, מה שגורם לשבירה מוגברת של תאים ולאנמיה מתונה. מטופלים חייבים להסתמך על דלק חלופי כגון חומצות שומן, מה שהופך את הדיאטה לגורם משמעותי בהתנהלות התסמינים.
משמעות קלינית
חוסר בפוספופרוקטוקינאז (Phosphofructokinase deficiency) גורם ל-glycogenosis type VII (להלן מחלת טארוי - Tarui disease), שהוא מפגע אוטוזומלי-רצסיבי המאופיין על ידי בחילות, הקאות, התכווצויות שרירים ומיוגלובינוריה, בתגובה לפעילות גופנית עצימה.
הוראות לביצוע הבדיקה
את הדם יש ליטול במבחנה כימית (פקק אדום או צהוב), אך מתקבלת גם נטילת הדם במבחנת ספירת-דם (EDTA פקק בצבע סגלגל). יש להפוך את המבחנה מספר פעמים כדי לקבל דם מעורבב מרבי. יש לשלוח למעבדה דם מלא במבחנה המקורית ללא aliquoting.
שיטת הבדיקה Kinetic Spectrophotometry (KS).
יציבות הדגימה הנשלחת בקירור - 11 יום.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק