פפטיד דמוי גלוקגון-1 - Glucagon-like peptide-1
| מדריך בדיקות מעבדה | |
| פפטיד דמוי גלוקגון-1 | |
|---|---|
| Glucagon-like peptide-1 | |
| שמות אחרים | incretin, GLP-1 |
| מעבדה | אנדוקרינולוגיה בדם |
| תחום | הורמון בעל תפקיד מרכזי בוויסות משק הסוכר בדם. |
| טווח ערכים תקין | רמות בפלזמה בצום 0–15 פיקומול/ליטר. |
| יוצר הערך | פרופ' בן-עמי סלע |
ההיסטוריה והאבולוציה של GLP-1
ההורמון הגלוקו-רגולטורי גלוקגון התגלה בשנת 1923 בתמצית לבלבית, ויוחס לו מיד תפקיד היפרגליקמי (Murlin וחב' ב-J Biol Chem משנת 1923). מחקר מאוחר יותר של Sutherland ו-DeDuve שהתפרסם באותו כתב-עת בשנת 1948, זיהה חומרים היפר-גליקמיים גם במיצוי של רירית המעיים, וקבע שגלוקגון אינו ייחודי ללבלב בלבד, ואכן תאים ברירית המעי של חולדה הדומים לתאי α בלבלב זוהו בהמשך (Orci וחב' ב-Diabetologia משנת 1968). תוך שימוש ב-radioimmunoassay עם נוגדנים כנגד גלוקגון, נמצא האחרון במערכת העיכול (Unger וחב' ב-Metabolism משנת 1966). בנוסף, זוהו במעי תאים אנדוקריניים שנצבעו על ידי נוגדנים כנגד גלוקגון, אך תאים אלה היו שונים מתאי α בלבלב בהיבט של מורפולוגיית הגרנולות שלהם, ותאים אלה כונו תאי L (Buffa וחב' ב-Cell Tissue Res משנת 1978). יתרה מכך, בשנת 1968 התברר שחומר בעל אימונו-ריאקטיביות דומה לזו של גלוקגון, הופרש בתגובה לנטילה פומית של גלוקוזה, שהיה שונה מגלוקגון מבחינה פיזיו-כימיקלית וביולוגית (Unger וחב' ב-J Clin Invest משנת 1968). בהמשך הסתבר שחומר דמוי-גלוקגון זה המופיע במעי הוא הטרוגני, ומורכב מלפחות שתי מולקולות שונות במשקלן המולקולרי (Valverde וחב' ב-Am J Med Sci משנת 1968). מחקרים אחדים הראו ששתי המולקולות האחרונות מכילות מקטע שלם של 29 חומצות אמינו המופיעות ברצף של גלוקגון (Holst ב-Biochem J משנת 1980 ובאותו כתב-עת משנת 1982, Bataille וחב' ב-FEBS Lett משנת 1982, ו-Thim ו-Moody ב-Peptides משנת 1981). אחת משתי הצורות מכילה הרחבה של octapeptide בקצה ה-C טרמינלי, והשנייה המכילה בנוסף להרחבה האמורה בקצה ה-C טרמינלי, גם תוספת של 30 חומצות אמינו בקצה ה-N טרמינלי. המולקולה הראשונה כונתה oxyntomodulin בשל השפעותיה על הרירית האוקסינטית בחזיר (Bataille וחב' ב-FEBS Lett משנת 1982), ואילו המולקולה השנייה כונתה glicentin כיוון שבזמנו הייתה השערה שהיא מכילה 100 חומצות אמינו (Sundby וחב' ב-Horm Metab Res משנת 1976), אם כי בהמשך התגלה בריצוף שלם שמולקולה זו מכילה רק 69 חומצות אמינו. ההרחבה של גלוקגון בקצה ה-N טרמינלי של glicentin זוהתה גם בתמציות של הלבלב, ממנו מולקולה זו נמצאה מופרשת במקביל לגלוקגון (Moody וחב' ב-Nature משנת 1981, ו-Thim ו-Moody ב-Biochim Biophys Acta משנת 1982). נראה אם כך ש-glicentin הוא proglucagon אשר בלבלב מבוקע לגלוקגון ולכמויות שווה-מולריות של הפפטיד עם ההרחבה בקצה ה-N טרמינלי שכונה GRPP או glicentin-related pancreatic polypeptide.
ממחקרים על הביוסינתזה של גלוקגון בתאי הלבלב השתמע שמולקולה עם משקל מולקולרי של בערך 10,000 דלטון, שכונתה בהמשך MPGF או major proglucagon fragment שלא הכילה רצף של גלוקגון, נוצרת במקביל לגלוקגון (Patzelt ו-Schug ב-FEBS Lett משנת 1981). כאשר פוענחו המבנים של הגן לגלוקגון וה-mRNA (Bell וחב' ב-Nature משנת 1983), התברר שביונקים מקטע עיקרי זה של proglucagon מכיל שני רצפים דמויי-גלוקגון המכונים GLP-1 ו-GLP-2 בהתאמה. דגים ועופות מכילים רק פפטיד דמוי-גלוקגון המתאים ל-GLP-1 (Lund וחב' ב-Proc Natl Acad Sci USA משנת 1982). העיבוד הדיפרנציאלי הבתר-תרגומי של proglucagon בלבלב לעומת עיבוד זה במעי ובמוח מתואר בתרשים למטה.
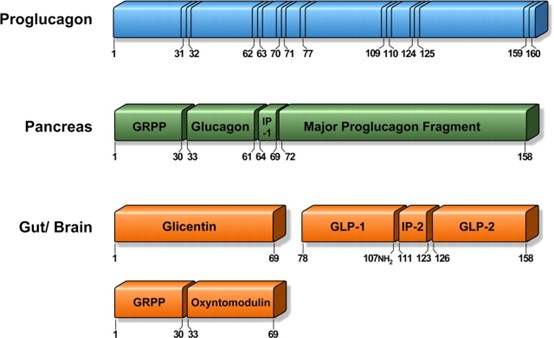
GRPP – glicentin-related pancreatic polypetide;
IP-1 - inverting peptide-1;
IP-2 – inverting peptide-2.
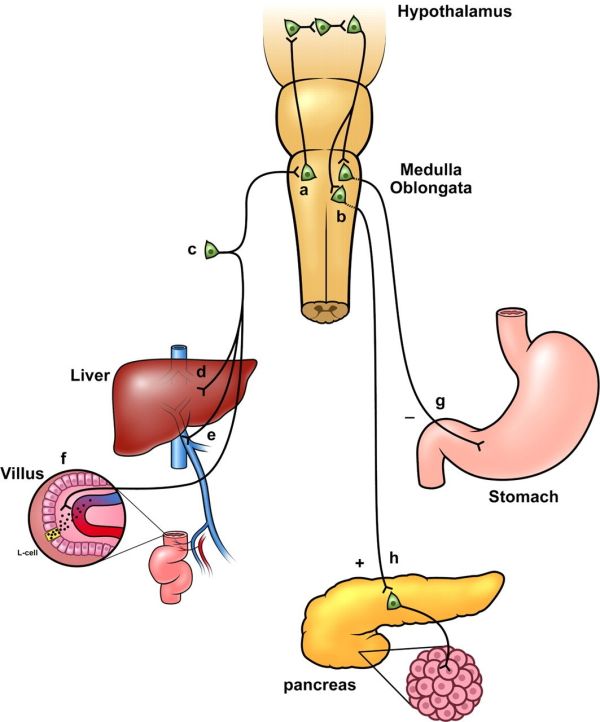
Glucagon-like peptide-1 (להלן GLP-1) הוא הורמון פפטידי שמשקלו המולקולרי 30–31 קילו-דלטון, הנובע מבתר-תרגום רקמתי ספציפי של הגן המקודד לפפטיד proglucagon. GLP-1 מיוצר ומופרש מתאי L האנטרו-אנדוקריניים במעי, כמו גם ממספר נוירונים בגרעין ה-solitary tract שהוא צרור הסיבים המוליך ב-medulla oblongata שבגזע המוח בעת צריכת אוכל.
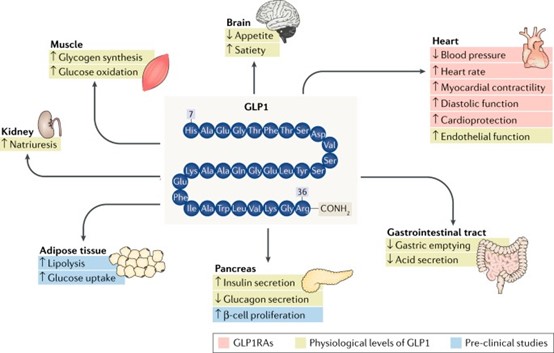
התפקודים הפיזיולוגיים של GLP-1
ל-GLP-1 יש מספר תפקודים פיזיולוגיים שהופכים אותו לנושא של מחקר אינטנסיבי כטיפול פוטנציאלי של סוכרת, שכן טיפול זה בעל משמעות ארוכת-טווח כמו גם השפעה מיידית (Toft-Nielsen וחב' ב-J Clin Endocrinol Metab משנת 2001, Meier וחב' ב-Crit Care Med משנת 2004, ו-Graaf וחב' ב-Pharmcol Rev משנת 2016). אף על פי שבעבר היו סבורים שהפרשת GLP-1 בחולים עם סוכרת type 2 מופחתת כתוצאה מהשפעה מוחלשת של incretin, נכון למועד כתיבת מאמר זה ברור שהפרשת GLP-1 אינה מופחתת בסוכרת type 2 בהשוואה לזו באנשים בריאים (Callana וחב' ב-Diabetologia משנת 2013). ההשפעה הבולטת ביותר של GLP-1 היא יכולתו לעודד הפרשת אינסולין במצבים של גלוקוזה מוגברת בדם. כאשר GLP-1 נקשר לקולטנים שלו המבוטאים על גבי תאי בטא בלבלב, הקולטנים נצמדים לתת-יחידות של חלבון G, תוך שפעול של adenylate cyclase המגביר את יצירת cAMP מ-ATP (Holst ב-Physiol Rev משנת 2007). בנוסף, GLP-1 מוודא שמאגרי אינסולין בתאי β מתמלאים מחדש למנוע חסר בהורמון האחרון בעת הפרשתו לדם, על ידי סיוע לשעתוק של הגן המקודד לאינסולין, ייצוב mRNA, וביוסינתזה של ההורמון (Baggio ו-Drucker ב-Gastroenterology משנת 2007, ו-Rondas וחב' ב-Obes Metab משנת 2013).
נראה ש-GLP-1 גם מגדיל את המסה של תאי β על ידי סיוע לשגשוג ול-neogenesis של תאים אלה בכך שהוא מעכב את האפופטוזיס שלהם (Rachmany וחב' ב-Age משנת 2013). נמצא ש-GLP-1 מעכב הפרשת גלוקגון כאשר רמות גלוקוזה בדם הן מעל הרמות של סוכר זה בצום. באופן קריטי, המהלך האחרון אינו משפיע על תגובת גלוקגון להיפו-גליקמיה. ההשפעה המעכבת של הפרשת גלוקגון מתווכת באופן בלתי-ישיר על ידי הפרשת סומטוסטטין, אם כי השפעה ישירה של סומטוסטטין לא יכולה להישלל באופן מוחלט (Gautier וחב' ב-Diabet Metab משנת 2008, ו-Seino וחב' ב-J Diabet Invest משנת 2010).
במוח, שפעול הקולטן של GLP-1 נכרך עם השפעות נוירו-טרופיות הכוללות נוירוגנזה (Li וחב' ב-Neurosci Lett משנת 2010, ו-Bertilsson וחב' ב-J Neurosc Res משנת 2008), כמו גם השפעות הגנתיות של מערכת העצבים הכוללות הפחתת איתות לנמק (DellaValle וחב' ב-Ann Clin Transl Neurol משנת 2014), והפחתת איתות לאפופטוזיס (Wang וחב' ב-w Neuroscience משנת 2012), הפחתת הפגיעה בתפקוד ובמות תאי תאי-עצב (Sharma וחב' ב-J Neurochem משנת 2014, ו-Perry וחב' ב-J Neurosc משנת 2014). במוח חולה, טיפול עם אגוניסט של הקולטן של GLP-1, כרוך בהגנה מפני מודלים של מחלות מושרות במכרסמים כגון פרקינסון (Li וחב' ב-Proc Natl Acad Sci USA משנת 2009), אלצהיימר (Wang וחב' ב-Neuroscience משנת 2010, ו-Perry וחב' ב-J Neurosci Res משנת 2003), פגיעה מוחית טראומטית, שבץ מוחי וטרשת נפוצה (DellaValle וחב' ב-Front Pharmacol משנת 2016). בהתאמה עם הביטוי של הקולטנים של GLP-1 בגזע המוח ובהיפותלמוס, נמצא ש-GLP-1 מסייע לתחושת השובע, ולפיכך מפחית את צריכת האוכל. כתוצאה מכך אנשים סוכרתיים המטופלים עם אגוניסטים של הקולטן של GLP-1, חווים הפחתה במשקלם. בקיבה, GLP-1 מעכב את התרוקנות הקיבה, את הפרשת החומצה בקיבה, ואת נדידת המזון אל מחוץ לקיבה, המפחיתים את התיאבון. על ידי האטת התרוקנות הקיבה, GLP-1 מפחית את עליית רמת גלוקוזה בדם לאחר ארוחה, שהיא תוצאה רצויה בסוכרתיים. בנוסף להשפעת GLP-1 במעי ובמוח, יש לו השפעות רגולטוריות ברקמות אחרות דוגמת הלב, הלשון, רקמת השומן, השרירים, העצמות הכליות, הכבד והריאות.
התוצר הראשוני GLP-1 (1-37) חשוף ורגיש לאמידציה ולביקוע פרוטאוליטי, המביאים ליצירת שני פפטידים (truncated) פעילים ביולוגית במידה דומה, GLP-1 (7-36) ו-GLP-1 (7-37) . המבנה השניוני של GLP-1 פעיל, כולל שני סלילוני α מעמדת 13-20 של חומצות האמינו, ומעמדה 24-35, המופרדים על ידי אזור מקשר. במקביל ל-GIP (או glucose-dependent insulinotropic peptide) GLP-1 הוא incretin ולפיכך בעל יכולת להפחית רמות סוכר על ידי תגבור הפרשת אינסולין. מלבד השפעותיו האינסולינו-טרופיות, נכרך GLP-1 עם מספר השפעות רגולטוריות וכאלה המסייעות להגנה. GLP-1 אנדוגני מתבקע במהירות על ידי dipeptidyl-peptidase-4 (להלן DPP-4) כמו גם על ידי neutral endopeptidase 24.11 (להלן NEP 24.11) והוא מתפנה דרך הכליות, מה שמקנה לו זמן מחצית חיים קצר של 2 דקות. כתוצאה מכך, רק 10-15% של GLP-1 מגיעים שלמים לצירקולציה, עם רמות פלזמה בצום של 0–15 פיקומולר. כדי להתגבר על ריכוז נמוך זה, פותחו אגוניסטים של הקולטן של GLP-1 כדי להגביר את פעילותו. בניגוד לתכשירים כלליים לטיפול כגון אינסולין או sulphonylurea, טיפול המבוסס על GLP-1 הנכרך עם איבוד משקל, וסיכון נמוך יותר של היפו-גליקמיה, שני שיקולים חשובים באלה עם סוכרת type 2.
ביטוי הגן
הגן המקודד ל-proglucagon מבוטא במספר איברים כולל בלוטת הלבלב (תאי α של איי לנגרהנס), המעיים (תאי L אנטרו-אנדוקריניים), והמוח (גזע המוח הקאודלי וההיפותלמוס). הביטוי של הגן הפנקראטי של proglucagon מגביר פעילותו בצום המשרה היפו-גליקמיה, ומעוכב על ידי אינסולין. לעומת זאת, הביטוי של הגן האינטסטינלי של proglucagon מופחת בצום, ופעילותו גדלה תוך צריכת מזון. ביונקים, שעתוק מביא ליצירת mRNA זהה בכל שלושת האיברים, מה שמתורגם לקודמן הפרוגלוקגוני של 180 חומצות אמינו. עם זאת, פפטידים שונים מיוצרים בתאים שונים (Marathe וחב' ב-Peptides משנת 2013). בתאי α בלבלב, proglucagon מבוקע על ידי prohormone convertase 2 (להלן PC 2) ליצירת glicentin-related pancreatic peptide (להלן GRPP ), גלוקגון, inverting peptide-1 (להלן IP-1) ו- major proglucagon fragment (להלן MPGP) במעי ובמוח, proglucagon עובר קטליזה על ידי PC 1/3 ליצירת glicentin המעובד בהמשך ל-GRPP ל-oxyntomodulin, ל-GLP-1, ל-intervening peptide-2 (להלן IP-2) ול-glucagon-like peptide-2 (להלןGLP-2). בתחילה, GLP-1 נחשב כמתאים ל-proglucagon (72-108) אך ריצוף של GLP-1 אנדוגני גילו מבנה המתאים ל-proglucagon (78-107), וממצא זה הוליד שתי מסקנות: האורך המלא של GLP-1 (חומצות אמינו 1–37) עובר קטליזה על ידי אנדו-פפטידאז ליצירת המקטע הפעיל ביולוגית GLP-1 (7-37). שנית, שייר גליצין בעמדה 108 של proglucagon, נמצא משמש כמצע לאמידציה של ארגינין בקצה ה-C טרמינלי, מה שיוצר אמיד GLP-1 (7-36) פעיל במידה שווה. באדם, למעלה מ-80% מה-GLP-1 המופרש עבר אמידציה (Deacon ו-Holst ב-Best Practice Res משנת 2009).
הפרשה
GLP-1 ארוז בגרנולות מפרישות ומופרש לתוך המערכת השערית של הכבד על ידי תאי L במעי, הממוקמים בעיקר בחלק הרחיקני (דיסטלי) של האילאום ובמעי הגס, אך גם בתריסריון ובמעי הריק (jejunum). תאי L הם תאים אפיתליאליים דמויי-משולש הנמצאים במגע ישיר עם נהור (lumen) המעי ועם הרקמה הנוירו-וסקולרית ולכן תאים אלה מגורים על ידי מרכיבי מזון שונים, או על ידי גורמים עצביים ואנדוקריניים. GLP-1 מופרש באופן דו-שלבי שהראשון בהם נמשך 10-15 דקות, והשלב השני נמשך 30-60 דקות מרגע צריכת המזון. שלב ההפרשה המוקדם נוצר על ידי איתות עצבי, על ידי פפטידים במעי או על ידי נוירוטרנסמיטרים. ראיה אחרת מציעה שכמות תאי-L הממוקמים בחלק הקריבני (פרוקסימלי) של ה-jejunum מספקת כדי לסייע לשלב המוקדם של הפרשת GLP-1 על ידי מגע ישיר עם חומרי המזון החולפים בנהור המעי הריק. פחות שנוי במחלוקת הוא השלב המאוחר של הפרשת GLP-1, הנגרם על ידי סטימולציה ישירה של תאי L במגע עם מזון מעוכל. לפיכך, קצב התרוקנות הקיבה, מהווה היבט חשוב בהיותו מווסת את כניסת המזון המעוכל למעי הדק בו מתרחש גירוי ישיר של תאי L. בעת ארוחה ומיד אחריה רמת GLP-1 בדם של בני-אדם עולה פי-2–3 בתלות בגודל הארוחה וסוג המזון. מרכיבי מזון כגון חומצות שומן, חומצות אמינו הכרחיות וסיבים תזונתיים, נמצאו מעודדים הפרשת GLP-1.
פחמימות במזון נכרכו עם מסלולי איתות שונים, המאתחלים דה-פולריזציה של ממברנת תאי L, מה שגורם לרמות מוגברות של +Ca2 ציטוזולי, ומשרה הפרשת GLP-1. חומצות שומן נכרכו עם גיוס של מאגרי +Ca2 תוך-תאי וכתוצאה מכך הפרשת +Ca2 לתוך הציטוזול. המנגנונים של הפרשת GLP-1 על ידי גירוי של חלבונים במזון, פחות ברורים, אך יש רמזים לכך שרמת חומצות אמינו במזון והרכבם, משחקים אף הם תפקיד בהפרשת GLP-1 (Ma וחב' ב-J Diabet משנת 2014).
פירוק והַפְחָתָה של GLP-1
מיד לאחר הפרשתו, GLP-1 חשוף ורגיש ביותר לפעילות קטליטית של האנזים פרוטאוליטי DPP-4. באופן ספציפי, DPP-4 מבקע את הפפטיד בקשר שבין Ala8-Glu9, מה שיוצר את האמיד (9–36) GLP-1 המהווה 60-80% מסך GLP-1 בצירקולציה. האנזים DPP-4 מבוטא באופן נרחב ברקמות אחדות ובסוגי תאים שונים ומופיע בהן כאנזים הקשור לממברנה והן בצורה מסיסה בצירקולציה. DPP-4 מבוטא על פני תאי אנדותל, כולל אלה הסמוכים ישירות לאתרי הפרשה של GLP-1. כתוצאה מכך, פחות מ-25% מ-GLP-1 מופרש מהמעי כמולקולה שלמה. בנוסף, ולכאורה בגלל הריכוז הגבוה של DPP-4 שמוצאים בהפטוציטים, 40-50% משאר ה-GLP-1 הפעיל, עובר פירוק בכבד. לפיכך רק 10-15% מהפעילות של GLP-1 המופרש מגיעה לצירקולציה. האנדופפטידאז הנייטרלי NEP24.11 הוא מטלופפטידאז המכיל אבץ הקשור לממברנה שמופיע באופן נרחב במספר רקמות, אך ריכוזו גבוה במיוחד בכליות, והוא מקובל כאחראי לפירוק המהיר של GLP-1. אנזים זה מפרק בעיקר פפטידים בצד ה-N טרמינלי של חומצות אמינו ארומטיות, ומוערך שהוא אחראי לפירוק של עד 50% מ-GLP-1. עם זאת, הפעילות של NEP24.11 באה לביטוי רק אם נמנעת פעילות DPP-4, שכן עד ש-GLP-1 מגיע לכליות הוא כבר עבר ביקוע מסיבי על ידי DPP-4.
הקולטן של GLP-1
הקולטן של GLP-1 הוא קולטן class 2 הקשור לחלבון G (Mayo וחב' ב-Pharmacol Rev משנת 2003), ושובט לראשונה על ידי Thorence בשנת 1992. בהמשך שובט גם הקולטן של GLP-1 על פני תאי β בלבלב (Thorence וחב' ב-Proc Natl Acad Sci USA משנת 1992). הקולטן של GLP-1 שייך לאותה משפחת קולטנים של גלוקגון ושל GIP (או gastric inhibitory peptide}, קולטן הנקשר באופייניות לחלבון G דרכו הוא מפעיל את האנזים adenylate cyclase (Thorence ו-Widmann ב-Acta Physiol Scand משנת 1996, ו-Wheeler וחב' ב-Endocrinology משנת 1995). קולטן זה מפוזר באופן נרחב באיי הלבלב, במוח, בלב, בכליות ובמעי (Alvarez וחב' ב-J Neurochem משנת 2005, Bullock וחב' ב-Endocrinology משנת 1996, Campos וחב' באותו כתב-עת משנת 1994, ו-Wei ו-Mojsov ב-Acta Physiol Scand משנת 1996). גם על גבי התאים הפריאטלים בקיבה מבוטא הקולטן ל-GLP-1 (Schmidtler וחב' ב-Am J Physiol Gastrointest Liver Physiol משנת 1994). בתאים הפריאטלים, שפעול של קולטן זה, מגביר את הצטברות aminopyrine המהווה אינדיקטור בלתי ישיר של הפרשת חומצה (Schepp וחב' ב-J Pharmacol משנת 1994), כאשר in vivo, GLP-1 מעכב בחוזקה הפרשת חומצה. זוהה רק קולטן אחד של GLP-1 בלבלב, במוח או בקיבה. בריאות של חולדה זוהה קולטן השונה מזה של הלבלב בנדידה האלקטרופורטית שלו, ואף על פי שרצף חומצות האמינו של שני הקולטנים היה זהה, נראה שיש הבדל בהרכב השרשרת הסוכרית שלהם, אם כי משמעות ביולוגית של הבדל זה אינה ברורה (Lankat-Buttgereit וחב' ב-Exp Clin Endocrinol משנת 1994). Exendin 9-39 פועל כאנטגוניסט ספציפי ופוטנטי כנגד הקולטן של GLP-1. קיימים חילוקי דעות בדבר ההשפעות של GLP-1 על רקמת השומן, על רקמת השריר ועל הכבד, וזאת סביב השאלה האם הקולטן של GLP-1 מבוטא ברקמות אלו. נראה שבכלבים קולטן זה מבוטא ברקמות השריר והשומן (Sandhu וחב' ב-Diabetes משנת 1999), ועכברים מבטאים קולטן זה בכבד.
GLP-1, תפקוד תאי β, וסוכרת type 1
אגוניסטים של GLP-1R יכולים להפחית דלקת באיי הלבלב, למנוע או לעכב התפתחות של כשל של תאי β במודל של עכברים סוכרתיים לא-שמנים, על בסיס סוכרת אוטו-אימונית, תרחיש שעודד מחקרים על הפוטנציאל התרפויטי של אגוניסטים של GLP-1R בטיפול בסוכרת type 1. טיפול אינטנסיבי עם exenatide (במינון יומי של עד 40 מיקרוגרם) של אנשים שסובלים מסוכרת זו לתקופה של 21 שנים, עם או ללא daclizumab למשך 6 חודשים הביא לירידה במשקל, לירידה במינון השגרתי של אינסולין, ואף שיפר את התגובה לאינסולין (Rother וחב' ב-Diabetes Care משנת 2009). אף-על-פי-כן, ולמרות קריטריונים של היכללות בניסוי זה שכללו זיהוי של c-peptide בדם, לא נמצא שיפור בתפקוד השארי של תאי בטא במטופלים עם exenatide.
אגוניסטים של GLP-1R משפרים ex vivo את ההישרדות של איי הלבלב באדם, או לאחר השתלת איים אלה לחיות (Campbell ו-Drucker ב-Cell Metab משנת 2013). עם זאת, היעילות של השפעת אגוניסטים אלה כתרפיה אדג'ובנטית לשימור התפקוד של תאי בטא בחולים עם סוכרת type 1 שעברו השתלת איי לבלב, נותרה בלתי מוכחת. למרות מחקרים קדם-קליניים שכרכו אגוניזם של GLP-1R עם הפחתת דלקת, הגברת התפקוד של תאי β והישרדות של האיים המושתלים, לא נמצאה עדיין עדות משכנעת ליתרונות של טיפול עם אגוניסטים של GLP-1R. מאכזבות במידה שווה התוצאות של ניסויים קליניים שבחנו את היעילות של liraglutide כתרפיה אדג'ובנטית לאינסולין בחולים עם סוכרת type 1. הוספת liraglutide במקביל לטיפול עם אינסולין, אמנם הביאה לירידה במשקל, ולהפחתה במינון אינסולין, אך רק לירידה צנועה בהמוגלובין A1C, ואף הגבירה תופעות לוואי גסטרו-אנטרליות, קטואצידוזיס והיפו-גליקמיה תסמינית (Ahren ב-Diabetes Care משנת 2016, ו-Mathieu וחב' באותו כתב-עת מאותה שנה).
GLP-1 ורגישות לאינסולין ברקמות היקפיות
איבוד משקל ואגוניזם ל-GLP-1 משפרים את הרגישות לאינסולין בבעלי חיים ובאדם. עם זאת, יש ראיות לכך שאגוניזם ל-GLP-1 הבלתי תלוי בגירוי להפרשת אינסולין, או בעיכוב של הפרשת גלוקגון, אינו משפיע ישירות על האיתות של אינסולין או על קליטת גלוקוזה בכבד, בשריר או ברקמת השומן. מחקרים בהם נעזרו בריצוף של RNA, בהיברידיזציה in situ ובכימות של נוגדנים בנסיוב כנגד GLP-1R, לא זיהו ביטוי של GLP-1R בהפאטוציטים, במיוציטים בשריר או באדיפוציטים (Panjwani וחב' ב-Endocrinology משנת 2013). קולטנים של GLP-1 ב-CNS, מפקחים על הרגישות לאינסולין בבעלי חיים, והשפעול של קולטנים אלה בעצבים היקפיים או בכלי-דם, עשוי להגביר שפיעת דם ברקמות, ולווסת באופן בלתי ישיר פעילות אינסולין. לדוגמה, עירוי של GLP-1 מגביר גיוס מיקרו-וסקולרי בשרירי שלד באדם באופן בלתי תלוי באינסולין מה שעשוי לחזק פעילות מקומית של אינסולין (Sjoberg וחב' ב-Am J Physiol Endocrinol Metab משנת 2014). לעומת זאת, החדרה כרונית של liraglutide במינון יומי של 1.8 מיליגרם למשך 12 שבועות לחולים עם סוכרת type 2, לא שינתה את הזליחה הקפילרית או את הפעילות הואזו-מוטורית שנמדדה במצבי צום או מיד לאחר ארוחה, זאת למרות ירידה של 1.7% ברמת המוגלובין A1C על פי Smits וחב' ב-Diabetes Obes Metab משנת 2016). תוצאות סותרות אלו יכולות לשקף הבדלים במצעים הווסקולריים, הבדלים בשפעול החריף או הכרוני של GLP-1R, הבדלים מבניים או תפקודיים באגוניסטים של GLP-1R, או הבדלים באוכלוסיות הנחקרות.
אגוניזם של GLP1-R והבקרה על משקל הגוף
יש ראיות חזקות לכך שאגוניזם לקולטן של GLP-1 מפחית צריכת מזון ומסייע להורדה במשקל (Drucker ו-Nauck ב-Lancet משנת 2006). ואגוניסט אחד של GLP-1R, liraglutide, אושר לטיפול ב- obesity (Astrup וחב' ב-Lancet משנת 2009). אגוניסט זה משפעל את רקמת השומן החום, ומגביר את הוֹצָאָת האנרגיה במכרסמים באופן שאינו תלוי בפעילות לוקו-מוטורית, דרך מסלולי המערכת העצבית הסימפתטית. עירוי של GLP-1 גם כן מפחית אגירת שומנים היקפית באדיפוציטים לבנים של עכברים רזים, על ידי מנגנונים התלויים בשפעול של SNS או somatic nervous system), פעילות הנחסמת בעכברים המוזנים בדיאטה עתירת-שומן (Nogueiras וחב' ב-J Neurosci משנת 2009). טיפול של אנשים מאוד שמנים עם Liraglutide במינון יומי של 1.8-3.0 מיליגרם, הביא לצריכת אנרגיה מופחתת ולאיבוד משקל, לחמצון מתון של שומנים, ולהפחתה בהוצאת אנרגיה, תהליך שאושש על ידי קלורימטריה (van Can וחב' ב-Int J Obes משנת 2014).
הפרשה, מדידה ומטבוליזם של GLP-1
מדידה בפלזמה של הביטוי של תוצרי הגן המקודד לפרוגלוקגון, תדרוש מדידה של לפחות 8 פפטידים שונים, שלושה מבלוטת הלבלב (גלוקגון, GRPP ומקטע עיקרי של proglucagon) וחמישה פפטידים שמקורם במעי (glicentin oxyntomodulin ,GLP-1,GLP-2 ו-intervening peptide 2). לצורך הערכה של הסטאטוס ההפרשתי של תאי L במעי, מוצע למדוד רק תוצר יחיד של proglucagon, כיוון שכבר הוכח שתוצרים של הלבלב ושל המעי מופרשים תוך סינכון ובכמויות אקווי-מולריות. עם זאת, כל אחד מתוצרי proglucagon מופרש מהצירקולציה בקצב הספציפי שלו, ולפיכך הערכה אמינה של ההפרשה והריכוז בפלזמה של כל אחד מהתוצרים האמורים, מחייבת מדידה ספציפית שלו. השיטות למדידת תוצרים המכילים גלוקגון, חוזרות שנים לאחור למדידות המקוריות של גלוקגון בשיטת RIA (Heding ב-Diabetologia משנת 1971, ו-Holst ב-Gastroenterology משנת 1983). התגובה הצולבת של מספר antisera עם חומר של המעי, גרם לבלבול משמעותי באותן מדידות קדומות. Antisera המכוונים כנגד המקטע המרכזי של גלוקגון, מגיבים עם כל תוצר המכיל מקטע זה, כגון גלוקגון, glicentin ,oxyntomodulin ו-proglucagon 1-61 (Baldissera ו-Holst ב-Diabetologia משנת 1986), שהאחרון בהם יכול להיות מופרש בכמויות קטנות מהלבלב וכן מהמעי. צריכה פומית של פחמימות, הפרשה של תאי α בלבלב מדוכאת, ואילו הפרשת תאי L במעי מתגברת, ובמקרה זה הפרשת תאי L נותנת הערכה סבירה, והיא זכתה להגדרה "enteroglucagon secretion". מידע יותר ספציפי עשוי להתקבל עם antisera המגיבה באופן בלעדי עם הקצה ה-C טרמינלי הלא מאורך של גלוקגון. Antisera זו אינה מגיבה עם glicentin או עם oxyntomodulin, ומודדת לפיכך גלוקגון לבלבי. על ידי החסרה של התוצאה המתקבלת עם ה-antisera כנגד הקצה ה-C טרמינלי, מהתוצאה המתקבלת עם ה-antisera כנגד המקטע המרכזי של גלוקגון, ניתן לקבל בעיקרון את הריכוז של הפפטידים המופרשים מהמעי, glicentin ו-oxyntomodulin.
בעיות הספציפיות והדיוק ששיבשו את מדידות גלוקגון, רלוונטיות גם למדידות של GLP-1 ו-GLP-2 . גם כאן נוגדנים כנגד המקטע המרכזי של גלוקגון, מגיבים עם תוצרי המעי והלבלב. באדם, כמעט כל הקצה ה-C טרמינלי של GLP-1 מהמעי עבר אמידציה, ולכן מדידות המכוונות כנגד הקצה ה-C טרמינלי שעבר אמידציה תראינה באופן אמין הפרשת של GLP-1 מהמעי (זאת אף על פי שריכוזים קטנים של GLP-1 351-amide המופרשים מהלבלב אינן יכולות להישלל. מדידות במכרסמים או בחזירים בהם GLP-1 7-36amide כמו גם GLP-1 7-37 מיוצרים במעי מהוות בעיה מיוחדת. בעיקרון, מדידות המכוונות כנגד הקצה ה-N טרמינלי השלם, יכולות להיות שימושיות כאן (Gutniak וחב' ב-Diabetes Care משנת 1997), כמו גם מדידות בשיטת sandwich בהן נוגדן אחד מכוון כנגד הקצה ה-N טרמינלי, והנוגדן האחר מכוון כנגד הקצה ה-C טרמינלי אך מסוגל להגיב עם הצורה שעברה אמידציה וכן עם זו עם הארכה של גליצין. מספר מדידות מבוססות על עיקרון זה (Vilsboll וחב' ב-J Clin Endocrinol Metab משנת 2003), וערכה אחת אף זמינה מסחרית. הבעיה הגדולה ביותר עם הגישה הזו, קשורה להתפרקות המהירה של GLP-1 הרגיש במיוחד לפעילות הקטליטית של האנזים dipeptidyl peptidase IV (להלן DDP-IV) המבקע את 2 חומצות האמינו בקצה ה-N טרמינלי (Deacon וחב' ב-J Clin Endocrinol Metab משנת 1995).
המטבוליט שנוצר, GLP-1 9-36 amide אינו פעיל, ויכול אף לפעול כאנטגוניסט תחרותי לקולטן של GLP-1 (Knudsen ו-Pridal ב-Eur J Pharmacol משנת 1996), אף על פי שיצירתו אינה גורמת לאנטגוניזם in vivo (Zander וחב' ב-Diabetologia משנת 2006). במחקרים על ההפרשה של GLP-1 מהאילאום של חזירים נמצא שחלק גדול מאוד של GLP-1 שעוזב את המעי כבר התפרק למטבוליט בלתי-פעיל (Hansen וחב' ב-Endocrinology משנת 1999). בראשונה, פירוק זה נחשב שהוא מהווה כשני שלישים מכלל הכמות המופרשת של GLP-1, אך מחקרים בהמשך גילו שגם המעי של חזיר מפריש כמויות משמעותיות של GLP-1 9-37 שלא עבר אמידציה, נתון שלא נלקח בחשבון במחקר המקורי (Hansen וחב' ב-Am J Physiol Endocrinol Metab משנת 2000). לפיכך, פחות מ-25% מה-GLP-1 המופרש עוזב את המעי כמולקולה פעילה ובלתי מבוקעת. דגרדציה דומה של 40-50% של ה-GLP-1 מתרחשת בכבד (Deacon וחב' באותו כתב-עת משנת 1996), ולכן החישוב הוא שרק 10-15% מ-GLP-1 שהופרש זה עתה משם מגיע לצירקולציה הסיסטמית כמולקולה בלתי פגועה. נתון זה מנוגד לעובדה שלמעשה כל ה-GLP-1 האגור בגרנולות של תאי L, מצוי כמולקולה בלתי מבוקעת. האנזים המבקע, DDP-IV מבוטא לא רק ב-brush border של האנטרוציטים, אלא גם בתאי האנדותל המרפדים את הקפילרות של ה-lamina propria. המטבוליטים של GLP-1 מתפנים במהירות בעיקר בכליות, עם זמן מחצית חיים של 4–5 דקות (Meier וחב' ב-Diabetes משנת 2004). ידוע גם ש-GLP-1 משמש מצע לאנזים neutral endopeptidase 24.11 (Hupe-Sodmann וחב' ב-Peptides משנת 1997), ועיכוב של אנזים זה יגביר את ההישרדות של GLP-1 אנדוגני ואקסוגני in vivo. כתוצאה מהביקוע האינטנסיבי של GLP-1 על ידי 2 האנזימים האמורים, הרמות בפלזמה של ההורמון השלם נמוכות ביותר, והן אפילו לא תעלינה משמעותית לאחר ארוחה קלה (Vilsboll וחב' ב-Diabetes משנת 2001).
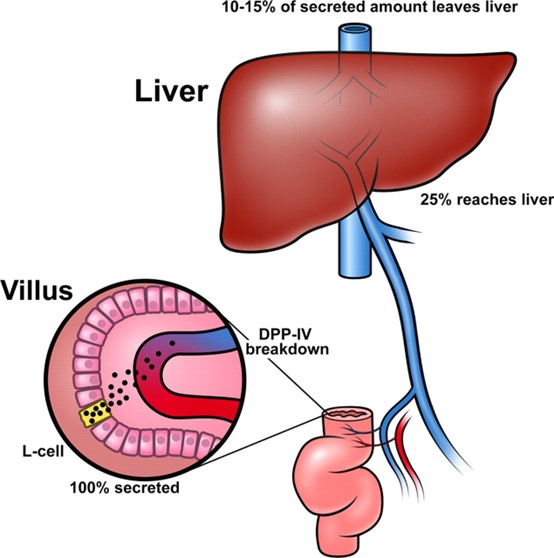
הפרשת GLP-1 מגורה על ידי חומרי מזון בנהור המעי, וההורמון הזה עובר דיפוזיה תוך חציית ה-basal lamina לתוך ה-lamina propria, ובקפילרות הוא נבקע על ידי DPP-IV, וכך רק 25% ממנו מגיע לצירקולציה השערית. בכבד, 40-50% של ה-GLP-1 נהרסים, וכך רק 10-15% של GLP-1 נכנסים לצירקולציה הסיסטמית ויכולים להגיע ללבלב או למוח דרך המסלול האנדוקריני.
הוראות לביצוע הבדיקה
רמת GLP-1 בנסיוב צריכה להתבצע לפחות 8 שעות לאחר הארוחה האחרונה. לאחר דגימת הדם במבחנה כימית (פקק אדום או צהוב) יש לסרכז ואת הנוזל העליון יש להקפיא מיד. בגלל הרגישות הגדולה של GLP-1 לפעילות פרוטאוליטית מומלץ להוסיף למבחנה לפני נטילת הדם מעכב סרין פרוטאזה phenylmethylsulfonyl fluoride (PMSF) או מעכב טריפסין כגון אפרוטינין (trasylol). המדידה מתבצעת בשיטת ELISA.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק