קווי הנחיה קליניים לתסמונת דלקתית רב-מערכתית בילדים בעקבות תחלואה בקורונה
|
| ||
|---|---|---|
| קווי הנחיה קליניים לתסמונת דלקתית רב-מערכתית בילדים בעקבות תחלואה בקורונה (תדר"ק) | ||
| 250px | ||
תסמיני המחלה
| ||
| הוועדה המקצועית | האיגוד הישראלי לרפואת ילדים | |
| תחום | ילדים | |
| קישור | באתר חיפא | |
| תאריך פרסום | 1 בספטמבר 2020 | |
| הנחיות קליניות מתפרסמות ככלי עזר לרופא/ה ואינן באות במקום שיקול דעתו/ה בכל מצב נתון | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – קורונה
מבוא
הביטויים של זיהום עם 2-SARS-Cov בילדים הם לרוב קלים, אולם במקרים נדירים, פחות מ-1 אחוז, עלולים להופיע לאחר תקופת הזיהום החריף ביטויים קשים, שהתבטאותם שונה מאשר במבוגרים. באפריל 2020, הופיעו דיווחים ראשונים על ילדים שמחלתם הסתמנה כשילוב בין מחלת Kawasaki לא קלאסית ובין Toxic Shock Syndrome) TSS)[1] מאז הופיעו דיווחים ממקומות שונים בעולם[2][3][4][5][6].
התסמונת כבר זכתה בכינויים שונים. בגלל הדימוי וחפיפה לתסמונת Kawasaki והקשר שלה עם מחלת 19-Covid, המונח Co-wasaki הוצע לשם קצר ונוח. השם הרשמי המקובל ביותר הוא Paediatric Inflammatory Multisystem Syndrome-Temporally associated with Covid-19 או לקיצור PIMS-TC. כינויים אחרים כוללים:
- Paediatric Multisystem Inflammatory Syndrome (PMIS)
- Multisystem Inflammatory Syndrome in Children (MIS-C)
- Pediatric Hyperinflammatory Syndrome
- Pediatric Hyperinflammatory Shock
במסמך זה הביטוי "תסמונת" מכוון לתסמונת זו (תדר"ק - תסמונת דלקתית רב-מערכתית בילדים בעקבות תחלואה בקורונה).
הפתוגנזה ופתופיזיולוגיה של תדר"ק
הפתופיזיולוגיה של תדר"ק אינה מובנת היטב. הוצע כי התסמונת נובעת מתגובה חיסונית חריגה לנגיף, עם קווי דמיון למחלת Kawasaki, MAS (Macrophage Activation Syndrome) ו-CRS (Cytokine Release Syndrome). המנגנונים שבאמצעותם מפעילה 2-SARS-CoV את התגובה החיסונית הלא תקינה אינם ידועים. התאוריה המוצעת היא שמדובר התהליך בתר-זיהומי, בהתבסס על תזמון העלייה של מקרים אלה כחודש לאחר שיא מקרי 19-Covid.
מבוגרים הסובלים מאי ספיקת נשימה חמורה מזיהום 2-SARS-CoV, חווים התדרדרות קלינית, לרוב, כשבוע לאחר הופעת המחלה, הנגרמת מדיסרגולציה (Dysregulation) של מערכת החיסון, ופחות מפגיעה נגיפית ישירה בתאי הריאה. נראה כי לילדים ביטויים ריאתיים חמורים פחות בהשוואה למבוגרים, ייתכן שכתוצאה מביטוי גנטי נמוך יותר של קולטן 2 ACE (Angiotensin Converting Enzyme)[7][8]. הפרעת האיזון של מערכת החיסון ב 19-Covid במבוגרים מאופיינת בלימפופניה, בעיקר תאי NK ,CD4 ו-B, וייצור מתמשך של ציטוקינים פרואינפלמטורים כגון 6-IL (Interleukin-6) ו-TNF-a (Tumor Necrosis Factor-a). במחלת Kawasaki, קיים מצב Hyper-inflammatory המאופיין ברמות גבוהות של TNF ,IL-6 ,IL-10 ,IL-17 ו-G-CSF[9]. כמו כן, ניתן לשער כי תסמונת זו מהווה תגובה של Hyper-inflammatory לאחר מחלת 19-Covid סימפטומטית/א-סימפטומטית[10].
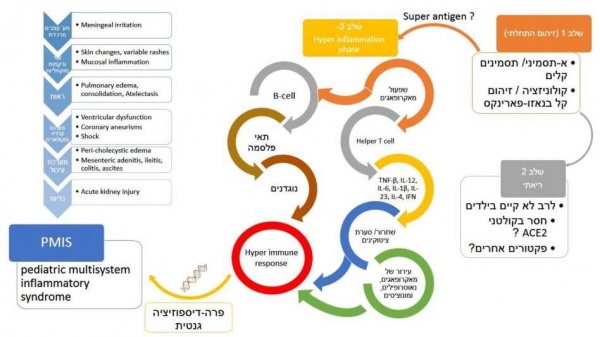
התסמונת מתפתחת ב-3 שלבים:
זיהום ראשוני (I Phase) הוא לרב א-תסמיני/מביא לתסמינים קלים בילדים.
השלב הריאתי (Phase II) עלול להיות חמור במבוגרים, בילדים לרב קל או שאינו קיים.
הזיהום הראשוני מעורר מצב היפר-אינפלמטורי (Stage III): אקטיבציה של מאקרופאגים, ובהמשך עירור של תאי T-helper > שחרור של ציטוקינים, מאקרופאגים, נויטרופילים ומונוציטים, וכן תאי B, תאי פלזמה ויצירת נוגדנים.
חוסר איזון זה קשור בסינדרום תדר"ק בילדים[10].
היבטים קליניים ואפידמיולוגיים
חלק זה מחולק לתיאור תסמונת הקלינית והאפידמיולוגית, האפיונים המעבדתיים, והגדרת מקרה. התסמונת תדר"ק מאופיינת על ידי תמונה קלינית ואפידמיולוגית, אולם, כמו בכל מצב ברפואה, חולים שונים מתייצגים עם מגוון וחומרה שונה של תסמינים.
להלן התסמינים המדווחים בתסמונת על פי סיווג למספר מרכיבים.
- תסמינים כלליים ומערכתיים:
- תסמינים המודינמיים:
- הלם קרדיווסקולארי או נפילת לחץ דם
- תסמיני מיוקרדיטיס, פריקרדיטיס או וולבוליטיס
- פגיעה בעורקים כליליים
- עליה ב-Pro-BNP או בטרופונין
- מעורבות מערכת נוספת כולל כליתית או עצבית להוציא נשימתית
- העדר תסמינים של זיהומים אחרים ספציפיים
- קריטריונים אפידמיולוגים ב־6 שבועות לפני המחלה הנוכחית:
- מגע קרוב וממושך עם חולה קורונה מאומת מעבדתית
- מגע קרוב וממשוך עם חולה עם תסמינים קליניים מתאימים למחלת קורונה שהיה לו מגע קורונה מאומת מעבדתית
- שהייה באזור עם התפרצות משמעותית של מחלת קורונה
- מתגורר במוסד או מעון של קשישים או חסויים
בדיקות ובירור
מטרות
מטרות הבירור של התסמונת הן:
- לאושש את האבחנה של תדר"ק
- לשלול מחלות אחרות
- להעריך את חומרת השינויים המעבדתיים
הגדרות מקרה שפורסמו, בעיקר אלה של הארגון העולמי לבריאות WHO (World Health Organisation)[11], המכללה המלכותית של פדיאטריה ובריאות הילד הבריטי RCPCH (Royal College of Paediatrics and Child Health)[12], ה-CDC (Centers for Disease Control) האמריקאי[13] והחברה הקנדית לרפואת ילדים Canadian Paediatric Society) CPS) מדגישות שאין בדיקה מעבדתית אחת המאפיינת את התסמונת. עדות להפרעה תפקודית רב-מערכתית, עליה במדדי דלקת והפרעות במערכת הקרישיות אינם ספציפיים או מספיקים, אבל הכרחיים בכדי לקבוע את אבחנה. לאור החפיפה עם מחלות קשות אחרות, חשוב לשלול זיהומים אחרים על ידי בירור מתאים. החשש שקיים קשר בין התסמונת ובין 19-Covid הוא בעיתוי הופעתה באמצע פנדמיה של 2-SARS-CoV. קיימת חשיבות באיתור עדות לזיהום עם הנגיף, או בעזרת איתור DNA (Deoxyribonucleic acid) דרך RT-PCR (Reverse Transcription Polymerase Chain Reaction) או דרך סרולוגיה, ואכן ברוב החולים (אבל לא בכולם) נמצאה עדות כזאת.
בלוחות מטה מופיעים:
- אפיונים מעבדתיים והדמיתיים
- הבירור המומלץ
רצוי לבצע בירור מקיף אם כי לא כול הבדיקות זמינות בכול בית חולים.
אפיונים מעבדתיים והדמיתיים
| סוג בירור | בירור | תוצאה צפויה | ציטוט |
|---|---|---|---|
| המטולוגיה | המוגלובין | אנמיה | [4][12] |
| ספירה לבנה | Neutrophilia או תקין | [4][12][13][14][15] | |
| Bandaemia | [5] | ||
| Lymphopaenia | [4][5][12][13][15] | ||
| טסיות דם | Thrombocytopaenia | [1][4][5][12][15] | |
| NK cells | נמוך | [3] | |
| Fibrinogen | תקין או לא תקין | [3][4][12][13] | |
| D-dimers | גבוהים | [1][3][5][11][12][13][16] | |
| PT, PTT | מאורך | [11] | |
| מדדי דלקת | CRP | גבוה | [1][4][11][12][13][14][15][16] |
| Procalcitonin | גבוה | [1][11][13][14][17] | |
| Ferritin | גבוה | [1][4][5][12][13][15] | |
| ESR | מואצת | [3][11][13] | |
| מיקרוביולוגיה | |||
| תרבית דם | שלילית | [3][11][12] | |
| משטח נסו-פרינגיאלי או אורו-פרינגיאלי לSARS-CoV-2-PCR | חיובי או שלילי | [1][3][4][11][12][16][18] | |
| סרולוגיה ל-SARS CoV-2 | רובם חיובי IgG ו/או IgM (Spike nucleocapsid ,trimer) | [3][4][5][11][16][18] | |
| IgA | [16] | ||
| בדיקה אנטיגנית ל-SARS-CoV-2 | [5] | ||
| וירוסים אחרים | שלילי | [12] | |
| ביוכימיה | אוראה, קריאטנין | תקין או לא תקין | [4][12] |
| נטריום | נמוך | [3][12] | |
| אנזימי כבד | גבוהים | [3][4] | |
| LDH | גבוה | [4][12][13][15] | |
| Triglycerides | גבוהים | [3][12] | |
| גזים | ייתכן חמצת, היפוקסיה | [12] | |
| לקטט | גבוהה | [12] | |
| Troponin | גבוה | [1][3][4][5][11][12][16] | |
| CK | גבוה | [3][12] | |
| אלבומין | נמוך | [1][4][12][13][15] | |
| IL-10 | גבוה | [12] | |
| IL-6 | גבוה | [3][5][12][13][14][16][19] | |
| Cytokines: IL-2R, IL-18, CXCL9, IL-8, IFN-Y | מוגברים | [5] | |
| Cytokines: TNF-a, IL-1b, 2, 4, 5, 13 | תקין | [5] | |
| (NT-pro BNP (BNP | גבוה | [1][3][4][5][11] | |
| הדמיה | בדיקת על-שמעית של הבטן (US) | אילאיטיס, קוליטיס, הגדלת בלוטות לימפה, מיימת, הגדלת כבד/טחול | [12] |
| בדיקה על-שמעית של הלב (אקו) ו-ECG | מיוקרדיטיס, וולווליטיס, תפליט מסב הלב, הרחבת עורקי הלב | [4][11][12][16] | |
| צילום חזה | תסנינים מפוזרים, תפליט | [5][12] | |
| CT חזה עם חומר ניגוד | תסנינים מפוזרים, תפליט, עורקי לב לא תקינים | [12][16] |
בירור מומלץ[12][15]
בירור מקרה החשוד לתסמונת תדר"ק כולל מספר מרכיבים:
- בסיסי דלקתי
- מכוון לתסמונת Kawasaki
- מכוון למעורבות לבבית
- למצוא עדות לזיהום על ידי 19-Covid
- לשלול זיהומים אחרים
- לחפש סממנים של Macrophage Activation Syndrome) MAS/(Cytokine Storm Syndrome) CSS)
| המטולוגיה | ספירת דם, משטח |
| מדדי דלקת | CRP, פריטין, פרוקלציטונין, ESR |
| קרישיות | D-dimers ,Fibrinogen ,PTT,PT |
| ביוכימיה | גלוקוז, אוראה, קריאטינין, אלקטרוליטים |
| גזים | |
| לקטט | |
| אנזימי כבד, LDH, טריגליצרידים | |
| אלבומין | |
| Troponin, CK, NTPro-BNP | |
| אמילאז | |
| ויטמין D | |
| שתן | אנאליזה כללית |
| סרולוגיה | לשמור נסיוב ב-EDTA (Ethylene-Diamine-Tetraacetic Acid) לפני מתן IVIg |
| נסיוב ל-IgG and IgM SARS-CoV-2 | |
| מיקרוביולוגיה | תרביות דם, שתן, לוע |
| שאיבה או משטח אפי-פרינגיאלי ל- PCR SARS CoV-2 | |
| צואה ודם ל- SARS-CoV-2 PCR | |
| דם ל-PCR ל- Pneumococcus, Meningococcus, Group A streptococcus, Staph. aureus | |
| דם ל-PCR CMV, EBV, Adenovirus, Enterovirus | |
| צואה לוירולוגיה, אנטרוטוקסינים/טוקסין של Staphylococcus | |
| הדמיה ופיזיולוגיה | צילום חזה, ECG |
נוסף בזאת, כל מקרה קורונה הוא מקרה שעשוי לתרום למאמץ המחקרי החיוני במחלה. יש לדאוג לקחת דגימות מתאימות לפרוטוקול מחקר לאחר קבלת הסכמה מדעת ומתחילת הטיפול.
הגדרת מקרה ואבחון תדר"ק
הגדרת מקרה מדויקת (Case definition) היא אבן בסיס חיונית לצורך חקר השכיחות והאפידמיולוגיה של התסמונת, הכרת ההופעה הקלינית ובדיקת האפשרויות הטיפוליות. אולם, לצערנו הרב, אין הגדרה המוסכמת על כלל הארגונים הרפואיים וקיימת וריאבליות אף על פי שההבדלים בהגדרות המקרה הם קטנים, וההגדרות משתנות החל מהגדרת גיל החולה, מידת ומשך החום, המערכות המעורבות והביטויים הקליניים, מדדי מעבדה ונתונים מחריגים שקיומם אינו עולה בקנה אחד עם הגדרת מקרה של התסמונת, ואמצעי ההוכחה לזיהום ותחלואה ב־19-Covid.
להלן הגדרות מקרה כפי שפורסמו על ידי 4 גופים רפואיים עולמיים, והמלצת הוועדה להגדרת מקרה בישראל:
הגדרת ארגון הבריאות העולמי - WHO[11]
חולה המציג את הקריטריונים להלן:
- גיל עד 19 שנים
- זיהום בנגיף הקורונה המגפתי - בדיקת PCR, תבחין אנטיגני או סרולוגיה חיובית או מגע עם חולה בקורונה
- חום של 38 מעלות צלזיוס ומעלה למשך 3 ימים או יותר
- מעורבות רב-מערכתית: קיום לפחות שניים מההסתמנויות הבאות:
- מדדי דלקת מוגברים - שקיעת דם, CRP או פרוקלציטונין
- גורם מחריג: ללא עדות לזיהום חיידקי כגורם לדלקת, כגון אלח דם או הלם רעלני (Toxic shock) על ידי סטפילוקוקים או סטרפטוקוקים
הגדרת המרכזים להגדרת מחלות ומניעה - CDC[13]
הגדרת המרכזיים האמריקאים לבקרת מחלות ומניעה שונה במספר מרכיבים מזו של ארגון הבריאות העולמי, לפי הפירוט להלן:
- גיל עד 21 שנים (הערה: אינו מקובל בארץ בהגדרת ילדים)
- הגדרה זהה לזיהום בנגיף הקורונה המגפתי, עם מגבלה שעל העדות לזיהום להיות בארבעת השבועות שלפני הופעת התסמינים
- חום של 38 מעלות צלזיוס לפחות, אך גם אפשרות שהילד נימוש חם, וזאת מעל 24 שעות
- מעורבות רב מערכתית: מעורבות של שתי מערכות לפחות מתוך מערכות הלב, הנשימה, הכליות, העיכול, העור, ההמטולוגית או הנוירולוגית, עם תוספת של צורך באשפוז
- מדדי דלקת מוגברים: בדוצה למדדי ארגון הבריאות העולמי, וכן פיברינוגן, פריטין, לקטט דהידרוגנאז (IL-6 ,(LDH או D-Dimer מוגברים; או אלבומין נמוך, או נויטרופיליה או לימפופניה
- גורם מחריג: רחב יותר "ללא אתיולוגיה ברורה אחרת"
הגדרת הגוף הממלכתי הבריטי לרפואת ילדים - RCPCH[12]
כולל מספר הבדלים בהשוואה להגדרת ארגון הבריאות העולמי, לפי הפירוט להלן:
- גיל עד 18 שנים
- עדות לזיהום על ידי נגיף קורונה המגפתי - הגדרה רחבה, עם אפשרות לבדיקות מעבדה (PCR, סרולוגיה) שליליות
- חום: ההגדרה שלהם - 38.5 מעלות צלזיוס לפחות, "ממושך" (ללא הגדרה מדויקת)
- מעורבות רב-מערכתית: הדרישה לאי-ספיקה של מערכת אחת או יותר מתוך המערכות לב, לחץ דם (הלם), נשימה, עיכול, כליות או הפרעה נוירולוגית
- מדדי דלקת מוגברים - כולל האפשרויות של נויטרופיליה או לימפופניה
- גורם מחריג: העדר זיהום אחר היכול להסביר את ההתסתמנות (חיידקי או נגיפי)
הגדרת הניטור הקנדי לתחלואה בילדים - CPSP[15]
דומה להגדרת ארגון הבריאות העולמי, עם ההבדלים להלן:
- בהסתמנות הכללית: תסמינים של תסמונת קוואסקי או הלם רעלני, מלאה או חלקית
- במדדי הדלקת המוגברים: גם פריטין
- בהחרגה: העדר אטיולוגיה אחרת להתייצגות הקלינית
המלצה להגדרת מקרה בישראל
הוועדה ממליצה לאמץ את הגדרת ארגון הבריאות העולמי להגדרת מקרה, אך עם שני שינויים בקריטריונים:
- עדות מעבדתית לזיהום על ידי נגיף הקורונה המגפתי - PCR או סרולוגיה
- החרגה: עדות לזיהום אחר - חיידקי או נגיפי - היכול להסביר את ההסתמנות הקלינית
אבחנה ודאית
נקבעת לפי קריטריונים קליניים ומעבדתיים הנדרשים.
אבחנה עם חשד גבוה
אם האבחון מתבסס על קריטריונים קליניים ואפידמיולוגים.
אבחנה מבדלת של תדר"ק
כוללת שתי הסתמנויות עיקריות:
מחלת קוואסקי
זוהי תסמונת דלקתית המופיעה אף היא לאחר זיהום ומציגה תסמינים שבחלקם חופפים את ההסתמנות הדלקתית השורה לזיהום על ידי 19-COVID.
מבחינה אפידמיולוגית - מחלת קוואסקי מופיעה באופן טיפוסי בגיל יותר צעיר, 80 אחוזים מתחת לגיל 5 שנים ללא קשר לתחלואה בנגיף הקורונה;
מבחינה קלינית - במחלת קוואסקי לרוב אין מעורבות של מערכת הנשימה או מערכת העיכול וערוב העורקים הכליליים עם דלקת במיוקרד היא שכיחה;
מבחינת בדיקות מעבדה - לויקופניה, לימפופניה ותרומבוציטופניה פחות אופייניים למחלת קוואסקי;
מבחינת התגובה לטיפול - מחלת קוואסקי מגיבה טוב יותר לטיפול באימונוגלובולינים;
מבחינת הסיבוכים - הרחבה ואניאוריזמות של העורקים הכליליים מהווים סיבוך טיפוסי של מחלת קוואסקי.
מחלות זיהומיות
מספר מחוללים זיהומיים, ובפרט החיידקים .Streptococcus sp ו-Staph. aureus, יכולים לגרום להלם רעלני (Toxic shock) עם חפיפה מסוימת בתסמינים. זיהומים אלה מאופיינים במהלך חד ומהיר יותר, בירידת לחץ דם עד מצב של הלם, וכן - לרוב עדות מעבדתית למחוללים אלה, המהווה בעצם קריטריון לאי הכללה בתסמונת הדלקתית הכרוכה בזיהום על ידי נגיף הקורונה[5][6].
הטיפול והניהול בתסמונת תדר"ק
זירת הטיפול
ילדים עם מצב קל ופחות מארבעה ימי חום שאינם סובלים ממעורבות רב-מערכתית ושמעקבם מובטח - הערכה וניהול בזירה אמבולטורית אפשריים. לילדים עם תסמינים חדשים ו/או חום ממושך, הערכה יומית במחלקה לרפואה דחופה או ביחידה לאשפוז יום מומלצת. מכיוון שהתסמונת היא לרוב קשה ובעלת פוטנציאל לסיבוכים קשים, ההמלצה, כאשר ישנם סימנים וסימפטומים משמעותיים, תהיה לתת טיפול במסגרת אשפוז. אופי וסוג הטיפול ייקבעו לפי חומרת ההתייצגות. חלק מהחולים אינם יציבים המודינמית (הלם, הפרעות קצב) או שיש אי ספיקה נשימתית או עם סיבוכים אחרים מסכני חיים, ואלו זקוקים לאשפוז ביחידה לטיפול נמרץ ילדים.
הצוות המטפל
היות שהתסמונת היא רב-מערכתית, התווית התוכנית הטיפולית דורשת צוות רב- תחומי. אנחנו ממליצים שתהיה השתתפות של המקצועות הבאים:
- מומחה ברפואת ילדים בכיר בעל ניסיון ניהול חולים מורכבים
- מומחה במחלות זיהומיות בילדים
- מומחה בקרדיולוגיה ילדים
- מומחה בטיפול נמרץ ילדים
מומחים נוספים כגון גסטרואנטרולוגיה ילדים, אימונולוגיה ילדים, דרמטולוגיה ילדים, ראומטולוגיה ילדים ומומחים אחרים נזקקים לפי הצורך.
טיפול אנטי-מיקרוביאלי
בעת ההתייצגות, המחלה כוללת פעמים רבות סימנים וסימפטומים שיכולים לדמות אלח דם (הלם ספטי) או לחלופין תסמונת הלם רעלני (Toxic Shock Syndrome, TSS). אין אפשרות לשלול את האפשרות של זיהום חיידקי קשה בתחילת המחלה. לכן אנו ממליצים לשקול לתת תחילה טיפול ראשוני על פי ההמלצות המקובלות בטיפול באלח דם, כולל מתן טיפול אנטי-מיקרוביאלי, עד לקבלת מידע אודות קיום מחוללי זיהום, על פי הפרוטוקולים המקומיים המקובלים ובתיאום עם ייעוץ של מומחה במחלות זיהומיות ילדים. יש לשקול טיפול עם Clindamycin אם יש עדות של מחלה מתווכת-רעלן (למשל התפתחות תפרחת בעלת אופי אריתרודרמה מפושטת). מומלץ להפסיק טיפול האנטי-חיידקי לאחר שלילת מחולל חיידקי.
טיפול אנטי-נגיפי
היות שתסמונת זה מהווה ככל הנראה סיבוך בתר-זיהומי ולא תגובה לזיהום נגיפי פעיל, אין התוויה ברורה לטיפול בתרופות אנטי-נגיפיות. בחולים עם התייצגות קלינית קשה ובדיקות RT-PCR ל־2-SARS-CoV חיוביות בעת ההתייצגות, ניתן לשקול טיפול אנטי-נגיפי לפי המקרה תוך התייעצות עם מומחי מחלות זיהומיות בילדים. נושא טיפול אנטי-נגיפי מתפתח מהר ומומלץ לעקוב אחרי הספרות לעיתים קרובות. בעת כתיבת מסמך זה, ישנה עדות שהתרופה Remdesivir (אנלוג נוקלאוטיד עם פעילות מעבדתית נגד SARS Cov-2) יעילה במבוגרים עם זיהום חריף[20][21].
טיפולים נוספים
טיפולים נוספים תלויים בהתייצגות הקלינית ומתחלקים לשלוש קבוצות עיקריות:
- טיפול תומך
- טיפול למחלת קוואסקי (אם קיימות אמות מידה מלאות/חלקיות)
- טיפול אימונו-מודולטורי
הלם
הטיפול ניתן בהתאם לפרוטוקולי PALS (Pediatric Advanced Life Support) או APLS (Advanced Paediatric Life Support), תוך הקפדה על ניטור הדוק, החייאת נוזלים ותמיכה אינוטרופית. טיפול זה ייתן ביחידה לטיפול נמרץ ילדים אמנם מומלץ להתחיל טיפול טרם הגעת הילד ליחידה. ברוב המקרים שדווחו, הילדים התייצגו עם שוק וזודילטורי (Distributive shock) שלא הגיב להחייאת נוזלים. עם זאת בחלק מהילדים נצפתה גם מעורבות לבבית עם ירידה בתפקוד הלב.
- החייאת נוזלים - בולוסים חוזרים של נוזלים קריסטולואידים איזוטונים (Saline או תמיסת Ringer) בכמות של 10–20 מיליליטר/קילוגרם
- יש לעקוב קליני להופעת סימנים של עודף נוזלים (קרפיטציות, מצוקה נשימתית מחמירה או הפטומגליה)
- טיפול אינוטרופי/פרסורי - מומלץ להתחיל מוקדם יחסית בטיפול עם Adrenaline/Noradrenaline (בקצב התחלתי של 0.1-0.3 מיקרוגרם/קילוגרם/דקה) בעירוי רציף דרך וריד פריפרי או עירוי תוך-גרמי. אין לדחות את הטיפול הפרסורי/אינטרופי עד להעברה לטיפול נמרץ ילדים. אם יש עדות לפגיעה בתפקוד הלבבי תרופת הבחירה היא Adrenaline וכן מומלץ לשקול הוספת Milrinone. מומלץ לשקול בחולים בהלם ניטור באמצעי Arterial line ווריד מרכזי לצורך מעקב אחר ערכי לחץ ורידי מרכזי וכן רוויון חמצן ורידי ב-SVC
תסמינים של מחלת קוואסקי
- אם יופיעו קריטריונים של מחלת קוואסקי מליאה או חלקית, מומלץ לתת טיפול כנהוג במחלה זאת - כולל IVIG ואספירין
- חולים בסיכון גבוה לעמידות לטיפול ב- IVIg - הרחבת עורקים כליליים בקבלה, גיל מתחת לשנה, הלם, עדות ל- MAS (Macrophage Activation Syndrome) - מומלץ לתת טיפול מלכתחילה גם בסטרואידים
- אם ממשיכים סימנים של הליך דלקתי פעיל (חום), יש לתת מנה חוזרת של ^^ולשקול טיפול בסטרואידים אם לא ניתן
פגיעה בתפקוד הלבבי
במהלך השלב הדלקתי של המחלה חלק מהילדים מפתחים פגיעה קלינית ומעבדתית בתפקוד הלבבי ו/או הפרעות קצב. על מנת לעקוב אחרי התפקוד הלבבי ואת הפרפוזיה הפריפריאלית, מומלץ כדלקמן:
- מומלץ על ביצוע בדיקה אקו-קרדיוגרפית תוך לווי של קרדיולוגי ילדים
- מומלץ ניטור הדוק:
- המודינמי/קליני
- אק"ג (ECG)
- Troponin
- BNP
- ריווי חמצן בווריד מרכזי (70 אחוזים <)
- לקטט
- תפוקת שתן
- Near Infra-Red tissue Spectroscopy) NIRS)
- אם התמונה מתאימה למיוקרדיטיס ניתן לשקול IVIG, אף על פי שאין עדויות ברורות לתועלת בספרות
- על מנת להוריד עומס על חדר שמאל ועבודת נשימה, חלק מהחולים נזקקים לטיפול תומך עם הנשמה בלחץ חיובי. מומלץ לתת תרופות משתנות ותרופות אינוטרופית כגון Adrenaline ,Milrinone ו-Dobutamine
- במקרים של כשל קרדיו-וסקולארי למרות תמיכה תרופתית והנשמתית מליאה ייתכן ויהיה צורך בתמיכה עם ECMO (Extra-Corporeal Membrane Oxygenation)
סיבוכי קרישה
חולים עם התסמונת נמצאים בסיכון לפתח היפר-קרישיות ולפתח סיבוכי קרישה כמו:
- קרישים בחדר שמאל בחולים עם ירידה בתפקוד החדרי
- אוטם לבבי בחולים עם מפרצות גדולות בעורקים הכליליים
- קרישים בוורידים עמוקים
- תסחיף ריאתי כתוצאה
ככלל ההמלצות לתת טיפול נוגד קרישה חלות על בני נוער ובילדים מבוגרים. בתינוקות אין המלצה גורפת ויש לשקול כל מקרה בגופו. ההחלטה על שימוש בנוגדי קרישה תיקח בחשבון הסיכון לדמם או להתערבות בלתי מתכוננת דחופה. להלן המלצות הטיפול נוגד קרישה או מעכבי טסיות בחולים אלו:
- בתמונה קלינית המתאימה למחלת קוואסקי יש לטפל ב-Aspirin במינון 3–5 מיליגרם/קילוגרם/יממה
- טיפול נוסף אנטי-קרישתי או נוגד טסיות יישקל לפי גודל מפרצת וכנהוג במחלה זאת
- בתמונה של ירידה בינונית/קשה בתפקוד הלבבי יש לשקול טיפול בנוגדי קרישה Heparin או LMWH (Low Molecular-Weight Heparin) כטיפול מניעתי או מלא
- בחולים ללא פגיעה לבבית או תסמינים של מחלת קוואסקי, ההחלטה על טיפול למניעת קרישי דם במערכת הוורידית היא אינדיבידואלית ואין הנחיות ברורות בנושא
- אם הוחלט על טיפול בנוגדי קרישה, שימוש באמצעים לא פרמקולוגיים למזער סיכון לקרישים מומלץ בכל הילדים (שרווליות לשוקיים מותאמות וניוד מוקדם של הילדים במידת האפשר)
טיפולים אימונו-מודולאטוריים נוספים
מדווחים מגוון של תרופות נוספות אימונו-מודולאטריות כגון: סטרואידים, מעכבי 1-IL (Anakinra), מעכבי 6-IL (כמו Tocilizumab), פלזמה מחולים שהבריאו מ-19-COVID, ותרופות כגון Rituximab. התועלת של כל אלה אינה ברורה ויש לשקול ניסיון טיפולי בהתאם לייעוץ מומחה לזיהומים ילדים, ראומטולוג ילדים תוך הערכת חומרת המחלה והסמנים הדלקתיים. ניתן לשקול טיפול בסטרואידים באותם חולים שמפגינים עדות לרמות ציטוקינים גבוהות (Cytokine Release Syndrome) שמפגינים חום ממושך, עליה במדדי דלקת (כגון CRP, די-דימר, פריטין ורמות 6-IL) בחולים שלא יכולים לקבל סטרואידים או שמפגינים עמידות להם ניתן לשקול טיפול ב-Anakrina או Toclizumab. בסדרה גדולה שהתפרסמה מאנגליה דווח כי כשלושה רבעים מהחולים טופלו בסטרואידים וב-IVIG ואילו 22 אחוזים טופלו בתרופות ביולוגיות.
פרוגנוזה
מאחר שמדובר בתסמונת חדשה יחסית, הפרוגנוזה ארוכת הטווח עדיין אינה ברורה. לראיה, אחוז הילדים הנזקקים לאשפוז בטיפול נמרץ ילדים גדול יחסית לאלו הסובלים ממחלת קוואסקי לה התסמונת דומה. התמותה המדווחת היא סביב 2–3 אחוזים. מבחינת מעורבות עורקים כליליים, בעוד שבשלב החריף דווח על מפרצות בכחמישית מהילדים, אין בידינו מידע אודות הפרוגנוזה ארוכת הטווח של ילדים אלו עם מעורבות כלילית משמעותית.
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 1.8 1.9 Riphagen S, Gomez X, Gonzalez-Martinez C, Wilkinson N, Theocharis P. Hyperinflammatory shock in children during COVID-19 pandemic. Lancet. 2020;395(10237):1607-1608. doi:10.1016/S0140-6736(20)31094-1
- ↑ Licciardi F, Pruccoli G, Denina M, et al. SARS-CoV-2-Induced Kawasaki-Like Hyperinflammatory Syndrome: A Novel COVID Phenotype in Children. Pediatrics. Published online 2020:e20201711. doi:10.1542/peds.2020-1711
- ↑ 3.00 3.01 3.02 3.03 3.04 3.05 3.06 3.07 3.08 3.09 3.10 3.11 3.12 3.13 3.14 Verdoni L, Mazza A, Gervasoni A, et al. An outbreak of severe Kawasaki-like disease at the Italian epicentre of the SARS-CoV-2 epidemic: an observational cohort study. Lancet. Published online 2020. doi:10.1016/S0140- 6736(20)31103-X
- ↑ 4.00 4.01 4.02 4.03 4.04 4.05 4.06 4.07 4.08 4.09 4.10 4.11 4.12 4.13 4.14 4.15 4.16 Whittaker E, Bamford A, Kenny J, et al. Clinical Characteristics of 58 Children with a Pediatric Inflammatory Multisystem Syndrome Temporally Associated with SARS-CoV-2. JAMA - J Am Med Assoc. Published online 2020. doi:10.1001/jama.2020.10369
- ↑ 5.00 5.01 5.02 5.03 5.04 5.05 5.06 5.07 5.08 5.09 5.10 5.11 5.12 5.13 5.14 Cheung EW, Zachariah P, Gorelik M, et al. Multisystem Inflammatory Syndrome Related to COVID-19 in Previously Healthy Children and Adolescents in New York City. JAMA - J Am Med Assoc. Published online 2020. doi:10.1001/jama.2020.10374
- ↑ 6.0 6.1 Feldstein LR, Rose EB, Horwitz SM, et al. Multisystem Inflammatory Syndrome in U.S. Children and Adolescents. N Engl J Med. Published online 2020. doi:10.1056/NEJMoa2021680
- ↑ Rawat, M.; Chandrasekharan, P.; Hicar, M.D.; Lakshminrusimha S. COVID-19 in newborns and infants-low risk of severe disease: Silver lining or dark cloud? Am J Perinatol. Published online 2020.
- ↑ Bunyavanich, S.; Do, A.; Vicencio A. Nasal Gene Expression of Angiotensin-Converting Enzyme 2 in Children and Adults. JAMA. Published online 2020.
- ↑ Fujimaru, T.; Ito, S.; Masuda, H.; Oana, S.; Kamei, K.; Ishiguro, A.; Kato, H.; Abe J. Decreased levels of inflammatory cytokines in immunoglobulin-resistant Kawasaki disease after plasma exchange. Cytokine. 2014;70:156-160.
- ↑ 10.0 10.1 Nakra NA, Blumberg DA, Herrera-Guerra A, Lakshminrusimha S. Multi-System Inflammatory Syndrome in Children (תדר"ק) Following SARS-CoV-2 Infection: Review of Clinical Presentation, Hypothetical Pathogenesis, and Proposed Management. Child (Basel, Switzerland). 2020;7(7). doi:10.3390/children7070069
- ↑ 11.00 11.01 11.02 11.03 11.04 11.05 11.06 11.07 11.08 11.09 11.10 11.11 11.12 Multisystem Inflammatory Syndrome in Children and Adolescents with COVID- 19 Scientific Brief 15 May 2020 Background.; 2020. https://www.who.int/news-
- ↑ 12.00 12.01 12.02 12.03 12.04 12.05 12.06 12.07 12.08 12.09 12.10 12.11 12.12 12.13 12.14 12.15 12.16 12.17 12.18 12.19 12.20 12.21 12.22 12.23 12.24 12.25 12.26 12.27 12.28 Guidance: Paediatric multisystem inflammatory syndrome temporally associated with COVID-19.
- ↑ 13.00 13.01 13.02 13.03 13.04 13.05 13.06 13.07 13.08 13.09 13.10 13.11 13.12 Preparedness E. Emergency Preparedness and Response Multisystem In ammatory Syndrome in Children ( תדר"ק ) Associated with Coronavirus Disease 2019. CdcGov. Published online 2020:2019-2021. doi:10.1016/S0140- 6736(20)31094
- ↑ 14.0 14.1 14.2 14.3 Toubiana J. Outbreak of Kawasaki disease in children during COVID-19 pandemic a prospective observational study in Paris France. Medrxiv. 2020;5:1-21. doi:10.1101/2020.05.10.20097394
- ↑ 15.0 15.1 15.2 15.3 15.4 15.5 15.6 15.7 15.8 Statement P. Paediatric inflammatory multisystem syndrome temporally associated with COVID-19 Principal author ( s ) Association with COVID-19. Published online 2020:1-10.
- ↑ 16.0 16.1 16.2 16.3 16.4 16.5 16.6 16.7 16.8 Belhadjer Z, Bonnet D. Acute heart failure in multisystem inflammatory syndrome in children (תדר"ק) in the context of global SARS-CoV-2 pandemic Running title: Belhadjer et al.; Pediatric acute heart failure and SARS-CoV-2 infection Covid-19. Circulation. 2020;33(0). doi:10.1161/CIRCULATIONAHA.120.048360
- ↑ סקירה בעברית
- ↑ 18.0 18.1 Viner RM, Whittaker E. Kawasaki-like disease: emerging complication during the COVID-19 pandemic. Lancet. 2020;6736(20):1741-1743. doi:10.1016/S0140-6736(20)31129-6
- ↑ Ecdc. Suggested Citation: European Centre for Disease Prevention and Control. Paediatric Inflammatory Multisystem Syndrome and SARS-CoV-2 Infection in Children Paediatric Inflammatory Multisystem Syndrome and SARS-CoV-2 Infection in Children.; 2020.
- ↑ Wang M, Cao R, Zhang L, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res. 2020;30(3):269-271. doi:10.1038/s41422-020-0282-0
- ↑ Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet. 2020;395(10236):1569-1578. doi:10.1016/S0140-6736(20)31022-9


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק