תסמונת המעי הרגיז - Irritable bowel syndrome
| תסמונת המעי הרגיז | ||
|---|---|---|
| Irritable Bowel Syndrome | ||
| 250px | ||
| שמות נוספים | IBS (קיצור), תסמונת המעי הרגיש, Spastic colon | |
| ICD-10 | Chapter K 58. | |
| ICD-9 | 564.1 | |
| MeSH | D043183 | |
| יוצר הערך | ד"ר מיקי דובלין, עודכן ב-2025 על ידי ד"ר ליאור זורניצקי | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – תסמונת המעי הרגיז
תסמונת המעי הרגיז (IBS) היא הפרעה במערכת העיכול המאופיינת בכאבי בטן כרוניים ושינויים בהרגלי היציאות, ללא גורם אורגני ברור. מדובר באחת המחלות הגסטרואנטרולוגיות השכיחות ביותר, והיא אחראית לכ-30 אחוזים מהפניות לרופאי גסטרו[1].
הגורמים להתפתחות התסמונת אינם מובנים לחלוטין[2], ולמרות מחקרים רבים, אין ממצא בודד או בדיקה ספציפית שיכולים לאשר את האבחנה. ההשערה הרווחת היא כי מדובר בהפרעה הנובעת משילוב של מספר גורמים המשפיעים יחדיו על תפקוד מערכת העיכול.
בעבר, החוקרים התמקדו בעיקר בהפרעות בתנועתיות המעי (Motility) ובתגובתיות יתר של מערכת העצבים הוויסצרלית (Visceral Hypersensitivity). עם זאת, מחקרים עדכניים מצביעים גם על מעורבות של תהליכים דלקתיים, שינויים בהרכב חיידקי המעי (Microbiome), צמיחת יתר של חיידקים במעי הדק ורגישות למזון. בנוסף, נבחנת האפשרות כי לתסמונת קיים רקע גנטי מסוים.
המחלה מתוארת כבר מ-1818 (Richard Powell), כאשר בשנת 1962 Chaudhary ו-Troulove הכתירו אותה בשם "תסמונת הקולון העצבני", וב-1966 Delor נקב בשם "תסמונת המעי הרגיז".
אפידמיולוגיה
תסמונת המעי הרגיז היא הפרעה שכיחה המשפיעה על כ-10 אחוזים עד 15 אחוזים מהאוכלוסייה, אך השכיחות שלה משתנה בהתאם לגיל, מגדר וזהות מגדרית. מחקרים הראו כי IBS נפוץ יותר בנשים (14 אחוזים) מאשר בגברים (9 אחוזים), וכי אנשים לא-בינאריים ואנשים מקהילת הלהט"ב נמצאים בסיכון גבוה יותר לפתח את ההפרעה. בנוסף, הסיכון ל-IBS יורד עם הגיל, כאשר השכיחות נמוכה יותר בקרב אנשים מעל גיל 50.
בנוסף לשכיחות התופעה, בהשוואה לאוכלוסייה ללא התסמונת, החולים בתסמונת המעי הרגיז נעדרים יותר מהעבודה (עד פי שלוש), מגיעים לרופא המשפחה הרבה יותר בשל תלונות הקשורות למערכת העיכול ושלא ממערכת העיכול. במתבגרים קיימת בעיה זהה של היעדרות מבית הספר.
מעבר לכך, IBS לרוב אינו מופיע לבד. מחקרים הראו כי אנשים עם IBS נוטים יותר לסבול גם מפיברומיאלגיה, תסמונת התשישות הכרונית, מחלת ריפלוקס קיבתי-ושטי (GERD), כאבים בחזה ממקור שאינו לבבי, הפרעות עיכול תפקודיות, וכן מחרדה ודיכאון. קשרים אלו מחזקים את ההבנה כי IBS היא לא רק בעיה במערכת העיכול, אלא תסמונת המשפיעה על מערכת העצבים והקשרים בין המוח למעי, ושהטיפול בה צריך להתייחס למכלול רחב של גורמים גופניים ונפשיים.
אטיולוגיה
תסמונת המעי הרגיז (IBS) היא הפרעה מורכבת עם גורמים מרובים, המאופיינת בשינויים בתנועתיות המעי, תחושת כאב מוגברת, ושינויים בהרכב החיידקים במעי. אין גורם אחד מובהק שמסביר את התסמונת, אלא שילוב של מנגנונים פיזיולוגיים, עצביים, חיסוניים ופסיכו-סוציאליים, אשר עשויים להשתנות בין חולה לחולה. בעוד שאצל חלק מהמטופלים מדובר בעיקר בהפרעה בתנועתיות המעי, אצל אחרים הגורם העיקרי עשוי להיות דלקת במערכת העיכול, שיבוש בהרכב חיידקי המעי, רגישות יתר לגירויים פנימיים, או השפעה משמעותית של סטרס נפשי.
בין המנגנונים
הפרעה בתנועתיות המעי (Motility Disorder) - תוארו מגוון של הפרעות תנועתיות במעי הגס ובמעי הדק. תנועתיות יתר עלולה לגרום לשלשול כתסמין בולט. תנועתיות מופחתת עלולה לגרום לעצירות כתסמין בולט. עדיין לא הוכח קשר חד-משמעי בין שינויים אלו בתנועתיות לבין הופעת התסמינים. עם זאת, דווח כי גירוי פרמקולוגי של תנועתיות מערכת העיכול בקרב מטופלים עם IBS עשוי להפחית לכידת גזים ולשפר את התסמינים, דבר המרמז כי הפרעה בתנועתיות עשויה לתרום לחלק מהתסמינים של ההפרעה.
רגישות יתר ויסרלית (Visceral hypersensitivity) - אצל חלק מהלוקים בתסמונת קיים סף נמוך לתחושת הכאב המשודר מדופן המעי גם בנוכחות מתח (לחץ) ונפח של תוכן נמוך באופן יחסי, אשר לרוב אינו גורם אצל מרבית האוכלוסייה לתחושה של כאב. התמלאות של פי הטבעת או חלקי מעי אחרים בנפח בכמות קטנה יחסית, שמיצר לחץ נמוך של גז באופן יחסי, עלולה לגרום להופעה של כאב בטן וצורך להתרוקן בתכיפות. מחקרים הראו כי תכולת הגז, המרכיבים, הנפח והלחץ במעי של חולים אלו תקינה[3].
דלקת במערכת העיכול (Intestinal inflammation) - בדיקות אימונו-היסטולוגיות מצביעות על הפעלה של מערכת החיסון ברירית המעי בקרב חלק מהמטופלים עם IBS, במיוחד באלה עם IBS המאופיין בשלשולים ובמטופלים עם חשד ל-IBS שלאחר זיהום (postinfectious IBS). נמצאו רמות מוגברות של לימפוציטים ברירית המעי הגס והדק[4][5], לצד תאי פיטום (Mast Cells) פעילים, אשר מפרישים חומרים דלקתיים כמו היסטמין ותחמוצת חנקן, הגורמים לרגישות יתר ולשינויים בתנועתיות המעי[6][7].
לאחר זיהום (postinfectious) - מחקרים מצאו כי כ-15 אחוזים מהאנשים שסבלו מגסטרואנטריטיס חריפה מפתחים IBS ושהסיכון לכך גבוה יותר בקרב נשים, אנשים עם היסטוריה של חרדה, ואלו שחוו שלשולים ממושכים או אשפוז בעקבות המחלה[8][9][10]. הסיבה לכך אינה לגמרי ברורה, אך ישנן כמה תאוריות: ייתכן שהזיהום משבש את האיזון החיידקי במעי, פוגע בספיגת חומרים חיוניים[11][12], או מפעיל תגובה חיסונית מתמשכת, שמשפיעה על הרגישות והעצבוב של מערכת העיכול. גם שימוש באנטיביוטיקה במהלך הזיהום נמצא כגורם אפשרי, מאחר שהוא עשוי לגרום לשינויים קבועים בהרכב חיידקי המעי[13][14].
הרכב חיידקי הצואה (alteration in fecal microflora) - מחקרים מצביעים על כך שהרכב חיידקי הצואה של חולי IBS שונה מזה של אנשים בריאים, ואף משתנה בהתאם לסוג התסמינים מהם הם סובלים[15][16][17][18][19]. באחד המחקרים נמצא כי כאשר השתילו חיידקי צואה מחולי IBS לחיות מעבדה חסרות חיידקים, הן פיתחו רגישות יתר במעי, בדומה לתסמיני IBS. ממצא זה מרמז כי ייתכן שלחיידקי המעי יש תפקיד בהתפתחות ההפרעה[20]. בהתחשב בשינויים האפשריים במיקרוביום בקרב חולי IBS, עלתה הסברה כי פרוביוטיקה עשויה להועיל, במיוחד עבור חולים עם IBS המאופיין בשלשולים[21]. עם זאת, מחקרים שבדקו את ההשפעה של זני חיידקים פרוביוטיים, כמו Lactobacillus plantarum, לא מצאו שינוי מובהק בהרכב חיידקי המעי, אך כן דווח על הפחתה בתסמינים כמו נפיחות וגזים[22]. ממצאים דומים נצפו במחקר אחר שבו נבדק יוגורט פרוביוטי המכיל B. animalis subsp lactis Bb12 ו-K. marxianus B0399, אשר שיפר תסמינים אך לא השפיע על הרכב החיידקים[23].
צמיחת יתר של חיידקים (bacterial overgrowth) - מצב שבו יש עלייה חריגה במספר או בסוג החיידקים במעי הדק, מה שעשוי לגרום לתסמינים במערכת העיכול. אצל חולי IBS נמצאו רמות חריגות של גזים בבדיקות נשיפה, ושיפור בתסמינים לאחר טיפול באנטיביוטיקה שמטרתה להפחית את כמות החיידקים במעי הדק[24][25][26]. יש גם עדויות לכך שייצור מוגבר של מתאן – תוצר של חיידקי מעי – נפוץ יותר אצל חולי IBS הסובלים מעצירות. עם זאת, מחקרים אחרים לא הצליחו להוכיח שצמיחת יתר של חיידקים היא הגורם הישיר ל-IBS. למשל, בבדיקות מעבדה נמצא שצמיחת יתר של חיידקים מופיעה גם אצל אנשים בריאים, והשיפור שנצפה אצל חולי IBS שטופלו באנטיביוטיקה עשוי לנבוע משינוי בהרכב חיידקי המעי או משיפור בתנועתיות מערכת העיכול[27].
רגישות למזון (Food sensitivity) - מחקרים מראים כי 45 אחוזים עד 60 אחוזים מהחולים מדווחים על החמרת תסמינים לאחר אכילה, וחלקם אף סבורים שהם סובלים מאי-סבילות למזונות מסוימים[28][29][30]. המחקרים בתחום בחנו מספר גורמים שעשויים להיות מעורבים ברגישות למזון בקרב חולי IBS, כולל נוגדנים ייחודיים למזון, תת-ספיגה של פחמימות ורגישות לגלוטן[31]. התאמת תזונה אישית, כמו דיאטת FODMAPs או הימנעות ממזונות מסוימים, עשויה לסייע בהפחתת התסמינים בקרב חלק מהמטופלים.
גנטיקה (Genetics) - מחקרים גנטיים ומשפחתיים מצביעים על כך שייתכן מרכיב גנטי בהתפתחות תסמונת המעי הרגיז (IBS), אך היקפו והשפעתו אינם ברורים לחלוטין[32]. כמה מחקרים מצאו קשרים אפשריים בין IBS לבין שינויים גנטיים, במיוחד בגן האחראי על וויסות הסרוטונין, אשר משפיע על תנועתיות המעי[33][34]. עם זאת, מחקרים אחרים לא הצליחו לאשש את הקשר הזה[35][36]. יש גם עדויות לכך שחלק מהאנשים עם IBS עשויים להיות בעלי רגישות גנטית לדלקות קלות במעי, מה שיכול להשפיע על תפקוד מערכת העיכול שלהם[37].
סיבות פסיכו סוציאליות (psychosocial dysfunction) - יותר ממחצית מהחולים הלוקים בתסמונת המעי הרגיז שפונים לעזרה רפואית סובלים מבעיות כמו דיכאון או חרדה. הבעיות הפסיכולוגיות יכולות להשפיע על תגובת החולה לתחושת הכאב. אחד ההסברים המדעיים לקשר הזה מתמקד במנגנון תגובת הסטרס של הגוף, המווסת על ידי חלבון בשם CRF (Corticotropin-Releasing Factor). מחקרים הראו כי אצל חולי IBS, פעילות יתר של CRF במוח מגבירה את רגישות המעי לכאב ומשפיעה על תנועתיות מערכת העיכול[38]. כאשר החוקרים חסמו את פעילות החלבון הזה, התסמינים השתפרו – מה שמרמז על כיוון טיפולי אפשרי לעתיד[39].
הפרעה בציר מוח-מעי (Brain-Gut Axis Disorder) - למרות ההשערות הרבות לגבי מהות המחלה ברור כי מדובר בתופעה שמתווכת על ידי Serotonin עם רגישות יתר לכאב ותנועתיות של המעי. Serotonin הוא נגזרת של Tryptophan (חומצת אמינו (Amino acid) הנמצאת במזון) ומשמש באופן פיזיולוגי (Physiological) בגופנו כנוירוטרנסמיטר (Neurotransmitter) המקשר בהולכה בין תאי עצב. 5 אחוזים מה-Serotonin בגוף נמצא במערכת העצבים המרכזית (המוח) ו-95 אחוזים ממערכת העיכול - רובו המכריע בתאים המפרישים הורמונים לאורך מערכת העיכול. ההשפעה המקומית על מערכת העיכול של Serotonin כוללת תווכו בהחזרים השולטים על תנועתיות וההפרשה של מערכת העיכול, בנוסף להיותו מעורב גם בתאי עצב תחושתיים של מערכת העיכול ובשל קיומו גם במוח מעורב בבניית התפיסה של כאב ותפקוד מערכת העיכול.
קליניקה
תסמונת המעי הרגיז היא תסמונת כרונית. התסמינים מתחילים בדרך כלל בשנות העשרה המאוחרות עד שנות העשרים. משך התסמינים לפני אבחון התסמונת - לפחות שלושה חודשים. האבחנה נעשית לאחר הערכת התסמינים בהתאם למאפיינים ולאחר שנשללה בעיה גופנית (Organic).
כאב בטן - מתואר לרוב כהתכווצויות (Cramping) בעוצמות משתנות, עם תקופות של החמרה. המיקום והאופי של הכאב יכולים להשתנות מאדם לאדם[40][41]. הכאב קשור לרוב לפעולת מעיים, אך תגובת המטופלים שונה – יש חולים המדווחים כי היציאות מקילות על הכאב, בעוד שאחרים חווים החמרה בעקבות היציאות[42]. לחץ רגשי וארוחות עשויים להחמיר את הכאב.
נפיחות בטנית - נגרמת עקב ייצור מוגבר של גזים, המתבטא בגיהוקים או בגזים מרובים.
שינויים בהרגלי היציאות - החולים עשויים לסבול משלשולים, עצירות, שילוב של שניהם, או פרקי זמן של יציאות תקינות לסירוגין עם שלשול או עצירות.
- שלשול (Diarrhea) - מתאפיין ביציאות רכות ותכופות, בנפח קטן עד בינוני, לרוב מתרחש בשעות הבוקר או אחרי ארוחות. מרבית המטופלים חווים כאב בטן תחתונה ועוויתות לפני היציאה, לצד דחיפות וצורך חזק להתרוקן. כ-50 אחוזים מהמטופלים מדווחים על ריר ביציאות[43]. שלשול בנפח גדול, דם בצואה, שלשול לילי או צואה שומנית אינם אופייניים ודורשים בירור נוסף
- עצירות (Constipation) - הצואה לרוב קשה, ולעיתים מתוארת כבעלת צורה של כדורים קטנים (Pellet-shaped stools). חלק מהמטופלים חווים תחושת חוסר התרוקנות גם כאשר הרקטום ריק
אבחנה
האבחנה של IBS מתבססת בעיקר על קריטריונים קליניים, תוך שלילת מחלות אורגניות באמצעות בדיקות ממוקדות[44][45]. לרוב, אין צורך בבדיקות מרובות אם התסמינים תואמים לקריטריוני רומא IV ואין נוכחות של דגלים אדומים. גישה זו מאפשרת אבחון מדויק ומהיר, תוך הימנעות מבדיקות פולשניות מיותרות.
- אנמנזה (history) טובה של הרופא המטפל לגבי הרגלי היציאות ואופי התלונות. בשלב הראשון הרופא יעריך את אופי התלונות, משך התלונות, מחלות עבר, היסטוריה רפואית קודמת, שימוש קבוע בתרופות, הרגלים (תזונה, עישון, שתייה, אלכוהול (Alcohol), יחסי מין ועוד) וכן בדיקה גופנית מלאה
- בדיקות מעבדה הכוללות - ספירת דם, כימיה, תפקודי בלוטת התריס, בדיקות סרולוגיות (Serology) לנגיפים ובדיקות אימונולוגיות (Immunology) הכוללות בדיקות דם למחלת צליאק, הליקובקטר פילורי ו-CRP (C Reactive Protein) או קלפרוטקטין (calprotectin) או לקטופרין (lactoferrin) לשלילת מחלת קרוהן (Crohn), בדיקות צואה לג'יארדיה ושתן
- אנדוסקופיות (Endoscopies), CT (Computer Tomography) בטן לפי צורך ספציפי
- בדיקות רגישות למזון לפי הצורך
קריטריונים
לפי קריטריוני רומא IV (Rome IV criteria) תסמונת המעי הרגיז מוגדרת ככאב בטן חוזר, המופיע לפחות יום אחד בשבוע בשלושת החודשים האחרונים, ומלווה בלפחות שניים מהמאפיינים הבאים[40][44]:
- קשור ליציאות
- מלווה בשינוי בתדירות היציאות
- מלווה בשינוי בצורה או במרקם הצואה
תסמינים אחרים התומכים באבחנה כוללים:
- תדירות יציאות שאינה תקינה (יותר משלוש יציאות ליום או פחות משלוש יציאות לשבוע)
- צורת צואה שאינה תקינה (גושית וקשה או מימית)
- תהליך התרוקנות שאינו תקין (מאמץ, תכיפות או תחושה של התרוקנות לא מלאה)
- יציאה מלווה עם ריר
- תחושת נפיחות בבטן
תסמינים נוספים היכולים להצטרף לאבחנה זו:
דגלים אדומים[46]
- הופעת תסמינים לראשונה אחרי גיל 50
- דימום רקטלי או מלנה
- שלשול לילי
- כאב בטן שהולך ומתגבר
- ירידה בלתי מוסברת במשקל
- אנמיה מחסר ברזל, CRP גבוה, או קלפרוטקטין/לקטופרין צואתי מוגבר
- היסטוריה משפחתית של מחלות מעי דלקתיות (IBD - Inflammatory Bowel DIsease) או סרטן המעי הגס
אבחנה מבדלת
- סומטיזציה (Somatization) במקרי דיכאון או חרדה
- מחלת Crohn / Ulcerative Colitis
- מחלת Celiac (כרסת)
- רגישות לחלב / רגישות ספציפית ללקטוז
- זיהומי מעי / טפילים / פטריות
- תופעות לוואי לתרופות
- ממאירות ראשונית במעי / השפעות מגידולים מפרישים
טיפול
לאחר אבחון IBS יש לקבוע את תת-הסוג של התסמונת על מנת להנחות את בחירת הטיפול התרופתי.
תתי-הסוגים של IBS נקבעים לפי הדפוס השולט של הצואה בימים עם יציאות חריגות, באמצעות סולם BSFS (Bristol Stool Form Scale). אנו מבקשים מהמטופלים למלא יומן יציאות של שבועיים בכדי לקבוע את הרגלי היציאות. יומן זה יש למלא ללא נטילת תרופות שעשויות להשפיע על פעילות המעיים, כולל תרופות לטיפול ב-IBS. בנוסף, אנו מבקשים מהמטופלים למלא יומן תזונה של שבועיים לצד יומן היציאות, מאחר ששינויים תזונתיים מהווים רכיב מרכזי בטיפול הראשוני[47][48][49].
קביעת תת-סוג של IBS
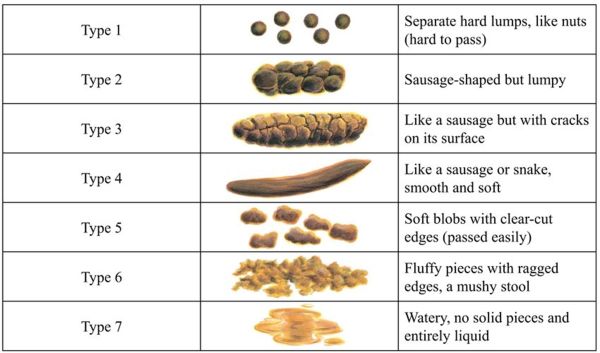
- IBS עם עצירות דומיננטית - (IBS-C) כאשר התנועות החריגות במעיים הן לרוב עצירות (סוג 1 ו-2 בסולם BSFS)
- IBS עם שלשולים דומיננטיים (IBS-D) - כאשר התנועות החריגות במעיים הן לרוב שלשולים (סוג 6 ו-7 בסולם BSFS)
- IBS עם הרגלי יציאות מעורבים (IBS-M) - כאשר קיימת תדירות דומה של עצירות ושלשולים (יותר מ-25 אחוזים מהיציאות החריגות הן עצירות (סוג 1 ו-2 בסולם BSFS) ויותר מ-25 אחוזים מהיציאות החריגות הן שלשול (סוג 6 ו-7 בסולם BSFS))
- IBS לא מסווג (IBS-U) - כאשר המטופלים עומדים בקריטריונים לאבחון IBS אך אינם מתאימים לאחד משלושת תתי-הסוגים האחרים
תתי-הסוגים של IBS הם דינמיים. מחקרים מראים כי למעלה ממחצית מהמטופלים משנים תת-סוג במהלך שנה אחת[50]. לכן, אנו בודקים מחדש את תסמיני המטופל ואת יומן היציאות בכל ביקור על מנת לאמת את תת-הסוג של IBS. כמו כן, יש להעריך מחדש את תת-הסוג של IBS בקרב מטופלים עם תסמינים עמידים או במגמת החמרה.
טיפול ראשוני לכל המטופלים
הצלחה בטיפול ב-IBS דורשת יחסי אמון בין הרופא למטופל, הכרה בתסמינים, קביעת ציפיות ריאליות והבטחת המשכיות טיפול. מומלץ לשלב שינויים באורח החיים, הכוללים פעילות גופנית סדירה, שיפור איכות השינה והפחתת סטרס[51][52][53].
השלמה תזונתית
השלמה תזונתית של Lactase שהוא האנזים המפרק את ה-Lactose מאפשרת לסובלים מתסמונת המעי הרגיז לצרוך מוצרי חלב במידה סבירה ללא הופעת תסמינים. השלמות תזונתיות של שמן דגים (עשיר ב-Omega-3) ושמן נר הלילה (עשיר ב- GLA - Gamma Linolenic Acid) משפרות את ריריות מערכת העיכול ומסייעות בהקלת התסמינים. תוספת של חיידקים טובים (Acidophilus) משפרת את תהליך העיכול על-ידי השבת האיזון החיידקי למעי ומקלה על התסמינים, בעיקר גזים ונפיחות.
שינוי אורחות חיים
שינויים באורח החיים והתערבויות התנהגותיות מהווים את קו הטיפול הראשון לכל המטופלים עם IBS.
- פעילות גופנית - אנו ממליצים על פעילות גופנית קבועה כמרכיב חיוני בטיפול ב-IBS. מחקרים מצביעים על כך שפעילות גופנית משפרת את הסימפטומים הכלליים של IBS. בניסוי אקראי עם 102 מטופלים, 12 שבועות של פעילות גופנית מוגברת (20–60 דקות של פעילות מתונה, 5-3 פעמים בשבוע) שיפרו משמעותית את תסמיני IBS בהשוואה לשמירה על רמת פעילות קבועה[54]
- היגיינת שינה - הפרעות שינה שכיחות יותר בקרב מטופלים עם IBS ומתקשרות לכאב הקשור ל-IBS[55][56][57]. יש לסקור גורמים אפשריים המשפיעים על איכות השינה, כולל תרופות ותנאי סביבה
- טיפולים פסיכולוגיים והפחתת סטרס - מחקרים מצביעים על כך שטכניקות להפחתת סטרס, כגון מיינדפולנס, טיפול קוגניטיבי-התנהגותי והיפנוזה ממוקדת-מעי, עשויות לשפר תסמינים גופניים ונפשיים ב-IBS[58][59][60][61][62][63]. טיפולים אלו מוצעים לרוב כתוספת לטיפול במטופלים עם תסמינים עמידים, אך יש להפנות אליהם מוקדם במקרים של הפרעות מצב רוח נלוות או העדפה לטיפול לא-תרופתי
רצוי מאוד להקפיד על ארוחות קבועות ומסודרות. ארוחות קטנות ומרובות במשך היום עשויות להקל על שלשול. ארוחות גדולות ועשירות בסיבים יקלו על סמני העצירות.
שינוי תזונתי
שינויים תזונתיים מהווים מרכיב מרכזי בניהול תסמיני IBS. לרוב נדרשת גישה של ניסוי וטעייה עם התאמות לאורך הזמן למציאת התזונה המיטיבה ביותר עם המטופל.
- לפני ביצוע שינויים תזונתיים, יש לבקש מהמטופלים למלא יומן תזונה ויומן יציאות של שבועיים, כדי לאפשר הערכה מדויקת יותר של דפוסי התסמינים וזיהוי גורמי טריגר אפשריים בתזונה[64][65]
- הערכה תזונתית ראשונית צריכה לכלול גם סקר להפרעות אכילה, הפרעות נפשיות לא מאוזנות, חוסר ביטחון תזונתי, או גורמי סיכון אחרים לתת-תזונה. במקרים כאלה, לא מומלץ לבצע דיאטות מגבילות, ויש להתמקד בטיפול תרופתי מותאם ובתמיכה התנהגותית מפוקחת
- אנו ממליצים על ייעוץ תזונתי עם דיאטנית קלינית לכל המטופלים עם IBS[66]. ייעוץ זה מסייע להתאמת התזונה האישית, שיפור ההיענות התזונתית, ותכנון ארוחות מותאם[67]
הנחיות תזונתיות
אנו ממליצים על הנחיות תזונתיות מסורתיות כקו ראשון לשינוי תזונתי, הכוללות:
- תוספת סיבים מסיסים - מומלץ לצרוך סיבים מסיסים כגון פסיליום ושיבולת שועל. מומלץ להתחיל במינון נמוך (3–4 גרם ביום) ולהעלות את המינון בהדרגה בהתאם לתגובה
- הימנעות ממזונות מייצרי גזים - מומלץ להימנע ממזונות הידועים כמייצרי גזים, כגון כרוב, ברוקולי, כרובית, קטניות, משקאות מוגזים וממתיקים כמו פרוקטוז וסורביטול
- הגבלת לקטוז - מטופלים עם אי-סבילות ידועה ללקטוז או כאלה שיומן המזון שלהם מעיד על קשר בין צריכת לקטוז להופעת תסמינים, צריכים לנסות דיאטה מופחתת לקטוז
דיאטת Low-FODMAP
למטופלים שתסמיניהם נמשכים לאחר יישום ההנחיות התזונתיות המסורתיות, אנו ממליצים על דיאטת Low-FODMAP[68].
FODMAP הם ראשי תיבות של - Fermentable Oligosaccharides, Disaccharides, Monosaccharides, And Polyols קבוצת פחמימות קצרות שרשרת אשר אינן נספגות היטב במעי הדק. חומרים אלו נותרים במעי, מושכים מים באופן אוסמוטי, ומותססים במעי הגס על ידי חיידקים. כתוצאה מכך, עלולה להיווצר נפיחות, גזים, כאבי בטן ושינויים ביציאות – תסמינים אופייניים ל-IBS[69].
הדיאטה מחולקת לשלושה שלבים עיקריים[68][70]:
- שלב ראשון - הימנעות ממזונות עשירים ב-FODMAP למשך 4–6 שבועות תוך מעקב אחר תסמינים
- שלב שני - החזרה הדרגתית של מזונות עתירי FODMAP לזיהוי המזונות הספציפיים המעוררים תסמינים
- שלב שלישי - התאמה אישית של התזונה לטווח הארוך בהתבסס על הממצאים
מחקרים רבים הראו כי הפחתת FODMAP משפרת משמעותית את תסמיני IBS[71][72][73][74][75][76]. מטא-אנליזה של 10 מחקרים אקראיים מצאה שדיאטה דלת FODMAP שיפרה את התסמינים הכלליים של IBS בהשוואה לדיאטה רגילה[76].
מטופלים עם IBS-M עשויים להרוויח במיוחד מהתערבויות באורח החיים והתזונה. אם תסמינים מתמשכים, אנו ממליצים על חזרה על ניסיונות תוספת סיבים ודיאטה דלת FODMAP, ובמידת הצורך שילוב טיפול תרופתי.
הטיפול הראשוני ב-IBS משלב גישה הוליסטית של שינויים באורח החיים, תזונה, והתערבויות התנהגותיות, עם אפשרות לשילוב טיפולים תרופתיים בהתאם לצורך. התאמת התוכנית האישית לכל מטופל חשובה למקסום ההקלה בתסמינים ולשיפור איכות החיים.
טיפול תרופתי מותאם לתת סוג של IBS
כאשר שינויים באורח החיים והתאמות תזונתיות (כגון תוספת סיבים מסיסים כמו פסיליום, שיבולת שועל) אינם מספקים הקלה, נעשה שימוש בטיפול תרופתי נוסף בהתאם לתת-הסוג של IBS.
טיפול תרופתי ל-IBS עם עצירות דומיננטית (IBS-C)
קו ראשון
PEG (פוליאתילן גליקול) - חומר משלשל אוסמוטי המועדף לטיפול ראשוני, בשל יעילותו, זמינותו הגבוהה, והיותו נסבל היטב. חומר זה משפר עצירות אך אינו מקל על כאבי בטן[77][78]. אם הכאב נמשך, ניתן להוסיף טיפול נוסף לתסמינים כלליים.
קו שני
- Linaclotide (לינקלוטיד) - תרופה שמשפרת הן עצירות והן כאבי בטן
- Plecanatide (פליקנטייד) – תרופה שמשפרת כאבי בטן ותדירות יציאות
חלופות
- Lubiprostone (לוביפרוסטון) - מאושר בארצות הברית רק לנשים, אך מחקרים מראים יעילות גם בגברים. תופעת לוואי של בחילה ב-8 אחוזים מהמקרים אך פחות שלשולים בהשוואה לטיפולים אחרים
- Tenapanor (טנאפאנור) - תרופה חדשה יותר, המתאימה למטופלים שלא הגיבו לטיפולים קודמים
טיפול תרופתי ל-IBS עם שלשולים דומיננטיים (IBS-D)
קו ראשון
Loperamide (לופרמיד) - טיפול הבחירה הראשון ל-IBS-D בשל בטיחותו, זמינותו, וקלות התאמת המינון. מפחית תדירות יציאות ומשפר את מרקמן, אך אינו משפר נפיחות או כאבי בטן[79][80][81].
קו שני
סופחי חומצות מרה (כולסטיראמין, כולסטיפול, כולסבלם) - משפר את זמן מעבר הצואה ואת הרגלי היציאות. כ-50 אחוזים מחולי IBS-D סובלים מספיגה לקויה של חומצות מרה, מה שמגביר את שלשולים. סופחי חומצות מרה קושרים את החומצות ומונעים את השפעתן[82][83].
חלופות
- Rifaximin (ריפקסימין) - אופציה לחולים עם תסמינים חמורים ונפיחות משמעותית[84]
- Alosetron (אלוסטרון) - לטיפול ב-IBS-D קשה, בעיקר בנשים
- Eluxadoline (אלוקסדולין) - למקרים עמידים בלבד, תחת פיקוח רפואי קפדני בשל סיכון לתופעות לוואי חמורות כמו דלקת לבלב חריפה[85][86][87]
טיפול ב-IBS עם הרגלי יציאות מעורבים (IBS-M) או לא מסווגים (IBS-U)
בניגוד ל-IBS עם עצירות דומיננטית (IBS-C) או שלשולים דומיננטיים (IBS-D), מטופלים עם IBS-M ו-IBS-U אינם מציגים דפוס יציאות ברור. לכן, אין להמליץ על טיפול תרופתי ממוקד ליציאות, שכן הוא עלול להחמיר את התסמינים. במקום זאת, הגישה מבוססת על התערבות תזונתית והתנהגותית והתאמה שוטפת של האבחנה בהתאם לשינויים בתסמינים.
טיפול תרופתי לתסמינים כלליים של IBS
תסמינים כלליים של IBS כוללים כאבי בטן, עוויתות ונפיחות. כאשר תסמינים אלו נמשכים אף על שינויים באורח החיים, התאמות תזונתיות וטיפול ממוקד לתת-הסוג של IBS, משתמשים בגישה משולבת של:
- טיפול תרופתי קצר-טווח לשליטה בהתקפים חריפים:
- אנטיכולינרגים (Anticholinergics) - חסימת קולטני אצטילכולין במערכת העיכול מובילה להפחתת עוויתות וכאב
- שמן מנטה (Peppermint oil) - בעל השפעה אנטי-מיקרוביאלית, אנטי-דלקתית ומרפה שרירים[88]
- Alverine (אלברין), Mebeverine (מבברין), Pinaverium (פינאבריום) – פועלים על חסימת תעלות סידן להרפיית שרירי המעי
- טיפול תרופתי ממושך לתסמינים יומיומיים:
טיפולים פסיכולוגיים משלימים לטיפול ב-IBS
טיפולים פסיכולוגיים, כגון היפנוזה ממוקדת-מעי (Gut-directed hypnotherapy), טיפול קוגניטיבי-התנהגותי (CBT) וטיפול מבוסס מיינדפולנס (MBSR), משפרים את תסמיני IBS ואת המצב הפסיכולוגי של המטופלים. טיפולים אלו מומלצים במיוחד עבור:
- מטופלים עם הפרעות מצב רוח נלוות
- מטופלים המעדיפים גישה לא-תרופתית
- מטופלים עם תסמינים עמידים לטיפולים אחרים
טיפולים אלו מתמקדים בשיפור הקשר בין המוח למערכת העיכול, אשר משוער כי הוא הגורם העיקרי ל-IBS.
טיפול קוגניטיבי-התנהגותי (CBT)
טיפול ממוקד-מטרה שנועד להפחית מחשבות והתנהגויות הקשורות ללחץ. מסייע בהפחתת כאב, חרדה ודיכאון, ומשפר את תדירות וחומרת התסמינים[94]. מטא-אנליזה של 19 מחקרים הראתה כי כל צורות ה-CBT (כולל טיפול טלפוני, פרטני, קבוצתי או עצמאי) היו יעילות יותר משמירה על שגרת טיפול רגילה[95].
היפנוזה ממוקדת-מעי (Gut-directed hypnotherapy)
מבוססת על הנחיות של מטפל להירגעות והרגעת מערכת העיכול. המטופלים שומרים על שליטה מלאה בתודעה ובגוף לאורך כל הטיפול. מחקר אקראי בקרב 354 מטופלים הראה כי 41 אחוזים מהמטופלים בהיפנוזה פרטנית השיגו הקלה בתסמינים לאחר 3 חודשים, בהשוואה ל-17 אחוזים בלבד שקיבלו טיפול תומך חינוכי[95][96][97][98][99].
טיפול מבוסס מיינדפולנס (MBSR)
טכניקת הרפיה המסייעת להתמודדות עם סטרס וכאב כרוני. מחקר שכלל 68 מטופלים מצא כי תוכנית בת 8 שבועות של MBSR שיפרה את חומרת ה-IBS ואת איכות החיים והפחיתה פחד וחרדה הקשורים למערכת העיכול.
לסיכום הטיפול
הטיפול בתסמונת המעי הרגיז (IBS) מבוסס על גישה רב-תחומית הכוללת התאמות באורח החיים, שינויים תזונתיים, טיפול תרופתי לפי תת-הסוג, ותמיכה פסיכולוגית. הדגש הראשוני הוא על פעילות גופנית, שיפור איכות השינה וניהול סטרס, לצד התאמת התזונה למטופל. במקרים בהם שינוי אורח החיים אינו מספק, נעשה שימוש בטיפול תרופתי בהתאם לדפוס היציאות, ובמידת הצורך משולבים טיפולים פסיכולוגיים כמו CBT או היפנוזה ממוקדת-מעי. במקרים עמידים, משלבים גישות טיפוליות נוספות להקלה על התסמינים ושיפור איכות החיים.
ביבליוגרפיה
- ↑ Drossman DA, Camilleri M, Mayer EA, Whitehead WE. AGA technical review on irritable bowel syndrome. Gastroenterology 2002; 123:2108.
- ↑ Camilleri M. Peripheral mechanisms in irritable bowel syndrome. N Engl J Med 2012; 367:1626.
- ↑ Houghton LA, Lea R, Agrawal A, et al. Relationship of abdominal bloating to distention in irritable bowel syndrome and effect of bowel habit. Gastroenterology 2006; 131:1003.
- ↑ Chadwick VS, Chen W, Shu D, et al. Activation of the mucosal immune system in irritable bowel syndrome. Gastroenterology 2002; 122:1778.
- ↑ Törnblom H, Lindberg G, Nyberg B, Veress B. Full-thickness biopsy of the jejunum reveals inflammation and enteric neuropathy in irritable bowel syndrome. Gastroenterology 2002; 123:1972.
- ↑ Guilarte M, Santos J, de Torres I, et al. Diarrhoea-predominant IBS patients show mast cell activation and hyperplasia in the jejunum. Gut 2007; 56:203.
- ↑ Barbara G, Stanghellini V, De Giorgio R, et al. Activated mast cells in proximity to colonic nerves correlate with abdominal pain in irritable bowel syndrome. Gastroenterology 2004; 126:693.
- ↑ Halvorson HA, Schlett CD, Riddle MS. Postinfectious irritable bowel syndrome--a meta-analysis. Am J Gastroenterol 2006; 101:1894.
- ↑ Thabane M, Kottachchi DT, Marshall JK. Systematic review and meta-analysis: The incidence and prognosis of post-infectious irritable bowel syndrome. Aliment Pharmacol Ther 2007; 26:535.
- ↑ Porcari S, Ingrosso MR, Maida M, et al. Prevalence of irritable bowel syndrome and functional dyspepsia after acute gastroenteritis: systematic review and meta-analysis. Gut 2024; 73:1431.
- ↑ Niaz SK, Sandrasegaran K, Renny FH, Jones BJ. Postinfective diarrhoea and bile acid malabsorption. J R Coll Physicians Lond 1997; 31:53.
- ↑ Sinha L, Liston R, Testa HJ, Moriarty KJ. Idiopathic bile acid malabsorption: qualitative and quantitative clinical features and response to cholestyramine. Aliment Pharmacol Ther 1998; 12:839.
- ↑ Törnblom H, Holmvall P, Svenungsson B, Lindberg G. Gastrointestinal symptoms after infectious diarrhea: a five-year follow-up in a Swedish cohort of adults. Clin Gastroenterol Hepatol 2007; 5:461.
- ↑ Maxwell PR, Rink E, Kumar D, Mendall MA. Antibiotics increase functional abdominal symptoms. Am J Gastroenterol 2002; 97:104.
- ↑ Kassinen A, Krogius-Kurikka L, Mäkivuokko H, et al. The fecal microbiota of irritable bowel syndrome patients differs significantly from that of healthy subjects. Gastroenterology 2007; 133:24.
- ↑ Malinen E, Rinttilä T, Kajander K, et al. Analysis of the fecal microbiota of irritable bowel syndrome patients and healthy controls with real-time PCR. Am J Gastroenterol 2005; 100:373.
- ↑ Rajilić-Stojanović M, Biagi E, Heilig HG, et al. Global and deep molecular analysis of microbiota signatures in fecal samples from patients with irritable bowel syndrome. Gastroenterology 2011; 141:1792.
- ↑ Saulnier DM, Riehle K, Mistretta TA, et al. Gastrointestinal microbiome signatures of pediatric patients with irritable bowel syndrome. Gastroenterology 2011; 141:1782.
- ↑ Jeffery IB, O'Toole PW, Öhman L, et al. An irritable bowel syndrome subtype defined by species-specific alterations in faecal microbiota. Gut 2012; 61:997.
- ↑ Crouzet L, Gaultier E, Del'Homme C, et al. The hypersensitivity to colonic distension of IBS patients can be transferred to rats through their fecal microbiota. Neurogastroenterol Motil 2013; 25:e272.
- ↑ Camilleri M. Probiotics and irritable bowel syndrome: rationale, mechanisms, and efficacy. J Clin Gastroenterol 2008; 42 Suppl 3 Pt 1:S123.
- ↑ Nobaek S, Johansson ML, Molin G, et al. Alteration of intestinal microflora is associated with reduction in abdominal bloating and pain in patients with irritable bowel syndrome. Am J Gastroenterol 2000; 95:1231.
- ↑ Maccaferri S, Candela M, Turroni S, et al. IBS-associated phylogenetic unbalances of the intestinal microbiota are not reverted by probiotic supplementation. Gut Microbes 2012; 3:406.
- ↑ Yu D, Cheeseman F, Vanner S. Combined oro-caecal scintigraphy and lactulose hydrogen breath testing demonstrate that breath testing detects oro-caecal transit, not small intestinal bacterial overgrowth in patients with IBS. Gut 2011; 60:334.
- ↑ Lin EC, Massey BT. Scintigraphy Demonstrates High Rate of False-positive Results From Glucose Breath Tests for Small Bowel Bacterial Overgrowth. Clin Gastroenterol Hepatol 2016; 14:203.
- ↑ Spiegel BM. Questioning the bacterial overgrowth hypothesis of irritable bowel syndrome: an epidemiologic and evolutionary perspective. Clin Gastroenterol Hepatol 2011; 9:461.
- ↑ Posserud I, Stotzer PO, Björnsson ES, et al. Small intestinal bacterial overgrowth in patients with irritable bowel syndrome. Gut 2007; 56:802.
- ↑ Monsbakken KW, Vandvik PO, Farup PG. Perceived food intolerance in subjects with irritable bowel syndrome-- etiology, prevalence and consequences. Eur J Clin Nutr 2006; 60:667.
- ↑ Simrén M, Månsson A, Langkilde AM, et al. Food-related gastrointestinal symptoms in the irritable bowel syndrome. Digestion 2001; 63:108.
- ↑ Arsiè E, Coletta M, Cesana BM, Basilisco G. Symptom-association probability between meal ingestion and abdominal pain in patients with irritable bowel syndrome. Does somatization play a role? Neurogastroenterol Motil 2015; 27:416.
- ↑ Ford AC, Staudacher HM, Talley NJ. Postprandial symptoms in disorders of gut-brain interaction and their potential as a treatment target. Gut 2024; 73:1199.
- ↑ Saito YA, Petersen GM, Locke GR 3rd, Talley NJ. The genetics of irritable bowel syndrome. Clin Gastroenterol Hepatol 2005; 3:1057.
- ↑ Kim HJ, Camilleri M, Carlson PJ, et al. Association of distinct alpha(2) adrenoceptor and serotonin transporter polymorphisms with constipation and somatic symptoms in functional gastrointestinal disorders. Gut 2004; 53:829.
- ↑ Yeo A, Boyd P, Lumsden S, et al. Association between a functional polymorphism in the serotonin transporter gene and diarrhoea predominant irritable bowel syndrome in women. Gut 2004; 53:1452.
- ↑ Pata C, Erdal ME, Derici E, et al. Serotonin transporter gene polymorphism in irritable bowel syndrome. Am J Gastroenterol 2002; 97:1780.
- ↑ Lee DY, Park H, Kim WH, et al. [Serotonin transporter gene polymorphism in healthy adults and patients with irritable bowel syndrome]. Korean J Gastroenterol 2004; 43:18.
- ↑ Gonsalkorale WM, Perrey C, Pravica V, et al. Interleukin 10 genotypes in irritable bowel syndrome: evidence for an inflammatory component? Gut 2003; 52:91
- ↑ Keck ME, Holsboer F. Hyperactivity of CRH neuronal circuits as a target for therapeutic interventions in affective disorders. Peptides 2001; 22:835.
- ↑ Fukudo S, Nomura T, Hongo M. Impact of corticotropin-releasing hormone on gastrointestinal motility and adrenocorticotropic hormone in normal controls and patients with irritable bowel syndrome. Gut 1998; 42:845.
- ↑ 40.0 40.1 Longstreth GF, Thompson WG, Chey WD, et al. Functional bowel disorders. Gastroenterology 2006; 130:1480.
- ↑ Swarbrick ET, Hegarty JE, Bat L, et al. Site of pain from the irritable bowel. Lancet 1980; 2:443
- ↑ Simren M, Palsson OS, Whitehead WE. Update on Rome IV Criteria for Colorectal Disorders: Implications for Clinical Practice. Curr Gastroenterol Rep 2017; 19:15.
- ↑ Manning AP, Thompson WG, Heaton KW, Morris AF. Towards positive diagnosis of the irritable bowel. Br Med J 1978; 2:653.
- ↑ 44.0 44.1 Mearin F, Lacy BE, Chang L, et al. Bowel Disorders. Gastroenterology 2016; 150:1393 .45
- ↑ Smalley W, Falck-Ytter C, Carrasco-Labra A, et al. AGA Clinical Practice Guidelines on the Laboratory Evaluation of Functional Diarrhea and Diarrhea-Predominant Irritable Bowel Syndrome in Adults (IBS-D). Gastroenterology 2019; 157:851.
- ↑ American College of Gastroenterology Task Force on Irritable Bowel Syndrome, Brandt LJ, Chey WD, et al. An evidence-based position statement on the management of irritable bowel syndrome. Am J Gastroenterol 2009; 104 Suppl 1:S1.
- ↑ Mearin F, Lacy BE, Chang L, et al. Bowel Disorders. Gastroenterology 2016; 150:1393.49
- ↑ Longstreth GF, Thompson WG, Chey WD, et al. Functional bowel disorders. Gastroenterology 2006; 130:1480
- ↑ Blake MR, Raker JM, Whelan K. Validity and reliability of the Bristol Stool Form Scale in healthy adults and patients with diarrhoea-predominant irritable bowel syndrome. Aliment Pharmacol Ther 2016; 44:693.
- ↑ Palsson OS, Baggish JS, Turner MJ, Whitehead WE. IBS patients show frequent fluctuations between loose/watery and hard/lumpy stools: implications for treatment. Am J Gastroenterol 2012; 107:286.
- ↑ Owens DM, Nelson DK, Talley NJ. The irritable bowel syndrome: long-term prognosis and the physician-patient interaction. Ann Intern Med 1995; 122:107.
- ↑ Drossman DA, Thompson WG. The irritable bowel syndrome: review and a graduated multicomponent treatment approach. Ann Intern Med 1992; 116:1009.
- ↑ Kaptchuk TJ, Kelley JM, Conboy LA, et al. Components of placebo effect: randomised controlled trial in patients with irritable bowel syndrome. BMJ 2008; 336:999.
- ↑ Johannesson E, Simrén M, Strid H, et al. Physical activity improves symptoms in irritable bowel syndrome: a randomized controlled trial. Am J Gastroenterol 2011; 106:915.
- ↑ Patel A, Hasak S, Cassell B, et al. Effects of disturbed sleep on gastrointestinal and somatic pain symptoms in irritable bowel syndrome. Aliment Pharmacol Ther 2016; 44:246.
- ↑ Topan R, Vork L, Fitzke H, et al. Poor Subjective Sleep Quality Predicts Symptoms in Irritable Bowel Syndrome Using the Experience Sampling Method. Am J Gastroenterol 2024; 119:155.
- ↑ Siah KT, Wong RK, Ho KY. Melatonin for the treatment of irritable bowel syndrome. World J Gastroenterol 2014; 20:2492.
- ↑ Naliboff BD, Smith SR, Serpa JG, et al. Mindfulness-based stress reduction improves irritable bowel syndrome (IBS) symptoms via specific aspects of mindfulness. Neurogastroenterol Motil 2020; 32:e13828.
- ↑ Kearney DJ, McDermott K, Martinez M, Simpson TL. Association of participation in a mindfulness programme with bowel symptoms, gastrointestinal symptom-specific anxiety and quality of life. Aliment Pharmacol Ther 2011; 34:363.
- ↑ Horn A, Stangl S, Parisi S, et al. Systematic review with meta-analysis: Stress-management interventions for patients with irritable bowel syndrome. Stress Health 2023; 39:694.
- ↑ Black CJ, Thakur ER, Houghton LA, et al. Efficacy of psychological therapies for irritable bowel syndrome: systematic review and network meta-analysis. Gut 2020; 69:1441.
- ↑ Slouha E, Patel B, Mohamed A, et al. Psychotherapy for Irritable Bowel Syndrome: A Systematic Review. Cureus 2023; 15:e51003.
- ↑ Nakao M, Shirotsuki K, Sugaya N. Cognitive-behavioral therapy for management of mental health and stress-related disorders: Recent advances in techniques and technologies. Biopsychosoc Med 2021; 15:16.
- ↑ Monsbakken KW, Vandvik PO, Farup PG. Perceived food intolerance in subjects with irritable bowel syndrome-- etiology, prevalence and consequences. Eur J Clin Nutr 2006; 60:667.
- ↑ Simrén M, Månsson A, Langkilde AM, et al. Food-related gastrointestinal symptoms in the irritable bowel syndrome. Digestion 2001; 63:108.
- ↑ Ireton-Jones C, Weisberg MF. Management of Irritable Bowel Syndrome: Physician-Dietitian Collaboration. Nutr Clin Pract 2020; 35:826.
- ↑ Tuck CJ, Reed DE, Muir JG, Vanner SJ. Implementation of the low FODMAP diet in functional gastrointestinal symptoms: A real-world experience. Neurogastroenterol Motil 2020; 32:e13730.
- ↑ 68.0 68.1 Chey WD, Hashash JG, Manning L, Chang L. AGA Clinical Practice Update on the Role of Diet in Irritable Bowel Syndrome: Expert Review. Gastroenterology 2022; 162:1737
- ↑ Gibson PR. History of the low FODMAP diet. J Gastroenterol Hepatol 2017; 32 Suppl 1:5.
- ↑ McKenzie YA, Alder A, Anderson W, et al. British Dietetic Association evidence-based guidelines for the dietary management of irritable bowel syndrome in adults. J Hum Nutr Diet 2012; 25:260.
- ↑ Rao SS, Yu S, Fedewa A. Systematic review: dietary fibre and FODMAP-restricted diet in the management of constipation and irritable bowel syndrome. Aliment Pharmacol Ther 2015; 41:1256.
- ↑ Shepherd SJ, Parker FC, Muir JG, Gibson PR. Dietary triggers of abdominal symptoms in patients with irritable bowel syndrome: randomized placebo-controlled evidence. Clin Gastroenterol Hepatol 2008; 6:765.
- ↑ Ong DK, Mitchell SB, Barrett JS, et al. Manipulation of dietary short chain carbohydrates alters the pattern of gas production and genesis of symptoms in irritable bowel syndrome. J Gastroenterol Hepatol 2010; 25:1366.
- ↑ Austin GL, Dalton CB, Hu Y, et al. A very low-carbohydrate diet improves symptoms and quality of life in diarrhea-predominant irritable bowel syndrome. Clin Gastroenterol Hepatol 2009; 7:706.
- ↑ Eswaran SL, Chey WD, Han-Markey T, et al. A Randomized Controlled Trial Comparing the Low FODMAP Diet vs. Modified NICE Guidelines in US Adults with IBS-D. Am J Gastroenterol 2016; 111:1824.
- ↑ 76.0 76.1 Wang J, Yang P, Zhang L, Hou X. A Low-FODMAP Diet Improves the Global Symptoms and Bowel Habits of Adult IBS Patients: A Systematic Review and Meta-Analysis. Front Nutr 2021; 8:683191.
- ↑ Khoshoo V, Armstead C, Landry L. Effect of a laxative with and without tegaserod in adolescents with constipation predominant irritable bowel syndrome. Aliment Pharmacol Ther 2006; 23:191.
- ↑ Chapman RW, Stanghellini V, Geraint M, Halphen M. Randomized clinical trial: macrogol/PEG 3350 plus electrolytes for treatment of patients with constipation associated with irritable bowel syndrome. Am J Gastroenterol 2013; 108:1508.
- ↑ Cann PA, Read NW, Holdsworth CD, Barends D. Role of loperamide and placebo in management of irritable bowel syndrome (IBS). Dig Dis Sci 1984; 29:239.
- ↑ Hovdenak N. Loperamide treatment of the irritable bowel syndrome. Scand J Gastroenterol Suppl 1987; 130:81.81
- ↑ Efskind PS, Bernklev T, Vatn MH. A double-blind placebo-controlled trial with loperamide in irritable bowel syndrome. Scand J Gastroenterol 1996; 31:463.
- ↑ Wedlake L, A'Hern R, Russell D, et al. Systematic review: the prevalence of idiopathic bile acid malabsorption as diagnosed by SeHCAT scanning in patients with diarrhoea-predominant irritable bowel syndrome. Aliment Pharmacol Ther 2009; 30:707.
- ↑ Fernández-Bañares F, Esteve M, Salas A, et al. Systematic evaluation of the causes of chronic watery diarrhea with functional characteristics. Am J Gastroenterol 2007; 102:2520.
- ↑ Menees SB, Maneerattannaporn M, Kim HM, Chey WD. The efficacy and safety of rifaximin for the irritable bowel syndrome: a systematic review and meta-analysis. Am J Gastroenterol 2012; 107:28.
- ↑ Lembo A, Sultan S, Chang L, et al. AGA Clinical Practice Guideline on the Pharmacological Management of Irritable Bowel Syndrome With Diarrhea. Gastroenterology 2022; 163:137
- ↑ Dove LS, Lembo A, Randall CW, et al. Eluxadoline benefits patients with irritable bowel syndrome with diarrhea in a phase 2 study. Gastroenterology 2013; 145:329.
- ↑ FDA drug safety communication: FDA warns about increased risk of serious pancreatitis with irritable bowel drug Viberzi (eluxadoline) in patients without a gallbladder. US Food and Drug Administration, 2017. https://www.fda.gov/drugs/drug-safety-and-availability/fda-drug-safety-communication-fda-warns-about-increased-risk-serious-pancreatitis-irritable-bowel (Accessed on March 15, 2017).
- ↑ Chumpitazi BP, Kearns GL, Shulman RJ. Review article: the physiological effects and safety of peppermint oil and its efficacy in irritable bowel syndrome and other functional disorders. Aliment Pharmacol Ther 2018; 47:738.
- ↑ Gorard DA, Libby GW, Farthing MJ. Effect of a tricyclic antidepressant on small intestinal motility in health and diarrhea-predominant irritable bowel syndrome. Dig Dis Sci 1995; 40:86.
- ↑ Bueno L, Fioramonti J, Delvaux M, Frexinos J. Mediators and pharmacology of visceral sensitivity: from basic to clinical investigations. Gastroenterology 1997; 112:1714.
- ↑ Ford AC, Talley NJ, Schoenfeld PS, et al. Efficacy of antidepressants and psychological therapies in irritable bowel syndrome: systematic review and meta-analysis. Gut 2009; 58:367.
- ↑ Ruepert L, Quartero AO, de Wit NJ, et al. Bulking agents, antispasmodics and antidepressants for the treatment of irritable bowel syndrome. Cochrane Database Syst Rev 2011; :CD003460.
- ↑ American College of Gastroenterology Task Force on Irritable Bowel Syndrome, Brandt LJ, Chey WD, et al. An evidence-based position statement on the management of irritable bowel syndrome. Am J Gastroenterol 2009; 104 Suppl 1:S1.
- ↑ Nakao M, Shirotsuki K, Sugaya N. Cognitive-behavioral therapy for management of mental health and stress-related disorders: Recent advances in techniques and technologies. Biopsychosoc Med 2021; 15:16.
- ↑ 95.0 95.1 Black CJ, Thakur ER, Houghton LA, et al. Efficacy of psychological therapies for irritable bowel syndrome: systematic review and network meta-analysis. Gut 2020; 69:1441.
- ↑ Goodoory VC, Khasawneh M, Thakur ER, et al. Effect of Brain-Gut Behavioral Treatments on Abdominal Pain in Irritable Bowel Syndrome: Systematic Review and Network Meta-Analysis. Gastroenterology 2024; 167:934.
- ↑ Lindfors P, Unge P, Arvidsson P, et al. Effects of gut-directed hypnotherapy on IBS in different clinical settings-results from two randomized, controlled trials. Am J Gastroenterol 2012; 107:276.
- ↑ Flik CE, Laan W, Zuithoff NPA, et al. Efficacy of individual and group hypnotherapy in irritable bowel syndrome (IMAGINE): a multicentre randomised controlled trial. Lancet Gastroenterol Hepatol 2019; 4:20.
- ↑ Moser G, Trägner S, Gajowniczek EE, et al. Long-term success of GUT-directed group hypnosis for patients with refractory irritable bowel syndrome: a randomized controlled trial. Am J Gastroenterol 2013; 108:602.
המידע שבדף זה נכתב על ידי ד"ר מיקי דובלין, מומחה ברפואת ילדים, עודכן ב-2025 על ידי ד"ר ליאור זורניצקי


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק