לוקמיה לימפואידית חדה - חידושים בטיפול - 2015 - Acute lymphoblastic leukemia - new treatments
הופניתם מהדף ALL – new treatments לדף הנוכחי.
| לוקמיה לימפואידית חדה – חידושים בטיפול | ||
|---|---|---|
| Acute Lymphoblastic Leukemia – New treatments | ||
| 250px | ||
Two girls with ALL demonstrating intravenous access for chemotherapy
| ||
| יוצר הערך | ד"ר רון רם | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לוקמיה לימפובלסטית חדה (חריפה)
לויקמיה לימפואידית חריפה (לל"ח) היא לויקמיה עם ביטוי ביולוגי הטרוגני וניתן לחלקה ל־לל"ח של תאי B ולל"ח של תאי T. את הסוג הראשון ניתן לחלק לחולים עם לל"ח המלווה בהפרעה בכרומוזום פילדלפיה (BCR-ABL) ולחולים שמחלתם אינה מלווה בהפרעה זאת.
בעוד שלל"ח היא הממאירות השכיחה ביותר בילדות, במבוגרים הסוג הזה של לויקמיה נדיר יותר. יתר על כן, בעוד שסיכויי ההבראה בילדים הם גבוהים, מרבית המבוגרים המפתחים לל"ח נזקקים לטיפול כימותרפי ממושך ולהשתלת מח עצם כדי להביא לריפוי מלא של המחלה. גם לאחר השתלת מח עצם, סיכויי ההבראה במבוגרים עומדים על כ־40 אחוזים ולפיכך גישות חדשות נדרשות על מנת לטייב את הטיפול[1]. בחולים אשר מחלתם אינה מגיבה לטיפול ראשוני ובאלה אשר מחלתם נשנית לאחר טיפול ראשוני, סיכויי ההחלמה הם נמוכים ביותר.
מאמר זה יסקור ארבע גישות חדשות לטיפול במבוגרים עם לל"ח אשר נושאות בחובן שיפור משמעותי באיכות הטיפול ובהצלחתו.
אימונותרפיה
אימונותרפיה מהווה בסיס חשוב בטיפול של ממאירויות רבות, בהן גם לויקמיה. על הטיפול האימוני בלויקמיה להיות אפקטיבי ופעיל כנגד הבלסטים הלויקמים מחד, ומאידך עליו להראות פרופיל בטיחות טוב, כך שלא יעלה את רעילות הטיפול הכימותרפי.
השימוש הראשון באימונותרופיה היה באמצעות נוגדנים ספציפיים לאתרים ייחודיים על הבלסטים הלויקמים. כך למשל, הן Rituximab והן Ofatumumab הם נוגדנים ספציפיים כנגד CD20 המבוטא על חלק מהבלסטים הלויקמים מסוג B[2][3]. Alemtuzumab הוא נוגדן כנגד CD52 המבוטא בחלק מהמקרים של לל"ח מסוג B ומסוג T. הבעיה העיקרית בשימוש בנוגדן זה היא השכיחות הגבוהה של התפתחות מחלות זיהומיות ויראליות[2].
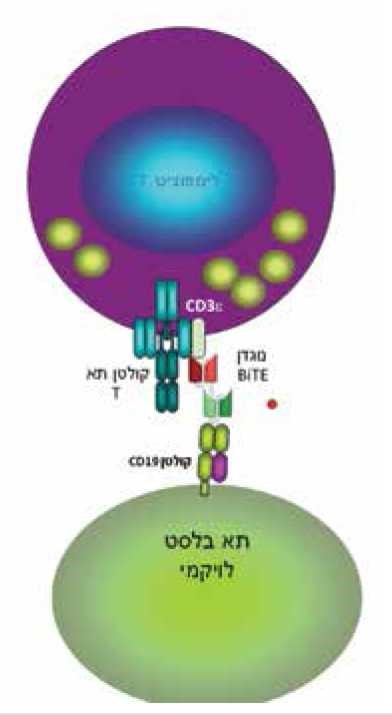
CD19 הוא קולטן שייחודו הוא בכך שהוא מצוי רק על לימפוציטים מסוג B ואינו מצוי על תאי דם אחרים. לפיכך, הוא מבוטא בעודף על רוב תאי לל"ח מסוג B (ניתן למצאו גם בממאירויות אחרות של תאי B כדוגמת לימפומה ולויקמיה לימפטית כרונית). הנוגדן הדו־ספציפי Blinatumomab (Bispecific CD19/CD3 T-cell engaging monoclonal antibody), היה הנוגדן הראשון אשר לו שתי זרועות ולא רק זרוע אחת כמו לשאר הנוגדנים המונוקלונלים[4]. הזרוע האחת היא נוגדן לחלבון CD19 המוצג על הבלסטים הלויקמים והזרוע השנייה היא נוגדן לחלבון CD3 המיוצג על תאים לימפוציטים (תמונה מספר 1). הקישור שנוצר בין הבלסט הלויקמי והתא הלימפוציטרי גורם להרס של התא הבלסטי. בנוסף, מתרחשת פרוליפרציה של תאי T מסוגים CD4 ,CD8 אשר הם סגוליים לבלסטים הלויקמים[4][5].
בוצעו מספר מחקרי פאזה שנייה באוכלוסיות חולים שונות שבדקו את יעילות התרופה (טבלה מספר 1). Blinatumomab הראה יעילות במספר מתארים של חולים על לל"ח:
- בחולים עם לל"ח שנשנתה והייתה עמידה לטיפול כימותרפי, שימוש בנוגדן הביא להשגת הפוגה ב־70-30 אחוזים מהחולים ובכ־30 אחוזים מהם אפשר המשך טיפול באמצעות השתלת מח עצם אלוגנאית כדי להשיג ריפוי מלא של המחלה[6]. נתון זה טוב בהרבה מהסיכוי להצלחת משלבים כימותרפים אחרים בחולים עם מחלה נשנית או עמידה. ב-2016 מסתיים מחקר רב מרכזי פאזה שלישית אשר משווה בין תוצאות הטיפול ב-Blinatumomab לכימותרפיה בחולים עם מחלה נשנית או עמידה. תוצאות מחקר זה, באם תמצאנה חיוביות, תבססנה את השימוש ב-Blinatumomab בחולים עם מחלה נשנית או עמידה לטיפול כימותרפי
- חולים עם לל"ח עם מחלה שאריתית מינימלית - כפי שיוסבר בהמשך, מחלה שאריתית מינימלית היא פקטור בעל משמעות פרוגנוסטית חשובה ביותר. במחקר פאזה שנייה נמצא שבחולים עם מחלה שאריתית מינימלית לאחר משלב כימותרפי, השימוש ב-Blinatumomab הביא להעלמת הלויקמיה בצורה מלאה ב־80 אחוזים מהחולים[7]. היעלמות מלאה של המחלה צפויה לשפר את הסיכוי לריפוי של המחלה ואנו ממתינים לנתונים ממחקרים אחרים כדי לראות האם בחולים אשר המחלה המינימלית נעלמה, ניתן יהיה להביא לריפוי מלא של המחלה גם ללא ביצוע של השתלת מח עצם מתורם
- מתבצעים מספר מחקרים הבודקים את השימוש ב-Blinatumomab כקו טיפולי ראשון הן בחולים צעירים, שם הוא ניתן בתוספת לכימותרפיה, והן בחולים מבוגרים, להם הוא ניתן כתחליף לטיפול כימותרפי. אם תוצאות מחקרים אלה תמצאנה חיוביות, Blinatumomab יינתן בעתיד כקו טיפולי ראשון בכל חולה לויקמיה של תאי B המבטאים את החלבון ל-CD19. בכל המחקרים שנסקרו, תופעת הלוואי העיקרית שנצפתה הייתה חום הקשור לעירוי מתן התרופה. בנוסף, בחולים עם מעורבות מוחית של לויקמיה נצפו מגוון של תופעות לוואי עצביות ועקב כך התרופה אינה ניתנת לחולים עם מעורבות מוחית של הלויקמיה. על סמך מחקרי הפאזה השנייה שפורטו לעיל, התרופה קיבלה אישור FDA (Food and Drug Administration) בדצמבר 2014 לטיפול בחולים עם הישנות של לל"ח של תאי B. שיטה חדשנית נוספת לטיפול אימוני בחולי לל"ח מסוג B היא שימוש בתאי T אשר נלקחים מהחולה ו"מהונדסים" כך שיבטאו חלבונים (Chimeric Antigen Receptors, CARs) ספציפיים כנגד תאי הלויקמיה[1][8]. חלבונים אלה מבוססים על נוגדן כנגד אחד מהאנטיגנים של הבלסטים (במקרה זה אנטיגן CD19) אשר מחובר לחלק טרנסממברנלי המקושר לאלמנט המפעיל את האיתות התוך־תאי של הלימפוציט. החיבור של הנוגדן לאנטיגן על הבלסט גורם להפעלה של תא ה-T ולהרס של הבלסט הלויקמי. מספר מחקרים הראו את היעילות של שיטה זו הן בלל"ח והן בלויקמיה לימפוציטית כרונית. הטכנולוגיה לשימוש בתאים אלה אינה קיימת עדיין בישראל אולם ניסיונות קליניים ראשונים אמורים להתחיל בארץ בתחילת 2016
| המחקר | פאזה, קוהורט | מספר חולים | הפוגה מלאה | שרידות (OS) חציונית |
|---|---|---|---|---|
| Topp et al. JCO 2014 | פאזה 2, מבוגרים - חולים עם מחלה נשנית או עמידה | 36 | (69 אחוזים) 25 | 9.8 חודשים |
| Topp et al., Lancet Oncol 2015 | פאזה 2, מבוגרים - חולים עם מחלה נשנית או עמידה | 189 | (43 אחוזים) 81 | 6.1 חודשים |
| Gore et al, Blood.2014;124: abstr3703 | פאזה 2, ילדים - חולים עם מחלה נשנית או עמידה | 39 | (31 אחוזים) 12 | 4.3 חודשים |
| Goekbuget, Blood. 2014;124: .abstr379 | פאזה 2, מבוגרים - חולים מחלה שאריתית (MRD) | 116 | 78 אחוזים מהחולים -העלמות מחלה שאריתית | לא מדווח |
טיפול במתבגרים ובמבוגרים צעירים (גיל 39-16)
לל"ח היא נדירה בקבוצת גיל זו ובמשך שנים היה מקובל לטפל בקבוצת חולים זו כאילו היו חולים מבוגרים. כיוון שהצלחת הטיפול בלל"ח היא טובה יותר בילדים, בתחילת שנות ה־90 של המאה הקודמת היו מספר ניסיונות לאמץ משלבים הניתנים בילדים (Pediatric inspired regimens) בחולים מבוגרים צעירים. מספר עבודות הוכיחו שכאשר חולים אלה מקבלים טיפול המבוסס משלבים הניתנים בילדים, התוצאות הכלליות של הטיפול משתפרות בצורה משמעותית[9]. סקירה סיסטמטית ומטה־אנליזה שבוצעה על ידי קבוצתנו הוכיחו שגישה טיפולית זו אכן יעילה יותר[10]. עם זאת, יש לזכור, שטיפולים אלה רעילים יותר בהשוואה למשלבים המקוריים שניתנו למבוגרים ויש להקפיד הקפדת יתר על ניטור תופעות הלוואי[10].
טיפול המבוסס על מחלה שאריתית מינימלית (Minimal Residual Disease, MRD)
השיפור בבדיקות המעבדה, ובייחוד היכולת שלנו לזהות ב-PCR (Polymerase Chain Reaction) שרידי מחלה גם כאשר אין עדות למחלה מורפולוגית, הביאו לבחינת ההשפעה של נוכחות מחלה שאריתית מינימלית על המהלך הצפוי של לל"ח[1][7]. בבדיקה זו, קלונים ספציפיים של האימונוגלובולין או הקולטן של תא T הייחודי לבלסט הלויקמי עוברים אמפליפיקציה וריצוף באמצעות מכשיר PCR. לאחר מכן, מייצרים גלאים (PRIMERS) ספציפיים לרצפים הללו אשר גורמים לאמפליקציה של קלון (Clone) התאים הלויקמים. שיטה זו מאפשרת מעקב ומסוגלת לזהות בלסט לויקמי גם כשהוא מהווה רק 1:100000 תאים. מספר מחקרים הראו שכאשר יש מחלה שאריתית מינימלית לאחר תום הטיפול משרה הפוגה הראשון, הסבירות של הישנות הלויקמיה היא גבוהה. יתר על כן, מספר עבודות הראו שגורמי סיכון שבעבר ייחסנו להם חשיבות משמעותית בהחלטה הטיפולית בחולים עם לל"ח, אינם משמעותיים היום כאשר נבדקת מחלה שאריתית מינימלית. מתנהלים מספר מחקרים אשר בודקים האם שינוי טיפולי בשלב זה (כמו ביצוע השתלת מח עצם או מתן Blinatumomab) יאפשר השגת הפוגה ארוכה ו/או ריפוי המחלה[7][11].
טיפול בחולים עם הפרעה בכרומוזום פילדלפיה
עד כ־40 אחוזים מהחולים עם לל"ח בגיל המבוגר הם בעלי לויקמיה ייחודית אשר מתפתחת, בין השאר, כתוצאה משחלוף בין כרומוזום 9 לכרומוזום 22 (כרומוזום פילדלפיה, BCR-ABL). עד לפני מספר שנים, גם בחולים אשר עברו השתלת מח עצם תוחלת החיים בחולים הללו הייתה קצרה. עם התקדמות הטיפול בלויקמיה מיאלואידית כרונית והכנסת תרופות מעכבות טירוזין קינז (כדוגמת: Gleevec, Tasygna ו-Sprycel), הותחל גם השימוש בתרופות אלו בלל"ח עם הפרעות בכרומוזום פילדלפיה. השימוש בתרופות מעכבות טירוזין קינז חולל מהפך בטיפול ובתוחלת החיים של חולים עם מחלה זו. הטיפול בחולים הללו מבוסס על טיפול ראשוני המבוסס על סטרואידים עם או ללא כימותרפיה ומעכבי טירוזין קינז בלבד ולאחר מכן השתלת מח עצם מתורם[12][13]. תוחלת החיים בחולים אלה השתפרה מ־10 אחוזים לאחר שלוש שנים ל־60 אחוזים לאחר שלוש שנים. אף על פי שעדיין מקובל לבצע השתלת מח עצם מתורם בחולים הללו, מתבצעים מספר מחקרים אשר בודקים את נחיצות ההשתלה.
לסיכום, לויקמיה לימפואידית חריפה הפכה למחלה אשר פריצות הדרך בה הן משמעותיות ביותר ומשפיעות הן על הטיפול הבסיסי במחלה והן על אחוזי הריפוי מהמחלה. הכנסת תרופות חדשות לסל התרופות והמשך גיוס חולים למחקרים קליניים במרכזים רפואיים יאפשרו המשך שיפור הטיפול והארכת משך החיים של החולים.
ביבליוגרפיה
- ↑ 1.0 1.1 1.2 Jabbour E, O'Brien S, Konopleva M, Kantarjian H. New insights into the pathophysiology and therapy of adult acute lymphoblastic leukemia. Cancer. 2015 Aug 1;121(15):2517-28
- ↑ 2.0 2.1 Jabbour E, O'Brien S, Ravandi F, Kantarjian H. Monoclonal antibodies in acute lymphoblastic leukemia. Blood. 2015 Jun 25;125(26):4010-6
- ↑ Thomas DA, O'Brien S, Faderl S, Garcia-Manero G, Ferrajoli A, Wierda W, Ravandi F, Verstovsek S, Jorgensen JL, Bueso-Ramos C, Andreeff M, Pierce S, Garris R, Keating MJ, Cortes J, Kantarjian HM. Chemoimmunotherapy with a modified hyper-CVAD and rituximab regimen improves outcome in de novo Philadelphia chromosome-negative precursor B-lineage acute lymphoblastic leukemia. J Clin Oncol. 2010 Aug 20;28(24):3880-9.
- ↑ 4.0 4.1 Nagorsen D1, Baeuerle PA. Immunomodulatory therapy of cancer with T cell-engaging BiTE antibody blinatumomab. Exp Cell Res. 2011 May 15;317(9):1255-60
- ↑ Baeuerle PA, Reinhardt C. Bispecific T-cell engaging antibodies for cancer therapy.Cancer Res. 2009 Jun 15;69(12):4941-4
- ↑ Topp MS, Gdkbuget N, Stein AS, Zugmaier G, O'Brien S, Bargou RC, Dombret H, Fielding AK, Heffner L, Larson RA, Neumann S, Foa R, Litzow M, Ribera JM, Rambaldi A, Schiller G, Bruggemann M, Horst HA, Holland C, Jia C, Maniar T, Huber B, Nagorsen D, Forman SJ, Kantarjian HM.Safety and activity of blinatumomab for adult patients with relapsed or refractory B-precursor acute lymphoblastic leukaemia: a multicentre, single-arm, phase 2 study. Lancet Oncol. 2015 Jan;16(1):57-66
- ↑ 7.0 7.1 7.2 Topp MS, Gdkbuget N, Zugmaier G, Klappers P, Stelljes M, Neumann S, Viardot A, Marks R, Diedrich H, Faul C, Reichle A, Horst HA, Bruggemann M, Wessiepe D, Holland C, Alekar S, Mergen N, Einsele H, Hoelzer D, Bargou RC. Phase II trial of the anti-CD19 bispecific T cell-engager blinatumomab shows hematologic and molecular remissions in patients with relapsed or refractory B-precursor acute lymphoblastic leukemia. J Clin Oncol. 2014 Dec 20;32(36):4134-40
- ↑ Maude S, Teachey D, Porter D, Grupp S. CD19-targeted chimeric antigen receptor T-cell therapy for acute lymphoblastic leukemia Blood. 2015 Jun 25;125(26):4017-23
- ↑ Boissel N, Auclerc MF, Lheritier V, Perel Y, Thomas X, Leblanc T, Rousselot P, Cayuela JM, Gabert J, Fegueux N, Piguet C, Huguet-Rigal F, Berthou C, Boiron JM, Pautas C, Michel G, Fibre D, Leverger G, Dombret H, Baruchel A. Should adolescents with acute lymphoblastic leukemia be treated as old children or young adults? Comparison of the French FRALLE-93 and LA^-94 trials. J Clin Oncol. 2003 Mar 1;21(5):774-80
- ↑ 10.0 10.1 Ram R, Wolach O, Vidal L, Gafter-Gvili A, Shpilberg O, Raanani P. Adolescents and young adults with acute lymphoblastic leukemia have a better outcome when treated with pediatric-inspired regimens: systematic review and meta-analysis. Am J Hematol. 2012 May;87(5):472-8
- ↑ Sutton R, Shaw PJ, Venn NC, Law T, Dissanayake A, Kilo T, Haber M, Norris MD, Fraser C, Alvaro F, Revesz T, Trahair TN, Dalla-Pozza L, Marshall GM, O'Brien TA. Persistent MRD before and after allogeneic BMT predicts relapse in children with acute lymphoblastic leukaemia. : Br J Haematol. 2015 Feb;168(3):395-40
- ↑ Foa R, Vitale A, Vignetti M, Meloni G, Guarini A, De Propris MS, Elia L, Paoloni F, Fazi P, Cimino G, Nobile F, Ferrara F, Castagnola C, Sica S, Leoni P, '. Zuffa E, Fozza C, Luppi M, Candoni A, lacobucci I, Soverini S, Mandelli F, Martinelli G, Baccarani M; GIMEMA Acute Leukemia Working Party. Dasatinib as first-line treatment for adult patients with Philadelphia chromosome-positive acute lymphoblastic leukemia. Blood. 2011 Dec : 15;118(25):6521-8
- ↑ Ravandi F, O'Brien SM, Cortes JE, Thomas DM, Garris R, Faderl S, Burger JA, Rytting ME, Ferrajoli A, Wierda WG, Verstovsek S, Champlin R, Kebriaei P, McCue DA, Huang X, Jabbour E, Garcia-Manero G, Estrov Z, Kantarjian HM. Long-term follow-up of a phase 2 study of chemotherapy plus dasatinib for the initial treatment of patients with Philadelphia chromosome-positive acute lymphoblastic leukemia. Cancer. 2015 Aug 26
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר רון רם היחידה להשתלות מח עצם, מרכז רפואי תל אביב ואוניברסיטת תל אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק