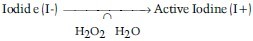נוגדן אנטי תרואיד פראוקסידאז - Anti thyroperoxidase antibodies
הופניתם מהדף Anti thyroperoxidase antibodies לדף הנוכחי.
| מדריך בדיקות מעבדה | |
| נוגדן אנטי תרואיד פראוקסידאז | |
|---|---|
| Anti Thyroperoxidase Antibodies | |
| שמות אחרים | TPO; Thyroid Microsomal Antibodies; Anti-TPO |
| מעבדה | אנדוקרינית בדם |
| תחום | הערכה של מחלות תירואיד |
| טווח ערכים תקין | פחות מ-35 IU/ml |
| יוצר הערך | פרופ' בן-עמי סלע |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – בלוטת התריס
מטרת הבדיקה
- לאבחון מחלת השימוטו
- לסייע באבחון של מפגעים אוטו-אימוניים של התירואיד כגון autoimmune thyroiditis
- להבדיל בין מפגעים אוטו-אימוניים של התירואיד לבין מחלת זפק (goiter) היפו-תירואידית שאינה על רקע אוטו-אימוני
- ככלי אבחוני בהחלטה האם לטפל בחולה עם היפו-תירואידיזם תת-קליני
- לאבחון מחלת Grave's
כמו כן תתבקש בדיקת TPO כאשר הרופא שוקל התחלת טיפול תרופתי כגון ליתיום, amiodarone, אינטרפרון-α או IL-2, הכרוך בסיכון להופעת תת-פעילות של הבלוטה בנוכחות נוגדנים ל-TPO. כאשר אישה נמצאת בהיריון עם מחלת תירואיד ידועה כהשימוטו או Grave's, מתבקשת בדיקת נוגדנים לבלוטת התריס בראשית ההיריון, ופעם נוספת לקראת סוף ההיריון. מטרת בדיקות אלה להעריך האם העובר הוא בסיכון להפרעה בפעילות התירואיד, שכן נוגדנים אלה עלולים לחצות את השליה ולגרום לתת-תריסיות או ליתר-תריסיות בוולד.
רקע פיזיולוגי
מחלה אוטואימונית של התירואיד, כולל מחלות השימוטו ו-Grave's, מאופיינות על ידי הסננה של לימפוציטים מסוג B לתוך הבלוטה, שהם המקור העיקרי לנוגדנים אנטי-תירואידאליים, כאשר שלושת הנוגדנים העיקריים הם אנטי-TPO, אנטי-תירוגלובולין ואנטי-קולטן של TSH. הנוגדנים כנגד TPO וכנגד תירוגלובולין הם אימונוגלובולינים רב-שבטיים (polyclonal) מסוג IgG, והם יכולים לקשור ולקבע משלים (complement) והם בעלי פעילות ציטוטוקסית, תפקידם במחלת השימוטו אינו ברור באופן מוחלט אם כי נראה שהמחלה נגרמת בתגובה לפגיעה שהם מחוללים לבלוטה. קיימת השערה על קרבה בין מחלת השימוטו ומחלת Grave's: בהשימוטו הזפק נגרם כתוצאה מהסננה של לימפוציטים לבלוטה, וגרימת הרס של התאים הפוליקולאריים . ב-Grave's הזפק יכול להיגרם מגירוי קולטנים של TSH.
האינטראקציה המורכבת בין גורמים גנטיים וסביבתיים קובעת את התפתחות המפגע האוטו-אימוני. גנים שזוהו בהקשר זה הם HLA-DR, וכן גנים שהם non-MHC כגון CTLA-4, CD40, PTPN22, וכן הגנים המקודדים לתירוגלובולין ולקולטן של TSH . הגורמים הסביבתיים כוללים רמת יוד נמוכה, הדבקות בפתוגנים, עישון, תרופות מסוימות ואף עקה נפשית (stress), זאת על פי Tomer ו-Huber ב-J Autoimmun משנת 2009. יש דיווחים אחדים שאכן stress משפיע על מערכת החיסון באופן שעלול להחמיר את התגובה האוטו-אימונית הגורמת למפגעי תירואיד.
מבדקי נוגדני התירואיד כוללים
- נוגדני אנטי thyroid peroxidase antibody או TPO;
- נוגדני אנטי thyroglobulin;
- נוגדנים כנגד הקולטן ל-TSH או TSHRAb (המתחלקים לנוגדנים המגרים אימונוגלובולין או TSI ולנוגדנים הידועים כ-thyroid binding inhibitory immunoglobulin או TBII).
TPO היא הבדיקה השכיחה ביותר באבחון מחלה אוטו-אימונית של התירואיד, והיא מתקבלת חיובית במחלות השימוטו ו-Grave's. בדיקת TSI נועדה לבחון רמת נוגדנים הנקשרים לקולטן של TSH ומעודדים את יצירת הורמוני הבלוטה באופן הגורם להיפר-תירואידיזם. בדיקת רמת TBII מנסה לבחון קישור אימונוגלובולינים אלה לקולטן של TSH באופן החוסם את יצירת הורמוני הבלוטה באופן הגורם להיפו-תירואידיזם. בדיקת TBII אינה מתבצעת באופן רוטיני, אך בדיקת TSI מסייעת לעתים קרובות באבחון מחלת Grave's.
האנזים thyroid peroxidase
TPO הוא אנזים ממברנלי גליקופרוטאיני בעל משקל מולקולארי של 105,000 דלטון, המעורב בסינתזה של הורמוני התירואיד, על ידי קטליזה של חמצון יודיד על שיירי תירוזין של החלבון תירוגלובולין והבאתו למצב אנרגטי שיאפשר את תהליך הסינתזה של T3 ו-T4 (על פי Taurog ב-thyroid משנת 1998). האנזים TPO קשור לממברנת תאים תירוציטים בלבד, ומוגדר כ-hemoglycoprotein, והוא אחד האנטיגנים החשובים בבלוטת התריס. מפגעים של בלוטה זו נגרמים לעתים קרובות על ידי מנגנונים אוטו-אימוניים. נוגדנים ל-TPO משפעלים את המשלים (complement) ונחשבים למעורבים באופן משמעותי באי-תפקוד בלוטת התריס ובפתוגנזה של תת-פעילות של בלוטה זו (Gharib וחב' ב-Thyroid משנת 2005).
האנזים TPO הוא אנזים מפתח בסינתזה של הורמוני בלוטה זו, על ידי מעורבותו בריאקציות אורגניפיקציה וצימוד. TPO הוא אנטיגן עיקרי המגיב לנוגדנים הידועים כ-thyroid-microsomal autoantibodies. חשיבות גילוי נוגדנים כנגד TPO אינה רק בזיהוי מפגע אוטו-אימוני של בלוטה זו, אלא גם בהערכה של המהלך הקליני של המחלה (Kotani ו-Ohtaki ב-J Clin Endocrinol Metab משנת 1991). TPO באדם נמצא שהוא מסוגל להיקשר לנוגדנים מסוג IgG ו-IgM המופיעים בדמם של חולים במחלה אוטו-אימונית של התירואיד. הקישור של IgG למיקרוזומים מעוכב על ידי TPO )על פי Kotani ב-J Biochem משנת 1992).
לאחר שיוד נכנס לבלוטת התירואיד, הוא נלכד ומועבר לאזור האֶפּיקלי של התאים הפוליקולאריים בבלוטה. החמצון של יודיד ליוד מקוטלז על ידי האנזים TPO. ריאקציה זו דורשת H2O2 ו- NADPH כאשר NADPH מגיע ממסלול Hexose Mono Phosphate. הצימוד של אטום יוד לחלבון תירוגלובולין מקוטלז גם כן על ידי TPO )על פי Saravanan ו- Dayanב-Endocrinol Metabol Clin North America משנת 2001).
אתרי הקישור של נוגדנים anti-TPO על פני אנזים זה, שונים לחלוטין ב- Hashimoto's thyroiditis ובמחלת Grave's. כמו כן, יש גם הבדל בתגובה שלanti-TPO לאנזים בשתי מחלות אלו (Bermann ב- J Clin Endocrinol Metab משנת 1993).
המשמעות של תוצאה חיובית במבחן TPO
ברוב האנשים עם thyroiditis כרונית מתקבלת תוצאה חיובית במבחן TPO. מבחן זה מתקבל חיובי באחוז קטן יותר של מטופלים עם מפגעים אחרים של בלוטת התריס. מפגעים אוטו-אימוניים אחרים שעשויים לתת תוצאה חיובית במבחן TPO כוללים את תסמונת Sjogren, לופוס, rheumatoid arthritis ו-pernicious anemia וכן במחלות אוטו-אימוניות של קולאגן במערכת הווסקולארית. בערך ב-3% מהנבדקים בהם מתקבלת תוצאה חיובית של מבחן TPO אין כל עדות למחלה. בנשים תוצאת TPO חיובית מתקבלת באחוז גבוה יותר מאשר בגברים. תוצאה חיובית של מבחן זה נוטה לעלות עם הגיל.
הנוגדן כנגד האנזים התירואידי peroxidase נחשב סמן ל-Hashimoto hypothyroidism. סמן זה, TPO, הוא הגורם המכריע להיפותירואידיזם במחלת Hashimoto, ולמעשה אם אין מוצאים נוגדנים ל-TPO, הסיכוי שמדובר ב-hypothyroidism קטן ביותר, אלא אם כן המטופל עבר לאחרונה ניתוח או הקרנות של הבלוטה. לכן, יש המבצעים בדיקת נוגדנים ל-TPO כדי לקבוע מי מאלה עם רמה נורמאלית-גבוהה של TSH או עם רמה מוגברת קלות של TSH, אמור לקבל טיפול תרופתי. אם בדיקת TPO מתקבלת חיובית ברוב המקרים יטופל החולה טיפול תרופתי. לעתים, אם המטופל מראה תסמינים אחדים של היפותירואידיזם, יש לו זפק ורמה חיובית של נוגדני TPO, גם אם רמת ה-TSH שלו תקינה, הוא יטופל במינון נמוך של תכשירים תירואידיים. לעומת זאת, אם בדיקת נוגדני TPO מתקבלת שלילית, וטיפול תרופתי אינו רצוי ברוב המכריע של המקרים.
אך יש מספר יוצאים מן הכלל: אמנם 95% מהסובלים ממחלת השימוטו הם בעלי נוגדנים עצמיים ל-TPO, אך 5% מהלוקים במחלה זו אינם נושאים בדמם נוגדנים אלה. אלה עם השימוטו אך שליליים לנוגדני אנטי-TPO, יאופיינו לרוב על ידי היפו-תירואידיזם במבחן על-שמע, כולל בלוטה מוגדלת והיפר-וסקולארית, ובמידה מסוימת נודולארית. מטופל כזה ראוי לטיפול תרופתי המקובל במחלת השימוטו.
קביעת רמות anti-TPO היא המבחן השכיח ביותר והרגיש ביותר לאבחון מחלה אוטו-אימונית של התירואיד כגון Hashimoto thyroiditis, מחלת Grave's ו-idiopathic myxedema, וריכוזים ניתנים למדידה של נוגדני anti-TPO נמצאים ברוב המטופלים עם המחלות הללו. את רמות anti-TPO הגבוהות ביותר מוצאים בהשימוטו תירואידיטיס. במחלה זו מוצאים נוגדני אנטי-TPO ב-90-95% מהמטופלים, מה שמאשש מקור אוטו-אימוני של המחלה; במחלת Grave's מוצאים נוגדנים אלה בתדירות של 55-80% מבין הלוקים במחלה; כן מוצאים נוגדנים אלה ב-30-40% מחולי סוכרת type 1, ב-14% מנשים בהיריון, ובאחוזים נמוכים יותר באלה עם sporadic multinodular goiter, באלה עם isolated thyroid nodule, ובאלה עם סרטן הבלוטה.
במטופלים עם היפותירואידיזם תת-קלינית, נוכחות של anti-TPO כרוך בסיכון מוגבר לפתח היפותירואידיזם גלוי (ב-4.3% מהמקרים מדי שנה, בהשוואה להתפתחות היפו-תירואידיזם גלוי ב-2.1% מדי שנה באלה ללא נוגדנים כנגד TPO). יתרה מכך, נוכחות של נוגדני anti-TPO מגבירה את הסיכון של נבדקים אלה לפתח מחלה אוטו-אימונית אחרת כמו סוכרת type 1 או אי-ספיקה של בלוטת האדרנל. התדירות של מציאת נוגדני anti-TPO במחלת תירואיד שלא על רקע אוטו-אימוני היא בערך 10-12% הדומה לאחוז הנבדקים בריאים עם תפקוד תקין של הבלוטה, בהם מוצאים נוגדנים אלה (Feldt-Rasmussen ב-Clin Chem משנת 1996).
רמות מוגברות באופן מתון של נוגדני anti-TPO ניתן למצוא בנבדקים במחלות אוטו-אימוניות שאינן קשורות לתירואיד כמו אנמיה ממאירה, סוכרת type 1, ובמפגעים אחרים המעוררים לפעולה את מערכת החיסון. באחדים מהמטופלים שנחשפו לאנטיגנים של בעלי חיים, אם בסביבת המגורים או במהלך פרוצדורות הדמיה, ניתן למצוא בדם נוגדני anti-TPO, ונוגדנים אלה עלולים להגיב עם מרכיבים בערכת הבדיקה, באופן שרמת הנוגדנים כנגד TPO המתקבלת אינה אמינה.
רוב הנוגדנים העצמיים מכוונים כנגד מבנים תלת-ממדיים (conformational epitopes) של האזורים הקרבוקסי-טרמינאלים האימונוגניים של TPO. עם זאת, יש גם נוגדנים עצמיים המגיבים עם מבניים קוויים (linear epitopes) של ה-TPO (על פי Utiger ב- Werner & Ingbar's The thyroid : a fundamental and clinical text (9th ed). משנת 2005). נוגדנים כנגד TPO הם הנוגדנים העצמיים השכיחים ביותר בין נוגדני האנטי-תירואיד האחרים, שמוצאים ב-90% ממקרי Hashimoto's thyroiditis, ב-75% ממקרי מחלת Grave's, וב-10-20% ממקרי זפק נודולארי או קרצינומה של הבלוטה. כמו כן, 10-15% מבין האנשים הבריאים יכולים להכיל נוגדנים כנגד TPO (על פי Saravanan ו-Dayan ב- Endocrinol Metabol Clin North America משנת 2001, ו-Boyd ו-Baker באותו כתב עת משנת 1996, ו- Chardès וחב' ב-Immunogenet משנת 2000).
נוגדנים עצמיים ברמה גבוהה ניתן למצוא בנסיוב בפאזה הפעילה של chronic autoimmune thyroiditis, לכן ניתן להשתמש ברמות של נוגדני אנטי TPO להערכה של פעילות ושלב המחלה (McLachlan ו- Rapoportב-Int Rev Immunol משנת 2000). רוב נוגדני anti-TPO מיוצרים על ידי הלימפוציטים המסתננים לבלוטה, עם תרומה מזערית של בלוטות הלימפה ושל מח העצם (Trbojević ו- Djuricaב- Srpski arhiv za celokupno lekarstvo.משנת 2005). נוגדנים אלה גורמים נזקים על ידי שפעול המשלים ו-ADCC.
כ-80% מהלוקים במחלת Grave's מכילים בדמם רמה גבוהה של נוגדנים כנגד TPO. בערך 4% מהמקרים של subclinical hypothyroid המכילים נוגדנים ל-TPO , מפתחים תסמינים של תת-תריסיות. נוגדנים ל-TPO גורמים ל-complement fixation, ומוצאים קומפלקסים של משלים וממברנות במטופלים עם מחלת תירואיד אוטו-אימונית. (Jameson ו-Weetman בפרק-Disorders of thyroid gland ב-Harrison's-Principle of internal medicine,16 th ed. משנת 2004).
SLE היא מחלה אוטו-אימונית בה מופרשים נוגדנים מסוג IgG כנגד TPO, אך נוגדנים אלה אינם מעכבים את פעילות TPO בניגוד לנוגדני IgG המופרשים בדמם של מטופלים עם מפגעי תירואיד (Kohno וחב' ב-Clin Exp Immunol משנת 1989).
פתוגנזה
יצירת נוגדנים במחלת Grave's נובעת על ידי שפעול של תאי T מסוג +CD4, ולאחריו גיוס של תאי B החודרים לתוך הבלוטה. תאי B אלה יוצרים נוגדנים הספציפיים לאנטיגנים של התירואיד. לעומת זאת, ב-Hashimoto's thyroiditis, שפעול של תאי T מסוג +CD4 מביא לייצור של interferon-γ, מה שגורם לתאי התירואיד להציג את אנטיגני MHC class II. פעולות אלה מרחיבות את הרפרטואר של תאי-T המגיבים כנגד אנטיגנים עצמיים ומאריך את משך התגובה הדלקתית (Stassi ו-De Maria ב- Nat Rev Immunol משנת 2002). למרות שנוגדנים עצמיים למרכיבי תירואיד משמשים לזהות נוכחות של autoimmune thyroiditis, הם אינם נחשבים באופן כללי כתורמים להרס הבלוטה (Gregory וחב' ב- Williams Textbook of Endocrinology. Hypothyroidism and Thyroiditis. 12th ed. משנת 2011.
רמות מוגברות של נוגדנים ל-TPO בנשים הרות עם פעילות תירואיד תקינה, מגבירות את הסיכון להפלה ספונטנית ל-preeclampsia, ללידה טרם-עת או כישלון של הפריות מחוץ לרחם. טיפול של נשים אלה ב-levothyroxine נראה כמפחית את סיכוני ההפלה, אך אין עדיין המלצה לטיפול כזה בנשים הרות עם פעילות תקינה של הבלוטה (Chen ו-Hu ב-Clin Endocrinol (Oxf) משנת 2011, ו- Thangaratinam וחב' ב-BMJ משנת 2011). רמה מוגברת בנסיוב של נוגדנים ל-TPO, ורמת מוגברת של נוגדנים כנגד תירוגלובולין, חיונית לאבחון של המפגע השנוי במחלוקת של Hashimoto encephalopathy.
בדיקות המעבדה לאבחון מחלת השימוטו
ברוב המקרים מחלת השימוטו מאובחנת במעבדה על ידי בדיקה משולבת של רמת 2 נוגדנים: anti TPO ו-anti-thyroglobulin. באחוז קטן מאוד של נבדקים בהם מבדקי הנוגדנים מתקבלים שליליים, למרות שיש אצלם חשד גדול להשימוטו, על פי תחושות של פעילות-יתר של הבלוטה או תת-פעילות שלה, או במקרים של הנמכת ועיבוי קולם, או התעבות באזור הצוואר. במקרים אלה תתבצע בדיקת FNA , תוך ניסיון לאתר תאי Hürthle, שהם תאים מגורגרים גדולים שיכולים להופיע במחלת השימוטו. יש גם הנוקטים במבדק על-שמע לנסות ולאבחן במקרים אלה מחלת השימוטו.
הוראות לביצוע הבדיקה
אין צורך בצום מוקדם. הדם נלקח במבחנה כימית (פקק אדום) או במבחנת ג'ל. לאחר הפרדת הדם בסרכוז יש לקרר מיד את הנסיוב המופרד ולשלחו למעבדה בקירור. יציבות הדגימה בקירור 7 ימים ובהקפאה עד 30 יום. יש לפסול לביצוע נסיוב מאוד המוליטי, אך ניתן להשתמש בדגימה המוליטית באופן קל. ליפמיה אפילו ניכרת אינה משפיעה על הבדיקה. יש לפסול דגימות פלזמה. הבדיקה מתבצעת בשיטת chemiluminometric immunoassay.
ראו גם


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק