דלקות מפרקיות - טיפול תרופתי - 2018 - Arthritis - medications
הופניתם מהדף Arthritis - medications לדף הנוכחי.
| דלקות מפרקיות - טיפול תרופתי - 2018 | ||
|---|---|---|
| ' | ||

| ||
| שמות נוספים | תרופות לטיפול בדלקות מפרקיות | |
| יוצר הערך | פרופסור הווארד עמיטל | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – דלקת מפרקים
דלקת מפרקית שיגרונתית (Rheumatoid arthritis), היא מחלה דלקתית באופייה הפוגעת במרקם התקין של מפרקי הגוף. המחלה שכיחה לגמרי ומופיעה בכאחוז אחד מכלל האוכלוסייה הבוגרת בעולם ובישראל. המחלה מתאפיינת, בין השאר, בתבנית ייחודית של כאבים אשר המכונים כאבים דלקתיים. סוג זה של כאבים מוכר פחות לאוכלוסייה הכללית ולעיתים אף רופאים מחטיאים את זיהוים. כאבים אלה גוברים בשעת מנוחה, מעירים את החולה משנתו ומוקלים בפעילות גופנית. אי הכרתם תורמת לאבחון מאוחר של קבוצה זו של מחלות.
בסקירה זו ארחיב אודות שפע הטיפולים הקיימים לחולים הלוקים במחלות אלה. בסקירה זו יתוארו התכשירים המוצעים לכאבים.
תכשירים שנועדו להקל על תסמיני הכאב בלבד
קבוצה זו מונה תכשירים רבים המוכרים מהשימוש היומיומי, דוגמת Acamol, אופטלגין ותכשירים המשתייכים לקבוצת ה-NSAIDS (Non-Steroidal Anti-Inflammatory Drugs).
היפוקרטס, הרופא היווני הקדום שחי כארבע מאות שנים לפני הספירה, תיאר את מעלתיו של מיצוי שהופק מקליפת שיח הערבה. ברבות השנים השתמשו בו רופאים שונים לשם הורדת חום והפחתת כאבים. הכימאי הגרמני Johann Andreas Buchner הצליח לבודד ב-1827 את הגליקורזיד המכונה salicin והכימאי הצרפתי Henri Leroux מיצה כשנתיים לאחר מכן 30 גרם של salicin מ-1.5 קילוגרם של קליפת הערבה. ההיסטוריה השתנתה ב-1897 עת הצליח הכימאי Felix Hoffman יחד עם חברת Bayer לסנטז את החומצה האצטילסליצילית והביאו לעולם את הטיפול באספירין.
יעילותם של תכשירים אלה רבה ומביאה להפוגה משמעותית בכאב. עם זאת, לא אחת נתקלים בתופעות לוואי דוגמת אי נוחות בדרכי העיכול, צרבות ובמקרים קשים אף דמם מדרכי העיכול, אשר נגרמים בגין השפעתם של תכשירים אלה על רירית התריסריון. שימוש יומיומי רצוף בתכשירים מקבוצה זו לאורך תקופה של למעלה משנתיים עלול להביא לעלייה קלה בשיעורי התחלואה של מחלות לב וכלי דם, ועל כן יש להשתמש בתכשירים אלה באופן מושכל. אין להסס לרשום אתם לחולים הסובלים מכאב, אף למשך מספר שבועות, אם יש בכך צורך, אולם יש תמיד לזכור שאין הם מהווים מענה לתהליך הדלקתי עצמו ולפגיעה במרקם של המפרק הדלקתי אלא רק לכאב שנובע מתהליך זה. תכשירים אלה אינם מומלצים לחולים הלוקים באי ספיקת כליות, אי ספיקת לב קשה או לחולים הלוקים ביתר לחץ דם שאינו תחת שליטה.
ה- Etoricoxib וה-Celecoxib מוכרים לנו כמשתייכים לתת קבוצה המכונה קוקסיבים, אשר ייחודם בכך שמעכבים את אנזים הציקלואוקסיגנאזה מסוג 2 (COX-2 inhibitors) ובכך מונעים פגיעה ברירית מערכת העיכול ואינם מביאים לדימום מדרכי העיכול העליונות. תכשירים אלה מהווים נדבך חשוב בארסנל כנגד הכאב הדלקתי. במשך השנים למדנו שהעלייה בתחלואה הקרדיווסקולארית מאפיינת את כל סוגי ה-NSAIDS ואינה נחלתם של חוסמי ה-COX-2 בלבד. עם זאת מגמה זו נצפית רק לאחר שימוש מתמיד ולאורך זמן רב, שנמדד כחודשים רבים. דפוסי הצריכה שלנו ברבות השנים השתנו כאופן ניכר ואנו משתמשים בתכשירים אלה למיגור כאב הנובע בדרך כלל מאי שליטה מיטבית על תסמיני המחלה. שינוי בתמהיל של התרופות האחרות בנגד דלקה מפרקת שיגרונתית יביא בדרך כלל לשיפור במצבו של החולה וימנע את הצורך בטיפול ממושך ב-NSAIDS.
תכשירים קורטיקוסטרואידיים
קבוצה שנייה של תכשירים בהם משתמשים היא קבוצת התכשירים הקורטיקוסטרואידיים. אל קבוצה זו משתייכים הקורטיזון, הידרוקורטיזון, דקסמטזון, פרדניזון ותרופות נוספות. ב-1950 זכו המדענים Tadeusz Reichstein, Edward Calvin Kendall ו-Philip Showalter Hench בפרס נובל לפיזיולוגיה ורפואה בשל גילוי מנגנוני הפעולה של ההורמונים הסטרואידיאלים ובידודו של הקורטיזון. מאז פשט השימוש בהם באופן ניכר במחלות רבות ובפרט במחלות אוטואימוניות. עם השנים למדו הרופאים לחלוש על המינונים המתאימים לטיפול ולהפחית עז־ כמה שניתן בתופעות הלוואי הנגרמות מעצם השימוש.
היתרון הבולט של התכשירים המשתייכים לקבוצה הוא ביכולתם להביא להפחתה מהירה בעוצמת הדלקת ובתסמיניה. אך הסטרואידים אינם מונעים את השחתתם של המפרקים המעורבים בתהליך הדלקתי ואין בכוחם לבלום את הנזקים כפי שנצפים בצילומי רנטגן עוקבים (תהלך המכונה בשפה המקצועית התקדמות רדיוגראפית).
שימוש ממושך בתכשירים אלה עלול לגרום לתופעות לוואי מרובות כעלייה ביתר לחץ הדם, עלייה בריכוז הגלוקוזה, פיזור שומנים למרכז הגוף (פנים, בטן), אוסטאופורוזיס, בעיות עיניות כקטרקט וגלאוקומה ובעיות רבות אחרות. לכן השימוש בתכשירים אלה במינונים גבוהים נועד רק בעת התלקחות חדה של מחלות אוטואימוניות ולשם דיכוי חיסוני שנועד לבלום סכנה לחיים או לאיבר חיוני. אם החולה נזקק לשימוש מתמשך בתכשיר מקבוצה זו, יש להפחית את המינון למינימום האפשרי. דבר זה הוא בדרך כלל בהחלט בר השגה בדלקות מפרקים באמצעות שילובם של הסטרואידים עם תרופות אחרות (steroid sparing medications).
DMARDS
קבוצה משמעותית לחולים הלוקים בדלקת מפרקית שיגרונתית היא ה-DMARDS (Disease Modifying Anti-Rheumatic Drugs).
תרופות אלה מצטיינות ביכולתן לשנות את המהלך הטבעי של המחלה, קרי הן יכולות לגרום לשיכוך הדלקת ואף למניעת הנזק המפרקי המתפתח בעטייה. השפעתן של תרופות אלה אינה מיידית ונדרש זמן הנמדד בשבועות או חודשים עד אשר יושג השיפור המיוחל ועל המטופלים והרופאים להתאזר בסבלנות בטרם יכריזו על כישלונן של תרופות אלה. אחד התכשירים המשמעותיים המהווה אבן פינה בטיפול במחלות ראומטולוגיות הוא ה-Methotrexate.
התכשירים נוגדי החומצה הפולית אליהם משויך ה-Methotrexate פותחו ב-1947 ושמם הראשון היה אמינופטרינים. הכוונה המקורית הייתה לייצר תכשירים אשר יוכלו לשמש כטיפול לחולים הלוקים במחלות ממאירות והדבר נבע מתצפית שהעלתה שחולי לוקמיה חשו טוב יותר כאשר קיבלו תזונה דלת חומצה פולית. ב-1950 פותח התכשיר Ameihopterin המוכר כ-Methotrexate, הייעוד הראשוני לתכשיר זה היה טיפול בלוקמיה ובהמשך גם במחלות ממאירות סולידיות שונות. המינונים היו גבוהים לאין שיעור מאלה הניתנים בעולם הראומטולוגי. אל עולם זה הגיע ה-Methotrexate דרך הדרמטולוגיה: רופאי עור נוהגים לטפל בחולי פסוריאזיס באמצעות Methotrexate במינונים נמוכים מאוד למעלה מיובל שנים עם הצלחה מרובה בהרגעת וייצוב המחלה. באמצעות ה-Methotrexate חולים רבים נהנים מהפוגה ארוכת טווח והוא בהחלט מהווה חלק מהארסנל הטיפולי של רופאי העור.
לראומטולוגיה הוכנס ה-Methotrexate על ידי הראומטולוג האמריקאי מייק ודנבלאט, אשר פרסם בשנות ה-80 של המאה ה-20 את ההשפעה המטיבה של Methotrexate בחולים הלוקים בדלקת מפרקית שיגרונתית: ה-Methotrexate בולם את השחתת המפרקים על ידי הדלקת. לא אחת אנו נתקלים באמירות לא מדויקות כלפי תכשיר זה, שלכאורה שייך לקבוצת התכשירים הכימותרפיים בשל מקורותיו, אולם אין הדבר מדויק כלל, ונכון יהיה להגדירו Anti-metabolite ובמינונים בהם הראומטולונים מטפלים יהיה נכון יותר לכנותו כאימונומודלוטור. ה-Methotrexate נלקח אחת לשבוע בלבד במינון שנע בין 7.5 מיליגרם ל-25 מיליגרם, בניגוד למינונים של גרמים הניתנים בחולים הלוקים במחלות ממאירות. עם זאת ל-Methotrexate תופעות לוואי שיכולות להיות משמעותיות אך בהחלט ברות שליטה ובקרה כגון פגיעה בכבד, בחילות, הקאות, נשירת שיער, או דיכוי לשד העצם, על כן חובה לבצע בדיקות תפקודי כבד וספירת דם מדי חודשיים. חל איסור להרות בעת השימוש בתכשיר ויש לחכות לפחות 3 חודשים מהשימוש האחרון בו ועד הכניסה להיריון, Methotrexate אינו פוגע בפוריות האישה או הגבר אלא יש "להתנקות" ממנו פן ייגרם נזק לעובר.
ניתן להפחית את הסיכונים הנגרמים כתוצאה משימוש ב-Methotrexate על ידי מתן מקביל של הוויטמין חומצה פולית, וכך יש לנקוט בחולים הלוקים במחלות ראומטולוגיות. מקובל לשלב טיפול ב-Methotrexate יחד עם תרופות אחרות ובעיקר עם התרופות הביולוגיות, כדי להעצים את השפעתן.
תרופה נוספת המשתייכת לקבוצה זו היא ההדירוקסיכלורוקווין (פלקווניל) שהייתה מוכרת לעולם הרפואי כתרופה נוגדת מלריה. התיאור הראשון של טיפול בעזרת הכינין כתרופה למלריה היא משנת 1633 כאשר הובאה לאירופה על ידי מסיונרים ישועיים מפרו שלמדו כיצד לטפל במלריה. האינדיאנים נהגו להשתמש בחומר האבקתי בצבע הקינמון שהופק מקליפת העץ שנקרא Arbol de calenturas (עץ "גלי החום" או בשפת הילידים "קינה"). מהר מאוד נמצא שהיא מקלה על החום ועל הצמרמורות הנובעות מהמלריה. הבריטים וההולנדים תושבי המושבות באזורים מוכי מחלת המלריה, נהגו לערבב את מי הטוניק שהכילו אבקה זו עם המשקה האלכוהולי ג'ין וצרכו אותו באופן שוטף כתרופה מונעת שטעמה היה נסבל ומכאן נולד המשקה ג'ין עם טוניק.
לעולם הראומטולוגי הגיע התכשיר ררך מלחמות. במהלך מלחמת העולם השנייה כאשר צבאות רבים שהוו במזרח הרחוק ובאפריקה וטופלו באופן מונע בכינין נצפה שיפור כקרב אלו שלקו בדלקות מפרקיות. מחקרים שנעשו בשנות החמישים ביססו את המקום של הטיפול בדלקות מפרקיות כזאבת אדמנתית מערכתית (systemic lupus erythematosus, SLE) ובדלקת מפרקית שיגרונתית. מאז התכשיר מצוי בארסנל הטיפולים. תרופה נוספת הניתנת לעיתים שכיחות כעולם המערבי היא הסלזופירין (Sulfasalazine). תכשיר זה פותח בשנות החמישים והגיע לראומטולוגיה מעולם מחלות המעי הדלקתיות. הוא על פי רוב ניתן בקומבינציה יחד עם תרופות פומיות אחרות, אולם בחולים הלוקים במחלה קלה ניתן לתת טיפול זה בלבד. התכשיר ניתן גם לחולים הלוקים בדלקת מפרקית פסוריאטית.
תרופות ביולוגיות
מאז שפותחו התכשירים המכונים תכשירים ביולוגיים דומה שהם שינו את עולמם של החולים הלוקים בדלקות מפרקיות. תכשירים אלה מבוססים על חלבונים אנושיים, לרוב נוגדנים חד שבטיים (monoclonal), אשר הביאו למהפכה של ממש בטיפול בחולים הלוקים בדלקת מפרקים שיגרונתית בינונית עד קשה. הרוב המכריע של תכשירים אלה ניתן להשגה בישראל וחולים רבים נהנים מבריאות טובה ויציבה הודות לתכשירים אלה. מלכתחילה לא יועדו התכשירים הביולוגיים כלל לטיפול בחולים הלוקים בדלקוח מפרקיות. הניסיונות הראשוניים נועדו להגן על חולים הלוקים בספטיסמיה כי ריכוז הציטו׳קין Tumor necrosis factor α) TNF-α) מרקיע שחקים במצבים אלה. מחקר פרוספקטיבי אקראי וכפול סמיות שנערך בקרב חולים הלוקים בספסיס הופסק טרם זמנו לאור ריבוי מקרי תמותה בקרב החולים המטופלים בתכשיר נוגד ה-TNF-α אטנרספט. ניסיון כושל נוסף היה בקרב חולים הלוקים באי ספיקת לב. אשר גם בו יש ריכוז גבוה של TNF-α. בטרם נשלחו תכשירים אלה אל תהום הנשייה המדעי, הוכיח ראומטולוג בריטי יליד הודו בשם Sir Ravinder Nath Maini כי תכשירים אלה משנים את מהלך המחלה של עכברים הלוקים בתסמונת מושתת של דלקת מפרקית. מכאן הדהירה לשימוש קליני כמצבים ראומטיים הייתה מהירה וקצרה מאוד והתכשירים הוכחו כהצלחה מרשימה במחלות אלה.
בתכשירים השונים הוכחה יעילות רבה יותר עת שולב הטיפול יחד עם Methotrexate. בשורות הבאות אפרט על התכשירים החדשים והישנים המוכרים לקהל הרחב.
הומירה - Adalimumab ,Humira
הומירה היא תרופה ביולוגית המיוצרת ממרכיבים ביולוגיים ולא כימיים. תכשיר זה משתייך לקבוצת התרופות הנקראות anti-TNF והיא הראשונה שהיא ממקור אנושי מלא. התרופה היא נוגדן המיוצר בהנדסה גנטית (רקומביננטי), הפועל באופן ממוקד כנגד מרכיב מרכזי בתהליך הדלקתי, הציטוקין TNF-α. ה-TNF-α הוא חלבון (ציטוקין) המופרש ממערכת החיסון ומעודד תהליכי דלקת. מחלות אוטואימוניות שונות כדלקת מפרקים שיגרונתית מאופיינות בהפרשת יתר של TNF. מנגנון הפעולה של תכשירים אלה גורם לקשירה של התרופה לחלבון ה-TNF ובכך מפחית את הדלקת. התכשיר זמין בכל קופות-החולים וקיים בתצורה של זריקה רגילה ומזרק אוטומטי. הזריקה נעשית אל מתחת לעור. בישראל ההתוויות הרשומות של הומירה כוללות את המחלות האוטו-אימוניות הבאות: דלקת מפרקים שגרונית (Rheumatoid Arthritis, RA), דלקת מפרקים פסוריאטית (Psoriatic Arthritis, PsA), דלקת חוליות מקשחת (Ankylosing Spondylitis, AS), דלקת מפרקים אידיופתית רב-מפרקית של גיל הילדות (Juvenile Idiopathic Arthritis - JIA), מחלת קרוהן (Crohn's Disease), דלקת כיבית של המעי הגס (Ulcerative colitis) ופסוריאזיס (Psoriasis). נעשה רישום תחת הכותרת של Nonradiographic spondyloarthropathy הכוללות את כל הדלקות הריאומטיות המערבות אח עמוד השדרה לאורכו עוד קודם להופעתן בצילומי רנטגן וכן לאובאיטיס ומחלת המעי הגס של חולים הלוקים בתסמונת בכצ'ט.
אנברל - Etanercept - Enbrel
אנברל היא תרופה ממשפחת נוגדי TNF - אלפא המשמשת לטיפול בדלקת מפרקים. אנברל הוא Fusion protein כלומד חלבון שמושתת על בסיס החלק הקבוע של אימונוגלובולין מסוג IgG והקולטנים ל-TNF-α. גודלו של התכשיר קטן יותר והרצף שלו אנושי ועל כן נוצרים כנגדו פחות נוגדנים מנטרלים מנוגדנים חד שבטיים. התכשיר משמש לטיפול בדלקת מפרקים שגרונית, פסוריאזיס ודלקת מפרקים פסוריאטית וכן כנגד nonradiographic spondyloarthropathy ו-ankylosing spondylitis.
האנברל הוא תכשיר ותיק המצוי בשוק למעלה מ-20 שנים ומיליונים של מטופלים משתמשים בתכשיר זה, מבוגרים וילדים כאחד. המינון השבוע הוא בן 50 מיליגרם למבוגר. האנברל ניתן בזריקה תת-עורית בין פעם לפעמיים בשבוע. בפרוטוקול לטיפול בדלקת מפרקים שיגרונתית בדומה לתכשירים האחרים כנגד TNF הוא ניחן בהעדפה כשילוב עם Methotrexate. קיימים שני סוגי מזרקים לאנברל, האחד רגיל והשני אוטומטי.
בעור שבעבר הייתה המלצה חד משמעית נגד היריון בשילוב עם תכשירים כנגד TNF הרי שהמלצה זו התמתנה, כפי הנראה אין נטילתו בעת היריון מסוכנת במיוחד.
רמיקד - Infliximab - Remicade
רמיקד היא תרופה המבוססת על נוגדן כימרי חד שבטי. הנוגדן מתקבל כתוצאה מאיחוי של חלקי נוגדן עכברי ונוגדן אנושי. הנוגדן נקשר באופן ספציפי לציטוקין TNF-α ומנטרל את פעולתו. רמיקייד מיועדת לטיפול בבוגרים הסובלים ממחלות אוטואימוניות מסוימות - מחלת קרוהן, קוליטיס כיבית, דלקת מפרקים. פסוריאזיס (ספחת) ו-Ankylosing spondylitis. התרופה משווקת כאבקה סטרילית. לאחר המסתה בתמיסת מלח פיזיולוגית היא ניתנת בעירוי אל תוך הווריד, לפי מינון מומלץ שנע בין 3–5 מיליגרם לקילוגרם. המינון הרשמי לחולים הלוקים בדלקת מפרקיתה שגרונתית הוא 3 מיליגרם לקילוגרם ואילו לאלה הלוקים בפסוריאזיס או בדלקת מסוג ספונדילוארתרופטיה 5 מיליגרם לקילוגרם. קופות החולים מאפשרות מרווח של התאמה אישית במינונים ובאינטרוולים שבין העירויים. על פי המלצת היצרן בדלקת מפרקים המטופל מקבל את העירוי השני והשלישי כשבוע ושישה שבועות בהתאמה מן העירוי הראשון. לאחר מכן עירוי כל 6–8 שבועות.
סימפוני - Golimumab ,Simponi
סימפוני היא תמיסה להזרקה תת-עורית המכילה את הנוגדן הפעיל גולימומב (golimumab). סימפוני זמינה כמזרק אוטומטי במינון בן 50 מיליגרם. הסימפוני אף הוא נוגדן המבוסס הנקשר TNF אלפא. הסימפוני יעילה על כן בהפחתת ומניעת הכאב הדלקתי ובבלימה של ההשחתה של המפרקים. סימפוני רשומה לטיפול במחלות הדלקתיות הבאות: דלקת מפרקים שיגרונית (Rheumatoid Arthritis) מתונה עד חמורה, כאשר סימפוני ניתנת בשילוב עם methotrexate. דלקת מפרקים ספחתית (Psoriatic Arthritis) פעילה, ניתן להשתמש בסימפוני לבד או בשילוב עם methotrexate. דלקת חוליות מקשחת (Ankylosing Spondylitis) פעילה. המינון של הסימפוני בזריקה תת-עורית הוא 50 מיליגרם, אחת לחודש.
סימזיה - Certolizumab pegol - Cimzia
הסימזיה היא מקטע של האזור קושר של הנוגדן (Fab) שנקשר אף הוא לציטוקין TNF אלפא. מקטע הנוגדן עבר תהליך של פגלציה המאריך את חיי המולקולה למספר שבועות. בכך מושגת מחד גיסא חיות ארוכה ביותר של התכשיר ומאידך גיסא אין הוא מייצר נוגדנים מנטרלים מפאת גודלו הקטן. יתרון נוסף לתכשיר זה הוא בכך שאינו חודר את השליה ובכך בטיחותו גבוהה יותר מנוגדי TNF אלפא אחרים הואיל ואין הוא מגיע ומשפיע על העובר המתפתח ברחם אמו.
מבטרה - Rituximab ,MabThera
התרופה מבטרה הגיעה לעולם הריאומטלוגי מהטיפל בלימפומות. דיאומטלוג בריטי בשם Edwards הבחין שחולים הלוקים בדלקת מפרקים אשר פיתחו לימפומה וטופלו במבטרה נהנו בהפוגה קלינית משמעותית בזכות תכשיר זה. מכאן הדרך הייתה קצרה למתן התכשיר לחולים הלוקים בדלקת מפרקים ללא לימפומה. מחקרים הראו שבניגוד למה שהיה מקובל לפני כעשרים שנים הרי שבהחלט יש תפקיד מפתח לתאי לימפוציטים מסוג B בהתפתחות מחלות אוטואימוניות בכלל ודלקת מפרקים שיגרונתית בפרט. מבטרה היא נוגדן אשר נקשר לחלבון CD20 המצוי על פני תאי B ועל ידי כך גורם לשרשרת תגובות המביאות להפחתה ניכרת במספרם. הפחתה סלקטיבית זו מורידה את עוצמת הדלקת במפרק ואת תסמיני המחלה, מונעת נזקים מבניים ארוכי טווח למפרקים ומשפרת את איכות חיי החולה. הטיפול במבטרה אושר בישראל לחולי דלקת מפרקים שגרתית אשר הגיבו בצורה בלתי מספקת לטיפול במעכב אנטי TNF אחד או יותר, או לחולים שלא יכולים לסבול תרופה מקבוצה זו. הטיפול במבטרה הוא פשוט ונוח. סדרה טיפולית מורכבת משני עירויים בלבד הניתנים בהפרש של שבועיים האחד מרעהו כל אחד במינון של 1 גרם. משך כל עירוי הוא מספר שעות. מועד קבלת טיפל נוסף ייקבע על ידי הריאומטלוג המטפל, בדרך כלל לאחר 6–9 חודשים מזוג העירויים הראשון, כאשר ישנה עדות להישנותם של תסמיני המחלה. מחקרים רבים הראו את יעילותה של מבטרה בטיפול בחולי דלקת מפרקים שיגרונתית. למנטרה פרופיל בטיחותי גבוה שהוכח בלמעלה ממיליון מטופלים במחלות שונות. תופעות לוואי יכולות להופיע בזמן קבלת העירוי כגון חום, צמרמורת או רעד, בשל הזלפתו של הנוגדן למחזור הדם. לפיכך, לפני מתן כל עירוי של מבטרה ניתנות תרופות שמטרתן לצמצם או למנוע תופעות לוואי אלה. שכיחותן ועוצמתן של תופעות אלו קטן מעירוי לעירוי. לא נמצא סיכון לפגיעה משמעותית בתפקודה של המערכת החיסונית, הופעת מקרי שחפת, עלייה בשיעור זיהומים חמורים או ממאירויות בקרב המטופלים במבטרה. תופעת לוואי נדירה שדווחה בחלים המקבלים טיפול זה יחד עם טיפולים מדכאי חיסון נוספים היא PML (Progressive multifocal leukocnccphalopathy). בשל החומרה של מחלה ניוונית זו של מערכת העצבים המרכזית הוחלט ברשויות הבריאות בעלם שטיפל זה יינתן כקו טיפול ביולוגי שני בלבד. מחלה ניוונית זו מתפתחת בשל התעוררות של זיהום מנגיף JC, נגיף אשר במצבים תקינים מדוכא באופן משמעותי מאוד על ידי מערכת החיסון. תיאורים של PML רווחים יותר בקרב חולים המקבלים טיפולים אלה בשל ממאירויות המטלוגיות בשל המשלב של טיפולים שונים המדכאים את מערכת החיסון. יש אינדיקציות אוטואימוניות נוספות לשימוש במבטרה דוגמת תרומבוציטופניה אוטואימונית, לעיתים כטיפול חמלה שאינו רשום במקרים עמידים של זאבת אדמנתית מערכתית ותסמונת הנוגדנים כנגד פוספוליפידים.
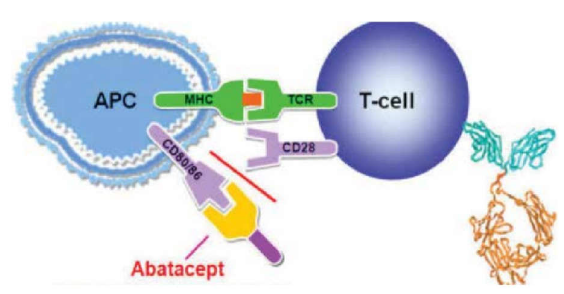
אורנציה, אבטספט - Abatacept
אורנציה היא תרופת מרשם המיועדת להפחתת סימנים ותסמינים של מחלת מפרקים בחולים הלוקים בדלקת מפרקים שגרונית (Rheumatoid Arthritis, RA) מתונה עד חמורה, כולל את אלה שתסמיני המחלה לא הוקלו לאחר שימוש בתרופות אחרות לדלקת מפרקים שגרתית. אורנציה עשויה למנוע נזק נוסף לעצמות ולמפרקים, ולשפר את היכולת לבצע פעולות יומיומיות. ה-FDA (Food and Drug Administration) האמריקאי אישר את הטיפול גם בדלקת מפרקית פסוריאטית וייתכן והתכשיר יוסף לסל השירותים בקרוב גם באינדיקציה זו.
התרופה אורנציה ניתנת או באמצעות עירוי אל תוך הווריד או באמצעות זריקות שבועיות תת-עוריות. העירוי המכיל את מלוא מנת התרופה נמשך 30 דקות בערך וניתן אחת לחודש. מנגנון הפעולה של התכשיר הוא בעיכוב התקשורת שבין תאי מערכת החיסון ושיבושה. תקשורת זו חיונית להתפתחות התגובה הדלקתית בדלקת מפרקים שיגרונתית. אף האורנציה ניתנת בשילוב עם מטוטרקסאט וגם בתרופה זו העיקרון נשמר, כלומר הקומבינציה טובה יותר מהטיפול בתכשיר הביולוגי בלבד (ראו תמונה).
אקטמרה - Tocilizumab ,Actemra
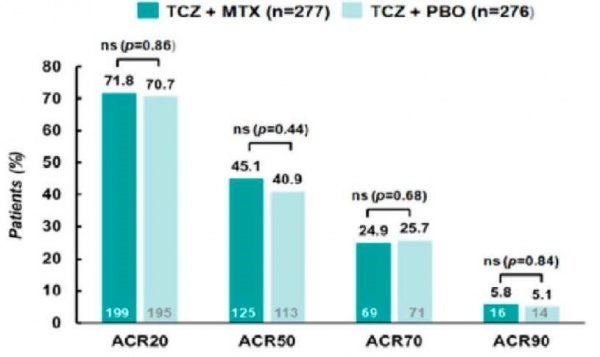
Actemra היא תרופה לטיפול בדלקת מפרקים שיגרונתית. אקטמרה היא נוגדן חד־שבטי, אשר מעכב את ההתקשרות של החלבון מעודד הדלקת IL-6. ל-IL-6 תפקיד מרכזי בתהליך הדלקת והוא מעורב בתהליכים רבים הגורמים לנזק המפרקי. בנוסף, IL-6 קשור למדדי דלקת גבוהים, לאנמיה ולאוסטאופורוזיס בחולי RA. על ידי חסימת הקישור של ה-IL-6 לקולטן שלו על פני התא אקטמרה מפחיתה את עוצמת הדלקת, מונעת נזקים מבניים ארוכי טווח למפרקים, משפרת את איכות חיי החולה ומביאה להפוגה מהמחלה. אקטמרה ניתנת כעירוי אל תוך הווריד מדי חודש במינון של 8 מיליגרם קילוגרם. משך העירוי כשעה אחת בלבד. כמו כן התכשיר יכול להינתן באמצעות זריקה שבועית מתחת לעור במינון של 162 מיליגרם. לאקטמרה פרופיל בטיחותי טוב, אשר אופיין ביסודיות על סמך מחקרים רבים באלפי חולים. אקטמרה רשומה לטיפול בישראל, בארצות הברית, באיחוד האירופי ובמדינות רבות נוספות ברחבי העולם לטיפול בדלקת מפרקים שגרתית. אושר השימוש בתכשיר זה גם ב-Giant cell arteritis. השימוש בתכשיר הביא להפחתה ניכרת בתלות בסטרואידים בטיפול בחולים אלה ומאפשר נסיגה מהירה במינונם והימנעות מתופעות הלוואי אשר נגרמות מהטיפול הסטרואידי. סקרנות מרובה עודדו תוצאות מחקר כפול הסמיות ACT-RAY, אשר בין השאר בחן את יעלותה של האקטמרה כשילוב עם Methotrexate מול חולים שטופלו באקטמרה בלבד. טיפול בן שנה לא הדגים שינוי משמעותי בין שתי קבוצות הטיפול, קרי אקטמרה עם Methotrexate ובלעדיו הייתה יעילה כאותה המידה (ראו תמונה מספר 2).
מדדים שונים הוערכו כמו פעילותה של המחלה באופן כוללני, הנזק המפרקי המצטבר, מידת השיפור באיכות החיים והשיפור שחל בתפקוד היומיומי. בכל המדדים, כאמור, לא נצפה כל הבדל בין הקבוצות. 30-10 אחוזים מהחולים לא נוטלים Methotrexate בשילוב עם תכשירים ביולוגיים מסיבות מוצדקות לא מוצדקות כאחד, החל מכאבי בטן בלתי נסבלים ועד לרצונן של מטופלות לתכנן היריון.
מחקרים נוספים אודות אקטמרה דוגמת מחקר FUNCTION הדגימו בכל זאת שחולים עם הבחנה חדשה של דלקת מפרקים שיגרונתית בכל זאת נהנים מהשילוב של האקטמרה יחד עם Methotrexate, המונע בין השאר הידרדרות בהשחתה של המפרקים וזאת באופן משמעותי טוב יותר מאשר טיפול באקטמרה בלבד. תוצאות אלה מעודדות באשר למיצובו של האקטמרה כטיפול שניתן לתת במונותרפיה. אולם, המידע אודות השילוב של תרופות ביילוגיות עם Methotrexate הוא רב שנים ומתוקף מאוד. טובות ככל שתהיינה התוצאות אודות טיפול באקטמרה בלבד, אין בהן כדי לגרום לציבור הרופאים להעדיף מתן עצמאי של אקטמרה על פני שילובו עם Methotrexate. כאשר אין מנוס ולא ניתן לשלח בהחלט יש עדיפות לשימוש בתכשיר זה בעוד שיעלותן של יתרת התכשירים הביולוגיים נפגעת באופן ניכר מאי שלובן עם Methotrexate. לפיכך המסקנה של הכותב היא, שיש לשאוף ככל הניתן לשלב תכשירים אלה יחדיו.
קבזרה - Sarilumab ,Kevzara
קבזרה היא תרופה שנקשרת לקולטן ל-IL-6 ובכך חוסמת אח האפשרות של הציטוקין הטבעי להתקשר לקולטן ולייצר את התהליך הטבעי של שפעול תאים. דפוס העבודות של ה-Kevzara דומה מאוד לאלה של האקטמרה. הן האקטמרה והן ה-Kevzara הוכיחו את יעילותן על פני התכשיר Humira (נוגד TNF-α) כאשר הן ניתנות כמונותרפיה, ללא הוספת Methotrexate.
חוסמי Janus kinase (JAK) (Tofacitinib - Xeijanz)
תרופה זו הצטרפה לשוק הישראלי בעשור השני של המאה ה-21. החידוש שבה הוא שהטיפול ניתן באופן פומי ולא באמצעות הזרקה. תכשיר זה משפיע על יצירתם של ציטוקינים בכתוך התא באמצעות חסימת שפעול של תאים לבנים בשל מניעת שפעולן של קינאזות תוך תאיות. מידותיו המולקלואריות של התכשיר קטנות ועל כן הוא נספג אל תוך התא בקלות רבה ואינו מייצר נוגדנים מנטרלים. התרופה מיועדת לטיפול בחולים הלוקים בדלקת מפרקית שיגרונתית ובעתיד אנו צפויים לראות שימוש בתכשיר גם כנגד דלקת מפרקית פסוריאטית ובעתיד תהיינה אינדיקציות נוספות.
בדומה להכשיר זה חברות תרופות נוספות מפתחות תכשירים רבים אחרים הניטלים אף הם דרך הפה אשר פועלים במנגנון דומה ובקרוב נראה שפע של תכשירים שייכנסו לשוק התרופות.
תרופות ביו-סימילאריות
בניגוד לעולם התרופות הסטנדרטי, ייצורן של התרופות הביולוגיות מחייב תחכום ותקורות רבות ויקרות. כמו כן, בטכנולוגיה לפיתוחן של תרופות ביולוגיות מושקעים משאבים רבים, אך עם זאת תכולת הפטנט מוגבלת לתקופה בת 15 שנים בלבד. חברות עתירות הון ובעלות אמצעים טכנולוגיים מתקדמים מצטרפות לשוק הייצור של תרופות הדומות לתרופות הביולוגיות ומכאן השם ביו-סימילאריות. לשם כך עליהן לגייס את מיטב המידע והאמצעים הביולוגיים העומדים בבסיס פיתוח תכשירים אלה.
ה-FDA מחייב שחברה המפתחת תכשיר מסוג זה תוכיח יעילות ובטיחות קלינית לפחות בהתוויה אחת ובמקביל תדגים שהתנהגותה של התרופה באדם תהיה זהה לתרופת המקור (המכונה originator).
התרופה הביולוגית הראשונה בתחום הראומטולוגי היא Remsima. תכשיר זה הוא תעתיק של ה-remicade) infliximab). תכשיר זה זכה במכרז במדינות רבות באירופה ותפס באופן מוחלט את מקומו במדינות אחדות המתבססות על שיטח מכרזים את מקומו של תכשיר המקור בשוק. תרופה נוספת העתידה להצטרף לתהליך זה היא ה-Benepali, ועתידה להתחרות מול תרופת המקור Enbrel (etanercept) המפותחת על ידי חברת סמסונג. העלות של תרופות אלה פחותה מתרופות המקור, ולכן צפויה תחרות עזה בשוק התרופות הביולוגיות.
סיכום
במאמר זה סוקרו בקצרה את ההתפתחויות מרחיקות הלכת שחלו בשוק התרופות בעולם הראומטולוגי.
המחקר והפיתוח הובילו לבלימה מרשימה בנזקיהן של דלקות מפרקיות, מה שמאפשר לחולים רבים לנהל אורח חיים שלם ובריא.
המידע שבדף זה נכתב על ידי פרופ׳ הווארד עמיטל. מנהל מחלקה פנימית ב' והמרכז למחלות אוטורימוניות, המרכז הרפואי ע"ש שיבא. חל-השומר והפקולטה לרפואה ע"ש מקלר, אוניברסיטת תל-אביב
פורסם ב-חוברת סל הבריאות עמ' 42


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק