דיסקציה של עורק צווארי - Cervical artery dissection
הופניתם מהדף Carotid artery dissection לדף הנוכחי.
| דיסקציה של עורק צווארי | ||
|---|---|---|
| Cervical artery dissection | ||

| ||
| שמות נוספים | Carotid artery dissection Vertebral artery dissection |
|
| ICD-10 | Chapter I 67.0 | |
| ICD-9 | 443.21
, 443.24 |
|
| MeSH | D020217 | |
| יוצר הערך | ד"ר עפר סדן וד"ר חן הלוי | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – אירוע מוח
דיסקציה עורקית היא אטיולוגיה שכיחה לשבץ מוח איסכמי בקבוצת הגיל הצעירה מ-50. הביטוי הקליני של דיסקציה עורקית לרב מתחיל כאירוע איסכמי חולף (TIA), המלווה בסימפטומים אופייניים נוספים כתלות במיקום האנטומי של הפתולוגיה. דיסקציה של עורק צווארי מאובחנת יותר, בשל הזמינות של הדמיה עורקית לא פולשנית. לאבחנה זו יש משמעות הן מבחינת הטיפול המיידי והן מבחינת הטיפול לטווח הארוך. הטיפול המוצע מתרכז בעיקר במניעת סיבוכים או אירוע איסכמי נוסף, וכולל טיפול תרומבוליטי, טיפול בנוגדי קרישה ובנוגדי טסיות או צנתור.
העלייה באבחנה של דיסקציה עורקית הובילה למצב בו באחוז ניכר מחולי השבץ הצעירים, שהוגדרו בעבר כקריפטוגנים, נמצא מנגנון ברור למחלה. עדיין, רב מקרי הדיסקציה הם קריפטוגנים בעצמם, שכן הדיסקציה מוגדרת כ"ספונטנית". בספרות הרפואית נמצא כי במקרים רבים ישנה עדות לפתולוגיה סיסטמית ברקמת החיבור, אף על פי שמוטציות ספציפיות הוכחו רק במיעוט מהחולים. על אף כי מסתמן שקיימת נטייה טבעית לחלות, שנראית כתכונה אינהרנטית של החולה, נטייה זו אינה מובילה להישנות המחלה בשיעור גבוה. מחקרים עתידיים עשויים לאבחן ביתר דיוק את גורמי הסיכון לדיסקציה, וכן את שילוב האירועים שמוביל לאירוע הקליני. אמצעים אלו יאפשרו טיפול מונע יעיל יותר וייתכן וגם אבחון טרום לידתי של פגמים הגורמים לסיכון גבוה במיוחד.
אפידמיולוגיה
לפי סקר שערך ה-NASIS (רישום שבץ המוח הלאומי) ב-2010, קבוצת הגיל הצעירה מ-50 מהווה כ-8.1 אחוזים ממקרי השבץ המוחי האיסכמי בישראל, שיעור שהולך ועולה עם השנים. במטופלים הסובלים מדיסקציה עורקית, גורמי הסיכון השכיחים למאורעות איסכמיים הם בעלי תרומה נמוכה, בשונה ממקרי שבץ מוחי איסכמי בגיל המבוגר. כך למשל, יתר לחץ דם נמצא רק בכרבע מהחולים וסוכרת רק בכ-2 אחוזים. מיגרנה מופיעה בכשליש מהחולים ומהווה ככל הנראה גורם סיכון.
אטיולוגיה
החולה השכיח שמתייצג עם דיסקציה צווארית ידווח על חבלת צוואר מזערית בשבועות שקדמו לדיסקציה.
מחקרי סדרות מראים ש-36–50 אחוזים מהחולים מעידים על חבלה או תנועה חדה של הצוואר שאירעה קודם לכן, כולל טיפול כירופרקטי, הרמת משאות, פגיעות ספורט או מעורבות בתאונת דרכים. ככל שהחולה צעיר יותר, הסבירות לזהות חבלה כטריגר גבוהה יותר. במקרים אלו, עולה החשד שמדובר בתופעה מבודדת לעורק הנפגע כתוצאה מחבלה ישירה, לפחות בחלק מהמקרים.
אולם, חלק מהטריגרים הידועים מתאימים פחות לתאוריה של אירוע מקומי הגורם לדיסקציה. למשל, מחלת חום בשבועות שקדמו לדיסקציה דווחה כממצא שכיח (עד 10 אחוזים מהחולים במחקר סדרה מסוים). כך גם שיעור גבוה של לויקוציטוזיס בחולים עם שבץ על רקע דיסקציה בהשוואה לחולי שבץ מאטיולוגיה אחרת ובהשוואה לקבוצת ביקורת, וכן השכיחות הגבוהה יותר של המחלה בחודשי הסתיו והחורף לעומת האביב והקיץ, ממצאים שהתגלו בסדרה הגדולה ביותר של חולים עם דיסקציה צווארית, ה-CADISP (Cervical Artery Dissection and Ischemic Stroke Patients), שכללה קרוב ל-1,000 חולים מ-18 בתי חולים באירופה.
פרה דיספוזיציה לפיתוח דיסקציה - בעיה מבנית מקומית או הפרעה סיסטמית ברקמת החיבור
מחקרים שונים ותצפיות העלו השערות בנוגע לנטייה (פרה-דיספוזציה) של אדם מסוים לפתח דיסקציה, והעלו אפשרויות למספר גורמי סיכון אפשריים:
וריאנטים מבניים מסוכנים
- בחלק ממקרי הדיסקציה ישנה קרבה יתרה בין הזיז הסטילואידי של העצם הטמפורלית לבין עורק התרדמה (Carotid Artery), מה שמכונה גם "תסמונת הנשר" (Eagle syndrome, תמונה 1). במחקר שהשווה את אותו המרחק בעורקי תרדמה שעברו דיסקציה לעומת עורקים בריאים או לעומת עורקים שעברו דיסקציה חולייתית, נמצא כי המרחק בין השניים בעורקי תרדמה פתולוגיים קטן בממוצע באופן מובהק סטטיסטית. המרחק בין הזיז הסטילואידי לעורק היה קטן יותר באופן מובהק ססטיסטי גם כשהשוו צד פגוע לצד הנגדי באותו מטופל. ייתכן שקרבה זו גורמת לחיכוך כרוני של העורק בעצם ולהחלשת דופן העורק. אפשרות נוספת היא שהקרבה בין השניים גורמת לפגיעה עורקית בעת תנועה חריגה של הצוואר או בעת חבלה באזור
- מהלך מפותל של עורק התרדמה, מהלך המשנה את מהירויות הזרימה בתוך העורק, מהווה גם הוא גורם סיכון
- עלייה גדולה בקוטר עורק התרדמה המשותף בזמן הסיסטולה (נמדדה בסיוע אולטרה-סאונד), או קוטר גדול של אבי העורקים (אאורטה) (מעל 34 מילימטר) תורמים גם הם לנטיה לפתח דיסקציה
אפשרויות מבניות אלו יכולות להסביר חולשה מקומית של העורק המעורב, אך השוני המבני הקיים לאורך כל חיי המטופל לא מסביר התרחשות של אירוע קליני במועד ספציפי. בנוסף, שיעור ההישנות של דיסקציה עורקית עומד על כ-1 אחוז לשנה בלבד (במקרים שאינם משפחתיים), כך שהסבר מבני אינו מציג את מלוא התמונה. דרך אחת להסביר את שיעורי ההישנות הנמוכים היא ההשערה שקיימת נטייה מולדת הבאה לידי ביטוי בסיטואציה ספציפית - כמו במצב דלקתי לאחר מחלת חום. השערה נוספת היא שבתהליך מעורבים מזהמים ספציפיים שטרם זוהו.
הפרעה תורשתית ברקמת החיבור
אטיולוגיה מסוג נוסף, היא הפרעה תורשתית סיסטמית ברקמת החיבור. האפשרות המוכרת ביותר, גם אם נדירה יחסית, היא התסמונת Ehlers Danlos type IV. בתסמונת זו קיימת מוטציה באחת משרשראות הקולגן מסוג III{. דיספלזיה פיברומוסקולרית (Fibromuscular dysplasia) היא מצב נוסף בו ישנה הפרעה בדופן העורק עם נטייה לדיסקציה, בייחוד בעורקי התרדמה, אך למרות הנטייה המשפחתית הקיימת, טרם התגלה הגן הגורם לכך. פרט לשתי מחלות אלו, ידועה נטייה להתקבצות משפחתית של מקרי דיסקציה גם ללא מחלה מאובחנת. מחקר מסוים שבדק מעל 110 זוגות אחאים, מצא שלאדם סיכון גבוה פי 6.6 לסבול מדיסקציה או ממפרצת מוחית אם לאחד מאחאיו הייתה דיסקציה או מפרצת. בסדרה אחרת, נמצא שקרוב משפחה מדרגה ראשונה נמצא בכ-2 אחוזים מהחולים עם דיסקציה. עוד ידוע, שדיסקציה חוזרת שכיחה יותר בחולים עם סיפור משפחתי.
הנטייה המשפחתית הובילה לגילויים של מוטציות וגנים נוספים המעורבים בתהליך, כגון מוטציה בגן המקודד לקולגן I, בגן המקודד לקולגן III או בגן המקודד לקולגן V. אולם, בדיקה של גנים אלו ואחרים בסדרות של חולים לא מצאה שמדובר בממצא שכיח. גורם סיכון תורשתי נוסף הוא היפר-הומוציסטאינמיה קלה בגנוטיפ של MTHFR TT (Methylenetetrahydrofolate reductase).
חיפוש הפרעות גנטיות בגנים הידועים כמעורבים בדיסקציות של אבי העורקים העלה ממצאים שליליים: לא נמצאה הפרעה בביטוי של אלפא-1-אנטי טריפסין (Alpha-1-anti trypsin) או מוטציה בגן המקודד ל-Tropoelastin. אמנם נמצאה שכיחות גבוהה של פולימורפיזם ספציפי בגן המקודד לאלפא-1-אנטי טריפסין בחולים עם דיסקציה צווארית לעומת קבוצת ביקורת, אך ללא שינוי בביטוי של הגן.
גישה אחרת לחיפוש אחר חלבונים המעורבים בפגמים ברקמת החיבור היא דרך ביופסיות עור. תרבית מתאים פיברובלסטים שנלקחה מסדרת מטופלים עם דיסקציה צווארית, מצאה שב-5.5 אחוזים מהם ישנה רמה נמוכה של קולגן III ביחס לקולגן I, ללא עדות למוטציה בגן 21.
דוגמה נוספת, היא תיאור מקרה בודד של גבר בן 38, בריא ברקע, שהתייצג עם דיסקציה קורונרית. בבדיקות שנעשו על ביופסית עור שנלקחה ממנו נמצא כי האנזים ליזיל אוקסידז (Lysyl oxidase - LOX), שהוא אחד האנזימים שיוצר את הקישוריות (Cross linking) בין הסיבים האלסטיים קולגן ואלסטין, מבוטא באופן נמוך משמעותית בהשוואה לאוכלוסייה הבריאה. כתוצאה מכך קיים חוסר ארגון במראה ההיסטולוגי של העור. במחקר זה לא התבצע חיפוש אחר מעורבות הגן הזה גם בדיסקציות צוואריות.
ביופסיות עור היוו כר נרחב לחיפוש הפרעות סיסטמיות ברקמת החיבור של חולים עם דיסקציה עורקית. אחד המחקרים הראשונים בתחום נטל ביופסיות עור מ-65 חולים עם דיסקציה צווארית, ומצא שאמנם רק 5 אחוזים מהם הראו ממצאים קליניים של מחלת רקמת חיבור (עור גמיש או מפרקים גמישים) אך לכ-55 אחוזים היו ממצאים לא תקינים בביופסיית העור תחת בחינה במיקרוסקופ אלקטרוני כגון הסתיידות וקיטוע (פרגמנטציה) של הסיבים האלסטיים. ביופסיות חוזרות שנלקחו לשמונה מהחולים הוכיחו שהמראה הפתולוגי ברקמה נשמר לאורך זמן, ובמקרים בהם הייתה דיסקציה חוזרת הייתה גם קורלציה לחומרת ההפרעה ברקמת החיבור. מחקר אחר בתחום, נטל ביופסיות עור מ-7 חולים לאחר דיסקציה עורקית ומצא בשישה מהם שינויים האופייניים ל-Ehlers Danlos syndrome. מחקר נוסף בדק ביופסיות עור מ-31 חולים לאחר דיסקציה ספונטנית לעומת 17 בריאים, ומצא של-20 אחוזים מהחולים עם הדיסקציה היה מבנה לא תקין של סיבי הקולגן, בעוד שבקבוצת הביקורת לא היו ממצאים פתולוגים באף אחת מהדגימות. הבדיקה נעשתה תחת מיקרוסקופ אלקטרוני תוך שימוש בצביעת Immunogold שהיא צביעה מיוחדת לקולגן I ו-III.
כשנדגמו ביופסיות מעורק הרקה (Temporal artery) של חולים עם דיסקציה, נמצאו ממצאים פתולוגיים גם כן. בביופסיות מעורק הרקה של חולים עם דיסקציה בשלב האקוטי, נמצאו ברובם (8/9) פתולוגיות שונות, כגון הפרדה בין שכבות העורק והסננה דלקתית בין השכבות. במחקר המשך נלקחו ביופסיית מעורק הרקה ל-14 חולים נוספים עם דיסקציה עורקית והודגמה דופן לא תקינה בכולם, בדגש על המעבר בין שכבת האדוונטיציה לשכבת המדיה, ללא מעורבות של שכבת האנדותל. החוקרים מצאו שטפי דם מיקרוסקופים שמקורם בצינורי הצינורות (ה-Vasa vasorum, אותם כלי דם שמזינים את דפנות כלי הדם הגדולים). הממצאים הנזכרים למעלה מהווים עדות תומכת הן לאופי הסיסטמי של תופעת הפגיעה ברקמת החיבור והן לפתוגנזה המקומית הנעה מחלקו החיצוני של העורק פנימה, ללא פגיעה באינטימה בתחילת התהליך (מה שנוגד את ההשערה המקובלת בתחום).
למרות כל ממצאים אלו, המעידים על הפרעה סיסטמית ברקמת החיבור, קשה מבחינה קלינית לזהות את האנשים המועדים לדיסקציה. מחקר מסוים ניסה ליצור דירוג קליני שינבא הפרעות ברקמת החיבור בחולים עם דיסקציה ספונטנית, על ידי בחינת סימנים קלאסיים כמו גמישות יתר של מפרקים, גמישות יתר של העור, חזה קעור (Pectus excavatum) או חזה יונה (Pectus carinatum), לובן עין כחול וכדומה. במחקר נבחנו סך הכל 25 פרמטרים, אך אלו לא הצליחו להבחין קלינית בין חולים אלו לבין חולי שבץ קריפטוגנים אחרים. פרט לכך, במחקר זה נמדד גם קוטר עורק התרדמה המשותף (Common carotid artery) כאמצעי נוסף המכוון למחלות עורקיות אולם לא נמצא הבדל מובהק בקוטר בין הקבוצות.
לסיכום: מחקרים רבים מוצאים עדות להפרעה ברקמת החיבור בחולים הסובלים מדיסקציה, גם אם לא ניתן לאבחן מחלה או תסמונת ספציפיות. שינויים אלו נמצאו הן במבנה העולה והן במבנה דופן העורק. לשינויים אין פנוטיפ חיצוני בולט, ולכן החולים לא מזוהים מראש. ממצאים אלו מכוונים לבעיה מולדת או לכל הפחות להפרעה ארוכת טווח.
קליניקה
הביטוי הקליני של דיסקציה עורקית מתחיל במקרים רבים כאירוע איסכמי חולף, תופעה שלרוב מודעים אליה בדיעבד לאחר הופעת השבץ. הסימנים והסימפטומים שונים בהתאם למיקום האנטומי של הפתולוגיה, כלומר בין דיסקציה בעורק התרדמה, לבין דיסקציה בעורק החוליות (Vertebral artery). פרט לטריטוריה הווסקולרית השונה, המובילה לביטוי קליני נפרד על פי מיקום השבץ, ישנם סימנים אופייניים לכל עורק. תלונות על כאבי צוואר וראש אחוריים שכיחים יותר בדיסקציה של עורקי החוליות (דיסקציה אחורית), בעוד שכאבים מעל העין, תסמונת הורנר (Horner syndrome) וטנטון (Tinnitus) שכיחים יותר בדיסקציה של עורקי התרדמה (דיסקציה קדמית). דימום מוחי תת-עכבישי (Subarachnoid hemorrhage) כסיבוך משני שכיח פי עשרה במקרים של דיסקציה אחורית (כ-6 אחוזים לעומת 0.6 אחוזים בדיסקציה קדמית) עקב הנטייה של דיסקציה בעורק החוליות להתפשט לתוך הגולגולת.
ככלל, דיסקציה בעורקי התרדמה שכיחה יותר לעומת דיסקציה בעורקי החוליות. מיקום הדיסקציה הוא כמעט בכל המקרים חוץ גולגולתי. דיסקציה תוך-גולגולתית ראשונית נדירה אמנם, אך התפשטות של דיסקציה חוץ גולגולתית לחלקו התוך-גולגולתי של העורק מופיעה בכרבע מהמקרים. בעורק החוליות המיקום השכיח הוא בגובה החוליה C2, ב-Loop atlas (בעגה הרדיולוגית נקרא "מקטע V3"). בעורק התרדמה, המיקום השכיח הוא כסנטימטר מעל לפיצול עורק התרדמה המשותף לעורק הפנימי ולעורק החיצוני. עם זאת, לא נדיר למצוא דיסקציות בחלקו הפרוקסימלי יותר של עורק החוליות או בחלקו הדיסטלי יותר של עורק התרדמה.
אבחנה
על מנת לאבחן דיסקציה עורקית יש לבצע הדמיה של העורק החשוד. אולטרה-סאונד דופלר (Doppler ultrasonography) יכול לסייע בבדיקה ללא צורך בחומר ניגוד. בבדיקה זו, ניתן להדגים הפרעה דיסטלית בזרימת הדם, חוסר סדירות של העורק המתבטאת ב-Intimal flap (כאשר מדובר בעורק התרדמה), או היפוך של כיוון הזרימה בדיסקציה חולייתית. הרגישות והסגוליות של בדיקת דופלר באבחון דיסקציה הן נמוכות למדי ולכן לא ניתן להסתמך על בדיקה זו לחלוטין כאשר יש חשד קליני מבוסס. נכון ל-2014, אבחנת דיסקציה צווארית נעשית באמצעות טומוגרפיה ממוחשבת (CT-Angio ,CTA) או בדיקת תהודה מגנטית להדגמת כלי דם (Magnetic Resonance Angio ,MRA), המאפשרים הדמיה של העורק לכל אורכו כולל המוצא והמקטעים התוך-גולגולתיים שלו.
פתוגנזה
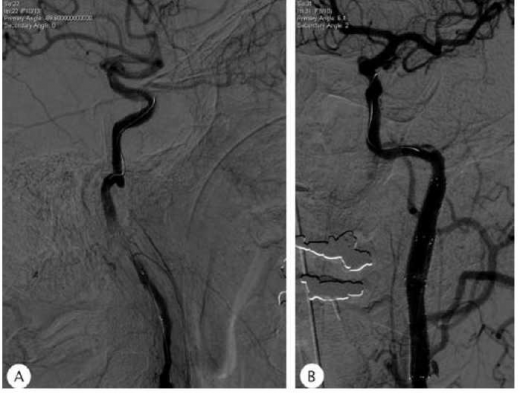
התהליך הבסיסי המתרחש בדיסקציה הוא פגם בדופן העורק, לרוב בין שכבת המדיה לשכבת האדוונטיציה, שבתוכו מתארגן קריש דם. תופעה זו יוצרת בליטה לתוך חלל העורק, המצרה אותו ואף יכולה לחסום אותו לחלוטין. ההיצרות ההדרגתית גורמת לסימן "מקור הציפור" (Bird-beak sign) האופייני בהדמיה (תמונה 1). בחלק קטן מהמקרים, ישנו קרע בשכבת האינטימה, שיכול אף להוביל לחלק בלתי יציב בתוך חלל העורק (Intimal flap כמוזכר לעיל).
סיווג
החלוקה הקלאסית של דיסקציה על פי המראה הרדיולוגי שלה מחלקת אותה לארבעה סוגים:
- דימום בדופן כלי הדם (Dissecting hemorrhage) ללא היצרות של החלל
- דימום בדופן כלי הדם עם היצרות של החלל
- יצירת מפרצת דמה (Pseudoaneurysm) בדופן, לרוב ללא היצרות של החלל
- יצירת חלל מדומה (False lumen) בתוך דופן כלי הדם
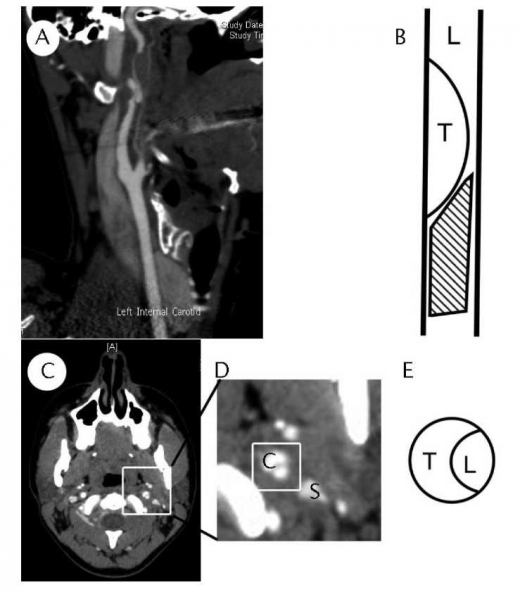
(A) CT angio בשחזור סגיטלי (Sagittal), ניתן להבחין בהיצרות הדרגתית של עורק התרדמה הפנימי, עם מילוי רטרוגרדי.
(B) ציור סכמטי של העורק - L - חלל העורק, T - קריש דם בדופן העורק באתר הדיסקציה, החלק המקווקו מזכיר "מקור ציפור" בחתך.
(C) חתך אקסיאלי (Axial) והגדלה של האזור הרלוונטי ב-(D). ניתן לשם לב לקרבה משמעותית בין עורק התרדמה (מסומן ב-C) לבין זיז הסטילואיד (Styloid process) (מסומן ב-S).
(E) ציור סכמטי של העורק הפגוע בחתך אקסיאלי (L - חלל העורק, T - קריש הדם בדופן).
טיפול
דיסקציה של עורק צווארי עשויה לגרום לשבץ מוחי באחד משלושה מנגנונים:
- תסחיף של קריש דם לעורק מוח דיסטלי וגרימת אוטם קורטיקלי במנגנון של קטיעה ישירה של אספקת הדם לרקמה - אוטם ישיר
- חסימה או היצרות קשה בצוואר וגרימת שבץ במנגנון המודינמי (נקרא "Watershed infarct")
- תסחיף של קריש דם לעורק מוחי (למשל לעורק הצרברלי האמצעי בחלקו הפרוקסימלי - Proximal Middle cerebral artery ,MCA) וגרימת אוטם קורטיקלי ותת קורטיקלי במנגנון משולב - המודינמי וישיר
כשחולה עובר שבץ על רקע דיסקציה, אחד המאפיינים של המהלך האקוטי הוא הנטייה להחמיר ביממה הראשונה. במחקר שבדק חולים שהחמירו ביממה הראשונה (כלומר כאלו שציון ה-NIHSS שלהם עלה ב-8 נקודות ומעלה), התברר שדיסקציה עורקית מעלה את הסיכון להחמרה כזו פי 9.5, ובאופן בלתי תלוי ביתר המשתנים. נטייה זו מדגישה את המרכיב ההמודינמי שמופיע כמעט בכל מקרי הדיסקציה העורקית הצווארית, ומחייבת ניטור קפדני של המדדים ההמודינמיים של החולים תוך הימנעות מירידות לחץ דם.
טיפול תרומבוליטי
אין בנמצא מחקר מבוקר שמאפשר הנחיה מבוססת ידע בנוגע לטיפול בדיסקציה עורקית. מטרת הטיפול, כבכל מקרה שבץ אחר, היא מניעת שבץ נוסף או החמרה של הפגיעה הקיימת. במקרים המועטים של חולים המגיעים בחלון ההזדמנויות, ניתן לטפל באמצעות תרומבוליזה כבכל שבץ איסכמי חריף. בסדרת מטופלים שנחקרו במסגרת פרויקט CADISP (Cervical Artery Dissection and Ischemic Stroke Patients), נבחנה יעילותו של טיפול תרומבוליטי ב-tPA (Tissue Plasminogen Activator) לשיפור פרוגנוזה של דיסקציה עורקית. כ-11 אחוזים חולים טופלו בתרומבוליזה והשוו לתת קבוצה ששימשה כביקורת (Matched-control). במחקר לא הוכח כי tPA משפר את פרוגנוזת החולים כשהאטיולוגיה היא דיסקציה עורקית. עם זאת, מחקר זה כלל מספר חולים קטן, ללא קבוצת ביקורת סדורה, ולא צפוי היה כי יענה על שאלת יעילות הטיפול. בנוסף, אף על פי שלא נמצאה עדות לשיפור בפרוגנוזה, גם לא נמצאה עדות שהטיפול מביא לעלייה בשיעור הדימומים, כך שהסיכון הנלווה לטיפול התרומבוליטי אינו גבוה והוא לא מהווה התווית נגד.
נוגדי קרישה ונוגדי טסיות
תרומבוליזה היא טיפול נוח בחולי דיסקציה שנמצאים בחלון ההזדמנויות הטיפולי המתאים. אולם, היא איננה אפשרית עבור מטופלים רבים בשל הגעתם המאוחרת לחדר המיון, ועבורם נדרש פתרון טיפולי אחר.
בטווח הקצר (לשלושה חודשים) ישנן שתי גישות מקובלות למניעת הישנות של השבץ:
- טיפול בנוגדי קרישה למשך מספר חודשים ולאחר מכן טיפול בנוגדי טסיות
- טיפול בנוגדי טסיות בלבד
במרכזים רבים משתמשים בנוגדי קרישה על מנת למנוע היווצרות מחדש של קרישי דם באתר הדיסקציה, ובכך למנוע את נדידת התסחיף מעורק פרוקסימלי לעורק דיסטלי. יש כאלו המציעים טיפול כפול בנוגדי טסיות (Aspirin + Clopidogrel) לשלב החריף לטווח הארוך, נמצא יתרון קל לטיפול בנוגדי טסיות למניעת הסיבוכים האפשריים. יעילות הטיפול נבחנה במטא-אנליזה שסיכמה את כל המחקרים הקיימים, ומצאה שהיתרון שהטיפול מקנה אמנם אינו מובהק סטטיסטית, אולם לא בוצעו מחקרים כפולי סמיות בתחום ולכן קשה להסיק מכך מסקנות.
הגישה היא טיפול בנוגדי קרישה בשלב החריף למשך 3–6 חודשים, למעט במקרים בהם יש התווית נגד כגון אוטם גדול או התמרה דימומית.
צנתור
אפשרות טיפולית נוספת, השמורה למקרים נבחרים, היא צנתור והנחת תומכן (Stent). אפשרות זו טובה בעיקר לטיפול בחולים בהם יש חסימה של עורק פרוקסימלי בשלב החריף, או במקרים בהם הדיסקציה גורמת לתסמינים המודינמיים או המשך אמבוליזציה גם בהינתן טיפול תרופתי נאות. בספרות מתואר מקרה רפואי בו צנתור מסוג זה בוצע למעלה מ-12 שעות לאחר השבץ עקב חוסר יציבות על רקע המודינמי (תמונה 2).
פרוגנוזה
הפרוגנוזה של חולה עם שבץ כתוצאה מדיסקציה תלויה באתר הפגיעה ובהיקף האוטם המוחי. בסדרה שעקבה אחר כ-900 חולים עם דיסקציה עורקית צווארית, נמצאו הבדלים בתוצאה התפקודית לאחר שלושה חודשים, כשהשוו דיסקציה בעורק התרדמה לעומת עורק החוליות: במקרים בהם עורק החוליות נפגע, כ-89 אחוזים מהמטופלים נמצאו עם דרגת mRS (עצמאות תפקודית) של 0–2, ואילו במקרים של דיסקציה בעורק התרדמה רק כ-59 אחוזים הגיעו לתוצאה זו.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר עפר סדן וד"ר חן הלוי, המחלקה לנוירולוגיה, המרכז הרפואי ת"א


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק