ציקלין - Cyclin - D1
הופניתם מהדף Cyclin D1 לדף הנוכחי.
| מדריך בדיקות מעבדה | |
| ציקלין D1 | |
|---|---|
| Cyclin D1 | |
| שמות אחרים | CYCD1, CCND1 |
| מעבדה | פתולוגיה |
| תחום | קלסיפיקציה של low-grade B-cell lymphoma. |
| יוצר הערך | פרופ' בן-עמי סלע |
הפיזיולוגיה של Cyclin D1
Cyclin D1 הוא חלבון המווסת את הכניסה של התא ל-cell cycle. הוא מסייע למעבר בין פאזות G0 ו-G1. ברקמות נורמליות, תאים אפיתליאליים בזליים, תאי אנדותל ותאי סטרומה נצבעים לרוב באופן חיובי ל-cyclin D1. כתוצאה מטרנסלוקציה בה קשורים הגן ל-cyclin D1 ו-IgH, t(11;14), הרוב המכריע של mantle cell lymphomas מבטאים ביתר את cyclin D1. הגן המקודד ל-cyclin D1 באדם שובט במקור כ-break-point rearrangement באדנומה של הפארא-תירואיד (Motokura וחב' ב-Nature משנת 1991). במקביל, ההומולוג של cyclin D1 במכרסמים זוהה כ-colony-stimulating factor-1-responsive gene במקרופאגים (Sherr וחב'-Cell משנת 1985). ידוע שכאשר cyclin D1 מוחדר בעכברים לבלוטת הפארא-תירואיד, הוא מסוגל להשרות אדנומה בבלוטה זו, ואף לווסת בעכברים את החישה של ++Ca (על פי Imanishi וחב' ב-Journal of Clinical Investigation משנת 2001). במקרופאגים, cyclin D1 חיוני לנדידת תאים אלה המכוונת על ידי colony-stimulating factor-1 (על פי Neumeister וחב' ב-Mol Biol Cell משנת 2003). בעשור הראשון של המאה ה-21, הבנת הפעילות של cyclin D1 סייעה ליתר הבנה של סינתזת DNA בתאים, ואת המנגנונים המולקולריים המניעים את התהליך הטומורוגני. התגברה ההבנה כיצד cyclin D1 מווסת את ההתמיינות והשגשוג של תאים (Wang וחב' ב-Cancer Treat Res משנת 2004, Sherr ב-Cell משנת 2004, ו-Hanahan ו-Weinberg ב-Cell משנת 2000).
התפקוד הנורמלי של cyclin D1
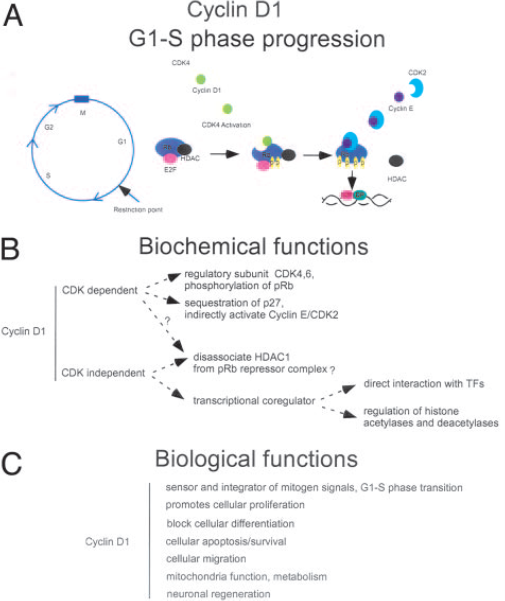
ממצאים אחדים מתיישבים עם המודל לפיו cyclin D1 משמש כחיישן מפתח וכמשלב של איתותים חוץ-תאיים בשלבים המוקדמים עד האמצעיים של פאזת G1, כאשר הוא מתפקד על ידי התקשרות ל-CDKs או Cyclin-dependent kinases שהיא משפחת אנזימים המעורבים בוויסות מחזור חיי התא, כמו גם התקשרות ל-histone acectylase ול-histone deacetylases כמודולטור של מבנה הכרומטין של גנים המעורבים ברגולציה של שגשוג תאים והתמיינותם. הנוכחות של cyclin D1 מושרית על ידי גורמי גדילה הכוללים EGF, IGF-1 ו-IGF-2 (Holnthoner וחב' ב-J Biol Chem משנת 2002); על ידי חומצות אמינו (Nelsen וחב' ב- J Biol Chem משנת 2003), על ידי lysophosphatidic acid (Hu וחב' ב- J Natl Cancer Inst משנת 2003), על ידי הורמונים כולל אנדרוגנים (Fu וחב' ב-Mol Cell Biol משנת 2003), על ידי חומצה רטינואית (Suzui וחב' ב-Cancer Res משנת 2002), על ידי γ(PPAR) peroxisome proliferator-activated receptor ligand (Wang וחב' ב- Mol Cell Biol משנת 2003), ועל ידי גורמים המופרשים מאדיפוציטים (Iyengar וחב' ב-Oncogene משנת 2003).
הורמונים גסטרו-אינטסטינליים כגון gastrin מווסתים את ביטוי של cyclin D1 בסוגי תאים ספציפיים (Song וחב' ב-Am J Physiol Gastrointest Liver Physiol משנת 2003 ו-Pradeep וחב' ב-Oncogene משנת 2004), TGFβ ו-PTHrP מווסתים ביטוי של cyclin D1 בכונדרוציטים (Beier וחב' ב-Mol Biol Cell משנת 2001), ואילו endostatin גורם לעצירת מחזור תאי אנדותל בפאזת G1 על ידי עיכוב של cyclin D1 (Hanai וחב' ב-J Biol Chem משנת 2002). איתותים אונקוגניים רבים משרים את הביטוי של cyclin D1 על ידי רצפים ייחודיים של DNA בפרומוטר של cyclin D1, ובין אונקוגנים אלה ניתן למצוא את Ras (Albanese וחב' ב-J Biol Chem משנת 1995), Src (Lee וחב' ב-J Biol Chem משנת 1999), ErbB2 (Lee וחב' ב-Mol Cell Biol משנת 2000), β -catenin (Shtuman וחב' ב-Proc Natl Acad Sci USA משנת 1999, ו-Lin וחב' באותו כתב עת משנת 2000), STATs שהם signal transducers activators of transcription & (Bromberg וחב' ב-Cell משנת 1999, ו-Matsumura וחב' ב-EMBO J משנת 1999), וכן על ידי SV40 small t antigen שהוא אונקוגן קריטי במיוחד בהתמרה סרטנית של תאי אדם (Watanabe וחב' ב-Proc Natl Acad Sci USA משנת 1996).
Cyclin D1 הוא תת-היחידה הרגולטורית של holo-enzymes המזרחנים, וביחד עם זרחון רציף על ידי cyclin E/CDK2 גורמים לאינאקטיבציה של מחזור התא על ידי העיכוב של retinoblastoma protein (להלן pRb). ה-pRb משמש כ"שומר השער" של פאזת G1 כאשר מעבר דרך נקודת הקִטּוּעַ (restriction point) מוביל לסינתזה של DNA (Baldin וחב' ב-Genes Dev משנת 1993, ו-Sherr ב-Cancer Res משנת 2000). ביטוי-יתר של cyclin D1 מקובל ככרוך באתחול המוקדם של תהליך סרטני ובסכנה של התפתחות הסרטן וגרורותיו (Motokura ו-Arnold ב-Genes Chromosomes Cancer משנת 1993, Zhang וחב' ב-Biochim Biophys Res Commun משנת 1993, Bartkova וחב' ב-Int J Cancer משנת 1994, Afar וחב' ב-Proc Natl Acad Sci USA משנת 1995, Callanan וחב' ב-Crit Rev Oncog משנת 1996, Gansauge וחב' ב-Cancer Res משנת 1997, Barnes ו-Gillett ב-Breast Cancer Res Treat משנת 1998, Diehl ב-Cancer Biol Ther משנת 2002, Stacey ב-Curr Opin Cell Biol משנת 2003, ו-Chung ב-Ann NY Acad Sci משנת 2004). עם זאת, מספר מחקרים לא מצאו במפתיע קשר בין ביטוי מוגבר של cyclin D1 לבין סינתזה מוגברת של DNA בגידולים סרטניים (Oyama וחב' ב-Cancer Res משנת 1998, ו-Shoker וחב' ב-Br J Cacer משנת 2001).
pRb משוער כחלבון "המשתיק" גנים ספציפיים הפעילים בפאזת S של מזור התא על ידי דיכוי פעיל של הפעילות השעתוקית של E2F, ופעילות זו של pRb מדוכאת על ידי cyclin D1. הדיכוי של pRb מתווך דרך גיוס של חלבונים בעלי פעילויות אינטרינזיות של histone deacetylase (להלן HDACs) וכן של חלבונים המבצעים remodeling של כרומטין, כגון Brm/SWI-related gene I (להלן BRGI). pRb המתחבר עם ADAC1 דרך מקטע ה-pRb pocket ומגייס HDACs לדכא את E2F. PRb בשיתוף עם HDAC1 מדכא את פעילות E2F בפרומוטר של cyclin E. עיכוב הפעילות של histone deacetylase על ידי trichostatin A מעכב את הדיכוי בתיווך של pRb של הפרומוטר המווסת על ידי E2F שעבר אינטגרציה לכרומוזום, מה שמרמז לכך שפעילות HDAC נחוצה לפעילות המדכאת של pRb (Luo וחב' ב-Cell משנת 1998, ו-Brehm וחב' ב-Nature מאותה שנה). BRG1 שהוא האורתולוג האנושי של hSWI/SNF, גם כן יוצר ביחד עם pRb קומפלקס של מעכב שעתוקי, הנדרש לדיכוי הגדילה המתווך על ידי pRb (Zhang וחב' ב-Cell משנת 2000).
בנוסף לתפקוד שלהם בקישור ל-CDK, יש ראיות לכך ש-cyclins מסוג D הם גם בעלי פעילויות שאין תלויות ב-CDK (Dey ו-Lee ב-Biochim Biophys Acta משנת 2000, ו-Pestell וחב' ב-Endocr Rev משנת 1999). לפעילויות אלו תפקיד מהותי בהתמיינות, בגדילה ובמטבוליזם של התא. Cyclin D1 יוצר קשר פיזי עם למעלה מ-30 גורמי שעתוק (Zhang וחב' ב-EMBO J משנת 1999, Horstmann וחב' ב-Oncogene משנת 2000, ו-Inoue ו-Sherr ב-Mol Cell Biol משנת 1998). מספר קולטנים בגרעין התא, הכוללים את הקולטן לאנדרוגן )AR), את הקולטן α לאסטרוגן (ER), את הקולטן להורמון התירואיד, וכן את PPARγ, הנקשרים ישירות ל-cyclin D1, בתאים בתרבית. השפעול הבסיסי כמו גם השפעול על ידי קישור לליגנד של הקולטנים בגרעין התא, מווסתים על ידי cyclin D1 (Knudsen וחב' ב-Cancer Res משנת 1999, Reutens וחב' ב-Mol Endocrinol משנת 2001, Petre וחב' ב-J Biol Chem משנת 2002, Petre-Draviam וחב' ב-Cancer Res משנת 2003, Zwijsen וחב' ב-Cell משנת 1997, Neuman וחב' ב-Mol Cell Biol משנת 1997, Lamb וחב' באותו כתב עת משנת 2000, ו-Qin וחב' ב-Cancer Res משנת 2003). Cyclin D1 נקשר לפקטור הכרוך עםp300/CBP (להלן P/CAF) ומסייע לשפעול של ERα (McMahon וחב' ב-Proc Natl Acad Sci USA משנת 1999), בה שעה ש-cyclin D1 מדכא את האיתות של הקולטן לאנדרוגן (AR) באופן התלוי ב-P/CAF. מחקרים עם נתוני microarray מגידולים סרטניים המבטאים cyclin D1 ביתר, זיהו את CCAAT/enhancer binding protein (להלן C/EBP beta) כיעד של cyclin D1 (Lamb וחב' ב-Cell Cycle משנת 2003). יש ראיות לכך ששמט (deletion) של 20 חומצות אמינו בקצה ה-N טרמינלי של cyclin D1, פגע בפעילות הקינאזה של pRb, אך לא השפיע על כושר ההתמרה שלו (Zwicker וחב' ב-Oncogene משנת 1999), מה שמצביע על כל שמקטעים אחרים מאלה שגורמים לאינאקטיבציה של pRb, עשויים לתרום לתפקוד ההתמרה של cyclin D1.
סטיות גנטיות במעגלים רגולטוריים השולטים במעבר דרך G1 של מחזור התא מתרחשות באופן תדיר בסרטן בבני אדם, וביטוי-יתר של cyclin D1 מהווה את אחת הסטיות השכיחות ביותר באדם, כאשר ריכוז גבוה של cyclin D1 מופיע בשלב מוקדם של התהליך הסרטני (Weistein ב-J Cell Biochem משנת 1996). Cyclin D1 שובט לראשונה וזוהה כאונקוגן בהתפתחות של גידולים בבלוטת הפארא-תירואיד (Mallya ו-Arnold ב-Front Biosci משנת 2000, ו-Arnold וחב' ב-Cold Spring Harb Symp Quat Biol משנת 1991). נמצא ש-20–40% מהאדנומות של הפארא-תירואיד מבטאות ביתר את cyclin D1 (Hemmer וחב' ב-Am J Pathol משנת 2001, Vasef וחב' ב-Mod Pathol משנת 1999, Tominaga וחב' ב-Kidney Int מאותה שנה, ו-His וחב' ב-J Clin Endocrinol Metab משנת 1996). ביטוי יתר של cyclin D1 אינו מוגבל רק לפרוליפרציה סרטנית של רקמת הפארא-תירואיד, אלא גם נצפה ברקמה נורמלית של הפארא-תירואיד (Hosokawa ו-Arnold ב-Genes Chromosomes Cancer משנת 1998). עכברים טרנסגניים בהם הושרתה רמה מוגברת של cyclin D1 לא רק פיתחו שגשוג לא נורמלי של תאי פארא-תירואיד, אלא גם פיתחו היפר-פארא-תירואידיזם. כלומר cyclin D1 לא רק מפקח על שגשוג תאי הבלוטה, אלא גם תורם להפרשה א-נורמלית של הורמוני הבלוטה.
CCND1 הגן המקודד ל-cyclin D1 עובר אמפליפיקציה ב-15%, וביטוי-יתר ב-30–50% בתאי סרטן שד ראשוניים באדם. ברוב סוגי הסרטן, כולל סרטן ריאות, שד, סרקומה, וסרטן המעי הגס (Salem Amir וחב' ב-Open J Pathol משנת 2018, Parvin וחב' ב- Indian J Surg Oncol משנת 2019, ו-Li וחב' ב- Pathol Oncol Res משנת 2020). ביטוי היתר של cyclin D1 נובע שהשרייה על ידי איתותים אונקוגניים, ולא כתוצאה ממוטציה סומטית קלונלית, או כתוצאה מ-rearrangement בגן CCND1. פולימורפיזם בנוקלאוטיד בודד ,A/G הבא לביטוי כ-A870G ב-intron 4 של הגן CCND1, אחראי לשני עותקים נבדלים של mRNA איזופורמים a ו- b. איזופורם b מקודד לחלבון בו 55 חומצות האמינו האחרונות בקצה ה-C טרמינלי של cyclin D1 מותמרות על ידי רצף קצר יותר המקודד על ידי intron 4 (Kong וחב' ב- J Natl Caner Inst משנת 2001). צורה קטומה (truncated) של cyclin D1 נכרכה עם שכיחות גדולה יותר של גידולים, כולל סרטני הריאות, השד, המעי הגס וסוגים נוספים (Wang וחב' ב-Carcinogenesis משנת 2002, Bala ו-peltomaki ב-Cancer Res משנת 2001, ו-Le Marchand וחב' ב-JAMA משנת 2003). חקר התפקודים הביולוגיים של cyclin D1 כמו גם של cyclin E, על ידי שימוש בחיות טרנסגניות, מצא עודף מפתיע של גנים אלה לצורך התפתחות נורמלית ולקידום מחזור התא. עכברים חסרי cyclin D1 לקו באפופטוזיס של רשתית העין, כשל בהתפתחות ההנצה המכתשית (אלבאולרית) של השד בתגובה להיריון, שינויים במטבוליזם של שומנים והתפתחות כבד שומני, ופגמים בנדידה של מקרופאגים (Sicinski וחב' ב-Cell משנת 1995, ו-Fantl וחב' ב-Genes Dev משנת 1995). פיברובלסטים של עוברי עכברים -/-cyclin D1 מאופיינים על ידי אפופטוזיס מוגבר, ותמותת תאים מוגברת מהקרנת UV. ביטוי של cyclin E מסייע למניעה של א-נומליות התפתחותיות של בלוטות החלב ושל רשתית העין רק ב-30% מעכברי -/-cyclin D1, מה שמצביע על תפקוד ספציפי של cyclin D1 ברקמות אלו. חסר של p27KIP1 (שהוא מעכב של פעילות קינאזה התלויה ב-cyclin גם כן מסייע למנוע את התפתחות של בלוטות החלב ושל רשתית העין, בעכברים cyclin D1, מה שמצביע על כך ש-p27KIP1 יכול להיות מווסת באופן שלילי על ידי cyclin D1 (Tong ו-Pollard ב-Mol Cell Biol משנת 2001, ו-Geng וחב' ב-Proc Natl Acad Sci משנת 2001).
אינאקטיבציה של cyclin E/CDK2 בעכברים גם כן הסתכמה רק באי-סדירויות מקומיות. עכברי knockout ב-cyclin E1/E2 היו פגועים בספרמטוגנזה וביצירה של תאי-ענק טרופובלסטים (Chang וחב' ב-Cell משנת 2003), סוג תאים הדורש אנדו-רה-דופליקציה (מחזורי פאזת S ללא חלוקת התא (Gladden ו-Diehl ב-Cancer Cell משנת 2003). ניסויים בתאים בתרבית מראים ש-cyclin D1 מתפקד כ"אונקוגן מסייע" המחיש התמרה אונקוגנית של אונקוגנים אחרים כגון Ras, Src ו-E1A בתאים בתרבית (Hinds וחב' ב-Proc Natl Acad Sci USA משנת 1994, Robles וחב' ב-Genes Dev משנת 1998, ו-Lovec וחב' ב-Oncogene משנת 1994). ביטוי מושרה של cyclin D1 או של cyclin E השרה גידולים בבלוטות החלב של עכברים טרנסגניים (Wang וחב' ב-Nature משנת 1994, ו-Bortner ו-Rosenberg ב-Mol Cell Biol משנת 1997). לעומת זאת, עכברי -/-cyclin D1 היו עמידים מפני מצב של טומורוגניות של בלוטות החלב המושרה על ידי ErbB2 או על ידי Ras (Yu וחב' ב-Nature משנת 2001), מה שתמך במחקרים מוקדמים תוך שימוש ב-antisense של cyclin D1. עכברים חסרים cyclin D1 לקו בטומורוגניות מוגברת של בלוטות החלב בתגובה לשפעול על ידי מסלול האיתות של β-catenin (Hatsell וחב' ב-J Mammary Gland Biol Neoplasia משנת 2003), אך היו עמידים מפני השרייה של גידולים בדרכי המעי על ידי מוטציה בגן ApcMin (Hulit וחב' ב-Mol Cell Biol משנת 2004). מחקרים מציעים ש-cyclin D1 יהפוך יעד לתרפיה פוטנציאלית בממאירות של דרכי העיכול, כיוון שעכברים טרנסגניים עם ביטוי מופחת של cyclin D1 לוקים פחות בגידולים בדרכי המעי.
Cyclin D1 כרגולטור של הקולטן להורמונים בגרעין התא
Cyclin D1 הוא רגולטור חיובי של שעתוק בתיווך של ERα (על פי Zwijsen וחב' ב-Genes Dev משנת 1998). Cyclin D1 מעודד שעתוק של הגנים של estrogen element-responsive ללא תלות בפעילות הקישור של CDK.
Erα נקשר ל-Cyclin D1 in vivo ו-in vitro. השפעול של Erα על ידי cyclin D1 אינו מעוכב על ידי אנטי-אסטרוגנים. נראה ש-cyclin D1 מעודד את השפעול של Erα על ידי גיוס של P/CAF. ביטוי יתר של cyclin D1 תואם תוצא קליני מעודד ותגובה טובה יותר לטמוקסיפן בתאי סרטן שד אנושי חיוביים ל-Erα (על פי Hwang וחב' ב-Pathol Int משנת 2003, ו-Han וחב' ב-Oncol Rep משנת 2003).
D1 מעכב באופן בררני את התפקוד של קולטני האנדרוגנים (AR) במספר סוגי תאים, כולל תאי סרטן השד, סרטן שלפוחית השתן, ושורות תאים בלתי-תלויים באנדרוגנים של אדנוקרצינומה של הערמונית. Cyclin D1 יוצר קומפלקס ספציפי עם AR, דרך המקטע ה-C טרמינלי שלו. המנגנון דרכו cyclin D1 מעכב את AR נראה תלוי בחלקו ב-HDACs או ב-histone acyltransferases (להלן HATs). יצוין ש-cyclin D1 ו-AR נקשרים למקטעים דומים של P/CAF, ובהתאם cyclin D1 מונע in vitro את הקישור של AR ל-P/CAF.
Cyclin D1 מווסת את פעילותם של גורמי שעתוק אדיפוגני ובהתאם מעכב גם אדיפוגנזה
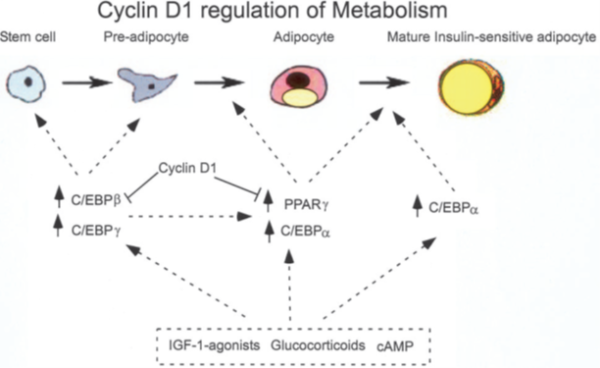
התוכנית השעתוקית האחראית לקואורדינציה של התמיינות אדיפוציטים מופתה in vivo וגם in vitro (Rosen ו-Spiegelman ב-Ann Rev Cell Dev Biol משנת 2000). PPARγ הוא גורם שעתוק המשופעל על ידי ליגנד, המושרה באופן בררני על ידי ליגנדים מקבוצת ה-thiazolidinedione. PPARγ הוא בעל תפקיד קריטי במטבוליזם של חומצות שומן, בהומאוסטאזיס האנרגטי, ובאדיפוגנזה (Koeffler וחב' ב-Clin Cancer Res משנת 2003). גורם שעתוק שני המשחק תפקיד מפתח באדיפוגנזה הואC/EBP שהוא CCAAT-enhancer-binding protein (תמונה למטה). שני מחקרים מציעים ש-cyclin D1 מעכב מסלול התמיינות זה בגין יכולתו לעכב את הטרנס-אקטיבציה של C/EBPbeta (על פי Lamb וחב' ב-Cell משנת 2003), וכן לעכב את הטרנס-אקטיבציה והתפקוד של PPARγ.
Cyclin D1 והתמיינות מיוגנית
ההתמיינות של מיובלסטים שלדיים מפוקחת על ידי basic helix-loop-helix (להלן bHLH) שהוא מוטיף (motif) מבני של חלבון המתאר את אחת המשפחות הגדולות ביותר של גורמי שעתוק הגורמים לדימריזציה (Neuhold ו-Wold ב-Cell משנת 1993, Braun וחב' ב-Genes Dev משנת 1992, Rudnicki וחב' ב-Cell משנת 1992, ו-Lassar וחב' באותו כתב עת משנת 1991). השפעול של שעתוק גן שרירי במיובלסטים שלדיים שעברו התמיינות, דורש את נסיגת תאים אלה מהמחזור התאי. ביטוי אקטופי של cyclin D1 מעכב את השפעול השעתוקי של גן בשריר על ידי מווסתים מיוגניים דוגמת bHLH, והשפעה זו תלויה בקצה ה-C טרמינלי ולא במוטיף הקישור ל-pRb של cyclin D1 (Rao וחב' ב-Mol Cell Biol משנת 1994). הוצע שפעילות G1 cyclin-CDK חוסמת את אתחול ההתמיינות של שריר השלד על ידי מנגנונים התלויים ב-pRb ומנגנונים שאינם תלויים ב-pRb (Skapek וחב' באותו כתב עת משנת 1996). Cyclin D1 עשוי לווסת את ההתמיינות של מיובלסטים על ידי הפרעה לאינטראקציה של MyoD-CDK4 הפוגעת ביכולת הנורמלית של myoD להשרות מיוגנזה.
הדיכוי של STAT3 על ידי cyclin D1
Cyclin D1 הוא יעד חשוב של מסלול האיתות של STAT במספר סוגי תאים (Brockman וחב' ב-Mol Endocrinol משנת 2002, Turkson ו-Jove ב-Oncogene משנת 2000, Simon וחב' ב- Am J Physiol Lung Cell Mol Physiol משנת 2002, ו-Quintanilla-Martinez וחב' ב-Am J Pathol משנת 2003). מחקרים הראו ש-cyclin D1 מעכב את השפעול של STAT3. בשיטה של co-immunoprecipitation נמצא ש-cyclin D1 מתקשר עם מקטע השפעול של STAT3 בגירוי על ידי IL-6. ביטוי-יתר של cyclin D1 עיכב את השפעול השעתוקי של חלבוני STAT3, כאשר גם השפעה זו לא הייתה תלויה בפעילות CDK4 kinase. אחת ההשערות היא שההתקשרות של cyclin D1 למקטע השפעול של STAT3 יכולה לחסום את האינטראקציה של STAT3 עם מערכת השפעול של RNA polymerase II, או לחסום את האינטראקציה של STAT 3 עם הקו-פקטורים החיוניים שלו כגון CBP/p300. לחלופין, המיקום בגרעין התא של STAT3 יכול להיות מווסת על ידי cyclin D1 באופן התלוי במחזור התא.
רגולציה של פעילות B-Myb על ידי cyclin D1
B-Myb הוא חבר משומר במשפחת Myb של גורמי שעתוק, המשחק תפקיד במעבר G1/S של מחזור התא. ביטוי קונסטיטוטיבי של B-Myb cDNA אנושי בתאים פיברובלסטים מסוג BALC/c ,3T3 הפחית את הדרישה ל-B-Myb כגורם גדילה, והשרה את הפנוטיפ המותמר (Sala ו-Calabretta ב-Proc Natl Acad Sci USA משנת 1992). יש עדויות לכך, ש-cyclin D1 בניגוד ל-cyclin A, מעכב את פעילות B-Myb על ידי יצירת קומפלקס B-Myb-cyclin D1. Cyclin D1 מתחבר עם המקטע המרכזי של B-Myb בתאים בתרבית. ההשפעה המעכבת של cyclin D1 על B-Myb תלויה ב-CDK.
Cyclin D1 ו-HAT
Cyclin D1 נכרך עם HATs, עם HDACs וכן עם חלבונים הגורמים ל-remodeling של כרומטין. p300 ו-P/CAF (שהוא p300/CBP-associated factor) הם קו-משפעלים שעתוקיים, המכילים באופן אינטרינזי פעילויות אנזימטיות של HAT. Cyclin D1 עובר אינטראקציה פיזית עם p300/CBP ועם P/CAF. בהתאם, הנוכחות של cyclin D1 משפיעה על האצטילציה המקומית של histone, וכן משפיעה על המתילציה של פרומוטרים ספציפיים בכרומטין. P/CAF ו-p300 נקשרים באופן ישיר עם cyclin D1 בתאים בתרבית, והם יכולים להיות מגויסים לתוך קומפלקס עם ERα או עם AR על ידי.cyclin D1 בדומה, cyclin D1 מדכא את הקולטן להורמוני התירואיד על ידי גיוס של HDAC3 ליצירת קומפלקס משולש (Lin וחב' ב-J Biol Chem משנת 2002).
מודל מוצע של רגולציה של מבנים כרומטיניים על ידי cyclin D1
אצטילציה של זנבות ה-lysine של hisone על ידי HATs מביאה לפתיחת המבנה של כרומטין, מה שהופך את DNA לזמין יותר למנגנון השעתוקי (Felsenfeld ו-Groudin ב-Nature משנת 2003). Cyclin D1 נכרך פיזיקלית עם P/CAF וכן עם HDACs. הגיוס של HDACs על ידי cyclin D1 כנראה מביא לדה-אצטילציה של זנבות ה-lysine של ה-histone ומפחית את האצטילציה של H4 בהקשר של מבנה של כרומטין מקומי של גנים ספציפיים. היצירה של מבנים קומפקטיים של כרומטין מפוקחת לכאורה על ידי cyclin D1 בפרומוטרים ספציפיים.
התפקוד של pRb נמצא תחת רגולציה של תהליכי פוספורילציה ואצטילציה. p300 ו-P/CAF נמצאו גורמים לאצטילציה של pRb, המונעת פוספורילציה יעילה על ידי cyclin E/CDK2 אך מסייעת לקישור של pRb ל-MDM2 (שהוא mouse double minute-2 protein) (Chan וחב' ב-Nature Cell Biol משנת 2001). באופן בלתי צפוי, האצטילציה אינה משפיעה על בלימת הגדילה התלויה ב-pRb או על הדיכוי של הפעילות השעתוקית של E2F. במקום זאת, אצטילציה דרושה ליציאה הטרמינלית ממחזור התא המתווכת על ידי pRb ולאינדוקציה של ביטוי מאוחר של הגן המיוגני. לאור ההתקשרות הפיזיקלית בין cyclin D1 ו-HATs, והקישור הידוע של cyclin D1 ו-pRb, ולאור העובדה ש-pRb עבר אצטילציה, מחקרים יצטרכו להחליט על התפקיד היחסי של cyclin D1 ברגולציה לעומת פוספורילציה של pRb.
Cyclin D1 ספיחה תאית ותנועת תאים
ספיחת תאים למשתית החוץ-תאית (ECM) המתווכת על ידי integrin והנדרשת לגידול הנורמלי של תאים, מותמרת לפחות חלקית על ידי cyclin D1 בעזרת adhesion kinase ו-integrin-linked kinase (להלן ILK). איתות על ידי integrin דרך adhesion kinase מקומי, מווסת את התקדמות מחזור התא ואת הנוכחות של cyclin D1 ברמה השעתוקית בתלות בספיחת התאים בתיווך integrin כמו גם בתלות באיתות על ידי ERK (Zhao וחב' ב-Mol Cell Biol משנת 2001). Cyclin D1 מושרה גם על ידי ה-repeat של ankrin המכיל serine-threonine protein kinase (D'Amico וחב' בJ Biol Chem- משנת 2000), אשר מעלים את רמות cyclin D1 ומגבירים את השעתוק דרך PI3 kinase ומסלול AKT/PKB. Wnt-1 משרה את ה-mRNA של ILK ושל cyclin D1, מה שנתמך על ידי ראיות מתרבות שאיתות מיתוגני ושלמות ציטו-שלדית נדרשים לאפשר התקדמות של מחזור התא דרך cyclin D1 (Bohmer וחב' ב-Mol Cell Biol משנת 1998).
Cyclin D1 חיוני לספיחה תאית, לתנועת תאים ולנדידת מקרופאגים במח העצם. יכולת הנדידה של מקרופאגים בתגובה לפציעה או בתגובה ל-chemotaxis בתיווך של ציטוקינים, או הנדידה הטרנס-אנדותליאלית של מקרופאגים במח העצם של חיות -/-cyclin D1 פחתו. נראה אם כן שהשפעתו של cyclin D1 על נדידת תאים, יכולה להעיד על מעורבותו בחדירת תאים סרטניים לרקמות סמוכות ובתהליך הופעת גרורות, ללא קשר מיידי להשפעתו על התקדמות מחזור התאים.
Cyclin D1 כיעד תרפויטי בסרטן
- עיכוב של פעילות cyclin D1: עיכוב של תרגום cyclin D1 mRNA על ידי מעכבי mTOR (Musgrove ב-Growth Factors משנת 2006) ועל ידי משפעלים של RXR שהוא retinoic X receptor, אחד מהקולטנים בגרעין התא (Dragnev וחב' ב-J Clin Oncol משנת 2005, ו-Kim וחב' ב-Cancer Prevent Res משנת 2011)
- הפחתת הדגרדציה של cyclin D1: דגרדציה בתיווך של חומצה רטינואית של הרס cyclin D1 דרך המסלול הפרוטאוליטי של ubiquitin (Boyle וחב' ב-J Natl Cancer Inst משנת 1999). ניתן לגרום להפחתת הדגרדציה של cyclin D1 גם על ידי השרייה בעזרת דגרדציה של DIF-1 (או differentiation-induced factor-1) המושרית על ידי ubiqitin (על פי Mori וחב' ב-Exp Cell Res משנת 2005), וכן על ידי עיכוב של סינתזת cyclin D1 (Baliga וחב' ב-J Biol Chem משנת 1969, ו-Obrig וחב' באותו כתב עת משנת 1971)
- השריית יציאה של cyclin D1 מתוך גרעין התא: שימוש במעכבים של האנזים histone deacetylase להשרייה של ייצוא של cyclin D1 מהגרעין (Vigushin ו-Coombes ב-Anti-Cancer Drugs משנת 2002)
- עיכוב של cyclinD1-CDK4/6: שימוש במולקולות קטנות המעכבות CDK (Lapenna ו-Giordano ב-Nature Rev Drug Discov משנת 2009, ו-Shapiro ב-J Clin Oncol משנת 2006)
הוראות לביצוע הבדיקה
הבדיקה מתבצעת על די צביעה אימונו-היסטוכימית של הרקמה הנבדקת. החומר אמור להגיע למעבדה על 2 זכוכיות נושא טעונות חיובית, כאשר עובי החתך הוא 4 מיקרון. בלוק הרקמה עובר קיבוע בפורמלין ו-embedding בפרפין. עדיף שהחומר יועבר בטמפרטורת החדר, אך יכול להתקבל גם בקירור. יש לפסול משטח ציטולוגי קפוא או רטוב, רקמה שלא קובעה בפורמלין או לא עברה embedding בפרפין, ויש לפסול זכוכיות נושא לא טעונות או זכוכיות נושא ProbeOn.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק