מלנומה - טיפול ממוקד מונע התפתחות גרורות - Metastatic melanoma - preventive targeted therapy
הופניתם מהדף Melanoma - preventive targeted therapy לדף הנוכחי.
| מלנומה - טיפול ממוקד מונע התפתחות גרורות | ||
|---|---|---|
| Metastatic melanoma - preventive targeted therapy | ||
| ||
| שמות נוספים | טיפול ממוקד מונע התפתחות גרורות בחולי מלנומה בסיכון להתקדמות | |
| יוצר הערך | פרופסור יעקב שכטר | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מלנומה
חולי מלנומה עם מעורבות של בלוטות הלימפה נמצאים בסיכון גבוה להישנות המחלה. הטיפול היחיד שאושר בישראל למניעת הישנות מלנומה בחולים בסיכון הוא אינטרפרון במינון גבוה. עם זאת, קיימים טיפולים חדשים שנמצאו יעילים במניעת הישנות מלנומה אך עדיין לא אושרו להתוויה זו, ואלה כוללים את האימונותרפיות Pembrolizumab ו-Nivolumab ואת הטיפול המשולב ממוקד המטרה Dabrafenib ו-Trametinib.
הטיפול המשולב של דבראפניב וטרמטיניב הוא טיפול פומי מוכוון-מטרה. ל-40–50 אחוזים מחולי המלנומה יש מוטציה בגן BRAF הפועל במסלול התאי MAP. מוטציה בגן זה גורמת להתחלקות תאית בלתי מבוקרת וכד מביאה להתפתחות גידול סרטני. לפני מספר שנים פותחה קבוצת תרופות המתמקדות במוטציות בגן BRAF, מנטרלות את המוטציה ומביאות לחלוקה תאית מווסתת. התרופה הראשונה ממשפחה זו שפותחה הייתה Vemurafenib והשנייה הייתה דבראפניב.
חוסמי ה-BRAF, וומורפניב ודבראפניב, חוללו מהפכה ושיפרו באופן ניכר את שיעורי התגובה לטיפול, ההישרדות ללא התקדמות וההישרדות הכללית בקרב מטופלים עם מלנומה גרורתית ומוטציה בגן BRAF. עם זאת, במהרה התפתחה עמידות נרכשת לחוסמי BRAF, על ידי שפעול מסלול MAP kinase. עמידות זו קיצרה את ההישרדות ללא התקדמות ל-6–8 חודשים בלבד. כמו כן, השימוש בחוסמי BRAF נקשר להתפתחות גידולים עוריים משניים עקב שפעול פרדוקסלי של מסלול MAP kinase בתאים ללא מוטציה בגן BRAF. על מנת לעקוף את מגבלות המונותרפיה עם חוסמי BRAF, ניתנות שתי תרופות הפועלות על מסלול מטבולי שונה: דבראפניב עוצרת את הפעילות הממאירה של המוטציה בגן BRAF וטרמטיניב עוצרת את הפעילות של גן אחר, MEK. שילוב תרופתי זה מעכב את התפתחות העמידות התרופתית, מפחית את ההיארעות של גידולים עוריים הקשורים לטיפול ומנגד, משפר את ההישרדות ללא התקדמות המחלה. השילוב של דבראפניב עם טרמטיניב מהווה טיפול נוח עם היענות גבוהה, שכן הוא פומי ואין צורך בזריקות או ניטור קפדני של רמות התרופה.
מחקר שפורסם בשנת 2015 הוכיח כי בעוד שחציון ההישרדות הכללית של למעלה מ-400 מטופלים עם מלנומה בשלבים III—IV היה ממושך עם דבראפניב ועמר על שנה וחצי, הוספת טרמטיניב לרבראפניב הביאה להארכת חציון ההישרדות הכללית ב-6.5 חודשים, בעוד ששיעור תופעות הלוואי החמורות היה דומה בשתי קבוצות המטופלים. בנוסף, כפי שנמצא במחקר אחר שפורסם באותה שנה, טיפול משולב בדבראפניב עם טרמטיניב עבור מלנומה בלתי נתיחה או גרורתית מביא לשביעות רצון גבוהה מצד המטופלים, שנהנים מאיכות חיים טובה יותר הקשורה לבריאות הכללית וספציפית לסרטן וגם ליכולת תפקודית גבוהה יותר בהשוואה למטופלים המקבלים מונותרפיה עם חוסם BRAF.
דבראבניב וטרמטיניב אושרו לשימוש כמשלב על ידי ה-FDA (Food and Drug Administration) ונכנסו לסל התרופות עבור מטופלים עם מלנומה גרורתית ומוטציה בגן BRAF. הטיפול המשולב הביא אף להעלמת גרורות במטופלים עם מלנומה. באפריל 2018 אישר ה-FDA את השימוש בדבראפניב וטרמטיניב עבור מטופלים עם מלנומה בשלב III ומוטציות V600E או V600K בגן BRAF הנמצאים בסיכון גבוה לפתח גרורות.
האישור התבסס על מחקר מחקר פאזה III מבוקר, כפול סטיות בחלוקה אקראית שכלל 870 חולים במלנומה שלב III עם מוטציה BRAF מסוג V600E או V600K מעל גיל 18, אשר עברו כריתה מלאה של הגידול. המחקר נערך ב-169 מרכזים ב-26 מדינות, מינואר 2013 ועד דצמבר 2014 וכלל שתי זרועות טיפול: זרוע אחת (438 חולים) קיבלה טיפול משולב בדבראפניב וטרמטיניב למשך 12 חודשים, וזרוע הביקורת (432 חולים), טופלה בטבליות תואמות של פלצבו למשר 12 חודשים.
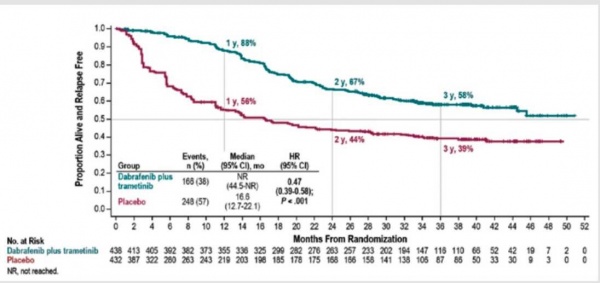
בזמן פתיחת נתוני המחקר (data cut off), לאחר זמן מעקב חציוני של 2.8 שנות מעקב, הישנות המחלה דווחה ב-37 אחוזים (163 חולים מתור 438) מהחולים שנכללו בזרוע הטיפולית של המחקר וב-57 אחוזים (247 מתוך 432 חולים) בקבוצת הביקורת.
לפי תוצאות המחקר, טיפול משלים בשילוב התכשירים למשר 12 חודשים מיום הניתוח הביא להורדת הסיכון להישנות המחלה ב-53 אחוזים (המטרה הראשונית של המחקר). כמו כן הטיפול הביא להורדת הסיכון למוות ב-43 אחוזים בתום 3 שנים.
שיעור החולים ללא הישנות המחלה (RFS) בזרוע ההתערבות דבראפניב עם טרמטיניב היה 88 אחוזים בשנה הראשונה, 67 אחוזים בשנה השנייה, 58 אחוזים בשנה השלישית, לעומת קבוצת הביקורת בה שיעור החולים ללא הישנות המחלה היה 56 אחוזים בשנה בראשונה, 44 אחוזים בשנה השנייה, 39 אחוזים בשנה השלישית. שיעור ההישרדות (OS - Overall Survival) בזרוע ההתערבות דבראפגיב בשילוב טרמטיניב היה 97 אחוזים בשנה הראשונה, 91 אחוזים בשנה השנייה, 86 אחוזים בשנה השלישית, לעומת קבוצת הביקורת בה שיעור ההישרדות היה 94 אחוזים בשנה הראשונה, 83 אחוזים בשנה השנייה ו-77 אחוזים בשנה השלישית.
תופעות הלוואי של הטיפול המשולב כוללות חום החולף בתוך מספר ימים ואינו דורש את הפסקת טיפול קבועה, עייפות, בחילה וכאבי ראש.
דבראפניב בשילוב טרמטיניב מפחיתים באופן משמעותי את הסיכון להישנות המחלה ביחס לפלצבו בחולי מלנומה שלב III הנושאים מוטצית BRAF V600E/K עם סיכון גבוה להישנות המחלה.
הטיפול המשולב הביא לשיעורי תגובה גבוהים גם מחוץ לעולם המחקר, בקרב מטופלים שלא תמיד עונים על קריטריוני ההכללה של מחקרים קליניים. מחקר איטלקי שכלל 66 מטופלים עם מלנומה גרורתית מצא כי דברפניב בשילוב טרמטיניב הביאו למחלה יציבה בקרב 72 אחוזים מהמטופלים ולתגובה מלאה בקרב 12 אחוזים. במחקר תצפית אחר הטיפול המשולב הביא לתגובה בקרב 90 אחוזים מהמטופלים ושיעורי ההישרדות הכללית עמדו על 60 אחוזים לאחר שגה ו-36 אחוזים לאחר שנתיים.
בשנת 2017 אושר הטיפול הכפול עבור סרטן ריאות גרורתי של תאים שאינם קטנים (NSCLC - Non-Small Cell Lung Cancer) עם מוטציה בגן BRAF, במאי 2018, מספר ימים לאחר אישור הטיפול המשולב כטיפול משלים לחולי שלב III הנושאים מוטצית BRAF V600E/K, אושר השימוש המשולב בדברפניב וטרמטיניב לטיפול בסרטן אנאפלסטי של בלוטת התריס עם מוטציה בגן BRAF, סוג סרטן אלים במיוחד. אישורים אלו התבססו על תוצאות מחקרים שהראו כי גם בסוגי סרטן אלו, דבראפניב וטרמטיניב מביאים לשיעורי תגובה גבוהים ושיפור בהישרדות, ללא החמרה בפרופיל הבטיחות המוכר. שיעור הגידולים עם מוטציה בגן BRAF גבוה יותר במלנומה מאשר בסרטן בלוטת התריס ובסרטן ריאות. אנו רואים מגמה דומה לזו שנצפתה עם אימונותרפיות כגון פמברוליזומאב (Keytruda - Pembroiozumab), אשר אושרה קודם לטיפול במלנומה מתקדמת ולאחר מכן התוויית הטיפול הורחבה לגידולים מוצקים נוספים.
השלב הבא בטיפול הרפואי והמניעתי במלנומה מתקדמת צפוי להיות שילוב של טיפולים ממוקדים ואימונותרפיה. בפעילות המשותפת של דבראפניב וטרמטיניב להשגת שליטה מהירה במחלה עם שיעורי תגובה גבוהים בקרב מטופלים עם מלנומה מתקדמת, הם מספקים מצע נוח לפעילות אנטי-סרטנית חיסונית. לא זאת בלבד שאין לשילוב תרופתי זה השפעה שלילית על מערכת החיסון, אלא גם שהם יוצרים מיקרו-סביבה המעודדת פעילות חיסונית באזור הגידול, מגבירים את הסתננות תאי מערכת החיסון לגידולים ומשפרים את זיהוי תאי המלנומה על ידי תאים אפקטוריים ואת התפקוד העוקב של התאים האפקטוריים.
אנו מקווים כי טיפול משולש של חוסם BRAF, חוסם MEK ואימונותרפיה יביא לקפיצת מדרגה נוספת בטיפול ובמניעת התקדמות של מלנומה.
ביבליוגרפיה
- Depenni R De Rosa F, Greco S et al (2018). Dabrafenib-trametinib combination in 'field-practice': an Italian experience. Future Oncol. 2018 Aug; 14(20):2045-2052.
- Grob JJ, Amonkar MM, Karaszewska B etal (2015). Comparison of dabrafenib and trametinib combination therapy with vemurafenib monotherapy on health-related quality of life in patients with unresectable or metastatic cutaneous BRAF Val600-mutation-positive melanoma (COMBI-v): results of a phase 3, open-label, randomisea trial. Lancet Oncol. 2015 Oct;16{13):1389-98.
- Kuske M1, Westphal D2, Wehner R et al (2018). Immunomodulatory effects of BRAF and MEK inhibitors: Implications for Melanoma therapy. Pharmacol Res. 2018 Aug 23:136:151-159.
- Long GV, Hauschild A, Santinami M et al (2017). Adjuvant Dabrafenib plus Trametinib in Stage II BRAF-Mutated Melanoma. N Engl J Med. 2017 Nov 9;377(19):1813-1823.
- Long GV, Stroyakovskiy D, Gogas H et al (2015). Dabrafenib and trametinib versus dabrafenib and placebo for Val600 BRAF-mutant melanoma: a multicentre, double-blind, phase 3 randomised controlled trial. Lancet. 2015 Aug 1:386(9992)444-51.
- Martin Algarra S1, Soriano V2, Fernandez-Morales L et al (2018). Dabrafenib plus trametinib for compassionate use in metastatic melanoma: A STROBE-compliant retrospective observational postauthorization study. Medicine (Baltimore). 2017 Dec;96(52):e9523.
- RobertC1, Karaszewska B, Schachter J etal (2015). Improved overall survival in melanoma with combined dabrafenib and trametinib. N Engl J Med. 2015 Jan 1;372(1):30-9.
המידע שבדף זה נכתב על ידי פרופסור יעקב שכטר מנהל מכון אלה לאימונו-אונקולוגיה, מומחה באונקולוגיה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק