הידרוצפלוס נורמוטנסיבי - Normal pressure hydrocephalus
הופניתם מהדף Normal pressure hydrocephalus לדף הנוכחי.
| הידרוצפלוס תקין-לחץ | ||
|---|---|---|
| Normal pressure hydrocephalus | ||
| שמות נוספים | NPH | |
| ICD-10 | Chapter G 91.2 | |
| ICD-9 | 331.9
, 331.5 |
|
| MeSH | D006850 | |
| יוצר הערך | ד"ר אחינועם סוחר, ד"ר גליה צרפתי, ד"ר זאב פלדמן, ד"ר שרון חסין (בר) | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – הידרוצפלוס, שיטיון
הידרוצפלוס תקין-לחץ (NPH ,Normal Pressure Hydrocephalus) הוא מצב רפואי המאופיין בטריאדה של הפרעת הליכה, ירידה קוגניטיבית והפרעה בשליטה על סוגר השתן, המלווה בלחץ תוך-גולגולתי תקין או נמוך. מאז שהוגדרה תסמונת NPH בשמה על ידי חאכים ואדאמס בשנת 1965, הועלו ספקות וחילוקי דעות באשר לפתוגנזה, הגדרת התמונה הקלינית ודרכי האבחון שלה. ספקות אלה טרם יושבו עד כה, ונותרה תמונה קלינית לא מאד מוגדרת, אך כזו שטומנת בחובה אפשרות טיפולית ממשית לחולה המבוגר שסובל מהתסמינים האופייניים.
הידרוצפלוס כרוני במבוגר, המוגדר לפי קריטריונים הדמייתיים שונים, כולל את המצבים הבאים: הידרוצפלוס מולד שנעצר (Compensated/arrested congenital hydrocephalus), היצרות תעלה של הגיל המבוגר (Adult-onset aqueductal stenosis), וכן שני סוגים של NPH:
- NPH ראשוני (אידיופתי): כאשר לא ניתן לזהות גורם מקדים ידוע.
- NPH שניוני: מקרים בהם יש סיבה ידועה שגרמה להתפתחותו (כגון סיפור קודם של דלקת קרומי המוח, דמם תוך מוחי, טראומה מוחית ועוד).
חולים מבוגרים או קשישים אשר סובלים מהתסמונת המוכרת של NPH עשויים להגיע לכדי נכות קשה ובלתי הפיכה אם לא יטופלו במועד. אבחון נכון וזיהוי של החולים אשר עשויים להשתפר עם הטייה של נוזל המוח והשדרה (CSF, Cerebrospinal Fluid) ממערכת החדרים לחלל הצפק על ידי טיפול ניתוחי מוקדם עם השתלת מערכת ניקוז מתכווננת מהווה פתרון עבור חולים נבחרים.
אפידמיולוגיה
טרם התקבל מידע מהימן ומספק אודות שכיחות NPH. נתונים משבדיה מצביעים על היארעות הידרוצפלוס כרוני במבוגרים של 2.6 ל-100,000 לשנה ונתונים מנורבגיה מצביעים על שכיחות של 0.1% באנשים מגיל 60 ומעלה, שמכפילה את עצמה בכל עשור. מקובל להתייחס לשכיחות NPH כ-5% מכלל המקרים של דמנציה, אך נראה שמדובר בתת-הערכה של התופעה, שכן רבים מחולי NPH אינם לוקים בדמנציה ומתייצגים כהפרעת הליכה בלבד.
אטיולוגיה
קיימות מספר תיאוריות בנוגע לפתוגנזה של NPH אך אף אחת לא מסבירה באופן מלא את התסמונת. הגדלת חדרי המוח אינה מספיקה, כשלעצמה, לגרום לתסמינים של NPH; דוגמה לכך היא אותם חולים עם הגדלת חדרים משנית למומים מולדים כמו היצרות התעלה על שם סילביוס, אשר אינם סובלים מכל ליקוי נוירולוגי.
הסבר להתפתחות של הידרוצפלוס כרוני תסמיני דורש להכיר את השינויים ברקמת המוח ובהידרו-דינמיקה של CSF המתרחשים בהקשר של תהליכי הזדקנות רגילה ובמחלות כלי-הדם של המוח. קיימות עדויות לירידה בביטויו של אקוופורין 1 (תעלת מים שמבוטאת על הקוטב האפיקלי של תאי האפיתל במקלעת הדמית ומווסתת את מעבר המים לחדרים) במצבים פתולוגיים בהם יש הפרעה בפרפוזיה המוחית. ירידה זו יכולה להוות מנגנון בקרה על ייצור CSF. קצב ייצור ה-CSF על ידי המקלעת הדמית יורד עם הגיל, ירידה הבולטת במיוחד במצבים כמו הידרוצפלוס כרוני ומחלת אלצהיימר. באופן תקין, ה-CSF מופרש בכמות כמעט כפולה בלילה לעומת הייצור ביום; בקשישים, שינויים במחזור ערנות-שינה וכן הקטנת הפרפוזיה למקלעת הדמית יכולים להסביר באופן חלקי את הירידה בייצור CSF. הסבר אפשרי נוסף לירידה זו הוא העלייה ברמות ואזופרסין (חלבון שמעורב בבקרה על ייצור CSF) שמתרחשת עם הגיל.
בנוסף להפחתת הייצור, ישנן עדויות להפרעה בספיגת CSF הקשורה גם היא לשינויים של הגיל המבוגר: עיבוי (פיברוזיס) של הקרום העכבישי, שקיעה של עמילואיד מסוג בטא בקרומי המוח ועלייה בלחץ הוורידים הקורטיקליים.
קיימת סברה שירידה במחזור (Turnover) של CSF מפריעה לפינוי חומרים שהצטברותם עלולה לגרום לנזק מוחי, כגון עמילואיד מסוג בטא. גם ריכוזים של חומרים בעלי תכונות נוגדות חמצון וחומרים נוירו-פרוטקטיביים אחרים שבקרתם ושינועם תלוי במקלעת הדמית נפגעים במוח המזדקן. בהידרוצפלוס כרוני קיים, ככל הנראה, תהליך מוקדם ומוגבר של הצטברות חומרים פתולוגיים במוח מחד גיסא, וירידה בחומרים המגנים מאידך גיסא, שתורמים במשותף לנזק המוחי שמביא לביטויים קליניים בכלל ולירידה הקוגניטיבית בפרט [1].
גם בהזדקנות וגם במצבי הידרוצפלוס יש ירידה בקצב ספיגת ה-CSF דרך הסיסים העכבישיים ויש יתר חשיבות למסלולים עקיפים כדוגמת ספיגה טראנס-אפנדימלית מחדרי המוח. הדבר קשור, כנראה, לשינויים ניווניים בכלי הדם במוח שקורים עם הגיל. ישנן עדויות מוצקות לקשר שבין הידרוצפלוס כרוני תסמיני ומחלות כלי הדם של המוח, ובפרט על זיקה חזקה ליתר לחץ דם. סתימה של עורקיקים מוחיים מביאה לסגירת הוורידים המנקזים, דבר התורם להפרעה בספיגת CSF. בנוסף יש לציין כי חומרת השינויים האיסכמיים בחומר הלבן העמוק על-פי הדמיה, נמצאת ביחס הפוך לשיפור המתרחש לאחר הכנסת דלף חדרי-צפקי (Ventriculoperitoneal shunt).
קליניקה
קיום בו-זמני של ירידה קוגניטיבית, הפרעת הליכה וקושי בשליטה בסוגר השתן הוא שילוב קליני לא נדיר במחלות מוח של הגיל המבוגר, כמו למשל מחלת פרקינסון מתקדמת או מחלת כלי דם קטנים של המוח, אך חשוב להכיר את המאפיינים הספציפיים של התסמונת ולזהותם. יחד עם זאת, ראוי לציין ש-NPH יכול ללוות מחלות נוירולוגיות אחרות, כדוגמת מחלת אלצהיימר, שבץ מוח בעבר ועוד, וקיומן אינו שולל מראש את קיומו של מרכיב של NPH [2][3].
הפרעת הליכה
הפרעת הליכה היא לרוב התסמין המוקדם ביותר אצל חולים עם NPH, ותסמין זה יכול להופיע באופן מבודד. הפרעת ההליכה היא התסמין בעל הסיכוי הרב ביותר להשתפר לאחר טיפול בדלף חדרי-צפקי [3]. ככל הנראה הבסיס להפרעה הוא פגיעה במסלולים קדם-תנועתיים (Premotor) ולא מעורבות של מסילות פירמידליות במוח, שעשויה לקרות בשלבים מאוחרים. הפרעת ההליכה עשויה להיות קשורה גם לפגיעות בגרעיני הבסיס, כולל החומר השחור (Substantia nigra).
סטולצה ועמיתיו אפיינו את הפרעת ההליכה ב-NPH בעזרת מדדים שנאספו מבדיקות במעבדת הליכה: בהשוואה להליכה של אנשים תואמי גיל בריאים, מהירות ההליכה בחולים עם NPH הייתה נמוכה יותר, אורך הצעדים היה קצר יותר, אורך שלב הדריכה בהליכה (Stance) ושלב התמיכה על ידי שתי רגליים היה ארוך יותר, ואצל מספר נבדקים נצפתה "קפיאה" (Freezing) תוך כדי ההליכה. רוחב הצעד היה גדול יותר בקבוצת ה-NPH (הרחבת בסיס ההליכה) עם שינויים במנח וזוויות המפרקים של הרגליים, המתבטאים ברוטציה חיצונית של כף הרגל בזמן ההליכה. המחקר גם אפיין את דפוס השיפור במדדי ההליכה לאחר ניקור מותני והוצאה של 30 מילי-ליטרים (מ"ל) של CSF וציין שיפור ניכר במדדים הבאים בלבד: מהירות ההליכה (עליה ב-23.9%), אורך הצעדים (עלייה ב-20.9%), שלב התמיכה על ידי שתי רגליים בהליכה (ירד ב-16.4%), שלב הדריכה (ירד ב-8.9%) ועלייה בשלב ההנפה (Swing). לא נמצאו הבדלים משמעותיים במדדי הליכה תלויי שיווי משקל (רוחב בסיס וזוויות כפות הרגליים) אחרי ניקוז הנוזל [4].
במחקר אחר שהתמקד בהפרעות שווי משקל ב-NPH, השוו החוקרים קבוצה של חולי NPH לעומת חולים עם פגיעה מוחית על רקע מחלת כלי דם קטנים של המוח (אנצפלופתיה תת-קליפתית טרשתית) ונבדקים בריאים. מדדי יציבה נבדקו ליד מיטת החולה וכן על ידי בדיקת FP (Force Platform). החוקרים מצאו דמיון רב בדפוס ההפרעה בתפקוד התנועתי ובשיווי המשקל בין שתי קבוצות החולים, בשונה מהבריאים.
בבדיקת FP שיווי המשקל הלקוי אופיין בקבוצת ה-NPH על ידי הסטה גדולה יותר של מרכז הכובד במישור הפרונטלי, יחס סגיטלי/פרונטלי נמוך, שטח טלטול הגוף (Sway area) גדול יותר, מהירות גבוהה לאחור והטיה קדמית של הגוף יחסית לנבדקים בריאים. לאחר ניקור מותני נראה שיפור בהטיית הגוף, בשטח טלטול הגוף ובהסטה הסגיטלית [5]. במקרים מסוימים חורגת הפרעת התנועה המלווה NPH מהפרעת הליכה וכוללת אף סימנים פרקינסוניים, בין היתר ברדיקינזיה, רעד, נוקשות - עם או ללא מרכיב דמוי "גלגל שיניים" (Cogwheel), ירידה בטלטול ידיים, הליכה מכופפת, פסטינציה, הטיה אחורנית (Retropulsion) ועוד. לעתים תסמינים אלה עשויים להגיב לטיפול דופמינרגי ולעתים לטיפול בדלף חדרי-צפקי.
סימנים פירמידליים לעומת זאת אינם נפוצים בחולי NPH, ולרוב אין חולשת רגליים בבדיקה נוירולוגית [2].
הפרעה בשליטה על סוגר השתן
הפרעה בשליטה על מתן שתן אינה נדירה בגיל המבוגר וקשורה לגורמים רבים; בגברים היא קשורה, בין היתר, להגדלה שפירה של הערמונית וחסימת מוצא השלפוחית, הפרעות לב וכלי דם ותרופות המשפיעות על מערכת השתן, ובנשים — לצניחה של הרחם והשלפוחית.
ב-NPH, אי ספיקת שלפוחית השתן היא תסמין מאוחר יחסית המתבטא בדחיפות במתן שתן, תכיפות יתר בהטלת השתן ולעתים גם באי-נקיטה. על סמך בדיקות אורודינמיות נמצא שהדבר נובע מפעילות יתר של שריר הדטרוסור, ככל הנראה עקב פגיעה במסלולים סביב החדרים למקלעת הסקרלית המעצבב את השלפוחית [3].
כאשר חולה עם NPH מוגבל בהליכתו, הקשיים התנועתיים תורמים אף הם לבריחת השתן כי החולה אינו מצליח להגיע לשירותים בזמן ולהתרוקן. בחולה מתקדם עם דמנציה משמעותית, קיימת תרומה של המצב הקוגניטיבי מכיוון שהחולה אינו מוטרד או שאינו מודע לבריחת השתן. פוג׳ארי וחבריו בדקו תוצאות קליניות ארוכות טווח של הכנסת דלף חדרי-צפקי בחולי NPH ומצאו שיפור של 84% בתסמינים האורינריים לאחר כשלוש שנים מהטיפול, וכ-80% שיפור לאחר שבע שנים. השיפור הוגדר כירידה בתדירות, בדחיפות ובבריחות שתן שדווחו על ידי החולה ומשפחתו [6].
ירידה קוגניטיבית
ב-NPH ניתן למצוא טווח רחב של הפרעות קוגניטיביות, החל בפגיעה תת קלינית וכלה בדמנציה גלובלית קשה. ככל שהירידה הקוגניטיבית מתקדמת היא הופכת להיות פחות ממוקדת ויותר עמידה לטיפול הכירורגי. נראה שהירידה הקוגניטיבית קשורה לשינויים וסקולריים או ניווניים, בנוסף לשינויים המטבוליים ההפיכים משנית להידרוצפלוס.
התחומים הקוגניטיביים הפגועים בחולים עם NPH אידיופתי שתוארו עד כה כוללים תפקודי קשב וריכוז, מהירות פסיכומוטורית, יכולות ראייתיות-תפיסתיות, יכולות קונסטרוקציה, יכולות למידה וזכירה, הבנה מרחבית, חישובים, קריאה, כתיבה, פתרון בעיות, קונספטואליזציה, חשיבה מופשטת ותפקודים ניהוליים. בחולים עם מבחן קצר לאבחון מנטלי (MMSE ,Minimental test) בגבולות התקין ניתן עדיין להתרשם מקיומה של פגיעה קוגניטיבית עם תבנית של פגיעה תת-קליפתית עם מרכיב פרונטלי בולט: ירידה בקשב, הפרעה בביצוע מטלות עיבוד מידע מורכבות, תכנון, יוזמה, קבלת החלטות וכיוצא בזה. בשונה ממחלת אלצהיימר, הפגיעה בזיכרון בולטת יותר בשליפה מאשר בקידוד ובזיהוי [2][3][7].
בחולים עם NPH שטופלו על ידי דלף חדרי-צפקי נמצא שיפור נוירופסיכולוגי בולט (80.8%) ברוב המבחנים בהם היו ליקויים, אך השיפור לא הביאם לרמה של אוכלוסיה בריאה [8]. במחקרו של פוג'ארי מ-2008, נבדקה יעילות הטיפול בדלף חדרי-צפקי לגבי התסמינים הקוגניטיביים של NPH על ידי שימוש במבחן MMSE (שיפור הוגדר כעלייה בשלוש נקודות ומעלה ב-MMSE), וכן על ידי שאלונים בנוגע לשינויים הקוגניטיביים שמולאו על ידי המטופלים ובני משפחותיהם. נמצא כי היה שיפור מתמשך במדדים הקוגניטיביים אצל כ-84% מהמטופלים לאחר שלוש שנים וב-86% מהמטופלים שהמשיכו מעקב גם לאחר שבע שנים [6]. מתוך התרשמות כללית ניתן לסכם שלפחות 50% מהחולים עם NPH אידיופתי משתפרים בתפקודים הקוגניטיביים כתוצאה מטיפול בדלף חדרי-צפקי.
לאחרונה נחקר המתאר של הפרעות ההתנהגות בחולי NPH (64=n) ובין היתר הושווה לזה שבמחלת אלצהיימר (126=n) בעזרת ה-Neuropsychiatry Inventory. החוקרים מצאו שב-NPH ההפרעה השכיחה ביותר הייתה אפאתיה (70.3%) ולאחריה חרדה (25%). בסך הכל, הפרעות ההתנהגות היו שכיחות יותר בחולים עם מחלת אלצהיימר (91.3% לעומת 73.4%). לאחר טיפול כירורגי נצפה אמנם שיפור במדדי ההתנהגות אך הוא לא היה מובהק סטטיסטית [9].
בשני מחקרים שפורסמו בשנת 2010 ב-Annals of Neurology, בדקו חוקרים מפינלנד ומפנסילבניה חולים החשודים ל-NPH שעברו במסגרת הבירור ביופסית מוח, ובחנו את הקשר בין שינויים נוירופתולוגיים האופייניים למחלת אלצהיימר לבין הסיכוי להשתפר עם דלף חדרי-צפקי. נמצא, שנוכחות שינויים אלה מורידה את הסיכוי לשיפור מתמשך בעקבות הטיפול בדלף [10].
אבחנה
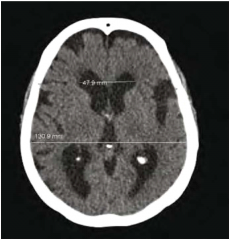
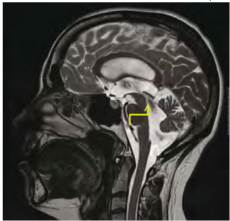
למבוגרים אשר מפתחים הידרוצפלוס בשנות חייהם המתקדמות יש כנראה יותר מנגנוני פיצוי אשר מונעים עלייה מסוכנת בלחץ התוך-גולגולתי מאשר לילדים וההידרוצפלוס מתפתח אצלם יותר באיטיות. הידרוצפלוס כרוני הוא מצב המוגדר הדמייתית בבדיקות טומוגרפיה ממוחשבת (CT ,Computed Tomography) ו/או תהודה מגנטית (MRI ,Magnetic Resonance Imaging) על ידי אומדן הגדלת החדרים. אחד המדדים לגודל החדרים הוא Evans index, היחס בין רוחב הקרניים המצחיות לרוחבו המירבי של המוח. בהידרוצפלוס כרוני מדד זה יהיה גדול מ-0.3 (תמונה מספר 1). מדדים הדמייתיים נוספים הם הרחבת הקרניים הרקתיות, שינויי אות או בצקת סביב חדרי המוח ושינויים באות הזרימה בתעלה (Aqueductal/fourth ventricular flow void) (תמונה מספר 2), בנוכחות לחץ CSF תקין או מעט גבוה. התמונה ההדמייתית מלווה בהתפתחות של תסמינים קליניים דומים, ללא קשר לגורם הראשוני.
בשנת 2004, ביפן, נקבעו הנחיות לאבחנה וטיפול בחולי NPH [11]. ההמלצות כללו:
- MRI מוח: התייחסות למדדים הדמייתיים שניתן לראות בחתכים קורונליים הכוללים קמירות גבוהה והרחבה של התעלה על שם סילוויוס, בנוסף להרחבה קלה-בינונית של מערכת החדרים.
- בדיקת ניקור מותני: הליך אבחנתי פשוט יחסית שבו מעריכים את החולה מבחינה קלינית (מהירות ההליכה, איכותה והתפקוד הקוגניטיבי) לפני ניקור מותני ולאחריו עם ניקוז חיצוני של CSF בכמות של 50-30 מ"ל; בדיקה זו היא בעלת ערך ניבוי גבוה ליעילות של מערכת דלף בעתיד.
בשנת 2005 התפרסם מחקר שכלל סקירת 653 מאמרים קליניים על NPH שהיוו בסיס להנחיות לאבחנה של NPH אידיופתי. במחקר זה נקבעו שלוש דרגות אבחנה: סבירה (Probable), אפשרית (Possible) או בלתי סבירה (Unlikely) על פי אנמנזה, הדמיה מוחית, והסתמנות קלינית הכוללת בדיקה נוירולוגית וקוגניטיבית [2]. סיכום של בדיקות העזר לאבחון NPH מובא בטבלה מספר 1.
| עקרון | פעולה | פרטי השיטה | מדדים | אמינות בניבוי שיפור עם התקנת דלף חדרי-צפקי |
| ניקוז חיצוני של CSF | ניקור מותני | הוצאה חד-פעמית של 50-30 מ"ל. הערכה קלינית לפני ההערכה וכן 60-30 דקות לאחריה ולמחרת | שינוי במהירות ההליכה ובאיכותה וכן בציונים במבחנים קוגניטיביים | כאשר נצפה שיפור בבדיקה, קיים סיכוי גבוה לשיפור עם דלף חדרי-צפקי |
| ניקוז חיצוני מתמשך (Continuous drainage) | ניקוז CSF לתוך שקית בקצב של 10-5 מ"ל בשעה (עד 200 מ"ל ביממה) הערכה במשך 7-2 ימים | שינוי במהירות ההליכה ובאיכותה וכן בציונים במבחנים קוגניטיביים | מעט אמין יותר מהניקור. סיכוי גבוה יותר לסיבוכים (דלקת קרום המוח) | |
| ניטור לחץ תוך-גולגולתי | שימוש במתמר תוך-גולגולתי | רישום של שינויי לחץ מחזוריים (Lundberg B waves) | תדירות גבוהה של גלים אלה היא ערך ניבוי חיובי לניתוחי דלף חדרי-צפקי | נמצא קשר סטטיסטי חלש בין תדירות הגלים לשיפור לאחר דלף חדרי-צפקי [12] |
| דינמיקה של CSF | הזלפת נוזלים לתוך השק התקאלי | הזלפת תמיסת מלח נורמלית, רינגר לקטט או CSF לתוך החלל התת-עכבישי. מודדים את הלחץ כאשר מגיעים לאיזון בין ספיגה והזלפה |
תנגודת גבוהה במבחני תנגודת CSF מנבאת שיפור לאחר התקנת דלף חדרי-צפקי | רגישות גבוהה יותר (100%-57%) מאשר בניקור מותני וערך ניבוי חיובי דומה [13] |
| ציסטרנוגרפיה | הזלפת חמר רדיו-איזוטופי לתוך הציסטרנה המותנית וצפייה בפיזורו בציסטרנות, בחדרים ומעל הכיפה | עדות לחזרה (Reflux) חדרית מלווה בתצרוכת קליפתית נמוכה | העדר צביעה לאחר 72 שעות מחשידה ל-NPH | מבחן לא אמין לניבוי שיפור לאחר הכנסת דלף חדרי-צפקי [3] |
| דימות מבני | CT או MRI של המוח | דימות מבני |
|
המדדים הללו חשובים לאבחנה סבירה של NPH אידיופתי |
| MRI | דימות מבני | Flow void של התעלה או של החדר הרביעי | ||
| דימות תפקודי | נפח פעימה (Stroke volume) — מוגדר כממוצע נפח ה-CSF העובר דרך התעלה בסיסטולה ובדיאסטולה. נפח פעימה מעל 42 מיקרוליטר יכול לנבא שיפור בתר-ניתוחי | יכול לשמש כמדד מנבא תומך להצלחת הניתוח |
הקריטריונים לאבחנה סבירה (Probable) של NPH אידיופתי
- אנשים בגיל מעל 40 עם התחלה הדרגתית של התסמינים על פני תקופה של שלושה חודשים לפחות.
- הסתמנות קלינית: הפרעת הליכה בתבנית המתאימה ל-NPH ובנוסף הפרעה לפחות באחד ממרכיבי הטריאדה הנוספים.
- על מנת לעמוד בקריטריונים להפרעה בשליטה בסוגר השתן מספיק דיווח על דחיפות או על תכיפות במתן שתן.
- הפרעה קוגניטיבית צריכה להתייצג כהפרעה בשני תפקודים קוגניטיביים לפחות, כגון: ריכוז, האטה פסיכומוטורית, תפקוד ניהולי ושינויי התנהגות.
- היעדר מחלת מוח אחרת או ממצא מוחי אחר שיסביר את התמונה הקלינית הרלוונטית.
- לחץ פתיחה של CSF בטווח של 245-70 מילימטר (מ"מ) מים.
- מדדים הדמייתיים הכוללים 0.3<Evans index, שינויי אות סביב החדרים, הגדלת קרניים רקתיות ועוד.
הקריטריונים לאבחנה אפשרית (Possible) של NPH אידיופתי
אלה כוללים את הקריטריונים האבחנתיים לרמה של אבחנה סבירה, ובנוסף:
- החולים בגיל מתחת 40.
- הסתמנות קלינית שנמשכת פחות משלושה חודשים.
- לחץ פתיחה של CSF אינו תקין או שאינו נמדד.
- קיימים תסמינים שאינם מתקדמים.
- עדות הדמייתית לניוון מוחי בדרגה חמורה מספיק על מנת לתרום לתמונה של הגדלת החדרים.
אבחנת NPH אינה סבירה כאשר קיים ממצא של בצקת דיסקות, הסתמנות קלינית שיכולה להיות מוסברת על ידי גורמים אחרים, היעדר הגדלת חדרים בהדמיה או הסתמנות קלינית לוקה בחסר לפי הטריאדה של חאכים [14].
כהמשך להנחיות אלו, הציעו ברגסניידר ועמיתיו שלא כל מטופל המאובחן באופן סביר או אפשרי עם NPH יזדקק להתקנת דלף. על אף שחולים רבים יפיקו תועלת מן הניתוח, עלולים להיות לפעולה זו גם סיבוכים לא מבוטלים. הם המליצו להתייחס לשכיחות הגבוהה של הסיבוכים ולנסות לחזות מראש האם הנזק שיצמח מהתערבות זו במקרה מסוים יהיה רב מן התועלת. מן הראוי שלמטופל תהיה נכות משמעותית שעשויה להשתפר ויכולת לעמוד בניתוח בהרדמה כללית [15].
טיפול
אין בנמצא טיפול תרופתי יעיל ב-NPH. הטיפול הניתוחי המקובל ביותר הוא התקנת דלף חדרי-צפקי. למרות שטיפול זה מקובל מזה שנים רבות, במאגר המידע של קוכריין ב-2002 לא נמצאו עדויות ברמה סבירה של ביסוס מדעי על יעילות מערכות לניקוז CSF מחדרי המוח עבור חולי NPH.
הומלץ על שימוש בדלף חדרי-צפקי מתכוונן (בעל שסתום שמונע מצבים של ניקוז יתר של CSF או תת-ניקוז), שניתן לשנות בו את לחץ הפתיחה על ידי שימוש לא פולשני במגנט חיצוני גם לאחר הניתוח [11].
התקנת דלף חדרי-צפקי
הניתוח להתקנת דלף חדרי-צפקי הוא פשוט וקצר. נקז חדרי מוחדר דרך חור מחדר, בדרך כלל באזור מצחי. הנקז מחובר לשסתום מתכוונן, ולחץ הפתיחה הראשוני נקבע בזמן הניתוח. הצינורית הרחיקנית מועברת תת-עורית לאזור הבטן, ושם מוחדרת לחלל הצפק. משך האישפוז הממוצע הוא 48 שעות, ובמהלך הביקורות בשבועות העוקבים, נבדק הצורך בהתאמת לחץ הפתיחה, וזאת למניעת ניקוז-יתר או תת-ניקוז העלולים לפגוע ביעילות הטיפול.
הסיבוכים המיידיים של הניתוח להתקנת דלף חדרי-צפקי כוללים את סיבוכי ההרדמה (כמו אוטם שריר הלב) ודימום מוחי חריף. במאמר רטרוספקטיבי על 36 חולי NPH אידיופתי, שכיחותו של דימום מוחי הייתה כ-3%, אך נטען כי קיימת תת-הערכה.
הסיבוכים המאוחרים כוללים זיהום של מערכת הדלף (19%-0% בסדרות שונות), פרכוסים (8%-0%), דמם או קולקציה תת-קשתית (53%-0%) ותפקוד לא תקין של הדלף. האחרון, שמתרחש ב-30%-0% מהמקרים, מתבטא, בין היתר, בכאבי ראש מתת-לחץ תוך-גולגולתי משני ליתר ניקוז, תת-ניקוז של המערכת או חסימה שלה [11][16].
בשנת 2002 פורסמה עבודה על הכנסת מערכת דלף עם שסתום מתכוונן ב-218 חולים עם NPH. שיעור הסיבוכים בעבודה זו היה 19.7%. הפרעה בתפקוד מערכת הדלף החדרי-צפקי נמצאה בשלושה חולים (1.3%), זיהום ב-6.4% ותפליט תת-קשתי ב-15%. התוצאות הקליניות לאחר הניתוח היו טובות או מצוינות ב-78.9% בקבוצת ה-NPH האידיופתי וב-69.8% בקבוצת ה-NPH השניוני [17].
פרוגנוזה
פוג'ארי ועמיתיו ערכו מחקר רטרוספקטיבי שסקר 55 מטופלים עם אבחנה של NPH אידיופתי שעברו ניתוח להכנסת דלף חדרי-צפקי, בתקווה למצוא מדדים לניבוי ההצלחה של הניתוח. המטופלים שנבחרו עמדו בהנחיות משנת 2005 של רלקין ועמיתיו לאבחנה סבירה של NPH. זמן המעקב הממוצע היה 5.9±2.5 שנים.
בעקבות הניתוח נמצא שיפור במידה קבועה בכל התסמינים שנבדקו (הליכה, קוגניציה, מתן שתן, כאבי ראש) ושיפור לאורך זמן בעיקר בקשיי ההליכה. ב-55% מהניתוחים הותקנה מערכת דלף עם שסתום מתכוונן ובשאר הניתוחים בכזו עם שסתום עם לחץ קבוע. לאחר הניתוח הראשוני היה שיפור ניכר בתסמינים ב-87% מהמטופלים. 52% מהמטופלים נזקקו לניתוח חוזר ויותר ממחציתם נזקקו לו יותר מפעם אחת. מתוך 62 ניתוחי תיקון של הדלף (חלקם בוצעו עם הטייה אדרית או הטייה לעלייה הלבבית) ניכר שיפור בתסמינים העיקריים ב-74%. החוקרים הסיקו כי ישנה תת קבוצה של מאובחני NPH שיכולים ליהנות משיפור ארוך טווח בתסמינים אפילו בטווח של עד שבע שנים. במחקר זה לא נמצאו מדדי ניבוי מובהקים סטטיסטית לשיפור לאחר הניתוח. שיעור ההצלחה הגבוה של הניתוחים יוחס לבחירה קפדנית של המטופלים וכן למעקב מסודר וקבוע המאפשר אבחון של כל תקלה במערכות הדלף [6].
עד היום לא נעשו מחקרי עוקבה המשווים את שיעור הסיבוכים בין דלף חדרי-צפקי עם שסתום מתכוונן לאלו עם שסתום שאינו מתכוונן בחולים עם NPH. על פי תוצאות של מחקרים רטרוספקטיביים וריבוי מקרים של בעיות בהטיית ה-CSF בעקבות ניקוז יתר וסיבוכיו או תת ניקוז ותגובה לא מספקת, קיימת עדיפות אינטואיטיבית להתקנת שסתום מתכוונן המאפשר התאמת לחץ הפתיחה לצרכי החולה. כ-50% מהחולים נזקקים להתאמת לחץ הפתיחה בשבועות שלאחר הניתוח [14][12].
במקרים בהם הסתמנות המחלה מתחילה עם הפרעת הליכה בולטת, ומשך ההסתמנות קצר (פחות מששה חודשים), הסיכוי לשיפור עם התקנת דלף עולה. לחולים עם NPH שניוני סיכוי טוב יותר מאשר עם NPH ראשוני להשתפר עם דלף. בחולים בהם חל שיפור עם הוצאת CSF (בניקור או בניקוז מתמשך) יש סיכוי טוב לשיפור עם דלף, אך העדר שיפור בעקבות ניקוז חיצוני אינו שולל שיפור לאחר התקנת דלף. לעומת זאת, בחולים עם דמנציה כהסתמנות ראשונית ו/או עיקרית, דמנציה בחומרה בינונית-קשה או דמנציה שנמשכת מעל שנתיים, הסיכוי לשיפור משמעותי עם דלף נמוך יותר. גם חולים המתייצגים ללא הפרעת הליכה וכאלה עם ממצאי MRI המעידים על שינויים בולטים בחומר הלבן וניוון משמעותי הם בעלי סיכוי נמוך יותר לשיפור.
ביבליוגרפיה
- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה1- ↑ 2.0 2.1 2.2 2.3 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה2- ↑ 3.0 3.1 3.2 3.3 3.4 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה3- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה4- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה5- ↑ 6.0 6.1 6.2 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה6- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה7- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה8- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה9- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה10- ↑ 11.0 11.1 11.2 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה11- ↑ 12.0 12.1 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה16- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה17- ↑ 14.0 14.1 שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה12- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה13- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה14- ↑ שגיאת ציטוט: תג
<ref>לא תקין; לא נכתב טקסט עבור הערות השוליים בשםהערה15
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר אחינועם סוחר, המחלקה לנוירולוגיה; המרכז הרפואי ע"ש שיבא, תל-השומר
ד"ר גליה צרפתי, מכון הדימות, המרכז הרפואי ע"ש שיבא, תל-השומר וביה"ס לרפואה ע"ש סאקלר, אוניברסיטת תל-אביב, תל-אביב
ד"ר זאב פלדמן, המחלקה לנוירוכירורגיה, המרכז הרפואי ע"ש שיבא, תל-השומר וביה"ס לרפואה ע"ש סאקלר, אוניברסיטת תל-אביב, תל-אביב
ד"ר שרון חסין (בר), המחלקה לנוירולוגיה ומרפאת פרקינסון והפרעות תנועה, המרכז הרפואי ע"ש שיבא, תל-השומר וביה"ס לרפואה ע"ש סאקלר, אוניברסיטת תל-אביב, תל-אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק