סולפהמוגלובין - Sulphemoglobin
הופניתם מהדף Sulfhemoglobinemia לדף הנוכחי.
| מדריך בדיקות מעבדה | |
| סולפהמוגלובין | |
|---|---|
| Sulphemoglobin | |
| שמות אחרים | sulfHb, Sulfhemoglobin |
| מעבדה | המטולוגיה בדם. |
| תחום | ציאנוזיס כתוצאה מ-sulphemolobin. |
| טווח ערכים תקין | שלילי |
| יוצר הערך | פרופ' בן-עמי סלע |
כללי
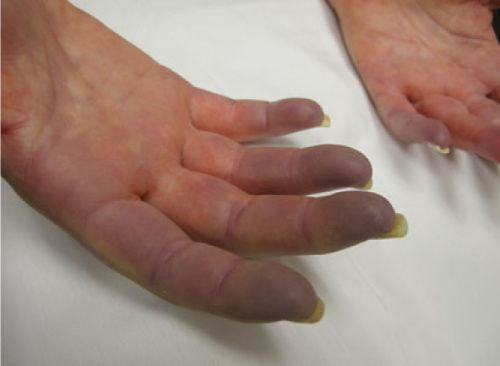
תרחיש של sulphemoglubinemia נדיר ובו עודף של Sulfhemoglobin (להלן SulfHb) בדם. פיגמנט זה הוא נגזר ירקרק של המוגלובין שאינו יכול להיות מוסב בחזרה להמוגלובין נורמלי ומתפקד. הוא גורם לציאנוזיס אפילו ברמות נמוכות בדם. תרחיש זה בו טבעת β-pyrrole של מולקולת המוגלובין היא בעלת היכולת לקשור באופן בלתי-הפיך לכל תרכובת המכילה אטום גפרית (Gharahbaghian וחב' ב-Western J Emergency Med משנת 2009). כאשר גפרית מימנית (H2S) או יוני גפרית ויוני ברזל דו-ערכי מתחברים ב-heme של המוגלובין, הדם אינו מסוגל להעביר חמצן לרקמות. התסמינים כוללים גוון ירקרק-כחלחל של הדם (ציאנוזיס), של העור, ושל ממברנות ריריות, זאת אף על פי שספירת הדם יכולה להיות תקינה. השינוי בגוון נגרם על ידי רמה של deoxyhemoglobin הגבוהה מ-5 גרם/דציליטר, או מרמה של 1.5 גרם/דציליטר של methemoglobin, או מ-0.5 גרם/דציליטר של SulfHb, כאשר כל אלה הם אנומליות קליניות חמורות.
סיבות
תרחיש של sulfhemoglubiniemia בדרך כלל נגרם על ידי טיפול תרופתי עם תרופות הכוללות סולפונאמידים כגון sulfasalazine או sumatriptan. סיבה אפשרית נוספת היא בחשיפה תעסוקתית לתרכובות גפרית. התרחיש יכול להיגרם גם על ידי phenazopyridine (Gopalachar וחב' ב-Ann Pharmacother משנת 2005). בנוסף לציאנוזיס ועצירות. המוגלובין א-נורמלי זה מורחק מהצירקולציה רק כאשר האריתרוציטים מגיעים לסוף חייהם אחרי 120 יום.
טיפול
התרחיש בדרך כל מתפוגג בעצמו עם משך חיי האריתרוציט, אם כי עירוי דם יכול לסייע. מצב זה יכול לנבוע משימוש כרוני בתרופות כגון acetanilide או phenacetin.
היסטוריה
תרחיש של Sulfhemoglobinemia תואר לראשונה בשנת 1863 על ידי הפתולוג הגרמני Felix Hoppe-Seyler, שהבחין בפיגמנט הירקרק היציב בדגימות דם, והוא ייחס זאת לראשונה לאינטראקציה של מימן סולפידי עם המוגלובין. תצפית זו הייתה ההכרה המוקדמת ביותר של sulfhemoglobinemia, אם כי האופי המדויק שלה נותר בלתי ברור עשרות שנים. המושג "sulfhemoglobin" נקבע בסוף המאה ה-19 והופיע לראשונה בספרות המדעית ב-1896, תוך הבדלתו מנגזר אחר של המוגלובין דוגמת methhemoglobin. הבנה מוקדמת של תרחיש זה נתקלה בקשיים על ידי התרחשות של methemoglobinemia, שכן שני התרחישים יצרו ציאנוזיס ושינוי בפיגמנטציה של הדם, מה שגרם לאבחון שגוי עד תחילת המאה ה-20. חשיפה תעשייתית הופיעה במקרים של sulfhemoglubinemia, באותה תקופה בעיקר בקרב עובדים שהיו במגע עם trinitrotoluene במלחמת העולם הראשונה, כאשר תרכובות המכילות גפרית גרמו ליצירת sulfhemoglobin לצד השפעות המוליטיות. בשנות ה-40 התרבו דיווחים קליניים שקשרו את התרחיש עם תרופות sulfonamide ששימשו כחומרים אנטיביוטיים והיו ידועים כמחמצנים המוגלובין, דיווחים שכללו מעל 60 מקרים בקליניקת Mayo ומכונים אחרים. התקדמות בנושא תוך מדידות בשיטות סספקטרופוטומטריות, אפשרה אישור מדויק יותר של sulfhemoglobin על ידי גילוי ספקטרום הספיגה שלו ותכונות קישור החמצן, המבדילות אותו מ-methemoglobin. מחקר משנות ה-2000 מצא ש-sulfhemoglobin נוצר על ידי יצירה מוגברת של סולפיד מימני על ידי חיידקי בטן כגון Morganella morganii במקרים של עצירות כרונית או בשעת דיסביוזה של המעי. מקרים עדכניים של שנות ה-2020, מדגישים את הסיכון הנובע מרכישה ללא מרשם רופא של משככי כאבים דוגמת phenazopyridine.
רקע
התרחיש קורה כאשר אטום גפרית נקשר לטבעת הפורפירין של המוגלובין, מה שגורם לחמצון קבוע של הברזל התלת-ערכי, ומונע טרנספורט של חמצן. לרוב הדבר כרוך עם תרופות כגון dapsone ,sumatriptan ,metoclopramide ו-phenazopyridine. כמו כן התרחיש כרוך בכימיקלים תעשייתיים הכוללים hydrogen Sulfide ,dimethyl sulfoxide,trinitrotoluene ו-hydroxyl amine sulfate.
גורמים התומכים ביצירת sulfhemoglobinemia
תרחיש זה יכול להופיע על רקע גנטי המונע מהגוף את היכולת להתנגד לעקה חמצונית. לדוגמה, חסר באנזים glucose-6-phosphate dehydrogenase להלן G6PD), שהוא מפגע X-linked המשפיע על מעגל ה-pentose phospate, המפחית את יצירת NADPH ומפחית רמות גלוטתיון, תוך החמרת הנזק החמצוני להמוגלובין בחשיפה לגורמים מגרים. אף על פי שלא ברור עדיין המנגנון, יש ראיות לכך שחסר ב-G6PD עלול להיות גורם סיכון ליצירת סולפהמוגלובין במהלך עקה חמצונית, כגון מינון יתר של acetaminophen, על ידי הגבלת היכולת האנטי-חמצונית של האריתרוציטים. פולימורפיזמים באנזימים של הציטוכרום P450, המשמשים במטבוליזם של תרופות מחמצנות רבות הכרוכות ב-sulfhemoglobinemia, כגון סולפונאמידים, עלולים לשנות את פינוי אותן תרופות, ובכך יכולים פוטנציאלית להגביר את החשיפה למטבוליטים טוקסיים באנשים הלוקים בתרחיש זה. מפגעים נוספים שעלולים לפגוע בתהליכים פיזיולוגיים כגון מחלת כליות כרונית הפוגעת בפינוי הכלייתי של סולפונאמידים כרוכים בהצטברות תרופות ומגבירים את הסיכון לשינויים הקשורים בעקה חמצונית של המוגלובין. מחלה דלקתית במעי מסייעת לדיסביוזה ומעלה את האוכלוסיות של חיידקים מחזרי סולפט היוצרים עודף של מימן סולפידי (H₂S). דיסביוזה הוא מונח שזכה לתשומת לב רבה, במיוחד בתחומי הגסטרואנטרולוגיה והאימונולוגיה. הוא מתייחס לחוסר איזון בקהילות המיקרוביאליות המאכלסות את גופנו, ובמיוחד במעיים. קהילות מיקרוביאליות אלו, המכונות המיקרוביום, ממלאות תפקיד מכריע בבריאותנו הכללית, ומשפיעות על הכול, החל מעיכול ועד לתפקוד מערכת החיסון. קלינית, התסמינים מוגבלים לציאנוזיס ועלולים לכלול קריאות pulse oximetry נמוכות (דהיינו, ריוויון חמצן בערך 82% באוויר החדר). הסולפציה יוצרת תוצר ביניים שהוא episulfde התורם לגוון הירקרק כתוצאה מתזוזות בספקטרום הבליעה שלו. המשקל המשקל המולקולרי של sulfhemoglobin נותר אקווי-ולנטי לזה של המוגלובין נורמלי, שהוא בערך 64,500 דלטון, אך השינוי המבני פוגע משמעותית ביכולת הקישור שלו לליגנד.
מאפיינים של sulfhemoglobinemia
תכונות מפתח של sulfHb כוללות יכולת נשיאה מוגבלת של חמצן, כאשר הזיקה שלו לחמצן פוחתת פי 135–185 בהשוואה להמוגלובין נורמלי. בנוסף, sulfHb מדגים יציבות מוגברת, המתקיימת לאורך כל משך החיים של האריתרוציטים הפגועים ללא היפוך, ומראה הבדלים ספקטרליים כגון שיא ספיגה מינורי באורך גל של 620 ננומטר. SulfHb גם מדגים השפעה אלקלינית ע"ש Bohr, תוך שחרור של יותר פרוטונים מאשר המוגלובין נורמלי.
פתו-פיזיולוגיה
SulfHb נוצר לאחר תהליך ביוכימי בו חמצון של ברזל דו-ערכי (Fe²⁺) באתר ה-heme של המוגלובין הופך אותו למצב של ברזל ferryl (Fe⁴⁺) על ידי גורמי מחמצנים דוגמת hydrogen peroxide.
סימנים פיזיים
במקרים מתונים עלולה להופיע טכיקרדיה כמו גם tachypnea כתגובות המפצות על ההיפוקסיה ברקמות. Pulse oximetry עלולה לתת קריאות שגויות של ריוויון חמצן. במקרים חמורים תופענה באופן נדיר תופעות של בלבול הנובעות מהיפוקסיה של רקמות.
אטיולוגיות נרכשות
Dapsone במינון של 100 מיליגרם/יום, המשמש לטיפול בצרעת ובפרופילקציה של pneumocystis, משרה sulfhemoglobinemia אפילו במינונים תרפויטיים על ידי חמצון הברזל בהמוגלובין למצב התלת-ערכי שלו, מה שמעודד אינקורפורציה של גפרית. סולפונאמידים, כגון sulfamethoxazole, גורמים נזק חמצוני המוביל ליצירת sulfhemoglobin, במיוחד שילוב עם מחמצנים אחרים. Phenazopyridine, משכך כאבים של מערכת השתן הנרכש ללא מרשם רופא, הוא הגורם לבעיה בגלל מבנה צבע ה-azo שלו, המחמצן המוגלובין ומעודד קישור סולפיד. חשיפות סביבתיות הכרוכות במגע עם H₂S, גז טוקסי התורם ישירות ליצירת sulfHb על ידי תגובה עם חלבוני ה-heme. שאיפה תעשייתית של גז טבעי תוך טיפול במצבורי אשפה או בזיקוק שמנים, נמצאו משרים רמות כרוניות נמוכות של sulfhemoglobinemia בעובדים הנחשפים לריכוזי H₂S עד ppb משך 1–30 שנה.
שיטות אבחון
האבחון של sulfHB מתחיל עם מדידות מעבדה המגלות אי-התאמה במדידות של חמצן. שיטת ה-pulse oximetry מראה ריוויון נמוך של חמצן. שיטה זו עושה שימוש בספקטרומטריה של דגימות דם המוליטיות, היא שיטה המאשרת הראשונית לקביעת רמות sulfhemoglobin. היא מכמתת sulfHb על ידי בחינת הספיגה שלו ברצף של אורכי גל בין 500 ל-700 ננומטר, עם סף אבחוני של יותר מ-1-2% מסך ההמוגלובין, המצביע על משמעות קלינית. אישור מתקדם משתמש במס-ספקטרומטריה, בעיקר בספקטרומטרית - matrix-assisted laser desorption/ionization time-of-flight (להלן MALDI-ToF). ניטור מתמשך כרוך במדידות סדרתיות של co-oximetry לזיהוי של sulfHb ההולך ודועך בהדרגה כאשר האריתרוצים הנגועיפ מתפנים מהצירקולציה, לאחר שמשך החיים של אריתרוציטים אלה (120 יום) מסתיים. Methemoglobinemia גורמת לציאנוזיס ולדם בצבע חום-שוקולד, שאינה מגיבה לחמצן, אך נבדלת מ-sulfhemoglobinemia בהגיבה לטיפול עם mthylene blue ושיא ספיגה ב-630 ננומטר בקו-אוקסימטר, לעומת sulfhemoglobinemia עם שיא ספיגה ב-618 ננומטר ובכך שאינה מגיבה ל-methylene blue. חומר נוסף הנבדל מ-sulfhemoglobinemia הוא carboxyhemoglobin הנגרם על ידי הרעלת CO ומאופיין על ידי דם בצבע דובדבן-אדום, כאבי ראש ובחילה. זאת בניגוד הגוון הירקרק שנצפה בסיבות לבביות ונשימתיות הנגרמות על יד sulfHb. הניטור כרוך בסדרה של קו-אוקסימטריה עד שרמות sulfHb יורדות מתחת ל-1%
אבחון דיפרנציאלי
אבחון זה מזהה ישירות השתרבבות גפרית ל-heme, באורך גל של 668–670 ננומטר. דגימת דם קטנה (1 מיקרוליטר שנמהלה 1:2000, עוברת אנליזה ל-adducts כגון sulfur dioxide-heme ב-m/z 652wh683–685, מה שמספק ראיה ישירה ל-sulfHb. מבחן מבדיל בין sulfHb לבין methemoglobin היא על ידי הוספת ציאניד המבטל את שיא הספיגה של methemoglobin באורך גל 639 ננומטר, אך מותיר בשלמותו את השיא של sulfHb באורך גל 618–620 ננומטר. קו-אוקסימטים ישנים יותר עלולים לדווח בשוגג על sulfHb כ-methemoglobin, בגלל חפיפה של הספקטרומים של השניים באזור 630 ננומטר, אך דגמים חדשים יותר המשתמשים ב-8 אורכי-גל, מבדילים בין השניים במדויק. לצורך כימות מדויק, אחוז ה-sulfHb ניתן להערכה דרך הנוסחה:
sulfHb%=(absorbance at 618–620 nm minus baseline absorbance) divided by a reference absorbance (at 530 nm for oxyhemoglobin), normalized agaimst total hemoglobin cnoncentration.
על מנת לשלול המוליזה כגורם מערפל, רמות haptoglobin נקבעות ונמצאות נורמליות, שכן רמות מוגברות של haptoglobin היו אמורות להצביע על תהליך המוליטי במקום יצירה של sulfHb.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק