השפעות העישון והגמילה מעישון על תחלואת לב וכלי דם - The effects of smoking and smoking cessation on cardiovascular diseases
הופניתם מהדף The effects of smoking and smoking cessation on cardiovascular diseases לדף הנוכחי.
| השפעות העישון והגמילה מעישון על תחלואת לב וכלי דם | ||
|---|---|---|
| The effects of smoking and smoking cessation on cardiovascular diseases | ||

| ||
| יוצר הערך | ד"ר אהרון ארז, פרופ' אילן גולדנברג 
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – עישון, טרשת עורקים ומחלות כלי דם
עישון בכל צורותיו השונות קשור בעלייה ניכרת בשיעורי התמותה מכל סוג ובפרט בתחלואה קרדיו-וסקולרית. העלייה היחסית בסיכון אצל מעשנים לעומת כאלו שאינם מעשנים קיימת כשבוחנים מגוון רחב של מחלות קרדיו-וסקולריות, כולל תחלואה לבבית, עלייה בשכיחות אירועים מוחיים ומחלת כלי דם היקפיים. נשים חשופות לנזקי העישון יותר מגברים. מעשן סביל, הגם שהחשיפה לעשן היא כ-1 אחוז מזו של המעשן הפעיל הנמצא בקרבתו, חשוף לסיכון משמעותי לעלייה במחלות לב. מנגנוני הפעולה של העישון אינם ברורים לחלוטין, אולם מנגנונים אלו מערבים עלייה בהיווצרות טרשת עורקים ונטייה לקרישיות יתר. הפסקת עישון היא הדרך היעילה ביותר על מנת להקטין את הסיכון לתחלואה קרדיו-וסקולרית, גם אצל מעשנים שעישנו שנים רבות וגם במבוגרים. ההשפעות של הפסקת העישון על הירידה בסיכון לתחלואה קרדיו-וסקולרית מופיעות כבר בטווח זמן קצר, וככל שעובר זמן ללא עישון הסיכון לתחלואה אצל מעשנים לשעבר מתקרב לסיכון של כאלו שאינם מעשנים. תהליך הגמילה מעישון הוא קשה. באמצעות הדרכה של רופא המשפחה ועזרים תרופתיים אפשר להעלות באופן ניכר את הסיכוי לגמילה מוצלחת מעישון. במאמר זה נסקור מחקרים עדכניים העוסקים בהשפעת העישון על מחלות לב, השפעת הגמילה מעישון והטיפול המוכח העוזר לגמילה.
מבוא: השפעת עישון על תחלואה קרדיו-וסקולרית
ערך מורחב – נזקי העישון והדרכים למניעה ולגמילה - Smoking morbidity and cessation
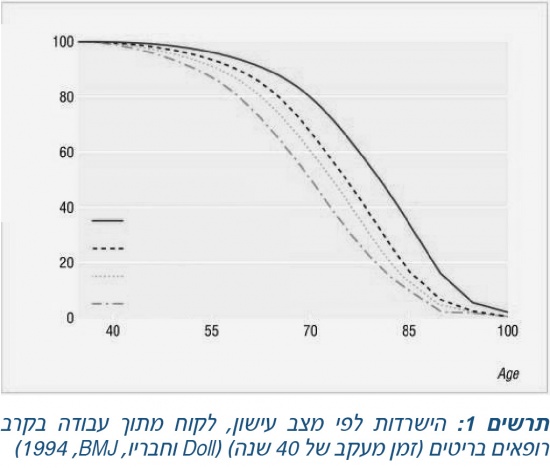
עישון גורם למגוון מחלות ואחראי לכ-50 אחוזים מכל מקרי המוות הניתנים למניעה במעשנים. כמחצית ממקרי המוות הללו הם כתוצאה מתחלואה קרדיו-וסקולרית. התחלואה הנלווית לעישון היא רבה וקשורה במגוון רב של מחלות. תרשים 1, הלקוח מתוך עבודתם של Doll וחבריו, מדגים את הקשר בין עישון לתמותה במעקב ארוך טווח לאורך 40 שנה אחר בקרב מ-34,000 רופאים בריטיים. התרשים מדגים עלייה משמעותית בתמותה אצל מעשנים לעומת לא מעשנים. כמו כן אפשר לראות שהעלייה בתמותה קשורה לכמות העישון וקיימת אף כאשר כמות העישון קטנה יחסית[1].
במונחים מספריים, האפקט הגדול ביותר של עישון קשור במחלות של מערכת הנשימה והמערכת הקרדיו-וסקולרית. עישון קשור בכל מגוון המחלות הקרדיו-וסקולריות, בהן מחלות קורונריות, שבץ מוחי, מחלת כלי דם פריפרית ואנאוריזמה של האאורטה.
העישון קשור בעלייה של כ-50 אחוזים בסיכון לשבץ מוחי. הסיכון של חולה מעשן למות ממחלה כלילית גבוה לפחות פי 2 מחולה שאיננו מעשן, וכשני שלישים ממקרי המוות הפתאומי כתוצאה מהתקפי לב קורים אצל מעשנים[2]. הראינו שמעשנים חשופים יותר להפרעות קצב מסכנות חיים. בעבודה שבדקה את הקשר בין עישון לטכיאריתמיות חדריות באוכלוסייה של חולים עם אי ספיקת לב וירידה בתפקוד הסיסטולי, וכללה 465 לא-מעשנים, 780 מעשנים לשעבר ו-197 מעשנים פעילים, נמצא שהסיכון לטכיקרדיה חדרית או מוות פתאומי גבוה בכ-50 אחוזים יותר במעשנים לעומת לא מעשנים או מעשנים לשעבר[3]. אצל חולים המושתלים עם מכשיר דה-פיברילטור, עישון הוא גורם סיכון למתן שוק מהמכשיר שאינו לצורך, שנגרם כתוצאה מטכיקרדיה על-חדרית[4].
הסיכונים היחסיים הקשורים בעישון גדולים יותר במעשנים צעירים מאשר במעשנים מבוגרים. לדוגמה, בעוד שאצל מעשנים מעל גיל 60 הסיכון היחסי להתקף לב הוא כפול מכאלו שאינם מעשנים, אצל מעשנים בגילאים מתחת ל-50 הסיכון גבוה פי חמישה מאלו שאינם מעשנים[2][5],
נשים חשופות יותר מגברים לנזקי העישון. Perscot וחבריו הראו במחקר אורכי שכלל יותר מ-24,000 גברים ונשים עם זמן מעקב ממוצע של כ-12 שנה, שהסיכון היחסי להתקף לב אצל נשים מעשנות הוא פי 2 מנשים שאינן מעשנות (RR*=2.24, C.I** 1.85-2.71) ואצל גברים מעשנים הסיכון היחסי הוא פי 1.5 (RR=1.57, C.I 1.25-1.97), ביחס של 1.57 לרעת הנשים[5][6], ייתכן שאחד ההסברים לכך הוא ההבדלים במטבוליזם של ניקוטין בין המינים. המטבוליזים של ניקוטין אצל נשים בגיל הפוריות מהיר יותר מאצל גברים, והמטבוליזם של ניקוטין מהיר יותר בנשים שנוטלות טיפולים הורמונליים לעומת נשים שלא נוטלות טיפולים הורמונליים[7]. ייתכן שההבדלים במטבוליזים של ניקוטין בין גברים לנשים מוביל לאפקט אפשרי של עישון מפצה.
עבודה שהתפרסמה ב-2014 מנתוני סקר ישראלי של חולים לאחר אירוע קורונרי חריף הראתה שבעוד שיעורי השרידות של חולים, שאינם מעשנים, לאחר אירוע של STEMI (ST Elevation Myocardial Infarction) השתפרו בסוף העשור האחרון לעומת תחילתו, וזאת כצפוי במקביל להתקדמות הטיפולים התרופתיים והמיכשור הפולשני, אצל חולים שמעשנים לאחר STEMI לא נצפתה הטבה בשיעורי התמותה[4], כך שנראה שיעילות הטיפולים המודרניים בחולים לאחר אירוע לבבי חריף מופחתת בחולים מעשנים.
*RR - Relative Risk
**C.I - Confidence Interval
כמות וסוג העישון
הסיכון הכרוך בעישון קשור בעיקר לכמות הטבק הנצרך ביום וקיים יחס ברור של כמות-תוצאה, אך האפקט השלילי של העישון קיים גם בכמויות קטנות. במחקר פרוספקטיבי מקופנהגן שכלל כ-11,000 גברים ונשים ועקב אחר התפתחות של התקף לב או מוות, נמצא שאצל נשים צריכת טבק בכמות של 3–5 גרם ליממה הייתה קשורה בסיכון מוגבר להתקף לב ולתמותה עם סיכון יחסי של 2.14 (95% C.I 1.11-4.13) ו-1.86 (95% C.I 1.37-2.51), בהתאמה[8]. משך זמן העישון גם משחק תפקיד בעלייה בסיכונים היחסיים למחלות השונות. כל אמצעי העישון מזיקים כולל סיגריות קלות (Light), עם פילטר, סיגארים, מקטרות ונרגילות[9][10]., גם מעשנים, הטוענים שאינם שואפים את העשן לריאות (למשל, מעשני מקטרות), נמצאים בסיכון מוגבר לתחלואה קרדיו-וסקולרית[8][9]., צריכת טבק ללא עישון (למשל, מסטיקים, סיגריות אלקטרוניות) גם היא קשורה בסיכון גבוה יותר להתקף לב ולשבץ מוחי[11].
עישון סביל
עישון סביל קשור בעלייה ניכרת בסיכון לתחלואה קרדיו-וסקולרית. Steenland וחבריו[12][13][14], דיווחו שהסיכון למוות כתוצאה ממחלה קרדיו-וסקולרית גדל בכ-30 אחוזים אצל לא מעשנים שגרים יחד עם מעשנים[15]. חשיפה לעישון בעבודה קשורה בהגדלת הסיכון בשיעור דומה[13]. גם בעישון סביל ישנו יחס ברור של כמות-תוצאה עם עלייה בסיכון היחסי למחלת לב איסכמית של 1.23 ו-1.31, בהתאמה, אצל לא מעשנים שנחשפו לעישון של 1–19 סיגריות ביום ואצל כאלו שנחשפו ליותר מ-20 סיגריות ביום, בהשוואה לכאלו שאינם מעשנים ואינם חשופים לעישון[12]. הסיכון היחסי בעישון סביל הוא גדול באופן מפתיע ומגיע כמעט למחצית הסיכון של עישון 20 סיגריות ליום, וזאת אף שהחשיפה לעשן היא רק כ-1 אחוז מהחשיפה של מעשן פעיל. הסיכון העודף בעישון סיגריה אחת ליום הוא כ-39 אחוזים, דומה לסיכון של מעשן סביל שגר עם מעשן. האפקט הזה מוסבר על ידי קשר לא ליניארי של כמות-תוצאה בין חשיפה לעישון טבק לבין הסיכון למחלת לב איסכמית[13]. מחקרים קליניים וניסויים רבים הדגימו שההשפעות המיידיות של חשיפה לעישון, בהן ירידה בתפקוד האנדותל, שפעול טסיות, עקה חימצונית ותגובות דלקתיות, משתתפות בתהליך הטרשת. עישון סביל ככל הנראה יכול לעורר את ההתייצגות החריפה של מחלות קרדיו-וסקולריות, והנזק הלבבי אצל מעשנים סבילים ממשיך לגדול כל עוד החשיפה לעישון נמשכת[14].
מנגנוני פעולה
עישון משפיע על כל השלבים של המחלה הטרשתית מהפרעה בתפקוד האנדותל ועד להתפתחות האירוע הקליני החריף. המרכיבים הרעילים של עישון סיגריה והמכניזם המדויק שדרכו עישון מעלה את הסיכון לתחלואה קרדיו-וסקולרית אינם מובנים במלואם, אבל מגוון רב של עבודות שפכו אור על המנגנונים האפשריים והראו את ההשפעות המזיקות של העישון על תפקוד האנדותל, התהליכים החימצוניים, תפקודי טסיות, פיברינוליזה, דלקת, שינוי של שומנים ותפקוד וזו-מוטורי. רדיקלים חופשיים, הנמצאים בעשן הנשאף, גורמים לחימצון של LDL (Low Density Lipoprotein). ה-LDL המחומצן משפעל את התגובה הדלקתית בתוך דופן העורק, ובכך גורם להגדלת הטרשת[16][17][18].
במודלים ניסויים, חלק מתהליכים אלו הם הפיכים במלואם/חלקם תוך זמן קצר מאוד. Moreno וחבריו הראו שהשפעת העישון הפוגמת בתפקוד האנדותל חולפת לאחר 24 שעות מהפסקת העישון[19]. עבודה נוספת של Morita הראתה שכבר לאחר שבועיים מהפסקת העישון קיימת ירידה באגרגציה המוגברת של הטסיות שקיימת אצל מעשנים[20]. יש בממצאים אלו לחזק את המוטיבציה של מעשנים להפסיק לעשן.
טיפול
הפסקת עישון
עבודות על נבדקים ללא מחלה קרדיו-וסקולרית מראות שהסיכון למחלה קרדיו-וסקולרית אצל כאלו שעישנו בעבר הוא בינוני בהשוואה לסיכון של אלו שלא עישנו כלל או לסיכון אצל מעשנים. הפסקת עישון לאחר התקף לב היא אולי הדרך האפקטיבית ביותר למניעה שניונית. מטה-אנליזה שבחנה 20 עבודות שבדקו הפסקת עישון לאחר התקף לב, הראתה ירידה של כ-36 אחוזים בתמותה אצל חולים שהפסיקו לעשן בהשוואה לכאלו שהמשיכו לעשן[21]. הירידה בתחלואה הקרדיו-וסקולרית מתרחשת במהירות לאחר הפסקת העישון. Chow וחבריו הראו באוכלוסייה של 18,809 חולים לאחר התקף לב שהפסקת עישון הורידה את הסיכון להתקף לב חוזר כבר לאחר שישה חודשים ב-43 אחוזים בהשוואה למעשנים שלא הפסיקו (OR, 0.57; 95% confidence interval, 0.36-0.89).[22] בגברים מתחת לגיל 55 הראו שהסיכון היחסי להתקף לב אצל מעשנים הוא פי 2.9 לעומת לא מעשנים. הסיכון היחסי יורד אצל נגמלים מעישון, ולאחר כשנתיים של הימנעות מעישון הסיכון דומה לסיכון של אלה שלא עישנו מעולם[23].
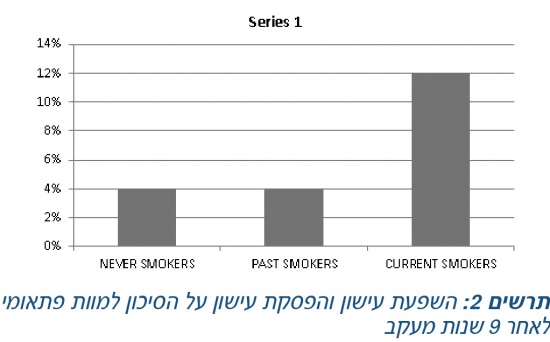
בעבודה שנערכה בקרב 3,122 משתתפי מחקר Bezafibrate Infarction Prevention Trial שנערך בארץ לפני יותר מעשור באוכלוסייה של חולים עם מחלת לב כלילית ידועה מצאנו כי הסיכון למוות לבבי פתאומי (Sudden cardiac death) גבוה פי 3 במעשנים לעומת לא מעשנים או חולים שהפסיקו לעשן[24]. לאחר 9 שנות מעקב אחר האוכלוסייה נמצא כי הסיכון למוות פתאומי היה 4 אחוזים בקרה חולים שלא עישנו מעולם, 4 אחוזים בקרב אלה שהפסיקו לעשן, לעומת 12 אחוזים בקרב חולים שהמשיכו לעשן (תרשים 2). בעבודה אף מצאנו שהירידה בסיכון למוות לבבי פתאומי מופיעה כבר בשנה הראשונה לאחר הפסקת העישון[24].
קיימים כמה מנגנונים אפשריים להשפעת עישון על הסיכון למוות לבבי פתאומי, כולל השפעה פרו-אריטמית ישירה של ניקוטין והשפעת עישון על הסיכון לקרישיות יתר תוך הגברת הסיכון לאירוע כלילי חד.
הנתונים לעיל מצביעים באופן חד-משמעי על העובדה כי יש לעודד הפסקת עישון אצל כל המעשנים, ועל כך שההשפעות של הפסקת העישון ניכרות יותר ככל שמפסיקים לעשן מוקדם יותר. למעשנים לשעבר תוחלת חיים ארוכה יותר מאשר מעשנים פעילים, ללא תלות בגיל הפסקת העישון. ההישרדות של מעשנים שהפסיקו לעשן לפני גיל 35 היא כמעט זהה להישרדות של כאלו שאינם מעשנים. ההנחיות של האיגוד האירופי לקרדיולוגיה (2012 European Guidelines on Cardiovascular Disease Prevention in Clinical Practice) למניעת תחלואה לבבית מגדירות את צורך הרופא המטפל לעודד הפסקת עישון כ-Class I indication. ההנחיות אף מפרטות את חמש הפעולות שעל הרופא המטפל לבצע כדי לעודד הפסקת עישון אצל כל מטופל, כולל בירור יסודי אצל כל מטופל אם מעשן, המלצה חד-משמעית להפסקת עישון, הערכת יכולת למטופל להפסיק לעשן, סיוע והסכמה משותפת עם המטופל על תהליך הפסקת העישון (כולל קביעת מועד הפסקה, וקביעה משותפת של אסטרטגיה להפסקה) ומעקב מסודר אחר התהליך.
המנבא החשוב ביותר להצלחת הגמילה מעישון הוא מוטיבציה, שאפשר להגביר באמצעות עזרה מקצועית. הצעת הרופא להפסיק לעשן היא חשובה כדי להתחיל את תהליך הגמילה מעישון ולהעלות את הסיכויים להצלחתה. במטה-אנליזה שבדקה את ההשפעה של הצעת הרופא הראשוני להפסיק לעשן על הסיכויים לגמילה, נצפתה עלייה משמעותית בסיכויים לגמילה מעישון (סיכון יחסי של 1.66; C.I1.42 - 1.94).24,14 יש להדריך מעשנים על כך שהם צפויים להעלות כ-5 קילוגרם במשקלם בתהליך הגמילה, אבל הפסקת העישון מיטיבה הרבה יותר מאשר הנזק הכרוך בעלייה במשקל.
עזרים פרמקולוגיים לגמילה מעישון
ערך מורחב – עישון - טיפול תרופתי להפסקת עישון - Smoking cessation - pharmacological treatment
כאשר מעשנים מנסים להיגמל מעישון הם חווים תסמיני גמילה קשים ביותר הכוללים אי שקט, רגזנות, שינויים בתיאבון, קשיי ריכוז ותסמינים נוספים. תסמינים אלה גורמים בסופו של דבר לכישלון של ניסיון הגמילה, ותוך כמה ימים הם חוזרים לעשן על מנת להפסיק את תסמיני הגמילה הקשים.
רוב הנגמלים מעישון עושים זאת ללא עזרים. אולם, עזרים תרופתיים מעלים את הסיכוי להפסיק לעשן. לכן, בצירוף להסברים ועידוד, אפשר להציע גם תחליפי ניקוטין ולעיתים גם Varenicline או Bupropion על מנת לתמוך בתהליך הגמילה.
- בקו הראשון לגמילה מעישון נכללות התרופות הבאות
- תחליפי ניקוטין: מטרתם להקטין את המוטיבציה לעשן ולהקטין את תסמיני הגמילה הפיזיולוגים והפסיכולוגיים המופיעים לעיתים בתהליך הגמילה. הם מופיעים בכמה צורות: מדבקות במגוון מינונים, גומי לעיסה, לכסניות מציצה, טבליות, תרסיס ומשאף. אפשר להשיג את התחליפים הללו ללא מרשם רופא
- Bupropion (זייבן): פותח כנוגד דיכאון ממשפחת הטרי-ציקליים. האפקט האנטי דיכאוני של התרופה מספק לנגמלים נוגד מצב רוח, ומלבד זאת התרופה מקלה תסמיני גמילה אחרים. המינון המקובל לגמילה מעישון הוא 150 מיליגרם אחת ליום במשך 3 ימים, ואז 150 מיליגרם פעמיים ביום למשך 7–12 שבועות. מכיוון שהשפעת התרופה אינה מיידית (לוקח כשבוע עד שהשפעתה מורגשת) מומלץ להתחיל את השימוש בתרופה שבוע-שבועיים לפני תאריך היעד להפסקת העישון
- Varenicline (צ'מפיקס): זהו אגוניסט חלקי סלקטיבי לרצפטור לניקוטין, מאושר לשימוש מ-2006. ככל הנראה התרופה עוזרת להיגמל מעישון על ידי פעולתה המשולבת כאגוניסט שמובילה לשחרור של דופמין וכך מפחיתה את תסמיני הגמילה, ועל ידי פעולתה כאגוניסט חלקי המונע את קשירת הניקוטין לרצפטור ומפחית את ההנאה מעישון. תופעות הלוואי כתוצאה מנטילת התרופות נדירות מאוד. תופעת הלוואי העיקרית של התרופה היא בחילה, שנוטה להיעלם עם הזמן. כמו כן מומלץ לברר היסטוריה של הפרעות פסיכיאטריות בשל דיווחים על תופעות לוואי נדירות הכוללות מצב רוח דיכאוני, אגיטציה ומחשבות אובדניות (הנמצאות כעת תחת בדיקה). המינון המקובל הוא של 1 מיליגרם פעמיים ביום למשך 12 שבועות, כשבשבוע הראשון מבצעים טיטרציה של מינונים על מנת להקטין תופעות לוואי. מומלץ להתחיל את השימוש בתרופה שבוע-שבועיים לפני תאריך היעד להפסקת העישון
כל תחליפי הניקוטין הם אפקטיביים. בסקירה סיסטמטית, תחליפי הניקוטין העלו את הסיכוי להפסקת עישון ביותר מ-50 אחוזים (C.I 1.50-1.66 ,95%). קיימת עדות לכך שהיעילות של מדבקת הניקוטין בצירוף תחליף ניקוטין מהיר-פעולה היה יעיל יותר מאשר סוג אחד של תחליף ניקוטין. ככל הנראה, האפקט של תחליפי הניקוטין למיניהם אינו תלוי בעצימות התמיכה הנוספת בתהליך הגמילה[25]. במטה-אנליזה שהשוותה בין הטיפולים השונים לגמילה מעישון נמצא כי יעילות תחליפי הניקוטין דומה ליעילות של Bupropion.[26]
Varenicline מעלה את הסיכוי להפסיק לעשן פי 2–3 בהשוואה להפסקת עישון ללא עזרים תרופתיים. Varenicline נמצאה יעילה יותר מ-Bupropion ומתחליפי הניקוטין בצורתם השונה (מדבקה, גומי לעיסה, משאף, טבליות), אך לא יעילה יותר מאשר שילוב של תחליפי ניקוטין[26]. במחקר אקראי כפול-סמיות שנמשך 52 שבועות וכלל 714 מעשנים עם מחלת לב איסכמית יציבה בדקו את היעילות והבטיחות של Varenicline לעומת פלצבו בהפסקת עישון. נמצא שחולים שטופלו ב-Varenicline נגמלו בהצלחה בשיעורים גבוהים יותר מחולים שטופלו בפלצבו (19.2 אחוזים לעומת 7.2 אחוזים; סיכון יחסי של 3.14). לא נמצא הבדל בין פלצבו לתרופה לגבי תופעות לוואי משמעותיות, אבל גודל המדגם ומשך זמן המעקב מגבילים את המסקנות לגבי בטיחות התרופה[27].
בקו השני לתרופות שעוזרות לגמילה מעישון מצויות התרופות Nortriptyline האנטי-דיכאונית ו-Clonidine כנגד יתר לחץ דם[28].
סיכום
עישון הוא גורם סיכון משמעותי למגוון מחלות קרדיו-וסקולריות. קשה להפריז בחשיבות של מניעת העישון והצורך להיגמל מעישון. ההשפעה המיטיבה של הגמילה מעישון מבחינת הורדת התחלואה מתרחשת באופן מהר. באמצעות עידוד ועזרים תרופתיים אפשר להגדיל את הסיכוי להפסקת העישון בצורה משמעותית.
ביבליוגרפיה
- ↑ Doll, R., Peto, R., Wheatley, K., Gray, R. & Sutherland, I. Mortality in relation to smoking: 40 years' observations on male British doctors. Bmj 309, 901-911 (1994).
- ↑ 2.0 2.1 Edwards, R. The problem of tobacco smoking. Bmj 328, 217-219, doi:10.1136/bmj.328.7433.217 (2004).
- ↑ Plank, B. et al. Smoking is associated with an increased risk of first and recurrent ventricular tachyarrhythmias in ischemic and nonischemic patients with mild heart failure: a MADIT-CRT substudy. Heart rhythm : the official journal of the Heart Rhythm Society 11, 822-827, doi:10.1016/j.hrthm.2014.02.007 (2014).
- ↑ 4.0 4.1 Arbel, Y. et al. Temporal trends in all-cause mortality of smokers versus non-smokers hospitalized with ST-segment elevation myocardial infarction. International journal of cardiology 176, 171-176, doi:10.1016/j.ijcard.2014.07.010. 2014.
- ↑ 5.0 5.1 Prescott, E., Hippe, M., Schnohr, P., Hein, H. O. & Vestbo, J. Smoking and risk of myocardial infarction in women and men: longitudinal population study. Bmj 316, 1043-1047.1998.
- ↑ Mucha, L., Stephenson, J., Morandi, N. & Dirani, R. Meta-analysis of disease risk associated with smoking, by gender and intensity of smoking. Gender medicine 3, 279-291.2006.
- ↑ Benowitz, N. L., Lessov-Schlaggar, C. N., Swan, G. E. & Jacob, P., 3rd. Female sex and oral contraceptive use accelerate nicotine metabolism. Clinical pharmacology and therapeutics 79, 480-488, doi:10.1016/j.clpt.2006.01.008. 2006.
- ↑ 8.0 8.1 Prescott, E., Scharling, H., Osler, M. & Schnohr, P. Importance of light smoking and inhalation habits on risk of myocardial infarction and all cause mortality. A 22 year follow up of 12 149 men and women in The Copenhagen City Heart Study. Journal of epidemiology and community health 56, 702-706. 2002.
- ↑ 9.0 9.1 in How Tobacco Smoke Causes Disease: The Biology and Behavioral Basis for Smoking-Attributable Disease: A Report of the Surgeon General Publications and Reports of the Surgeon General. 2010.
- ↑ Akl, E. A. et al. The effects of waterpipe tobacco smoking on health outcomes: a systematic review. International journal of epidemiology 39, 834-857, doi:10.1093/ije/dyq002. 2010.
- ↑ Boffetta, P. & Straif, K. Use of smokeless tobacco and risk of myocardial infarction and stroke: systematic review with meta-analysis. Bmj 339, b3060, doi:10.1136/bmj.b3060.2009.
- ↑ 12.0 12.1 He, J. et al. Passive smoking and the risk of coronary heart disease--a meta-analysis of epidemiologic studies. The New England journal of medicine 340, 920-926, doi:10.1056/NEJM199903253401204. 1999..
- ↑ 13.0 13.1 13.2 Law, M. R., Morris, J. K. & Wald, N. J. Environmental tobacco smoke exposure and ischaemic heart disease: an evaluation of the evidence. Bmj 315, 973-980. 1997.
- ↑ 14.0 14.1 Raupach, T., Schafer, K., Konstantinides, S. & Andreas, S. Secondhand smoke as an acute threat for the cardiovascular system: a change in paradigm. European heart journal 27, 386-392, doi:10.1093/eurheartj/ehi601. 2006.
- ↑ Steenland, K. Risk assessment for heart disease and workplace ETS exposure among nonsmokers. Environmental health perspectives 107 Suppl 6, 859-863. 1999.
- ↑ Yamaguchi, Y., Matsuno, S., Kagota, S., Haginaka, J. & Kunitomo, M. Oxidants in cigarette smoke extract modify low-density lipoprotein in the plasma and facilitate atherogenesis in the aorta of Watanabe heritable hyperlipidemic rabbits. Atherosclerosis 156, 109-117 (2001).
- ↑ Yamaguchi, Y., Haginaka, J., Morimoto, S., Fujioka, Y. & Kunitomo, M. Facilitated nitration and oxidation of LDL in cigarette smokers. European journal of clinical investigation 35, 186-193, doi:10.1111/j.1365-2362.2005.01472.x . 2005.
- ↑ Ambrose, J. A. & Barua, R. S. The pathophysiology of cigarette smoking and cardiovascular disease: an update. Journal of the American College of Cardiology 43, 1731-1737, doi:10.1016/j.jacc.2003.12.047. 2004
- ↑ Moreno, H., Jr. et al. Endothelial dysfunction in human hand veins is rapidly reversible after smoking cessation. The American journal of physiology 275, H1040-1045. 1998
- ↑ Morita, H., Ikeda, H., Haramaki, N., Eguchi, H. & Imaizumi, T. Only two-week smoking cessation improves platelet aggregability and intraplatelet redox imbalance of long-term smokers. Journal of the American College of Cardiology 45, 589-594, doi:10.1016/j.jacc.2004.10.061. 2005.
- ↑ Critchley, J. & Capewell, S. Smoking cessation for the secondary prevention of coronary heart disease. The Cochrane database of systematic reviews, CD003041, doi:10.1002/14651858.CD003041.pub2. 2004.
- ↑ Chow, C. K. et al. Association of diet, exercise, and smoking modification with risk of early cardiovascular events after acute coronary syndromes. Circulation 121, 750-758, doi:10.1161/CIRCULATIONAHA.109.891523. 2010.
- ↑ Rosenberg, L., Kaufman, D. W., Helmrich, S. P. & Shapiro, S. The risk of myocardial infarction after quitting smoking in men under 55 years of age. The New England journal of medicine 313, 1511-1514, doi:10.1056/NEJM198512123132404. 1985.
- ↑ 24.0 24.1 Goldenberg I, Jonas a, Tennebaum A, et al. Current smoking, smoking cessation, and the risk of sudden cardiac death in patients with coronary artery disease. Arch Intern Med. 2003 Oct 27;163(19):2301-5.
- ↑ Stead, L. F., Bergson, G. & Lancaster, T. Physician advice for smoking cessation. The Cochrane database of systematic reviews, CD000165, doi:10.1002/14651858.CD000165.pub3. 2008.
- ↑ 26.0 26.1 Stead, L. F., Perera, R., Bullen, C., Mant, D. & Lancaster, T. Nicotine replacement therapy for smoking cessation. The Cochrane database of systematic reviews, CD000146, doi:10.1002/14651858.CD000146.pub3. 2008.
- ↑ Cahill, K., Stevens, S., Perera, R. & Lancaster, T. Pharmacological interventions for smoking cessation: an overview and network meta-analysis. The Cochrane database of systematic reviews 5, CD009329, doi:10.1002/14651858.CD009329.pub2. 2013.
- ↑ Rigotti, N. A. et al. Efficacy and safety of varenicline for smoking cessation in patients with cardiovascular disease: a randomized trial. Circulation 121, 221-229, doi:10.1161/CIRCULATIONAHA.109.869008. 2010.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר אהרון ארז - מרכז הלב, המרכז הרפואי על שם שיבא, תל השומר ופרופ' אילן גולדנברג - מנהל המחלקה הקרדיולוגית והעמותה הישראלית למחקרילב וכלי דם, מרכז הלב, המרכז הרפואי של שם שיבא, תל השומר


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק