פגם במחיצה הבין חדרית - Ventricular septal defect
הופניתם מהדף Ventricular septal defect לדף הנוכחי.
אם הינך רופא/ה, אנחנו מזמינים אותך לשפר את הערך ולהוסיף את המידע הדרוש להשלמתו. אם אין לך הרשאות עריכה ניתן לבקש זאת (קבלת הרשאות), וללמוד כיצד לערוך (עריכה בוויקירפואה). |
| פגם במחיצה הבין חדרית | ||
|---|---|---|
| Ventricular septal defect | ||
| 250px | ||
Echocardiographic image of a moderate ventricular septal defect in the mid-muscular part of the septum. The trace in the lower left shows the flow during one complete cardiac cycle and the red mark the time in the cardiac cycle that the image was captured. Colours are used to represent the velocity of the blood. Flow is from the left ventricle (right on image) to the right ventricle (left on image). The size and position is typical for a VSD in the newborn period.
| ||
| ICD-10 | Chapter Q 21.0 | |
| ICD-9 | 745.4 | |
| MeSH | C14.240.400.560.540 | |
| יוצר הערך | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מום לב מולד
פגם במחיצה הבין חדרית (Ventricular Septal Defect - VSD) הוא ליקוי בלב. חור במחיצה (Septum) אשר מפרידה בין החדר השמאלי של הלב לחדר הימני.
בלב בריא, דם עם רמות חמצן נמוכות חוזר מהגוף לפרוזדור הימני של הלב, ומשם לחדר הימני. מהחדר הימני, הדם נשאב אל הריאות כדי להתמלא בחמצן, ממשיך אל הפרוזדור השמאלי ומשם אל החדר השמאלי, לפני שהוא מבצע סיבוב בגוף. כאשר קיים הפגם, חור במחיצה בין החדר השמאלי לחדר הימני גורם לדם העשיר בחמצן, מהחדר השמאלי, להתערבב בדם בחדר הימני, שם רמות החמצן נמוכות. כתוצאה מכך, דם עשיר בחמצן נשאב שנית אל הריאות כדי לקבל חמצן. הלב כעת נאלץ להתמודד עם כמויות דם גדולות יותר, ועשוי לגדול כתוצאה מכך. הדבר עשוי גם לגרום לעליית הלחץ בכלי הדם של הריאות, מכיוון שכעת עובר שם יותר דם. אם הליקוי גדול ואינו מטופל בזמן, כלי הדם בריאות עשויים להיפגע בשל לחץ הדם הגובר, והדבר מוביל בסופו של דבר לאי ספיקת לב ימני ומוות.
הפגם במחיצה הבין חדרית הוא פגם הלב המולד הנפוץ ביותר. הוא נמצא ב-30% מהלידות עם פגם לב מולד, וב2-3 לידות מתוך 1000. ליקוי זה מכונה לעתים "חור בלב".
פגם במחיצה הבין חדרית יכול להיווצר בעיקר בעת הלידה, ולעתים גם כתוצאה מהתקף לב.
אפידמיולוגיה
אטיולוגיה
אמבריולוגיה
במהלך החיים העובריים הלב מורכב מחדר פרימיטיבי אחד, אשר בנוי מדופן שרירית. כחלק מתהליך של קיפול (Folding), החלק הבסיסי של הדופן מתחיל להתקפל כלפי פנים ולחלק את החדר לשני חללים. החלק של המחיצה נוצר מהשריר ולכן נקרא מחיצה שרירית (Muscular septum).
במקביל, מופיע מבנה עשוי ג'ל הנקרא כרית אנדוקרדיאלית (Endocardial cushion), שקוטרו מילימטר. המבנה מתפשט ושולח שלוחות:
- שלוחה כלפי מטה להשלמת המחיצה הבין חדרית.
- שלוחה כלפי מעלה למחיצה בין העליות.
- שלוחה שמאלה, התורמת לעלה הקדמי של המסתם הדו-צניפי (מיטרלי).
- שלוחה ימינה, היוצרת את העלה הספטלי של המסתם הטריקוספידלי.
הכרית תורמת ליצירת מחיצה בין שני החדרים, בין העליות, עלה קידמי של המסתם המיטרלי, ועלה ספטלי של המסתם הטריקוספידאלי. פגם, הופעה חלקית או התפתחות לא תקינה של הכרית יכולה לגרום לפגם משולב - וזוהי תמונה של פגם במחיצה האטריוונטריקולרית (Atrioventricular canal, Atrioventricular septal defect, Endocardial cushion defect) שמופיעה בחולי תסמונת דאון (Down syndrome).
למחיצה שבין שני החדרים שני מרכיבים:
- מרכיב שרירי (Muscular) - מהדופן של החדר הפרימיטיבי.
- מרכיב ממברנוטי (Membarontic) - מהכרית האנדוקרדיאלית.
מעשית, מחלקים את המחיצה הבין חדרית ל-3 מרכיבים:
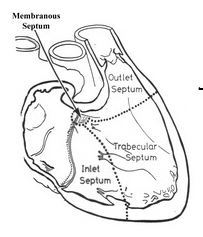
- האיזור הממברנוטי (Membranous) - החלק העליון. מופיע תמיד כחלק מקומפלקס (נוצר מהכרית האנדוקרדיאלית ולכן פגם בו יופיע עם עוד פגמים).
- האיזור הפריממברנוטי (Perimembranous) - האיזור השרירי שקרוב לממברנה.
- האיזור השרירי (Muscular) - החלק התחתון של המחיצה.
המחיצה בעלת עומק ומחולקת לחלק קדמי ולחלק אחורי. המנתח נכנס תמיד דרך החלל בו הלחצים הנמוכים ביותר, ולכן נכנס לעליה הימנית שבה הלחצים נמוכים (2-3 מ"מ כספית לעומת 120 מ"מ כספית בחדר שמאל), ומשם לחדר הימני. בדרך, הוא עובר במסתם הטריקוספידלי ויוצא לכיוון עורק הריאה (Pulmonary artery). המסתם הטריקוספידלי הוא אחורי (Posterior) ואילו הפולמונרי קדמי (Anterior).
- Inlet - ברמה האחורית של המסתם הטריקוספידלי (הכניסה לחדר): Posterior septum.
- Outlet - ברמה הקדמית של עורק הריאה: Anterior septum.
לדוגמא, מקובל לומר: פגם במחיצה הבין חדרית, פריממברנוטי, Outlet (ממברנוטי תמיד יהיה ב-Inlet, אבל יהיו לו עוד מרכיבים).
קליניקה
המרכיבים שיקבעו את ההתייצגות הקלינית של ילד עם פגם במחיצה הבין חדרית הם:
- גודל הפגם – בהדמית אולטרסאונד (Ultrasonography) בודקים את הקצוות.
- התנגודת הריאתית.
אם הפגם במחיצה הבין חדרית מאוד קטן, לעולם לא ידלוף הרבה דם. למשל, בפגם של מ"מ אחד לא נתייחס בכלל לתנגודת הריאתית.
- גודל הפגם
קוטר הטבעת של אבי העורקים (Aortic annulus) בתינוק בשל (3.5 ק"ג בשבוע 40) הוא 10 מ"מ - מודדים קוטר הפגם באמצעות אקוקרדיוגרפיה (Echocardiography) ומחשבים יחס לאבי העורקים (Aorta).
- עד 30% - קטן (מקוטר אבי העורקים)
- בין 30-60% - בינוני
- מעל 60% - גדול
- תנגודת ריאתית
נניח כי קיים פגם של 4 מילימטר במחיצה בין חדרית.
בימים הראשונים התנגודת הריאתית גבוהה ולכן החדר הימני צריך להפעיל הרבה לחץ. לכן, בשבוע הראשון כמעט ואין הבדל בין הלחצים. כיוון שהדם זורם בהפרש לחצים, בשבוע זה לא תהיה זרימה. בטווח של 4-6 שבועות הלחץ בחדר הימני הולך ויורד, הפרש הלחצים הולך ועולה ומתחילה דליפה שהולכת ומתגברת (מכיוון שהתנגודת הריאתית יורדת). כלומר, ייתכן שלתינוק יש פגם גדול ומשמעותי במחיצה בין חדרית שלא נראה מכיוון אין דליפה. ככל שהזמן מתקדם לכיוון 4-6 שבועות, יש יותר זרימה של דם לריאות ויופיעו קשיי נשימה.
כלומר, יכול להיות שלא נשמע את הפגם כי איוושה נשמעת רק כאשר מתרחשת זרימה מערבולתית. ולכן, אם אין זרימה: המצב תקין או שמדובר בפגם במחיצה בין חדרית בשלבים הראשונים.
פגם קטן
בפגם קטן במחיצה בין חדרית, למשל של 2 מ"מ, בתחילה לא תשמע האיוושה, אלא רק אחרי כמה שבועות.
ככל שהחור קטן יותר, כך עוצמת האיוושה חזקה יותר. פגם קטן במחיצה הבין חדרית נקרא גם על שם הרופא שתיאר זאת לראשונה - Maladie de Roger. ב-60-80% מהמקרים החור יקטן או יסגר במהלך השנה הראשונה לחיים, הילדים אינם סובלים ואין ממצאים למעט איוושה ששומעים בהאזנה. האיוושה היא איוושה סיסטולית כי יש הפרש לחצים בין החדרים בזמן הסיסטולה, ולא בדיאסטולה. בזמן דיאסטולה אין כמעט הפרש לחצים בין החדר הימני לחדר השמאלי (חדר ימני 2-3 מ"מ כספית, חדר שמאל- 3-5 מ"מ כספית).
ככל שהחור קטן יותר הסיכון לדלקת זיהומית של פנים הלב (Infective endocarditis) גבוה יותר, כיוון שכאשר החדר השמאלי מתכווץ נוצר סילון דם (Jet) משמאל לימין וככל שהחור קטן יותר הסילון מרוכז יותר. סילון הדם פוגע ב-3 מקומות בחדר ימני: היישר מול נקודת יציאת הדם על החדר ובעוד 2 נקודות על המחיצה. דבר זה יכול לגרום לקרע באנדוקרד (Endocard). אם קיימת בקטרמיה (Bacteremia) מטיפול בשיניים או ניתוח אף, אוזן, גרון למשל, החיידקים יכולים להתיישב על האנדוקרד. מחלה זו מאד קשה לטיפול ולכן, לפני פעולות חודרניות (טיפול שיניים, טיפול אף, אוזן, גרון) נותנים מנה גדולה של אנטיביוטיקה כשעה לפני הטיפול (דרך הפה או תוך ורידית).
פגם בינוני
במצב שבו קיים פגם בינוני במחיצה הבין חדרית, למשל של 5 מ"מ, כאשר התנגודת הריאתית מתחילה לרדת, הלחץ בצד ימין הולך ויורד. הכדוריות האדומות נחלקות בין אבי העורקים לעורק הריאתי. ככל שהזמן עובר, הלחץ הריאתי יורד והדם יגיע לשם יותר. בממוצע תוך 4-6 שבועות צריכה להסתיים ירידת התנגודת הריאתית למידה המירבית התקינה. חלק מהדם בורח לריאות, החדר השמאלי צריך לעבוד יותר קשה והעץ הריאתי מוצף. הדם שמגיע לעץ הריאתי, מגיע מהוריד החלול העליון (Superior vena cava) ומהוריד החלול התחתון (Inferior vena cava), יחד עם הדלף מהחדר השמאלי.
העליה השמאלית מקבלת נפח עודף (Volume overload). הדפנות שלה אינן שריריות וקשיחות, ולכן העליה השמאלית עולה בנפח. בשלב מסויים ממשיכה זרימה אבל העליה השמאלית לא יכולה לגדול (גם מכנית מוגבלת בדברים אחרים) ולכן עולה הלחץ על ורידי הריאות. בגלל הלחץ ההידרוסטטי מתחילה זרימה לתוך הורידים הריאתיים ועל גבי שטח בועיות הריאה (Alveoli). מתחילה דליפה של נוזלים לתוך בועיות הריאה, הגורמת לבצקת ריאות.
- ביטוי קליני
- התינוק מתחיל להכנס לדחק (Stress) נשימתי מכיוון שההיענות (Compliance) הינה פחות טובה, מתחיל לנשום מהר, ויהיה טכיפנאי.
- טאכיקרדיה (Tachycardia) בשל פעילות מערכת סימפטטית.
- הזעה (בעיקר במצח בשל ריבוי בלוטות זיעה בתינוקות).
- סימני אי ספיקת לב - בעיקר בצקות למיניהן. סימני אי ספיקת לב בתינוקות שונה ממבוגרים. הכבד בתינוקות יכול לקלוט הרבה נוזלים ולכן יש הגדלת כבד מרשימה של התינוק.
- התינוק אינו מסוגל לאכול בשל קצב נשימות מהיר (Tachypnea) וקצב לב מהיר (Tachycardia), ולכן אינו עולה במשקל.
תהליך זה הדרגתי ותלוי בתנגודת הריאתית ועל כן אינו מתרחש בין לילה, והתינוק נכנס לתמונה של אי ספיקת לב.
- בהאזנה – נשמעת בעיקר איוושה סיסטולית אבל גם איוושה דיאסטולית - שנוצרת כי העליה השמאלית מלאה בנוזלים וכל הדם צריך לעבור דרך המסתם המיטרלי לחדר השמאלי (Volume overload). המסתם המיטרלי נמצא בתוך טבעת קשיחה ולכן נפח גדול של דם עובר במפתח שלא גדל כך שקיימת היצרות במסתם המיטראלי (Mitral stenosis) יחסי. קיימת זרימה מערבולתית (טורבולנטית) בזמן הדיאסטולה מעל הנקודה המיטרלית בחוד הלב.
- בצילום חזה - הלב גדול כי העליה השמאלית והחדר השמאלי גדולים, העץ הריאתי והעורק הריאתי מתרחב ומתרחשת בצקת ריאות (לא תהיה פגיעה משמעותית בלחץ באבי העורקים אלא לאחר זמן רב).
אבחנה
טיפול
בתינוק עם פגם בינוני ומעלה במחיצה הבין חדרית, יש להזהיר את ההורים, בעיקר לגבי האוכל. בנוסף, יש להזמין בגיל 4 שבועות לביקורת (הזמן הדרוש להורדת תנגודת ריאתית). אם הפגם במחיצה קטן, יש זמן.
תינוק עם פגם במחיצה בין חדרית מזדהם באופן שכיח כי הריאות רטובות, כאשר התינוק במצב של:
- אי ספיקת לב
- זיהום ריאתי
- תת תזונה
יש לחשוב על מצב קשה ולהתחיל טיפול.
טיפול שמרני
- בין 60-80% מהפגמים במחיצה הבין חדרית יקטנו ואפילו יסגרו במהלך השנה הראשונה לחיים (בעיקר הקטנים יותר).
- יש להפריד את הארוחות למנות יותר קטנות. (עקב התעייפות התינוק אינו מסוגל לאכול מנות גדולות ומגביר את קצב נשימותיו).
- בשל הבצקת, יהיה קל יותר לתינוק אם ישב.
- תרופות ב-3 רמות:
- Preload - מתן תרופות שמורידות מעמסת נוזלים על הלב. למשל משתנים.
- יכולת כיווץ (Contractility) - החדר השמאלי עובד קשה וצריך לעזור לו על ידי טיפול ביכולת הכיווץ. ניתן לעשות ע"י Digoxin (בבית), ו-Dopamine. נותנים טיפול למרות שניתן לראות באקוקרדיוגרפיה שהלב עובד בצורה נמרצת. בעבודות קליניות התברר שמתן Digoxin משפר את המצב. ככל הנראה, ברמת המיקרו קיימות בעיות שהתרופה עוזרת להם. לא ידוע בדיוק מנגנון הפעולה (Digoxin מאט).
- Afterload - הכי הגיוני להוריד אותו. ניתן לכוון כך את הכדוריות האדומות לאבי העורקים על ידי הורדת התנגודת הסיסטמית. נותנים למשל Captopril. צריך להיזהר לא להוריד מדי את התנגודת ולכן צריך לעשות זאת בצורה מבוקרת.
אפשר להתחיל עם כל התרופות יחד או בהדרגה, ומתחילים לטפל בילד כשמנסים להשיג זמן. אם מתחילים לטפל והילד נרגע ומתחיל לגדול ולהעלות במשקל והחור מתחיל להסגר - הטיפול הצליח. במידה ומגיעים לטיפול מירבי והילד לא מגיב, יש לפנות לכירורגיה (כאשר התינוק מגיע כבר לגיל של 2-3 חודשים).
טיפול ניתוחי
קיימות שתי אפשרויות:
- ניתוח פליאטיבי (Palliative) - Pulmonary artery banding. ניתוח זה עוזר אך לא פותר בעיה. זהו ניתוח לב סגור. דרך בית השחי חושפים את העורק הריאתי ומצרים את הקוטר שלו על ידי רצועה (Band). בהצרות העורק הריאתי מעלים את התנגודת שלו ולכן הדלף קטן, והילד נרגע.
- מגבלות הניתוח
- בהידוק חזק מדי – הילד הופך לכחול (היפוך הלחצים).
- בהידוק חלש מדי - הריאות ממשיכות להיות מוצפות.
- בקישור בעייתי של אבי העורקים – נגרם נזק בשל הפסקת זרימת הדם לגוף.
- בכל מקרה יש להסיר את הטבעת גם אם הפגם במחיצה הבין חדרית קטן.
הניתוח היה פופולרי לפני 10 שנים. זהו ניתוח פשוט, ובשנים האחרונות נוטים יותר לעשות ניתוחי לב פתוחים.
- ניתוח לריפוי (Curative) - מבצעים פעולה בניתוח לב פתוח וסוגרים על ידי טלאי. במהלך הניתוח משתמשים במכונת לב ריאה. התמותה בניתוחי לב פתוחים היא כ-5%, עם הצלחה ב-95% עד 97% מהמקרים. אחרי סגירת הפגם במחיצה הבין חדרית איכות החיים ותוחלת החיים מצוינים.
פרוגנוזה
סיבוכים
- בפגם קטן במחיצה בין חדרית - דלקת זיהומית של פנים הלב.
- בפגם בינוני או גדול במחיצה הבן חדרית - במקומות שלא מטופלים עשויה להיווצר תסמונת אייזנמנגר (Eisenmenger's syndrome). העץ הריאתי מוצף על ידי זרימה ומנסה להתגונן. בכלי דם ריאתי, כמנגנון הגנה, מתרחש כיווץ של שריר הדופן, בעקבותיו קטנים החלל ועובי הדופן, כך שלא יגיע כל כך הרבה דם. שינוי זה הוא הפיך. בהפסקת הזרימה הכיווץ נפסק והקוטר חוזר למצבו הרגיל. התהליך קורה במידה והגירוי נמשך זמן רב (כשנתיים באופן לא מטופל). בילדים עם חור גדול מסוג פגם במחיצה האטריוונטריקולרית, מדובר על כשנה. לאחר זמן רב נוצר תהליך של פרוליפרציה (Proliferation) של הדופן שגורמת להתחלה של היפרטרופיה (Hypertrophy) של הדופן, השריר והאנדוקרד. כלי הדם נעשים קטנים בשל בניה. אט אט, שטח הפנים של הריאות הולך וקטן. התנגודת גדלה, הלחץ בחדר הימני צריך לעלות כדי להזרים לריאות. לכן, הזרימה מואטת. לכאורה זהו תהליך חיובי, מעין תקופת "ירח דבש" ("Honey moon") משום שאין דלף משמאל לימין (הלחצים קרובים לשוויון). עם הזמן, הדלף עובר היפוך והופך להיות מצד ימין לשמאל והילד הופך מורוד לכחול. אם הילד מגיע בגיל 3 למשל, ורוצים לנתח ולסגור פגם במחיצה הבין חדרית, לא ניתן לעשות זאת מבלי להרוג אותו. בסגירת פגם בשלב זה, לחדר ימין אין לאיפה להזרים את הדם ולכן מתרחשת אי ספיקת לב ימנית ומוות. כמו כן, ניתן להשתיל ריאות חדשות ולרוב גם לב חדש. בתסמונת זו מגיעים למצב בלתי הפיך. לכן, פגם בינוני או גדול במחיצה בין חדרית צריך להיות סגור עד גיל שנה. אם לילד יש תסמונת דאון עם פגם במחיצה האטריוונטריקולרית עושים זאת אפילו קודם.
יש לעקוב אחרי הילדים ולבדוק לחצים. בודקים באקוקרדיוגרפיה את מהירות הזרימה בין החדר השמאלי לימני:
עד שנתיים המצב הפיך. אחרי כן, מתחילים תהליכים בלתי הפיכים.
בתסמונת רואים דווקא מפרצות (אנוריזמות) של כלי הדם הגדולים.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק