נוגדנים כנגד hydroxylase-21
| מדריך בדיקות מעבדה | |
| נוגדנים כנגד hydroxylase-21 | |
|---|---|
| שמות אחרים | Hydroxylase Antibody 21 OH Ab-21 Adrenal antibody |
| מעבדה | אימונולוגיה בדם |
| תחום | אבחון מחלת אדיסון |
| טווח ערכים תקין | רמת נוגדנים הנמוכה מ- 1U/mL בכל קבוצות הגיל ול-2 המינים. רמת נוגדנים מעל 1 U/mL יכולה לרמוז על מחלת אדיסון. |
| יוצר הערך | פרופ' בן-עמי סלע |
ראו גם – Steroid 21-hydroxylase
מטרת ביצוע הבדיקה
בחינת הסיבה למצבי אי-ספיקה של האדרנל;
זיהוי מטופלים בסיכון לפתח כשל אוטו-אימוני של האדרנל בעתיד;
בחינת אפשרות שהמטופל סובל מ-Polyglandular autoimmune syndrome, type 2.
בסיס קליני
מחלת אדיסון או בשמה הסיסטמתי chronic primary adrenal insufficiency נגרמת בעיקר על ידי הרס קליפת בלוטת יותרת הכליה (להלן אדרנל) במנגנון אוטו-אימוני, והיא מאופיינת על ידי נוכחות בנסיוב של נוגדנים עצמיים כנגד הקורטקס האדרנלי. מחלת אדיסון יכולה להופיע באופן ספורדי או בשילוב עם מחלות אוטו-אימוניות אנדוקריניות, המהוות ביחד את מה שמוגדר כ-APS או autoimmune polyglandular syndrome על שני סוגיה (type 1 ו-type 2). נמצא שהאנטיגן העצמי שכנגדו מתקיימת התגובה האוטו-אימונית העיקרית, הוא האנזים המיקרוזומאלי hydroxylase-21 שהוא חלבון בעל משקל מולקולארי של כ-55,000 דלטון. לכן משמשים הנוגדנים כנגד hydroxylase-21 כסמנים של מחלת אדיסון. נוגדנים כנגד OH-21 יכולים להופיע אפילו לפני הופעת תסמינים של הפחתת התפקוד האנדוקריני.
פתולוגיה
השינויים הפתולוגיים באי-ספיקה אוטו-אימונית של האדרנל משתנים עם שלב המחלה: בשלב ההתחלתי בלוטות האדרנל עשויות לגדול, עם הסננה אינטנסיבית של לימפוציטים (Neville ו-Mackay ב-Cin Endocrinol Metab משנת 1972, ו-Guttman ב-Arch Pathol משנת 1930). במחלה ארוכת טווח, בלוטות קטנות ועתים אף קשה לזהותם. קפסולת הבלוטות מעובה ופיברוטית, והקורטקס נהרס בשלמותו, למרות שעשויים להיות מספר צברים קטנים של תאים אדרנו-קורטיקליים, המוקפים על ידי לימפוציטים. מליבה (medulla) של האדרנל נשמרת באופן יחסי ללא פגיעה.
ההתפתחות של אי-ספיקה של האדרנל עוברת מסלול של 4 שלבים:
- stage 1 בו מוצאים רמה גבוהה של פעילות renin בפלזמה ופעילות נורמאלית או אף מעט נמוכה של אלדוסטרון בנסיוב;
- stage 2 בו מוצאים תגובה לקויה של קורטיזול לגירוי עם cosyntropin שהוא פפטיד סינתטי המשמש כאנלוג של ACTH או קורטיקוטרופין;
- stage 3 בו מוצאים רמה גבוהה של רמת ACTH ורמה נורמאלית של קורטיזול בדגימת בוקר;
- stage 4 בו מוצאים רמה קורטיזול נמוכה בדגימת בוקר.
ריכוז הנוגדנים העצמיים בנסיוב, בעיקר אלה כנגד CYP21A2, נמצא במתאם חזק עם דרגת אי התפקוד של האדרנל. אי ספיקת האדרנל מגיע לביטוי קליני רק לאחר שלפחות 90% מקורטקס האדרנל נהרס (Saenger וחב' ב-J Clin Endocrinol Metab משנת 1982, ו-De Bellis וחב' ב-J Clic Endocrinol Metab משנת 1993). בתרחיש של אי-ספיקה אוטו-אימונית של האדרנל, מוצאים בנסיוב גם נוגדנים עצמיים כנגד בלוטות אנדוקריניות אחרות (Laureti וחב' ב- J Clin Endocrinol Metab משנת 1998).
מחלת אדיסון היא תרחיש אנדוקריני בו נהרסים חלקים של קליפת האדרנל, מה שגורם לחסר של הורמונים סטרואידים המופרשים על ידי בלוטות אלו, כגון קורטיזול ואלדוסטרון. מחלה זו עלולה להיגרם מסיבות שונות אם כי שני הגורמים העיקריים הם ריאקציה אוטו-אימונית בארצות המערב או הדבקות בפתוגנים שונים בארצות מתפתחות. זוהו שלושה חלבונים באדרנל בעלי פוטנציאל לשמש כאנטיגנים כנגדם נוצרים נוגדנים אנטי-קורטיקאלים:
- hydroxylase-21 (או OH-21)
- hydroxylase-17 (או OH-17)
- ציטוכרום P-450.
מבין שלושת האנטיגנים הללו, הבדיקה השכיחה ביותר היא זו הבודקת רמת נוגדנים כנגד OH-21, כיוון ש-2 החלבונים האחרים נמצאים גם ברקמות שאינן קשורות לאדרנל, ולכן נוגדנים כנגדם אינם ספציפיים וראויים לאבחון מחלת אדיסון.
האם ייתכן שתוצאות בדיקת הנוגדנים כנגד OH-21 תתקבלנה שליליות ובכל זאת מדובר ללא ספק במחלת אדיסון? התשובה היא חיובית שכן מחלת אדיסון אינה תמיד מחלה אוטו-אימונית באופייה, והיא יכולה להיגרם על ידי הדבקה בפתוגנים שונים, על ידי טראומה, מחלה סרטנית ואטיולוגיות אחרות, כל שניתן ללקות במחלה ללא כל נוגדנים עצמיים.
תסמינים כגון היפר-פיגמנטציה, חולשה, לחץ-גם נמוך וכמיהה למלח, עלולים להחשיד תרחיש של אי-ספיקה של האדרנל, בעיקר אם תסמינים אלה נוטים להחמיר במקביל למצבי עקה (stress).
hydroxylase-21
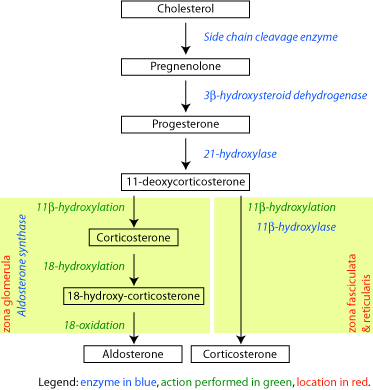
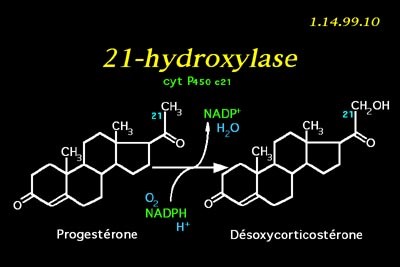
האנזים Steroid 21-hydroxylase הוא אנזים הכלול בציטוכרום P450, ותפקידו מרכזי בביו-סינתזה של ההורמונים הסטרואידים אלדוסטרון וקורטיזול. באדם, Hydroxylase-21 מקודד על ידי הגן CYP21A2. חלבוני ציטוכרום P450 הם מונו-אוקסינאזות המקטלזות ריאקציות רבות הקשורות במטבוליזם של תרופות ובסינתזה של כולסטרול, סטרואידים וליפידים אחרים. האנזים hydroxylase-21 ממוקם ברטיקולום האנדופלזמי, והוא מביא להידרוקסילציה של סטרואידים בעמדה 21.
שכיחות הנוכחות של נוגדנים עצמיים כנגד בלוטת האדרנל או כנגד רקמות אחרות במטופלים עם אי-ספיקה אוטו-אימונית של האדרנל
נוגדנים כנגד האדרנל ב-60-70% מהמקרים;
נוגדנים כנגד thyroid peroxidase ב-50% מהמקרים;
נוגדנים כנגד ה- parathyroidב-26% מהמקרים;
נוגדנים כנגד איי בלוטת הלבלב ב-8% מהמקרים;
נוגדנים כנגד השחלות ב-22% מהמקרים;
נוגדנים כנגד האשכים ב-5% מהמקרים;
נוגדנים כנגד תאים פריאטליים ב-30% מהמקרים;
נוגדנים כנגד intrinsic factor ב-9% מהמקרים.
השכיחות של נוגדנים כנגד האדרנל במטופלים עם פעילות תקינה של בלוטה זו, אך עם מחלות אנדוקריניות אוטו-אימוניות אחרות, היא נמוכה (כ-2%), עם יוצאי הדופן שהם מטופלים עם hypoparathyroidism, כאשר ב-16% מתוכם ניתן למצוא נוגדנים עצמיים כנגד האדרנל. רמת השכיחות של נוגדנים כנגד האדרנל במטופלים עם מחלה אוטו-אימונית של בלוטה אנדוקרינית אחרת היא כדלקמן:
Hypoparathyroidism (16%);
מחלת זפק Goitrous autoimmune thyroiditis (1.9%);
Hyperthyroidism (1.9%);
Atrophic autoimmune thyroiditis (1.7%);
סוכרת (1.2%);
Pernicious anemia (פחות מ-1%).
בשלושה מחקרים שכללו במקובץ למעלה מ-2,000 ילדים ומבוגרים, נמצא ש-1-2% מהנבדקים עם סוכרת type 1 הכילו בדמם נוגדנים כנגד hydroxylase-21 (ע"פ Brewer וחב' ב-N Eng J Med משנת 1997, Yu וחב' ב-J Clin Endocrinol Metabol משנת 1999 ו-Triolo וחב' ב-Diabetes Care משנת 2011). לכן, אין המלצה לסקירה שגרתית של חולי סוכרת type 1 לנוכחות נוגדנים כנגד hydroxylase-21.
תסמונת autoimmune adrenalitis מתאפיינת בנוכחות נוגדנים כנגד האנזימים המפורטים להלן הקשורים לסינתזת סטרואידים:
P450scc (CYP11A1, side-chain cleavage enzyme),
P450c17 (CYP17, 17-alpha-hydroxylase)
(P450c21 (CYP21A2, 21-hydroxylase (על פי Nerup ב-Acta Endocrinol משנת 1974, ו-Boscaro וחב' ב-J Clin Endocrinol Metab משנת 1994, כמו גם Song וחב' באותו כתב עת ובאותה שנה). אנזימים אלה כרוכים בביקוע של שרשרת צדדית ובהמשך בהידרוקסילציה של סטרואידים. הנוגדנים העצמיים כנגד CYP21A2 הם מתת הסוגים IgG1 או-IgG2a (על פי Chen וחב' ב-J Clin Endocrinol Metab משנת 1998, ו-Brozzetti וחב' ב-Eur J Endocrinol משנת 2010), מה שמרמז שתאי Th משתתפים בהרס הקורטקס של בלוטות האדרנל בחולים עם מחלת אדיסון אוטו-אימונית (Bøe וחב' ב-Eur J Endocrinol משנת 2004).
חסינות הומוראלית
- נוגדנים אנטי-אדרנאליים
מחקרים מוקדמים העריכו את היכולת של נוגדנים בנסיוב להגיב עם קליפת בלוטות האדרנל בפרימטים על ידי שימוש בטכניקה בלתי-ישירה של immunofluorescence. כיוון שבדיקה זו מגלה נוגדני IgG כלשהם הקשורים לקורטקס האדרנל, היא אינה ספציפית לאנטיגן מסוים. לכן מתייחסים בתוצאות לנוגדנים אלה כאל anti-adrenal antibodies, מה שמשקף את האופי הבלתי-ספציפי שלהם. מחקרים מאוחרים יותר מראים שנוגדני אנטי-אדרנל המתגלים על ידי אימונו-פלואורסצנציה על חתכי רקמת האדרנל היו מכוונים בעיקר כנגד CYP17 ו-CYP21A2 (על פי Chen וחב' ב-J Clin Endocrinol Metab משנת 1996).
נוגדנים עצמיים לכל שלושת האזורים של הקורטקס האדרנלי נמצאים בנסיוב של 60-75% מהנבדקים עם אי-ספיקה ראשונית של האדרנל (primary adrenal insufficiency) הנגרמת על ידי אדרנליטיס אוטואימונית; לעומת זאת, נוגדנים אלה נמצאים אך לעתים נדירות בנסיוב של נבדקים המאובחנים עם סיבות אחרות לאי-ספיקה של האדרנל, או בנסיוב של בני-משפחה מדרגה ראשונה של חולים עם אי-ספיקה ראשונית של האדרנל מסיבות אוטו-אימוניות, או באנשים בריאים (Blizzard וחב' ב-Clin Exp Immunol משנת 1967, Irvine ו-Barnes ב-Clin Endocrinol Metabol משנת 1975, Colls וחב' ב-Clin Chem משנת 1995, ו-Falcorni וחב' ב-J Clin Endocrinol Metab משנת 1995).
נוגדנים כנגד האדרנל שכיחים יותר בנשים, בעיקר באלו עם polyglandular autoimmune syndrome type 2. מטופלים המכילים בנסיוב נוגדנים אלה מפתחים אי-ספיקה של האדרנל בקצב של עד 19% בשנה (Ahonen וחב' ב-J Clin Endocrinol Metab משנת 1987, ו-Betterle וחב' ב-J Endocrinol משנת 1988). בשתי התסמונות, autoimmune polyendocrinopathy syndrome type 1 ו- autoimmune polyendocrinopathy-candidiasis- ectodermal dystrophy syndrome, הנוכחות של נוגדנים עצמיים לאדרנל היא בעלת ערך ניבוי של 92% להתפתחות של אי-ספיקה של האדרנל (Gylling וחב' ב-J Clin Endocrinol Metab משנת 2000).
רגישות גנטית
אי-ספיקה אוטו-אימונית של האדרנל, יכולה להיות משפחתית או לא-משפחתית. בערך שליש מהמטופלים הם אלה שבמשפחתם יש פרטים נוספים עם תסמונת זו, בהשוואה לכמחצית מהמטופלים עם אי-ספיקה של האדרנל כחלק ממצב של polygladular autoimmune syndrome מסוג I או מסוג II. רגישות גנטית לאי-ספיקה אוטו-אימונית של האדרנל כרוכה באופן חזק עם האללים HLAB8 HLADR3 ו- HLADR4, פרט למצב בו אי-ספיקת אדרנל זו מופיע כחלק מ-polygladular autoimmune syndrome type I, תרחיש בו לא נמצא כל קשר עם HLA.
הגן האחראי ל- polygladular autoimmune syndrome type I, ממוקם על כרומוזום 21q22.3, גן זה מכונה AIRE או Autoimmune regulator, והוא מקודד לחלבון שהוא כנראה גורם שעתוק (transcription factor). יחד עם זאת, הגנים ל- CYP11A1 ול-Cyp17, שני היעדים הנוספים לפעילות של נוגדנים עצמיים כנגד האדרנל במטופלים של אי-ספיקה אוטו-אימונית של האדרנל, יושבים על כרומוזומים 15q23-q24 ו-10q24-q25, בהתאמה. לכן גנים אלה אינם קשורים להפלוטיפים של HLA, ואינם מעורבים בכל רגישות גנטית של אדרנליטיס אוטו-אימונית.
במחקר אחד של 94 מטופלים בנורווגיה, 38 מתוך 40 (95%) עם אי-ספיקה של האדרנל למשך פחות מ-5 שנים, ו-6 מתוך 10 מטופלים (60%) שסבלו מאי-ספיקה של האדרנל משך יותר מ-35 שנה היו בעלי נוגדנים עצמיים לאדרנל (Myhre וחב' ב-J Clin Endocrinol Metab משנת 2002). הנוכחות של נוגדנים עצמיים לאדרנל יכולה להיות מנבא חזק יותר של אי-ספיקה של האדרנל בילדים מאשר במבוגרים.
מחקר אחד העריך 10 ילדים עם hypoparathyroidism אוטו-אימוני או עם סוכרת, בהם נמצאו נוגדנים עצמיים כנגד הקורטקס של האדרנל וכן נוגדנים כנגד CYP21A2: נמצא שתשעה מתוך 10 ילדים אלה פיתחו אי-ספיקה של האדרנל בפרק זמן של 3-121 חודשים של המעקב (Betterle וחב' ב-J Clin Endocrinol Metab משנת 1997). לעומת זאת, מחקר אחר של אותם חוקרים שהתפרסם באותו כתב-עת ובאותה שנה העריך 48 מבוגרים עם מפגע אוטו-אימוני ונוגדנים עצמיים כנגד הקורטקס של האדרנל (44 מתוך 48 הנבדקים הכילו נוגדנים כנגד CYP21A2); רק 21% ממדגם זה פיתחו אי-ספיקה גלויה של האדרנל, בעוד ש-29% מתוך המדגם פיתחו אי-ספיקה תת-קלינית של האדרנל לאורך 4 שנות מעקב. במחקר נוסף נמצא שב-100 מטופלים עם נוגדנים עצמיים כנגד הקורטקס האדרנלי, הסיכון לפתח אי-ספיקה גלויה של האדרנל לאורך מעקב של 6 שנים, היה של 100% בקרב ילדים ורק של 32% בקרב מבוגרים (Coco וחב' ב-J Clin Endocrinol Metab משנת 2006).
במחקר שכלל 90 מטופלים בשוודיה, נורבגיה וגרמניה עם type I polyglandular autoimmune syndrome, מדידת פעילות CYP21A2 לבדו, הייתה מספקת כדי לנבא מצב של אי-ספיקת האדרנל (Söderbergh וחב' ב-J Clin Endocrinol Metab משנת 2004). מחקר נוסף שנערך באיטליה וכלל 222 מטופלים עם אי-ספיקה ראשונית של האדרנל, נוכחות סימולטאנית של נוגדנים עצמיים כנגד הקורטקס של האדרנל כמו גם כנגד CYP21A2, אפשרו לקבוע אבחנה מוחלטת של אי-ספיקה אוטו-אימונית של האדרנל (Falorni וחב' ב-J Clin Endocrinol Metab משנת 2004).
נוגדנים כנגד בלוטות אנדוקריניות אחרות
אנשים בריאים מכילים בדמם אך לעתים נדירות נוגדנים עצמיים כנגד בלוטות אנדוקריניות אחרות, אך תופעה זו שכיחה באלה עם אי-ספיקה אוטו-אימונית של האדרנל ((Blizzard וחב' ב-.Clin Exp Immunol משנת 1966, ו- McHardy וחב' ב- Clin Endocrinolמשנת 1972). אצל למעלה ממחצית המטופלים עם אי-ספיקה אוטו-אימונית של האדרנל ניתן למצוא בנסיוב רמה מוגברת של נוגדנים עצמיים כנגד האנזים peroxidase של בלוטת התריס (Zelissen וחב' ב-J Autoimmun משנת 1995), כאשר כמעט מחצית מהאחרונים סובלים מתת-פעילות גלויה של הבלוטה (overt hypothyroidism). רבים אחרים סובלים מהיפו-תירואידיזם תת-קליני (עם רמה מוגברת שלTSH ורמה נורמאלית של T4), אך פרטים אלה נמצאים בסיכון לפתח היפו-תירואידיזם גלוי (תסמונת Schmidt). הנוכחות של DQB1*0602 נראית כבעלת השפעה המגינה על נושאיה המאובחנים עם APECED או autoimmune polyendocrinopathy-candidiasis-ectodermal dystrophy מפני פיתוח סוכרת type 1, אך הגנה כזו אינה מתקיימת במטופלים עם polyglandular autoimmune syndrome type 2.
האסוציאציות הללו נובעות מהמיקום של הגנים CYP21A1P (P450c21A) ו-CYP21A2 (P450c21B) ביחד עם הגן TNFB*1 המקודד ל-tumor necrosis factor, והגנים המקודדים ל- complement C4A ול-complement C4B באזור class III בין המיקום של class I MHC ו-class II MHC בזרוע הקצרה של כרומוזום 6 (על פי Miller ב- Endocr Rev משנת 1988). עם זאת, במספר משפחות אין כל קשר בין polyglandular autoimmune syndrome type II ל-HLA (על פי Butler וחב' ב-Nature Genet משנת 1994).
יתרה מכך, תירואידיטיס אוטו-אימונית כרונית, אנמיה ממאירה וכשל מוקדם של השחלות, הם כולם מרכיבים של polyglandular autoimmune syndrome type II, אך אינם קשורים לאיזשהם haplotypes של HLA. תצפיות אלה מרמזות שגן או גנים הקשורים ל-haplotypes מסוימים של HLA, גורמים לרגישות לפיתוח אי-ספיקה אוטו-אימונית של האדרנל וסוכרת, בעוד שגנים אחרים שאינם קשורים ל-haplotypes של HLA רלוונטיים לתירואידיטיס אוטו-אימונית כרונית ולמחלה אוטו-אימונית של הקיבה.
יעדים אנטיגניים לנוגדנים עצמיים
פותחו בדיקות ספציפיות לנוגדנים כנגד האנזימים הסטרואידוגנייםP450scc (CYP11A1, side-chain cleavage enzyme), P450c17 (CYP17, 17-α-hydroxylase) ו-p450c21 (CYP21A2, 21-hydroxylase)). מהשוואת תוצאות מ-4 מעבדות שונות, נמצא שנוגדנים עצמיים כנגד CYP21A2, הם השכיחים ביותר בקרב המאובחנים עם APECED (14 מתוך 15 נבדקים), או בקרב אלה עם מחלה ספורדית (83% מתוך 205 נבדקים). בה בשעה, נוגדנים עצמיים כנגד CYP11A1 או CYP17 נמצאו ב-50% בקרב הנבדקים עם מפגעים מסוג polyglandular autoimmune, ובפחות מ-10% מאלה עם מחלות ספורדיות.
גנים non-HLA
הגן האחראי ל-polyglandular autoimmune syndrome type I ממוקם בכרומוזום 21q22.3, שכינויו AIRE או autoimmune regulator, והוא המקודד לגורם שעתוק (Nagamine וחב' ב-Nature Genet משנת 1997). ב-10 מתוך 12 נבדקים עם APECED באוכלוסייה בפינלנד נתגלתה מוטציית Stop בשייר Arg257, ומוטציית שחלוף Lys83Glu נמצאה בשוויץ וב-2 הנבדקים הפיניים הנותרים, כאשר עוד 11 מוטציות התגלו בסריקה ב-36 נבדקים נורבגיים. עם זאת, הגנים המקודדים ל-CYP11A1 ול-CYP17, שהם 2 האנזימים המשמשים יעד לנוגדנים עצמיים ברוב המטופלים עם אי-ספיקה אוטו-אימונית של האדרנל, ממוקמים על כרומוזומים 15Q23-24 ו-10q24-25 (על פי Sparks וחב' ב-Cell Biol משנת 1991). לכן גנים אלה אינם קשורים ל-haplotypes של HLA, ואינם משחקים תפקיד בגרימת רגישות לאדרנליטיס אוטו-אימונית. כללית ניתן לומר שתאים נורמאליים של הקורטקס האדרנלי מבטאים מולקולות של MHC class II, וביטוי שגוי של מולקולות אלו כנראה אינו קשור לפתוגניות שגורמת לאי-ספיקה אוטו-אימונית של האדרנל (Jackson וחב' ב-J Pathol משנת 1988).
בדיקות מעבדה
- רמות קורטיזול משתנות בדם, והן נמצאות בשיאן בשעות הבוקר המוקדמות. אם בלוטת האדרנל אינה מתפקדת באופן תקין או שאינה מגורה על ידי ACTH, רמות קורטיזול תהיינה נמוכות באפן תמידי. לכן מדידת רמות קורטיזול ו-ACTH, בשילוב בדיקת ACTH stimulation test, יסייעו באבחון אי-ספיקת האדרנל.
- ACTH הוא הורמון של בלוטת יותרת המוח (היפופיזה) המאותת לבלוטות האדרנל לייצר קורטיזול. מדידת רמת ACTH בדם תתבצע כבדיקת baseline, להעריך האם ההיפופיזה מייצרת די ACTH. אם לנבדק עם אי-ספיקת האדרנל יש רמות נמוכות של ACTH, הדבר מצביע על אי-ספיקה שניונית של האדרנל, בה בשעה שרמות גבוהות שלACTH מצביעות על מחלת אדיסון או אי-ספיקה ראשונית של האדרנל.
- ACTH stimulation test: בבדיקה זו נמדדת רמת קורטיזול לפני ואחרי הזרקה של ACTH סינתטי. זהו המבחן המתבצע בשכיחות הגבוהה ביותר לאבחון אי-ספיקת האדרנל. אם בלוטות האדרנל מתפקדות היטב, רמת קורטיזול תעלה בתגובה לסטימולציה עם ACTH. אם בלוטות האדרנל ניזוקו או שאינן מתפקדות, התגובה שלהן לסטימולציה עם ACTH תהיה מזערית. מבחן סריקה מהיר זה יוזמן במקביל לבדיקת רמת הבסיס של ACTH, ואם התוצאה המתקבלת אינה תקינה, ניתן לבצע מבחן מתמשך של סטימולציה עם ACTH למשך עד 3 ימים, שיכול לסייע להבדיל בין אי-ספיקה ראשונית או שניונית של האדרנל.
- Corticotropin-releasing hormone (CRH) stimulation test: מבדק זה מתבצע כאשר בדיקת ACTH אינה מתקבלת תקינה. CRH הוא ההורמון ההיפותלמי המעודד יצירת ACTH בהיפופיזה. בבדיקה זו מזריקים CRH סינתטי לווריד ורמות קורטיזול ו-ACTH נמדדות בפרקי זמן של 30 ו-60 דקות לאחר הזרקת CRH. תגובה תקינה תהיה רמת שיא של ACTH, ולאחריה רמת שיא בריכוז קורטיזול. במבחן זה, אלה עם מחלת אדיסון מייצרים רמות גבוהות של ACTH, אך אינם מייצרים קורטיזול. נבדקים עם אי-ספיקה שניונית של האדרנל אינם מגיבים ביצירת ACTH או שיצירת ACTH מתעכבת. אם לנבדק יש היפופיזה פגועה, גירוי של CRH לא יגרום סטימולציה ליצירת ACTH, וחסר בהורמון האחרון מצביע על ההיפופיזה כסיבה. אם התגובה ביצירת ACTH מתעכבת, הדבר מצביע על ההיפותלמוס כסיבה.
- אלדוסטרון: רמות אלדוסטרון בדם או בשתן נמדדות לסייע באבחון מחלת אדיסון, על ידי קביעה אם האדרנל מייצר הורמון זה. אם רמת אלדוסטרון נמוכה, זו ראייה נוספת שמדובר באי-ספיקה ראשונית של הבלוטה.
- אלקטרוליטים (נתרן, אשלגן, כלוריד ופחמן דו-חמצני) נמדדים לסייע לזהות ולהעריך את חומרת מחלת אדיסון. במחלה זו ריכוזי נתרן, כלוריד ופחמן דו חמצני בדרך כלל נמוכים, בעוד שרמת אשלגן עשויה להיות גבוהה מאוד.
- רמות urea וקראטינין נמדדות לנטר את תפקודי כליה.
- רמת גלוקוזה נמדדת שכן סוכר זה יכול להיות נמוך מאוד ברמתו במהלך משבר של האדרנל.
בדיקות המתבצעות באופן מזדמן
- מבחן היפוגליקמיה המושרית על ידי הזרקת אינסולין: בדחיקה הנדרשת לעתים להיווכח האם מחלת היפופיזה היא שגורמת לאי-ספיקה שניונית של האדרנל. בבדיקה זו נמדדות רמות גלוקוזה וקורטיזול לאחר הזרקת אינסולין, זאת על מנת לגרום לעקה בהיפופיזה: באנשים בריאים, רמת הסוכר בדם נופלת ורמת קורטיזול עולה. לעומת זאת, באלה עם אי-ספיקה של האדרנל, רמות קורטיזול תישארנה נמוכות, ואילו רמות גלוקוזה תיפולנה, ולאחר מכן תעלינה באיטיות.
- בדיקת renin: פעילות ההורמון renin עולה בתרחיש של אי-ספיקה ראשונית של האדרנל כיוון שחסר באלדוסטרון גורם להגברת ההפרשה בשתן של נתרן. איבוד זה של רמות נתרן בדם והפחתת כמות הנוזלים בדם גורמת ל-hypovolemia ולהפחתת לחץ הדם, אשר לחילופין גורמים לסטימולציה של יצירת renin בכליה.
- לעתים נדרשת מדידת רמת נוגדנים כנגד hydroxylase-21 כאשר מחלת אדיסון נחשדת. בדיקה זו נחשבת מדד אמין למחלת אדיסון אוטו-אימונית, אך מספר המעבדות המבצעות אותה נמוך יחסית.
- צילום רנטגן עשוי להידרש כדי לבחון הסתיידות (calcification) בקורטקס האדרנלי, שעלול להיגרם במצב של הדבקה עם חיידק שחפת.
הנחיות לביצוע הבדיקה
את הדם יש ליטול במבחנה כימית (פקק אדום) או במבחנת ג'ל (פקק צהוב). ניתן לפסול דגימות מאוד המוליטיות או מאוד ליפמיות, אך דגימות המוליטיות או ליפמיות במידה מתונה ראויות לשימוש. דגימות נסיוב מאוד איקטריות ראויות אף הן לשימוש. דגימות נסיוב מופרד שנשמרו בקירור טובות לשימוש למשך 7 ימים, ואילו נסיוב שנשמר בהקפאה טוב לשימוש עד 14 יום ממועד ההקפאה. לא תתקבל דגימת דם שנשמרה בטמפרטורת החדר. שיטת הבדיקה היא ברוב המעבדות על ידי radioimmunoprecipitation עם אנטיגן ריקומביננטי או בשיטת RIA.
פענוח התוצאות
ממצאים חיוביים של רמת נוגדנים הגבוהה מ-1 U/ml, מצביעים על נוכחות נוגדנים עצמיים כנגד בלוטת האדרנל, מה שתואם את מחלת אדיסון.
ראו גם
- חזרה לדף מדריך בדיקות מעבדה
- בדיקות מעבדה - אבחון מחלות ומפגעים מטבוליים-גנטיים
- בדיקות מעבדה - מחלות אוטו-אימוניות
- בדיקות מעבדה - תפקוד בלוטת האדרנל
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק