הבדלים בין גרסאות בדף "ביומרקרים בסרטן מעי גס גרורתי"
| (9 גרסאות ביניים של אותו משתמש אינן מוצגות) | |||
| שורה 12: | שורה 12: | ||
|יוצר הערך=ד"ר רוית גבע | |יוצר הערך=ד"ר רוית גבע | ||
|אחראי הערך= | |אחראי הערך= | ||
| − | }} | + | }} |
{{הרחבה|סרטן מעי גס גרורתי}} | {{הרחבה|סרטן מעי גס גרורתי}} | ||
| − | סרטן המעי הגס הוא מהממאירויות השכיחות בישראל וגורם התמותה השני מבין גידולי הסרטן בישראל {{הערה|שם=הערה1|הרישום הלאומי לסרטן והמרכז הלאומי לבקרת מחלות, משרד הבריאות. סרטן המעי הגס והחלחולת בישראל - עדכון הנתונים, | + | סרטן המעי הגס הוא מהממאירויות השכיחות בישראל וגורם התמותה השני מבין גידולי הסרטן בישראל{{הערה|שם=הערה1|הרישום הלאומי לסרטן והמרכז הלאומי לבקרת מחלות, משרד הבריאות. סרטן המעי הגס והחלחולת בישראל - עדכון הנתונים, מרץ 2017. [הודעה לעיתונות]. מתוך: https://www.health.gov.il/PublicationsFiles/ICR_05032017.pdf}}. הטיפול במחלה גרורתית מבוסס על ניתוחים, [[כימותרפיה]], טיפולים מכווני מטרה, [[אימונותרפיה]] וטיפולים מקומיים שונים. ככל שהמטופל "חשף לסוגי הטיפולים השונים, כך ניתן יהיה להאריך את חייו. |
| − | לא כל טיפול מתאים לכל מטופל או לכל גידול. יש לחשוף את המטופל לטיפולים המתאימים לו ביותר, משמע לבצע התאמה מרבית בין המאפיינים השונים של המטופל ושל הגידול ובין מאגר הטיפולים הקיים. גישה טיפולית זו, הנקראת "גישה מותאמת אישית", היא הבסיס לאונקולוגיה המודרנית, והיא מתבססת מצד אחד על עבודת צוות רב-תחומי ומצד שני על הבנה ביולוגית הולכת וגדלה של הגידול על ידי שימוש מושכל בביומרקרים - סמנים. ביומרקרים הם מאפיינים ביולוגיים, המבוססים בעיקר על שינויים ברצף הגנטי של הגידול, ועוזרים לסווג את הגידול לתתי-סוגים ובכך להתאים את הטיפול. גישה זו הובילה לשיפור משמעותי בפרוגנוזה של סרטן מעי גס גרורתי עם תוחלת חיים חציונית של בין שנתיים וחצי לשלוש שנים {{הערה|שם=הערה2|Van Cutsem E, Cervantes A, Adam R, et al. ESMO consensus guidelines for the management of patients with metastatic colorectal cancer. Ann Oncol. 2016 Aug;27(8):1386-422. Epub 2016 Jul 5.}}. | + | לא כל טיפול מתאים לכל מטופל או לכל גידול. יש לחשוף את המטופל לטיפולים המתאימים לו ביותר, משמע לבצע התאמה מרבית בין המאפיינים השונים של המטופל ושל הגידול ובין מאגר הטיפולים הקיים. גישה טיפולית זו, הנקראת "גישה מותאמת אישית", היא הבסיס לאונקולוגיה המודרנית, והיא מתבססת מצד אחד על עבודת צוות רב-תחומי ומצד שני על הבנה ביולוגית הולכת וגדלה של הגידול על ידי שימוש מושכל בביומרקרים - סמנים. ביומרקרים הם מאפיינים ביולוגיים, המבוססים בעיקר על שינויים ברצף הגנטי של הגידול, ועוזרים לסווג את הגידול לתתי-סוגים ובכך להתאים את הטיפול. גישה זו הובילה לשיפור משמעותי בפרוגנוזה של סרטן מעי גס גרורתי עם תוחלת חיים חציונית של בין שנתיים וחצי לשלוש שנים{{הערה|שם=הערה2|Van Cutsem E, Cervantes A, Adam R, et al. ESMO consensus guidelines for the management of patients with metastatic colorectal cancer. Ann Oncol. 2016 Aug;27(8):1386-422. Epub 2016 Jul 5.}}. |
==RAS== | ==RAS== | ||
| − | RAS הוא סמן מרכזי לניבוי התגובה לתרופות מסוג [[נוגדי EGFR]]{{כ}} (Epidermal growth factor receptor) שהם סטוקסימאב [[Cetuximab]] - (ארביטוקס - | + | RAS הוא סמן מרכזי לניבוי התגובה לתרופות מסוג [[נוגדי EGFR]]{{כ}} (Epidermal growth factor receptor) שהם סטוקסימאב [[Cetuximab]] - (ארביטוקס - Erbitux) ופאניטומומאב - [[Panitumumab]] (וקטיביקס - Vectibix)*. נוגדי EGFR הם נוגדנים החוסמים את שרשרת הפעילות התאית המתחילה ברצפטור EGFR לאחר קישורו לליגנד. הסיגנל התאי מוביל בסופו של דבר לתהליכים מהותיים בתא, כגון פרוליפרציה, התמיינות והיצמדות תאים. עיכוב מסלול זה גורם להאטת צמיחת התאים ואף לנסיגת הגידול. |
| + | |||
| + | לאחר קישור הליגנד 7-EGFR, השרשרת התוך תאית ממשיכה למספר חלבונים מהותיים, מהם חלבוני משפחת RAS - חלבונים מסוג small GTPases המפרקים מולקולות GTP {{כ}} ( (guanosine triphosphate) ל-GDP {{כ}}(guanosine diphospRate). כאשר הגידול, מפתח מוטציה בחלבונים אלו, השרשרת התאית מופעלת באופן עצמא׳ ללא צורך בקשירת הליגנד לרצפטור. לאור כך, גידולים המבטאים מוטציה ב-RAS אינם מגיבים לטיפולים בנוגדי EGFR ואין תועלת משמעותית לשילובם בטיפול{{הערה|שם=הערה3|Aprile G, Macerelli M, De Maglio G, et al. The relevance of BRAF and extended RAS mutational analyses for metastatic colorectal cancer patients. OA Mol Oncol. 2013 Dec 25;1(1):7-15.}}. (תרשים מס' 1). | ||
| − | |||
[[קובץ:EGFR1.jpg|ממוזער|מרכז|600 פיקסלים|תרשים מס׳ 1: השרשרת התאית של EGFR]] | [[קובץ:EGFR1.jpg|ממוזער|מרכז|600 פיקסלים|תרשים מס׳ 1: השרשרת התאית של EGFR]] | ||
| − | |||
| − | מוטציה ב-KRAS או NRAS נמצאת בעד כ-50% מגידולי המעי הגס הגרורתיים. גידולים אלו נחשבים אגרסיביים יותר, ולמטופלים יש תוחלת חיים נמוכה יותר {{הערה|שם=הערה3}}. | + | המוטציות המרכזיות שהוכחו כמנבאות עמידות לסטוקסימאב ופאניטומומאב נמצאות בגנים לקידוד חלבוני [[KRAS]] ו-NRAS. גידול ללא מוטציה ב-NRAS ו-KRAS מוגדר כ-wild type) RAS-WT), ובטיפול בו ניתן לשלב תרופות אלו עם המשלבים הכימותרפיים השונים. |
| + | |||
| + | מוטציה ב-KRAS או NRAS נמצאת בעד כ-50% מגידולי המעי הגס הגרורתיים. גידולים אלו נחשבים אגרסיביים יותר, ולמטופלים יש תוחלת חיים נמוכה יותר{{הערה|שם=הערה3}}. | ||
בדיקת מוטציות ב-RAS היא בדיקה בסיסית בהתאמת הטיפול ונמצאת בסל הבריאות. הבדיקה מבוצעת מיד עם האבחנה של מחלה גרורתית כדי לעזור בהכוונת הקו הטיפולי הראשון. | בדיקת מוטציות ב-RAS היא בדיקה בסיסית בהתאמת הטיפול ונמצאת בסל הבריאות. הבדיקה מבוצעת מיד עם האבחנה של מחלה גרורתית כדי לעזור בהכוונת הקו הטיפולי הראשון. | ||
| שורה 34: | שורה 36: | ||
==BRAF== | ==BRAF== | ||
| − | החלבון | + | החלבון הבא בשרשרת התאית לאחר RAS הוא BRAF. בתהליך דומה ל-RAS, מוטציה בגן המקודד לחלבון זה מאפשרת לשרשרת התוך תאית לפעול ללא ליגנד ומוריד האת יעילות העיכוב ברמת הרצפטור המבוצע על ידי סטוקסימאב ופאניטומומאב. בניגוד למוטציה ב-RAS, מוטציה ב-BRAF נדירה יותר ונמצאת בכ-8% מהגידולים {{הערה|שם=הערה3}}. (תרשים נוס' 1). |
| − | לאור מיעוט החומים המתגלים עם מוטציה זו וכן מורכבות השרשרת התוך תאית, קיום מוטציה זו נחשב כמפחית משמעותית את יעילות נוגדי EGFR | + | |
| − | או בשילוב הנ"ל עם עיכוב מסלולים תוך תאיים נוספים, כגון דרך מעכבי MEK. קיימים מחקרים רבים הבודקים את התשלובות השונות לתת קבוצה זו | + | לאור מיעוט החומים המתגלים עם מוטציה זו וכן מורכבות השרשרת התוך תאית, קיום מוטציה זו נחשב כמפחית משמעותית את יעילות נוגדי ה-EGFR אך לא מבטל אותה לחלוטין. גידולים אלו נחשבים תת-אוכלוסייה אגרסיבית במיוחד במעי גס גרורת׳ עם תוחלת חיים נמוכה ועמידות לטיפולים. מחקרים שונים מציעים לאוכלוסייה זו טיפולים במשלבים מורכבים יותר, כגון [[FOLFOXIRI]] ובווציזומאב - [[Bevacizumab]] (אווסטין - Avastin)*, בשילובים של כימותרפיה + נוגדי EGFR + מעכבי BRAF שונים, כגון ומורפניב - [[Vemurafenib]] (זלבורף - Zelboraf)* או בשילוב הנ"ל עם עיכוב מסלולים תוך תאיים נוספים, כגון דרך מעכבי MEK. קיימים מחקרים רבים הבודקים את התשלובות השונות לתת קבוצה זו {{הערה|שם=הערה4|Abdel-Rahman O. Targeting BRAF aberrations in advanced colorectal carcinoma: from bench to bedside. Future Oncol. 2016 Jan;12(1):25-30. Epub 2015 Nov 30.}}. הבדיקה מבוצעת באופן שגרתי במקומות רבים בעולם, אך אינה כלולה בסל שירותי הבריאות בישראל. |
(*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים. | (*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים. | ||
| + | ==MSI-H / MMR== | ||
| + | קיום microsatellite instability) MSI) משמעו קיום רצפים החוזרים על עצמם בתדירות גבוהה לאורך דנ"א הגידול. החזרות גורמות למוטציות רבות. כאשר קיימות חזרות, הגידול נחשב MSI-H) high microsatellite instable), וכאשר הן לא נמצאות, הגידול נחשב microsatellite stable) MSS). קיום הרצפים הוא למעשה סמן לפגיעה בחלבוני תיקון הדנ"א - MMR {{כ}}(mismatch repair proteins ולכן פגיעה זו ניתן לבדוק על ידי PCR (Polymerase Chain Reaction), ברמת הדנ"א הגידולי או ברמת ביטוי החלבונים באמצעות אימונוהיסטוכימיה. | ||
| + | כ-15% מגידולי המעי הגס מתפתחים על רקע פגיעה זו במנגנון תיקון הדנ"א. הפגיעה יכולה להיות אקראית או תורשתית המקושרת לתסמונת לינץ' (Hereditary non-polyposis colon cancer - HNPCC). באוכלוסיית סרטן המעי הגס הגרורתי הפגיעה מאותרת בכ-4-3% מהגידולים. | ||
| + | עבודות ראשוניות בקבוצות קטנות של חולים מראות יעילות גבוהה לטיפול אימונותרפי בנוגדי PD1 פמברוליזומאב - [[Pembrolizumab]] (קיטרודה - Keytruda)* וניבולומאב - [[Nivolumab]] (אופדיבו - Opdivo)* או PD-L1 כגון אטזוליזומאב - [[Atezolizumab]] (טסנטריק - Tecentriq)* בגידולים עם MSI-H במטופלים שמיצו את הקווים הטיפוליים המקובלים {{הערה|שם=הערה6|Diaz LA, Marabelle A, Delord JP, et al. Pembrolizumab therapy for microsatellite instability high (MSI-H) colorectal cancer (CRC) and non-CRC. [abstract]. J Clin Oncol. 2017; 35(15_suppl): 3071.}}, {{הערה|שם=הערה7|Tejpar S, Stintzing S, Ciardiello F, et al. Prognostic and predictive relevance of primary tumor location in patients with RAS wild-type metastatic colorectal cancer. JAMA Oncol. 2017;3(2):194-201. Epub 2016 Oct 10.}}. מחקרים נוספים מבוצעים לאישור שילוב האימונותרפיה בשלבי הטיפול השונים בגידולים עם MSI-H. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
בארצות רבות בדיקת MSI נכנסת לשימוש קבוע בחולי סרטן מעי גס גרורתי. הבדיקה עדיין אינה כלולה בסל שירותי הבריאות בישראל לאינדיקציה זו, אך מבוצעת כחלק מהבירור הגנטי במטופלים הנחשדים לתסמונת לינץ'. | בארצות רבות בדיקת MSI נכנסת לשימוש קבוע בחולי סרטן מעי גס גרורתי. הבדיקה עדיין אינה כלולה בסל שירותי הבריאות בישראל לאינדיקציה זו, אך מבוצעת כחלק מהבירור הגנטי במטופלים הנחשדים לתסמונת לינץ'. | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | (*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים. | |
| − | או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים. | + | |
| + | ==ימין ושמאל== | ||
| + | התפתחות המעי הגס בעובר נובעת משני מקורות שונים - האחד מפתח את המעי הימני, והשני את המעי השמאלי, המתחברים בסופו של דבר לאיבר המשכי אחד. אנו למדים שהמקורות השונים גורמים להתפתחות סוגי סרטן מעי גס בעלי מאפיינים מולקולריים שונים, ועל כן בעלי התנהגות שונה, כולל תגובה שונה לטיפולים. | ||
| + | גידולים בצד שמאל של המעי המתפתחים מהמעי האחורי (hindgut) הם בעלי פרוגנוזה טובה יותר ומגיבים טוב יותר לטיפולים השונים. בגידולי RAS-WT במעי שמאלי נראית עדיפות להתחיל טיפול קו ראשון בתשלובת עם נוגדי EGFR. גידולים ימניים המתפתחים מהמעי האמצעי (midgut) הם בעלי פרוגנוזה גרועה יותר, עם שכיחות גבוהה יותר של BRAFm{{כ}} ו-MSI-H. בגידולים אלו, גם כאשר הם RAS-WT אין עדיפות להתחלת טיפול בתשלובת עם נוגדי EGFR וניתן להתחיל טיפולים בתשלובות עם בווציזומאב {{הערה|שם=הערה7}}. | ||
| + | הצד במעי ממנו התפתח הגידול מהווה למעשה ביומרקר עקיף למדדים ביולוגיים רבים, והוא חלק מהשיקולים לקביעת התשלובת לטיפול בקו ראשון. | ||
| − | + | ==HER2== | |
| − | + | אמפליפיקציה של הרצפטור ל-HER2 {{כ}}(human epidermal growth factor receptor 2) מוכר יותר כביומרקר בשד ובקיבה, שם הוכח שביטוי יתר שלו כפי שמתבטא בבדיקה אימונוהיסטוכימית או ב-FISH {{כ}} (Fluorescent in situ hybridization) מנבא תגובה לנוגדי HER2 כגון טרסטוזומאב - [[Trastuzumab]] (הרצפטין - Herceptin)*. ישנן עדויות ראשוניות שתיתכן תת-אוכלוסייה של כ-3% המבטאת HER2 ומגיבה למניפולציות שונות על מסלול תאי זה {{הערה|שם=הערה8|Sartore-Bianchi A, Trusolino L, Martino C, et al. Dual-targeted therapy with trastuzumab and lapatinib in treatment-refractory, KRAS codon 12/13 wild-type, HER2-positive metastatic colorectal cancer (HERACLES): a proof-of-concept, multicentre, open-label, phase 2 trial. Lancet Oncol. 2016 Jun;17(6):738-46. Epub 2016 Apr 20.}}. מחקרים אלו נמצאים בשלבים ראשוניים של איסוף המידע, ועל כן השימוש בביומרקר זה עדיין אינו שגרתי. | |
| − | |||
| − | + | (*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים. | |
| − | + | ||
| + | ==סיכום== | ||
| + | ההבנה הגדלה בשינויים הגנטיים והביולוגיים של סרטן המעי הגס והיכולת לאפיין תתי-אוכלוסיות באמצעות הביומרקרים השונים, מאפשרות טיפול טוב ומדויק יותר המותאם באופן אישי לכל מטופל. האפיון של הביומרקרים השונים מומלץ כבר בשלב הראשוני של אבחון מחלה גרורתית. | ||
==ביבליוגרפיה== | ==ביבליוגרפיה== | ||
{{הערות שוליים|יישור=שמאל}} | {{הערות שוליים|יישור=שמאל}} | ||
| + | <div class="mw-content-ltr"> | ||
| + | *Overman MJ, McDermott R, Leach JL, et al. Nivolumab in patients with metastatic DNA mismatch repair-deficient or microsatellite instability-high colorectal cancer (CheckMate 142): an open-label, multicentre, phase 2 study. Lancet Oncol. 2017 Sep;18(9):1182-91. Epub 2017 Jul 19 | ||
| + | </div>. | ||
==קישורים חיצוניים== | ==קישורים חיצוניים== | ||
גרסה אחרונה מ־11:09, 26 בינואר 2021
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| ביומרקרים בסרטן מעי גס גרורתי | ||
|---|---|---|
| ' | ||

| ||
Diagram of the stomach, colon, and rectum
| ||
| ICD-10 | Chapter C 18.-Chapter C 20./Chapter C 21. | |
| ICD-9 | 153.0 | |
| יוצר הערך | ד"ר רוית גבע | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן מעי גס גרורתי
סרטן המעי הגס הוא מהממאירויות השכיחות בישראל וגורם התמותה השני מבין גידולי הסרטן בישראל[1]. הטיפול במחלה גרורתית מבוסס על ניתוחים, כימותרפיה, טיפולים מכווני מטרה, אימונותרפיה וטיפולים מקומיים שונים. ככל שהמטופל "חשף לסוגי הטיפולים השונים, כך ניתן יהיה להאריך את חייו.
לא כל טיפול מתאים לכל מטופל או לכל גידול. יש לחשוף את המטופל לטיפולים המתאימים לו ביותר, משמע לבצע התאמה מרבית בין המאפיינים השונים של המטופל ושל הגידול ובין מאגר הטיפולים הקיים. גישה טיפולית זו, הנקראת "גישה מותאמת אישית", היא הבסיס לאונקולוגיה המודרנית, והיא מתבססת מצד אחד על עבודת צוות רב-תחומי ומצד שני על הבנה ביולוגית הולכת וגדלה של הגידול על ידי שימוש מושכל בביומרקרים - סמנים. ביומרקרים הם מאפיינים ביולוגיים, המבוססים בעיקר על שינויים ברצף הגנטי של הגידול, ועוזרים לסווג את הגידול לתתי-סוגים ובכך להתאים את הטיפול. גישה זו הובילה לשיפור משמעותי בפרוגנוזה של סרטן מעי גס גרורתי עם תוחלת חיים חציונית של בין שנתיים וחצי לשלוש שנים[2].
RAS
RAS הוא סמן מרכזי לניבוי התגובה לתרופות מסוג נוגדי EGFR (Epidermal growth factor receptor) שהם סטוקסימאב Cetuximab - (ארביטוקס - Erbitux) ופאניטומומאב - Panitumumab (וקטיביקס - Vectibix)*. נוגדי EGFR הם נוגדנים החוסמים את שרשרת הפעילות התאית המתחילה ברצפטור EGFR לאחר קישורו לליגנד. הסיגנל התאי מוביל בסופו של דבר לתהליכים מהותיים בתא, כגון פרוליפרציה, התמיינות והיצמדות תאים. עיכוב מסלול זה גורם להאטת צמיחת התאים ואף לנסיגת הגידול.
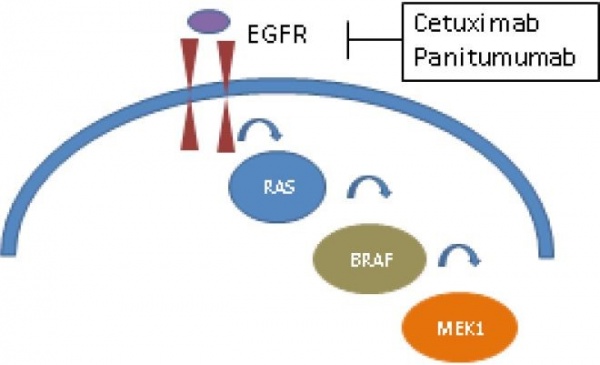
לאחר קישור הליגנד 7-EGFR, השרשרת התוך תאית ממשיכה למספר חלבונים מהותיים, מהם חלבוני משפחת RAS - חלבונים מסוג small GTPases המפרקים מולקולות GTP ( (guanosine triphosphate) ל-GDP (guanosine diphospRate). כאשר הגידול, מפתח מוטציה בחלבונים אלו, השרשרת התאית מופעלת באופן עצמא׳ ללא צורך בקשירת הליגנד לרצפטור. לאור כך, גידולים המבטאים מוטציה ב-RAS אינם מגיבים לטיפולים בנוגדי EGFR ואין תועלת משמעותית לשילובם בטיפול[3]. (תרשים מס' 1).
המוטציות המרכזיות שהוכחו כמנבאות עמידות לסטוקסימאב ופאניטומומאב נמצאות בגנים לקידוד חלבוני KRAS ו-NRAS. גידול ללא מוטציה ב-NRAS ו-KRAS מוגדר כ-wild type) RAS-WT), ובטיפול בו ניתן לשלב תרופות אלו עם המשלבים הכימותרפיים השונים.
מוטציה ב-KRAS או NRAS נמצאת בעד כ-50% מגידולי המעי הגס הגרורתיים. גידולים אלו נחשבים אגרסיביים יותר, ולמטופלים יש תוחלת חיים נמוכה יותר[3].
בדיקת מוטציות ב-RAS היא בדיקה בסיסית בהתאמת הטיפול ונמצאת בסל הבריאות. הבדיקה מבוצעת מיד עם האבחנה של מחלה גרורתית כדי לעזור בהכוונת הקו הטיפולי הראשון.
(*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים.
BRAF
החלבון הבא בשרשרת התאית לאחר RAS הוא BRAF. בתהליך דומה ל-RAS, מוטציה בגן המקודד לחלבון זה מאפשרת לשרשרת התוך תאית לפעול ללא ליגנד ומוריד האת יעילות העיכוב ברמת הרצפטור המבוצע על ידי סטוקסימאב ופאניטומומאב. בניגוד למוטציה ב-RAS, מוטציה ב-BRAF נדירה יותר ונמצאת בכ-8% מהגידולים [3]. (תרשים נוס' 1).
לאור מיעוט החומים המתגלים עם מוטציה זו וכן מורכבות השרשרת התוך תאית, קיום מוטציה זו נחשב כמפחית משמעותית את יעילות נוגדי ה-EGFR אך לא מבטל אותה לחלוטין. גידולים אלו נחשבים תת-אוכלוסייה אגרסיבית במיוחד במעי גס גרורת׳ עם תוחלת חיים נמוכה ועמידות לטיפולים. מחקרים שונים מציעים לאוכלוסייה זו טיפולים במשלבים מורכבים יותר, כגון FOLFOXIRI ובווציזומאב - Bevacizumab (אווסטין - Avastin)*, בשילובים של כימותרפיה + נוגדי EGFR + מעכבי BRAF שונים, כגון ומורפניב - Vemurafenib (זלבורף - Zelboraf)* או בשילוב הנ"ל עם עיכוב מסלולים תוך תאיים נוספים, כגון דרך מעכבי MEK. קיימים מחקרים רבים הבודקים את התשלובות השונות לתת קבוצה זו [4]. הבדיקה מבוצעת באופן שגרתי במקומות רבים בעולם, אך אינה כלולה בסל שירותי הבריאות בישראל.
(*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים.
MSI-H / MMR
קיום microsatellite instability) MSI) משמעו קיום רצפים החוזרים על עצמם בתדירות גבוהה לאורך דנ"א הגידול. החזרות גורמות למוטציות רבות. כאשר קיימות חזרות, הגידול נחשב MSI-H) high microsatellite instable), וכאשר הן לא נמצאות, הגידול נחשב microsatellite stable) MSS). קיום הרצפים הוא למעשה סמן לפגיעה בחלבוני תיקון הדנ"א - MMR (mismatch repair proteins ולכן פגיעה זו ניתן לבדוק על ידי PCR (Polymerase Chain Reaction), ברמת הדנ"א הגידולי או ברמת ביטוי החלבונים באמצעות אימונוהיסטוכימיה.
כ-15% מגידולי המעי הגס מתפתחים על רקע פגיעה זו במנגנון תיקון הדנ"א. הפגיעה יכולה להיות אקראית או תורשתית המקושרת לתסמונת לינץ' (Hereditary non-polyposis colon cancer - HNPCC). באוכלוסיית סרטן המעי הגס הגרורתי הפגיעה מאותרת בכ-4-3% מהגידולים.
עבודות ראשוניות בקבוצות קטנות של חולים מראות יעילות גבוהה לטיפול אימונותרפי בנוגדי PD1 פמברוליזומאב - Pembrolizumab (קיטרודה - Keytruda)* וניבולומאב - Nivolumab (אופדיבו - Opdivo)* או PD-L1 כגון אטזוליזומאב - Atezolizumab (טסנטריק - Tecentriq)* בגידולים עם MSI-H במטופלים שמיצו את הקווים הטיפוליים המקובלים [5], [6]. מחקרים נוספים מבוצעים לאישור שילוב האימונותרפיה בשלבי הטיפול השונים בגידולים עם MSI-H.
בארצות רבות בדיקת MSI נכנסת לשימוש קבוע בחולי סרטן מעי גס גרורתי. הבדיקה עדיין אינה כלולה בסל שירותי הבריאות בישראל לאינדיקציה זו, אך מבוצעת כחלק מהבירור הגנטי במטופלים הנחשדים לתסמונת לינץ'.
(*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים.
ימין ושמאל
התפתחות המעי הגס בעובר נובעת משני מקורות שונים - האחד מפתח את המעי הימני, והשני את המעי השמאלי, המתחברים בסופו של דבר לאיבר המשכי אחד. אנו למדים שהמקורות השונים גורמים להתפתחות סוגי סרטן מעי גס בעלי מאפיינים מולקולריים שונים, ועל כן בעלי התנהגות שונה, כולל תגובה שונה לטיפולים.
גידולים בצד שמאל של המעי המתפתחים מהמעי האחורי (hindgut) הם בעלי פרוגנוזה טובה יותר ומגיבים טוב יותר לטיפולים השונים. בגידולי RAS-WT במעי שמאלי נראית עדיפות להתחיל טיפול קו ראשון בתשלובת עם נוגדי EGFR. גידולים ימניים המתפתחים מהמעי האמצעי (midgut) הם בעלי פרוגנוזה גרועה יותר, עם שכיחות גבוהה יותר של BRAFm ו-MSI-H. בגידולים אלו, גם כאשר הם RAS-WT אין עדיפות להתחלת טיפול בתשלובת עם נוגדי EGFR וניתן להתחיל טיפולים בתשלובות עם בווציזומאב [6].
הצד במעי ממנו התפתח הגידול מהווה למעשה ביומרקר עקיף למדדים ביולוגיים רבים, והוא חלק מהשיקולים לקביעת התשלובת לטיפול בקו ראשון.
HER2
אמפליפיקציה של הרצפטור ל-HER2 (human epidermal growth factor receptor 2) מוכר יותר כביומרקר בשד ובקיבה, שם הוכח שביטוי יתר שלו כפי שמתבטא בבדיקה אימונוהיסטוכימית או ב-FISH (Fluorescent in situ hybridization) מנבא תגובה לנוגדי HER2 כגון טרסטוזומאב - Trastuzumab (הרצפטין - Herceptin)*. ישנן עדויות ראשוניות שתיתכן תת-אוכלוסייה של כ-3% המבטאת HER2 ומגיבה למניפולציות שונות על מסלול תאי זה [7]. מחקרים אלו נמצאים בשלבים ראשוניים של איסוף המידע, ועל כן השימוש בביומרקר זה עדיין אינו שגרתי.
(*) או תרופות המכילות חומר פעיל דומה בעלות שמות מסחריים אחרים.
סיכום
ההבנה הגדלה בשינויים הגנטיים והביולוגיים של סרטן המעי הגס והיכולת לאפיין תתי-אוכלוסיות באמצעות הביומרקרים השונים, מאפשרות טיפול טוב ומדויק יותר המותאם באופן אישי לכל מטופל. האפיון של הביומרקרים השונים מומלץ כבר בשלב הראשוני של אבחון מחלה גרורתית.
ביבליוגרפיה
- ↑ הרישום הלאומי לסרטן והמרכז הלאומי לבקרת מחלות, משרד הבריאות. סרטן המעי הגס והחלחולת בישראל - עדכון הנתונים, מרץ 2017. [הודעה לעיתונות]. מתוך: https://www.health.gov.il/PublicationsFiles/ICR_05032017.pdf
- ↑ Van Cutsem E, Cervantes A, Adam R, et al. ESMO consensus guidelines for the management of patients with metastatic colorectal cancer. Ann Oncol. 2016 Aug;27(8):1386-422. Epub 2016 Jul 5.
- ↑ 3.0 3.1 3.2 Aprile G, Macerelli M, De Maglio G, et al. The relevance of BRAF and extended RAS mutational analyses for metastatic colorectal cancer patients. OA Mol Oncol. 2013 Dec 25;1(1):7-15.
- ↑ Abdel-Rahman O. Targeting BRAF aberrations in advanced colorectal carcinoma: from bench to bedside. Future Oncol. 2016 Jan;12(1):25-30. Epub 2015 Nov 30.
- ↑ Diaz LA, Marabelle A, Delord JP, et al. Pembrolizumab therapy for microsatellite instability high (MSI-H) colorectal cancer (CRC) and non-CRC. [abstract]. J Clin Oncol. 2017; 35(15_suppl): 3071.
- ↑ 6.0 6.1 Tejpar S, Stintzing S, Ciardiello F, et al. Prognostic and predictive relevance of primary tumor location in patients with RAS wild-type metastatic colorectal cancer. JAMA Oncol. 2017;3(2):194-201. Epub 2016 Oct 10.
- ↑ Sartore-Bianchi A, Trusolino L, Martino C, et al. Dual-targeted therapy with trastuzumab and lapatinib in treatment-refractory, KRAS codon 12/13 wild-type, HER2-positive metastatic colorectal cancer (HERACLES): a proof-of-concept, multicentre, open-label, phase 2 trial. Lancet Oncol. 2016 Jun;17(6):738-46. Epub 2016 Apr 20.
- Overman MJ, McDermott R, Leach JL, et al. Nivolumab in patients with metastatic DNA mismatch repair-deficient or microsatellite instability-high colorectal cancer (CheckMate 142): an open-label, multicentre, phase 2 study. Lancet Oncol. 2017 Sep;18(9):1182-91. Epub 2017 Jul 19
.
קישורים חיצוניים
- במה עמ' 98
המידע שבדף זה נכתב על ידי ד"ר רוית גבע - המרכז לגידולי מערכת העיכול, המערך האונקולוגי, המרכז הרפואי תל אביב ע"ש סוראסקי


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק