הבדלים בין גרסאות בדף "פסוריאזיס - ספחת - Psoriasis"
| שורה 103: | שורה 103: | ||
* [[מחלת הפסוריאזיס ודרכי הטיפול בה - מאז ועד היום]] | * [[מחלת הפסוריאזיס ודרכי הטיפול בה - מאז ועד היום]] | ||
{{שש}} | {{שש}} | ||
| − | {{ייחוס|ד"ר בתיה ב. דוידוביץ |פרופ' רוני וולף, יחידת עור, המרכז רפואי קפלן, רחובות.{{ש}}המידע עודכן על ידי פרופ' יובל רמות, מחלקת עור, המרכז הרפואי הדסה עין-כרם, ירושלים.}} | + | {{ייחוס|ד"ר בתיה ב. דוידוביץ |פרופ' רוני וולף, יחידת עור, המרכז רפואי קפלן, רחובות.{{ש}}המידע עודכן ב-2021 על ידי פרופ' יובל רמות, מחלקת עור, המרכז הרפואי הדסה עין-כרם, ירושלים.}} |
| + | |||
[[קטגוריה:עור ומין]] | [[קטגוריה:עור ומין]] | ||
[[קטגוריה:ראומטולוגיה]] | [[קטגוריה:ראומטולוגיה]] | ||
גרסה אחרונה מ־06:02, 9 בדצמבר 2024
| פסוריאזיס (ספחת) | ||
|---|---|---|
| Psoriasis | ||
| ||
| שמות נוספים | פסוריאזיס | |
| ICD-10 | Chapter L 40. | |
| ICD-9 | 696 | |
| יוצר הערך | פרופ' יובל רמות, פרופ' רוני וולף, ד"ר בתיה ב. דוידוביץ | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – פסוריאזיס
המילה Psora ביוונית פרושה גרד. הראשון שתבע את המונח פסוריאזיס (Psoriasis) במשמעותו הנוכחית, היה Hebra בשנת 1841. פסוריאזיס היא מחלה דלקתית כרונית התקפית. שכיחותה באוכלוסייה הכללית גבוהה יחסית. מצטברות עדויות שהשלכותיה הרפואיות, בעיקר בחולים הקשים, עלולות להיות מעבר למחלה בעור ובמפרקים ולערב איברים נוספים, כדוגמת המערכת הקרדיו-ווסקולרית.
הסיבות להתפתחות המחלה מורכבות, וכוללות מרכיב גנטי, חיסוני וסביבתי. חלה התקדמות משמעותית בהבנת הגורמים למחלה, בעיקר בתחום החיסוני, דבר שאפשר את פיתוחן של תרופות חדשות, הממוקדות כנגד מרכיבים במערכת החיסון הגורמים להתלקחות המחלה. העובדה כי תרופות אלה ספציפיות למרכיבים אלה, מאפשרת יעילות גבוהה עם סיכון קטן לתופעות לוואי. עם זאת, הטיפולים הקיימים כרוכים בצורך בהתמדה, עלותם למערכת הבריאות לעיתים גבוהה, והם אינם חפים מתופעות לוואי. לבסוף, יש לזכור את רמת הפרט, החולה, שבנוסף להתמודדות עם המחלה והטיפול בה, עליו להתמודד גם עם התגובות הקשות של החברה הנובעות מבורות ומפחד, ועל כן לא פעם הוא מתקשה במציאת מקום עבודה, ביצירת קשר זוגי וקשרים חברתיים אחרים. נמצא כי תופעות כגון דיכאון וחרדה שכיחות יותר בקרב חולי פסוריאזיס מאשר בקרב אנשים בריאים. מעבר לפן הקוסמטי/אסתטי , המחלה מתבטאת בגרד, כאבי מפרקים (לעיתים עם עיוות שלהם), ובהגברת הסיכון להופעת התסמונת המטבולית (Metabolic syndrome) ומחלת מעי דלקתית (Inflammatory bowel disease). מצטברות עדויות המראות קשר עם ממאירות מסוג לימפופרוליפרטיבי (Lymphoproliferative) ועם מחלות קרדיו-ווסוקולריות. על כן לא מפתיע שבעבודות שונות נמצא כי ההפרעה באיכות החיים בקרב חולי פסוריאזיס דומה למתואר בחולי מחלות כרוניות קשות אחרות כגון: מחלות לב, מחלות ריאה כרוניות וסוכרת.
אפידמיולוגיה
ההיארעות הכללית באוכלוסייה היא בסביבות 2–3 אחוזים ללא הבדל בין המינים. בשחורים ובאסייתים השכיחות נמוכה יותר מאשר בלבנים. אין שינוי בהיארעות הפסוריאזיס במהלך המחצית השנייה של המאה ה-20 בניגוד למחלות אימונולוגיות אחרות כגון מחלת קרוהן (Crohn's disease) או סוכרת מסוג 1 שבהן ההיארעות עולה.
בניגוד לדרמטיטיס אטופית (Atopic dermatitis) השכיחה יותר במעמד סוציואקונומי גבוה, פסוריאזיס אינה קשורה למצב הסוציואקונומי, אם כי מעמד סוציואקונומי נמוך קשור למחלה קשה יותר ולטיפול לוקה בחסר במחלה. כשני שלישים בממוצע מפתחים מחלה קלה והשאר מחלה בחומרה בינונית וקשה.
קליניקה
יש צורות קליניות רבות של פסוריאזיס. נזכיר את העיקריות שבהן:
- פסוריאזיס רובדית (Plaque type) - הצורה השכיחה ביותר ובה יש שתי תת-קבוצות:
- Type I - צורת מחלה זו מופיעה בגיל צעיר (בממוצע בקרב נערות בגיל 16 ואצל נערים בגיל 19–20 שנים). נמצא קשר גנטי מובהק בין החולים. ב-44 אחוזים מהחולים אחד ההורים הוא חולה פסוריאזיס ובמקרים רבים נמצא קשר ל-HLA-CW6
- Type II - צורת מחלה זו מופיעה בגיל מבוגר יותר (עשור 5), הקשר הגנטי רופף ורק בכ-14 אחוזים נמצא קשר ל-HLA-CW6
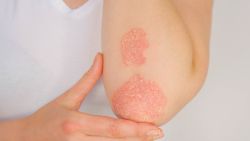
בצורה קלינית זו לרוב הפריחה סימטרית, מורכבת מרבדים אדומים בגדלים ועוביים שונים המכוסים בקשקשת כסופה. ישנה נטייה להופעת הפריחה באזור הקרקפת, הגפיים בצד המיישר (ברכיים ומרפקים), בטבור ובגב תחתון. יש גם שינויים אופייניים בציפורניים ובהם שקערוריות קטנות (Pitting), כתמים צהובים חומים (Oil spots) או התעבות הציפורן עם היווצרות היפרקרטוזיס (Hyperkeratosis) הדומה לפטרת הציפורן
- פסוריאזיס טיפתית (Guttate psoriasis) - בה הנגעים קטנים אך מפוזרים על פני השטח כטיפות, מופיעה יותר בצעירים או לאחר זיהומים סטרפטוקוקיים
- Psoriasis inversa - מופיעה באזורי הקיפולים (בתי שחי, מפשעות, תחת השדיים וקפל העכוז), בניגוד לאזורים שבהם מופיעה הפסוריאזיס הרובדית השכיחה יותר
- פסוריאזיס פוסטולרית (Pustular psoriasis) - מופיעה במספר סוגים:
- Generalized pustular psoriasis - מחלה על שם Von Zumbusch, שהיא קשה וחריפה המתפתחת לרוב בחולים עם פסוריאזיס ידועה או עם היסטוריה משפחתית של פסוריאזיס. המחלה מתבטאת כאודם דיפוזי בעור ועליו אגמי מוגלה. לרוב יופיעו גרד ותחושת צריבה. החולה מרגיש ברע, עם חום גבוה וצמרמורות. ייתכנו גם סיבוכים כלליים כגון: דלקת ראות עד כדי כשל נשימתי חריף, אי ספיקת לב והפטיטיס
- Pustular psoriasis of pregnancy (נקראה בעבר Impetigo herpetiformis): צורה ייחודית של Generalized pustular psoriasis, המופיעה בנשים הרות ומלווה בהיפוקלצמיה. צורה זו יכולה להתפתח למחלה קשה, העלולה לסכן את חיי האם והעובר, ואף יכולה להוות התוויה להשראת לידה מוקדמת
- צורה ממוקמת של פסוריאזיס פוסטולרית, המתבטאת כעור אדום הזרוע בפוסטולות זעירות על גבי כפות הידיים והרגליים, שלעיתים מתלכדות ליצירת אגמי מוגלה. פוסטולות אלו מתייבשות לאחר כשבוע-שבועיים ומשאירות גלדים חומים שלבסוף נושרים. פוסטולות חדשות יופיעו מעבר לגבולות הנגעים. המהלך הוא התקפי. הציפורניים לרוב מעורבות על ידי חריצים, עיוותים ואיבוד הצבע והברק. צורה זו מגיבה טוב לרטינואידים סיסטמיים (Systemic Retinoids)
- Erythrodermic psoriasis - אריתרודרמה מוגדרת כאודם וקשקשת המערבת למעלה מ-90 אחוזים משטח הגוף. אריתרודרמה יכולה להופיע כסיבוך של מחלות עור ומחלות סיסטמיות שונות ובתוכן השכיחה ביותר היא פסוריאזיס. היא יכולה להיות הביטוי הראשון של פסוריאזיס קשה או להופיע בחולים עם פסוריאזיס מפושט או כסיבוך של פסוריאזיס על שם Von Zumbusch. זהו מצב חירום רפואי המחייב טיפול תומך כללי בנוסף לטיפול בעור
- דלקת פרקים פסוריאטית - בקרב כ-20 אחוזים מהחולים תופיע בנוסף למחלה העורית גם מחלה מפרקית. המחלה המפרקית מופיעה במרבית המקרים לפני או במקביל למחלה העורית, אך לעיתים יכולה להופיע גם לפני הסימנים העוריים. יש חמש הסתמנויות קליניות שונות של דלקת מפרקים פסוריאטית, כאשר השכיחה ביניהן היא דלקת במפרק אחד עם נפיחות וטנוסינוביטיס (Tenosinovitis) באחד ממפרקי כפות הידיים. בחלק מהמקרים יכולים להופיע דפורמציות במפרקים הנגועים, דבר שעלול להביא לפגיעה תפקודית שאינה הפיכה
מדדים להערכת המחלה
- Psoriasis Area-and-Severity Index) PASI) מגלם את ההערכה של שטח הגוף המעורב בחלוקה לארבעה אזורים אנטומיים (ראש, גו, גפיים עליונות ותחתונות), יחד עם חומרת הקשקשת, האודם ועובי הרבדים בכל אחד מהאזורים הנזכרים למעלה ומגיע לניקוד שבין 0 (אין פסוריאזיס) ל-72 (פסוריאזיס חמורה)
- Physician's Global Assessment) PGA) - מדרג את החומרה הכוללת של הפסוריאזיס כולל שטח גוף מעורב, אודם, קשקשת ועובי הרבדים יחסית לנקודת ייחוס (Baseline) לפי שש דרגות 0 (נקי), 1 (מצוין), 2 (טוב), 3 (בינוני), 4 (לא טוב), 5 (גרוע ביותר)
- שאלון Dermatology Life Quality Index) DQLI ) - 10 שאלות שעליהן עונים החולים מודדות את מידת השפעת המחלה על איכות החיים של הלוקים בה. המדד הכולל נע בין 0 ("המחלה כלל לא משפיעה") ל-30 ("המחלה משפיעה מאוד")
אימונולוגיה
בשנים עברו התפיסה המקובלת הייתה כי פסוריאזיס היא מחלה של האפידרמיס, השכבה החיצונית של העור, ונובעת מהתחלקות מהירה של קרטינוציטים (Keratinocytes), התאים המרכיבים את האפידרמיס, במקביל להתמיינות פגומה שלהם. לפני כ-40 שנה חלה מהפכה בהבנה של הפתוגנזה של המחלה, כאשר התברר כי המחלה היא בעיקרה מחלה של מערכת החיסון, ובעיקר נובעת משפעול מוגבר של תאים מסוג T.
בבסיס התהליך עומדים התאים הדנדריטיים (Dendritic), שהם תאים מציגי אנטיגן, אשר מפרישים ציטוקינים דלקתיים, כגון IL-12 (InterLeukin), IL-6, IL-1, TNF-α (Tumor Necrosis Factor) ו- IL-23. ציטוקינים אלה מביאים בתורם לשפעול של תאי T, כאשר התאים העיקריים הלוקחים חלק בתהליך זה הם תאי T helper מסוג CD4+. בעקבות שפעול זה, תאי ה- T מתמיינים לתאים מסוג Th17 ותאי T helper נוספים, כגון תאי Th1. ידוע כי התאים המרכזיים הלוקחים חלק בהתפתחות המחלה הם תאי Th17, אשר מפרישים ציטוקינים רבים, כולל IL-17A, IL-17F, IL-21, IL-22 ו- TNF. ציטוקינים אלה מביאים בתורם לשפעול של הקרטינוציטים באפידרמיס, גיוס של נויטרופילים (Neutrophils) לדרמיס ולאפידרמיס, ולשגשוג של כלי דם. ההבנה המולקולרית של התהליכים הדלקתיים הלוקחים חלק במחלה והמתוארים לעיל היא זאת שאפשרה לפתח טיפולים ביולוגיים חדשים המכוונים ספציפית לציטוקינים הלוקחים חלק במחלה.
גנטיקה
פסוריאזיס היא מחלה בעלת רקע גנטי. בשליש מהחולים יש סיפור משפחתי של חולה נוסף מדרגה ראשונה. בתאומים לא זהים שכיחות המחלה בשני התאומים היא 25 אחוזים. בתאומים זהים השכיחות מגיעה ל-70 אחוזים והמחלה תופיע אצל שני התאומים.
מחקרים שונים אשר בוצעו על חולים מרקע אתני שונה מצאו כי קיימים מעל 50 אזורים שונים בגנום האנושי הקשורים למחלה. הקשר החזק ביותר להתפתחות מחלה נמצא לגן HLA-C*06, כאשר רוב האזורים האחרים קשורים לגנים המקודדים למולקולות הלוקחות חלק במערכת החיסון המולדת והנרכשת ובתפקוד החיץ העורי. עולה גם כי גם לשינויים אפיגנטיים (Epigenetic) תפקיד בהתפתחות המחלה.
גורמים המעוררים פסוריאזיס
מעבר להשפעה הגנטית שהוזכרה לעיל, המחלה מושפעת גם מגורמים סביבתיים, שהידועים שבהם:
- זיהומים סטרפטוקוקאליים (Streptococcal): תאי T לימפוציטים, שעוברים שפעול בעיקר עם חלבון M-6 של חיידק הסטרפטוקוק, יכולים לתקוף גם את העור, שכן יש Cross reactivity עם אנטיגנים אפידרמליים. בנוסף, ייתכן שגם רעלנים המופרשים על ידי החיידק יכולים לשמש כסופר-אנטיגנים (Super-antigens) המשפעלים את מערכת החיסון
- HIV (Human Immunodeficiency Virus): גם בנשאים יש התעוררות של המחלה ובחולי AIDS (Acquired Immunodeficiency Syndrome) תיתכן הופעת פסוריאזיס שהיא קשה לטיפול ורק במצב סופני כשמספר תאי ה-T נמוך מאוד, אז גם מחלת הפסוריאזיס נסוגה
- תרופות :חוסמי בטא ו-Lithium מעוררים בעיקר פסוריאזיס פוסטולרית גם זמן ארוך לאחר תחילת נטילת התרופה. Anti-Malaria ובעיקר Hydroxychloroquine, כמו גם חלק מה-NSAIDs (Non Steroidal Anti Inflammatory Drugs) יכולים להשרות פסוריאזיס. יש דיווחים על תרופות נוספות, ובעיקר על חוסמי תעלות סידן, ו- ACE inhibitors (Angiotensin Converting Enzyme) כטריגרים אפשריים. Inerferon Gamma, הניתנת בין היתר לטיפול בדלקת נגיפית מסוג C, יכולה לגרום להתלקחות קשה של פסוריאזיס
- תופעת Koebner (Isomorphic Response) - הופעה של נגעי פסוריאזיס כעשרה ימים עד 14 יום לאחר שאזור מסוים עבר טראומה. המנגנון הוא כנראה נוירואימונוגני (Neuroimmunogenic), שכן פסוריאזיס לא מופיעה באזורים נטולי עצבוב ואילו באזורי נגעים יש שגשוג של אקסונים. קרטינוציטים פסוריאטיים מבטאים קולטנים ל- -NGF (Nerve Growth Factor), ונראה שטראומה לעור גורמת להפרשה של NGF ובעקבות כך להשראה של התהליך הדלקתי המעורר את היווצרות נגעי הפסוריאזיס
- מתח נפשי (Stress): 70-40 אחוזים מהחולים מדווחים על מתח נפשי כסיבה להופעה ראשונית או להתלקחות של המחלה
- עישון ושתיית משקאות אלכוהוליים - בשנים קודמות או בעת התלקחות המחלה
- עונות השנה - אצל חולים רבים המחלה מחמירה בחורף ומשתפרת בקיץ. ייתכן שהדבר קשור לחשיפה לקרינת UV
טיפולים
יש אפשרויות טיפול רבות ומגוונות מאי פעם הנותנות מענה לחולים אלה, אולם תרופה אשר תביא לריפוי המחלה טרם נמצאה. על כן, את התרופות הקיימות יש להמשיך וליטול לתקופות ממושכות, בהינתן שפסוריאזיס היא מחלה כרונית. הטיפולים מתחלקים לטיפולים מקומיים ולטיפולים סיסטמיים, ובתוכם טיפולי פוטותרפיה (Phototherapy), טיפולים פומיים ותרופות ביולוגיות הניתנות בהזרקה.
טיפולים מקומיים
- סטרואידים (Steroids) - הטיפול בסטרואידים נחשב לאחד הטיפולים המקומיים המרכזיים במחלה. קיימות שבע קבוצות על פי העוצמה, והבחירה מתבצעת לפי חומרת הנגע ומיקומו. לטיפול זה ישנו מספר תופעות לוואי בשימוש ממושך ובעיקר באזורי קפלים, כגון התפתחות של אטרופיה עורית או סימני מתיחה. בנוסף, ישנה בעיה של התרגלות העור לתכשיר (Tachyphylaxis) ותופעת rebound – התפרצות המחלה עם הפסקת הטיפול
- חומצה סליצילית (Salicylic acid) - משמשת כתכשיר קרטוליטי (Keratolytic) (להסרת הקשקשת). יש להיזהר משימוש בשטחים נרחבים מחשש להרעלה (סליציליזם, Salicylism) המתבטאת בטיניטוס, בלבול והיפוגליצמיה רפרקטורית (Refractory hypoglycemia)
- תכשירים המבוססים על Tar: מקורו של ה-Tar בעצים או בנפט, אך היעיל ביותר הוא זה המופק מפחם (Coal tar). הוא מכיל כעשרת אלפים נגזרות פוליארומטיות של פוליקרבון (Polycarbonate polyaromatic). בין היתר הוא מדכא סינתזה של DNA (DeoxyriboNucleic Acid) בקרטינוציטים, ומהווה חומר פוטוסנסיטיבי (Photosensitive). על סמך תכונה זו התפתח טיפול על שם Goeckerman שעיקרו הוא מריחת Tar ולאחר מכן חשיפה ל-UVB צר טווח. שילוב זה הוא בעל אפקט סינרגיסטי (Synergistic effect), ויכול להביא לרמיסיה ממושכת
- Anthralin - טיפול המוכר קרוב ל-100 שנה. מקורו משרף של עצים. החומר מופיע בריכוזים שונים. דרך הטיפול היא מריחה לזמן קצר בהדרגה עד לחצי שעה. השימוש ב-Anthralin יכול לגרום לגירוי העור ולהכתמה באזור השימוש. גם לתכשיר זה, בדומה ל-Tar, פעילות סינרגיסטית בעת שימוש במקביל ל-UVB צר טווח (שיטה המכונה Ingram)
- Calcipotriol - אנלוגים של ויטמין D המשפיעים על משק הסידן התוך תאי וכך מווסתים את קצב ההתמיינות של הקרטינוציטים. יעילות רבה בשילוב עם סטרואידים או עם פוטותרפיה. בשימוש בכמות רבה או בתדירות גבוהה עלולה להיות ספיגה סיסטמית, דבר היכול להביא לשינויים במשק הסידן הכללי בגוף
- Tazarotene - רטינואיד סינתטי (Synthetic retinoid) מקומי. בחלק מהחולים עלול להתפתח גירוי מקומי במקום המריחה, ועל כן ניתן לשלב אותו עם סטרואיד מקומי, דבר שמפחית תופעה זו באופן ניכר. ניתן גם לשלב עם פוטותרפיה. חומר זה הוא טרטוגני ואסור בשימוש בנשים בהיריון
- מעכבי Calcineurin (תכשירים כדוגמת Pimecrolimus ו-Tacrolimus) – תכשירים בעלי אפקט אנטי דלקתי בדומה לסטרואידים, אך ללא תופעות הלוואי הקשורות באטרופיה עורית, ועל כן בטוחים לשימוש ממושך. בשל תכונות אלה, משמשים בעיקר בטיפול בנגעים באזורים רגישים, כדוגמת הפנים או אזור איבר המין
טיפולים סיסטמיים
- פוטותרפיה:
- טיפול ותיק מאוד לפסוריאזיס, המשמש בעיקר לטיפול במחלה בינונית-קשה, ובמיוחד למחלה שלא הגיבה לטיפולים מקומיים. קיימים מספר סוגים של טיפולי פוטותרפיה לפסוריאזיס, והם כוללים את השילוב של פסוראלן עם UVA (טיפול המכונה PUVA) ,UVB רחב-טווח (Broad band UVB) ו- UVB צר-טווח (Narrow band UVB ,NB-UVB). בזכות היעילות והבטיחות שלו, NB-UVB הוא הטיפול שנמצא בשימוש הנרחב ביותר לפסוריאזיס, וניתן להשתמש בו גם בילדים ובנשים בהיריון. טיפול זה אינו מלווה בפגיעה במערכת החיסון, כפי שניתן לראות עם השימוש בטפולים מקומיים או סיסטמיים אחרים. עם זאת, הטיפול ב-PUVA נמצא כקשור להתפתחות של סרטני עור והזדקנות מואצת של העור, ולכן יש להגביל טיפול זה בקרב חולים אשר נמצאים בסיכון גבוה לגידולי עור.
- החיסרון המרכזי בטיפולי פוטותרפיה הוא העובדה כי לצורך טיפול יעיל על החולה לפנות למכוני פוטותרפיה לתקופה של בין 20–30 טיפולים, כאשר הטיפולים ניתנים בתדירות של 3 פעמים בשבוע, דבר המוביל לחוסר נוחות בחלק ניכר מהחולים. ישנם גם מכשירים לשימוש ביתי, אך הם דורשים פיקוח של רופא עור. ניתן להגביר את היעילות של טיפולים ב- NB-UVB באמצעות טיפולים מקומיים משלימים, כפי שהוסבר לעיל.
- Methotrexate - טיפול המוכר כבר משנות ה-50. זהו Antagonist של חומצה פולית, אנטימטבוליט (Antimetabolite) המעכב סינתזת פורינים (Purines) ופירימידינים (Pyrimidines). במינונים הניתנים בפסוריאזיס (לרוב עד 25 מיליגרמים בשבוע) ההשפעה היא אימונומודולטורית (Immunomodulator) בעיקרה. תרופה זו ניתנת פעמים רבות כקו ראשון טיפולי מבין הטיפולים הפומיים, גם בזכות היעילות הגבוהה שלה, וגם בזכות העובדה כי היא יעילה בנוסף גם לטיפול בדלקת מפרקים פסוריאטית. התרופה ניתנת בתדירות של פעם בשבוע, ודורשת מעקב עתי אחר בדיקות דם, כולל ספירת דם ותפקודי כבד. בשימוש ממושך עלול להתפתח פיברוזיס כבדי
- Acitretin (Neotigason) – הוא רטינואיד מונו-ארומטי (Mono-aromatic) מדור שני, נגזרת של ויטמין A. יעילותו לפסוריאזיס רובדית נמוכה יחסית, אך אחוזי התגובה משתפרים בשילוב עם קרינת UV. טיפול זה יעיל לפסוריאזיס פוסטולרית ולפסוריאזיס אריתרודרמית (Erythrodermic). התרופה טרטוגנית, על כן מומלץ להימנע מהשימוש בה בנשים בגיל הפריון, שכן יש איסור מוחלט להרות בזמן הטיפול ושלוש שנים לאחר הפסקת השימוש בו. כמו כן התרופה יכולה להעלות טריגליצרידים או לגרום להפרעה באנזימי כבד. תופעות לוואי נוספות האופייניות לרטינואידים סיסטמיים הם יובש בריריות ובעור, כאבי מפרקים והגברת נשירת שיער
- Cyclosporine - מעכב Calcineurin בלימפוציטים ולכן מעכב הפרשת ציטוקינים מעודדי דלקת מסוג Th-1. החומר משמש בטיפול חולי פסוריאזיס כבר משנות ה-80. הטיפול ניתן בדרך כלל רק במצבים קשים ולתקופה מוגבלת, מאחר שהוא גורם ליתר לחץ דם במחצית מהמטופלים ולפגיעה כלייתית בקרב 70 אחוזים מהמטופלים שטופלו לאורך זמן. יש לבצע ניטור מדוקדק של לחץ הדם ותפקוד הכליות בזמן הטיפול. התגובה לטיפול מצוינת ומהירה אך יש Rebound (התפרצות חוזרת) עם הפסקת הטיפול ולכן יש להיערך ולתת טיפול חלופי
- Apremilast – הטיפול הפומי החדש ביותר לפסוריאזיס, אשר יעיל גם לטיפול בדלקת מפרקים פסוריאטית. התרופה מעכבת את האנזים Phosphodiesterase 4 4 (PDE-4), דבר המביא לעליה ברמות cAMP (Cyclic Adenosine Monophosphate) בתאים. עליה זו גורמת לירידה בשעתוק של ציטוקינים דלקתיים האופייניים לפסוריאזיס, כדוגמת TNF, IL-12 ו- IL-23. היתרון המרכזי של התרופה הוא העובדה כי התרופה בטוחה לשימוש, ואינה דורשת במרבית המקרים ניטור רוטיני (Routine) של בדיקות דם. תופעות הלוואי השכיחות הן בעיקר גסטרואינטסטינליות (Gastrointestinal), אך הן אינן מביאות במרבית המקרים להפסקת השימוש בתרופה
- טיפולים ביולוגיים:
- בניגוד לטיפולים הפומיים, שלהם השפעה כללית שאינה סלקטיבית על מערכת החיסון, הטיפולים הביולוגים הם טיפולים סלקטיביים, אשר ניתן לכוונם כנגד מרכיב או שניים במערכת החיסון אשר לוקחים חלק בתהליך הדלקתי במחלה. הדבר מאפשר יעילות גבוהה יותר של הטיפול ובטיחות גבוהה יותר. בזכות טיפולים אלה, ניתן להשיג שליטה במחלה באחוז גבוה מאוד של החולים, גם לתקופות ממושכות. הטיפולים הביולוגיים החדשים מאפשרים להגיע לעור נקי או כמעט נקי ממחלה במרבית החולים, ובכך לשיפור משמעותי באיכות חייהם. העובדה כי הטיפולים הביולוגיים ניתנים בהזרקות בתדירות נמוכה יחסית (אף בתדירות של פעם ב-12 שבועות בחלק מהתרופות) מאפשרת נוחות גבוהה לשימוש
- ניתן לחלק את הטיפולים הביולוגיים הקיימים לטיפול בפסוריאזיס לשתי קבוצות עיקריות:
- הדור הראשון של הטיפולים הביולוגיים: תרופות אלה כוללות תכשירים המכוונים כנגד TNF, וכוללות את התרופות Infliximab, Etanercept, Adalimumab ו-Certolizumab pegol
- הדור השני של הטיפולים הביולוגיים: טיפולים שהחלו להתפתח החל משנת 2009, והם כוללים נוגדנים המכוונים כנגד המסלול הדלקתי המערב את IL-23/IL-17. טיפולים אלה כוללים את התרופות Ustekinumab, Secukinumab, Ixekizumab, Guselkumab ו-Risankizumab
- טיפולים מהדור הראשון המכוונים כנגד TNF: TNF הוא ציטוקין חשוב הלוקח חלק במספר רב של מחלות דלקתיות, כולל בפסוריאזיס. עם זאת, אחוזי ההצלחה עם טיפולים אלה בקרב חולי פסוריאזיס נמוכים בהשוואה לטיפולים הביולוגיים מהדור החדש יותר, והתברר כי ככל הנראה הסיבה ליעילותם היא השפעה עקיפה על מסלול ה- IL-23/IL-17, ולא ההשפעה הישירה על TNF. היתרונות המרכזיים של טיפולים אלה הם הניסיון הרב שקיים עם טיפולים אלה והיעילות שלהם למגוון רחב של מחלות דלקתיות, ששכיחותן גבוהה בקרב חולי פסוריאזיס (כגון דלקת מפרקים פסוריאטית ודלקת מעי דלקתית).
ל-Certolizumab pegol תפקיד ייחודי בטיפול בפסוריאזיס, לאור העובדה כי הוא אינו חוצה את השלייה, ולכן הוא הטיפול המועדף בחולות בהיריון או המעוניינות להרות.
- לתרופות מקבוצה זו עלולות להיות תופעות לוואי, כגון שכיחות גבוהה יותר של זיהומים, וישנו חשש להתלקחות צהבת נגיפית מסוג B או שחפת חבויה. בנוסף, עלולה להתפתח מחלה דה-מיילינטיבית או עלולה להיות פגיעה בקרב חולים עם אי ספיקת לב מתקדמת.
- טיפולים מהדור השני:
- Ustekinumab: נוגדן המכוון כנגד תת-יחידה p40, המשותפת לציטוקינים IL-12/IL-23. תרופה זו השיגה הצלחה טיפולית משמעותית, וב־65 אחוזים עד 75 אחוזים מהחולים ניתן היה להגיע ל-75 אחוזים שיפור במחלתם. לתרופה זו ותק רב לטיפול במחלה, נחשבת בטוחה מאוד לשימוש, ויעילה גם כנגד דלקת מפרקים פסוריאטית פריפרית וכנגד מחלת מעי דלקתית. לתרופה זו גם תדירות נוחה של הזרקה, והיא ניתנת פעם ב־12 שבועות
- נוגדנים כנגד IL-17A: לקבוצה זו שייכות שתי תרופות הזמינות בישראל – Secukinumab ו-Ixekizumab. טיפולים אלה הביאו עמם בשורה חדשה לחולים, כאשר אחוזי ההצלחה עם טיפולים אלה היה גבוה משמעותית מהטיפולים הקודמים שהיו מאושרים למחלה. עם טיפולים אלה, כ-90 אחוזים מהחולים משיגים שיפור של לפחות 75 אחוזים במחלתם העורית. בנוסף ליעילותם הגבוהה, התגובה נצפית תוך זמן קצר מאוד, וניתן להגיע לעור נקי או כמעט נקי ממחלה תוך מספר שבועות. התרופות הללו יעילות מאוד גם לטיפול בדלקת מפרקים פסוריאטית פריפרית או אקסיאלית. פרופיל הבטיחות של תרופות אלה הוא טוב, תופעות לוואי היא זיהומים קלים בלבד במערכת הנשימה העליונה ובשכיחות נמוכה זיהומים ב-Candida של ריריות הפה ואיבר המין בנשים. התרופה אינה מיועדת לשימוש בחולים הסובלים ממחלקה דלקתית של המעי, ויש להימנע משימוש בתרופות אלה בקרב חולים שלהם היסטוריה של מחלת מעי דלקתית
- נוגדנים כנגד IL-23: לקבוצה זו שייכות שתי תרופות הזמינות בישראל – Guselkumab ו-Risankizumab. תרופות אלה הן החדשות ביותר שאושרו לשימוש בארץ. התרופות הללו מכוונות כנגד תת-יחידה p19, שהיא ייחודית ל- IL-23. בכך בעצם נמנעת החסימה של IL-12 (שנחסם בשימוש עם Ustekinumab). בכך מתאפשרת הפעילות של ציטוקין זה, שהוא חשוב בהגנה מפני מזהמים ומפני התפתחות של גידולים. העובדה כי תרופות אלו מכוונות כנגד IL-23, ציטוקין אשר ממוקם גבוה יותר במסלול הדלקתי, מאפשרת תגובה ארוכת טווח יותר מאשר טיפולים המכוונים כנגד IL-17, ולכן גם תדירות ההזרקות נמוכה יחסית (פעם ב־8 או 12 שבועות). תרופות אלו סלקטיביות מאוד לציטוקין הלוקח חלק בפסוריאזיס, דבר המתבטא ביעילות גבוהה מאוד של טיפולים אלה, וכן בפרופיל בטיחות מצוין
בשל העובדה כי הטיפולים הביולוגיים בעלי השפעה על מערכת החיסון, כהכנה לטיפולים אלה יש לוודא כי החולה אינו נשא של מחלות זיהומיות כרוניות כדוגמת צהבת נגיפית B או C, HIV או שחפת חבויה. כן על החולה להתחסן לשפעת עונתית וכנגד פנאומוקוק, ובזמן הטיפול יש להימנע מחיסונים חיים מוחלשים.
לקריאה נוספת
- פסוריאזיס - ספחת (דף פירושים)
- פסוריאזיס - ספחת - Psoriasis (ערך זה)
- פסוריאזיס - ספחת בילדים - Psoriasis in children
- פסוריאזיס - ספחת - טיפול במעכבי אינטרלויקין Psoriasis - treatment with interleukin 17A inhibitors - 17A
- חידושים בטיפול בפסוריאזיס - ספחת - Innovations in the treatment of psoriasis
- פסוריאזיס - ספחת - טיפולים חדשים - 2018 - Psoriasis - novel therapies
- מחלת הפסוריאזיס ודרכי הטיפול בה - מאז ועד היום
המידע שבדף זה נכתב על ידי ד"ר בתיה ב. דוידוביץ ופרופ' רוני וולף, יחידת עור, המרכז רפואי קפלן, רחובות.
המידע עודכן ב-2021 על ידי פרופ' יובל רמות, מחלקת עור, המרכז הרפואי הדסה עין-כרם, ירושלים.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק