לימפומה שאינה הודג'קין - Non-hodgkin lymphoma
| לימפומה שאינה הודג'קין | ||
|---|---|---|
| Non-hodgkin lymphoma | ||
| 250px | ||
Micrograph of mantle cell lymphoma, a type of non-Hodgkin lymphoma. Terminal ileum. H&E stain.
| ||
| שמות נוספים | NHL | |
| ICD-10 | Chapter C 82.-Chapter C 85. | |
| ICD-9 | 200
, 202 |
|
| MeSH | D008228 | |
| יוצר הערך | ד"ר שמרית רינגלשטיין, נערך על ידי ד"ר אורי גרינבוים ב 2024 | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – לימפומה
לימפומה שאיננה הודג'קין (non-Hodgkin lymphoma) או NHL היא ממאירות שמקורה בלימפוציטים שעברו התמיינות. לרוב המחלה מערבת בלוטות לימפה, אך כל איבר שיש בו פעילות לימפוציטים (כמו ריריות מערכת הנשימה ומערכת העיכול למשל), וכן לשד העצם ורקמות אקסטרה-לימפטיות יכולים להיות מעורבים גם הם.
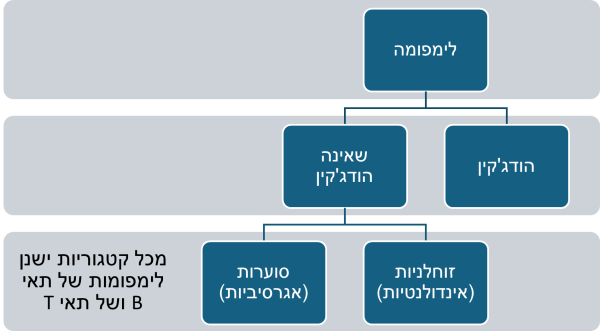
ישנם תתי סוגים רבים של לימפומות ומחלות לימפופרוליפרטיביות, להם מאפיינים היסטולוגיים, שינויים גנטיים ומופעים קליניים ייחודיים. על פי החלוקה האחרונה של ה-WHO שפורסמה ב-2022 הלימפומות מתחלקות לפי תא המקור - רובן ממקור של תאי B ומיעוט ממקור תאי T או תאי NK[1](איור 1).
ההיארעות המדווחת בארצות הברית היא 22 מקרים ל 100000 איש, המהווים כ 5 % מכלל הממאירויות, והגיל החציוני לאבחנה הוא 63[2]. בישראל ב 2012 כ-6 % מהחולים עם אבחנה של ממאירות אובחנו עם NHL, וזהו הגידול הרביעי בשכיחותו[3]. מדובר במחלה ששכיחותה עולה עם הגיל, והיחס בין גברים לנשים עומד על 1.4:1 לערך לטובת הגברים.
גורמי הסיכון לתחלואה דומים לגורמי סיכון לממאירויות אחרות, כגון עישון, השמנה, חשיפה לחומרי הדברה, ועובדי תעשיות מסוימות, אך הקשר הסטטיסטי בין גורמי הסיכון לתחלואה נמוך, ולחולים רבים לא היו גורמי סיכון מוכרים. דיכוי חיסוני על רקע HIV או על רקע טיפול תרופתי (כמו זה הניתן למושתלי איברים), וכן נטייה משפחתית, מוכרים גם כן. ישנו קשר אטיולוגי בין תתי סוגים מסוימים של NHL ומחוללים זיהומיים, כמו וירוס הפטיטיס C ו-marginal zone lymphoma (MZL), חיידק הליקובקטר פילורי ו-gastric MALT lymphoma או חיידק כלמידיה פסיטכי ו-MZL של גלגל העין[4]. בחלק ממקרים אלו טיפול בגורם הזיהומי בלבד יכול להביא את הלימפומה לרמיסיה.
גורמי הסיכון המתוארים אינם בזיקה גבוהה להיארעות, ודומים לגורמי סיכון לממאירויות אחרות, כגון עישון, השמנה, חשיפה לחומרי הדברה, עובדי תעשיות מסוימות. גורמי סיכון בזיקה טובה יותר להיארעות הם דיכוי חיסוני על רקע HIV או על רקע טיפול תרופתי (כמו זה הניתן למושתלי איברים), וכן נטייה משפחתית אך בלא שנמצא עד היום גורם תורשתי אחד מובהק. ישנו קשר אטיולוגי בין תתי סוגים מסוימים ומחוללים זיהומיים ספציפיים, כמו וירוס הפטיטיס C ו-marginal zone lymphoma (MZL), חיידק הליקובקטר פילורי ו-gastric MALT lymphoma או חיידק כלמידיה פסיטכי ו-MZL של גלגל העין[2]. בחלק ממקרים אלו טיפול בגורם הזיהומי יכול להביא את הלימפומה לרמיסיה.
ההתייצגות הקלינית נעה על ספקטרום רחב, שבין היעדר מוחלט של סיפמטומטים למשך פרקי זמן ארוכים מאד, דרך לימפאדנופאתיה לא כואבת, ועד לתסמיני B קשים (ירידה במשקל, חום סיסטמי והזעות לילה).
בדרך בכלל האיבחון מבוצע מביופסיה של אתר מעורב (פעמים רבות בלוטת לימפה), בהתבסס על הארכיטקטורה של הרקמה וצביעות אימונוהיסטוכימיות המזהות ביטוי חלבונים ספציפיים על תאי הגידול. הארכיטקטורה של הרקמה קריטית לצורך האיבחון, ולכן לא ניתן על סמך אספירציה בלבד לאבחן מחלה זו.
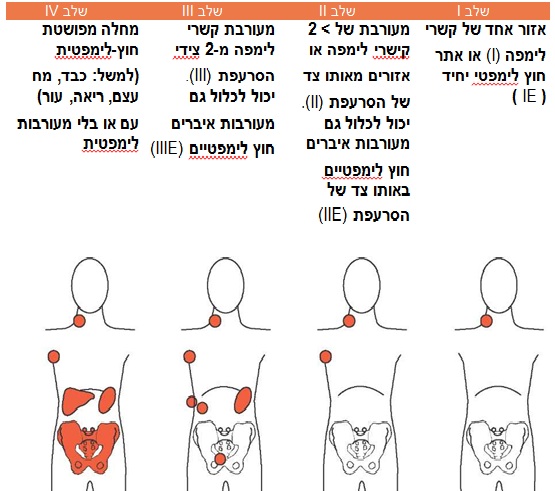
לאחר האיבחון נדרש שלב של staging לאומדן מידת פיזור המחלה, שכולל בדיקת CT כלל גופי וביופסית מח עצם. ברוב סוגי הלימפומה ישנה עדיפות לבדיקת PET-CT שנותנת מידע על פעילות מטאבולית, מעבר למידע האנטומי שנותנת בדיקת ה-CT הרגילה. המידע שנותן ה-PET עושה upstaging בעד 31% מהמקרים[5] באבחנה, ומבדיל טוב יותר בבדיקות המעקב בין אתרים צלקתיים של מחלה ישנה לבין אתרי מחלה פעילים.
איור 1 מראה את שיטת ה-staging בלימפומה, ובאיור 2 ו-3 דוגמאות לאינדקסים של פרוגנוזה (IPI) המקובלים ללימפומה מסוג diffuse large B-cell lymphoma (DLBCL) (2) ול- follicular lymphoma (FL) (3), וכפי שניתן לראות, הניקוד מבוסס הן על מידת פיזור המחלה לפי ה-staging והן על קריטריונים מעבדתיים נוספים ומאפיינים הנוגעים למצבו התפקודי של החולה.
ישנם תתי סוגים רבים של לימפומה, אך לצורך הבנת ההחלטות הטיפוליות חשובה ההבחנה הבסיסית בין לימפומות איטיות/אינדולנטיות המכונות low grade, לבין לימפמות אגרסיביות המכונות high grade. ההבחנה בין הסוגים האלו קשורה גם לדינמיקה של המחלה ולעיתים לקליניקה, אך גם להחלטות טיפוליות.
הלימפומה הנפוצה ביותר בקבוצת הלימפומות האינדולנטיות היא הלימפומה הפוליקולרית (FL). ההגדרה אינדולנטית משקפת את העובדה שפעמים רבות יש פנאי לרופא המטפל לעקוב למשך תקופה מסוימת אחרי המטופל על מנת לאמוד את קצב ההתקדמות שלה, שיכולה אפילו להראות נסיגה ספונטנית. ישנן מספר התוויות מקובלות לטיפול בלימפומה פוליקולרית (איור 4 מציג שני סטים מקובלים של קריטריונים כאלו), אך הפועל היוצא מזה הוא שישנה קבוצה לא מבוטלת שבה ננקוט בגישת watch & wait ונטפל רק אם המחלה תשנה את אופייה ותהפוך לפעילה יותר. הנ"ל מבוסס על תוצאות של מספר מחקרים שלא מצאו שטיפול מוקדם משפר את אורך חייהם של המטופלים (אינו מאריך overall survival) [6][7]. רוב מוחלט של מטופלים שבהם מתקבלת החלטה לתת טיפול יגיבו היטב לטיפול, אלא שברובם המחלה תחזור בעתיד והם יידרשו לפחות לעוד טיפול אחד בהמשך חייהם.
הלימפומה השכיחה בקבוצת הלימפומות האגרסיביות (ובכלל השכיחה ביותר בתוך ה-NHL) היא ה-DLBCL. לימפומות אגרסיביות דורשות טיפול מהיר לאחר האיבחון, ורוב החולים יסבלו בעת האיבחון מתלונות ותסמינים שונים הקשורים במחלתם. בזכות הטיפול כ-60-70% מהמטופלים יבריאו למעשה, ולא יידרשו בעתיד לעוד טיפולים[8]. למרות האמור לעיל ישנה רבגוניות משמעותית בתגובות לטיפול ובסיכון להישנות, תופעה שנחקרת באופן מעמיק כבר מתחילת המאה ה-21, ומלמדת כי ישנם שינויים ציטוגנטיים ושינויים בביטוי גנים בגידולים, אשר מאפיינים התנהגויות קליניות שונות, וחלק גדול מהמחקר בלימפומה מתמקד בניסיון להתגבר על ההשפעה ההרסנית של חלק מהשינויים הללו באמצעות תרופות שונות[9][10][11].
קו הטיפול הראשון בלימפומה היה ועודנו מבוסס על שלד כמותרפי ברוב המקרים, אך באנשים עם מחלות רקע קשות או בגיל מאוד מבוגר לעיתים טיפול זה אינו אפשרי בגלל תופעות לוואי. במקרים אלו נעשות אדפטציות שונות, כמו הורדת מינונים, קיצור משך הטיפול, או שמוצע טיפול במסגרת מחקרים קליניים הבוחנים אופציות לא כמותרפיות.
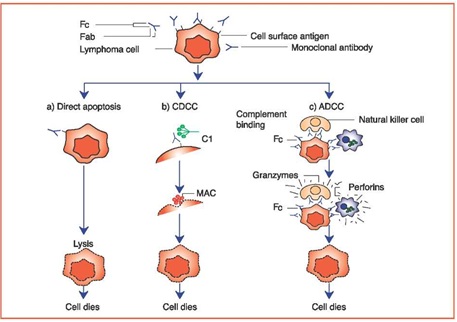
שיפור ניכר בתוצאות הטיפול בלימפומה של תאי B החל בשנות ה-90 של המאה ה-20 עם התוספת של הנוגדנים המונוקלונאליים לשלד הכמותרפי. הנוגדנן המונוקלנאלי הראשון שאושר על ידי רשויות הבריאות היה ה-Mabthera (שמו הגנרי Rituximab) המזהה את האנטיגן CD20 המבוטא על פני לימפוציטים B, ומפעיל את מערכת החיסון של המטופל להשמדת הגידול בעקבות זיהוי הזה. הוספת הטיפול בריטוקסימטב שיפר את ההישרדות של המטופלים לעומת כמותרפיה לבד הן בלימפומות אינדלונויות והן בלימפומות אגרסיביות [12][13][14] (איור 5 מראה מטהאנליזה של עבודות ב-FL ואיור 6 מראה גרפית את עקומות ההישרדות ב-DLBCL ממספר עבודות), ולכן ברוב הלימפומות קו הטיפול הראשון הוא כמואימונותרפיה (שילוב של כמותרפיה עם נוגדן מונוקלונאלי). נבדקו במחקרים קליניים ואף נכנסו לשימוש קליני מספר נוגדנים מונוקלנאליים נוספים המכוונים כנגד CD20 (בין אם תכשירים ביוסימילארים של Rituximab כמו Rixathon ו-Truxima ובין אם תכשירים הפועלים באופן שונה מעט כמו ה-Gazyva), אך גם כנגד אנטיגנים אחרים המבוטאים על תאי הלימפומה.
בלימפומה פוליקולרית מתן טיפול אחזקה בנוגדן מונוקלונאלי נגד CD20 משפר את זמן ההישרדות ללא התקדמות מחלה (progression free survival) ומקובל בהתוויה זו במקומות רבים למשך שנתיים מסיום הטיפול הראשוני[15].
ישנם טיפולים נוספים שנכנסו לארסנל התרופות לטיפול בלימפומה המבוססים על הבנה מדעית טובה יותר של מנגונים מקדמי סרטן ונוהגים לכנותם טיפולים "ממוקדי מטרה". הם משנים מעת לעת עת מיקומם בפרדיגמה הטיפולית בהתאם לתוצאות עדכניות של מחקרים קליניים.
להלן פירוט לגבי חלקם:
לנלידומיד- תרופה אימונומודלוטורית שהוכיחה יעילות בטיפול בלימפומות אינדולנטיות בשילוב עם ריטוקסימאב[16], ומאושרת לשימוש ב-FL נשנית.
CAR-T cells - מדובר בתאי T הנאספים מהחולה עצמו ובתהליך של הנדסה גנטית מוחדר להם רצפטור כימרי המזהה את תאי הגידול ומפעיל את תא ה- T לתקוף אותו. הם מאושרים כבר לשימוש בחלק מהלימפומות האגרסיביות בעקבות דיווחים על תוצאות תקדימיות באוכלוסיית חולים שהפרוגנוזה שלה טרם כניסת טיפול זה הייתה עגומה ביותר[17][18]. מחקר קליני כעת מתמקד בשיפור היעילות שלהם ובבדיקתם במגוון לימפומות אינדולנטיות.
נוגדנים מונוקלונאליים "חכמים" - אשר מצומד אליהם רעלן כלשהו החודר לתא הממאיר לאחר שזה מזוהה על ידי הנוגדן. הרעלן יכול להיות איזוטופ רדיואקטיבי או חומר ציטוטוקסי. ב-NHL מאושר לשימוש נוגדן בשם polatuaumab vedotin ב-DLBCL נשנית, אך ישנם נוספים ב-pipeline שישתלבו קרוב לוודאי ברצף הטיפול בהמשך[19].
Bispecific T-cell engagers הם נוגדנים מונוקלונאליים משוכללים יותר המזהים ומקרבים פיזית שני סוגי תאים, את התא הממאיר מחד, ומאידך תא תוקף של מערכת החיסון כמו תא T. בקרבה הפיזית מקדמת השמדה של התא הממאיר על ידי תא ה-T. תכשירים רבים נמצאים כעת בשלבי מחקר קליני מגוונים ויצטרפו גם הם לארסנל הטיפולים בשנים הקרובות.
מעכבי חלבונים תוך תאיים - בקבוצה זו נכללות תרופות המעכבות חלבונים שונים הנמצאים בשרשרת העברת הסיגנלים התוך תאיים ותפקידם להנחות את התא הסרטני להתחלק ולא לעבור מוות תאי מתוכנן. תכשירים אלו כוללים למשל משפחה של מעכבי החלבון PI3 kinase (כמו אידסללוסיב או קופנליסיב ודובליסיב) המאושרים כבר לטיפול ב-FL בקו טיפול שלישי ומעלה[20], כן מעכב של חלבון אחר הנקרא BTK, שמאושר לשימוש בקוים מתקדמים בלימפומות מסוימות כמו mantle cell lymphoma.
ישנם טיפולים אחרים רלוונטיים בלימפומה שיכולים להיכנס בשלבים שונים של הרצף הטיפולי ובהם:
קרינה שנחשבת טיפול בעל פוטנציל מרפא ב-stage I FL[21] אך נמצאת בשימוש גם לפליאציה במקרי לחץ על איבר או כאב בלתי נשלט.
השתלת תאי אב (נרא כם השתלת מח עצם) עצמיים רלוונטית באחת משתי התוויות עיקריות:
ראשונה כמיצוק של התגובה לטיפול קו ראשון בלימפומה של תאי T או ללימפומה מסוג mantle cell באנשים צעירים ללא ריבוי מחלות רקע ואילו השנייה למיצוק התגובה לטיפול כמואימונותרפי ללימפומה נשנית (רלוונטי גם ללימפומות אינדולנטיות וגם ל-DLBCL) [22][23]. השתלה מתורם זר אינה טיפול שכיח בלימפומה, ובעיקר רלוונטית לחולים עמידים לאחר קוי טיפול רבים שמחלתם הגיבה בסופו של דבר ולו באופן חלקי לטיפול האחרון שקיבלו.
ביבליוגרפיה
- ↑ Swerdlow SH, Campo E, Pileri SA, et al. The 2016 revision of the World Health Organization classification of lymphoid neoplasms. Blood. 2016;127(20):2375-2390.
- ↑ 2.0 2.1 Chihara D, Nastoupil LJ, Williams JN, Lee P, Koff JL, Flowers CR. New insights into the epidemiology of non-Hodgkin lymphoma and implications for therapy. Expert Rev Anticancer Ther. 2015;15(5):531-544.
- ↑ Paltiel O. Reasons for the Increase in Non-Hodgkin's Lymphoma Prevalence. Main statistics presented at the ICA press conference. February 09, 2015, Jerusalem, Israel. Available at: https://en.cancer.org.il/news_e/new.aspx?NewId=646. Accessed in 09.2020.
- ↑ Miranda-Filho A, Pineros M, Znaor A, Marcos-Gragera R, Steliarova-Foucher E, Bray F. Global patterns and trends in the incidence of non-Hodgkin lymphoma. Cancer Causes Control. 2019;30(5):489-499.
- ↑ Raanani P, Shasha Y, Perry C, et al. Is CT scan still necessary for staging in Hodgkin and non-Hodgkin lymphoma patients in the PET/CT era? Ann Oncol. 2006;17(1):117-122.
- ↑ Solal-Celigny P, Bellei M, Marcheselli L, et al. Watchful waiting in low-tumor burden follicular lymphoma in the rituximab era: results of an F2-study database. J Clin Oncol. 2012;30(31):3848-3853.
- ↑ Advani R, Rosenberg SA, Horning SJ. Stage I and II follicular non-Hodgkin's lymphoma: long-term follow-up of no initial therapy. J Clin Oncol. 2004;22(8):1454-1459.
- ↑ Kubuschok B, Held G, Pfreundschuh M. Management of diffuse large B-cell lymphoma (DLBCL). Cancer Treat Res. 2015;165:271-288.
- ↑ Nowakowski GS, Czuczman MS. ABC, GCB, and Double-Hit Diffuse Large B-Cell Lymphoma: Does Subtype Make a Difference in Therapy Selection? Am Soc Clin Oncol Educ Book. 2015:e449-457.
- ↑ Chapuy B, Stewart C, Dunford AJ, et al. Molecular subtypes of diffuse large B cell lymphoma are associated with distinct pathogenic mechanisms and outcomes. Nat Med. 2018;24(5):679-690.
- ↑ Wilson WH, Young RM, Schmitz R, et al. Targeting B cell receptor signaling with ibrutinib in diffuse large B cell lymphoma. Nat Med. 2015;21(8):922-926.
- ↑ Schulz H, Bohlius J, Skoetz N, et al. Chemotherapy plus Rituximab versus chemotherapy alone for B-cell non-Hodgkin's lymphoma. Cochrane Database Syst Rev. 2007(4):CD003805.
- ↑ Habermann TM, Weller EA, Morrison VA, et al. Rituximab-CHOP versus CHOP alone or with maintenance rituximab in older patients with diffuse large B-cell lymphoma. J Clin Oncol. 2006;24(19):3121-3127.
- ↑ Sehn LH, Donaldson J, Chhanabhai M, et al. Introduction of combined CHOP plus rituximab therapy dramatically improved outcome of diffuse large B-cell lymphoma in British Columbia. J Clin Oncol. 2005;23(22):5027-5033.
- ↑ Salles G, Seymour JF, Offner F, et al. Rituximab maintenance for 2 years in patients with high tumour burden follicular lymphoma responding to rituximab plus chemotherapy (PRIMA): a phase 3, randomised controlled trial. Lancet. 2011;377(9759):42-51.
- ↑ Leonard JP, Trneny M, Izutsu K, et al. AUGMENT: A Phase III Study of Lenalidomide Plus Rituximab Versus Placebo Plus Rituximab in Relapsed or Refractory Indolent Lymphoma. J Clin Oncol. 2019;37(14):1188-1199.
- ↑ Schuster SJ, Bishop MR, Tam CS, et al. Tisagenlecleucel in Adult Relapsed or Refractory Diffuse Large B-Cell Lymphoma. N Engl J Med. 2019;380(1):45-56.
- ↑ Neelapu SS, Locke FL, Bartlett NL, et al. Axicabtagene Ciloleucel CAR T-Cell Therapy in Refractory Large B-Cell Lymphoma. N Engl J Med. 2017;377(26):2531-2544.
- ↑ Sehn LH, Herrera AF, Flowers CR, et al. Polatuzumab Vedotin in Relapsed or Refractory Diffuse Large B-Cell Lymphoma. J Clin Oncol. 2020;38(2):155-165.
- ↑ Cheah CY, Fowler NH. Novel agents for relapsed and refractory follicular lymphoma. Best Pract Res Clin Haematol. 2018;31(1):41-48.
- ↑ Brady JL, Binkley MS, Hajj C, et al. Definitive radiotherapy for localized follicular lymphoma staged by (18)F-FDG PET-CT: a collaborative study by ILROG. Blood. 2019;133(3):237-245.
- ↑ Hagberg H, Gisselbrecht C, group Cs. Randomised phase III study of R-ICE versus R-DHAP in relapsed patients with CD20 diffuse large B-cell lymphoma (DLBCL) followed by high-dose therapy and a second randomisation to maintenance treatment with rituximab or not: an update of the CORAL study. Ann Oncol. 2006;17 Suppl 4:iv31-32.
- ↑ Diamond B, Kumar A. Mantle Cell Lymphoma: Current and Emerging Treatment Strategies and Unanswered Questions. Hematol Oncol Clin North Am. 2019;33(4):613-626.
ערכים נוספים בנושא
- לימפומה פוליקולארית - טיפול קו ראשון - Follicular lymphoma - first-line treatment
- לימפומה עורית - חידושים בטיפול - CTCL treatment updates - 2017
- טיפול קו ראשון בלימפומה מפושטת של תאי B גדולים - Diffuse Large B cell lymphoma
- לימפומה ראשונית של האשך - Primary testicular lymphoma
המידע שבדף זה נכתב על ידי ד"ר שמרית רינגלשטיין (באוקטובר 2020), רופאה בכירה, המערך ההמטולוגי במרכז הרפואי רמב"ם בחיפה ואחראית על שירות הלימפומה בבית החולים


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק